Область техники
Настоящее изобретение относится к способу получения фторалканола.
Уровень техники
Фторалканол пригоден в качестве промежуточного соединения для получения, например, гидрофобизующей и гидрофилизующей добавок, поверхностно-активного вещества или цветного проявителя в фотографии (например, JP-A-54-154707). Кроме этого, такое соединение не оказывает никакого растворяющего воздействия на субстрат из пластика, например из поликарбоната, и, таким образом, оно пригодно в качестве растворителя для материала для оптической записи, красителя и тому подобного (JP-А-4-8585, JP-A-5-258346 и тому подобное).
До сих пор фторалканол получали, например, используя способ с добавлением к метанолу тетрафторэтилена. В качестве такого способа были известны, например, (1) способ, в котором проводят загрузку и нагревание метанола, тетрафторэтилена и радикального инициатора сразу всех вместе (патент США 2559628), (2) способ, в котором проводят загрузку метанола, тетрафторэтилена и радикального инициатора сразу всех вместе и непрерывно проводят между ними реакцию в реакционной колонне (патент США 3022356), (3) способ, в котором проводят загрузку метанола и радикального инициатора сразу всех вместе, а тетрафторэтилен непрерывно добавляют, проводя с ним реакцию (JP-A-54-154707), или (4) способ, в котором в присутствии катализатора проводят непрерывную реакцию тетрафторпропанола и различных телогенов при температуре, не превышающей 100°С (JP-B-42-10782).
Однако проблема, возникающая при осуществлении способа (1), заключается в том, что трудно контролировать количество присоединений тетрафторэтилена, и даже если попытаться получить только в высшей степени подходящий желательный продукт с количеством присоединений в диапазоне от 1 до 4, молекулярно-массовое распределение продукта, как правило, является широким, а выход, как правило, является низким.
Проблема, возникающая при проведении способа (2), заключается в том, что в основном образуются соединения с количеством присоединений тетрафторэтилена, равным 3 или более, в то время как продукта с количеством присоединений тетрафторэтилена в диапазоне от 1 до 2 немного. Способу (3) присуща проблема, которая заключается в том, что необходимо добавлять твердый акцептор кислоты, или же для прохождения реакции потребуется долгое время. Кроме того, проблема, возникающая при осуществлении способа (4), заключается в том, что концентрация полученного теломера низкая, равная приблизительно 10%, а средняя степень полимеризации обычно чрезвычайно высокая на уровне 32, тогда как количество продуктов с количеством присоединений в диапазоне от 1 до 4 обычно чрезвычайно низкое.
Описание изобретения
Цель настоящего изобретения состоит в разрешении упомянутых выше проблем и в создании способа получения фторалканола, благодаря которому станет возможным массовое производство с высоким выходом, и который был бы выгоден для эксплуатации в промышленности.
А именно, настоящее изобретение предлагает способ получения фторалканола (формула 1) путем взаимодействия полифторолефина (формула 2) и алканола (формула 3) в присутствии радикального инициатора, где полифторолефин (формула 2), алканол (формула 3) и радикальный инициатор непрерывно подают в реактор, в котором осуществляется реакция при 105-135°С, и образованный фторалканол (формула 1) непрерывно отводят:
при условии, что символы в формулах имеют следующие значения:
Rf: атом фтора или С1-4 полифторалкильная группа;
R1, R2: каждый, независимо, атом водорода или С1-3 алкильная группа; и
n: целое число в диапазоне от 1 до 4.
Краткое описание чертежей
На чертеже представлена технологическая схема, демонстрирующая один из вариантов реализации настоящего изобретения.
Наилучший способ реализации изобретения
В формуле (1) Rf представляет собой атом фтора или С1-4 полифторалкильную группу. Полифторалкильная группа представляет собой группу, имеющую, по меньшей мере, два атома водорода в алкильной группе, замещенной атомами фтора. Полифторалкильная группа может иметь линейную структуру или разветвленную структуру. Rf предпочтительно представляет собой атом фтора или С1-2 полифторалкильную группу, в особенности предпочтительно атом фтора или трифторметильную группу.
В формуле (1) каждый из R1 и R2, которые не зависят друг от друга, представляют собой атом водорода или С1-3 алкильную группу. С1-3 алкильная группа может быть метильной группой, этильной группой, н-пропильной группой или изопропильной группой.
В формуле (1) n представляет собой целое число в диапазоне от 1 до 4, предпочтительно 1 или 2.
В качестве конкретных примеров фторалканола (формула 1) можно упомянуть следующие соединения.
H(CF2)2CH2OH,
H(CF2)3CH2OH,
H(CF2)4CH2OH,
CHF2CF2CH(CH3)OH,
CHF2CF2C(CH3)2OH,
CF3CHFCF2CH2OH,
CF3CHFCF2CH(CH3)OH,
CF3CHFCF2C(CH3)2OH.
Rf в полифторолефине (формула 2) имеет то же самое значение, что и Rf в формуле 1. Полифторолефин (формула 2) предпочтительно является перфторолефином, а говоря конкретно, например, можно упомянуть следующие соединения:
CF2=CF2,
CF3CF=CF2.
R1 и R2 в алканоле (формула 3) имеют те же самые значения, что и R1 и R2 в формуле 1. В качестве конкретных примеров алканола (формула 3) можно упомянуть следующие соединения:
СН3ОН,
СН3СН2ОН,
(СН3)2СНОН.
В качестве радикального инициатора, используемого в настоящем изобретении, можно упомянуть органический свободнорадикальный инициатор. В качестве такого органического свободнорадикального инициатора предпочтительны органический пероксид или азосоединение, а в особенности предпочтителен органический пероксид, такой, как алкилгидропероксид, диалкилпероксид, пероксикеталь, диацилпероксид, пероксикарбоксилат, пероксикарбоновая кислота или пероксикарбонат.
В качестве конкретных примеров радикального инициатора можно упомянуть следующие соединения:
1,1-бис(трет-бутилперокси)-3,3,5-триметилциклогексан,
1,1-бис(трет-бутилперокси)циклогексан,
трет-бутилпероксиизопропилкарбонат,
трет-бутилпероксиизобутират,
трет-бутилпероксипивалат,
ди-трет-бутилпероксид и трет-бутилгидропероксид.
Среди радикальных инициаторов предпочтителен диалкилпероксид, который обладает в особенности высокой способностью приводить к образованию радикалов из алканола (формула 3), а в особенности предпочтителен ди-трет-бутилпероксид.
Отношение количества молей подаваемого радикального инициатора к количеству молей алканола (формула 3) предпочтительно находится в диапазоне от 0,0001 до 0,1, в особенности предпочтительно от 0,001 до 0,05. Отношение количества молей подаваемого полифторолефина (формула 2) к количеству молей алканола (формула 3) предпочтительно находится в диапазоне от 0,01 до 1,2, в особенности предпочтительно от 0,05 до 0,5.
Настоящее изобретение предлагает способ получения фторалканола (формула 1), в котором полифторолефин (формула 2), алканол (формула 3) и радикальный инициатор непрерывно подают в реактор, где проводят между ними реакцию при 105-135°С, а фторалканол (формула 1) непрерывно отводят. Его предпочтительно реализуют следующим образом.
А именно, полифторолефин (формула 2) предпочтительно подают в реактор с загруженным в него алканолом (формула 3) так, чтобы давление в реакторе предпочтительно находилось бы в диапазоне от 0,2 до 1,5 МПа (избыточное давление, то же самое имеет место и далее в настоящем документе), в особенности предпочтительно от 0,5 до 1,0 МПа.
С другой стороны, алканол (формула 3) и радикальный инициатор предпочтительно непрерывно подают в реактор в виде их смешанного раствора. А во время реакции образованный фторалканол (формула 1) предпочтительно выводят из реактора таким образом, чтобы уровень жидкости в реакторе оставался бы постоянным.
Далее способ получения фторалканола настоящего изобретения будет описан еще более подробно со ссылкой на чертеж.
На чертеже представлена технологическая схема, демонстрирующая один вариант реализации настоящего изобретения.
В качестве реактора используют емкость для проведения реакции, и данная емкость для проведения реакции оборудована линией непрерывной подачи насосом из емкости для смешения в емкость для проведения реакции смешанного раствора алканола (формула 3) и радикального инициатора и линией подачи полифторолефина (формула 2). Кроме этого, емкость для проведения реакции соединена с емкостью для хранения реакционной жидкости для проведения отбора жидкости (здесь и далее в настоящем документе называемой реакционной жидкостью), содержащей фторалканол (формула 1), образованный в результате реакции в емкости для проведения реакции, и для хранения реакционной жидкости.
Прежде всего, алканол (формула 3) и радикальный инициатор смешивают в емкости для смешения, оснащенной перемешивающим устройством, для получения их смешанного раствора. С другой стороны, в емкость для проведения реакции, оснащенную перемешивающим устройством, загружают алканол (формула 3), и реактор нагревают до 105-135°С. После этого при непрерывной подаче в емкость для проведения реакции полифторолефина (формула 2) производят непрерывную подачу насосом в емкость для проведения реакции полученного ранее смешанного раствора алканола (формула 3) и радикального инициатора. В то же самое время в емкость для хранения реакционной жидкости отбирают реакционную жидкость таким образом, чтобы уровень жидкости в емкости для проведения реакции оставался бы постоянным. С другой стороны, также проводят непрерывную подачу полифторолефина (формула 2). Из реакционной жидкости, хранящейся в емкости для хранения реакционной жидкости, фторалканол (формула 1) можно получить, воспользовавшись способом очистки, таким как охлаждение или перегонка.
Реакция алканола (формула 3) и полифторолефина (формула 2) представляет собой так называемую реакцию теломеризации. Реакцией теломеризации является цепная реакция, в которой радикальный инициатор разлагается с образованием радикала, а радикал будет отрывать атом водорода на углероде, с которым связана гидроксильная группа алканола (формула 3), с получением радикала алканола, и сюда же будет присоединяться полифторолефин (формула 2). Реакция в настоящем изобретении представляет собой реакцию, в которой для такой реакции теломеризации, как цепная реакция, можно контролировать количество присоединений полифторолефина (формула 2), в результате чего желательный фторалканол (формула 1), где n находится в диапазоне от 1 до 4, можно получать с высоким выходом.
Среди условий проведения реакции, в первую очередь, требуется, чтобы температура реакции находилась бы в диапазоне от 105 до 135°С. Например, в случае, когда желательно получить продукт, у которого n равен 1 или 2, или в случае, когда в качестве радикального инициатора используют ди-трет-бутилпероксид (температура, при которой время полураспада равно 10 часам: 125°С), температура при промышленно выгодных условиях предпочтительно находится в пределах диапазона от 120 до 130°С. Время реакции предпочтительно равно, по меньшей мере, 3 часам, в особенности предпочтительно, по меньшей мере, 5 часам. Кроме этого, на верхний предел времени реакции особенных ограничений не накладывают. При промышленно выгодных условиях среднее время пребывания, рассчитанное в результате деления количества реакционной жидкости в реакторе на скорость подачи исходного вещества, с точки зрения конверсии предпочтительно находится в диапазоне от 2 до 100 часов, а в особенности предпочтительно оно находится в диапазоне от 5 до 20 часов. Давление в реакции с точки зрения конверсии предпочтительно находится в диапазоне от 0,2 до 1,5 МПа, в особенности предпочтительно в диапазоне от 0,5 до 1,0 МПа.
Кроме этого, в том, что касается подачи радикального инициатора и алканола (формула 3), то, для того чтобы инициировать реакцию в стабилизированных условиях, на начальной стадии реакции можно воспользоваться способом с неравномерной подачей, но после того, как реакция стабилизируется, их подачу в течение времени реакции предпочтительно проводить с постоянной скоростью. Кроме этого, что касается полифторолефина (формула 2), то в течение времени реакции подачу необходимого полного количества предпочтительно проводить при постоянной скорости.
Помимо этого, в соответствии со способом настоящего изобретения количеством присоединений можно легко управлять, регулируя количество подаваемого полифторолефина (формула 2), в результате чего становится возможным получение фторалканола (формула 1) с высокой селективностью и высокой производительностью. Полученный фторалканол (формула 1) подвергают обычной очистке с разделением для получения соединения с высокой степенью чистоты. Кроме этого, в способе настоящего изобретения осуществляется непрерывный отвод продукта и тому подобного, за счет чего подавляется увеличение содержания кислоты, и это выгодно, поскольку реакцию можно проводить в отсутствие акцептора кислоты (то есть, без акцептора кислоты).
Фторалканол (формула 1), полученный по способу настоящего изобретения, пригоден в качестве исходного вещества или растворителя для гидрофобизующей и гидрофилизующей добавок, поверхностно-активного вещества, цветного проявителя в фотографии и тому подобного.
Примеры
Далее настоящее изобретение будет подробно описано со ссылкой на примеры, которые ни в коей мере этим не ограничивают объем настоящего изобретения. В последующем изложении литр будет обозначаться через «л». Кроме этого, %, определенный при помощи газовой хроматографии, рассчитывают на массу.
Пример 1. Получение 2,2,3,3-тетрафтор-1-пропанола.
Реакцию проводили в соответствии с технологической схемой, продемонстрированной на чертеже. А именно, в качестве реактора использовали емкость для проведения реакции объемом 1 м3, изготовленную из сплава Хастеллой C, оснащенную перемешивающим устройством, и в нее загружали 341 кг (432 л) метанола. После этого температуру внутри реактора увеличивали до 125°С. Выдерживая данную температуру и проводя подачу тетрафторэтилена в емкость для проведения реакции таким образом, чтобы давление было равно 0,9 МПа, на начальной стадии реакции в течение 0,5 часа при помощи дозировочного насоса проводили непрерывную подачу в емкость для проведения реакции раствора, содержащего 5,5 кг ди-трет-бутилпероксида и 44 кг метанола, смешанных в емкости для смешения, при скорости подачи 25 л/час, а после этого для проведения реакции непрерывно проводили подачу со скоростью 4,2 л/час в течение нескольких часов.
После этого, при непрерывной подаче тетрафторэтилена таким образом, чтобы давление в емкости для проведения реакции было бы равным 0,9 МПа, при помощи дозировочного насоса проводили непрерывную подачу в емкость для проведения реакции раствора, содержащего 12 кг ди-трет-бутилпероксида и 1315 кг метанола, смешанных в емкости для смешения, при скорости подачи 56 л/час, а со дна емкости для проведения реакции реакционную жидкость непрерывно выводили в емкость для хранения реакционной жидкости таким образом, чтобы уровень жидкости оставался постоянным. Такие непрерывную подачу и непрерывный отвод реакционной жидкости проводили в течение 110 часов. По истечении 110 часов подачу раствора ди-трет-бутилпероксида в метаноле прекращали и после этого в емкость для проведения реакции подавали тетрафторэтилен таким образом, чтобы давление было бы равным 0,9 МПа. После выдерживания температуры на уровне 125°С в течение 3 часов проводили охлаждение до 40°С. В результате, используя общее количество метанола, равное 4,9 т, и общее количество тетрафторэтилена, равное 1,9 т, в качестве реакционной жидкости получали 6,7 т жидкой смеси, содержащей 2,2,3,3-тетрафтор-1-пропанол и метанол.
Жидкую смесь анализировали по методу газовой хроматографии, согласно которому она содержала 66% метанола, 28% 2,2,3,3-тетрафтор-1-пропанола и 4% 2,2,3,3,4,4,5,5-октафтор-1-пентанола. Кроме этого, степень превращения метанола составляла 15%, селективность для 2,2,3,3-тетрафтор-1-пропанола была равна 93%, а селективность для 2,2,3,3,4,4,5,5-октафтор-1-пентанола была равна 7%. Данную смесь очищали, проводя перегонку, с получением 2,2,3,3-тетрафтор-1-пропанола со степенью чистоты, по меньшей мере, равной 99%.
Пример 2. Получение 2,2,3,4,4,4-гексафтор-1-бутанола.
Реакцию проводили в соответствии с технологической схемой, продемонстрированной на чертеже. А именно, в качестве реактора использовали емкость для проведения реакции объемом 0,5 м3, изготовленную из сплава Хастеллой C, оснащенную перемешивающим устройством, и в нее загружали 170 кг (212 л) метанола. После этого температуру внутри реактора увеличивали до 130°С. На начальной стадии реакции в течение 0,25 часа при помощи дозировочного насоса проводили непрерывную подачу в емкость для проведения реакции раствора, содержащего 2,8 кг ди-трет-бутилпероксида и 22 кг метанола, смешанных в емкости для смешения, при скорости подачи 25 л/час, а после этого для проведения реакции непрерывно проводили подачу со скоростью 4,2 л/час в течение 4 часов. В то же самое время при помощи дозировочного насоса проводили непрерывную подачу в емкость для проведения реакции 20 кг гексафторпропена при скорости подачи 3 л/час. После этого при помощи дозировочного насоса проводили непрерывную подачу в емкость для проведения реакции раствора, содержащего 12 кг ди-трет-бутилпероксида и 1315 кг метанола, смешанных в емкости для смешения, при скорости подачи 28 л/час и в то же самое время при помощи дозировочного насоса проводили непрерывную подачу в емкость для проведения реакции гексафторпропена при скорости подачи 3 л/час. В течение данного периода со дна емкости для проведения реакции реакционную жидкость непрерывно выводили в емкость для хранения реакционной жидкости таким образом, чтобы уровень жидкости оставался бы постоянным. Такую непрерывную подачу исходных веществ и непрерывный отвод жидкого содержимого проводили в течение 40 часов. По истечении 40 часов подачу раствора ди-трет-бутилпероксида в метаноле прекращали и после этого температуру выдерживали на уровне 125°С в течение одного часа и затем проводили охлаждение до 40°С. В результате в качестве реакционной жидкости получали 1,2 т жидкой смеси, содержащей 2,2,3,4,4,4-гексафтор-1-бутанол и метанол.
Данную жидкую смесь анализировали по методу газовой хроматографии, согласно которому она содержала 73% метанола и 19% 2,2,3,4,4,4-гексафтор-1-бутанола. Кроме этого, степень превращения метанола составляла 8%, а селективность для 2,2,3,4,4,4-гексафтор-1-бутанола была равна 88%. Данную смесь очищали, проводя перегонку, с получением 2,2,3,4,4,4-гексафтор-1-бутанола со степенью чистоты, по меньшей мере, равной 99%.
Промышленная применимость
В соответствии с настоящим изобретением с высокой селективностью можно получить фторалканол (формула 1). Кроме этого, способ настоящего изобретения представляет собой непрерывный процесс, в котором производят непрерывную подачу исходных веществ, а продукт непрерывно отводят, и это способ, который чрезвычайно выгоден для эксплуатации в промышленности, потому что в данном способе нет необходимости использования каких-либо специальных условий реакции или режима проведения реакции.
Пример А
422 кг метанола загружают в реактор объемом 1 м3 и внутреннюю температуру повышают до 125°С. Поддерживая указанную температуру и подавая тетрафторэтилен (далее обозначенный как «ТФЭ») в реакционный резервуар таким образом, чтобы давление было 0,8 МПа, на начальной стадии реакции, в резервуар непрерывно подают раствор, содержащий 8,2 кг перекиси ди-трет-бутила, смешанные с 74 кг метанола, со скоростью 30 л/час в течение 1 часа, и затем непрерывно подают со скоростью 4 л/час в течение 7 часов для проведения реакции.
Затем, непрерывно подавая ТФЭ таким образом, чтобы давление в реакционном резервуаре было 0,8 МПа, в резервуар непрерывно подают раствор, содержащий 12 кг перекиси ди-трет-бутила, смешанные с 1280 кг метанола, со скоростью 50-60 л/час, и из нижней части реакционного резервуара непрерывно выпускают реакционную жидкость так, чтобы уровень жидкости оставался постоянным. Через 36 часов подачу метанольного раствора перекиси ди-трет-бутила прекращают и в реакционный резервуар подают ТФЭ таким образом, чтобы давление было 0,8 МПа. После поддерживания температуры на уровне 125°С в течение 20 минут, ее понижают до 40°С.
В результате, используя всего 2,1 т метанола и всего 0,95 т ТФЭ в качестве реакционной смеси, получают 2938 л смешанной жидкости, содержащей 2,2,3,3-тетрафтор-1-пропанола (далее обозначен как «ТФПО») и метанол.
Смешанную жидкость анализируют с применением газовой хроматографии (ГХ), в соответствии с которой она содержит 66% метанола, 26% ТФПО и 5% 2,2,3,3,4,4,5,5-октафтор-1-пентанола. Далее, превращение метанола составляет 11%, и селективность в отношении ТФПО составляет 84%, и селективность в отношении 2,2,3,3,4,4,5,5-октафтор-1-пентанола составляет 16%. Эту смесь анализируют с применением фтористого электрода для определения содержания кислоты и подтверждают, что содержание кислоты составляет 1152 ч/млн, на основе FH расчета.
Пример В
385 кг метанола загружают в реактор объемом 1 м3 и внутреннюю температуру повышают до 125°С. Поддерживая указанную температуру и подавая ТФЭ в реакционный резервуар таким образом, чтобы давление было 0,8 МПа, на начальной стадии реакции, в резервуар непрерывно подают раствор, содержащий 5,6 кг перекиси ди-трет-бутила, смешанные с 50 кг метанола, со скоростью 30 л/час в течение 1 часа, и затем непрерывно подают со скоростью 4 л/час в течение 9 часов для проведения реакции.
Затем, непрерывно подавая ТФЭ таким образом, чтобы давление в реакционном резервуаре было 0,8 МПа, в резервуар непрерывно подают раствор, содержащий 11,7 кг перекиси ди-трет-бутила, смешанные с 1280 кг метанола, со скоростью 50-60 л/час, и из нижней части реакционного резервуара непрерывно выпускают реакционную жидкость так, чтобы уровень жидкости оставался постоянным. Через 28 часов подачу метанольного раствора перекиси ди-трет-бутила прекращают и в реакционный резервуар подают ТФЭ таким образом, чтобы давление было 0,8 МПа. После поддерживания температуры на уровне 125°С в течение 20 минут, ее понижают до 40°С.
В результате, используя всего 1,2 т метанола и всего 0/73 т ТФЭ в качестве реакционной смеси, получают 2376 л смешанной жидкости, содержащей ТФПО и метанол.
Смешанную жидкость анализируют с применением газовой хроматографии (ГХ), в соответствии с которой она содержит 70% метанола, 23% ТФПО и 5% 2,2,3,3,4,4,5,5-октафтор-1-пентанола. Далее, превращение метанола составляет 9%, и селективность в отношении ТФПО составляет 82%, и селективность в отношении 2,2,3,3,4,4,5,5-октафтор-1-пентанола составляет 18%. Эту смесь анализируют с применением фтористого электрода для определения содержания кислоты и подтверждают, что содержание кислоты составляет 1115 ч/млн, на основе FH расчета.
Сравнительный пример С
480 кг метанола загружают в реактор объемом 1 м3 и внутреннюю температуру повышают до 125°С. Поддерживая указанную температуру и подавая ТФЭ в реакционный резервуар таким образом, чтобы давление было 0,8 МПа, на начальной стадии реакции, в резервуар непрерывно подают раствор, содержащий 8,2 кг перекиси ди-трет-бутила, смешанные с 74 кг метанола, со скоростью 28 л/час в течение 40 часа, и затем непрерывно подают со скоростью 6 л/час в течение 13 часов для проведения реакции в течение 14 часов.
Смешанную жидкость анализируют с применением газовой хроматографии (ГХ), в соответствии с которой она содержит 58% метанола, 39% ТФПО и 3% 2,2,3,3,4,4,5,5-октафтор-1-пентанола. Далее, превращение метанола составляет 14%, и селективность в отношении ТФПО составляет 93%, и селективность в отношении 2,2,3,3,4,4,5,5-октафтор-1-пентанола составляет 7%. Эту смесь анализируют с применением фтористого электрода для определения содержания кислоты и подтверждают, что содержание кислоты составляет 2636 ч/млн, на основе FH расчета.
Сравнительный пример D
Повторяют методику примера С за исключением того, что давление ТФЭ устанавливают на уровне 0,9 МПа.
Смешанную жидкость анализируют с применением газовой хроматографии (ГХ), в соответствии с которой она содержит 55% метанола, 40% ТФПО и 4% 2,2,3,3,4,4,5,5-октафтор-1-пентанола. Далее, превращение метанола составляет 15%, и селективность в отношении ТФПО составляет 91%, и селективность в отношении 2,2,3,3,4,4,5,5-октафтор-1-пентанола составляет 9%. Эту смесь анализируют с применением фтористого электрода для определения содержания кислоты и подтверждают, что содержание кислоты составляет 3043 ч/млн, на основе FH расчета.
Анализ
Как видно из представленных выше примеров (данное изобретение) и сравнительных примеров, доказано, что аккумуляция кислоты при непрерывном способе в соответствии с данным изобретением подавляется и неожиданно значительно меньше, чем при применении периодического способа Сравнительных примеров.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФТОРТЕЛОМЕРЫ АЛКИЛКЕТОНОВ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) И СПОСОБ ПОЛУЧЕНИЯ ФУНКЦИОНАЛЬНЫХ ПОКРЫТИЙ НА ИХ ОСНОВЕ | 2008 |
|
RU2381237C2 |
| СОПОЛИМЕР ТЕТРАФТОРЭТИЛЕНА | 2003 |
|
RU2315777C2 |
| СПОСОБ ПОЛУЧЕНИЯ СОПОЛИМЕРОВ ТЕТРАФТОРЭТИЛЕНА С 2 - 5 МОЛ.% ПЕРФТОРПРОПИЛВИНИЛОВОГО ЭФИРА | 1999 |
|
RU2156777C1 |
| СПОСОБ ПОЛУЧЕНИЯ МОДИФИЦИРОВАННЫХ СОПОЛИМЕРОВ ТЕТРАФТОРЭТИЛЕНА С ЭТИЛЕНОМ | 1999 |
|
RU2156776C1 |
| СПОСОБ ПОЛУЧЕНИЯ СТОЙКИХ К РАСТРЕСКИВАНИЮ СОПОЛИМЕРОВ ТЕТРАФТОРЭТИЛЕНА С ЭТИЛЕНОМ | 1978 |
|
SU1840101A1 |
| СПОСОБ ПОЛУЧЕНИЯ СОПОЛИМЕРОВ ТЕТРАФТОРЭТИЛЕНА С ГЕКСАФТОРПРОПИЛЕНОМ | 2001 |
|
RU2206580C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТЕРМОПЕРЕРАБАТЫВАЕМЫХ СОПОЛИМЕРОВ ТЕТРАФТОРЭТИЛЕНА С ГЕКСАФТОРПРОПИЛЕНОМ | 2011 |
|
RU2463312C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРФТОРИРОВАННОГО ФУНКЦИОНАЛИЗИРОВАННОГО СОПОЛИМЕРА МЕТОДОМ ЭМУЛЬСИОННОЙ СОПОЛИМЕРИЗАЦИИ | 2011 |
|
RU2454431C1 |
| СПОСОБ СЕЛЕКТИВНОГО ПОЛУЧЕНИЯ CFI | 2006 |
|
RU2395483C2 |
| СПОСОБ ОКИСЛЕНИЯ ТЕТРАФТОРЭТИЛЕНА ДО ПОЛУЧЕНИЯ ПЕРОКСИДНЫХ ПРОСТЫХ ПЕРФТОРПОЛИЭФИРОВ | 1997 |
|
RU2194725C2 |
Изобретение относится к усовершенствованному способу получения фторалканола с высокими степенью чистоты и селективностью, который используется для получения, например, гидрофобизующей или гидрофилизующей добавок, поверхностно-активного вещества или цветного проявителя. Способ получения фторалканола формулы 1 включает проведение реакции между полифторолефином формулы 2 и алканолом формулы 3 в присутствии радикального инициатора, где полифторолефин формулы 2, алканол формулы 3 и радикальный инициатор непрерывно подают в реактор, где между ними проводят реакцию при 105-135°С, а образованный фторалканол формулы 1 непрерывно отводят: H-(RfCFCF2)n-CR1R2-OH (1), RfCF=CF2 (2), CHR1R2-OH (3), при том условии, что символы в формулах имеют следующие значения: Rf: атом фтора или С1-4 полифторалкильная группа; R1, R2: каждый, независимо, атом водорода или С1-3 алкильная группа; и n: целое число в диапазоне от 1 до 4. 6 з.п. ф-лы, 1 ил.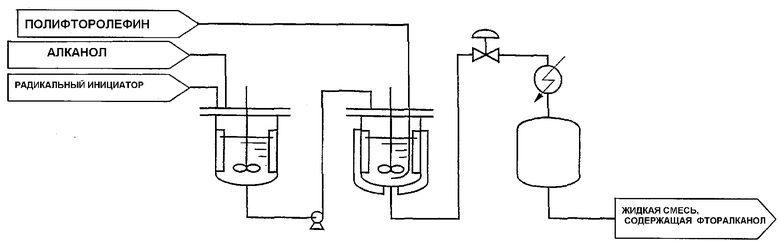
при том условии, что символы в формулах имеют следующие значения:
Rf - атом фтора или С1-4 полифторалкильная группа;
R1, R2 - каждый, независимо, атом водорода или С1-3 алкильная группа, и
n - целое число от 1 до 4.
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИФТОРИРОВАННЫХ СПИРТОВ | 1999 |
|
RU2150459C1 |
Авторы
Даты
2005-10-27—Публикация
2001-09-05—Подача