Изобретение относится к медицине, в частности к микробиологии, и предлагает средство для диагностики лекарственной чувствительности L-форм Mycobacterium tuberculosis к рифампицину. Использование указанного средства основано на применении биологического микрочипа «ТБ-Биочип (РИФ)» для обнаружения в rpoB-гене ДНК L-форм микобактерий мутаций, обусловливающих резистентность к рифампицину.
Туберкулез является одной из самых актуальных проблем современной медицины во всем мире. Сложившаяся в Российской Федерации эпидемическая ситуация с туберкулезом оценивается в последние годы как весьма неблагоприятная.
В связи с широким применением специфических противотуберкулезных препаратов и антибиотиков наблюдаются резкие изменения биологических свойств, морфологии и других характеристик возбудителя туберкулеза и переход его в нестабильные и условно стабильные L-формы (Шмелев Н.А., Дорожкова И.Р.., Земскова З.С. - Персистирование возбудителя туберкулеза в организме в виде L-форм и их повреждающее действие // Вестник АМН СССР - 1976. - №5 - С.29-37). L-формы микобактерий туберкулеза (МБТ) являются закономерной фазой филогенетического развития возбудителя и основной формой его персистирования в организме практически здоровых инфицированных МБТ людей, обусловливая потенциальную опасность развития эндогенной реактивации и рецидивов процесса при снижении иммунобиологической настроенности организма. Выделение L-форм МБТ у практически здоровых в отношении туберкулеза людей является важным прогностическим признаком, свидетельствующим о начале эндогенной реактивации процесса и/или развитии рецидива, а у больных туберкулезом - свидетельством активности процесса.
С другой стороны, одной из причин, способствующих подъему заболеваемости туберкулезом, является широкое распространение лекарственно-устойчивых штаммов микобактерий, устойчивых к одному из наиболее эффективных противотуберкулезных препаратов - рифампицину.
В то же время известно, что резистентность к рифампицину в 95% случаев является маркером лекарственной устойчивости к изониазиду, что опосредованно свидетельствует о наличии множественной лекарственной устойчивости.
До настоящего времени не существует способа определения лекарственной чувствительности L-форм. Классические методы определения лекарственной чувствительности бактериальных форм МБТ не могут быть использованы в отношении L-форм, так как последние культивируются с большим трудом и в процессе субкультивирования на питательных средах часто утрачивают жизнеспособность. Определение их лекарственной чувствительности возможно только в случае получения реверсии в бактериальную форму, что далеко не всегда достижимо и требует от 4 до 9 месяцев пассирования на питательных средах.
Развитие и совершенствование молекулярно-биологических методов открыло новые перспективы диагностики лекарственной чувствительности возбудителя туберкулеза, основанные на анализе последовательностей ДНК Mycobacterium, поскольку для ряда препаратов известны фрагменты генов, мутации в которых приводят к возникновению резистентности.
Определение типа мутации L-форм, выделяемых из организма больного, может оказаться ключевым моментом в выборе схемы лечения. На основании анализа мутаций, приводящих к устойчивости к рифампицину, а затем и к другим препаратам, можно до начала лечения определить, имеет ли смысл назначать данному больному рифампицин, или необходимо использовать резервные препараты второго ряда, или же своевременно решать вопрос о хирургическом вмешательстве и степени эпидемиологической опасности очага.
Принципиально новым подходом к выявлению мутаций, в том числе ответственных за возникновение лекарственной устойчивости у патогенных микроорганизмов, являются биологические микрочипы - уникальное средство биомедицинской диагностики. Микрочипы успешно применяют для оценки генетического полиморфизма ДНК. Способность зондов гибридизоваться с тестируемой ДНК сильно изменяется при наличии даже единичных мисматчей. Это позволяет с высокой эффективностью осуществлять поиск и выявление полиморфизма генома даже на уровне различий в отдельных нуклеотидах (Патрушев Л.И. Экспрессия генов. - М.: Наука, - 2000, - с.462-463).
В настоящее время в Институте молекулярной биологии им. В.А.Энгельгардта РАН создан биологический микрочип («ТБ-Биочип (РИФ)»), способный детектировать 28 вариантов мутаций гена rpoB, обусловливающих устойчивость микобактерий к рифампицину. Этот метод позволяет получить сведения о наличии лекарственной устойчивости к рифампицину в максимально короткие (двое суток) сроки, тогда как классические микробиологические методы требуют для этого 3-4 месяцев.
Изложенное определяет актуальность предлагаемого изобретения как средства для ускоренного определения лекарственной устойчивости L-форм МБТ к рифампицину с помощью вышеназванного микрочипа.
Таким образом, известен молекулярно-биологический метод определения резистентности МБТ к рифампицину с помощью биологических микрочипов.
Аналогом данного изобретения является работа коллектива сотрудников Института молекулярной биологии им. В.А.Энгельгардта Российской Академии Наук - разработчиков биологического микрочипа «ТБ-Биочип (РИФ)»: Михайловича В.М., Лапы, С.А., Грядунова Д.А и др. - «Использование методов гибридизации и ПЦР на специализированном ТБ-микрочипе для обнаружения рифампицин-резистентных штаммов Mycobacterium tuberculosis» // Бюлл. эксп. биол. и медицины. - 2001. - T.131. - №1. - С.112-117.
Метода определения лекарственной чувствительности L-форм до настоящего времени не существует.
Методика применения предлагаемого средства для определения лекарственной чувствительности L -форм МБТ включает следующие этапы:
1. Выделение из диагностического материала L-форм и доказательство их таксономической принадлежности к L-формам М.tuberculosis (Дорожкова И.Р., Кочемасова З.Н., Дыхно М.М. - Выделение L-форм микобактерий туберкулеза из патологического материала // Методические рекомендации. Минздрав СССР. - М., 1984, - 19 стр.).
2. Определение чувствительности к рифампицину с помощью биологического микрочипа «ТБ-Биочип (РИФ)»:
- выделение ДНК, полученных при культивировании L-форм МБТ с последующей ее амплификацией в процессе проведения двухстадийной мультиплексной ПЦР. Электрофорез полученных продуктов ПЦР в 3% агарозном геле, пропитанном этидиум бромидом;
- гибридизация полученных продуктов амплификации с дискриминирующими олигонуклеотидными зондами, находящимися на биологическом микрочипе. Регистрация и анализ результатов гибридизации производятся с помощью сверхчувствительной ПЗС-камеры по специальной компьютерной программе;
- наличие мутаций в исследуемой области rpoB-гена определяется по силе свечения меченного олигонуклеотида. Обнаружение их в исследуемом кодоне, с которым произошла гибридизация, свидетельствует о резистентности данного штамма к рифампицину.
Контроль результатов определения лекарственной чувствительности L-форм осуществлялся двумя методами:
- методом абсолютных концентраций для бактериальных штаммов МБТ, выделенных из того же материала, что и L-формы, и
- молекулярно-биологическим методом с помощью микрочипа «ТБ-Биочип (РИФ)» для образцов ДНК L-форм МБТ, а также ДНК бактериальных форм МБТ, полученных из биологических образцов и выделенных из них на питательных средах штаммов МБТ.
В процессе исследований было разработано предлагаемое средство, отличие которого состоит в том, что известный биочип «ТБ-Биочип (РИФ)» используется по новому назначению для определения чувствительности L-форм МБТ к лекарственному препарату рифампицину.
Предлагаемое средство было разработано в процессе исследования 414 образов диагностического материала от больных впервые выявленным туберкулезом легких. Результаты этого исследования представлены в таблице 1.
Результаты выделения различных форм МБТ из диагностического материала
Как видно из таблицы 1, в 18 случаях из одного и того же диагностического материала были одновременно выделены и бактериальные, и L-формы МБТ. Для контроля результатов определения лекарственной чувствительности L-форм к рифампицину использовали данные параллельного определения чувствительности 18 бактериальных штаммов МБТ, выделенных из того же диагностического материала.
Лекарственную чувствительность бактериальных форм МБТ к рифампицину определяли стандартным методом абсолютных концентраций и параллельно методом биологических микрочипов на «ТБ-Биочип (РИФ)», L-форм - только методом биологических микрочипов на «ТБ-Биочип (РИФ)». Результаты этого исследования представлены в таблице 2.
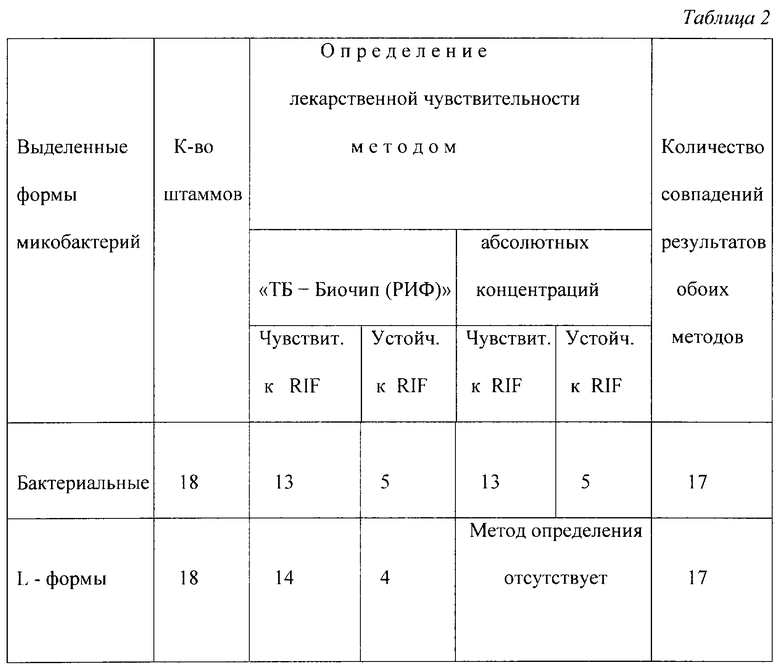
Как следует из таблицы 2, у 17 (94,4%) из 18 параллельно исследованных штаммов МБТ и L-форм отмечено полное совпадение результатов определения лекарственной чувствительности обоими методами. Один штамм L-форм МБТ (5,5%) оказался чувствительным к рифампицину, тогда как у выделенного из того же материала бактериального штамма МБТ классическим методом и биочипом установлено наличие устойчивости к рифампицину.
Таким образом, суммарный процент несовпадения результатов определения лекарственной чувствительности бактериальных и L-форм МБТ составил 5,5%.
Для демонстрации клинической значимости предлагаемого способа определения лекарственной чувствительности L-форм МБТ приводим следующее клиническое наблюдение.
Больной П., 32 лет, поступил в стационар с диагнозом впервые выявленного инфильтративного туберкулеза верхней доли правого легкого с наличием полости распада и обсеменения. При микробиологическом и молекулярно-биологическом исследованиях бронхоальвеолярного лаважа (БАЛ) и 3 порций мокроты выделить бактериальные формы МБТ не удалось. Обнаружены только L-формы МБТ (см. Методические рекомендации - стр.4). С помощью биологического микрочипа «ТБ-Биочип (РИФ)» в rpoB-гене ДНК L-форм была выявлена мутация, что свидетельствовало о наличии у больного лекарственной устойчивости к наиболее эффективному противотуберкулезному препарату - рифампицину.
На основании полученных лабораторных данных на 4-ые сутки пребывания больного в клинике была произведена коррекция первоначально назначенного химиотерапевтического режима с отменой ранее назначенного рифампицина и введением в схему лечения резервного препарата протионамида. Это способствовало эффективному лечению и впоследствии сравнительно быстрому излечению больного.
ЛИТЕРАТУРА
1. Михайлович В.М., Лапа С.А., Грядунов Д.А и др. - Использование методов гибридизации и ПЦР на специализированном ТБ-микрочипе для обнаружения рифампицин-резистентных штаммов Mycobacterium tuberculosis // Бюлл. эксп. биол. и медицины. - 2001. - Т.131. - №1. - C.112-117.
Изобретение относится к микробиологии и биотехнологии и может найти применение в медицине. В изобретении описывается применение биологического микрочипа «ТБ-Биочип (РИФ)» для определения лекарственной чувствительности к рифампицину L-форм микобактерий туберкулеза. Предварительно подтверждают таксономическую принадлежность L-форм к микобактериям туберкулеза и выделяют ДНК из L-форм микобактерий туберкулеза, которую затем исследуют с использованием микрочипа «ТБ-Биочип (РИФ)». Лекарственную чувствительность к рифампицину определяют по наличию мутации в rpoB-гене. Использование «ТБ-Биочипа (РИФ)» для определения лекарственной чувствительности к рифампицину L-форм микобактерий туберкулеза обеспечивает коррекцию лекарственного лечения больных туберкулезом, у которых своевременно выявлена лекарственная устойчивость L-форм микобактерий туберкулеза к рифампицину. 2 табл.
Применение биологического микрочипа «ТБ-Биочип (РИФ)» для определения лекарственной чувствительности L-форм Mycobacterium tuberculosis к рифампицину.
| СПОСОБ ОПРЕДЕЛЕНИЯ ТОЧЕЧНЫХ НУКЛЕОТИДНЫХ ЗАМЕН В ДНК МИКОБАКТЕРИЙ, СПОСОБ ДИАГНОСТИКИ УСТОЙЧИВОСТИ МИКОБАКТЕРИЙ К РИФАМПИЦИНУ, БИОЧИП ДЛЯ ОСУЩЕСТВЛЕНИЯ ЭТИХ СПОСОБОВ | 2000 |
|
RU2175015C1 |
| ВИШНЕВСКАЯ Е.Б | |||
| и др | |||
| Идентификация L-форм микобактерий туберкулезного комплекса с применением полимеразной цепной реакции | |||
| Научно-практический журнал «Проблемы туберкулеза», 4, 2001, с.38-41. | |||
Авторы
Даты
2005-10-27—Публикация
2003-12-16—Подача