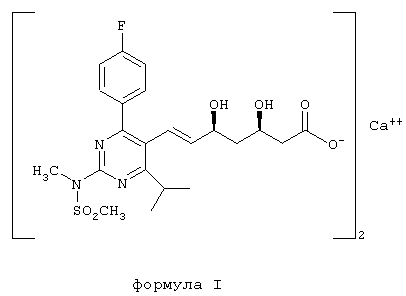
Настоящее изобретение относится к фармацевтическим композициям и, более конкретно, к фармацевтической композиции, содержащей (Е)-7-[4-(4-фторфенил)-6-изопропил-2-[метил(метилсульфонил)амино]пиримидин-5-ил]-(3R,5S)-3,5-дигидроксигепт-6-еновую кислоту или ее фармацевтически приемлемую соль (далее в тексте упоминаемая, как «Агент»). В частности, к натриевым и кальциевым солям, особенно к кальциевой соли, т.е. кальциевой соли бис [(Е)-7-[4-(4-фторфенил)-6-изопропил-2-[метил(метилсульфонил)амино]пиримидин-5-ил]-(3R,5S)-3,5-дигидроксигепт-6-еновой кислоты (Формула I которой представлена ниже).
Агент раскрыт как ингибитор 3-гидрокси-3-метилглютарил СоА редуктазы (HMG СоА редуктаза) в заявке на Европейский патент. Публикация №0521471 и в Bioorganic and Medicinal Chemistry, (1997), 5(2), 437-444, и он используется для лечения гиперхолестеринемии, гиперлипидпротеинемии, и атеросклероза.
Проблема, связанная с указанным Агентом, состоит в том, что это вещество особенно чувствительно к деградации в определенных условиях. Основными продуктами разложения являются соответствующий (3R,5S) лактон (далее в тексте «лактон») и продукт окисления (далее в тексте «В2»), в котором гидрокси группа, соседствующая с углерод-углеродной двойной связью, окисляется до кетонной функциональной группы. Существующая возможность значительной деградации Агента затрудняет получение и производство фармацевтической композиции с приемлемым сроком хранения как рыночного продукта.
Фармацевтические рецептуры некоторых солей 7-замещенных-3,5-дигидрокси-6-гептеновой кислоты, которые являются ингибиторами HMG СоА редуктазы, раскрыты в UK Patent 2262229 и отмечается, что они чувствительны к разложению под действием рН среды. Рассматриваемые рецептуры требуют присутствия щелочной среды (например, карбоната или бикарбоната), которая способна создавать рН, по меньшей мере, 8 в водном растворе или дисперсионной среде рассматриваемых композиций.
Однако авторы установили, что для рассматриваемого Агента недостаточно повышение стабильности только с помощью регулирования рН рецептуры. Заявители обнаружили, что стабильность Агента повышается в результате выбора неорганической соли, которую добавляют в композицию и которая содержит один или более поливалентных неорганических катионов. Не ограничиваясь конкретной теорией, заявитель полагает, что поливалентный неорганический катион стабилизирует структуру Агента и делает его менее чувствительным к окислению и/или лактонизации.
Отличительными признаками изобретения являются
(1) Фармацевтическая композиция, включающая Агент в качестве активного ингредиента и неорганическую соль с поливалентным катионом.
(2) Применение неорганической соли с поливалентным катионом в качестве стабилизирующего агента фармацевтической композиции, включающей Агент.
Предпочтительными отличительными признаками изобретения являются следующие:
(1) Агент присутствует в композиции в количестве более 5 мг, предпочтительно более 10 мг. Исключаются композиции, в которых Агент присутствует в количестве 1, 2, 5 и 10 мг. Предпочтительные композиции представляют собой такие, в которых количество Агента составляет 20, 40 или 80 мг.
(2) Стабилизирующее соединение не является синтетическим гидротальцитом.
(3) Фармацевтическую композицию формируют в виде таблетки или порошка.
Предпочтительная фармацевтическая композиция настоящего изобретения представляет собой таблетку.
Поливалентный катион неорганической соли может быть выбран из следующих элементов: кальция, магния, цинка, алюминия и железа или их смеси. Предпочтительными поливалентными катионами являются: кальций, алюминий и магний или их смесь. Особенно предпочтительные поливалентные катионы представляют собой алюминий и магний или их смесь.
Противоанион неорганической соли может быть выбран из фосфата, карбоната, силиката, оксида и метасиликата.
Предпочтительные противоанионы выбирают из карбоната, силиката, оксида и метасиликата. Наиболее предпочтительные противоанионы выбирают из силиката, оксида или метасиликата.
Индивидуальные аспекты настоящего изобретения включают неорганическую соль с поливалентным катионом, выбранным из любых из указанных выше, а противоанион также выбирают из любого из указанных выше.
Предпочтительными неорганическими солями, предназначенными для использования в настоящем изобретении, могут служить: алюминий-магний метасиликат (Neusolin™, Fuji Chemical Industry Limited), двухосновный или трехосновный фосфат кальция, трехосновный фосфат магния и трехосновный фосфат алюминия. Особенно предпочтительными соединениями являются алюминий-магний метасиликат и трехосновный фосфат кальция.
Также предпочтительно, чтобы рассматриваемая композиция обладала хорошей текучестью для облегчения переработки в единичные дозированные формы, предназначенные для перорального применения, например, в таблетки, а также хорошими характеристиками, касающимися дезинтеграции и растворения при формировании таблеток для перорального применения, причем такие таблетки могут включать различные эффективные дозы.
Соотношение между неорганической солью и Агентом в фармацевтической композиции находится в интервале 1:80-50:1 мас., например, 1:50-50:1 мас., вплоть до 1:10-10:1 мас., и более предпочтительно 1:5-10:1 мас.
Предпочтительно, фармацевтическую композицию настоящего изобретения формируют в пероральную лекарственную форму, например в таблетки. Согласно дополнительному аспекту настоящее изобретение включает фармацевтическую композицию, содержащую Агент, неорганическую соль с поливалентным катионом и один или более наполнителей, связующих агентов, дезинтеграторов или смазывающих агентов. Другой аспект настоящего изобретения относится к фармацевтической композиции для перорального применения, включающей Агент, один или более наполнителей, одно или более связующих, один или более дезинтеграторов, один или более смазывающих агентов и неорганическую соль с поливалентным катионом.
Подходящие наполнители включают, например, лактозу, сахар, крахмалы, модифицированные крахмалы, маннит, сорбит, неорганические соли, производные целлюлозы (например, микрокристаллическую целлюлозу, целлюлозу), сульфат кальция, ксилит и лактит.
Подходящие связующие агенты включают, например, поливинилпирролидон, лактозу, крахмалы, модифицированные крахмалы, сахара, аравийскую камедь, трагакант, гуаровую смолу, пектин, связующие на основе воска, микрокристаллическую целлюлозу, метилцеллюлозу, карбоксиметилцеллюлозу, гидроксипропилметилцеллюлозу, гидроксиэтилцеллюлоэу, гидроксипропилцеллюлозу, сополивидон, желатин и альгинат натрия.
Подходящие дезинтеграторы включают, например, кросскармелозу натрия, кросповидон, поливинилпирролидон, натрийкрахмалгликолят, кукурузный крахмал, микрокристаллическую целлюлозу, гидроксипропилметилцеллюпозу и гидроксипропилцеллюлозу.
Подходящие смазывающие агенты включают, например, стеарат магния, стеариновую кислоту, пальмитиновую кислоту, стеарат кальция, тальк, карнаубский воск, гидрированные растительные масла, минеральное масло, полиэтиленгликоли и стеарилфумарат натрия.
Дополнительные традиционные эксципиенты, которые могут добавляться в композицию, включают консерванты, стабилизаторы, антиоксиданты, кондиционеры на основе текучих оксидов кремния, антиадгезивы, или глиданты.
Другие подходящие наполнители, связующие агенты, дезинтеграторы, смазывающие вещества и дополнительные эксципиенты, которые могут использоваться, описаны в Handbook of Pharmaceutical Excipients, 2nd Edition, American Pharmaceutical Association; The theory and practice of industrial pharmacy, 2nd Edition, Lachman, Leon, 1976; Pharmaceutical dosage forms: Tablets Volume 1, 2nd edition, Lieberman, Hebert A., et al, 1989; Modern pharmaceutics, Banker, Gilbert and Rhodes, Christopher T, 1979; and Remington's Pharmaceutical Sciences, 15th Edition, 1975.
Обычно Агент присутствует в количестве в интервале 1-50%, например, 1-25%, или 1-20%, и предпочтительно 5-18 мас.%.
Обычно неорганическая соль, такая как трехосновный фосфат кальция, присутствует в количестве 1-25%, например, 1-20%, или 5-18 мас.%.
Как правило, один или более наполнителя присутствуют в композиции в количестве 30-90 мас.%.
Обычно один или более связующих агента присутствуют в количестве 2-90 мас.%.
Как правило, один или более дезинтеграторов присутствуют в количестве 2-10%, особенно, 4-6 мас.%.
Следует иметь в виду, что конкретный эксципиент может выполнять функции как связующего агента, так и наполнителя или связующего агента, наполнителя и дезинтегратора. Обычно, общее количество наполнителя, связующего агента и дезинтегратора составляет, например, 70-90% от массы композиции.
Как правило, в композиции присутствуют один или более смазывающих веществ в количестве 0,5-3%, особенно, 1-2 мас.%.
Фармацевтическая композиция настоящего изобретения может быть получена с использованием стандартных методик и способов производства, обычно известных в данной области техники, например, в результате сухого смешивания компонентов. Так например, Агент и неорганическая соль с поливалентным катионом, один или более наполнителей, один или более связующих веществ и один или более дезинтеграторов, а также дополнительных эксципиентов, если желательно, смешивают друг с другом. Компоненты смеси перед перемешиванием, или сама смесь могут быть пропущены через отверстия сита, например, сита с отверстиями 400-700 мкм. Смазочное вещество, которое также может пропускаться через сито, затем добавляют в смесь, и перемешивание продолжают до получения гомогенной смеси. Затем полученную смесь прессуют в таблетки. С другой стороны, можно использовать технику влажного гранулирования. Так например, Агент и неорганическая соль с поливалентным катионом, один или более наполнителей, одно или более связующих веществ и часть дезинтегратора, а также другие дополнительные эксципиенты, если желательно, смешивают друг с другом, например, с использованием гранулятора, и полученный порошок гранулируют в присутствии небольшого объема очищенной воды. Гранулят сушат и пропускают через мельницу. Оставшиеся количества дезинтегратора и смазочного вещества добавляют к размолотому грануляту и после перемешивания полученную в результате гомогенную смесь прессуют в таблетки. Следует иметь в виду, что различные модификации способа сухого перемешивания и влажной грануляции, включающие порядок добавления компонентов и их скрининга и перемешивания до прессования в таблетки, могут осуществляться в соответствии с принципами, известными в данной области техники.
Далее, на таблетки может быть нанесено покрытие, например, методом распыления пленкообразующих композиций на водной основе. Такое покрытие может содержать, например, лактозу, гидроксипропилметилцеллюлозу, триацетин, диоксид титана и оксиды железа. Комбинации ингредиентов покрытия являются коммерчески доступными продуктами, например, те, что описаны в следующих ниже примерах. Рассматриваемые покрытия могут составлять, например, 0,5-10% от массы состава для таблетирования, особенно, 1-6%, и предпочтительно, 2-3%. Покрытия, содержащие оксиды железа, особенно предпочтительны, поскольку они уменьшают скорость образования продуктов фотодеградации Агента.
В соответствии со сказанным выше отличительным признаком изобретения является фармацевтическая композиция, содержащая Агент, причем указанная композиция имеет светозащитное покрытие на основе оксидов железа.
Другой аспект настоящего изобретения относится к способу получения стабилизированной фармацевтической композиции, который заключается в смешивании Агента с неорганической солью с поливалентным катионом. Еще один аспект настоящего изобретения относится к способу получения стабилизированной фармацевтической композиции, который заключается в введении в фармацевтическую композицию, содержащую Агент, неорганической соли с поливалентным катионом.
Пример 1
Агент, микрокристаллическую целлюлозу, моногидрат лактозы, натрийкрахмалгликолят, трехосновный фосфат кальция и бутоксилированный гидрокситолуол перемешивали друг с другом в течение 10 минут. Стеарат магния пропускали через сито с отверстиями # 40 меш (425 мкм) и добавляли в смесь, после чего перемешивание продолжали в течение трех минут. Полученную в результате гомогенную смесь прессовали в таблетки.
Указанные таблетки хранили при 70°С/80% относительной влажности в течение одной недели. Через неделю было установлено, что смесь содержит всего 0,11% мас./мас. продукта окисления В2 и только 0,50% мас./мас. лактона.
Пример 2
Агент, повидон, маннит, микрокристаллическую целлюлозу, бутоксилированный гидрокситолуол, трехосновный фосфат кальция и натрийкрахмалгликолят (в указанных выше количествах) перемешивали в течение 5-60 минут. Стеарат магния пропускали через сито #40 меш (425 мкм) и добавляли в смесь, после чего перемешивание продолжали в течение трех минут. Полученную в результате гомогенную смесь прессовали в таблетки. На прессованные таблетки наносили покрытие путем распыления смеси из гидроксипропилметилцеллюлозы, полиэтиленгликоля 400, диоксида титана и оксида железа (выпускаемого под маркой Spectrablend™ фирмой Warner-Jenkinson) и воды в емкости для нанесения покрытия. Привес за счет нанесенного покрытия составил 1-6%, предпочтительно, 2-3% мас./мас.
Таблетки хранили при 70°С/относительной влажности 80% в течение одной недели. Через неделю было установлено, что образовалось всего лишь 0,06% мас./мас. продукта окисления В2 и лишь 2,22% мас./мас. лактона.
Пример 3
Агент и кросповидон смешивали друг с другом в течение 5 минут и полученную смесь пропускали через сито с размером отверстий 400-700 мкм. После этого через сито пропускали небольшое количество микрокристаллической целлюлозы. Просеянный материал в течение 10 минут перемешивали с другими ингредиентами, исключая смазочное вещество. Стеарат магния пропускали через # 40 меш (425 мкм) сито и добавляли к смеси, после чего перемешивание продолжали еще в течение 3 минут. Полученную в результате гомогенную смесь прессовали в таблетки. На спрессованные таблетки наносили покрытие путем распыления по поверхности смеси из моногидрата лактозы, гидроксипропилметилцеллюлозы, триацетина и оксида железа (выпускаемого фирмой Colorcon, как Opadry IIТМ), а также воды в емкости для нанесения покрытий. Привес за счет покрытия составил 1-6% мас./мас., предпочтительно, 2-3% мас./мас.
Полученные таблетки хранили при 70°С/80% относительной влажности в течение недели. По истечении указанного времени было зафиксировано образование лишь 0,19% мас./мас. продукта окисления В2 и только 2,71% мас./мас. лактона.
Пример 4
Часть трехосновного фосфата кальция и бутоксилированного гидрокситолуола смешивали в течение 30 секунд в мешке. Агент, повидон, оставшееся количество трехосновного фосфатата кальция, микрокристаллическую целлюлозу, моногидрат лактозы, смесь трехосновный фосфат кальция/бутоксилированный гидрокситолуол и часть натрийкрахмалгликолята смешивали в течение 30 секунд в грануляторе. Порошкообразную смесь гранулировали в присутствии очищенной воды в течение 1 минуты при скорости добавления 70мг/таблетка/минута. Гранулят сушили в сушилке с псевдоожиженным слоем при 50°С до тех пор, пока потери от сушки не достигали величины менее 2% мас./мас. Высушенный гранулят пропускали через мельницу (например, Comil™). Размолотый гранулят и оставшееся количество натрийкрахмалгликолята перемешивали в течение 5 минут. Стеарат магния пропускали через # 40 меш (425 мкм) сито и добавляли к смеси, после чего перемешивание продолжали в течение трех минут. Полученную в результате смесь прессовали в таблетки.
Полученные таблетки хранили при 70°С/80% относительной влажности в течение одной недели. По истечении указанного времени образовывалось лишь 0,23% мас./мас. продукта окисления В2 и только 0,28 мас./мас. лактона.
Изобретение относится к области фармацевтики и относится к фармацевтической композиции. Изобретение заключается в том, что содержит в качестве активного ингредиента (Е)-7-[4-(4-фторфенил)-6-изопропил-2-метил(метилсульфонил)амино]пиримидин-5-ил]-(3R,5S)-3,5-дигидроксигепт-6-еновую кислоту или ее фармацевтически применимую соль, а также неорганическую соль с поливалентным катионом. Также предлагается способ получения стабилизированной фармацевтической композиции. Изобретение обеспечивает получение стабилизированной фармацевтической композиции. 4 н. и 21 з.п. ф-лы.
(i) неорганическая соль не является синтетическим гидротальцитом и
(ii) противоанион неорганический соли не является фосфатом.
(i) неорганическая соль не является синтетическим гидротальцитом и
(ii) противоанион неорганической соли не является фосфатом.
(i) неорганическая соль не является синтетическим гидротальцитом и
(ii) противоанион неорганической соли не является фосфатом.
| СПОСОБ ОТБОРА ЖИВОТНЫХ ПО ПРИЗНАКАМ, НАСЛЕДУЕМЫМ ПО МЕХАНИЗМУ РОДИТЕЛЬСКОГО ИМПРИНТИНГА | 1999 |
|
RU2262229C2 |
| БЕНЗОЛСУЛЬФОНАМИДНЫЕ ПРОИЗВОДНЫЕ ПИРИМИДИНА ИЛИ ИХ СОЛИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С АКТИВНОСТЬЮ ЭНДОТЕЛИНА | 1992 |
|
RU2086544C1 |
| ПРОИЗВОДНЫЕ ПИРИМИДИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1994 |
|
RU2098411C1 |
| RU 94038256 A1, 27.08.1996. | |||
Авторы
Даты
2005-11-20—Публикация
2000-08-04—Подача