Изобретение относится к органической химии, точнее к методу синтеза замещенных нитроанилинов путем селективного восстановления нитрогруппы в 2- и 4-алкиламино-3,5-динитробензойных кислотах. Полученные таким путем замещенные орто-фенилендиамины могут использоваться для синтеза гетероциклических соединений, например бензимидазолов. Наличие в них карбоксильной и нитрогруппы дает возможность для дальнейшей модификации этих последних с получением большого набора соединений, обладающих потенциальной биологической активностью.
Известен способ получения аминонитрофенолов селективным восстановлением соответствующих динитрофенолов гидросульфидом натрия (патент США №4115652, 30.03.77, 19.09.78). Этот метод позволяет получить аминонитрофенолы с хорошим выходом (74-99%), однако он неприемлем для получения диаминонитробензойных кислот, поскольку дает низкие выходы продуктов, содержащих значительное количество примесей.
Наиболее близким к предлагаемому способу по технической сущности является способ получения 2,3-диамино-5-нитробензойной кислоты, который выбран за прототип, описанный в работе (F.Ullmann, Ann., 366 (1909), 82), заключающийся в селективном восстановлении 2-амино-3,5-динитробензойной кислоты сероводородом в среде водного аммиака. Для завершения реакции требуется 16 часов, количество аммиака не оговорено. Выделение продукта проводится довольно сложным методом: реакционный раствор отфильтровывают от серы, фильтрат упаривают досуха, что не всегда удобно, особенно при получении больших количеств аминонитросоединения. Выделенный продукт содержит примесь исходного динитросоединения, для отделения от которого требуется перекристаллизация. Для восстановления авторы используют "рассчитанное количество сероводорода", однако при таком способе проведения реакции восстанавливающими агентами являются как сульфид, так и гидросульфид аммония, поэтому нельзя точно рассчитать это количество, поскольку в первом случае по уравнению реакции требуется 3 моля сероводорода на 1 моль динитросоединения, во втором - 6 молей.
Задачей изобретения является разработка удобного, быстрого и селективного способа восстановления нитрогруппы в 2- и 4-алкиламино-3,5-динитробензойных кислотах, который позволяет синтезировать большой набор требуемых аминонитросоединений.
Поставленную задачу решает разработанный способ получения 2- и 4-алкиламино-5-нитробензойных кислот формулы Ia, Iб
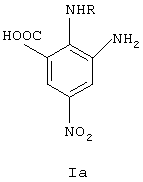
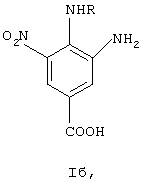
где R=H, алкил, арилалкил, гетероарилалкил, алкоксиалкил, N,N-диметиламиноалкил, восстановлением сероводородом соответствующих динитросоединений, сероводород получают всегда из нонагидрата сульфида натрия и берут в количестве не менее чем 4 моля на 1 моль динитросоединения, процесс ведут в присутствии 3.0-3.5 молей триэтиламина на 1 моль динитросоединения при температуре 50-60°С.
Изобретение иллюстрируется следующим примером
Суспендируют 10.0 г (33.9 ммоль) 2-циклопентиламино-3,5-динитробензойной кислоты в 50 мл воды, прибавляют 16.5 мл (118.7 ммоль) Et3N, полученный раствор нагревают на водяной бане до 57°С. Сероводород получают всегда из нонагидрата сульфида натрия следующим образом: в круглодонную колбу загружают сульфид натрия 32.5 г (135.6 ммоля, что составляет 4 моля на 1 моль динитросоединению), из капельной воронки прибавляют 10%-ный раствор HCl, выделяющийся сероводород пропускают через раствор динитросоединения. Ход реакции контролируют по ТСХ (элюент хлороформ:ацетон 1:1). По окончании реакции смесь охлаждают, подкисляют 10% раствором HCl, отфильтровывают оранжево-красный осадок, для очистки от серы переосаждают из раствора соды 10% раствором HCl, отфильтровывают осадок, получают 6.8 г (75%) 2-циклопентиламино-3-амино-5-нитробензойной кислоты (Ia, R=C5H9); т.пл. 195-200°С (разл.), спектр ЯМР 1Н, δ, м.д. (J, Гц): 8.04 д (1Н, Наром.J=2.80); 7.62, д (1Н, Наром.J=2.80); 4.31, п, (1Н, С5Н9); 1.36-1.85 м (8Н, С5Н9).
Условия проведения синтеза и свойства полученных продуктов сведены в таблицы 1 и 2.
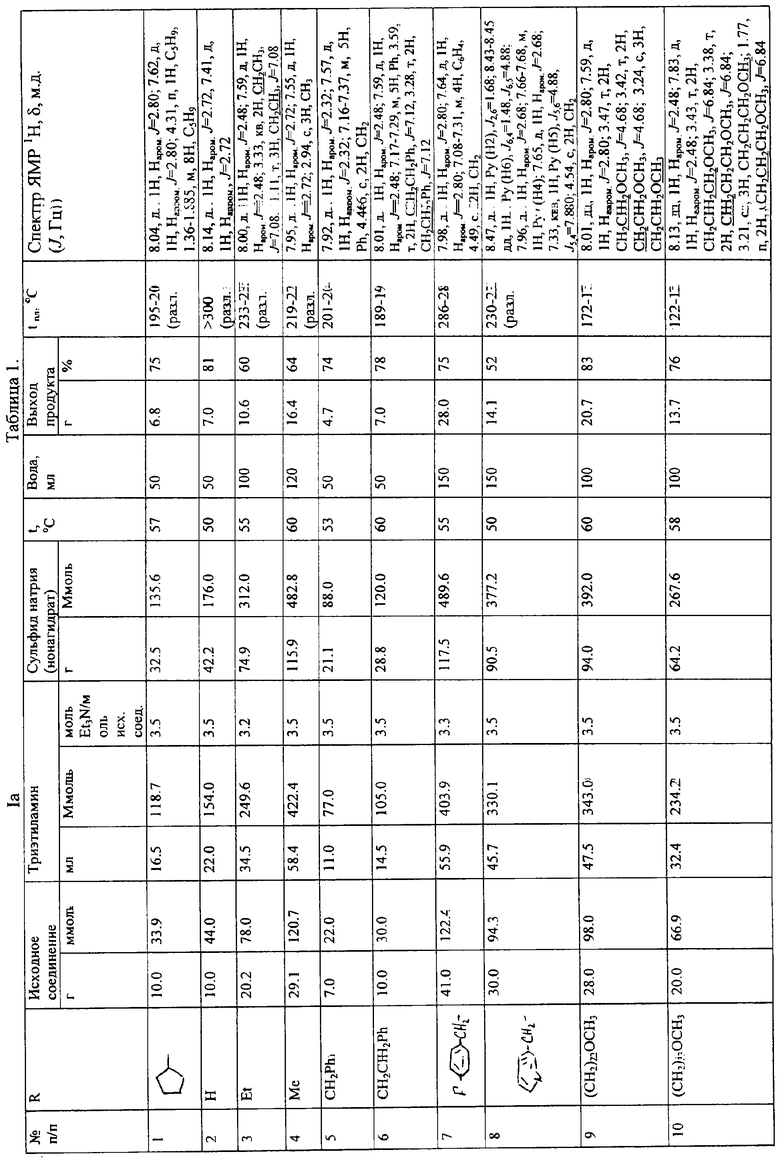
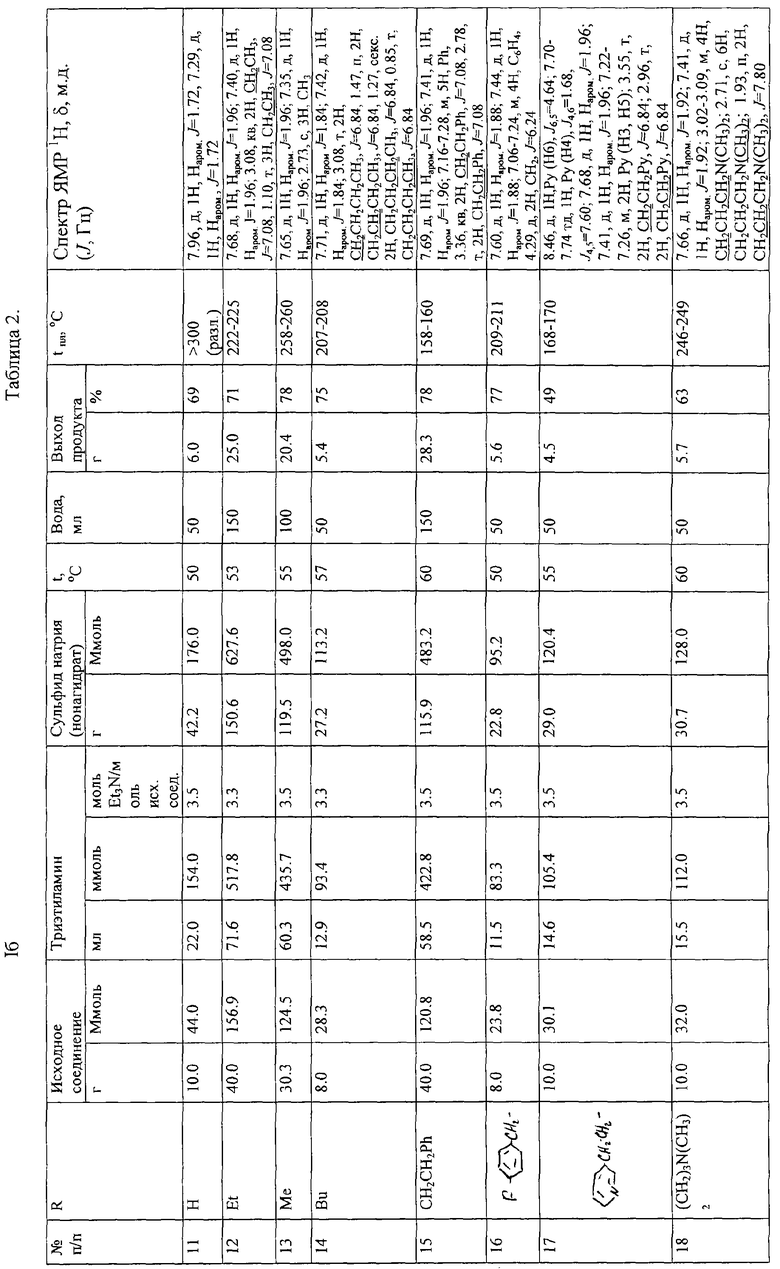
Как видно из приведенных примеров, предлагаемый метод позволяет получить большой набор 2- и 4-алкиламино-3-амино-5-нитробензойных кислот, отличающихся характером алкильного остатка в положении 2 или 4. Полученные продукты имеют высокую чистоту и не нуждаются в дальнейшей очистке, время реакции при одинаковой скорости подачи сероводорода определяется только количеством динитросоединения и составляет от 30 минут для 10-12 г и 1.5-2.0 часа для 30-40 г.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ПЯТИЧЛЕННЫХ ГЕТЕРОЦИКЛОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2000 |
|
RU2380362C2 |
| ПРОИЗВОДНЫЕ ПЯТИЧЛЕННЫХ ГЕТЕРОЦИКЛОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2009 |
|
RU2530882C2 |
| ПРОИЗВОДНЫЕ ПЯТИЧЛЕННЫХ ГЕТЕРОЦИКЛОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2000 |
|
RU2271355C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ МАКРОЛИДОВ И КЕТОЛИДОВ, И ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ ДЛЯ ИХ ПОЛУЧЕНИЯ | 2011 |
|
RU2608390C2 |
| СПОСОБ ПОЛУЧЕНИЯ, СПОСОБЫ ПРИМЕНЕНИЯ И КОМПОЗИЦИИ ЦИКЛОАЛКИЛМЕТИЛАМИНОВ | 2007 |
|
RU2462451C2 |
| КОМПОЗИЦИИ, СИНТЕЗ И СПОСОБЫ ПРИМЕНЕНИЯ АТИПИЧНЫХ НЕЙРОЛЕПТИКОВ НА ОСНОВЕ ХИНОЛИНА | 2008 |
|
RU2497819C2 |
| КОМПОЗИЦИИ, СИНТЕЗ И СПОСОБЫ ПРИМЕНЕНИЯ ИНГИБИТОРОВ ХОЛИНЭСТЕРАЗЫ НА ОСНОВЕ ИНДАНОНА | 2007 |
|
RU2478619C2 |
| ГИДРОКСАМАТНЫЕ ПРОИЗВОДНЫЕ, ПРИМЕНИМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ДЕЗАЦЕТИЛАЗЫ | 2001 |
|
RU2302408C2 |
| ПРОИЗВОДНЫЕ ХИНАЗОЛИНА | 2004 |
|
RU2356896C2 |
| Способ получения леналидомида и интермедиата для его производства | 2020 |
|
RU2730858C1 |
Способ получения 2- и 4-алкиламино-3-амино-5-нитробензойных кислот, использующихся в синтезе гетероциклических соединений, обладающих потенциальной биологической активностью. Способ синтеза 2- и 4-алкиламино-3-амино-5-нитробензойных кислот формулы Iа, Iб
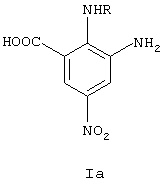
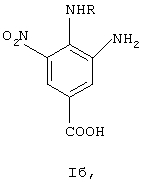
где R=H, алкил, арилалкил, гетероарилалкил, алкоксиалкил, N,N-диметиламиноалкил заключается в селективном восстановлении соответствующих динитросоединений сероводородом, который получают всегда из нонагидрата сульфида натрия, взятом в количестве не менее чем 4 моля на 1 моль динитросоединения, в присутствии 3.0-3.5 моля триэтиламина на 1 моль динитросоединения при температуре 50-60°С, что позволяет получить большой набор соединений, отличающихся заместителем в положении 2 или 4. Метод удобен в применении, а полученные соединения имеют высокую чистоту и не нуждаются в дальнейшей очистке, время реакции при одинаковой скорости подачи сероводорода определяется только количеством динитросоединения. 2 табл.
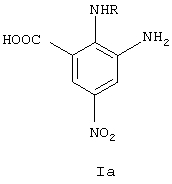

где R=H, алкил, арилалкил, гетероарилалкил, алкоксиалкил, N,N-диметиламиноалкил, восстановлением динитросоединений сероводородом, отличающийся тем, что в качестве динитросоединений используют 2- и 4-алкиламино-3,5-динитробензойные кислоты, сероводород получают всегда из нонагидрата сульфида натрия и берут в количестве менее чем 4 моля на 1 моль динитросоединения, процесс ведут в присутствии триэтиламина, взятого в количестве 3,0-3,5 моля на 1 моль динитросоединения.
| F | |||
| Ullmann Ann | |||
| Химический огнетушитель | 1924 |
|
SU1909A1 |
| Основы синтеза промежуточных продуктов и красителей | |||
| - М.: Госхимиздат, 1955, с | |||
| Арматура для железобетонных свай и стоек | 1916 |
|
SU259A1 |
Авторы
Даты
2005-11-20—Публикация
2004-02-03—Подача