Настоящее изобретение относится к применению волокна кокосового эндосперма в качестве диетической волокнистой составляющей в корме для домашних животных; применению волокна кокосового эндосперма в промышленном производстве кормов для домашних животных; способу приготовления таких кормов для домашних животных и способу кормления такими кормами домашних животных. Кроме того, настоящее изобретение касается применения волокна кокосового эндосперма для профилактики и лечения кишечных воспалений, а также для предотвращения появления болезнетворных бактерий в толстом кишечнике домашнего животного и борьбы с ними.
Поддержание и улучшение состояния здоровья домашних животных является постоянной задачей современной науки. Состояние здоровья животного можно определять разными способами, например, такими как качество фекальных масс и здоровье желудочно-кишечного (ЖК) тракта. Хорошее качество фекальных масс у домашних животных имеет двойное значение. Во-первых, это хороший индикатор здоровья животного. Известно, что хорошее качество фекальных масс обычно отражает здоровое состояние и нормальное функционирование толстого кишечника. Во-вторых, именно на этот показатель чаще всего обращает внимание владелец домашнего животного. Соответственно, поддержание хорошего качества фекальных масс и возможность улучшить его является неизменной задачей специалистов. Также актуальной задачей является улучшение здоровья ЖК тракта животного. Возможность поддерживать и улучшать состояние ЖК тракта может быть интересна для владельцев домашних животных, так как состояние ЖК тракта влияет на общее состояние здоровья животного.
Одним из способов поддержания нормального функционирования ЖК тракта и лечения хронической диареи у животных является включение в рацион питания домашних животных источника пищевых волокон.
Пищевые волокна оказывают обширное действие на работу кишечника, увеличивают выход фекаливых масс, сокращают время прохождения фекальных масс через кишечник и влияют на обмен веществ в кишечнике. Благоприятное воздействие волокон во многом обусловлено тем, что их полное расщепление происходит именно в толстом кишечнике. Этот анаэробный процесс, называемый ферментацией, является основным обменным процессом, проходящим в кишечнике. Ферментация является пищеварительной функцией, при которой разнообразные микроорганизмы, населяющие толстый кишечник, расщепляют сложные углеводы и другие основы, которые не были гидролизованы и абсорбированы в тонком кишечнике. Как микрофлора, так и организм, который она населяет, выигрывают от такого симбиоза.
Несколько сотен различных типов бактерий, значительно отличающихся физиологически и биохимически, находятся в толстом кишечнике. Понять, в чем заключается конкретное воздействие этой, обладающей огромным потенциалом, микрофлоры, весьма сложно и даже в части исследования человека это остается неясным. Однако некоторое понимание роли микрофлоры может быть достигнуто путем измерения ферментативной активности популяции бактерий в целом.
Основными продуктами ферментации сложных углеводов являются жирные кислоты с короткими цепочками (ЖККЦ), газы и энергия. Выделяемая энергия используется для роста клетки микроорганизма, в результате этого процесса большая часть азота из кишечника переходит в бактериальный белок и вызывает прирост микробиологической массы. ЖККЦ быстро абсорбируются и могут воздействовать на функцию ЖК тракта, обеспечивая энергооснову слизистой оболочки кишечника и нормализуя водный и электролитный баланс в кишечнике. Газ, образующийся в процессе ферментации, выводится как через легкие, так и через кишечник. В условиях недостатка углеводов бактерии будут расщеплять белки, что обеспечивает гораздо меньше энергии, так как образуются жирные кислоты с разветвленными цепочками, а также продукты обменных процессов, потенциально токсичные для организма (аммиак, амины, фенолы и т.д.). Одной из задач настоящего изобретения является включение в корм для домашних животных полезных диетических волокон.
При получении (или промышленном производстве) корма для животных используют небольшое число различных технологий. Во всех случаях основные ингридиенты продукта смешивают (часто нет необходимости их готовить/подвергать тепловой обработке) с необязательными ингридиентами, добавляемыми позже, а затем расфасовывают в различную тару. Процесс может включать прессование, например, это происходит при производстве сухих кормов. Другой вариант - процесс включает измельчение при производстве консервов. Любые процессы будут включать передвижение продукта из одной части производственной линии к другой, и затем возможна его упаковка. Желательно всегда достигать такой комбинации ингридиентов, при которой оптимизируется процесс их обработки до момента получения готового продукта. Рассмотрение диетического волокна, которое наибольшим образом подходит для промышленного производства, это еще одна цель настоящего изобретения.
Настоящее изобретение связано с добавлением в корм для домашних животных полезного источника волокон. При этом такого источника волокна, который наиболее легко использовать в производстве корма для домашних животных.
Соответственно, первый аспект данного изобретения касается применения волокна кокосового эндосперма как диетической волокнистой составляющей корма для домашних животных. Первый аспект изобретения включает применение волокна кокосового эндосперма в качестве диетической волокнистой составляющей при промышленном производстве корма для домашних животных.
Волокно кокосового эндосперма можно использовать как единственный источник диетических пищевых волокон или в комбинации с одним или несколькими другими источниками волокон, такими как мякоть свеклы, цикорий, мякоть цитрусовых, рисовые отруби, бобовые или gum talha.
Свежий кокосовый эндосперм содержит обычный набор питательных веществ, включающий воду (35%), масло (44%), белки (6%), сахар (7%), клетчатку (3%) и золу (1%). При этом, однако, ни одна из задач настоящего изобретения не накладывает ограничений на форму волокна кокосового эндосперма. Волокно кокосового эндосперма может быть в свежем или в любом другом виде, таком, как копра, обезжиренная копра (которую называют также, среди прочих брикетированной копрой, кокосовым жмыхом или пресованной копрой), кокосовая мука, обезжиренная кокосовая мука, цельные или обезжиренные высушенные кокосы, копра или переработанный кокосовый эндосперм, то есть эндосперм, который уже прошел тепловую обработку или обработан ферментами.
В соответствии с данным изобретением наиболее подходящим источником волокна кокосового эндосперма является копра. Копра представляет собой высушенный кокосовый эндосперм (обычно высушенный под действием солнца). В особенности подходит для вышеуказанных целей обезжиренная копра. Обезжиренную копру обычно получают из кокосового эндосперма, который высушен и из которого механическим путем отжато кокосовое масло. Для получения обезжиренной брикетированной копры вначале получают просто копру, затем пропускают ее через пресс или экспеллер для выгонки большей части масла. Остаток после процесса отжима называется брикетированной копрой, кокосовым жмыхом или пресованной копрой.
Хотя настоящее изобретение этим не ограничено, полагают, что добавление волокна кокосового эндосперма в корм для животных: а) поддерживает хорошее качество фекальных масс или улучшает его, и/или б) поддерживает состояние здоровья ЖК тракта или улучшает его, при этом указанного эффекта достигают за счет одного или более из следующих факторов: улучшения связывания воды фекалиями, снижения уровня рН, увеличения выделения полезных конечных продуктов и уменьшения выделения вредных конечных продуктов микробиологической ферментации, нарастает количество полезной микрофлоры, улучшается водно-электролитный баланс в желудочно-кишечном тракте, улучшается структура/здоровье кишечника и, благодаря хорошему связыванию воды, обеспечивается однородность содержимого кишечника. Настоящее изобретение полезно как для здоровых животных, в том числе чувствительных, так и для животных, страдающих от плохого качества фекальных масс или плохого состояния здоровья ЖК тракта. Соответственно первый аспект изобретения также связан с применением волокна кокосового эндосперма в производстве корма для домашних животных для поддержания или улучшения качества фекальных масс домашних животных или для поддержания или улучшения здоровья ЖК тракта. Критерии, по которым оценивается качество фекальных масс, отражены в приложении 1.
Методы оценки качества фекальных масс и методы анализа поддержания или улучшения этого качества хорошо известны и широко используются специалистами. Возможно применение нескольких методов (по отдельности или в сочетании друг с другом). Обычно работает группа подготовленных наблюдателей (это могут быть как просто обученные люди, так и профессионалы). Пробы фекальных масс домашнего животного собирают и оценивают в баллах, например, в соответствии с системой ранжирования, приведенной в приложении 1. Качество фекальных масс оценивают исходя из его соответствия качеству фекальных масс при нормальной функции желудочно-кишечного тракта. Как правило, это плотный стул, который сохраняет свою форму. Твердый сухой стул, в виде шариков (возможно, что он выводится из организма с усилием), или стул, который имеет такое содержание жидкости, что не сохраняет свою форму (включая диарею), указывает на нарушение функции желудочно-кишечного тракта. Оптимальная консистенция стула может варьировать в зависимости от вида животного, а также от конкретной особи, но может быть легко определена специалистом.
Методы оценки состояния здоровья ЖК тракта и оценки изменения данного состояния также хорошо известны и широко используются специалистами. Оценить, поддерживается или улучшается состояние здоровья ЖК тракта, можно путем сравнения с группой животных, получающих такое же питание, но без добавки волокна кокосового эндосперма. Состояние здоровья кишечника (состояние его пищеварительной или кишечной функций) может быть определено на основе качества стула и уровня рН, наличия и количества полезных и потенциально вредных бактерий в полости ЖК тракта и/или в фекальных массах, а также общего содержания жирных кислот, и содержания жирных кислот с короткими цепочками. Изучение таких характеристик in vivo является трудным, и не только из-за недоступности толстого кишечника и трудностей в сборе его содержимого, дополнительная трудность заключается в том, что жирные кислоты с короткими цепочками, производимые в кишечнике, затем в результате обмена веществ поступают в различные части организма и становятся недоступными для исследования без применения инвазивных технологий. Зато системы ферментации in vitro, в которых фекалии выступают в качестве посевного материала, могут быть ипользованы в качестве простых, быстрых (хотя неспецифических) методов, их можно использовать, чтобы спрогнозировать некоторые из физиологических воздействий волокна in vivo. В этом отношении понимания полезной роли микрофлоры в кишечнике можно достигнуть путем оценки ферментативной активности полезной популяции в целом. Образование ЖККЦ, измеренное в системе ферментации in vitro, обеспечивает индикатор бактериальной активности.
Особое преимущество настоящего изобретения заключается в том, что оно способствует образованию бутирата в результате ферментации волокна кокосового эндосперма в кишечнике, и тем самым увеличивает количество бутирата в кишечнике. Бутират представляет собой жирную кислоту с короткими цепочками, которая заслуживает особого внимания благодаря своему трофическому действию, которое она оказывает на кишечные клетки, а также благотворному воздействию на обмен веществ. При применении волокна кокосового эндосперма согласно настоящему изобретению было отмечено увеличение уровня образования бутиратов (в тестах in vitro) наряду с наблюдаемыми в той же тест-системе для образования в больших количествах бутиратов, например инулина.
Другое полезное действие волокна кокосового эндосперма согласно изобретению заключается в его способности предупреждать или лечить болезнетворные бактериальные инфекции в толстом кишечнике домашних животных. Болезнетворные инфекции в толстом кишечнике могут быть как клиническими, так и субклиническими. Оба типа нифекций наносят вред здоровью животного и ухудшают качество его фекальных масс. Более подробно роль волокна кокосового эндосперма рассмотрена ниже в связи с шестым и седьмым аспектами изобретения. Подробности, приводимые в отношении шестого и седьмого аспектов изобретения, также применимы к аспектам изобретения с первого по пятый.
В дополнение к вышеуказанным преимуществам следует отметить, что волокно кокосового эндосперма обладает еще одним полезным действием: его присутствие в корме для домашних животных снижает воспалительный статус кишечника животного или поддерживает низкий уровень воспаления в кишечнике. Более подробно роль волокна кокосового эндосперма в снижении воспалительного статуса в кишечнике животного описана ниже в связи с восьмым и девятым аспектами изобретения.
Выбор остальных компонентов, которые используются в корме для домашних животных, в сочетании с источником волокна кокосового эндосперма, для данного изобретения не является существенным; самые обычные продукты могут комбинироваться с необходимым количеством волокна кокосового эндосперма. Наиболее предпочтительно добавляемые корма для домашних животных обеспечивают все необходимые для конкретного домашнего животного витамины и минеральные вещества, например, как описано в: National Research Council, 1985, Nutritional Requirements for Dogs, National Academy Press, Washington D.C. (ISBN: 0-309-03496-5); National Research Council, 1986, Nutritional Requirements of Cats, National Academy Press, Washington D.C. (ISBN: 0-309-03682-8) or Association of American Feed Control Officials, Official Publication 1996.
Согласно настоящему изобретению источники волокна кокосового эндосперма в качестве компонента корма для домашних животных, полезны по следующим причинам. Источник волокон, в большинстве случаев, содержит в благоприятных количествах другие полезные вещества, такие как жиры и белки. Наличие этих питательных веществ обусловлено их наличием (также как и долей каждого из них) в исходном источнике волокна (кокосовом эндосперме). Известно, что кокосовое масло представляет собой жирные кислоты со средней длины цепочками и что такие жирные кислоты со средней длины цепочками наиболее легко абсорбируются в пищеварительном тракте животных. Соответственно кокосовое масло, присутствующее в источнике волокна кокосового эндосперма (даже в обезжиренной брикетированной копре, в которой жиры составляют от 5 до 10% от сухого остатка) обуславливает основную питательную ценность волокна. Поскольку такое масло является в особенности хорошим источником легко абсорбируемых жирных кислот, присутствие этого масла в источнике волокна очень полезно для определенных групп домашних животных.
Уровень содержания волокна кокосового эндосперма в корме для домашних животных как диетической волокнистой составляющей не ограничивается. Предпочтительно, содержание волокна кокосового эндосперма составляет в корме примерно от 0,15 до 8% от сухого остатка, предпочтительно, от 0,15 до 5% от сухого остатка по методу Энглиста (метод Энглиста изложен в следующей работе: Englist H.N., and Cumming J.H. (1984), Simplified method for the measurement of total non-starch polysaccharides by gas-liquid chromatography of constituent sugars as alditol acetates. Analyst. 109, 937-942, и его описание приведено здесь в виде ссылки). Уровни содержания, рассчитанные указанным методом, могут составлять от 0,15 до 5%, 6%, 7%, или 8%. Нижний предел может составлять от 1,5%, 2% или 3%. Описание метода Энглиста приведено в Приложении 2. В общем виде метод заключается в следующем. Крахмал после солюбилизации выделяют энзиматически, а содержание некрахмалистых полисахаридов (НКП) измеряют как сумму содержащихся сахаров, высвобождаемых путем кислотного гидролиза. Крахмал, содержащийся в источнике волокна, желатинизируют путем кипячения в горячей воде, а затем удаляют с альфа-амилазой и пуллуланазой. Крахмал и модифицированный, или устойчивый, крахмал диспергируют в деметилсульфоксиде (ДМСО). Для трех проб затем по дополнительной методике измеряют: (I) общий объем НКП, (II) водорастворимые НКП и (III) целлюлозу. Во всех случаях компоненты подвергают гидролизу с помощью серной кислоты. Содержащиеся в пробе сахара превращают в альдиты и затем измеряют в виде ацетатов альдитов посредством газожидкостной хроматографии (ГЖХ). В результате получают данные по общему содержанию диетического волокна, а также растворимых и нерастворимых фракций. Отдельно можно измерить содержание целлюлозы, а нецеллюлозные полисахариды определяют на основе измерения частных моносахаридов.
Необходимое содержание волокна кокосового эндосперма в корме (которое может различаться в зависимости от формы используемого кокосового эндосперма, например копры или обезвоженного кокоса) можно легко определить путем измерения количества диетического волокна в каждой конкретной форме кокосового эндосперма. Например, согласно методу Энглиста (Supra) обезжиренная копра содержит примерно 33,5% диетического волокна. Соответственно, чтобы обеспечить предпочтительный, согласно первому аспекту изобретения, уровень волокна, то есть примерно от 0,15 до 5% от сухого вещества, необходимо, чтобы в корме для домашних животных предпочтительно содержалось примерно 0,5 до 15% обезжиренной копры от сухого вещества корма.
Эти интервалы содержания относятся к первому аспекту изобретения для различных домашних животных. В особенности изобретение применимо к домашним животным, относящимся к млекопитающим, в частности к собакам, кошкам и лошадям.
Корм для животных согласно настоящему изобретению предпочтительно представляет собой коммерческий корм для домашних животных. Предпочтительно, такой корм продают в качестве продукта для кормления домашних животных, главным образом домашних кошек и собак.
Корм для домашних животных предпочтительно упаковывают. Таким образом покупатель может по упаковке узнать, какие ингредиенты входят в продукт и определить его пригодность для конкретного домашнего животного. Упаковка может быть металлической (обычно в форме консервной банки или пакета из фольги), пластика, бумаги или картона. Корм может быть сухим, влажным или мокрым. Влажные продукты включают продукты, которые продают в консервных банках и которые имеют содержание влаги от 70 до 90%. Сухие корма включают продукты с аналогичным составом, но которые имеют содержание влаги от 5 до 15% и представлены в виде маленьких кусочков, напоминающих сухое печенье. Количество влаги в продукте может влиять на тип упаковки, который можно использовать или является необходимым.
Корм для домашних животных согласно настоящему изобретению включает любой продукт, пригодный для кормления животных. Таким образом это изобретние включает стандартные пищевые продукты, а также пищевые закуски для домашних животных (например, легкие закуски, зерновые закуски, сухое печенье и кондитерские изделия). Продукты питания предпочтительно представляют собой обработанные продукты. Они могут быть в форме желатинизированной крахмалистой массы. Они могут быть в форме кусков в соусе, желе, формированные, или в воде. Они могут включать мясо или другие продукты животного происхождения (такие, как говядина, цыпленок, индейка, ягнятина, свинина, рыба, плазма крови, мозговые кости и т.д., при этом продукты могут включать один или несколько из вышеперечисленных ингредиентов). Альтернативно продукт может не содержать мяса (предпочтительно включая в этом случае заменители мяса, такие как соя, кукурузная клейковина или соевые продукты для того, чтобы обеспечить источник белка). Продукт может содержать дополнительные источники белка, такие как концентрат соевого белка, молочный белок, клейковину и т.п. Продукт также может содержать источник крахмала, например, один или несколько злаков (например, пшеницу, кукурузу, рис, овес, ячмень и т.п.) или не содержать источника крахмала. Обычный сухой корм для собак и кошек содержит примерно 20-30% натурального белка, примерно 10-20% жиров, остальное составляют углеводы, в том числе диетическое волокно, и зольный остаток. Обычный влажный или мокрый продукт содержит (в расчете на сухое вещество) примерно 40% жиров, 50% белков и остальное - волокно и зольный остаток. Настоящее изобретение в особенности относится к описанным выше продуктам питания домашних животных, которые продаются в качестве пищевого продукта для животных, особенно как пищевой продукт для собак и кошек. Кошки и собаки согласно данному изобретению представляют собой Felis domesticus или Canis domesticus.
Второй аспект изобретения относится к применению волокна кокосового эндосперма в производестве корма для домашних животных. Второй аспект настоящего изобретения не включает в себя производство продуктов питания, который включает гель, содержащий кокосовый эндосперм или ирландский мох. Такие продукты питания, которые включают в себя гель из кокосового эндосперма и ирланского мха, описаны ранее в WO 96/39046. Описание в WO 96/39046 ограничивается желирующей системой, включающей ирландский мох или кокосовый эндосперм. Согласно WO 96/39046 эндосперм используется только в качестве компонента желирующей системы.
Применение волокна кокосового эндосперма в производстве продуктов питания (согласно второму аспекту изобретения) имеет преимущества, описанные выше применительно к первому аспекту изобретения. Кроме того, изобретателями обнаружено, что источники диетического волокна кокосового эндосперма в особенности подходят для процесса производства корма для домашних животных. Применение кокосового эндосперма в качестве диетического волокна чрезвычайно удобно. Когда в процессе производства в продукт добавляют остальные ингредиенты, то проявляется одно из неожиданных преимуществ волокна кокосового эндосперма по сравнению с другими источниками волокна, а именно образуется эмульсия, имеющая меньшую, чем в других случаях, клейкость. Преимущества такого волокна особенно заметны в процессе выдавливания и формирования продукта. Оно особенно полезно в процессе «измельчении эмульсии» при производстве снеков. Дальнейшая обработка источников волокна кокосового эндосперма не приводит к серому цвету продукта, что часто происходит при применении других источников волокна. Напротив, продукт приобретает эстетически приемлемый цвет.
Все предпочтительные условия первого аспекта изобретения применимы также и ко второму аспекту.
Третий аспект изобретения обеспечивает корм, который включает волокно кокосового эндосперма. Третий аспект настоящего изобретения не включает продукты питания, которые содержат гель на основе кокосового эндосперма или ирландского мха, как описано в WO 96/39046. Продукты питания в соответствии с третьим аспектом изобретения имеют преимущества, которые уже описаны в вышеприведенных первом и втором аспектах изобретения. Они включают содействие хорошему качеству фекальных масс и здоровью ЖК тракта, особенно уровню жирных кислот с короткими цепочками, образующихся в результате ферментации, и неожиданно хорошие производственные характеристики. Продукты питания особенно подходят для кормления домашних животных.
Все предпочтительные условия первого и второго аспектов изобретения применимы также и к третьему аспекту. Они включают уровень и источники волокна кокосового эндосперма, типы продуктов питания, производство и другие составляющие корма.
Четвертый аспект настоящего изобретения обеспечивает способ приготовления корма в соответствии с третьим аспектом изобретения, включая смешивание ингредиентов и возможную последующую тепловую обработку продукта. Корм может быть сформирован до или после смешивания и/или тепловой обработки.
Как описано выше, включение волокна кокосового эндосперма обеспечивает целый ряд преимуществ по сравнению с включением других волокон как в процессе приготовления корма для домашних животных, так и в конечном продукте.
Способ включает смешивание источника волокна кокосового эндосперма с одним или несколькими ингредиентами продукта питания животного. Корм может быть произведен любым известным способом. Волокно кокосового эндосперма может быть добавлено до или в ходе тепловой обработки одного или нескольких ингредиентов. Способ может также включать шаг выделения волокна кокосового эндосперма из кокосового сырья.
Корм может быть изготовлен любым известным способом, например, как описано в Waltham Book of Dog and Cat Nutrition, Ed. ATB Edney, Chapter by A.Rainbird, озаглавленной "A Balanced Diet" стр.57-74 Pergamon Press Oxford.
Все предпочтительные условия аспектов изобретения с первого по третий применимы также и к четвертому аспекту. Они включают уровень и источники волокна кокосового эндосперма, типы продуктов питания, производство и другие составляющие корма.
Пятый аспект изобретения обеспечивает способ кормления домашних животных кормом, приготовленным в соответствии с третьим аспектом изобретения. Пятый аспект изобретения включает способ поддержания и улучшения состояния здоровья желудочно-кишечного тракта домашних животных, способа кормления домашних животных кормом в соответствии с третьим аспектом изобретения. Кормление домашних животных кормом согласно третьму аспекту изобретения поддерживает и улучшает состояние здоровья ЖК тракта животных за счет присутствия волокна кокосового эндосперма. Для того чтобы поддерживать и улучшать состояние здоровья ЖК тракта, животных кормят продуктом в значительном объеме и в течение значительного периода времени. Особенное улучшение ЖК тракта достигается благодаря образованию жирных кислот с короткими цепочками, в особенности бутиратов.
Пятый аспект изобретения включает способ поддержания и улучшения качества фекальных масс домашнего животного, способ кормления животного продуктами питания согласно третьему аспекту изобретения.
Кормление домашних животных продуктами питания согласно третьему аспекту изобретения поддерживает и улучшает качество фекальных масс за счет присутствия волокна кокосового эндосперма. Для того чтобы поддерживать и улучшать качество фекальных масс, животных кормят продуктом в значительном объеме и в течение значительного периода времени.
Количество корма и период кормления по пятому аспекту изобретения будет зависеть от ряда показателей, включая вид животного, породу, возраст и общее состояние здоровья. Тот, кто кормит домашнее животное, может легко использовать эти показатели, чтобы определить количество корма и период кормления.
Способ по пятому аспекту изобретения может оказывать ветеринарный эффект, но не ограничен этим. Кормление может быть и не терапевтическим. Термин «кормление» также включает понятие «назначение» корма домашнему животному. Способы могут быть профилактическими или терапевтическими. Все предпочтительные условия аспектов изобретения с первого по четвертый применимы также и к пятому аспекту. Они включают уровень и источники волокна кокосового эндосперма, типы продуктов питания, производство и другие составляющие корма.
Шестой аспект изобретения обеспечивает применение волокна кокосового эндосперма в производстве корма для домашних животных для профилактики и лечения бактериальных инфекций в толстом кишечнике домашнего животного.
Рассматривают инфекцию в толстом кишечнике домашнего животного, вызванную болезнетворными бактериями. Под болезнетворными бактериями в основном понимаются Campylobacter (особенно Campylobacter jejuni), Salmonella и Excherichia coli. Campylobacter jejuni, разновидность, представляющая собой источник большинства человеческих инфекций, является также главной инфекцией, поражающей кошек и собак. Инфекция может действовать как патогенная на молодых собак и кошек, и как условно-патогенная на взрослых животных. Клиническая картина болезни проявляется как диарея, колеблющаяся от легких форм до диареи, сопровождающейся выделением кровянистой слизи, тенизмом (болезненными ощущениями при испражнениях), рвотой, потерей аппетита и депрессией. Основная проблема, связанная с инфекцией Campylobacter, поражающей домашних животных, это зоонозный риск, который порождается поведением животного и его выделениями. Существуют оценки, что 5% всех человеческих C.jejuni, вызывающих диарею, являются результатом контакта с инфицированными собаками и кошками. В целом ряде самых новых исследований установлено, что владелец собаки подвержен значительному риску заболеть Campylobacter. Исследование, проведенное в Кристчече, Новая Зеландия, обнаружило, что риск заразиться Campylobacter у домовладельцев, контактирующих с собаками, в 1,25-2 раза выше чем у людей, не имеющие животных. Кроме того, важно, что попытки снизить или исключить инфекцию Campylobacter связаны с использованием антибиотиков, что может привести к появлению у организма устойчивости к антибиотикам.
Настоящее изобретение обеспечивает такой корм для домашних животных, содержащий волокно кокосового эндосперма, который является эффективным для целей профилактики и борьбы с инфекциями, вызываемыми болезнетворными бактериями, в толстом кишечнике домашних животных. Животными являются, в основном, кошки или собаки (главным образом речь идет о Felis domesticus или Canis domesticus). Болезнетворные бактерии включают, среди прочих, Campylobacter, Salmonella, болезнетворных Clostridium и E.coli, такие как enteropathogenic E.coli и verotoxigenic E.coli.
Седьмой аспект изобретения обеспечивает способ профилактики и лечения инфекций толстого кишечника домашних животных, вызванных болезнетворными бактериями, способа кормления названных домашних животных кормом, включающим волокно кокосового эндосперма.
Восьмой аспект изобретения обеспечивает применение волокна кокосового эндосперма в производстве корма для профилактики и лечения кишечных инфекций домашних животных.
В кишечнике собаки воспалительные процессы сопровождаются образованием различных химических веществ, в том числе простагландина эйкозаноида Е2 (PGE2).
Настоящее изобретение показывает, что в организме домашних животных, которых кормят продуктами, содержащими волокно кокосового эндосперма, образуется значительно меньше PGE2, чем при той же самой диете без волокнистого источника.
Девятый аспект изобретения обеспечивает способ профилактики и борьбы с кишечными инфекциями домашних животных, способа кормления указанных домашних животных кормами, содержащими волокно кокосового эндосперма.
В соответствии с шестым, седьмым, восьмым и девятым аспектами изобретения животным является животное из семейства псовых. Волокно кокосового эндосперма может быть в любой форме и предпочтительно, как описано в 1-5 аспектах изобретения. Содержание волокна кокосового эндосперма, измеренное по методу Энглиста, предпочтительно должно составлять 0,15-5% от сухого остатка. Все остальные предпочтительные условия те же, что и для аспектов изобретения с первого по пятый.
Изобретение описывается со ссылками на следующие приложения:
Фиг.1 - сравнение показателей фекальных масс для двух диет, содержащих кокосовый жмых;
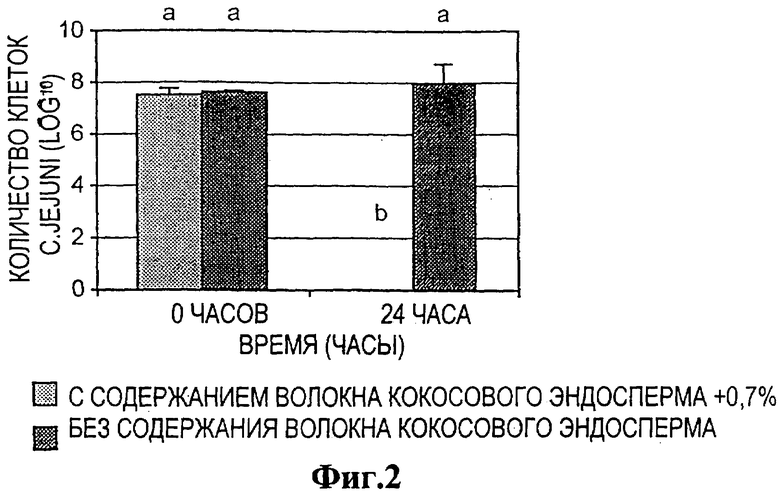
Фиг.2 - эффект от введения волокна кокосового эндосперма в толстый кишечник собаки, анализ на выживаемость Campylobacter jejuni;
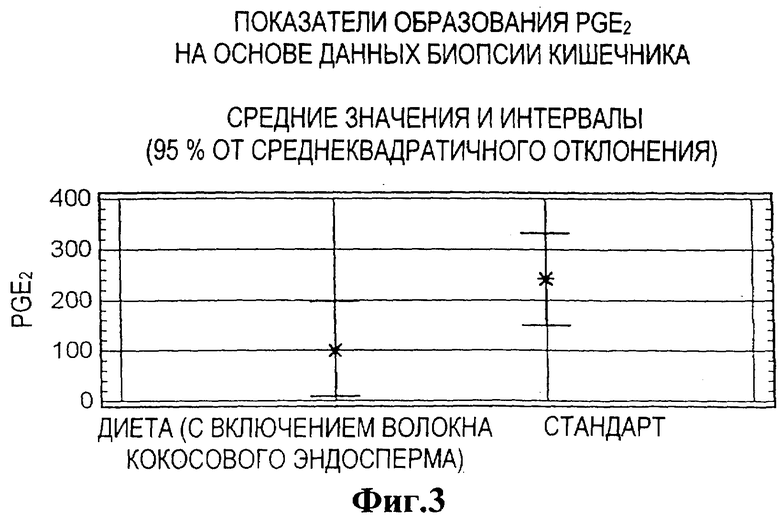
Фиг.3 - показатели образования простагландина эйкозаноида Е2 на основе данных биопсии кишечника.
Ниже приведено описание изобретения со ссылкой на следующие неограничительные примеры:
Пример 1
Этот пример описывает приготовление и применение обезжиренной высушенной кокосовой муки.
Кокосы были куплены на местном рынке; из них была извлечена белая мякоть, или эндосперм. Эндосперм был тщательно измельчен и неоднократно обработан ацетоном, чтобы отделить жир и воду. В результате была получена высушенная обезжиренная кокосовая мука.
Пример 2
Этот пример описывает приготовление механически обезжиренной брикетированной копры.
Кокосовый эндосперм, полученный из кокосового ореха, был измельчен. Измельченное сырье было нагрето максимум до 120°С, используя технологию, широко известную специалистам по производству масла, и пропущен через гидравлический пресс или экспеллер, чтобы извлечь большую часть масла. Полученный в этом процессе экстракт был высушен до необходимого уровня, то есть до уровня влажности примерно 15%.
Пример 3
Оценка волокна кокосового эндосперма как диетического волокна.
Исходный материал
Исходный материал, который использовался в системе ферментации in vitro, представлял собой исходный материал, который особенно подходит для добавления в сухой и консервированный корм для кошек и собак (таблица 1).
Источники волокна
Используя методику Энглиста и методику АОАС, в исходном материале определяли общее содержание диетического волокна (таблица 2). Методику АОАС можно найти в АОАС International 1995, Total, Soluble and Insoluble Dietary Fibre in Foods. АОАС Official method 991 43, Official Methods of Analysis, 16th Ed. Методика Энглиста приведена выше в тексте, а также в Приложении 2. Анализ диетического волокна обнаружил значительную разницу в уровнях общего содержания диетического волокна в исходных материалах. Анализ на основе АОАС в общем показал более высокий процент содержания диетического волокна по сравнению с анализом по Энглисту. По методике Энглиста используют энзимо-химический анализ для измерения содержания некрахмалистых полисахаридов (NSP), которые являются основными структурными компонентами клеточных стенок растений, охватывающих более традиционное понятие диетического волокна. Методика АОАС дает содержание волокна, используя комбинацию энзимных и гравиметрических методов, которые включают в расчет объем лигнина и некоторых устойчивых крахмалов, что и приводит к более высоким показателям удельного содержания диетического волокна.
Поскольку содержание диетического волокна в брикетированной копре (по Энглисту) составило менее 40%, был проведен дальнейший анализ, чтобы определить примерное содержание прочих веществ в источнике волокна (таблица 3). Основным неволокнистым составляющим оказался белок (20,8%). Белок и свободный сахар в брикетированной копре из конечного продукта, участвующего в процессе ферментации, можно искусственно отделить, так как в пищеварительном тракте in vivo они могут не достигнуть толстого кишечника. Однако усваиваемость этих питательных макроэлементов источника волокна in vivo зависит от их доступности для амилазы и протеазы в тонком кишечнике. Доля питательных веществ, содержащихся в брикетированной копре, относительно невелика, поэтому источник волокна можно рассматривать как основу.
Примерный состав сырья
Методика
Для характеристики ферментации волокна in vitro был принят несложный подход. Подобные методики представлены в Brobech Mortensen P., Hove, H., Rye Clausen, M. and Holtug, К. (1991) Fermentation to short-chain fatty acids and lactate in human faecal batch cultures. Scand. J. Gastroenterol. 26, 1285-1294, Tigemeyer, E.C., Bourquin, L.D., Fahey, G.C. and Garleb, K.A. (1991) Fermentability of various fibre sources by human faecal bacteria in vitro. Am. J. Clin. Nutri. 53, 1418-1428, Sunvold, G.D., Fahey, G.C., Merchen, N.R. and Reinhart, G.A. (1995) In vitro fermentation of selected fibrous substrate organic matter disappearance and short-chain fatty acid production. J. Anim. Sci. 73, 1110-1122 and Edwards, C.A., Gibson, G., Champ, M., Jensen, B-B., Mathers, J.C., Nagengast, F., Rumney, C. and Quehl, A, (1996) In vitro method for quantification of the fermentation of starch by human feacal bacteria. J. Sci. Food Agric. 71, 209-217. Такие системы, в том числе и та, которая использовалась в данном изобретении, являются полезными в качестве теста in vitro для рассмотрения результатов фекальной ферментации. Однако такие тесты неточные и не могут дать абсолютную картину из-за различных причин, в том числе из-за очень сложной системы миклофлоры фекальных масс животных.
Подготовка пробы волокна (первый день)
- В качестве волокнистой основы использовали брикетированную копру с концентрацией в ней волокна 0,7% (мас./об.). По 0,231 г (±0,05 г) брикетированной копры развесили в три стеклянных 60 мл бутылки с сывороткой (Jencons), при этом записали точный вес. Затем добавили по 30 мл ферментационной среды (таблица 4), закупорили бутылки ватными шариками и обернули металлической фольгой.
В качестве контрольных было подготовлено шесть бутылок без содержания в них источника волокна.
- В конических колбах приготовили по 200 мл 10 mM буферного раствора фосфата натрия, рН 7,4, и по 200 мл слабого анаэробного бульона; в колбах также содержались flea для ре-суспендирования фекалий. Сосуды стерилизовали путем автоклавирования (15 минут при 121°С). Сосуды поместили в анаэробную установку (Don Whitley) для предварительного восстановления немедленно после автоклавирования.
Состав ферментационной среды
Кошки и собаки
- В качестве источника посевного бактериального материала для ферментативной системы in vitro использовали фекальные массы кошки или собаки. Кошек кормили сухим полноценным кормом (состав приведен ниже) по меньшей мере последние три месяца, предшествующие исследованию. Собак кормили сухим кормом, разработанным для поддержания взрослых собак (состав приведен ниже), по меньшей мере в течение двух месяцев, предшествующих началу исследования.
- Рецепты сухих кормов:
- В течение 3 недель с последующим недельным перерывом кошек содержали в помещении, чтобы обеспечить возможность собирать свежие фекальные массы. Кошек кормили по отдельности кормом в количестве, необходимом для поддержания веса тела, и обеспечивали им постоянный доступ к свежей воде.
- Собак кормили по отдельности кормом в количестве, необходимом для поддержания веса тела, и обеспечивали им постоянный доступ к свежей воде.
Посев фекалий (второй день)
- Были собраны свежие фекальные массы. В пределах 60 минут после дефекации по 20 г фекальных масс добавили к предварительно восстановленному фосфатному буферному раствору. Колбу помещали на магнитный смеситель в аэнаэробную камеру для получения суспензии фекалий (примерно на 10 минут). Ватные затычки удаляли и аликвотные порции по 3 мл этой 10% (мас./об.) суспензии фекалий добавили в каждую из трех бутылок с сывороткой, содержащую источник волокна, а также в три контрольный бутылки без волокна. При этом содержание фекального посевного материала в каждой бутылке составило примерно 1%. Три бутылки были необходимы, чтобы обеспечить измерения в три временные интервала. Ватные затычки заменили бутиловыми резиновыми пробками и металлические крышки использовали для герметичной закупорки каждой бутылки.
- Три контрольные бутылки без волокна, в которые не добавляли посев, использовали в качестве контрольной среды. В три бутылки без волокна добавили посев и использовали в качестве контрольной среды с фекалиями. Бутылки инкубировали в анаэробной камере при температуре 37°С. Измерения проводили через 0, 6 и 24 часа после посева фекальных масс.
Конечные измерения ферментации (день 2 и 3)
I. Измерение ЖККЦ (0, 6, 24 часа)
- Аликвотные порции по 4 мл ферментационного бульона добавили в 15 мл пластиковые пробирки из Cortex'a, содержащие по 1,25 мл 20% (мас./об.) метафосфорной кислоты. Пробирки перевернули и оставили при комнатной температуре на 30 мин, чтобы высадить кислоты в осадок до того, как пробирки будут помещены при температуре -80°С перед проведением газовой хроматографии. Это позволяет обнаружить жирные кислоты с короткими цепочками: уксусную, пропионовую, N-масляную, изомасляную, N-валериановую, изовалериановую, капроновую, изокапроновую и гептановую.
- Пробы тщательно перемешали и поставили отстаиваться. В стеклянную тестовую пробирку с пришлифованным стеклянным горлышком накапали 1 мл раствора смешанного стандарта 0,01 М (0,01 М уксусной, пропионовой, изо-масляной, масляной, изовалериановой, валериановой, изо-капроновой и капроновой кислот в дистилированной воде), или ферментационный экстракт, и затем добавили примерно 0,4 г NaCl (чистой для хроматографии HPLC) и 0,3 мл 12 М H2SO4. Добавили 1,5 мл трет-бутилметилового эфира (ТВМЕ, чистой для хроматографии HPLC, 99,8%), после чего смесь взбалтывали в течение 1 мин. На 15 мин смесь оставили для разделения водного слоя и слоя растворителя с тем, чтобы частично отделить верхний слой эфира (примерно 0,5 мл, с помощью отборной пипетки), поместить в 2 мл завинчивающийся пузырек и опечатать парафином. Этот экстракт впрыскивали в газовый хроматограф, где измеряли концентрацию жирных кислот с короткими цепочками путем сравнения со стандартными растворами жирных кислот.
II. Измерение газа (6, 24 ч)
- Через 6 и 24 часа бутылки извлекли из анаэробной камеры. «Отрывные» металлические уплотнители приподняли, чтобы измерить давление газа внутри бутылки. Манометр, обнуленный перед каждым измерением, показывал изменение давления в миллибар.
III. Измерение уровня рН (0, 6, 24 ч)
- Уровень рН ферментационного бульона измеряли рН-метром (Orion, ISE 710A) после калибровки пробы в сравнении с известным стандартом.
Результаты
Конечные результаты бактериальной ферментации
Потенциальное воздействие обезжиренной брикетированной копры на бактериальную активность оценивали по количеству образованных жирных кислот с короткими цепочками, объему полученного газа и уровню рН в ферментационном бульоне in vitro после 6 и 24 ч инкубации в присутствии 1% посева фекалий. Результаты тестирования проб для 14 кошек проанализированы и представлены в таблице 6. Результаты тестирования проб собак (n=6) представлены в таблице 7.
В бутылках с контрольными пробами, которые не содержали дополнительных субстратов, было образовано значительное количество жирных кислот с короткими цепочками и газов. Для определения того, какая часть рассматриваемых веществ образовалась благодаря присутствию источника волокна кокосового эндосперма, базовые значения показателей контрольных образцов отняли из соответствующих значений, которые были получены в пробах с добавками. Положительный результат показывает дополнительное образование по сравнению с базовым уровнем, отрицательный результат, наоборот, указывает на подавление образования или потребление данного вещества в сравнении с контролем. Отрицательные значения рН показывают снижение уровня рН (результаты представлены в таблицах 6 и 7).
(a) Общее содержание жирных кислот с короткими цепями
Общее содержание образовавшихся жирных кислот с короткими цепочками увеличивалось со временем (см. таблицы 6 и 7). И у кошек, и у собак по истечении 6 часов после введения обезжиренной брикетированной копры наблюдалось значительное увеличение общего объема ЖККЦ (р<0,05) по сравнению с содержанием ЖККЦ в отсутствие источника волокна. Через 24 часа наблюдался аналогичный реультат.
Общий объем образовавшихся ЖККЦ оценивали более подробно путем определения составляющих ЖККЦ. В кишечнике in vivo уксусная, пропановая и масляная кислоты представляют собой основные конечные продукты ферментации углеводородов и составляют до 90% от общего объема ЖККЦ в кишечнике. Значительное (р<0,05) увеличение содержания уксусной и пропановой кислот наблюдали после 6 и 24 часов у кошек и собак (за исключением уксусной кислоты у кошек (n=14) после 24 часов).
I. Бутират
Бутират представляет особый интерес благодаря трофическому воздействию, которое он может оказывать на микрофлору, а также полезной роли в обмене веществ. Образование бутирата значительно превышает контроль (р<0,05) через 6 и 24 ч при наличии обезжиренной брикетированной копры (см. таблицу 6). У кошек после 24 ч наблюдалось увеличение образования бутирата из обезжиренной брикетированной копры на 80%. Такое почти удвоение объемов бутирата может иметь биологическую значимость in vivo. Увеличение объма бутирата через 24 ч наблюдалось и у собак, но оно не было столь значительным (см таблицу 7).
(b) Газ
Газ - это второй основной конечный продукт ферментации. Основными компонентами газа являются СО2, Н2 и СН4, которые образуются в основном в результате ферментации углеводородов. Образование газа измеряли как увеличение давления (мбар) от времени.
После 24 ч в присутствии волокна обезжиренной брикетированной копры наблюдали значительное увеличение (р<0,05) объемов газа по сравнению с его объемами у кошек и собак в отсутствие волокна (таблица 6).
Образование жирных кислот с короткими цепочками, газа и аммиака в присутствии и отсутствие брикетированной копры (0,7% (мас./об.)) через 6 ч и 24 ч инкубационного периода в 1% (мас./об.) гомогенизированной фекальной среде кошки. Значения усреднены при n=14
# Общий объем ЖККЦ представляет собой общий объем образовавшихся уксусной, пропановой, N-масляной, изо-масляной, валериановой, изо-валериановой, капроновой, изо-капроновой, гептановой кислот.
SE - стандартная погрешность.
Образование жирных кислот с короткими цепочками, газа и аммиака в присутствии и отсутствие брикетированной копры (0,7% (мас./об.)) через 6 ч и 24 ч инкубационного периода в 1% (мас./об.) гомогенизирванной фекальной среде собаки. Значения при n=6
# Общий объем ЖККЦ представляет собой общий объем образовавшихся уксусной, пропановой, N-масляной, изо-масляной, валериановой, изо-валериановой, капроновой, изо-капроновой, гептановой кислот.
SE - стандартная погрешность.
Выводы
- Процесс ферментации в основном определяется количеством и типом субстрата, который участвует в процессе. Приведенная система обеспечивает отличный способ для понимания активности волокнистых субстратов в ферментативных процессах и делает гораздо более понятной роль микрофлоры в толстом кишечнике.
- Было выдвинуто предположение о том, что идеальный источник волокна должен представлять собой вещество, которое подвергается медленной ферментациии с образованием больших объемов ЖККЦ (главным образом бутиратов). При применении такого медленно ферментирующего волокна волокно с сохранившейся ферментативной способностью способно достигать бактерий, населяющих отдаленную часть кишечника. Таким образом, возможно использовать такой источник волокна с тем, чтобы «подкармливать» бактерии по всей длине толстого кишечника. Волокно кокосового эндосперма подходит в качестве такого источника.
- В общем процесс ферментации брикетированной копры у кошек и собак оказался одинаковым в отношении общего объема ЖККЦ и образования газа.
- Конечные результаты показывают, что применение волокна кокосового эндосперма улучшает или поддерживает (хорошее) качество фекальных масс и улучшает или поддерживает (хорошее) здоровье желудочно-кишечного тракта.
- Значительное увеличение бутирата, наблюдавшееся у кошек, является важным фактором, который способствует здоровью кишечника. У кошек обезжиренная брикетированная копра как источник волокна проявила себя неожиданно хорошо по сравнению с другими источниками волокна в том, что ее применение привело к значительному увеличению уровня бутирата по отношению к базовому уровню. Аналогичные результаты наблюдались и у собак, хотя они не были столь значительными.
Пример 4
Введение
Задачей эксперимента была оценка качества фекальных масс, которые образовывались в результате кормления животных по двум рецептам с содержанием обезжиренной брикетированной копры.
Основой используемого корма для домашних животных послужили консервированные продукты в желе. Рацион по каждой из диет был следующий:
Рецепт 1 содержит более 100% вследствие потерь при термической обработке сырья. Оба типа консервов обрабатывали при температуре 125°С в течение 61 минуты.
Методика
Качество фекальных масс определяли в течение 2 недель cross-over эксперимента у 10 взрослых собак, представленных разными породами.
В опытах использовали породы следущих собак:
Гончая 1
Гончая 2
Гончая 3
Гончая 4
Гончая 5
Английский спрингер-спаниель б
Английский спрингер-спаниель 7
Золотой ретривер 8
Керн-терьер 9
Мини-шнауцер 10
Собакам давали следующее количество диетического корма в день (грамм в день, исходя из нормы для поддержания необходимого объема кормления)
Перед началом каждой недели эксперимента собак в течение 2 дней кормили стандартным кормом по нижеприведенному рецепту. Это обычная практика позволяет обеспечить общий базовый уровень для изучения фекальных масс.
Качество фекальных масс оценивали субъективно, используя оценочную шкалу из 17 категорий, в результате чего все значения качества дефекации были распределены между основными делениями 1 и 5 (каждое основное деление шкалы дробилось еще на четыре части, таким образом получилось 17 категорий) (см. приложение 1). Средний балл качества фекальных масс для каждой собаки рассчитывали на основе баллов для всех собранных за период эксперимента фекальных проб. Путем усреднения всех полученных значений подсчитывали общий средний балл для каждой собаки. Статистический анализ проводили на основе двухфакторной модели ANOVA (принимая диету как постоянный фактор, а собак как переменный).
Результаты
Прием пищи
Все собаки съедали 100% пищи, предлагаемой им в течение двухнедельного эксперимента.
Качество фекальных масс
Качество фекальных масс, определяемое в средних баллах согласно принятой шкале, было отличным для обеих диет.
Значительной разницы в средних значениях качества фекальных масс между двумя диетами как при доверительном уровне 95%, так и при уровне 90% (ANOVA, р=-0.77), не было.
На Фиг.1 показаны для сравнения средние значения качества фекальных масс и 95% LSD (среднеквадратичное отклонение) для разных диет.
Выводы
Качество фекальных масс, определяемое в средних баллах согласно принятой шкале, было отличным для обеих диет.
Значительной разницы в средних значениях качества фекальных масс между двумя диетами как при доверительном уровне 95%, так и при уровне 90% (ANOVA, р=-0,77), не было.
Пример 5
Введение
Задачей эксперимента была оценка качества фекальных масс при включении в сухой корм кокосового жмыха.
В качестве основного корма для домашних животных использовали экструдированный сухой однокомпонентный корм. Состав корма следующий:
Методика
Качество фекальных масс измеряли в течение одной недели эксперимента у 14 взрослых собак, представляющих разные породы.
Породы собак, которых использовали в эксперименте:
1 лабрадор-ретривер
3 колли
2 немецкие овчарки
1 йоркширский терьер
2 суссекских спаниеля
5 полукровок
Собак кормили в соответствии с энергетическими требованиями.
Качество фекальных масс оценивали субъективно, используя оценочную шкалу из 9 категорий, при этом все дефекации были ранжированы между основными делениями от 1 до 5 (каждое основное деление шкалы дробилось пополам, таким образом получалось 9 категорий) (см.приложение 1). Значение общего качества фекальных масс подсчитывали для каждой собаки на основании всех проб, собранных за период эксперимента. Среднее значение качества фекальных масс в условиях использования диеты подсчитывали на основе всех значений качества фекалий для каждой собаки.Общее среднее значение для диеты рассчитывали путем усреднения средних значений для каждой собаки.
Результаты
Прием пищи
Все собаки съедали 100% корма, предлагаемого им в течение двухнедельного эксперимента.
Качество фекальных масс
Общее качество фекальных масс, оцениваемое по принятой шкале, было превосходным.
Средний балл качества фекальных масс согласно шкале составил 2,5.
Выводы
Применение обезжиренной копры при кормлении сухим кормом обеспечивает идеальное качество фекальных масс.
Пример 6
Исследование влияния волокна кокосового эндосперма на жизнеспособность
Campylobacter в кишечнике собак.
Резюме
- Campylobacter является одной из основных болезнетворных бактерий, вызывающих клинические и неклинические инфекции у собак.
- Была создана модель толстого кишечника собаки in vitro для изучения воздействия нового волокна на жизнеспособность болезнетворных бактерий у собак.
- Включение волокна кокосового эндосперма в модель привело к выведению жизнеспособных клеток Campylobacter jejuni из системы.
Методики
1. Клетки С. jejuni были выращены из маточных культур и культивированы при температуре 37°С в микроаэробных условиях (5% O2, 10% СО2 и 85% N2). Жидкие культуры были выращены в объеме 20 мл в 50 мл конических колбах, которые встряхивали на вибрационном орбитальном смесителе. Культуры, помещенные на ночь в бульон Mueller Hinton (MH) (Oxoid), были доведены до А600 1.0 перед введением в аналитический состав.
2. В колбы было добавлено по 200 мл бульона MH, 1 мл приведенной культуры С.jejuni и 2 г свежих фекальных масс. В тестовые колбы было добавлено по 0,7% (мас./об.) брикетированной копры и затем флаконы встряхнули, чтобы смешать содержимое. В контрольные флаконы добавки не вводили.
3. Колбы исследовали в начале (0 ч) и конце (24 ч) эксперимента для определения количества жизнеспособных клеток С.jejuni путем последовательного разбавления проб из колб и нанесения разбавленных растворов на пластины с агаром (LabM), селективным к Campylobacter. Пластины инкубировали в микроанаэробных условиях в течение 48 ч, после чего определяли показатели жизнеспособности.
4. В конце эксперимента в каждом флаконе при помощи Мультистикс (Bayer) был определен уровень рН смеси.
5. Эксперимент проводили 6 раз, используя каждый раз фекальные пробы от разных собак. Всех собак в течение всего периода изучения кормили коммерчески доступным сухим кормом класса премиум (полным и сбалансированным).
Результаты
После 24 ч микроаэробной инкубации из проб, взятых из колб, которые содержали волокно кокосового эндосперма, не было получено ни одной жизнеспособной клетки С.jejuni. Напротив, из проб, взятых из колб, которые не содержали волокно, было получено около 108 клеток С.jejuni на мл. Результаты всех шести отдельных экспериментов представлены в таблице ниже и на графике, который суммирует полученные данные.
Количество жизнеспособных клеток Campylobacter jejuni (log10), полученных в модели толстого кишечника собаки в присутствии и отсутствие волокна кокосового эндосперма.
На Фиг.2 показан график влияния включения волокна кокосового эндосперма в модель толстого кишечника собаки на жизнеспособность Campylobacter jejuni. Буквами обозначены значения, имеющие статистически существенную разницу.
Ниже приведены показатели рН после 24 ч инкубации пробы каждой собаки с добавлением в нее волокна кокосового эндосперма и без него.
В конце инкубационного периода в каждом флаконе был измерен уровень рН и оказалось, что он составляет 7,5 (при среднеквадратичном отклонении 0) в тех колбах, которые не содержали волокно кокосового эндосперма, и 6,42 (среднеквадратичное отклонение 0,26) в колбах с волокном.
Выводы
Введение волокна кокосового эндосперма в модель толстого кишечника собаки привело к исключению жизнеспособных клеток Campylobacter jejuni. При отсутствии в модели волокна кокосового эндосперма клетки С.jejuni не утратили свою жизнеспособность в течение эксперимента. Поскольку уровень рН от 6,5 до 7,5 является оптимальным для Campylobacter, вряд ли разница в этом показателе оказалась определяющей разницу в жизнеспособности клеток. Напротив, вероятно, что непатогенные сахаролитические бактерии, присуствующие в фекалиях, участвуют в метаболизме волокна кокосового эндосперма. С.jejuni не способна к ферментации углеводородов, таким образом, волокно кокосового эндосперма создает благоприятную среду для неболезнетворных сахаролитических бактерий.
Пример 7
Объектом изучения является сравнительная характерика воспалительных процессов в кишечнике в условиях кормления пищей, содержащей волокно кокосового эндосперма и без него.
Методики
В эксперименте участвовали 7 собак разных пород. Собак на период эксперимента, включая время кормления и анализов, содержали отдельно. Эксперимент проводили как перекрестный. Собак кормили по отдельности в объеме, необходимом для поддержания веса тела (125×BW0.75), и обеспечивая постоянный доступ к питьевой воде все время в течение 4 недель, включая одну неделю очистки. Тестовая диета была полноценной влажной формы, она состояла из мясных кусочков, законсервированных в воде. Волокно кокосового эндосперма было введено в рацион в объеме 7,2% (мас./мас.). Содержание остальных компонентов корма было уменьшено пропорционально с учетом добавки волокна кокосового эндосперма в форме брикетированной копры. Питание в период очистки было полноценным и сбалансированным.
Пробы биопсии
Из среднего кишечника были взяты три пробы биопсии, перенесены в среду для выращивания бактерий (RPMI плюс гентомицин) и взвешены. В течение 30 мин пробы биопсии промывали в свежей среде и затем перемещали в свежую мультиячеечную пластину с 24 ячейками, содержащую 1 мл среды, где их культивировали в течение 24 ч при температуре 37°С и при содержании CO2 5%. Затем пробы биопсии в течение 5 мин центрифуговали при 13000 об/мин, образовавшийся верхний слой переместили в свежую eppendorf колбу и заморозили при температуре -20°С до тех пор, пока они не понадобятся. В пробы биопсии добавили 0,5 мл 1% лизисного раствора в тритоновом буфере (20 mM Tris рН 7,5, 20 mM NaCl2, 1% тритона×100), после чего оставили минимум на 1 ч. Затем пробы быстро гомогенизировали и измерили общее содержание белка с использованием аппарата Sigma Microprotein-PR™. Оказалось, что общее содержание белка значительно коррелирует с влажной массой образца, взятого на биопсию, при этом содержание использовали для стандартизации образования эйкозаноидов.
Измерение количества образовавшихся эйкозаноидов
Объем образования PGE2 в пробах биопсии среднего кишечника измеряли путем иммуноферментативного анализа (EIA). Пробы верхнего слоя разбавили 1 к 10 свежей средой. Иммуноферментативный анализ PGE2 проводили с помощью R&D System и результаты фиксировали в протоколе. Вкратце, 100 мкл пробы и стандарт PGE2 поместили на пластину с 96 микроячейками, на которую предварительно нанесли поликлональные антитела goat anti-mouse/rabbit. Добавили 50 μl PGE2, конъюгированного со щелочной фосфотазой, и 50 μl поликлональных антител мыши к PGE2. Пластину инкубировали в течение 2 ч при комнатной температуре на горизонтально-орбитальном вибрационном смесителе при 500±50 об/мин. После инкубации пластину промыли и добавили 200 мкл субстрата pNPP. После часа инкубации добавили 50 мкл стоп-раствора тринатрийфосфата, после чего при помощи считывающего устройства для микропластин с установкой длины волны 450 nm была определена оптическая плотность каждой ячейки. Концентрация эйкозаноидов на мг белка из пробы биопсии рассчитывали по стандартной кривой.
Результаты
Определение образования эйкозаноида путем биопсии проб кишечника
Пока собак кормили диетическим кормом, содержащим волокно кокосового эндосперма, при биопсии получали значительно меньше PGE2, чем при кормлении собак стандартным кормом (Р=0,08). Результаты отражены в приведенной ниже таблице и на Фиг.3, на которых показано образование PGE2, измеренное путем биопсии кишечника.
Одна и та же буква указывает на незначительную разницу (р<0,1)
Приложение 1 - качество фекальных масс
- Чтобы оценить все дефекации, использовали шкалу с 17 категориями, при помощи которой возможные значения качества фекальных масс были распределены между каждым из пяти основных делений еще на четыре уровня по нарастающей.
- Если для оценки качества фекальных масс шкалы с делением каждого из основных значений пополам было недостаточно, то использовалась шкала с делением каждого значения на четыре уровня. Шкала с точностью в полделения приведена ниже.
- Для оценки всех дефекаций использовали шкалу с 9 значениями, по которой определяли качество фекальных масс по нарастающей от 1 до 5 с учетом половинных значений. Шкала с точностью в полделения следующая:
- Ниже приведен пример оценки фекальных масс с использованием шкалы, когда качество определяется как идеальное и недопустимое:
Недопустимое (или плохое качество фекальных масс) (Н) = меньше чем 1,5 и больше чем 3,5 (не включая границы)
Идеальное (И) = между 1,5 и 2,5 (включительно)
- Определяли усредненное значение качества фекальных масс для каждой собаки и затем определяли конечное среднее значение за весь период эксперимента как среднее от всех полученных значений.
Приложение 2
Метод Энглиста (по Энглисту и Кумингу (Supra))
Экспериментальная установка
Фракцинирование проводили в 50-60 мл центрифужных стеклянных колбах с завинчивающимися крышками, как описано выше. Газожидкостную хроматографию проводили с применением хроматографа Pye Unicam 204 серии с пламенно-ионизационным детектором. Использовали стеклянную трубку 2,1 м × 2 мм, заполненную Supelcoport (100-200 меш), покрытым 3% SP 2330. Температура трубки была 215°С (изотермальная), а температура впрыскивателя и детектора была 250°С. Расход газа-носителя контейнера (азота) был 20 мл min-1.
Реагенты
Для всех анализов использовали высокопробные сертифицированные реагенты. Ферментные препараты были следующие: панкреатическая α-амилиза свиньи, Е.С.3.2.1.1. (Sigma, Cat.No. A4268); пуллуланаза, Е.С.3.2.1.41. (Boehringer, Cat. No.108944).
Методика
Последовательность операций методики представлена на Фиг.1.
Предварительная обработка проб
Насколько только это возможно, продукты следует анализировать без какой-либо предварительной обработки. Если со взятием проб возникают сложности, то продукты с низким содержанием воды можно раздробить в шаровой мельнице в течение 2-3 минут, а продукты с высоким содержанием воды - гомогенизировать или провести сушку вымораживанием и затем измельчить в шаровой мельнице.
Масса образца
Аккуратно взвесить от 50 до 1000 мг пробы, содержащей не более 150 мг крахмала и 50 мг NSP в 50-60 мл колбу для центрифуги с завинчивающейся крышкой и добавить мешалку.
Обезжиривание и высушивание
Пробы с содержанием сухого вещества от 90 до 100% и с содержанием жиров менее 203% можно анализировать без всякой дополнительной подготовки. В противном случае добавляют 40 мл ацетона, смешивают в течение 30 мин с использованием магнитного смесителя, затем центрифугируют и после этого путем откачивания извлекается столько верхнего слоя, сколько возможно, не нарушая осадка.
Дисперсия крахмала
Добавили 2 мл DMSO, колбу закрыли крышкой и нагревали на кипящей водяной бане в течение 1 ч после закипания при постоянном перемешивании. Затем, не охлаждая, добавили 8 мл 0,1 М буферного раствора ацетата натрия с рН 5,2 при 50°С и немедленно интенсивно смешали.
13 мл в уроновую кислоту
и 0,1 мл раствора NaBH4
Процедура анализа некрахмалистых полисахаридов
Ферментный гидролиз крахмала
Колбу охлаждают до 45°C и немедленно добавляют 0,1 мл ферментного раствора, содержащего 5000 единиц α-амилизы и 5 единиц пуллуланазы на 1 мл ацетатного буферного раствора с рН 5,2. Образцы инкубируют при температуре 45°С на 16-18 часов, желательно, при непрерывном перемешивании, как описано выше.
После ферментной обработки добавляют 40 мл чистого этанола, хорошо смешивают и оставляют отстаиваться в течение 1 часа при комнатной температуре. Центрифугируют в течение 10 мин или до появления прозрачного верхнего слоя жидкости. Отсасывают верхний слой насколько возможно, не нарушая осадка, и отбрасывают его. Осадок промывают дважды 50 мл 85% этанола путем смешивания с этанолом с образованием суспензии, центрифугирования до образования прозрачного слоя и и отделения верхнего слоя, как описано выше. Добавляют 40 мл ацетона к промытому осадку, перемешивают в течение 5 мин и затем центрифугируют. Верхний слой удаляют и осадок высушивают, как описано для обезжиривания и высушивания.
Кислотный гидролиз остатка после ферментного расщепления
Осадок диспергируют в 1 мл 12М серной кислоты с использованием вихревого смесителя. Оставляют при температуре 35°C на 1 ч для растворения целлюлозы, затем быстро добавляют 11 мл воды и смешивают.
Подогревают раствор в кипящей воде в течение 2 ч после закипания при постоянном перемешивании. Охлаждают при комнатной температуре, помещая колбу в воду, добавляют 2 мл внутреннего стандарта (2 мг аллозы на мл насыщенного раствора бензойной кислоты) и смешивают содержимое в колбе. Используют 1 мл гидролизата для приготовления ацетата альдита и оставляют часть для определения содержания уроновых кислот.
Уроновые кислоты
Для анализа применяли модифицированный метод Скотта. Смешивают 0,3 мл гидролизата (при необходимости разбавленного так, чтобы он содержал от 25 до 100 мкг уроновой кислоты на 1 мл) с 0,3 мл раствора борохлорида натрия (приготовленного смешиванием 2 г хлорида натрия и 3 г борной кислоты со 100 мл воды). Добавляют 5 мл концентрированной серной кислоты и интенсивно смешивают, затем помещают колбу в термостат, нагретый до 70°C. Оставляют колбу на 40 мин и затем охлаждают до комнатной температуры, поместив в воду. После охлаждения добавляют 0,2 мл раствора 3,5-диметилфенола (0,1 г (СН3)2-С6Н3ОН в 100 мл ледяной уксусной кислоты) и немедленно смешивают. Через 10-15 мин считывают поглощение при длине волны 400 и 450 нм в спектрофотометре по сравнению с водой. Для каждой пробы вычитают результат, считанный при 400 нм из результата при 450 нм и вычерчивают график для разницы, полученной со стандартом глюкуроновой кислотой (в интервале от 25 до125 μf мл-1). Считывают концентрацию проб по графику.
Приготовление ацетатов альдитола
К 1 мл гидролизата добавляют 0,2 мл 12М раствора аммония и 5 мкл октан-2-ола. Проверяют, что раствор имеет щелочную среду, и затем добавляют 0,1 мл свежеприготовленного раствора тетрагидрокарбоната натрия (III) (борогидрата натрия) на мл 3М раствора аммония. Смешивают, оставляют раствор на 1 ч при температуре 40°С и добавляют 0,1 мл кристаллизованной уксусной кислоты. Затем к 0,2 мл подкисленного раствора добавляют 0,3 мл N-метилимидазола и 2 мл уксусного ангидрида и смешивают. Оставляют на 10 мин при 20°С (при комнатной температуре), добавляют 5 мл воды, смешивают и после охлаждения добавляют 1 мл дихлорометана, сильно перемешивают содержимое на вихревом смесителе и помещают в центрифугу на несколько минут, чтобы разделить смесь на две фазы. Отделяют основную часть верхнего слоя путем откачивания и выливают его, затем перемещают нижнюю фракцию в маленькую емкость, запечатывают и хранят при температуре -20°С. Используют по 1-2 мкл для впрыскивания при хроматографии.
Другой способ приготовления ацетатов альдита
При использовании дихлорометана в качестве растворителя ацетатов альдита было обнаружено, что в ряде лабораторий, где нет газожидкостного хроматографа с атоматическим впрыскивателем методика впрыскивания является критичной для достижения воспроизводимых результатов. Более надежную методику можно получить при замене дихлорометана этилацетатом как растворителем ацетатов альдита. Эта процедура следующая:
К 1 мл гидролизата добавляется 0,2 мл 12М раствора аммония и 5 мкл октан-2-ола. Проверяют, что раствор имеет щелочную среду, и затем добавляют 0,1 мл свежеприготовленного раствора тетрагидрокарбоната натрия (III) (борогидрата натрия) на 1 мл 3М раствора аммония. Смешивают, оставляют раствор на 1 ч при температуре 40°С и добавляют 0,1 мл ледяной уксусной кислоты. К 0,5 мл подкисленного раствора добавляют 0,5 мл N-метилимидазола и 2 мл уксусного ангидрида и смешивают. Оставляют на 10 мин при 20°С (при комнатной температуре), затем добавляют 0,6 мл этанола и смешивают. После 5 мин добавляют 5 мл воды, помещают на водяную баню при комнатной температуре, добавляют 5 мл 7,5 М КОН и через несколько минут еще 5 мл 7,5 М КОН. Смешивают путем перевертывания и оставляют для разделения двух фракций. Переносят верхнюю фракцию в меньший сосуд и хранят при +5°С. Используют 1-2 мкл для впрыскивания в хроматограф.
Замечания
Следует понимать, что приведенное выше подробное описание и сопровождающие его иллюстрации служат исключительно для того, чтобы максимально понятно изложить суть настоящего изобретения, но не являются ограничивающими. Возможны другие аспекты, преимущества и модификации изобретения в пределах формулы изобретения, которая приведена ниже.
Изобретение относится к области кормопроизводства. Предложены корм для домашних животных, который содержит волокно кокосового эндосперма в качестве диетической волокнистой составляющей, способ приготовления корма, включающий смешивание волокна кокосового эндосперма с другими ингредиентами корма, способ кормления домашних животных, применение волокна кокосового эндосперма в качестве диетической волокнистой составляющей корма для домашних животных (варианты) и способ профилактики кишечных заболеваний у домашних животных (варианты). Изобретение позволяет поддержать нормальное функционирование желудочно-кишечного тракта у домашних животных. 11 н. и 18 з.п. ф-лы, 3 ил., 7 табл.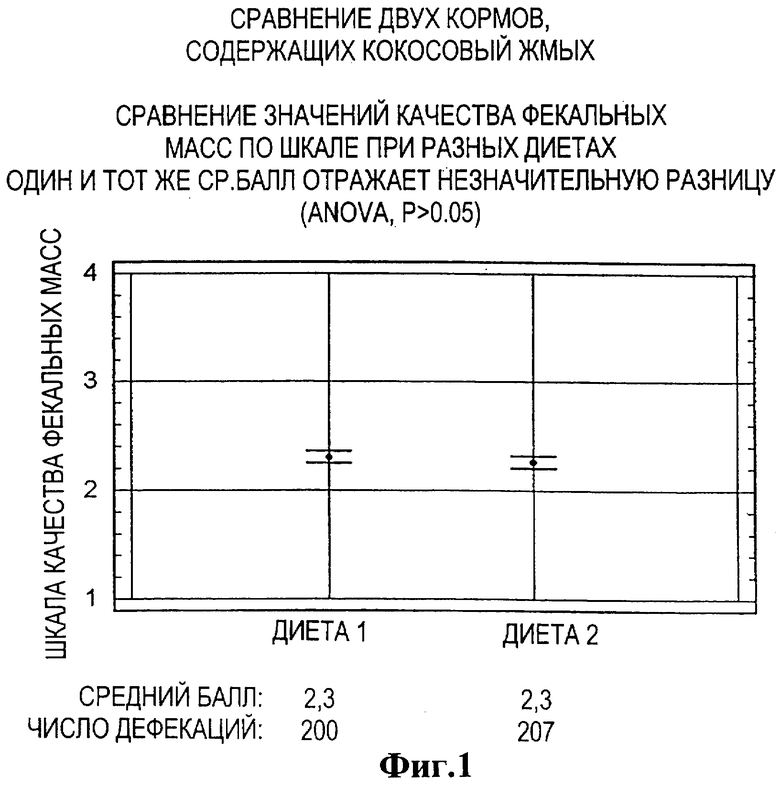
| WO 9639046, 12.12.1996 | |||
| Захватное устройство | 1981 |
|
SU1008138A1 |
| ХИМИЧЕСКИЙ СОСТАВ ПИЩЕВЫХ ПРОДУКТОВ: Справочник | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2006-02-10—Публикация
2000-03-10—Подача