Область техники, к которой относится изобретение
Настоящее изобретение имеет отношение к питанию млекопитающих и его влиянию на иммунный ответ. В частности, настоящее изобретение применяет пробиотические организмы, которые вводят животному для улучшения как врожденного, так и приобретенного иммунитета и для усиления эффективности вакцины у животного.
Предшествующий уровень техники
Различные публикации, включая патенты, опубликованные заявки, технические статьи и научные статьи цитируются на всем протяжении описания. Полный список публикаций, не процитированных полностью в описании, приведено в конце описания.
Пробиотики определяют как живые микроорганизмы, которые при введении в соответствующих количествах оказывают благоприятный эффект на здоровье хозяина (Schrezenmeir J et al. (2001)). Существует теория, согласно которой пробиотики могут передавать свой полезный для здоровья эффект или посредством увеличения устойчивости к заселению патогенными бактериями поверхностей слизистой оболочки (устойчивость к заселению) (Sanders ME (2003)) или оказывая прямое влияние на связанную с кишечником лимфоидную ткань (GALT), что приводит к образованию иммуномодулирующих соединений (Isolauri Е et al. (2001а) и Macpherson AJ et al. (2004)).
Пробиотики применяют для модулирования течения различных инфекционных заболеваний в терапии людей (Isolauri Е (2001b)). Напротив, в ветеринарии было проведено немного исследований, из них большинство ветеринарных исследований было проведено на больших животных. В этих исследованиях пробиотики применяли для того, чтобы попытаться изменить выделение в окружающую среду фекальных патогенных микроорганизмов (Kim LM et al. (2001)) или улучшить показатели продуктивности, такие как увеличение веса, скорость конверсии корма и снижение смертности. В одном из исследований на животных группе щенков, вакцинированных вирусом собачьей чумы (CDV), скармливали штамм SF68 (NCIMB10415) Enterococcus faecium и сравнивали с контрольной группой, которая получала только вакцинацию (Benyacoub J et al. (2003)). Щенки, у которых вакцинация была дополнена введением SF68, имели повышенную концентрацию общих IgA в сыворотке и в кале, повышенную концентрацию CDV-специфических IgG и IgA в сыворотке и повышенный процент циркулирующих В-лимфроцитов по сравнению с контрольной группой щенков, что подтверждает тот факт, что этот пробиотик индуцирует усиливающий иммунитет эффект.
Вирус панлейкопении кошачьих (FPV) представляет собой вирус, вызывающий вирусемию, сопровождающуюся тяжелым желудочно-кишечным заболеванием; надлежащим образом вакцинированные котята имеют стерильный иммунитет (Richards J et al. (2001)). Тем не менее, инфекции верхних дыхательных путей остаются основной проблемой ветеринарии кошек (Sykes JE et al. (1999)). Кошачий ринотрахеит FHV-1) и кальцивирус кошачьих (FCV) представляют собой два вирусных патогена, вовлеченных в этот синдром. Хотя относительная эффективность вакцины FCV после прививания вместе с патогенным штаммом для экспериментального заражения у вакцинированных животных по сравнению с невакцинированными животными составляет >95%, вакцины FHV-1 индуцируют только приблизительно 60% относительной эффективности (Lappin MR et al. 2002)). Таким образом, FHV-1 продолжает оставаться значительной проблемой, несмотря на повсеместную вакцинацию (Sykes JE et al. (1999)). Предыдущие попытки улучшить эффективность вакцинации включали интраназальное введение, которое вызывало сильные побочные эффекты (Scott FW et al. (1999)) и генетические изменения вирулентных штаммов, что приводило к снижению тяжести заболевания, но не снижало уровень распространения носительства возбудителей инфекции (Slater Е et al. (1976)). Носительство возбудителей инфекции может привести к рецидиву или повторному инфицированию хозяина, а также к передаче инфекции к живущим в доме. Хронические инфекции FHV-1 пытались лечить с применением разнообразных терапевтических подходов, включая интерферон альфа, трефинацию, противовирусные лекарственные препараты, рассечение носа, глюкокортикоиды, местные противоотечные средства и антибиотики, направленные на вторичные бактериальные инфекции (Van Pelt DR et al. (1994)). Тем не менее, ни один из этих походов не был способен устранить хроническую вирусную инфекцию; поэтому так распространены рецидивы выделения вируса в окружающую среду и случаи клинических заболеваний. Считается, что для предупреждения и контроля инфекций α-герпесвируса важны иммунные ответы, опосредуемые как клетками, так и IgA слизистой оболочки (Lappin MR et al. (2002) и Slater Е et al. (1976)). Для снижения смертности, вызываемой этим патогеном, необходимы улучшенные вакцины FHV-1 или улучшенные ответы на вакцинацию.
Раскрытие изобретения
Один аспект настоящего изобретения характеризует композицию, включающую один или более пробиотических организмов в количестве, эффективном для модуляции иммунитета или усиления эффективности вакцины у животного. Модуляция иммунного ответа и усиление эффективности вакцины служит для защиты животного и уменьшения заболеваемости и смертности, индуцируемой патогенами.
В некоторых воплощениях композиция представляет собой кормовую композицию для домашних животных или кормовую композицию для животных, диетическую добавку или пищевой продукт, составленный таким образом, что его могут потреблять люди. В различных воплощениях пробиотические организмы включают, по меньшей мере, один из видов Enterococcus spp., один или вместе с другими пробиотическими организмами, такими как Streptococcus spp., Lactobacillus spp., Lactococcus spp.. Bacillus spp., Bifidobacterium spp.или Saccharomyces spp. В предпочтительных воплощениях пробиотический организм представляет собой Enterococcus faecium NCIMB 10415 (SF68). Композиции могут включать дополнительные компоненты. Например, могут быть включены одно или более соединений, которые дополнительно усиливают иммунитет, такие как 7-оксо-дегидроэпиандростерон.
В некоторых воплощениях композиции были составлены для животных-компаньонов, таких как кошка. В других воплощениях композиции были составлены для животных, не являющихся животными-компаньонами, в особенности для членов семейства кошачьих. В других воплощениях композиции были составлены таким образом, что их могут потреблять люди.
Другой аспект изобретения характеризует способ модулирования иммунитета у животного, включающий регулярное введение животному композиции, включающей один или более пробиотических организмов, таких как были описаны выше, в количестве, эффективном для модулирования иммунитета у животного. В некоторых воплощениях способ применяли для животного-компаньона, такого как кошка. В других воплощениях способ применяли для животных, не являющихся животными-компаньонами, в особенности для членов семейства кошачьих. В других воплощениях способ применяли для людей.
Другой аспект изобретения характеризует способ для усиления эффективности вакцины у животного, включающий регулярное введение животному композиции, включающей один или более пробиотических организмов, таких как были описаны выше, в количестве, эффективном для усиления эффективности вакцины у животного. В предпочтительных воплощениях вакцина представляет собой вирус кошачьего ринотрахейта, кальцивирус кошек или вирус панлейкопении кошачьих. В некоторых воплощениях способ применяли для животного-компаньона, такого как кошка. Способ применяли для животных, не являющихся животными-компаньонами, в особенности для членов семейства кошачьих. В других воплощениях способ применяли для людей.
Другой аспект изобретения характеризует применение одного или более пробиотических организмов, таких как были описаны выше, в производстве лекарственного средства или композиции для модулирования иммунитета у животного. В некоторых воплощениях композиция представляет собой функциональный продукт или диетическую добавку. Композиция может быть скормлена животному-компаньону, такому как кошка. В других воплощениях композиция может быть применена для животных, не являющихся животными-компаньонами, в особенности для членов семейства кошачьих. В других воплощениях применение может быть направлено на людей.
Другой аспект изобретения характеризует применение одного или более пробиотических организмов, таких как были описаны выше, в производстве лекарственного средства или композиции для усиления эффективности вакцины у животного. В некоторых воплощениях композиция представляет собой функциональный продукт или диетическую добавку. Композицию можно вводить животному регулярно в количестве, эффективном для усиления эффективности вакцины у животного. В предпочтительных воплощениях вакцина представляет собой вирус кошачьего ринотрахеита, кальцивирус кошек или вирус панлейкопении кошачьих. В некоторых воплощениях композицию применяли для животного-компаньона, такого как кошка. В других воплощениях композицию применяли для животных, не являющихся животными-компаньонами, в особенности для членов семейства кошачьих. В других воплощениях композицию применяли для людей.
Другие особенности и преимущества изобретения будут объяснены с помощью ссылок на чертежи, подробного описания и последующих примеров.
Краткое описание чертежей
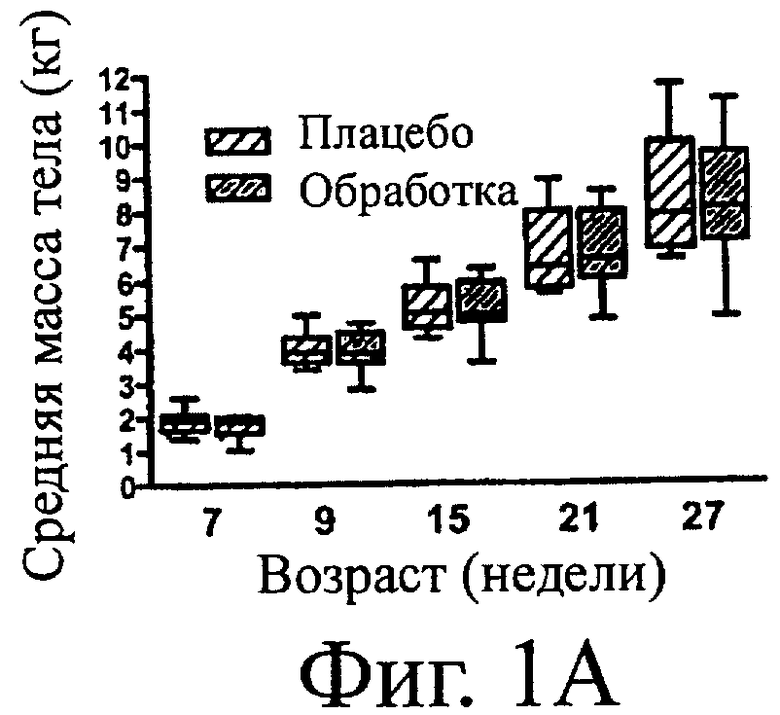
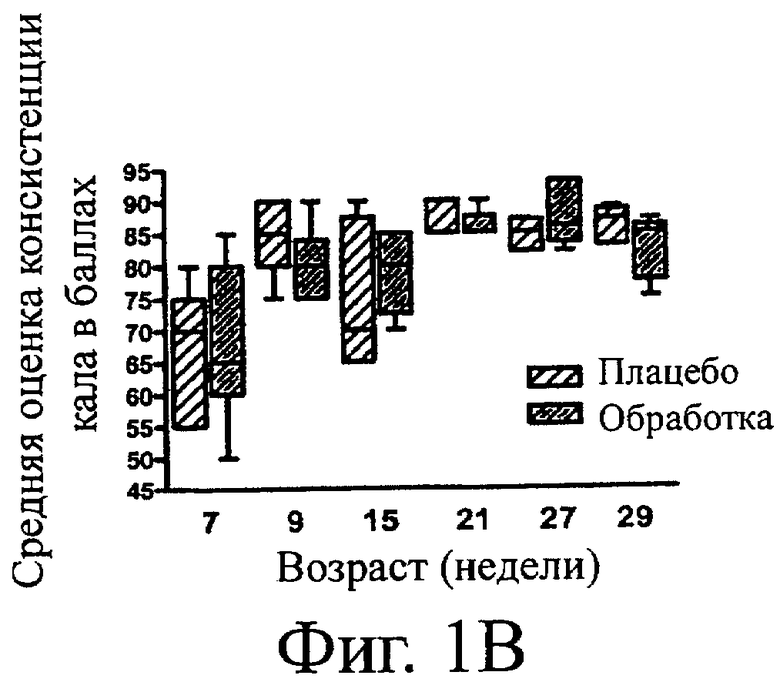
Фигура 1. Масса тела (А) и оценка консистенции кала в баллах (B), определенные в течение того времени, когда котята ежедневно, начиная с 7-ми недельного возраста и до возраста 27 недель, получали по 150 мг куриного гидролизата РО (Плацебо, n=9) или по 150 мг куриного гидролизата, смешанного с 5×108 КОЕ/день Enterococcus faecium штамм SF68 (Обработка, n=9). Котят вакцинировали подкожно коммерческой модифицированной живой вакциной FHV-1 на 9 и 12 неделях жизни. Прямоугольник и «усы» (планка погрешности) означают минимум, максимум, медиану и 25-й и 75-й процентили. р>0,05 во всех временных точках.
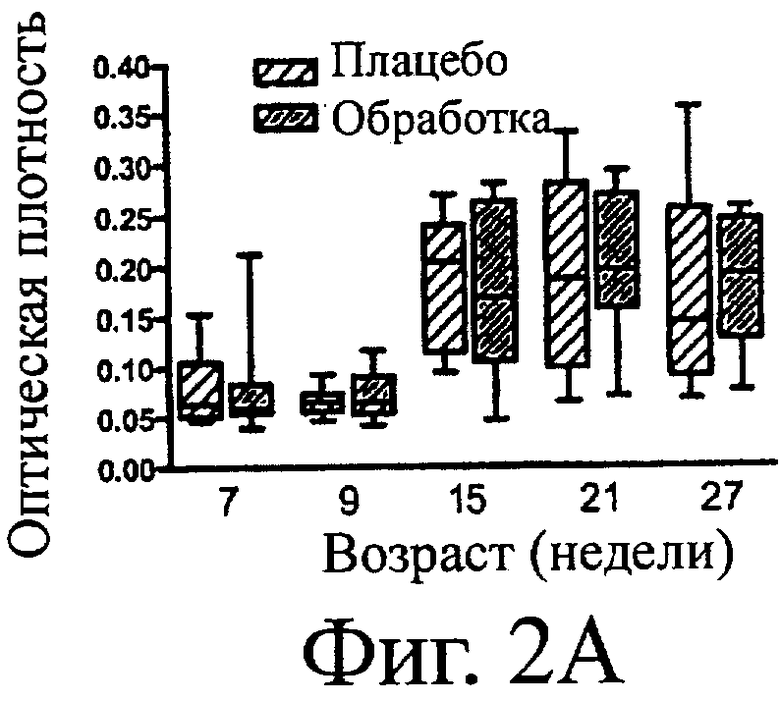
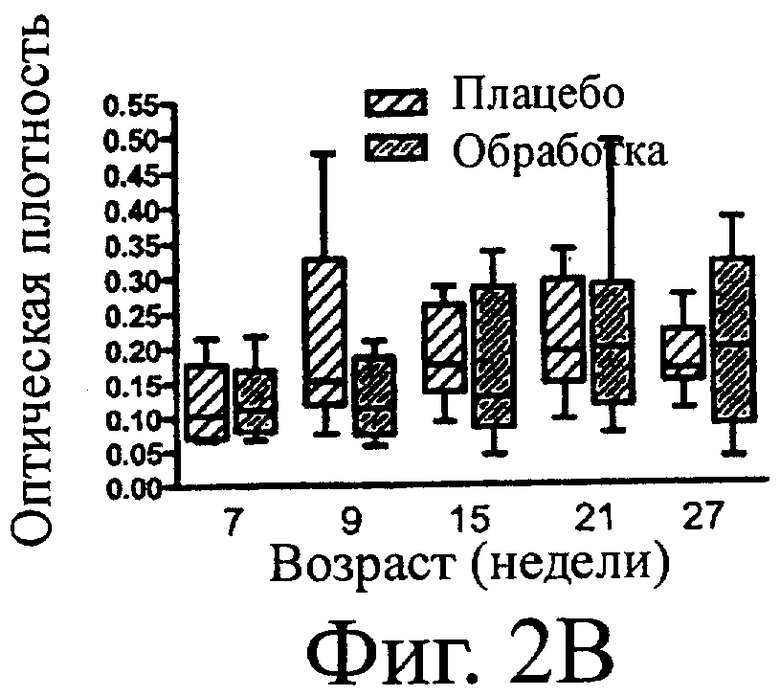
Фигура 2. FHV-1-специфические IgA, полученные из сыворотки (А) и слюны (B) котят, получавших (Обработка) или неполучавших (Плацебо) SF68. Прямоугольник и «усы» (планка погрешности) означают минимум, максимум, медиану и 25-й и 75-й процентили. р>0,05 для всех временных точек.
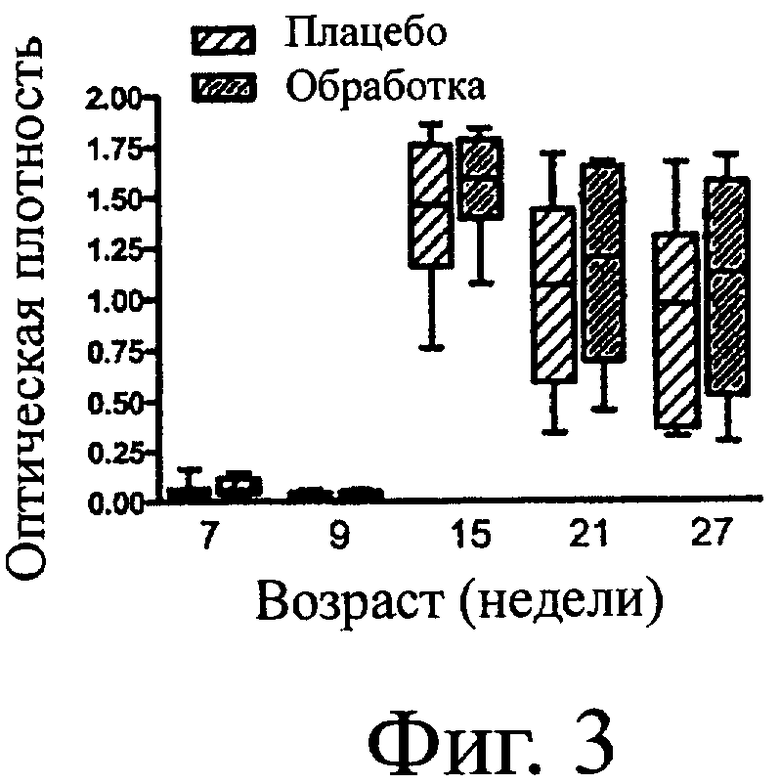
Фигура 3. FHV-1-специфические IgG, полученные из сыворотки котят, получавших (Обработка) или неполучавших (Плацебо) SF68. Прямоугольник и «усы» (планка погрешности) означают минимум, максимум, медиану и 25-й и 75-й процентили. р>0,05 для всех временных точек.
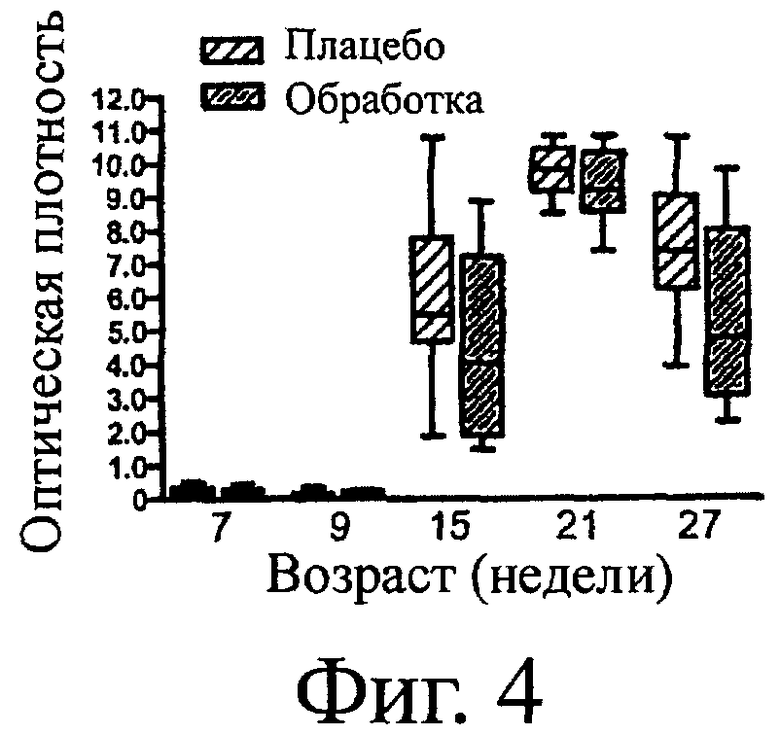
Фигура 4. FHV-1-специфические IgG, полученные от котят, получавших (Обработка) или неполучавших (Плацебо) SF68. Прямоугольник и «усы» (планка погрешности) означают минимум, максимум, медиану и 25-й и 75-й процентили. р>0,05 для всех временных точек.
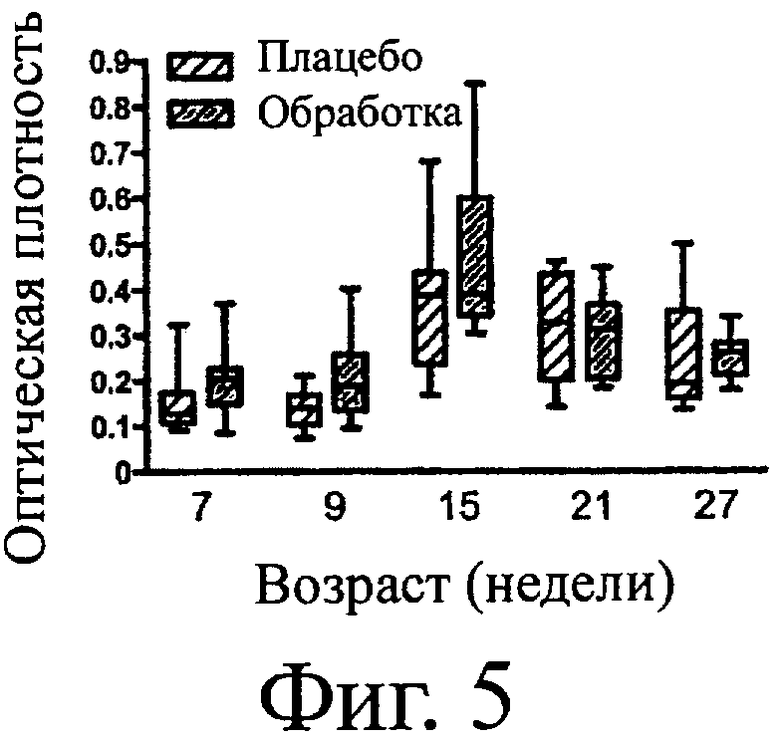
Фигура 5. FPV-специфические IgG, полученные от котят, получавших (Обработка) или неполучавших (Плацебо) SF68. Прямоугольник и «усы» (планка погрешности) означают минимум, максимум, медиану и 25-й и 75-й процентили. р>0,05 для всех временных точек.
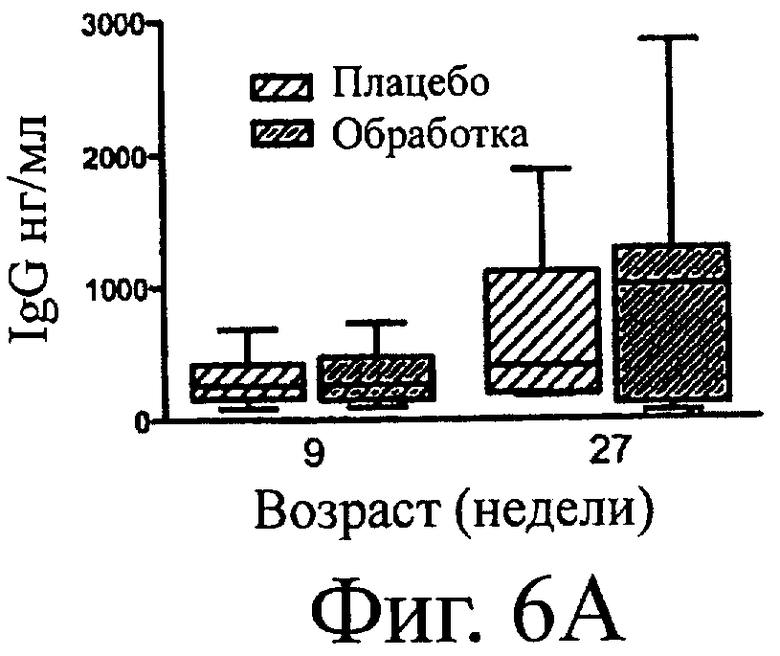
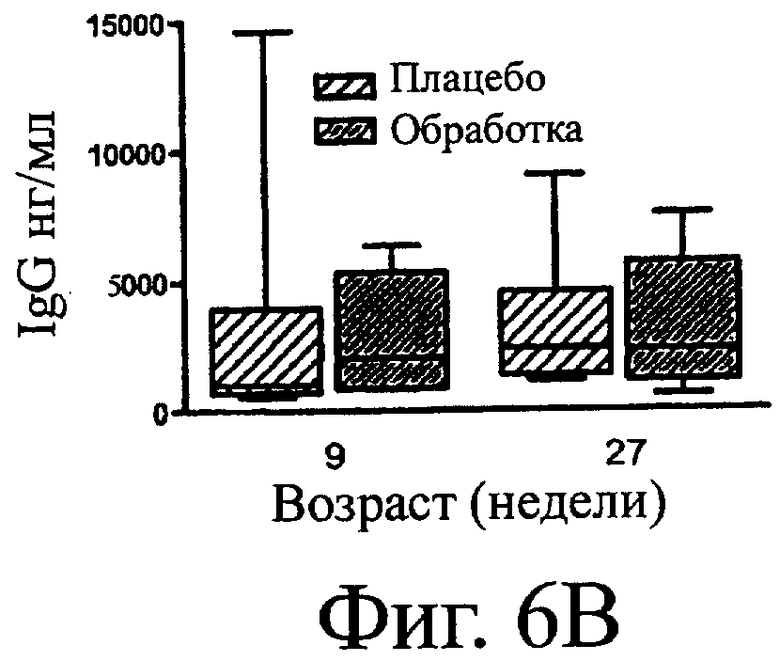
Фигура 6. Общие IgG (А) и IgA (B) в экстракте кала котят, получавших (Обработка) или неполучавших (Плацебо) SF68. Прямоугольник и «усы» (планка погрешности) означают минимум, максимум, медиану и 25-й и 75-й процентили. р>0,05 для всех временных точек.
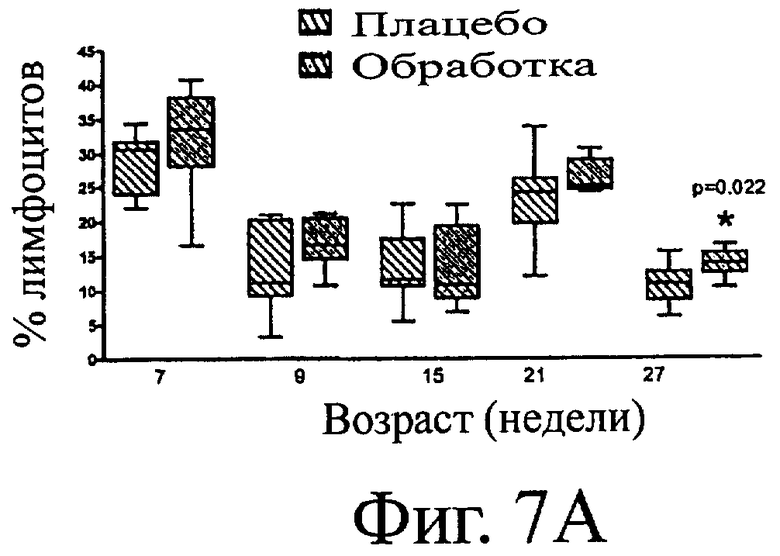
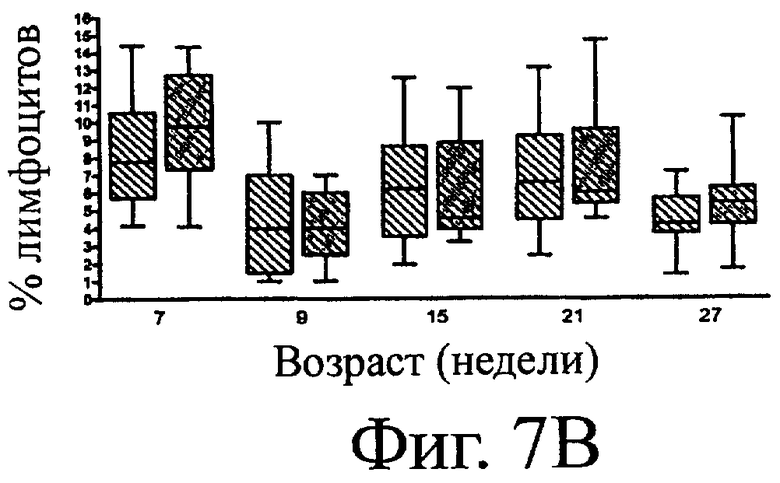
Фигура 7. Процент лимфоцитов в периферической крови, положительных в отношении CD4 (А) и CD8 (B), определенный с помощью проточной цитометрии у котят, получавших (Обработка) или неполучавших (Плацебо) SF68. Прямоугольник и «усы» (планка погрешности) означают минимум, максимум, медиану и 25-й и 75-й процентили. * обозначает временные точки, в которых величины для группы Обработка были значительно выше, чем для группы Плацебо.
Подробное описание иллюстративных воплощений
Определения
На протяжении описания изобретения и в формуле изобретения применяли различные термины, имеющие отношение к способам и другим аспектам настоящего изобретения. Если не указано иначе, то такие термины будут даны в их обычном для этой области техники значении. Другие специально определенные термины будут объяснены в соответствии с определением, предоставленным настоящим документом.
В описании и примерах могут быть применены следующие сокращения: FHV-1, вирус кошачьего ринотрахеита; FCV, кальцивирус кошек; FPV, вирус панлейкопении кошачьих; spp. виды; ELISA, твердофазный иммуноферментный анализ; СВ, сухое вещество; КОЕ, колониеобразующая единица; кг, килограмм; BW, масса тела.
Термин «эффективное количество» означает такое количество описанного в этом документе соединения, вещества или композиции, которое будет эффективно для достижения определенного биологического результата. Такие результаты включают, но не ограничиваются, улучшение иммунитета или усиление эффективности вакцины у животного. Такое эффективное действие может быть достигнуто, например, с помощью введения композиции по настоящему изобретению животному.
В рамках настоящего описания значение термина «приблизительно» следует понимать как, необязательно, плюс или минус 20%, более предпочтительно, как, необязательно, плюс или минус 10%, еще более предпочтительно, как, необязательно, плюс или минус 5%, еще более предпочтительно, как, необязательно, плюс или минус 2%, наиболее предпочтительно необязательно, как плюс или минус 1%.
Термин «включающий…» следует понимать как «включает в числе других вещей…» и не следует понимать как «состоящий только из…».
Термины «приобретенный иммунитет» или «адаптивный иммунный ответ» применяются в настоящем документе взаимозаменяемо и в широком смысле и означают иммунный ответ на антигенную стимуляцию, включая развитие иммунологической памяти. Адаптивный иммунный ответ включает, без ограничений, гуморальный и клеточный иммунитет.
Термины «гуморальный иммунитет» или «гуморальный иммунный ответ» применяются в настоящем документе взаимозаменяемо и означают образование молекул иммуноглобулинов в ответ на антигенную стимуляцию.
Термины «клеточный иммунитет», или «клеточный иммунный ответ», или «опосредуемый клеткой иммунитет» применяются в настоящем документе взаимозаменяемо и означают активацию цитотоксических Т-лимфоцитов или Т-лимфоцитов-хелперов, мононуклеарных клеток и цитокинов в ответ на антигенную стимуляцию. Термин охватывает все приобретенные иммунитеты, которые не могут быть переданы интактному реципиенту с антителами.
Термин «врожденный иммунитет» означает неспецифические механизмы организма, обеспечивающие устойчивость против патогенов, которые не усиливаются в результате стимуляции определенным антигеном.
Термин «модулированный иммунитет» или «модуляция иммунитета» означает любое усиление или ингибирование способности организма вырабатывать врожденный или адаптивный иммунный ответ на стимуляцию антигеном, измеренный с помощью любого из способов, применяемых в этой области техники.
Термин «эффективности вакцины» означает способность вакцины вызывать у животного желаемый терапевтический или защитный эффект против специфического патогена. Термин «усиленная эффективность вакцины» означает любое усовершенствование в способности вакцины вызывать у животного желаемый терапевтический или защитный эффект против специфического патогена, измеренный с помощью способов, применяемых в этой области техники.
Термин «пробиотический организм» означает любой организм, в особенности микроорганизм, который оказывает благоприятное воздействие на животное-хозяина, такое как улучшение здоровья или устойчивость к заболеванию. Пробиотические организмы могут обладать одной или более из следующих неограничивающих характеристик: непатогенные или нетоксичные по отношению к хозяину; существуют как жизнеспособные клетки, предпочтительно, в больших количествах; способны к выживанию, к метаболизму и устойчивости в среде кишечника (например, устойчивость к низкому рН и желудочно-кишечным кислотам и секретам); адгезия на клетках эпителия, в особенности на клетках эпителия желудочно-кишечного тракта; бактерицидная или бактериостатическая активность или влияние на патогенные бактерии; антиканцерогенная активность; иммуномодулирующая активность, в особенности усиление иммунитета; модулирующая активность в отношении эндогенной флоры; улучшение состояния мочеполового тракта; антисептическая активность в ранах или вокруг ран и ускорение заживления раны; ослабление диареи; ослабление аллергических реакций; ослабление некротизирующего энтероколита новорожденных; ослабление воспалительного заболевания кишечника и ослабление кишечной проницаемости (Reid G et al. (2003); Drisko JA et al. (2003) и Oyetayo VO et al. (2004)).
Настоящее изобретение имеет отношение к любому животному, предпочтительно млекопитающему, и в одном воплощении к животным-компаньонам. «Животное-компаньон» представляет собой любое одомашненное животное и включает, без ограничений, кошек, собак, кроликов, морских свинок, хорьков, хомяков, мышей, песчанок, лошадей, коров, коз, овец, обезьян, свиней и им подобных. Собаки и кошки наиболее предпочтительны, и кошки приведены в качестве примера в этом документе. В некоторых воплощениях «животное» может быть человеком. В другом воплощении изобретение имеет отношение к животным, отличным от животных-компаньонов. В особенности, способ имеет отношение к членам семейства Felidae, семейства кошачьих, к которым изобретение может быть применено в случаях, когда есть возможность ввести кошке пробиотическую композицию (например, в зоопарке, в ветеринарном учреждении, в охотничьем заповеднике и им подобных местах). Кроме домашней кошки Felis cattus, семейство Felidae включает членов родов: (1) Acinonyx, такого как гепард (A. jubatus), (2) Neofelis, такого как дымчатый леопард (N. nebulosa), (3) Panthera, такого как лев (Р. leo), ягуар (Р. onca), леопард (Р. pardus), тигр (Р. tigris); (3) Uncia, такого как снежный барс (U. uncial); (4) Puma, такого как кугуар, горный лев или пума (Р. concolor) и (5) различные виды неодомашненных кошек (Felis), включая, но не ограничиваясь, калимантанская кошка (F. badia), каракал (F. caracal), китайская горная кошка (F bieti), камышовая кошка (F. chaus), барханный кот (F. margarita), черноногая кошка (F. nigripes), дикие кошки (F. sylvestris, F. lybica), ягуарунди (F. yagouraroundi), оцелот (F. pardalis), онцилла (F. tigrina), длиннохвостая кошка (F. wieldi), сервал (F. serval), рысь (F. lynx), красная рысь (F. rufus), пампасская кошка (F. colocolo), кошка Жоффруа (F. geoffroyi), андская горная кошка (F. jacobita), манул (F. manul), чилийская кошка (F. guigna), бенгальская кошка (F. bengalensis, F. iriomotensis), суматранская кошка (F. planiceps), пятнисто-рыжая кошка (F. rubiginosus), виверровая кошка (F. viverrina) и золотая кошка (F. aurata). Так как он был применен в этом документе, термин «кошачий» или «кошачье животное» означает всех членов семейства кошачьих, если не оговорено иное.
Примененные в этом документе термины «корм для домашних животных», «кормовая композиция для домашних животных», «корм для животных» или «кормовая композиция для животных» означают композицию, которая предназначена для поедания животными, предпочтительно, животными-компаньонами. «Полный и сбалансированный по питательным веществам корм для домашних животных или корм для животных» представляет собой такой корм, который содержит все известные необходимые питательные вещества в надлежащих количествах и соотношениях, основанных на рекомендациях признанных авторитетов в области питания животных, и который поэтому может служить в качестве единственного источника питания для поддержания жизни или стимуляции продуктивности без введения дополнительных источников питания. Сбалансированные по питательным веществам кормовые композиции для домашних животных и кормовые композиции для животных широко известны и широко применяются в этой области техники.
Примененный в этом документе термин «диетическая добавка» представляет собой продукт, предназначенный для поедания в дополнение к нормальному питанию животного.
Примененный в этом документе термин «пищевой продукт, созданный для потребления человеком» представляет собой любую композицию, предназначенную для поедания людьми.
Для этих целей или для того, чтобы описание было ясным и сжатым, некоторые воплощения были раскрыты в этом документе, но следует понимать, что особенности этих воплощений могут быть различными способами скомбинированы или использованы по отдельности в рамках объема изобретения.
Осуществление
Авторы изобретения обнаружили, что диетическая добавка к рациону питания котят пробиотических организмов, таких как Enterococcus faecium NCIMB 10415 (SF68) увеличивает число лимфоцитов CD4+. Соответственно, различные аспекты настоящего изобретения применяют эти открытия путем обеспечения диетической композиций и способов улучшения иммунитета у животного и для усиления эффективности вакцины у животного.
Композиции
Один аспект изобретения характеризует композиции, включающие один или более пробиотических организмов в количестве, эффективном для модуляции иммунитета или усиления эффективности вакцины у животных. В одном предпочтительном воплощении пробиотические организмы модулируют врожденный иммунитет у животного. В более предпочтительном воплощении пробиотические организмы модулируют адаптивный иммунный ответ у животного. В другом предпочтительном воплощении пробиотические организмы усиливают эффективность вакцины против FHV-1, FCV и FPV у животного.
Пробиотические организмы могут присутствовать в композиции в качестве компонента или добавки. Пробиотические организмы могут быть представлены прокариотами, эукариотами или архебактериями. В различных воплощениях композиции пробиотические организмы включают, по меньшей мере, один из любых подходящих штаммов или подвидов одного Enterococcus или в сочетании с другими пробиотическими организмами, включенными в такие рода, как Streptococcus, Lactobacillus, Lactococcus, Bacillus, Bifidobacterium или Saccharomyce. Виды Enterococcus включают, без ограничений, Enterococcus facecium, в особенности Е. faecium штамм SF68, а также другие Enterococci, такие как Е. faecium DSM 10663 (М74), Е. faecium GHR 017 DSM 7134, Е. faecium CECT 4515, Е. faecium CL15/ATCC 19434, Е. faecium NCIMB 11181/DSM 5464, Е. faecium IMB 52/DSM 3530, Е. faecium CNCM MA 17/5U, Е. faecium 202 DSM 4788/ATCC 53519, Е. faecium 301 DSM 4789/ATCC 55593, Е. faecium ATCC 19434, Е. faecium EF-101 ATCC 19434 и Е. faecium AK 2205 BCCM/LMG S-16555. Виды Streptococcus включают, без ограничений, Streptococcus faecium, Streptococcus thermophilus и Streptococcus salivarus. Виды Lactobacillus включают, без ограничений, Lactobacillus acidophilus, Lactobacillus brevis, Lactobacillus bulgaricus, Lactobacillus casei, Lactobacillus cellobiosus, Lactobacillus crispatus, Lactobacillus curvatus, Lactobacillus fermentum, Lactobacillus GG (подвиды rhamnosus видов Lactobacillus rhamnosus или Lactobacillus casei), Lactobacillus gasseri, Lactobacillus johnsonii, Lactobacillus plantarum, Lactobacillus salivarus, Lactobacillus reuteri, Lactobacillus johnsonii LAI, Lactobacillus acidophilus NCFB 1748, Lactobacillus casei Shirota, Lactobacillus acidophilus NCFM, Lactobacillus acidophilus DDS-1, подвиды delbrueckii вида Lactobacillus delbrueckii, подвиды bulgaricus type 2038 вида Lactobacillus delbrueckii, Lactobacillus acidophilus SBT-2062, Lactobacillus salivarius UCC 118, Lactobacillus paracasei ST11 и подвиды paracasei F19 Lactobacillus paracasei. Виды Lactococcus включают, без ограничений, Lactococcus lactis и Lactococcus plantarum. Виды Bacillus включают, без ограничений, Bacillus subtilis. Виды Bifidobacterium включают, без ограничений, Bifidobacterium adolescentis, Bifidobacterium bifidum, Bifidobacterium animalis, Bifidobacterium thermophilum, Bifidobacterium breve, Bifidobacterium longum, Bifidobacterium pseudolongum, Bifidobacterium infantis и Bifidobacterium lactis. Виды Saccharomyces включают, без ограничений, Saccharomyces boulardii (cerevisiae).
В одном предпочтительном воплощении композиции изобретения представляют собой кормовые композиции для домашних животных и кормовые композиции для животных. Они преимущественно включают корма, предназначенные для обеспечения необходимых потребностей в питании, а также лакомства (например, бисквиты) или другие диетические добавки к рационам. Необязательно, кормовые композиции для домашних животных и кормовые композиции для животных могут быть сухой композицией (например, гранулированный корм), полувлажной композицией, влажной композицией или любыми их смесями. В особых воплощениях композиции составлены для поедания животными из семейства кошачьих, включая, но не ограничиваясь домашней кошкой.
В другом предпочтительном воплощении композиции изобретения представляют собой пищевые продукты, созданные для потребления людьми. Они преимущественно включают продукты питания и нутриенты, предназначенные для обеспечения необходимых потребностей в питании людей, а также другие диетические добавки к рациону человека. В подробном воплощении пищевые продукты, созданные для потребления людьми, представляют собой полные и сбалансированные по питательным веществам пищевые продукты.
В другом предпочтительном воплощении композиция представляет собой диетическую добавку к рациону, такую как соус, питьевая вода, напиток, жидкий концентрат, йогурт, порошок, гранулу, пасту, суспензию, жвачку, легкую закуску, лакомство, снэки, драже, пилюлю, капсулу, таблетку или любую другую доставляемую форму. Добавки к рациону могут быть специально созданы для потребления определенными животными, такими как животное-компаньон или животное, не являющееся животным-компаньоном, в особенности кошкой или человеком. В детальном воплощении диетическая добавка к рациону может включать пробиотические организмы в высоких концентрациях, таких что кормовая добавка может быть введена животному в небольших количествах или, альтернативно, может быть разбавлена перед введением животному. Может потребоваться смешать диетическую добавку к рациону с водой перед введением животному.
Композиция может быть охлаждена или заморожена. Пробиотические организмы могут быть предварительно смешаны с другими компонентами композиции для обеспечения необходимых полезных количеств, могут быть нанесены на кормовую композицию для домашних животных, на диетическую добавку к рациону или на пищевой продукт, созданный для потребления людьми, или могут быть добавлены к композиции до того, как ее предложат животному, например применяя порошок или смесь.
Композиции по изобретению включают пробиотические организмы в количестве, эффективном для модулирования иммунитета или для усиления эффективности вакцины у животного, которому композиция была введена. Корма для домашних животных и пищевые продукты, созданные для потребления людьми, могут быть составлены так, что они будут содержать пробиотические организмы в пределах приблизительно от 102 до приблизительно 1011 колониеобразующих единиц (КОЕ) на грамм композиции. Диетические добавки к рациону могут быть составлены так, что они будут содержать пробиотические организмы в несколько раз более высоких концентрациях, что делает их пригодными для введения животному в форме таблетки, капсулы, жидкого концентрата или других подобных лекарственных форм или для разведений перед введениями, таким как разведение водой, распыление или посыпание на корм для домашних животных, и другие подобных способы введения.
В одном воплощении концентрация пробиотических организмов в композиции представляет собой функцию количества, требуемого для модулирования функций иммунитета, включая увеличение доли и/или числа лимфоцитов CD4+ в крови животного. В другом воплощении концентрация пробиотических организмов в композиции представляет собой функцию количества, требуемого для увеличения концентрации иммуноглобулинов, действующих против антигенов специфических патогенов в сыворотке крови, кале, секретах, таких как молоко, слезы и слюна. Уровень CD4+ лимфоцитов и концентрация иммуноглобулинов в сыворотке крови, кале, секретах, таких как молоко, слезы и слюна животного, могут быть определены любым способом, признанным и оцененным по достоинству специалистом в этой области техники.
Композиции по изобретению могут необязательно включать дополнительные вещества, такие как минералы, витамины, соли, приправы, красители и консерванты. Неограничивающие примеры дополнительных минералов включают кальций, фосфор, калий, натрий, железо, хлор, бор, медь, цинк, магний, марганец, йод, селен и им подобные. Неограничивающие примеры дополнительных витаминов включают витамин А, различные витамины В, витамин С, витамин D, витамин Е и витамин К. Могут быть также включены дополнительные диетические добавки к рациону, например ниацин, пантотеновая кислота, инулин, фолевая кислота, биотин, аминокислоты и им подобные.
Композиции по изобретению могут необязательно включать одно или более дополнительных веществ, которые активизируют или поддерживают здоровую иммунную систему или дополнительно модулируют иммунитет. Такие вещества включают, без ограничений, L-аргинин, стероиды, такие как 7-оксо-дегидроэпиандростерон (7-оксо-DHEA), каротиноиды, такие как альфа- и бета-каротин, антиоксиданты, и лекарственные травы или экстракты лекарственных трав, такие как астрагал и эхинацея.
В различных воплощениях изобретения кормовые композиции или композиции диетических добавок к рациону для животного могут включать от приблизительно 15% до приблизительно 50% общего белка от массы композиции в пересчете на сухое вещество. Исходное белковое сырье может включать растительные белки, такие как белки соевых бобов, хлопковых семян и арахиса, или животные белки, такие как казеин, альбумин и мясной белок. Неограничивающие примеры мясных белков, применяемых в этом документе, включают свинину, молодую баранину, конину, мясо домашней птицы, рыбу и их смеси.
Композиции могут дополнительно включать жир от приблизительно 5% до приблизительно 40% от массы композиции в пересчете на сухое вещество. Композиции могут дополнительно включать источник углеводов. Композиции могут включать углеводы от приблизительно 15% до приблизительно 60% от массы композиции в пересчете на сухое вещество. Неограничивающие примеры таких углеводов включают зерна или крупы, такие как рис, кукуруза, сорго, люцерна, ячмень, соя, канола, овес, пшеница и их смеси. Композиции могут также необязательно включать другие материалы, такие как сухую сыворотку и другие побочные продукты молочного производства.
Композиции могут также включать, по меньшей мере, один источник волокон. Могут быть применены разнообразные растворимые и нерастворимые волокна, которые известны специалистам в этой области техники. Источник волокон может быть представлен свекольной стружкой (из сахарной свеклы), аравийской камедью, камедью талха, камедью подорожника, рисовыми отрубями, смолой бобов рожкового дерева, цитрусовой пульпой, пектином, фруктоолигосахаридом дополнительно к короткоцепочечной олигофруктозе, маннанолигофруктозой, волокном сои, арабиногалактаном, галактоолигосахаридом, арабиноксиланом или их смесями. Альтернативно, источник волокон может быть ферментируемым волокном. Ранее было описано, что ферментируемое волокно полезно для иммунной системы животного-компаньона. Ферментируемое волокно или другие известные специалистам в этой области техники композиции, обеспечивающие пребиотическую композицию для усиления роста пробиотических микроорганизмов в кишечнике, могут быть также включены в композиции с целью усиления пользы, обеспечиваемой настоящим изобретением для иммунной системы животного.
В детальном воплощении композиция представляет собой полный и сбалансированный по питательной ценности корм для домашних животных или корм для животных. В этом контексте корм для домашних животных может быть влажным кормом, сухим кормом или кормом с промежуточным содержанием влаги, что должно быть определено специалистами в области создания и производства кормов для домашних животных. «Влажный корм» означает корм для домашних животных, который обычно продают в консервных банках или в пакетах из фольги и содержание влаги в котором обычно находится в диапазоне от примерно 70% до примерно 90%. «Сухой корм» означает корм для домашних животных, который представляет собой сходную с влажным кормом композицию, но содержит ограниченное количество влаги, обычно в диапазоне от примерно 5% до примерно 15%, и поэтому представлен, например, мелким похожим на бисквиты гранулированным кормом. Композиции и диетические добавки к рациону могут быть специально созданы для взрослых животных, или для старых животных, или для молодых животных, например композиции «еда для щенков», «еда для котят» или «для взрослых животных». В целом, специализированные композиции учитывают энергетические и пищевые потребности, присущие животным на разных стадиях развития или животным разного возраста.
Некоторые аспекты изобретения предпочтительно применяли в сочетании с полным и сбалансированным кормом (например, таким, какой был описан Национальным научно-исследовательским советом (National Research Council), 2006, в издании Nutritional Requirements for Dogs и Cats, National Academy Press, Washington D.C. или Ассоциацией американских официальных контролеров по качеству кормов (Association of American Feed Control Officials), в издании Official Publication 1996). To есть композиции, включающие пробиотические организмы в соответствии с некоторыми аспектами этого изобретения, предпочтительно применяли вместе с высококачественным промышленным кормом. Примененный в этом документе термин «высококачественный промышленно изготовленный корм» означает корм, произведенный для обеспечения усвояемости ключевых питательных веществ на 80% или более, такой какой был постулирован выше для собак и кошек, например, в рекомендациях Национального научно-исследовательского совета или такой, как описан в нормативах Ассоциации американских официальных контролеров по качеству кормов. Такие же высокие стандарты питательных веществ следует применять и для других животных.
Специалисту понятно, как определить соответствующее количество пробиотических организмов, которое следует добавить к данной композиции. Факторы, которые могут быть приняты во внимание, включают тип композиции (например, кормовая композиция для домашних животных, диетическая добавка к рациону или пищевой продукт, созданный для потребления людьми), среднее потребление определенных типов композиции разными животными, условия производства, в которых композиция была получена. Концентрации пробиотических организмов, которые следует добавить к композиции, могут быть рассчитаны на основе энергетических и пищевых потребностей животного. В соответствии с некоторыми аспектами изобретения пробиотические организмы могут быть добавлены в любой момент при производстве и/или при обработке композиции. Это включает, без ограничений, как часть формирования кормовой композиции для домашних животных, диетические добавки к рациону или пищевой продукт, созданный для потребления людьми, так и покрытие, нанесенное на кормовую композицию для домашних животных, диетическую добавку к рациону или пищевой продукт, созданный для потребления людьми.
Композиции могут быть созданы в соответствии с любым из способов, применяемым в этой области техники, таким, например, как способ, описанный в Waltham Book of Dog and Cat Nutrition, Ed. ATB Edney, Chapter by A. Rainbird, озаглавленный как «Сбалансированная диета» «A Balanced Diet» на страницах с 57 по 74, издательство Pergamon Press Oxford.
Способы
Другой аспект изобретения характеризует способы для модулирования иммунитета у животного, включающие введение животному композиции, включающей один или более пробиотических организмов в количестве, эффективном для модуляции иммунитета у животного. Еще один аспект изобретения характеризует способы для усиления эффективности вакцины у животного, включающие введение животному композиции, включающей один или более пробиотических организмов в количестве, эффективном для усиления эффективности вакцины у животного. В некоторых воплощениях вакцина направлена против вируса панлейкопении кошачьих, вируса кошачьего ринотрахеита или кальцивируса кошек.
В детальных воплощениях любого из двух приведенных выше аспектов изобретения композиция представляет собой кормовую композицию для домашних животных или кормовую композицию для животных, диетическую добавку к рациону или пищевой продукт, созданный для потребления людьми, как приведено в качестве примера в этом документе. В дополнительном детальном воплощении пробиотические организмы включают, по меньшей мере, один из видов Enterococcus spp., предпочтительно, Е. faecium, наиболее предпочтительно штамм SF68, один или вместе с другими пробиотическими организмами, включая один или более из Streptococcus spp., Lactobacillus spp., Lactococcus spp.. Bacillus spp., Bifidobacterium spp. или Saccharomyces spp., такими как были описаны выше. Животные могут включать любых одомашненных животных или животных-компаньонов, таких какие были описаны выше, или могут включать людей. В некоторых воплощениях животное представляет собой животного-компаньона, такого как кошка. В другом воплощении животное представляет собой человека.
Композиции могут быть введены животному с помощью любого из множества альтернативных путей введения. Такие пути включают, без ограничений, пероральный, интраназальный, внутривенный, внутримышечный, внутрижелудочный, транспилорический, подкожный, ректальный и им подобные. Предпочтительно композиции вводили перорально. Так как применено в настоящем документе, термин «пероральное введение» или «перорально введенный» означает, что животное поедает само или человеку предписано кормить животное или он сам кормит животное одной или несколькими композициями по изобретению, описанными в настоящем документе.
В случае если человеку предписано кормить композицией, такое предписание может заключаться в том, чтобы проинструктировать и/или проинформировать человека о том, что применение композиции может обеспечить и/или обеспечит такую пользу, о которой его проинформировали, например модуляцию иммунитета или усиление эффективности вакцины у животного. Такая инструкция может быть устной инструкцией (например, устная инструкция, полученная, например, от врача, ветеринара или другого медицинского специалиста или из средств информации по радио или по телевизору (т.е. из рекламных объявлений), или письменной инструкцией (например, письменная инструкция, полученная, например, от врача, ветеринара или другого медицинского специалиста (например, рецепты), от торгового специалиста или от организации (например, из потребительских брошюр, буклетов или других информационных изданий), письменных средств информации (например, из Интернета, по электронной почте или с помощью других компьютерных средств информации) и/или из упаковки, связанной с композицией (например, этикетка, помещенная на тару, содержащую композицию).
Введение можно проводить по необходимости или по желанию, например, один раз в месяц, один раз в неделю, ежедневно или чаще, чем один раз в день. Аналогично, введение можно осуществлять через день, через неделю или через месяц, на каждый третий день, каждую третью неделю или каждый третий месяц, каждый четвертый день, каждую четвертую неделю или каждый четвертый месяц и т.п. Введение можно проводить много раз в день. При применении в качестве добавки к обычным диетическим потребностям композиция может быть введена непосредственно животному или в противном случае может контактировать или быть перемешана с ежедневной пищей или кормом. Введение вместе с ежедневной пищей или кормом хорошо известно специалистам.
Введение можно также проводить регулярно, например, как часть режима питания животного. Например, режим питания может включать регулярное поглощение животным композиции, включающей один или более пробиотических организмов в количестве, эффективном для модуляции иммунитета или для усиления эффективности вакцины у животного. Регулярное поглощение может быть осуществлено один раз в день или два, три, четыре или более раз в день на ежедневной или еженедельной основе. Подобным образом регулярное поглощение может быть осуществлено на каждый второй день или вторую неделю, на каждый третий день или третью неделю, на каждый четвертый день или четвертую неделю, на каждый пятый день или пятую неделю или на каждый шестой день или шестую неделю, при таком режиме питания, введение можно осуществлять много раз в день. Цель регулярного введения - обеспечение животного предпочтительной ежедневно дозой пробиотических организмов, примеры которых приведены в этом документе.
Ежедневная доза пробиотических организмов может быть измерена в терминах колониеобразующих единиц (КОЕ), введенных одному животному в день. Ежедневная доза пробиотических организмов может варьировать от приблизительно 105 до приблизительно 10 КОЕ/день. Более предпочтительно, ежедневная доза пробиотических организмов равна от приблизительно 107 до приблизительно 109 КОЕ/день. Более предпочтительно, ежедневная доза пробиотических организмов равна от приблизительно 108 до приблизительно 109 КОЕ/день. Наиболее предпочтительно, ежедневная доза пробиотических организмов равна приблизительно 10 КОЕ/день.
В соответствии со способами изобретения введение композиции, включающей один или более пробиотических организмов, включая введение как часть режима питания, может продолжаться от времени беременности и на протяжении всей жизни животного.
Следующие примеры обеспечивают более подробное описание изобретения. Они предназначены для того, чтобы проиллюстрировать, а не ограничить изобретение.
Пример 1
Животные и экспериментальные параметры
Популяция кошек, на которых проводилось исследование. Двадцать шестинедельных котят SPF приобрели в Liberty Laboratories (Liberty, NY). С помощью метода ELISA показали, что котята были серонегативными по отношению к антигену вируса лейкемии кошек и антителам вируса иммунодефицита кошек (Snap Combo, IDEXX Laboratories, Portland, ME).
План эксперимента. После 10-дневного периода адаптации котят случайным образом распределяли на две группы по десять котят в каждой и на 7-й недели жизни начинали исследования по влиянию обработки. В индивидуальные 50 мл полипропиленовые центрифужные пробирки с коническим дном добавляли от 0,25 до 0,28 г (~5×109 КОЕ на основании опытов по разведению) LBC ME5 PET E. faecium SF68 (NCIMB 10415) (Cerbios-Pharma SA, Switzerland), закрывали крышками и хранили при 4°С на протяжении исследования. Такие же препараты применяли для аликвот усилителя вкусовой привлекательности (типичное покрытие корма для домашних животных, включающее печеночный гидролизат в качестве основного примененного компонента) по 150 мг на пробирку. Аликвоты контролировали на поглощение воды и отбраковывали, если в них обнаруживали какое-либо образование комочков как пробиотиков, так и усилителя вкусовой привлекательности. Непосредственно перед введением одну аликвоту усилителя вкусовой привлекательности переносили в одну из хранившихся пробирок с E. faecium SF68 (Группа обработки) или в пустую пробирку (Группа плацебо) и разводили, применяя водопроводную воду комнатной температуры, до общего объема, равного 10 мл. Содержимое перемешивали на Вортексе по меньшей мере в течение трех минут и насасывали в шприц объемов 12 см3. Немедленно после перемешивания суспензии соответствующим котятам вводили перорально по 1 мл или E. faecium SF68 (общая суточная доза 5×108 КОЕ в день) или только усилитель вкусовой привлекательности (котята группы плацебо) до 27 недели жизни. Обе группы кормили сухим кормом для котят ad libitum (типичная смесь для роста котят, отвечающая всем требованиям AAFCO и основанная на цыпленке и рисе в качестве основных примененных ингредиентов), группы жили в отдельных комнатах для предотвращения перекрестного загрязнения пробиотиками. На 9-й и 12-й неделях жизни всех котят вакцинировали подкожно модифицированной живой комбинированной вакциной (Pfizer Animal Health, Exton, PA) против герпесвируса-1 кошек, кальцивируса и вируса панлейкопении в соответствии с рекомендациями Американской ассоциации ветеринаров-фелинологов (American Association of Feline Practitioners) (Richards J et al. (2001)).
Статистический анализ. Для образцов в каждой временной точке рассчитывали средние величины для группы для каждого измеренного параметра. Разницу между группой, обработанной пробиотиками, и группой, получавшей плацебо, анализировали, применяя комбинированную модель ANOVA, подходящую для эксперимента с повторными измерениями. Время было включено в модель в качестве непрерывной переменной. Процент кошачьих образцов, положительных в отношении энтеротоксина С.perfringens или токсинов А или В С.difficile, и процент клеток, позитивных в отношении маркеров клеточной культуры, рассчитывали для каждой группы кошек на протяжении всего времени исследования и сравнивали с помощью двустороннего критерия Стьюдента (GRAPHPAD Prism, GRAPHPAD Software, Inc., San Diego, CA). Статистическую достоверность считали равной р<0,05.
Пример 2
Сбор образцов и клиническое наблюдение
Состояние и поведение котят контролировали ежедневно на протяжении исследования. Массу тела измеряли еженедельно. Кровь, слюну и кал собирали от всех кошек перед началом добавления пробиотиков или усилителя вкусовой привлекательности на 7-й неделе жизни и на 9-й, 15-й, 21-й и 27-й неделях жизни. Дополнительно собирали кал от котят группы обработки на 28-й неделе жизни. Для каждой группы котят 5 образцов кала в день случайным образом собирали из общего лотка и подсчитывали очки, применяя стандартизированную графическую карту бальных оценок, и ежедневно определяли среднее для группы. Экстракты кала для измерения общих IgA и общих IgG получали согласно протоколу, описанному Benyacoub J et al. (2003). Все образцы перед исследованием хранили партиями при -80°С.
Стул у всех котят был нормальным в начале периода получения добавок (7-я неделя жизни). Один котенок из каждой группы был удален из исследования по причинам, не связанным с исследованием, и, следовательно, эти котята были удалены из окончательного анализа данных. Масса тела и оценка консистенции кала в баллах статистически не различались между двумя группами во времени или в любой индивидуальной временной точке (Фигура 1).
Полная формула крови, биохимические параметры и массы тела были одинаковыми между группами кошек на протяжении всего курса исследования. Оценки консистенции кала в баллах были одинаковыми между группами, что хорошо подтверждает тот факт, что применение SF68 в дозах, описанных в этом документе, не индуцирует заметных клинических отклонений.
Пример 3
Анализ кала
Для образцов в каждой временной точке кал от каждого котенка помещали в восьми серийных 10-кратных разведениях на агар KF Streptococcus и инкубировали аэробно в течение 48 часов при 37°C. Десять колоний каждого морфологического типа забирали с помощью стерильных петель, помещали в 1,2 мл питательной среды для инфузии мозга и сердца (BHI) (Becton Dickinson, Franklin Lakes, NJ) и хранили при -80°С до проведения анализа. RAPD-PCR проводили на бактериальных изолятах из каждого образца для определения, есть ли в стуле обработанных кошек жизнеспособные Е. faecium SF68 и для определения того, не были ли пробиотики случайно перенесены от обработанных котят к контрольным котятам. Параметры термоцикла были следующими: 30 циклов денатурации по одной минуте при 95°С, отжиг в течение одной минуты при 40°С, удлинение в течение 4-х минут при 72°С. 25,5 мкл реакционной среды, включавшей 2,45 мкл 10х свободного от магния буфера (100 мМ Tris-HCl, pH 8,3, 500 мМ KCl), 3,22 мМ MgCl2, 0,4 мкл (1 Ед) JumpStart Taq ДНК полимеразы (Sigma D-4184, Sigma-Aldrich, Inc., St. Louis, МО), 1,9 мкл смеси dNTP (2,5 мМ), 1 мкл праймера (100 µM), 15,47 мкл воды PCR и 1 мкл бактериальной культуры. Последовательность примененного праймера была следующей 5'-GGTTGGGTGAGAATTGCACG-3'. От пяти до десяти мкл продукта PCR разгоняли на двухпроцентном агарозном геле и полученные полосы сравнивали с позитивным контролем SF68. Для определения наличия эндотоксинов Clostridium perfringens или токсинов А/В С.difficile в кале всех котят применяли коммерческие тесты ELISA: для С.perfringens ELISA, набор No. 92-000-22 и для С.difficile ELISA, набор No. 94-0150-КТ (Techlabs, Blacksburg, VA.) Определение обычных для кала аэробных культур Salmonella spp. и Campylobacter spp. проводили в Лаборатории диагностики Колорадского Университета (Colorado State University Diagnostic Laboratory).
Кал семи из девяти обработанных кошек был положительным в отношении SF68, по меньшей мере, в одной временной точке во время исследования. Тем не менее, через 1 неделю после прекращения добавления (неделя 28) ДНК SF68 не была амплифицирована из кала ни у одной из обработанных кошек. Из кала не были выращены ни Salmonella spp., ни Campylobacter spp. Все образцы от кошек Группы плацебо были отрицательными по отношению к SF68, что было показано методом RAPD PCR. Число позитивных образцов для токсинов А/В С.difficile или эндотоксинов Clostridium perfringens (Table 1) не различалось между группами на протяжении курса исследования.
Добавление SF68 не индуцировало выделения в окружающую среду Salmonella spp. и Campylobacter spp. Некоторые образцы кала в обеих группах котят были положительными по отношению к токсинам С.difficile или С.perfringens; тем не менее, не было значительной разницы в числе положительных образцов между группами и положительные результаты не коррелировали с диареей. SF68 обнаруживали в кале большинства кошек на протяжении периода добавления, но его больше не обнаруживали в кале через 1 неделю после прекращения добавления, что указывает на то, что этот организм сохраняется в кошках только временно. Таким образом, введение SF68, применяя дозы, описанные в этом документе, не оказывает вредных воздействий и безопасен для введения на протяжении исследованного времени.
Пример 4
Иммунологические анализы
Полные подсчеты форменных элементов крови, полные биохимические исследования сыворотки и анализ мочи проводили в Лаборатории клинической патологии в Государственном Университете Колорадо (Colorado State University). Антиген-специфические гуморальные иммунные ответы определяли путем измерения сывороточных FHV-1-специфических IgG, FHV-1-специфических IgA, FCV-специфических IgG и специфических для кошачьей панлейкопении IgG10 в сыворотках, а также уровни FHV-1-специфических IgG и IgA в слюне, применяя адаптации ранее опубликованных анализов ELISA (Lappin MR et al. (2002) и Ditmer DA et al. (1998)). Для FHV-1-специфических IgG и IgA результаты рассчитывали как с помощью средней величины абсорбции для повторенных трижды тестируемых лунок для каждого образца и с помощью подсчета процента единиц ELISA (среднее поглощение тестируемого образца минус среднее поглощение образца негативного контроля/среднее поглощение образца позитивного контроля минус среднее поглощение образца негативного контроля, умноженного на 100). Для FCV и FPV применяли среднее поглощение. Общие концентрации IgG и IgA в сыворотках, экстрактах кала и слюне определяли с помощью коммерческих анализов ELISA или радиальным иммунодиффузионным анализом (Bethyl Laboratories, Inc., Montgomery, TX).
Клеточные иммунные ответы анализировали с помощью проточной цитометрии и анализа пролиферации цельной крови. Анализ проводили с помощью проточной цитометрии в течение 12 часов после отбора крови, применяя 500 мкл крови с антикоагулянтом (ЭДТА), инкубировали при комнатной температуре в буфере лизиса эритроцитов (0,155 М NH4Cl/0,010 М КНСО3/5×10-4 % феноловый красный (0,5%). Клетки промывали два раза PBS, полученные осадки клеток ресуспендировали в буфере FACS, содержащем PBS, 0,1% азид натрия и 2% фетальную бычью сыворотку, по возможности до концентрации 1×106 клеток/100 мкл. Образцы с неудовлетворительными клетками по меньшей мере для 500 мкл описанной выше суспензии подсчитывали и записывали концентрацию клеток. Сто мкл каждой клеточной суспензии добавляли в индивидуальные лунки в 96-ти луночный планшет с круглодонными лунками для иммуноокрашивания. Неспецифическое связывание блокировали добавлением 10%-ной нормальной кошачьей сыворотки (Jackson ImmunoResearch Laboratories, Inc., West Grove, PA). Иммуноокрашивание проводили при 4°С в темноте в буфере FACS. Лимфоциты прокрашивали на экспрессию CD4 и CD8 (vpg34; fitc-меченные антитела к CD4, vpg9; анти-CD8-rpe антитела; Serotec, Raleigh, NC (Oxford, UK.)) и экспрессию CD44 (IM7; анти-CD44-pe/cy5 антитело; Pharmingen, Franklin Lakes, NJ). Для анализа В-клеток лизированная цельная кровь была подвергнута иммуноокрашиванию с перекрестно-реагирующими антителами к В220 (ra3-b62; анти-В220-биотинилированным антителом; eBioscience, San Diego, CA), CD21(b-ly4; анти-С021-арс антитело; BD-Biosciences, Franklin Lakes, NJ) и МНС класс II (fitc-меченное антитело к МНС класса II; клон CAG5-3D1, Serotec, Raleigh, NC (Oxford, UK)). Клетки для анализа выбирали из популяций живых лимфоцитов, основываясь на параметрах прямого и углового светорассеяния. Данные накапливали с помощью цитометра Cyan MLE и анализировали с помощью программы Summit (Dako-Cytomation, Fort Collins, CO).
Анализы пролиферации проводили трижды, применяя по 10 мкл цельной гепаринизированной крови, предварительно подготовленной с помощью инкубирования в 100 мкл полной опухолевой среды при 37°С с 5% CO2 в течение 30 минут перед добавлением митогена или антигена (Полная опухолевая среда: модифицированная среда Игла, дополненнная незаменимыми и заменимыми аминокислотами +10% FBS). Клетки поддерживали в среде без добавок (нестимулированные) или стимулировали конкавалином А (10 мкг/мл: Con A Sigma-Aldrich, St. Louis, МО) или препаратом антигена FHV-1 (1 мкл/лунку, полученным перед началом исследования и хранившимся разделенным по аликвотам при -80°С) в течение 96 часов при 37°С с 5% CO2 (Veir JK et al. (2005)). К клеткам пульсом добавляли меченный тритием тимидин (1 мкКи на лунку) и 18 часов спустя клетки собирали на стекловолоконные фильтры-подложки (Wallac-Microbeta Perkin-Elmer, Boston, MA). Подложки считывали, применяя жидкостной сцинтилляционный счетчик MicroBetas. Средний индекс стимуляции (средний максимальный счет на стимулированный образец, деленный на средний максимальный счет на нестимулированный образец) рассчитывали для всех образцов.
Полные подсчеты форменных элементов крови и биохимические анализы были в границах нормы для всех кошек всех возрастов во всех временных точках. Не было статистической разницы между группами на протяжении всего времени или в каждой отдельной временной точке между проанализированными пробами. На 21-й и 27-й неделях жизни средние уровни FHV-1-специфических IgA в сыворотке и слюне были численно выше в Группе обработки, при сравнении с Группой плацебо, но эти различия не были статистическими различиями (Фигура 2). На 15-й, 21-й и 27-й неделях жизни средние уровни FHV-1-специфических IgG сыворотки были численно выше в Группе обработки при сравнении с помощью обоих анализов с Группой плацебо, но эти различия не были статистически значимыми различиями (Фигура 3). FHV-1-специфические IgG не были обнаружены в слюне. Уровни FCV-специфических IgG в сыворотке были одинаковыми для двух групп (Фигура 4). На 15-й неделе жизни средние уровни FPV-специфических IgG сыворотки Группы обработки были численно выше, чем в Группе плацебо, но эти различия не были статистически значимыми различиями (Фигура 5).
Концентрации общих IgG и IgA в сыворотке были одинаковыми для двух групп (данные не приведены). Общие IgG не были обнаружены в слюне и концентрации общих IgA в слюне были одинаковыми для двух групп (данные не приведены). На 27-й неделе жизни средние концентрации общих IgG в экстрактах кала Группы обработки были численно выше, чем в Группе плацебо, но эти различия не были статистически значимыми различиями (Фигура 6). Концентрации общих IgA в экстрактах кала были одинаковыми для двух групп (Фигура 6).
Анализы пролиферации, проведенные с применением как 10 мкг/мл конковалина А или 1 мкл препарата антигена FHV-1 в качестве стимулятора, не дали значительно различающихся средних максимальных счетов между группами в любой временной точке. Не было статистических различий между группами для какого-либо клеточного маркера в первых четырех временных точках (Фигура 7). На 27-й неделе жизни Группа обработки имела значительно более высокий процент лимфоцитов (среднее 13,87%), положительных в отношении CD4, чем Группа плацебо (среднее 10,61%, р=0,0220). Никакие другие сравнения не дали значительных различий.
Увеличение на 27-й неделе жизни количества CD4+в Группе обработки по сравнению с Группой плацебо без одновременного увеличения количества CD8+ показывает системные модулирующие иммунитет эффекты пробиотиков. Обнаружение численно более высоких параметров гуморального иммунного ответа для некоторых времен сбора данных предполагает, что имеет место стимуляция ответов The. Эта гипотеза подтверждается наблюдениями, сделанными в исследовании по добавлению SF68 щенкам (Benyacoub J et al. (2003)).
После вакцинации у каждого котенка развились ответы FHV-1-, FCV- и FPV-специфических антител в сыворотке, похожие на ответы, полученные в других исследованиях, что указывает на то, что они были иммунокомпетентными и что примененная модифицированная живая вакцина была жизнеспособна (Lappin MR et al. (2002)). Некоторые из результатов также указывают на то, что кормление пробиотиками влияет на гуморальные и опосредуемые клетками иммунные ответы этих котят. Эти результаты включают обнаружение статистически значительно более высоких количеств лимфоцитов CD4+ на 27-й неделе жизни и численно более высоких средних величин для FHV-1-специфических IgA в сыворотке и слюне на 21-й и 27-й неделях жизни для уровней FHV-1-специфических IgG в сыворотке на 15-й, 21-й и 27-й неделях жизни, для уровней FPV-специфических IgG в сыворотке на 15-й неделях жизни и для концентраций общих IgG в экстрактах кала на 27-й неделях жизни по сравнению с Группой плацебо.
Настоящее изобретение не ограничено воплощениями, описанными и приведенными в качестве примеров выше, но возможны изменение и модификация в рамках прилагаемой формулы изобретения.
Список цитируемой литературы
Benyacoub J, Czamecki-Maulden GL, Cavadini С, Sauthier Т, Anderson RE, Schiffrin EJ, von der WT (2003), Supplementation of food with Enterococcus faecium (SF68) stimulates immune functions in young dogs. J. Nutr.133:1158-1162.
Dinner DA, Lappin MR, Carman J, Collins JK (1998), Enzyme-linked immunosorbent assay for detection of feline herpesvirus I IgG in the serum, aqueous humor and cerebrospinal fluid. J. Vet. Diagn. Invest. 10:315-319.
Drisko JA, Giles CK, Bischoff BJ (2003), Probiotics in health maintenance and disease prevention. Altern. Med. Rev. 8:143-155.
Isolauri E, Sutas Y, Kankaanpaa P, Arvilommi H, Salminen S (2001a), Probiotics: effects on immunity. Am. J Clin. Nutr. 73: 444S.
Isolauri E (2001b), Probiotics in human disease. Am. J. Clin. Nutr. 73: 11425-11465.
Kim LM, Morley PS, Traub-Dargatz JL, Salman MD, Gentry-Weeks С (2001), Factors associated with Salmonella shedding among equine colic patients at a veterinary teaching hospital. J. Am. Vet. Med. Assoc. 218: 740-748.
Lappin MR, Andrews J, Simpson D (2002), Use of serologic tests to predict resistance to feline herpesvirus 1, feline calicivirus and feline parvovirus infection in cats. J. Am. Vet. Med. Assoc. 220:38-42.
Macpherson AJ, Uhr Т (2004), Induction of protective IgA by intestinal dendritic cells carrying commensal bacteria. Science 303: 1662-1665.
Oyetayo VO and Oyetayo FL (2004), Potential of probiotics as biotherapeutic agents targeting the innate immune system. Afr. J. Biotechnol. 4:123-127.
Reid G, Jass J, Sebulsky MT, McCormick JK (2003), Potential uses of probiotics in clinical practice. Clin. Microbiol. Rev. 16:658-672.
Richards J, Rodan I, Elston T, Flemmin D, Ford R, Henry S, Hustead D, Lappin MR, Paul M, Rosen D, Scherk M, Scott F, Welbom L (2001). Feline Vaccine Selection and Administration, Compend. Cont. Ed. Pract. Vet. 23: 71-80.
Sanders ME (2003), Probiotics: considerations for human health Nutr. Rev. 61: 91-99.
Schrezenmeir J, de Vrese M (2001), Probiotics, prebiotics and synbiotics-approaching a definition. Am. J. Clin. Nutr. 73:361S.
Scott FW, Geissinger CM (1999), Long-term immunity in cats vaccinated with an inactivated trivalent vaccine. Am. J. Vet. Res. 60: 652-8.
Slater E, York С (1976), Comparative studies on parenteral and intranasal inoculation of an attenuated feline herpes virus. Dev. Biol. Stand. 33: 410-6.
Sykes JE, Anderson GA, Studdert VP, Browning GF (1999), Prevalence of feline Chlamydia psittaci and feline herpesvirus 1 in cats with upper respiratory tract disease. J. Vet. Intern. Med. 13:153-162.
Van Pelt DR, Lappin MR (1994), Pathogenesis and treatment of feline rhinitis. [Review] [48 refs]. Veterinary Clinics of North America - Small Animal Practice. 24: 807-823.
Veir JK, Lappin MR, Radecke S. Whole blood proliferation assay to assess cell mediated immune responses to FHV-1. J. Vet. Diagn. Invest. 2005 (In Press).
Изобретение относится к кормлению животных. Применение пробиотического штамма бактерий Enterococcus faecium SF68 в производстве лекарственного средства для модулирования иммунитета у животного из семейства кошачьих против FVH-1, FCV или FPV и для усиления эффективности вакцины FVH-1, FCV или FPV у животного из семейства кошачьих. Способ усиления эффективности вакцины FVH-1, FCV или FPV у животного из семейства кошачьих, предусматривающий регулярное скармливание животному композиции, содержащей пробиотические бактерии Enterococcus faecium SF68 в количестве, по меньшей мере, приблизительно от 102 до приблизительно 1011 КОЕ в день. Изобретение позволяет повысить эффективность вакцинации. 2 н. и 12 з.п. ф-лы, 7 ил.
1. Применение пробиотического штамма бактерий Enterococcus faecium SF68 в производстве лекарственного средства для модулирования иммунитета у животного из семейства кошачьих против FVH-1, FCV или FPV и для усиления эффективности вакцины FVH-1, FCV или FPV у животного из семейства кошачьих.
2. Применение по п.1, в котором лекарственное средство представляет собой кормовую композицию для животных или диетическую добавку к рациону животных.
3. Применение по п.1 или 2, в котором пробиотик Enterococcus faecium SF68 присутствуют в количестве, по меньшей мере, приблизительно от 102 до приблизительно 1011 КОЕ на грамм композиции.
4. Применение по п.1 или 2, где дополнительно включают 7-okco-DHEA.
5. Применение по п.1 или 2, где дополнительно включают по меньшей мере один из пробиотических организмов другого типа.
6. Применение по п.1 или 2, где животное из семейства кошачьих представляет собой домашнюю кошку.
7. Применение по п.1 или 2, в котором усиление эффективности вакцины у животного приводит к усиленному образованию лимфоцитов CD4+ у животного.
8. Применение по п.1 или 2, в котором усиление эффективности вакцины у животного приводит к увеличению концентрации иммуноглобулинов, активных в отношении антигенов специфических патогенов в сыворотке крови, кале, молоке, слюне, слезах, в респираторном эпителии или желудочно-кишечном эпителии животного.
9. Способ усиления эффективности вакцины FVH-1, FCV или FPV у животного из семейства кошачьих, предусматривающий регулярное скармливание животному композиции, содержащей пробиотические бактерии Enterococcus faecium SF68 в количестве, по меньшей мере, приблизительно от 102 до приблизительно 1011 КОЕ в день.
10. Способ по п.9, в котором композиция представляет собой кормовую композицию для животных или диетическую добавку к рациону животных.
11. Способ по п.9 или 10, в котором пробиотические бактерии Enterococcus faecium SF68 предпочтительно скармливают животному в количестве 108 КОЕ в день.
12. Способ по п.9 или 10, в котором животное из семейства кошачьих представляет собой домашнюю кошку.
13. Способ по п.9 или 10, в котором усиление эффективности вакцины у животного приводит к усиленному образованию лимфоцитов CD4+ у животного.
14. Способ по п.9 или 10, в котором усиление эффективности вакцины у животного приводит к увеличению концентрации иммуноглобулинов, активных в отношении антигенов специфических патогенов в сыворотке крови, кале, молоке, слюне, слезах, в респираторном эпителии или желудочно-кишечном эпителии животного.
| 0 |
|
SU190311A1 | |
| US 5968569 A, 19.10.1999 | |||
| WO 9800035 A1, 08.01.1998. | |||
Авторы
Даты
2011-02-10—Публикация
2006-10-06—Подача