Изобретение относится к пищевой композиции для регулирования ответной реакции на гликемию после еды у домашних животных, таких как собака и кошка.
Несколько различных состояний ассоциируется с ухудшенным метаболизмом глюкозы у домашних животных, таких как собака и кошка. Эти состояния включают диабеты (инсулино-зависимого типа и инсулино-независимого типа, связанного с наступлением зрелого возраста), тучность, гериатрию и беременность I (беременность II). Установлено, что одна из каждых 100 собак, обследуемых ветеринаром, страдает диабетом. Установлено, что тучность наблюдается у 40% популяции собак. Конечно, то, что домашние животные, которые являются более старыми (полагают, что приблизительно 10% популяций собак и кошек в США находятся в возрасте 11 лет или старше), и беременные животные являются обычным явлением. Таким образом, существует значительный процент популяции собак и кошек, которые находятся в категориях, связанных с риском уже иметь проблемы или иметь развитие проблем, связанных с метаболизмом глюкозы и/или инсулина.
Кроме того, диагноз диабетов или ухудшенный метаболизм глюкозы у собак и кошек обычно имеет место только после эпизода гипергликемии у животного. Таким образом, животные, которые имеют диабеты в пограничном состоянии, или другими словами, имеют умеренные ухудшенные метаболизмы глюкозы, приобретают значительный риск быть не диагностироваными, с точки зрения диабетов, до тех пор, пока их состояние не прогрессирует и безошибочные симптомы проявятся сами по себе.
Поглощение пищи приводит к ответной реакции выделения глюкозы после еды. Эта ответная реакция характеризуется всплеском глюкозы в крови. Инсулин является первичным гормоном тела, который используется для сохранения глюкозы в крови. Таким образом, уровни инсулина в крови, так же как и глюкозы, обычно поднимаются после приема пищи. Относительно низкая ответная реакция выделения инсулина на прием пищи косвенно указывает на то, что поглощение глюкозы после еды было минимальным. Таким образом, способ предотвращения этого "всплеска" в уровнях глюкозы и инсулина после приема пищи будет преимущественно связан с животным с ухудшенным метаболизмом глюкозы.
Другим метаболическим нарушением, связанным с тучностью и диабетами, является гиперинсулинемия. Гиперинсулинемия представляет собой присутствие инсулина в крови при аномально высоких уровнях. Противодействие воздействиям гиперинсулинемии путем снижения уровней инсулина в крови может помочь снизить развитие тучности и диабетов.
В прошлом предпринимались попытки контроля диабетов не только с помощью лекарственной терапии, но также и с помощью диеты. Было обнаружено, что диетическая клетчатка оказывает влияние на контролирование диабетов при определенных обстоятельствах. Было обнаружено, что добавление определенных растворимых волокон, таких как гуар и пектин, в меньшей степени приводит к повышению уровней глюкозы в крови, происходящему после еды. Однако не все растворимые волокна оказывают благотворное влияние, а некоторые приводят к нежелательным побочным эффектам для животных, включая диарею, метеоризм и абдоминальный спазм.
Примеры известных композиций, направленные на специальные диеты, включают ЕР 205354, который раскрывает диетический бисквит для собаки, содержащий овощную кожуру. CN 1135850 раскрывает текущую композицию, включающую жидкую кашу, которая снижает заболеваемость такими заболеваниями, как диабеты, которую готовят из кукурузы, зерен сорго, бобов и риса.
M.Diez et.al., "Fibres alimentaires chez le chien: I. Definition et composition chimique" Ann. Med. Vet., vol. 140, N 6, 1966, pp. 385-391, раскрывает введение диетической клетчатки в пищу для домашних животных.
G. S. Mahdi et.al., "Терапевтическое значение ячменя при лечении диабетических меллитусов (mellitus)". Proceedings of the Nutrition Society, vol. 47, 3, 1988, раскрывает использование ячменной муки в диетах для устранения диабетических меллитусов.
Было бы желательным иметь возможность регулировать и улучшать метаболизм глюкозы и/или инсулина у животных, обладающих ухудшенным метаболизмом глюкозы и/или инсулина. Было бы также желательным иметь возможность регулировать и улучшать метаболизм глюкозы и/или инсулина даже у животных, которые кажутся здоровыми с отсутствием симптомов, для предотвращения наступления хронического диабетического состояния. Таким образом, еще остается необходимость в сфере регулирования и улучшения метаболизма глюкозы и/или инсулина у животных, сопутствующих человеку, хотя диета предотвращает или занимает промежуточное положение при начале ухудшенной функции глюкозы и/или инсулина у домашних животных с тучностью, гериатрией или диабетом.
В основу изобретения положена задача создания пищевой композиции для домашних животных для контролирования у этих животных ответных реакций на наличие глюкозы и инсулина в крови, происходящих после еды, что дает возможность регулировать и улучшать метаболизм глюкозы и/или инсулина у животных и предотвращать наступление хронического диабетического состояния.
Задача решена тем, что заявляемая пищевая композиция для домашних животных для регулирования ответной реакции на гликемию после еды у этих животных, включающая источник белка, источник жира и источник углеводов, согласно изобретению, содержит в качестве источника углеводов составной зерновой источник, включающий два или три источника зерна, которые выбирают из группы, состоящей из сорго, ячменя и кукурузы; в котором весовое отношение двух источников зерна составляет от 1:5 до 5:1, а отношение трех источников зерна составляет от 1:1:5 или 1:5:1 до 5:1:1.
Предпочтительным вариантом пищевой композиции для домашних животных является композиция, в которой отношение двух источников зерна составляет 1:1.
Пищевая композиция для домашних животных может дополнительно содержать трипиколинат хрома, а также водорастворимый эфир целлюлозы.
Предпочтительным вариантом заявляемой композиции является пищевая композиция для домашних животных, которая дополнительно содержит от 1 до 11 мас.% дополнительной общей диетической клетчатки ферментируемых волокон, которые содержат органическое вещество, исчезающее на 15-60 мас.% при ферментации фекальными бактериями в течение 24-часового периода.
Наиболее предпочтительной является пищевая композиция для домашних животных, в которой источник белка составляет от 20 до 40 мас.%, указанный источник жира составляет от 4 до 30 мас.% и указанная общая диетическая клетчатка составляет от 4 до 20 мас.%.
Другим предпочтительным вариантом пищевой композиции для домашних животных является композиция, в которой указанный составной зерновой источник содержит смесь сорго и ячменя, более предпочтительным отношение сорго к ячменю от 1:3 до 3:1, самым предпочтительным, отношение сорго к ячменю 1:1.
Другими предпочтительными вариантами пищевой композиции для домашних животных также являются композиции, в которых указанный составной зерновой источник включает смесь кукурузы и ячменя или смесь кукурузы и сорго, или смесь сорго, кукурузы и ячменя.
Когда композицию настоящего изобретения скармливают животным, сопутствующим человеку, у животных контролируют происходящую после еды ответную реакцию на наличие глюкозы в крови. Пищевая композиция для комнатных животных состоит, по существу, из источника белка, источника жира и источника углеводов из составного зернового источника, включающего смесь сорго и ячменя; смесь кукурузы и ячменя; смесь кукурузы и сорго; или смесь кукурузы, сорго и ячменя. Пищевая композиция настоящего изобретения является также полезной для контроля гиперинсулинемии у животных, сопутствующих человеку.
Таким образом, особенностью настоящего изобретения является обеспечение композиции для улучшения метаболизма глюкозы и/или инсулина у животных, сопутствующих человеку, за счет контролирования у этих животных ответной реакции на наличие глюкозы в крови и/или инсулина, происходящей после еды.
Эта и другие особенности и преимущества настоящего изобретения станут очевидными из следующего детального описания изобретения с сопровождающими чертежами, на которых:
фиг. 1 иллюстрирует графически влияние различных источников крахмала на уровни глюкозы у собаки в выбранные моменты времени после поглощения пищи;
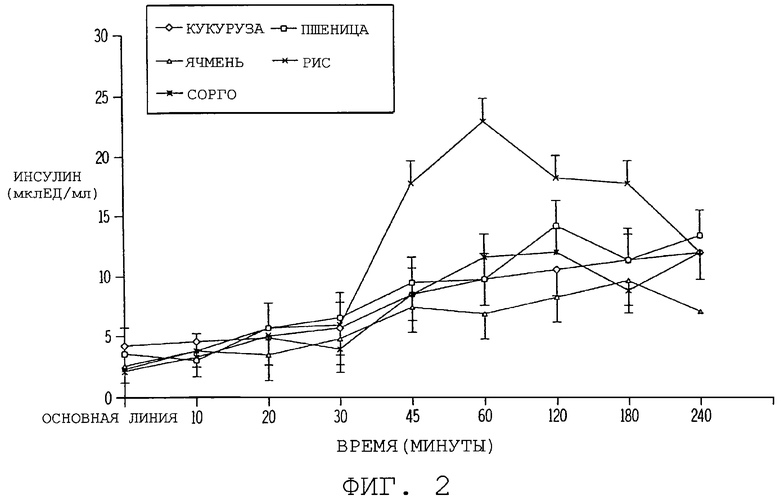
фиг. 2 иллюстрирует графически влияние различных источников крахмала на уровни инсулина у собаки в выбранные моменты времени после поглощения пищи;
фиг. 3 иллюстрирует графически влияние диеты настоящего изобретения на уровни глюкозы (мг/дл) в выбранные времени (минуты) после потребления диетической пищи у кошек и
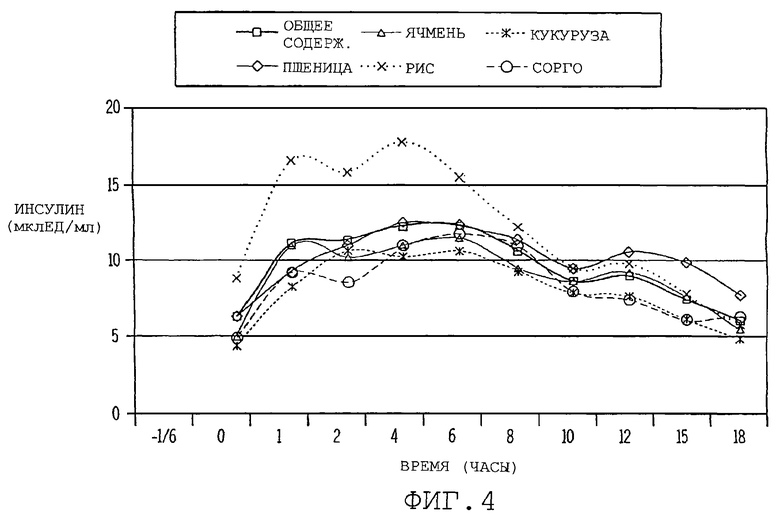
фиг. 4 иллюстрирует графически влияние диеты настоящего изобретения на уровни инсулина (мклЕД/дл) (μ1U/dl) в выбранные моменты времени (минуты) после потребления диетической пищи у кошек.
Настоящее изобретение использует пищевую композицию для комнатных животных, которая содержит составной зерновой источник, который включает смесь сорго и ячменя; смесь кукурузы и сорго; смесь кукурузы и ячменя; или смесь кукурузы сорго и ячменя в качестве источников крахмала для контроля увеличения уровней и глюкозы и инсулина у домашних животных, происходящего после еды. Использование дополнительных источников зерна в настоящем изобретении является оптимальным. Термин "составной зерновой источник", как он использован здесь, означает, по меньшей мере, два различных источника зерна. Благодаря использованию составного зернового источника, диета животных эффективным образом способствует регулированию метаболизма глюкозы у животных и ответной инсулиновой реакции после принятия пищи.
Композиция также, необязательно, содержит другие ингредиенты, которые также обладают эффектом уменьшения ответной реакции на наличие глюкозы в крови и/или инсулина у животных, происходящего после еды. Композиция может включать трипиколинат хрома в количестве от около 10 до около 500 мкг хрома в сутки. Трипиколинат хрома содержится в пивных дрожжах и дрожжи можно добавлять в пищевую композицию для домашних животных. Или же, трипиколинат хрома можно добавлять в композицию, по существу, в чистой форме.
Композиция может также содержать водорастворимый эфир целлюлозы, такой как, например, карбоксиметилцеллюлозу, или простой эфир гидроксипропилметил целлюлозы (НРМС). Если используют карбоксиметилцеллюлозу, она предпочтительно дает высоковязкую композицию в области от около 5000 до около 65000 спуаз (50-650 г/см с) и добавляется в композицию в количестве приблизительно 1 вес. %. Если используют НРМС, он предпочтительно также дает высоковязкую композицию в области от около 10000 до около 2000000 спуаз (100-20000 г/см с) и добавляется в композицию в количестве приблизительно около 1-2 вес.%. Пригодная марка НРМС является доступной от The Dow Chemical Company под торговой маркой METHOCELТМ К-100М. Было найдено, что такие водорастворимые эфиры целлюлозы обладают эффектом замедления увеличения уровней глюкозы в крови животных, происходящего после еды.
Пищевая композиция настоящего изобретения для комнатных животных может также необязательно включать источник ферментируемых волокон, которые демонстрируют исчезновение определенных количеств органического вещества. В ферментируемых волокнах, которые могут использоваться, исчезновение органического вещества (OMD) составляет от около 15 до около 60%, когда они ферментированы фекальными бактериями in vitro в течение 24-часового периода. Таким образом, от около 15 до 60% первоначально присутствующего общего органического вещества ферментируется и превращается фекальными бактериями. Исчезновение органического вещества волокон составляет предпочтительно 20-50%, и более предпочтительно, составляет 30-40%.
Таким образом, in vitro процентное содержание OMD можно рассчитать следующим образом:
{1-[(остаток ОМ-контрольная проба ОМ)/первоначальное ОМ]} х 100,
где остаток ОМ представляет органическое вещество, превратившееся после 24 часов ферментации, контрольная проба ОМ представляет органическое вещество, превратившееся в соответствующих контрольных пробирках (т.е. пробирках, содержащих среду и разбавленные фекалии, но не субстрат), и первоначальное ОМ представляет органическое вещество, помещенное в пробирку для ферментации. Дополнительные детали процедуры находятся в Sunvold et al., J. Anim. Sci. 1995, vol. 73:1099-1109.
Пищевая композиция для домашних животных может быть любой пригодной пищевой композицией для домашних животных, которая также обеспечивает адекватное питание для животных. Например, типичная собачья или кошачья диета для использования в настоящем изобретении может содержать от около 20 до около 40% неочищенного белка (и, предпочтительно, от около 25 до около 35%), от около 4 до около 30% жира (и, предпочтительно, от около 8 до около 12%), и от около 4 до около 20% общей клетчатки, вместе с многочисленными источниками крахмала, все проценты весовые. Однако не требуется конкретного отношения или процентного содержания этих питательных веществ.
Ферментируемые волокна могут быть любым источником волокна, который может ферментироваться кишечными бактериями, присутствующими у животных с продуцированием значительных количеств SCFAs. "Значительные количества" SCFAs для целей настоящего изобретения представляют количества свыше 0,5 ммоль общего количества SCFAs/г субстрата в 24-часовой период. Предпочтительные волокна включают мякоть свеклы, гуммиарабик (включая смолу talha), псиллиум (psyllium), рисовые отруби, смолу бобов рожкового дерева, мякоть цитрусов, пектин, фруктоолигосахариды и инсулин, маннанолигосахариды и смеси этих волокон.
Ферментируемые волокна используют в пищевой композиции для домашних животных в количествах от 1 до 11 вес.% дополнительной общей клетчатки, предпочтительно от 2 до 9 вес.%, более предпочтительно от 3 до 7 вес.%, и наиболее предпочтительно от 4 до 7 вес.%.
Определение "дополнительная общая диетическая клетчатка" сначала требует объяснения термина "общая диетическая клетчатка". "Общая диетическая клетчатка" определяется как остаток пищевых продуктов растительного происхождения, которые оказывают сопротивление процессу гидролиза пищеварительными ферментами животного. Основными компонентами общей диетической клетчатки являются целлюлоза, гемицеллюлоза, пектин, лигнин и смолы (в противоположность "сырой клетчатке", которая содержит только некоторые формы целлюлозы и лигнина). "Дополнительная общая диетическая клетчатка" означает, что клетчатка, которую добавляют в пищевой продукт, представляет большее или меньшее количество любой клетчатки, естественно присутствующей в других компонентах пищевого продукта. Кроме того "источник волокна" считается таковым, когда он преимущественно состоит из волокна.
Для того чтобы можно было более легко понять изобретение, делается ссылка на следующие примеры, которые предназначаются для иллюстрации изобретения, но не ограничивают его объем.
Пример 1
Использовали тридцать взрослых самок Beagles с удаленными яичниками и маткой. В начале исследования средний вес тела собак составлял 9,62 кг±0,78 (SEM-стандартная ошибка значения, область 8,78 до 10,11 кг). В течение всего периода исследования по желанию (ad libitum) обеспечивали свежую воду.
После стабилизационного периода, который продолжался в течение семи недель, собак произвольно разделяли на пять групп с диетическим питанием по шесть собак в каждой группе для первого параллельного эксперимента и они получали одну из пяти экспериментальных диет. Собак повторно произвольно разделяли и приписывали к другой экспериментальной диете для второго параллельного эксперимента. Параллельные эксперименты I и II продолжали минимум в течение двух недель и проверку ответной реакции на наличие глюкозы в крови выполняли по окончании каждого параллельного эксперимента.
Анализы ответной реакции на наличие глюкозы в крови проводили по окончании каждого параллельного эксперимента. Собак заставляли голодать в течение 24 часов до начала анализа на наличие глюкозы в крови. Участок катетеризации обривали, подвергали асептической обработке и проводили катетеризацию правой краниальной вены. Образцы крови собирали в вакуумированные пробирки, содержащие натрий ЭДТА (EDTA) Terumo® Venoject пробирки, 7,0 мл, Terumo Medical Corp., Elkton, MD). Два контрольных образца (два образца для определения нулевой линии) собирали с интервалом приблизительно в пять минут. Непосредственно после отбора последнего из контрольных образцов собак кормили пищей из расчета 1% от веса тела и позволяли есть экспериментальную диету максимум в течение 15 минут. Собак, которые не принимали экспериментальную диету, в течение 15 минут исключали из анализа на наличие глюкозы в крови на этот день и повторно анализировали на следующие сутки. Собирали дополнительные образцы крови через 10, 20, 30, 45, 60, 120, 180 и 240 минут после приема пищи. Образцы крови центрифугировали со скоростью 1300 х g (об/мин) в течение 15 минут и две аликвоты по 1,0 мл плазмы в каждый момент указанного времени замораживали в течение двух часов сбора. Концентрацию глюкозы в плазме (мг/дл) определяли с помощью гексокиназного ферментативного метода (Cobas Mira, Roche Diagnostic System, Somerville, NJ), a инсулин (IU/ml) (1 ЕД/мл) определяли стандартным методом радиоиммуноанализа с использованием RIA набора (DPC Diagnostic Products Corp., Los Angeles, CA).
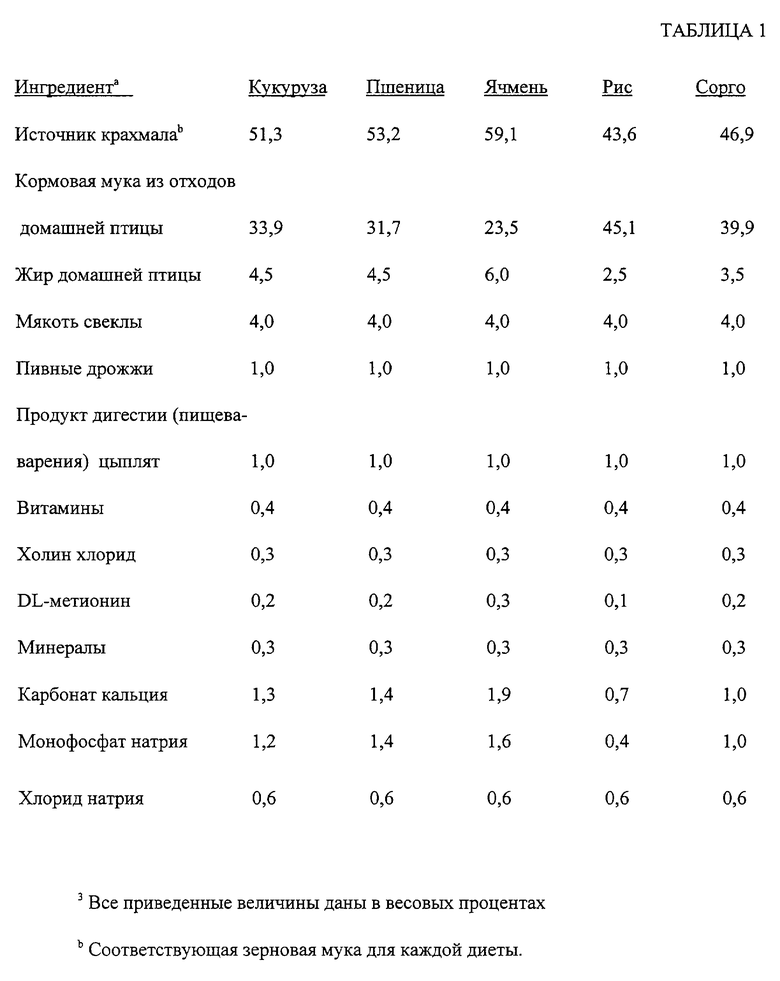
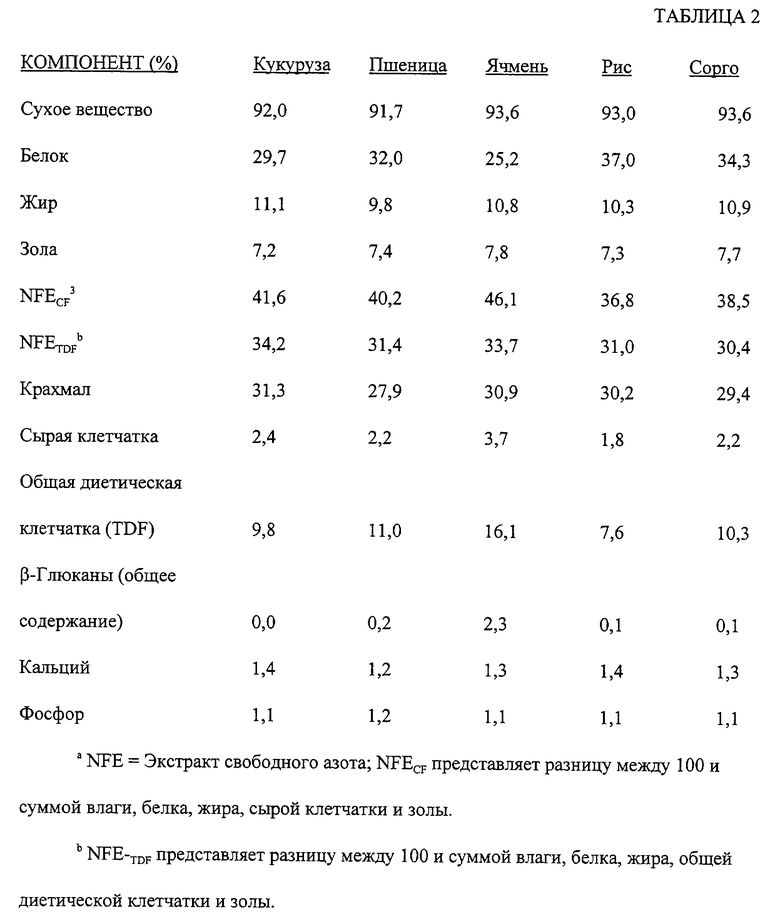
В течение стабилизационного периода собак кормили измельченной поддерживающей диетой (Eukanuba Adult Maintenance, The lams Company, Lewisburg, ОН) в течение семи недель. Ингредиенты композиции экспериментальных диет представлены в табл. 1, а химический состав экспериментальных диет представлен в табл.2. Ежедневное потребление пищи было доведено для индивидуальных собак в течение этого периода до достижения стабильного веса тела. В течение исследуемого периода были оценены пять экспериментальных диет. Все диеты были составлены с равным количеством крахмала (приблизительно 30%) из различных зерновых источников (кукурузы, пшеницы, ячменя, риса и сорго). Для достижения равных количеств крахмала, концентрациям белка позволили значительно изменяться, а концентрациям жира позволяли изменяться незначительно. Экспериментальные диеты подвергали обработке аналогичным образом с каждым из источников крахмала, состоящим из всего зерна без скорлупы. Допущенное индивидуальное ежедневное потребление пищи было основано на потреблении стабилизационного периода.
Ответная реакция появления глюкозы: Было обнаружено значительное различие (Р<0,01) в ответной реакции выделения глюкозы на диету, время и на взаимосвязь диеты и времени. Фиг.1 суммирует уровни глюкозы после еды через различные интервалы времени. На основной линии (базисной линии) уровни глюкозы в плазме были значительно ниже (Р<0,0001) для сорго, по сравнению с пшеницей и рисом. На основной линии не наблюдалось различий (Р>0,01) между кукурузой, пшеницей, ячменем и рисом. Диетические режимы не оказывают влияния на уровни глюкозы через 10, 120, 180 и 240 минут после приема пищи, но наблюдаются значительные различия через 20, 30, 45 и 60 минут. Сорго давало согласованно более низкие уровни глюкозы в плазме, чем другие диеты между 20 и 60 минутами, и постепенно повышавшиеся уровни для оставшихся временных интервалов. Уровни глюкозы в плазме для диеты с сорго не отличались (Р>0,10) от диеты с кукурузой, но были ниже (Р<0,05), чем для диеты с пшеницей и рисом на 20 минуте, и для диеты с пшеницей ячменем и рисом на 30 и 45 минуте, и для диеты с рисом на 60 минуте после приема пищи. Диета с рисом приводила к более высоким (Р<0,05) уровням глюкозы в плазме в моменты времени от 20 до 180 минут, по сравнению с другими диетами.
Средний уровень глюкозы в плазме был ниже (Р<0,05) для сорго, по сравнению с пшеницей и рисом (табл. 3). Рис приводил к более высоким значениям (Р<0,05) уровней глюкозы, чем кукуруза и сорго. Не наблюдалось значительных различий в средних уровнях глюкозы между пшеницей, ячменем и рисом. Пик (максимальное содержание) глюкозы в плазме был значительно выше (Р<0,05) для риса, по сравнению со всеми другими диетами, однако, не существовало значительных различий (Р>0,10) между кукурузой, пшеницей, ячменем и сорго. Источник диетического крахмала не влиял на время появления пика глюкозы. Площадь под кривой (AUC) была выше (Р<0,05) для пшеницы, по сравнению с кукурузой и сорго и не отмечалось различий (Р>0,10) между кукурузой, пшеницей, ячменем и сорго.
Ответная реакция инсулина: Было обнаружено значительное различие (Р<0,01) между диетами и временами (Р<0,0001), но взаимосвязь времени и диеты была незначительной (Р>0,10) в ответной реакции инсулина после еды. Фиг. 2 суммирует уровни инсулина в различные моменты времени. На основной линии уровень инсулина в плазме для диеты с кукурузой был выше (Р<0,05), чем для диеты с ячменем, рисом и сорго, и незначительные различия (Р<0,10) наблюдали между пшеницей, ячменем, рисом и сорго. Диетические режимы не оказывали влияния на ответную реакцию появления инсулина в моменты времени, соответствующие 10, 20, 30, 120, 180 и 240 минутам, однако, рис в диете приводил к более высокому значению (Р<0,05) инсулина в моменты времени, соответствующие 45 и 60 минутам, когда сравнивался с другими диетами. Ячмень в диете давал самый низкий уровень инсулина в моменты времени, соответствующие от 20 минут до 240 минут, хотя различия были незначительными, по сравнению с другими экспериментальными диетами.
Средний уровень инсулина в плазме был выше (Р<0,05) для риса, по сравнению с кукурузой, ячменем и сорго и не наблюдалось различий (Р>0,10) между кукурузой, пшеницей, ячменем и сорго (табл. 4). Пик (максимальное значение) инсулина в плазме был значительно выше (Р<0,05) для риса, по сравнению со всеми другими диетами, и не существовало различий (Р>0,10) между кукурузой, пшеницей, ячменем и сорго. Диетический режим не влиял на время появления пика инсулина. Площадь под кривой была выше (Р<0,05) для риса, по сравнению с кукурузой, ячменем и сорго и не наблюдалось различий (Р>0,10) между пшеницей и рисом, или между кукурузой, пшеницей, ячменем и сорго. Хотя статистически незначительно, ячмень, по существу, приводил к более низкому среднему значению инсулина, пику инсулина и площади под кривой (табл. 4).
Конечная, низкая ответная реакция глюкозы в крови и низкая ответная реакция инсулина для ячменя в пище является полезной для минимизации ответной реакции на появление гликемии на пищу для кошачьих. Кроме того, смеси сорго и ячменя будут оказывать объединенный эффект снижения и глюкозы в крови после еды, и снижения уровней инсулина после приема пищи.
Пример 2
Использовали тридцать взрослых здоровых самок Domestic Short Hair кошек (от Sinclair Research Center, Columbia, МО). Кошек содержали в индивидуальных вольерах согласно стандартам AAALAC (American Association for Accreditation of Laboratory Animal Care). Все процедуры были подвергнуты рассмотрению и одобрены Institutional Animal Care и Use Committee и обращение с кошками было гуманным и этическим в течение всего периода исследования. Животных подвергали вакцинации против вируса ринотрахеита (rhinotracheitis virus), вируса, повреждающего почечную чашку (calicivirus), и вируса панлейкопении (panleukopenia virus). У кошек отсутствовали паразиты. Средний вес тела кошек составлял 3,66 кг±0,99 (SEM (стандартная ошибка значения), область 2,36 до 6,19 кг) при начале исследования. В течение всего периода исследования по желанию (ad libitum) обеспечивали свежую воду.
Рассчитанное количество пищи для поддержания веса тела обеспечивали кошкам ежедневно. Из-за того что кошки быстро не потребляли свою пищу в течение периода стимуляции лейкемии, период предоставления пищи постепенно уменьшали в процессе стабилизационного периода до одного часа ежедневно. Оказалось, что кошки хорошо приспосабливались к ограниченному времени предоставления пищи. Ни одно из животных не болело и не требовало медицинского наблюдения (внимания) в течение периода исследования.
Были оценены пять диет для кормления в трехкратной воспроизводимой перекрестной схеме. После семи недель стабилизационного периода кошек произвольно разделяли в соответствии с весом тела и уровнями глюкозы в сыворотке на пять групп для диетического приема пищи по шесть кошек в каждой группе для первого параллельного эксперимента. Кошек повторно произвольно разделяли и приписывали к различным экспериментальным диетам для второго и третьего параллельного эксперимента. Каждый параллельный эксперимент продолжался минимум три недели и анализ ответной реакции на появление гликемии проводили в конце каждого параллельного эксперимента.
Анализы ответной реакции на появление гликемии проводили в конце каждого параллельного эксперимента. Кошек заставляли голодать в течение 24 часов до начала анализа на появление гликемии. За день до анализа на появление ответной реакции на гликемию, асептически подготовленный участок катетеризации обривали, и шейную вену подвергали катетеризации при легком воздействии седативного средства. Схема лечения седативным средством состояла из внутривенного введения комбинации кетамина (10 мг/фунт; 27 мг/кг) и диазепама (0,5 мг/фунт; 1,3 мг/кг). Образцы крови отбирали шприцом и переносили в вакуумированные пробирки, содержащие антикоагулянт (Terumo® Venoject пробирки (7,0 мл), доступные от Terumo Medical Corporation, Elkton, MD).
Два образца для основной линии собирали приблизительно с интервалом 10 минут.
Тотчас после сбора последнего образца для основной линии, кошек кормили кормом из расчета 1,09% от их веса и позволяли максимум 15 минут есть экспериментальные диеты.
Это потребление пищи (1,09% от веса тела) составляло половину ежедневно потребляемой пищи в течение семинедельного стабилизационного периода. Кошки, не потреблявшие экспериментальную диету, в течение 15 минут исключались из анализа на появление гликемии на этот день и подвергались повторному испытанию на следующий день. Время 0 соответствовало окончанию потребления пищи.
Дополнительные образцы крови собирали в моменты времени, соответствующие 1, 2, 4, 6, 8, 10, 12, 15, 18 часам после потребления пищи. Образцы крови центрифугировали при 1300 об (1300 х g) в течение 15 минут и по две аликвоты сыворотки в каждый из моментов времени замораживали в течение двух часов сбора. Концентрации глюкозы в сыворотке (мг/дл) определяли с помощью гексокиназного ферментативного метода (Cobas Mira, Roche Diagnostic system, Sommerville, NJ), a инсулина (млЕД/мл) определяли с помощью стандартного метода радиоиммунного анализа с использованием RIA набора (DPC Diagnostic Product Corporation, Los Angeles, CA).
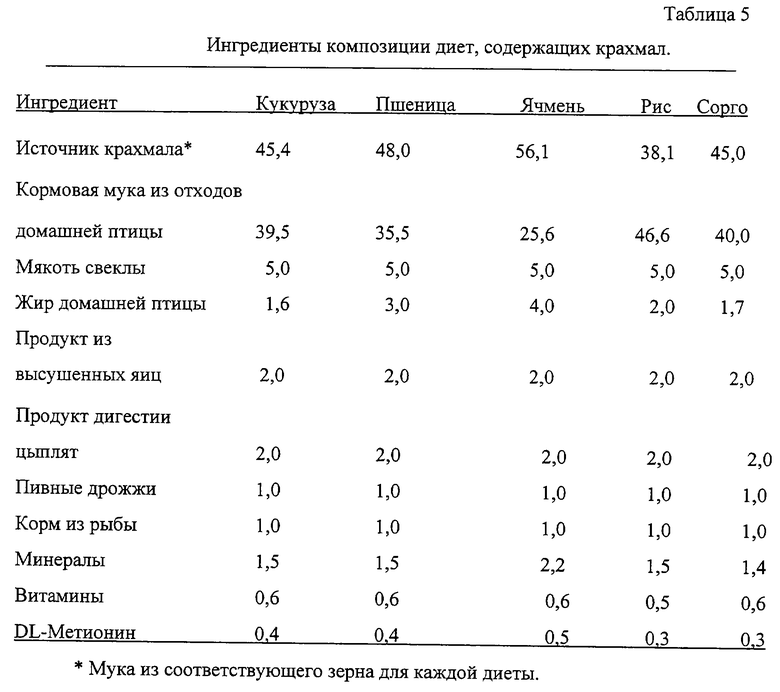
Ингредиенты композиции экспериментальных диет представлены в табл. 5.
В течение периода исследования были оценены пять экспериментальных диет. Все диеты были составлены с одинаковым содержанием крахмала (приблизительно 30%) из различных источников зерна, как представлено выше (кукурузы, пшеницы, ячменя, риса и сорго). Для достижения одинакового содержания крахмала уровням белка позволяли меняться. Экспериментальные диеты подвергали процессу переработки аналогично с каждым источником крахмала, состоящим из всего зерна без кожуры. Разрешенный индивидуальный ежедневный рацион основывался на потреблении пищи в течение стабилизационного периода.
Питательные вещества в диетах анализировали с помощью AOCS-AOAC методов (Association of Official Analytical Chemist-Official Methods of Analysis, Arlington, VA, 1994) (Ассоциация официальной аналитической химии. - Официальные методы анализа, Арлингтон, Вирджиния, 1994). Белок определяли с помощью анализатора горения Leco (AOAC 990.03), жир определяли с помощью кислотного гидролиза (AOAC 990.39), сырую клетчатку определяли с помощью Fibertec (AOAC 973.18), влагу определяли путем высушивания образца при 135oС в течение 2 часов (AOAC 30.15), и общую золу определяли путем сжигания (превращения в пепел) образца при 600oС в течение 4 часов (AOAC 920.39). Экстракт свободного азота (NFE) вычисляли как разницу между 100% и суммой белка, жира, клетчатки, золы и содержания воды. Содержание кальция и фосфора в диетах определяли с помощью атомного абсорбционного спекрофотометра (АОАС 968.08) и ванадий-молибдатным методом (АОАС 965.15), соответственно. Крахмал анализировали количественно (Bondar, R. J. L., and D.C-Mead "Evalution of glucose-6-phosphate dehydrogenase from Leuconostoc mesenteroides in the hexokinase method for detennining glucose in starch" (Оценка дигидрогеназы глюкоза-6-фосфата из мезентероидов лейконостока в методе гексокиназы для определения глюкозы в крахмале), Clin.Chem. 20:586 (1974); MacRae, J.C., and D. C. Annstrong, J. Sci. Food Agric. 19:578 (1968), фракции b-глюкана количественно оценивали ферментативно (АОАС 995.16), а общее содержание диетической клетчатки анализировали с помощью стандартного ферментативно/гравиметрического анализа (АОАС 991.43).
Отклонения, оцененные для статистических анализов, представляли: уровни инсулина и глюкозы в каждый момент времени и их соответствующий пик, время наступления пика, общие средние величины и площади под кривыми. Уровни инсулина и глюкозы на основной линии рассчитывали в виде среднего значения обоих образцов на основной линии. Различные площади под кривыми рассчитывали и для глюкозы, и для инсулина: 1) общая площадь под кривой (AUC) и 2) площадь под кривой до и после момента времени соответствующего 4 часам (AUC<4 и AUC>4 соответственно).
Обработку данных с помощью общей линейной модели SAS (системы статистического анализа) использовали для трех типов анализа. Сначала изучили ответную реакцию в зависимости от времени и исследовали линейную, квадратичную и кубическую временные тенденции, все ортогонально. Классификация включала источник обработки, время и взаимодействие обработки в зависимости от времени. Второй анализ был предназначен для изучения отклонений для всех измеренных и рассчитанных переменных величин. Классификация включала источник для параллельного эксперимента, обработку и взаимодействие параллельного эксперимента-обработки. Третий анализ был предназначен для изучения совместных отклонений с "увеличением промежутка времени при обработке" в виде совместного отклонения. Это нарушает одно из требований анализа для совместных отклонений, но полагают дает некоторую информацию о результатах изменения веса тела на ответную реакцию. Классификация была той же самой, как во втором анализе. Все значения интервалов представляли с помощью 5%, по крайней мере, значительного различия (LSD). LSD использовали, если экспериментальный F-тест отвергался при а<0,10.
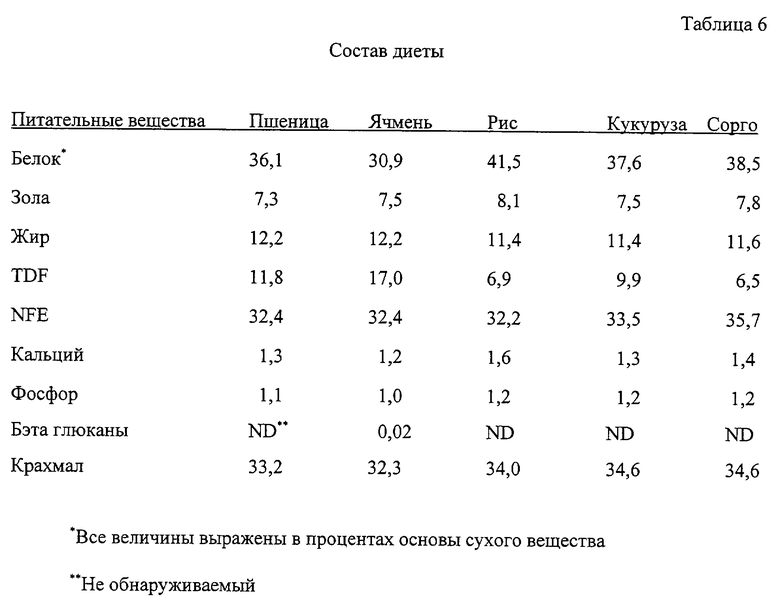
Химический состав экспериментальных диет суммируют в табл. 6.
Содержания сухого вещества и крахмала были аналогичны во всех диетах (91,7-93,6 вес. % и 32,3-34,6 вес.%, соответственно). Содержание жира менялось от 11,4 (для риса) до 12,2 вес.% (для ячменя) и содержание белка от 30,9 (для ячменя) до 41,5 вес.% (для риса). Содержание NFE было самым высоким для сорго (35,7 вес.%) и самым низким для риса (32,2 вес.%). Содержание общей диетической клетчатки было самым высоким (17,0 вес.%) для ячменя и самым низким для сорго (6,5 вес.%).
Для ответной реакции глюкозы обнаруживали сильное взаимодействие (Р<0,01) время-диета. Ортогональный анализ указывал на то, что рис имел значительно отличающуюся линейную тенденцию (Р<0,05), чем пшеница, ячмень и сорго, но не очень отличался от сорго (Р<0,10). Пшеница также обладала отличной линейной тенденцией (Р<0,05), чем рис, кукуруза и сорго основных диет, но была аналогична ячменю. Между диетами не наблюдали различий для квадратичных и кубических тенденций.
Табл. 7 суммирует уровни глюкозы после еды в различные моменты времени. Диетические режимы не оказывали влияния на уровни глюкозы в различные моменты времени (основная линия в моменты времени 1, 4, 6, 9, 10 и 18 часов после кормления), но значительные отличия наблюдали в моменты времени, соответствующие 2, 12 и 15 часам. В момент времени, соответствующий 2 часам после еды, рис приводил к самому высокому ((Р<0,05) уровню глюкозы, по сравнению с другими источниками крахмала (см. фиг.3 графического представления данных из табл. 7). Пшеница, ячмень и кукуруза приводили к самым низким уровням (Р<0,05) глюкозы.
В момент времени, соответствующий 12 часам после приема пищи, пшеница давала самый высокий уровень глюкозы (Р<0.05), в то время как рис приводил к самому низкому (Р<0.05) уровню глюкозы. Показано на фиг.3. В момент времени, соответствующий 15 часам после приема пищи, пшеница и ячмень приводили к самому высокому уровню глюкозы (Р<0,05), в то время как рис приводил к самому низкому (Р<0,05) уровню глюкозы.
Ячмень приводил к замедлению (Р<0.05) времени появления пика глюкозы, по сравнению с другими источниками крахмала, как показано в табл. 8, приведенной ниже. Рис приводил численно к самому высокому значению глюкозы для AUC<4, но к самому низкому (Р<0.05) значению глюкозы для AUC>4.
В заключение, все диеты давали аналогичные величины уровня глюкозы на основной линии и в момент времени, соответствующий 18 часам после еды. Рис приводил к быстрому подъему уровней глюкозы, но быстро снижался, указывая на появление эффектов и гипер- и гипогликемии. Пшеница давала умеренное увеличение уровней глюкозы с последующим продолжительным снижением уровней глюкозы. Наиболее желаемые эффекты имели место для кукурузы, сорго и ячменя с более смягченным увеличением и уменьшением ответной реакции появления глюкозы, по сравнению с другими диетами.
В ответной инсулиновой реакции у животных обнаруживали значительное взаимодействие диеты и времени. Ортогональный анализ указывает на то, что рис обладал значительно отличающейся (Р<0,05) линейной тенденцией, чем тенденция, которую наблюдали для пшеницы, ячменя, кукурузы или сорго. Диеты на основе пшеницы, ячменя, кукурузы и сорго имели аналогичные линейные тенденции. Не отмечено различий между диетами для квадратичной и кубической тенденций.
Табл. 9 суммирует уровни инсулина в различные моменты времени. Диетические режимы не влияли на ответную реакцию инсулина в моменты времени, соответствующие 8, 10, 12, 15 и 18 часам, но значительные различия наблюдали на основной линии в моменты времени, соответствующие 1, 2, 4 и 6 часам.
Рис приводил к более высоким уровням (Р<0.05) инсулина на основной линии, в моменты времени, соответствующие 1, 2, 4 и 6 часам, чем другие диеты, за исключением пшеницы, которая давала аналогичную ответную реакцию инсулина на основной линии в моменты времени, соответствующие 2 и 6 часам (см. фиг. 4), которая является графическим представлением данных, приведенных в табл. 9. Ответная реакция инсулина обычно была самой низкой для ячменя, кукурузы и сорго.
Общий средний уровень и пиковое значение инсулина для риса были значительно выше (Р<0,05), чем эти значения для ячменя, кукурузы и сорго, но не отличались от значений для пшеницы, как показано в табл. 10, приведенной ниже. Величина инсулина для AUC<4 для риса была значительно выше (Р<0,05), чем для других источников крахмала.
В заключение, рис, вслед за пшеницей, приводил к большей ответной реакции инсулина в течение первых шести часов стимуляции. Для всех измеренных отклонений инсулина, ячмень, кукуруза и сорго не приводили к различиям (Р>0,05) ответной реакции инсулина.
Сравнение риса, кукурузы, сорго и ячменя обычно показывало постепенное увеличение и снижение ответной реакции появления глюкозы. Кроме того, по сравнению с рисом, кукуруза, сорго и ячмень обычно приводили к более низкой ответной реакции инсулина. Смеси кукурузы и сорго, или сорго и ячменя, или кукурузы и ячменя, или кукурузы, сорго и ячменя давали суммарный эффект снижения уровней глюкозы и инсулина в крови после еды. Из-за того что источники ячменя, кукурузы и сорго помогают снижать уровни инсулина, они будет представлять практический интерес также в контролировании гиперинсулинемии.







Изобретение предназначено для использования в кормопроизводстве. Пищевая композиция для домашних животных для регулирования ответной реакции на гликемию после еды у этих животных включает источник белка, источник жира и источник углеводов, содержит в качестве источника углеводов составной зерновой источник, включающий два или три источника зерна, которые выбирают из группы, состоящей из сорго, ячменя и кукурузы; в котором весовое отношение двух источников зерна составляет от 1:5 до 5:1, а отношение трех источников зерна составляет от 1:1:5 или 1:5:1 до 5:1:1. Изобретение позволяет обеспечить улучшение метаболизма глюкозы и/или инсулина у животных, сопутствующих человеку, за счет контролирования у этих животных ответной реакции на наличие глюкозы в крови и/или инсулина, происходящей после еды. 11 з.п. ф-лы, 4 ил., 10 табл.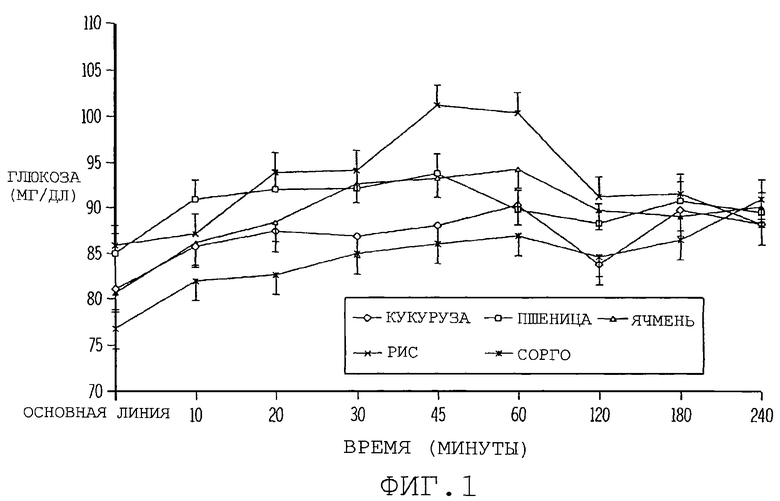
| УСТРОЙСТВО для ОПРЕДЕЛЕНИЯ СПЛОШНОСТИ | 0 |
|
SU205354A1 |
| ОПТИМИЗАЦИЯ МУЛЬТИМЕДИА В РЕАЛЬНОМ ВРЕМЕНИ ВО ВРЕМЯ УДАЛЕННЫХ СЕАНСОВ | 2011 |
|
RU2595548C2 |
| Штамм вируса нодулярного дерматита крупного рогатого скота Dermatitis nodularis bovum, рода Capripoxvirus для изготовления биопрепаратов для диагностики и специфической профилактики нодулярного дерматита крупного рогатого скота | 2016 |
|
RU2606254C1 |
Авторы
Даты
2003-02-10—Публикация
1999-04-02—Подача