Изобретение относится к производным ацилфенилмочевины, а также их физиологически совместимым солям и физиологически функциональным производным.
Применение производных ацилфенилмочевины в качестве инсектицидов уже описано в уровне техники (Европейские патенты EP 0136745, EP 0167197, Патент Германии DE 2926480, J. Agric. Food Chem. 1999, 47, 3116-3424).
Задачей данного изобретения является получение соединений, проявляющих действие, понижающее терапевтически приемлемый уровень сахара в крови.
Поэтому изобретение относится к соединениям формулы I,
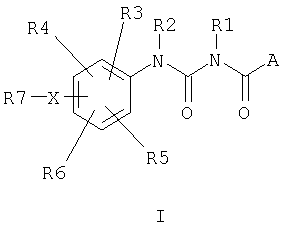
в котором означают
A фенил, нафтил, причем фенильная или нафтильная группа может содержать до трех заместителей, таких как F, Cl, Br, OH, CF3, NO2, CN, OCF3, O-(C1-C6)-алкил, O-(C1-C6)-алкенил, O-(C1-C6)-алкинил, S-(C1-C6)-алкил, S-(C1-C6)-алкенил, S-(C1-C6)-алкинил, SO-(C1-C6)-алкил, SO2-(C1-C6)-алкил, SO2-NH2, (C1-C6)-алкил, (C1-C6)-алкенил, (C1-C6)-алкинил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкилен, (C0-C6)-алкилен-COOH, (C0-C6)-алкилен-COO(C1-C7)-алкил, CONH2, CONH(C1-C6)-алкил, CON[(C1-C6)-алкил]2, CONH(C3-C6)-циклоалкил, (C0-C6)-алкилен-NH2, (C0-C6)-алкилен-NH(C2-C6)-алкил, (C0-C6)-алкилен-N[(C1-C6)-алкил]2, NH-CO-(C1-C6)-алкил, NH-CO-фенил, NH-SO2-фенил, при этом фенильное кольцо может содержать до двух заместителей, таких как F, Cl, CN, OH, (C1-C6)-алкил, O-(C1-C6)-алкил, CF3, OCF3, COOH, COO(C1-C6)-алкил или CONH2;
R1, R2 независимо друг от друга означают H, (C1-C6)-алкил, O-(C1-C6)-алкил, CO-(C1-C6)-алкил, COO-(C1-C6)-алкил, (C1-C6)-алкилен-COOH, (C1-C6)-алкилен-COO-(C1-C6)-алкил;
R3, R4, R5, R6 независимо друг от друга означают H, F, Cl, Br, OH, CF3, NO2, CN, OCF3, O-(C1-C6)-алкил, O-(C1-C6)-алкенил, O-(C1-C6)-алкинил, S-(C1-C6)-алкил, S-(C1-C6)-алкенил, S-(C1-C6)-алкинил, SO-(C1-C6)-алкил, SO2-(C1-C6)-алкил, SO2-NH2, (C1-C6)-алкил, (C1-C6)-алкенил, (C1-C6)-алкинил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкилен, COOH, COO(C1-C6)-алкил, CONH2, CONH(C1-C6)-алкил, CON[(C1-C6)-алкил]2, CONH(C3-C7)-циклоалкил, NH2, NH(C1-C6)-алкил, N[(C1-C6)-алкил]2, NH-CO-(C1-C6)-алкил, NH-CO-фенил, NH-SO2-фенил, причем фенильное кольцо может иметь до двух заместителей, таких как F, Cl, CN, OH, (C1-C6)-алкил, O-(C1-C6)-алкил, CF3, OCF3, COOH, COO(C1-C6)-алкил или CONH2;
X O, S;
R7 (C1-C10)-алкилен-COOH, (C6-C10)-алкилен-COO-(C1-C6)-алкил, (C1-C10)-алкилен-CONH2, (C1-C10)-алкилен-CONH-(C1-C6)-алкил, (C1-C10)-алкилен-CON-[(C1-C6)-алкил]2, (C1-C10)-алкилен-NH2, (C1-C10)-алкилен-NH(C1-C6)-алкил, (C1-C10)-алкилен-N[(C1-C6)-алкил]2, (C1-C10)-алкилен-B;
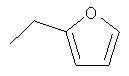
B (C3-C7)-циклоалкил, пирролил, имидазолил, тиазолил, ацетидинил, тиенил, пиперидинил, пирролидинил, морфолинил, пиридил-метил или фурил, причем циклоалкил, фенил, пирролил, имидазолил, тиазолил, ацетидинил, тиенилметил, пиперидинил, пирролидинил, морфолинил, пиридил или фурил могут содержать до двух заместителей, таких как Cl, F, CN, CF3, OCF3, COOH, COO-(C1-C6)-алкил, CONH2, CONH-(C1-C6)-алкил, CON-[(C1-C6)-алкил]2, (C1-C6)-алкил, OH, O-(C1-C6)-алкил;
а также их физиологически совместимые соли,
при этом исключаются соединения формулы
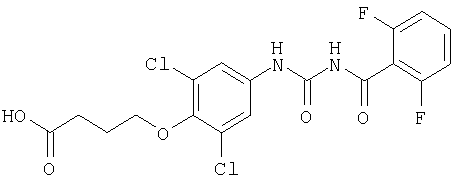
а также соединения формулы I, где остатки одновременно означают
Предпочтительны соединения формулы I, где означают
A фенил, нафтил, причем фенильная или нафтильная группа может содержать до трех заместителей, таких как F, Cl, Br, OH, CF3, NO2, CN, OCF3, O-(C1-C6)-алкил, O-(C1-C6)-алкенил, O-(C1-C6)-алкинил, S-(C1-C6)-алкил, S-(C1-C6)-алкенил, S-(C1-C6)-алкинил, SO-(C1-C6)-алкил, SO2-(C1-C6)-алкил, SO2-NH2, (C1-C6)-алкил, (C1-C6)-алкенил, (C1-C6)-алкинил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкилен, (C0-C6)-алкилен-COOH, (C0-C6)-алкилен-COO(C1-C6)-алкил, CONH2, CONH(C1-C6)-алкил, CON[(C1-C6)-алкил]2, CONH(C3-C7)-циклоалкил,(C0-C6)-алкилен-NH2, (C0-C6)-алкилен-NH(C2-C6)-алкил, (C0-C6)-алкилен-N[(C1-C6)-алкил]2, NH-CO-(C1-C6)-алкил, NH-CO-фенил, NH-SO2-фенил, при этом фенильное кольцо может содержать до двух заместителей, таких как F, Cl, CN, OH, (C1-C6)-алкил, O-(C1-C6)-алкил, CF3, OCF3, COOH, COO(C1-C6)-алкил или CONH2;
R1, R2 независимо друг от друга означают H, (C1-C6)-алкил, O-(C1-C6)-алкил, CO-(C1-C6)-алкил, COO-(C1-C6)-алкил, (C1-C6)-алкилен-COOH, (C1-C6)-алкилен-COO-(C1-C6)-алкил;
R3, R4, R5, R6 независимо друг от друга означают: H, F, Cl, Br, OH, CF3, NO2, CN, OCF3, O-(C1-C6)-алкил, O-(C1-C6)-алкенил, O-(C1-C6)-алкинил, S-(C1-C6)-алкил, S-(C1-C6)-алкенил, S-(C1-C6)-алкинил, SO-(C1-C6)-алкил, SO2-(C1-C6)-алкил, SO2-NH2, (C1-C6)-алкил, (C1-C6)-алкенил, (C1-C6)-алкинил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкилен, COOH, COO(C1-C6)-алкил, CONH2, CONH(C1-C6)-алкил, CON[(C1-C6)-алкил]2, CONH(C3-C7)-циклоалкил, NH2, NH(C1-C6)-алкил, N[(C1-C6)-алкил]2, NH-CO-(C1-C6)-алкил, NH-CO-фенил, NH-SO2-фенил, причем фенильное кольцо может содержать до двух заместителей, таких как F, Cl, CN, OH, (C1-C6)-алкил, O-(C1-C6)-алкил, CF3, OCF3, COOH, COO(C1-C6)-алкил или CONH2;
X O, S;
R7 (C1-C10)-алкилен-COOH, (C6-C10)-алкилен-COO-(C1-C6)-алкил, (C1-C10)-алкилен-CONH2, (C1-C10)-алкилен-CONH-(C1-C6)-алкил, (C1-C10)-алкилен-CON-[(C1-C6)-алкил]2, (C1-C10)-алкилен-NH2, (C1-C10)-алкилен-NH(C1-C6)-алкил, (C1-C10)-алкилен-N[(C1-C6)-алкил]2, (C1-C10)-алкилен-B;
B (C3-C7)-циклоалкил, пирролил, имидазолил, тиазолил, ацетидинил, тиенилметил, пиперидинил, пирролидинил, морфолинил, пиридил-метил или фурил, причем циклоалкил, фенил, пирролил, имидазолил, тиазолил, ацетидинил, тиенил, пиперидинил, пирролидинил, морфолинил, пиридил или фурил, могут содержать до двух заместителей, таких как Cl, F, CN, CF3, OCF3, COOH, COO-(C1-C6)-алкил, CONH2, CONH-(C1-C6)-алкил, CON-[(C1-C6)-алкил]2, (C1-C6)-алкил, OH, O-(C1-C6)-алкил;
а также их физиологически совместимые соли,
при этом исключаются соединения формулы

а также соединения формулы I, где остатки одновременно означают
Особенно предпочтительны соединения формулы I, где
A фенил, причем фенильная группа может содержать до двух заместителей, таких как F, Cl, Br, O-(C1-C6)-алкил;
R1, R2 независимо друг от друга означают H, (C1-C6)-алкил, CO-(C1-C6)-алкил, -О(С1-С6)-алкил;
R3, R4, R5, R6 независимо друг от друга означают H, Cl, F, (C1-C6)-алкил, COO-(C1-C6)-алкил;
X O;
R7 (C1-C10)-алкилен-COOH, (C6-C10)-алкилен-COO-(C1-C6)-алкил, (C1-C10)-алкилен-CONH2;
а также их физиологически совместимые соли,
при этом исключается соединение формулы

Кроме того, изобретение касается также применения соединений формулы I
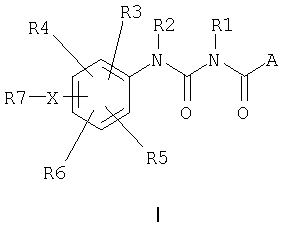
где означают
A фенил, нафтил, причем фенильная или нафтильная группа может содержать до трех заместителей, таких как F, Cl, Br, OH, CF3, NO2, CN, OCF3, O-(C1-C6)-алкил, O-(C1-C6)-алкенил, O-(C1-C6)-алкинил, S-(C1-C6)-алкил, S-(C1-C6)-алкенил, S-(C1-C6)-алкинил, SO-(C1-C6)-алкил, SO2-(C1-C6)-алкил, SO2-NH2, (C1-C6)-алкил, (C1-C6)-алкенил, (C1-C6)-алкинил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкилен, (C0-C6)-алкилен-COOH, (C0-C6)-алкилен-COO(C1-C6)-алкил, CONH2, CONH(C1-C6)-алкил, CON[(C1-C6)-алкил]2, CONH(C3-C7)-циклоалкил, (C0-C6)-алкилен-NH2, (C0-C6)-алкилен-NH(C1-C6)-алкил, (C0-C6)-алкилен-N[(C1-C6)-алкил]2, NH-CO-(C1-C6)-алкил, NH-CO-фенил, NH-SO2-фенил, при этом фенильное кольцо может иметь до двух заместителей, таких как F, Cl, CN, OH, (C1-C6)-алкил, O-(C1-C6)-алкил, CF3, OCF3, COOH, COO(C1-C6)-алкил или CONH2;
R1, R2 независимо друг от друга означают H, (C1-C6)-алкил, O-(C1-C6)-алкил, CO-(C1-C6)-алкил, COO-(C1-C6)-алкил, (C1-C6)-алкилен-COOH, (C1-C6)-алкилен-COO-(C1-C6)-алкил;
R3, R4, R5, R6 независимо друг от друга означают H, F, Cl, Br, OH, CF3, NO2, CN, OCF3, O-(C1-C6)-алкил, O-(C1-C6)-алкенил, O-(C1-C6)-алкинил, S-(C1-C6)-алкил, S-(C1-C6)-алкенил, S-(C1-C6)-алкинил, SO-(C1-C6)-алкил, SO2-(C1-C6)-алкил, SO2-NH2, (C1-C6)-алкил, (C1-C6)-алкенил, (C1-C6)-алкинил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкилен, COOH, COO(C1-C6)-алкил, CONH2, CONH(C1-C6)-алкил, CON[(C1-C6)-алкил]2, CONH(C3-C7)-циклоалкил, NH2, NH(C1-C6)-алкил, N[(C1-C6)-алкил]2, NH-CO-(C1-C6)-алкил, NH-CO-фенил, NH-SO2-фенил, причем фенильное кольцо может содержать до двух заместителей, таких как F, Cl, CN, OH, (C1-C6)-алкил, O-(C1-C6)-алкил, CF3, OCF3, COOH, COO(C1-C6)-алкил или CONH2;
X O, S;
R7 (C1-C10)-алкилен-COOH, (C1-C10)-алкилен-COO-(C1-C6)-алкил, (C1-C10)-алкилен-CONH2, (C1-C10)-алкилен-CONH-(C1-C6)-алкил, (C1-C10)-алкилен-CON-[(C1-C6)-алкил]2, (C1-C10)-алкилен-NH2, (C1-C10)-алкилен-NH(C1-C6)-алкил, (C1-C10)-алкилен-N[(C1-C6)-алкил]2, (C1-C10)-алкилен-B;
B (C3-C7)-циклоалкил, фенил, пирролил, имидазолил, тиазолил, ацетидинил, тиенил, пиперидинил, пирролидинил, морфолинил, пиридил или фурил, при этом циклоалкил, фенил, пирролил, имидазолил, тиазолил, ацетидинил, тиенил, пиперидинил, пирролидинил, морфолинил, пиридил или фурил могут содержать до двух заместителей, таких как Cl, F, CN, CF3, OCF3, COOH, COO-(C1-C6)-алкил, CONH2, CONH-(C1-C6)-алкил, CON-[(C1-C6)-алкил]2, (C1-C6)-алкил, OH, O-(C1-C6)-алкил;
а также их физиологически совместимых солей для получения лекарственного средства для снижения уровня сахара в крови и лечения диабета типа II.
Изобретение включает соединения формулы I в форме их рацематов, рацемических смесей и чистых энантиомеров, а также их диастереоизомеров и их смесей.
Алкильные группы в заместителях R1, R2, R3, R4, R5, R6, R7, A и B могут быть как линейными, так и разветвленными.
Для применений в медицине особенно пригодны фармацевтически приемлемые соли благодаря их высокой растворимости в воде по сравнению с исходными соединениями. Эти соли должны иметь фармацевтически приемлемый анион или катион. Подходящими фармацевтически приемлемыми солями присоединения кислот соединений согласно изобретению являются соли неорганических кислот, такие как соляная кислота, бромистоводородная кислота, фосфорная, метафосфорная, азотная кислоты, сульфоновая и серная кислоты, а также органических кислот, таких, например, как уксусная кислота, бензолсульфокислота, бензойная кислота, лимонная кислота, этансульфоновая, фумаровая, гликоновая и гликолевая кислоты, изотионовая, молочная, лактобионовая, малеиновая, яблочная, метансульфоновая, янтарная, п-толуолсульфоновая и винная кислоты. Подходящими фармацевтически приемлемыми основными солями являются соли аммония, соли щелочных металлов (например, соли натрия и калия) и щелочноземельных металлов (например, соли магния и кальция).
Соли с фармацевтически неприемлемым анионом, например трифторацетатом, также охватываются рамками изобретения как необходимые промежуточные продукты для получения или очистки фармацевтически приемлемых солей и/или для применения в нетерапевтических целях, например для применения in vitro.
Используемое здесь понятие "физиологически активное производное" означает любое физиологически совместимое производное соединения формулы I согласно изобретению, например сложный эфир, который при введении млекопитающему, например человеку, в состоянии (непосредственно или опосредованно) образовать соединение формулы I или активный метаболит.
К физиологически активным производным относятся также пролекарства соединений согласно изобретению, например, описанные H. Okada и др., Chem. Pharm. Bull. 1994, 42, 57-61. Такие пролекарства могут быть метаболизированы in vivo до соединений согласно изобретению. Сами эти пролекарства могут быть как эффективными, так и неэффективными.
Соединения согласно изобретению могут также находиться в различных полиморфных формах, например в виде аморфных и кристаллических полиморфных формах. Все полиморфные формы соединений согласно изобретению охватываются изобретением и являются объектом настоящего изобретения.
Далее все ссылки на "соединение(я) формулы I" относятся как к соединению(ям) формулы I, как они описаны выше, так и к их солям, сольватам и физиологически функциональным производным.
Количество соединения формулы I, необходимое для достижения желаемого биологического эффекта, зависит от ряда факторов, например конкретного выбранного соединения, планируемого применения, типа введения и клинического состояния пациента. В целом дневная доза находится в интервале от 0,3 до 100 мг (обычно от 3 до 50 мг) в день на килограмм веса, например 3-10 мг/кг/день. Внутривенная доза может составлять, например, от 0,3 до 1,0 мг/кг, при вливаниях подходящая доза составляет от 10 до 100 нг на килограмм в минуту. Подходящие для этих целей растворы для инъекций могут содержать например, от 0,1 нг до 10 мг, (обычно от 1 нг до 10 мг) на миллилитр раствора. Однократные дозы могут содержать, например, от 1 мг до 10 г активного вещества. Таким образом, ампулы для инъекций могут содержать, например, от 1 мг до 100 мг, а величина однократной орально вводимой дозы, например таблетки или капсулы, может содержать, например, от 1,0 до 1000 мг, обычно от 10 до 600 мг. Для лечения названных выше заболеваний могут применяться соединения формулы I непосредственно в виде соединения, однако предпочтительнее применять их с приемлемым наполнителем в форме фармацевтической композиции. Наполнитель должен быть, естественно, совместимым в том смысле, что он совместим с другими составными частями композиции и не вредит здоровью пациента. Наполнитель может быть как твердым веществом, так и жидкостью, или и тем и другим и предпочтительно применяется вместе с соединением в виде однократной дозы, например в виде таблеток, которые могут содержать от 0,05% до 95% вес. активного вещества. Могут иметь место также и другие фармацевтически активные вещества, включая другие соединения формулы I. Фармацевтические композиции согласно изобретению могут быть получены по какому-либо из известных фармацевтических методов, которые в основном заключаются в том, чтобы смешать составные части с фармакологически совместимым наполнителем и/или вспомогательными веществами.
Фармацевтические композиции согласно изобретению пригодны для орального, ректального, местного, перорального (например, под язык) и парентерального (например, подкожного, внутримышечного, внутрикожного или внутривенного) применения, хотя наиболее подходящие способы применения в каждом отдельном случае зависят от вида и тяжести состояния пациента и от вида применяемого соединения формулы I. Дражированные готовые лекарственные формы и дражированные пролонгированные лекарственные формы также относятся к настоящему изобретению. Предпочтительны готовые лекарственные формы, устойчивые к кислотам и желудочному соку. Подходящие оболочки, устойчивые к желудочному соку, охватывают ацетатфталат целлюлозы, поливинилацетатфталат, фталат гидроксипропилметилцеллюлозы и анионные полимеры метакриловой кислоты и метилметакрилата.
Фармацевтически пригодные соединения для орального применения могут изготавливаться в виде отдельных единичных доз, например в виде капсул, капсул с оболочкой, сосательных таблеток или таблеток, которые содержат определенное количество соединения формулы I; а также в виде порошка или гранул; в виде раствора или суспензии в водной или неводной среде; или в виде эмульсии "масло в воде" или "вода в масле". Эти композиция могут быть приготовлены, как уже указывалось, любым подходящим фармацевтическим методом, предусматривающим этап, на котором активное вещество и наполнитель (который может состоять из одного или нескольких дополнительных компонентов) приводятся в контакт. В целом композиция проходит через равномерное и гомогенное смешение активного вещества с жидким и/или размельченным твердым наполнителем, после чего, если это необходимо, продукт формуется. Так могут быть получены, например, таблетки, когда порошок или гранулят соединения прессуется или формуется, при необходимости, с одним или несколькими дополнительными компонентами. Прессованные таблетки могут быть получены путем таблетирования соединения, находящегося в свободнотекучей форме, например порошок или гранулы, при необходимости смешанные со связующим веществом, мягчителем, инертным разбавителем и/или одним (несколькими) поверхностно-активным/диспергирующим средством в подходящем аппарате. Формованные таблетки могут быть получены путем формования порошкообразного соединения, смоченного инертным жидким разбавителем в подходящем аппарате.
К фармацевтическим композициям, которые подходят для перорального применения (под язык), относятся сосательные таблетки, которые содержат соединение формулы I с вкусовой добавкой, обыкновенно это сахароза и гуммиарабик или трагант, и пастилки, к которым относятся соединения на инертной основе, такой как желатин и глицерин, или сахароза и гуммиарабик.
К фармацевтическим композициям, подходящим для парентерального применения, относятся предпочтительно стерильные водные композиции соединения формулы I, которые предпочтительно изотоничны с кровью предполагаемого реципиента. Эти композиции применяются преимущественно внутривенно, хотя могут также производиться подкожно, внутримышечно или внутрикожно в виде инъекций. Эти композиции могут быть предпочтительно получены путем смешения с водой, стерилизацией полученного раствора и приданием ему изотонических с кровью свойств. Композиции для инъекций согласно изобретению содержат, как правило, от 0,1 до 5 вес% активного соединения.
Фармацевтические композиции, подходящие для ректального применения, предлагаются предпочтительно в виде единичных доз-суппозиториев. Они могут быть получены путем смешения соединения формулы I с одним или несколькими традиционными твердыми наполнителями, например маслом какао, и формованием полученной смеси.
Фармацевтические композиции, подходящие для наружного применения на кожу, предлагаются предпочтительно в виде мази, крема, лосьона, пасты, спрея, аэрозоля или масла. Наполнителем может быть ланолин, полиэтиленгликоль, спирт и комбинация двух или больше этих веществ. Концентрация активного вещества составляет обычно от 0,1 до 15 вес% композиции, например от 0,5 до 2%.
Возможно также трансдермальное применение. Фармацевтические композиции, подходящие для трансдермального применения, могут быть в виде пластырей, которые пригодны для длительного тесного контакта с эпидермисом пациента. Такие пластыри содержат пригодное активное вещество, при необходимости в буферном водном растворе, растворены и/или диспергированы в адгезиве или диспергированы в полимере. Подходящая концентрация активного вещества составляет приблизительно от 1% до 35%, предпочтительно приблизительно от 3% до 15%. Согласно особой форме введения активное вещество может высвобождаться путем электрофореза или ионофореза, как описано, например, в Pharmaceutical Research, 2(6): 318 (1986).
Объектом изобретения далее является способ получения соединения общей формулы I, отличающийся тем, что соединения формулы I получают согласно следующей реакционной схеме:
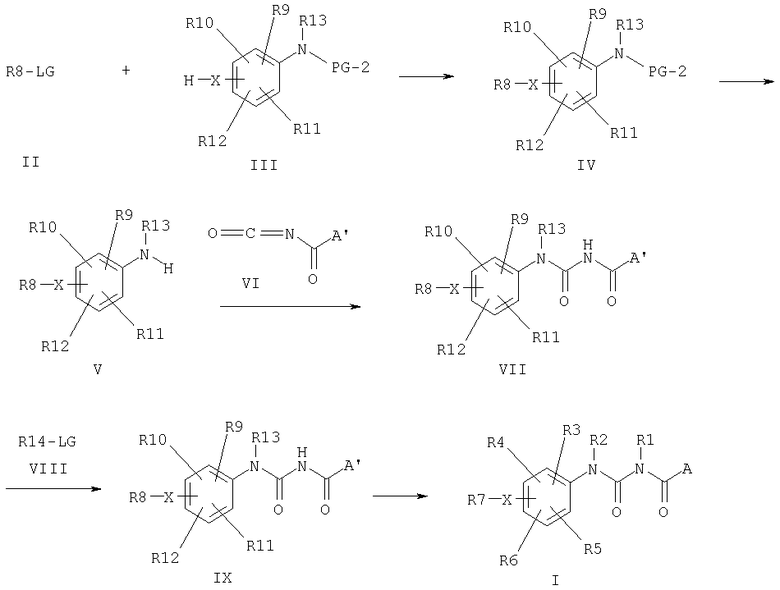
Для этого соединения общей формулы II
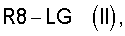
в которой
R8 означает (C1-C10)-алкилен-COO(PG-1), (C6-C10)-алкилен-COO-(C1-C6)-алкил, (C1-C10)-алкилен-CON-(PG-2)2, (C1-C10)-алкилен-CONH-(C1-C6)алкил, (C1-C10)-алкилен-CON-[(C1-C6)-алкил]2, (C1-C10)-алкилен-N-(PG-2)2, (C1-C10)-алкилен-NH(C1-C6)-алкил, (C1-C10)-алкилен-N[(C1-C6)-алкил]2, (C1-C10)-алкилен-B',
где PG-1 означает известную защитную для эфира группу, например (C1-C6)-алкил, бензил или п-метоксибензил, а
PG-2 - известную защитную группу для аминогруппы, например (C1-C6)-алкилкарбонил, (C1-C6)-алкилоксикарбонил или (C6-C12)-арил-(C1-C4)-алкилоксикарбонил, который замещает только один или оба атома водорода аминогруппы,
B' (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкилен, фенил, пирролил, имидазолил, тиазолил, ацетидинил, тиенил, пиперидинил, пирролидинил, морфолинил, пиридил и фурил, причем циклоалкил, фенил, пирролил, имидазолил, тиазолил, ацетидинил, тиенил, пиперидинил, пирролидинил, морфолинил, пиридил и фурил могут иметь до двух заместителей, таких как Cl, F, CN, CF3, OCF3, COO-(PG-1), COO-(C1-C6)-алкил, CON-(PG-2)2, CONH-(C1-C6)-алкил, CON-[(C1-C6)-алкил]2, (C1-C6)-алкил, O-(PG-3), O-(C1-C6)-алкил,
где PG-3 обозначает известную защитную группу для спирта, например бензил, карбонил, тетрагидропиранил или тетрагидрофуранил,
а
LG - известную удаляемую группу, например галоген, арилсульфонилокси- или алкилсульфонилокси-,
алкилируют с анилинами общей формулы III
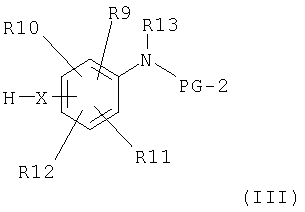
где X и PG-2 имеют значения, описанные выше, а
R9, R10, R11, R12 независимо друг от друга означают: H, F, Cl, Br, O-(PG-3), CF3, NO2, CN, OCF3, O-(C1-C6)-алкил, O-(C1-C6)-алкенил, O-(C1-C6)-алкинил, S-(C1-C6)-алкил, S-(C1-C6)-алкенил, S-(C1-C6)-алкинил, SO-(C1-C6)-алкил, SO2-(C1-C6)-алкил, SO2-N-(PG-2)2, (C1-C6)-алкил, (C1-C6)-алкенил, (C1-C6)-алкинил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкилен, COO-(PG-I), COO(C1-C6)-алкил, CON-(PG-2)2, CONH(C1-C6)-алкил, CON[(C1-C6)-алкил]2, CONH(C3-C7)-циклоалкил, N-(PG-2)2, NH(C1-C6)-алкил, N[(C1-C6)-алкил]2, NH-CO-(C1-C6)-алкил, NH-CO-фенил, NH-SO2-фенил, причем фенильное кольцо может иметь до двух заместителей, таких как F, Cl, CN, O-(PG-3), (C1-C6)-алкил, O-(C1-C6)-алкил, CF3, OCF3, COO-(PG-1), COO(C1-C6)-алкил или CON-(PG-2)2;
R13 H, (C1-C6)-алкил, O-(C1-C6)-алкил, CO-(C1-C6)-алкил, COO-(C1-C6)-алкил, (C1-C6)-алкилен-COO-(PG-1), (C1-C6)-алкилен-COO-(C1-C6)-алкил,
а PG-1, PG-2 и PG-3 имеют значения, описанные выше в присутствии основания, например карбоната калия или цезия, в органическом растворителе, например ацетоне или диметилформамиде, с получением соединения общей формулы IV
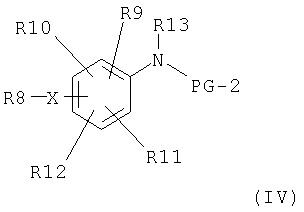
где X, R8, R9, R10, R11, R12, R13 и PG-2 имеют вышеописанные значения, время реакции составляет от 2 до 24 часов и температура реакции составляет от 10°C до точки кипения используемого растворителя, затем путем селективного отщепления защитной группы PG-2 получают соединение общей формулы V
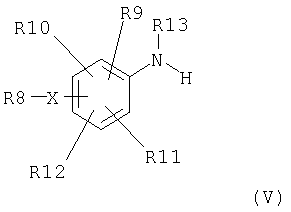
где X, R8, R9, R10, R11, R12 и R13 имеет вышеприведенные значения, соединения общей формулы V подвергают взаимодействию с изоцианатами общей формулы VI
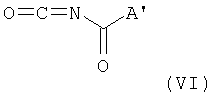
где
A' фенил, нафтил, причем фенильная или нафтильная группа может иметь до трех заместителей, таких как F, Cl, Br, O-(PG-3), CF3, NO2, CN, OCF3, O-(C1-C6)-алкил, (C1-C6)-алкенил, O-(C1-C6)-алкинил, S-(C1-C6)-алкил, S-(C1-C6)-алкенил, S-(C1-C6)-алкинил, SO-(C1-C6)-алкил, SO2-(C1-C6)-алкил, SO2-N-(PG-2)2, (C1-C6)-алкил, (C1-C6)-алкенил, (C1-C6)-алкинил, (C3-C7)-циклоалкил, (C3-C7)-циклоалкил-(C1-C4)-алкилен, (C0-C6)-алкилен-COO-(PG-1), (C0-C6)-алкилен-COO(C1-C6)-алкил, CON-(PG-2)2, CONH(C1-C6)-алкил, CON[(C1-C6)-алкил]2, CONH(C3-C7)-циклоалкил, (C0-C6)-алкилен-N-(PG-2)2, (C0-C6)-алкилен-NH(C1-C6)-алкил, (C0-C6)-алкилен-N[(C1-C6)-алкил]2, NH-CO-(C1-C6)-алкил, NH-CO-фенил, NH-SO2-фенил, при этом фенильное кольцо может иметь до двух заместителей, таких как F, Cl, CN, O-(PG-3), (C1-C6)-алкил, O-(C1-C6)-алкил, CF3, OCF3, COO-(PG-1), COO(C1-C6)-алкил или CON-(PG-2)2,
при этом PG-1, PG-2 и PG-3 имеют вышеописанные значения
в безводном органическом растворителе, например бензоле, толуоле или ацетонитриле, в атмосфере инертного газа при температуре реакции между 10°C и точкой кипения используемого растворителя до получения соединения общей формулы VII
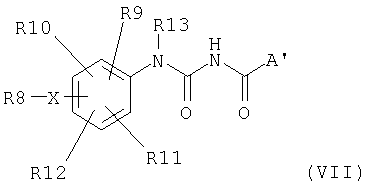
в котором X, R8, R9, R10, R11, R12, R13 и A' имеют вышеописанные значения, соединения общей формулы VII, если R1 в соединениях общей формулы I не является атомом водорода, алкилируют путем взаимодействия с соединениями общей формулы VIII

где LG имеет вышеописанное значение, а
R14 H, (C1-C6)-алкил, O-(C1-C6)-алкил, CO-(C1-C6)-алкил, COO-(C1-C6)-алкил, (C1-C6)-алкилен-COO-(PG-1), (C1-C6)-алкилен-COO-(C1-C6)-алкил,
причем PG-1 имеет значение, описанное выше,
с использованием основания, например,
1,8-диазабицикло[5.4.0]-ундец-7-ен, в органическом растворителе, например дихлорметане или ацетонитриле, с получением соединения общей формулы IX
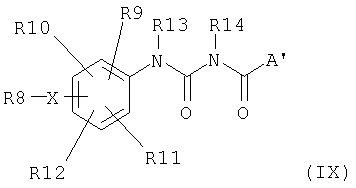
где X, R8, R9, R10, R11, R12, R13, R14 и A' имеют значения, описанные выше, и после известного из литературы отщепления всех возможных защитных групп в остатках R8, R9, R10, R11, R12, R13, R14, A' и B' получают соединения общей формулы I. Переведение соединения общей формулы I в его соли происходит при добавлении эквивалента соответствующей кислоты или основания в органическом растворителе, например ацетонитриле или диоксане, или в воде и путем последующего удаления растворителя.
Другая возможность получения соединений общей формулы I, где R2 является атомом водорода, показана на следующей схеме:
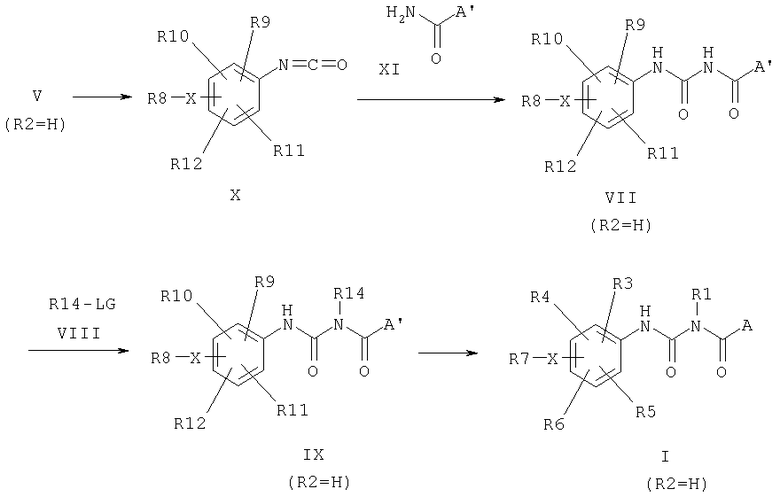
при этом соединения общей формулы V, в которых R2 означает атом водорода,
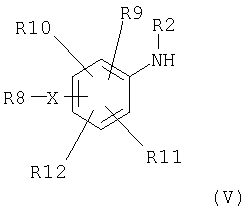
и X, R8, R9, R19, R11 и R12 имеют вышеописанные значения, превращаются в изоцианаты общей формулы X
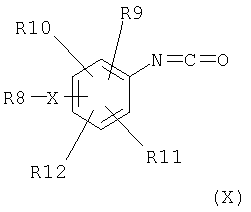
известными способами, например, взаимодействием с оксалилхлоридом в органических растворителях, например 1,2-дихлорэтане или дихлорметане, при температуре реакции между комнатной температурой и точкой кипения растворителя,
изоцианаты общей формулы X вводят в реакцию с амидами общей формулы XI
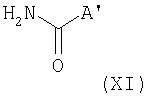
где A' - имеет вышеописанное значение,
и получают соединения общей формулы VII, где R2 означает атом водорода,
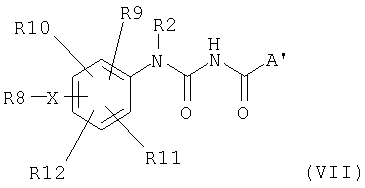
и X, R8, R9, R10, R11 и R12 имеют вышеописанные значения.
Если R1 не является атомом водорода, соединения общей формулы VII могут быть переведены, как уже описано выше, путем алкилирования с соединениями общей формулы VIII с получением соединения общей формулы IX, и, при необходимости, с последующим отщеплением защитных групп в соединения общей формулы I. Переведение соединений общей формулы I в их соли происходит при добавлении эквивалента соответствующей кислоты или основания в органическом растворителе, например ацетонитриле или диоксане, или в воде и путем последующего удаления растворителя.
Приведенные ниже примеры служат для пояснения изобретения, однако не ограничивая его. Измеренные точки плавления (Тпл) или разложения не корректировались и в общем случае зависят от скорости нагревания. (см. табл.1).
Примеры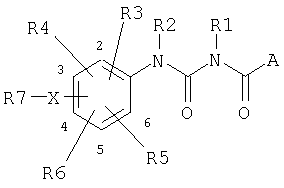
Формула I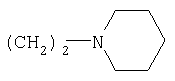
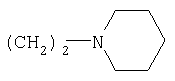


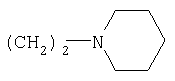
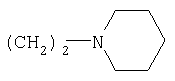
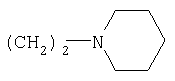
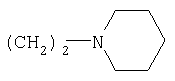
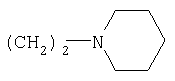
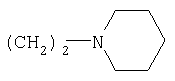
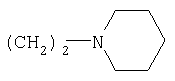
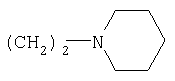
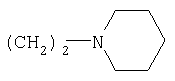
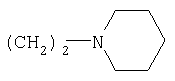
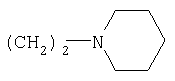
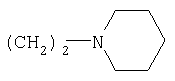
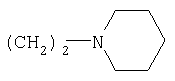
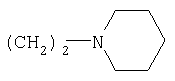
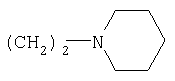
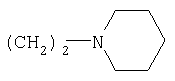
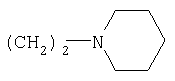
Соединения формулы I отличаются благоприятным воздействием на сахарный обмен, в частности они понижают содержание сахара в крови и пригодны для лечения диабета типа II. Соединения могут использоваться как самостоятельно, так и в комбинации с другими понижающими уровень сахар активными веществами. Такими понижающими содержание сахара в крови активными веществами являются, например, сульфонилмочевина (как, например, глимепирид, глибенкламид), глитазон (например, троглитазон, розиглитазон), ингибитор альфа-глюкозидазы (например, акарбоза, миглитол) или инсулин.
Эффективность соединения проверялась следующим образом:
Тест на активность гликогенфосфорилазы a
Влияние соединений на активность активной формы гликогенфосфорилазы (ГФа) измерялось в обратном направлении, путем наблюдения за синтезом гликогена из глюкозо-1-фосфата посредством определения высвобождения неорганического фосфата. Все реакции проводились с двойным определением на 96-луночных планшетах для микротитрования (Half Area Plates, Costar Nr. 3696), при этом с помощью прибора Multiskan Ascent Elisa Reader (Lab Systems, Финляндия) измерялось изменение поглощения при определенной длине волны в результате образования продукта реакции. Чтобы изменить активность фермента ГФа в обратном направлении, превращение глюкозо-1-фосфата C гликоген и неорганический фосфат измерялось по общему методу Энгерса и др. (Engers H.D., Shechosky S., Madsen N.B., Can. J. Biochem. 1970 Jul; 48(7):746-754) со следующими модификациями: человеческая гликогенфосфорилаза a (например, с 0,76 мг протеина/мл, (Aventis Pharma Deutschland GmbH), растворенная в буферном растворе E (25 мМ β-глицерофосфата, pH 7,0, 1 мМ ЭДТА и 1 мМ дитиотреитола) разбавлялась буфером T (50 мМ Hepes, pH 7,0, 100 мМ KCl, 2,5 мМ ЭДТА, 2,5 мМ MgCl2·6H2O) и добавлением 5 мг/мл гликогена до концентрации 10 мкг протеина/мл. Пробы для испытаний готовились в виде 10 мМ раствора в ДМСО и разбавлялись до 50 мМ раствором буфера T. К 10 мл этого раствора добавляли 10 мл 37,5 мМ глюкозы, растворенной в буферном растворе T, и 5 мг/мл гликогена, а также 10 мл раствора человеческой гликогенфосфорилазы a (10 мкг протеина/мл) и 20 мкл глюкозо-1-фосфата, 2,5 мМ. Базальное значение активности гликогенфосфорилазы a в отсутствие тестируемого вещества определялось путем добавления 10 мкл буферного раствора T (0,1% ДМСО). Смесь инкубировали в течение 40 минут при комнатной температуре, и высвобожденный неорганический фосфат измерялся с помощью общего метода Дрюкеса и др. (Drueckes P., Schinzel R., Palm D., Anal. Biochem 1995 Sep 1; 230(1): 173-177) со следующими модификациями: 50 мкл стопперирующего раствора 7,3 мМ молибдата аммония, 10,9 мМ ацетата цинка, 3,6% аскорбиновой кислоты, 0,9% ДСН добавлялось к 50 мкл смеси ферментов. После 60 минут выдерживания при 45°C измерялась абсорбция при 820 нм. Для определения фоновой абсорбции в отдельной пробе непосредственно после введения раствора глюкозо-1-фосфата добавлялся раствор стоппера. Этот тест проводился при концентрации тестируемых веществ 10 мМ, чтобы определить соответствующее гликогенфосфорилазы a in vitro ингибирование за счет тестируемого вещества. (см. табл. 2).
Биологическая активность
Из табл.2 видно, что соединения формулы I ингибируют активность гликогенфосфорилазы а и поэтому вполне пригодны для снижения содержания сахара в крови.
Далее подробно описывается пример, по аналогии с которым получают другие соединения формулы I.
Экспериментальная часть
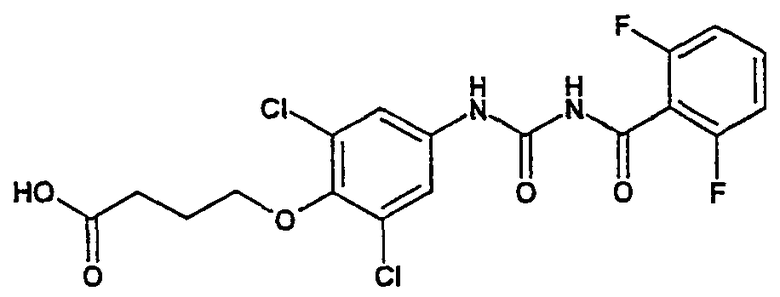
Пример 1:
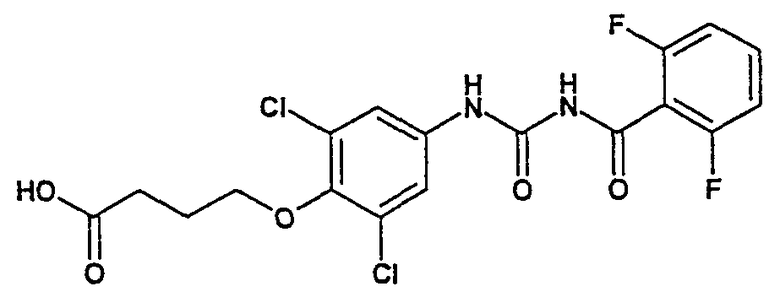
6-{(2,6-дихлор-4-[(2-хлорбензоил)аминокарбамоил]-фенокси}гексановая кислота
а) этиловый эфир 6-(4-ацетиламин-2,6-дихлорфенокси) гексановой кислоты
К раствору, содержащему 15,0 г (68,1 ммоль) N-(3,5-дихлор-4-гидроксифенил)ацетамида в 300 мл ацетона, добавляют 13,3 мл (74,9 ммоль) этилового эфира 6-бромгексановой кислоты и 52,1 г (160 ммоль) карбоната цезия. Суспензию кипятят 8 часов с обратным холодильником. Затем добавляют 600 мл воды, дважды экстрагируют с добавлением каждый раз по 400 мл дихлорметана и с 400 мл MTB-эфира. Объединенные органические фазы промывают водой и концентрируют на ротационном испарителе. Продукт без очистки подается на следующую стадию. Выход сырого продукта: 30 г.
b) 6-(4-ацетиламино-2,6-дихлорфенокси)гексановая кислота
30 г сырого продукта, полученного на стадии a), соединяют с 800 мл 1 М раствора хлорида калия и перемешивают 3 дня при комнатной температуре. Затем добавляют 600 мл воды и добавлением около 80 мл ледяной уксусной кислоты доводят до pH 5,5. Осажденный продукт отсасывают и дважды промывают, используя каждый раз 40 мл воды. Осадок сушат при высоком вакууме и получают 14,6 г желаемого соединения.
c) 6-(4-амино-2,6-дихлорфенокси)гексановая кислота
7,5 г (22,4 ммоль) 6-(4-ацетиламино-2,6-дихлорфенокси)гексановой кислоты добавляют в 140 мл 1 М раствора гидрохлорида калия в смешанном растворителе метанол-вода (3:1) и кипятят в течение ночи с обратным холодильником. Метанол удаляют на ротационном испарителе, остаток разбавляют водой в количестве около 30 мл и подкисляют ледяной уксусной кислотой до pH 5. Смесь перемешивают в течение 30 минут в ледяной бане и затем отсасывают. Сырой продукт разделяют на хроматографической колонне с применением смеси н-гептан/этилацетат = 1/1 и получают 4,3 г (14,7 ммоль, 66%) желаемого продукта.
d) 6-{2,6-дихлор-4-[(2-хлорбензоил)аминокарбамоил]фенокси}гексановая кислота
К суспензии 10,0 г (34,2 ммоль) 6-(4-амино-2,6-дихлорфенокси)гексановой кислоты в 700 мл осушенного ацетонитрила в атмосфере инертного газа при комнатной температуре добавляют раствор 7,5 г (41,1 ммоль) 2-хлорбензоилизоцианата в 300 мл ацетонитрила. Кипятят в течение 2 часов с обратным холодильником и охлаждают до комнатной температуры. Образовавшийся осадок отсасывают и промывают 50 мл ацетонитрила. Остаток размешивают с 100 мл метанола, отсасывают, промывают с небольшим количеством метанола и сушат в течение ночи при 40°C под вакуумом. Получают 13,7 г (28,9 ммоль, 85%) желаемого продукта. Температура плавления: 171-173°C.
Изобретение относится к новым производным ацилфенилмочевины формулы (I), а также их физиологически приемлемым солям, обладающим свойствами ингибиторов гликогенфосфорилазы. Соединения могут найти применение для получения фармацевтической композиции, пригодной для снижения уровня сахара в крови и для лечения диабета типа II. В соединении формулы (I)
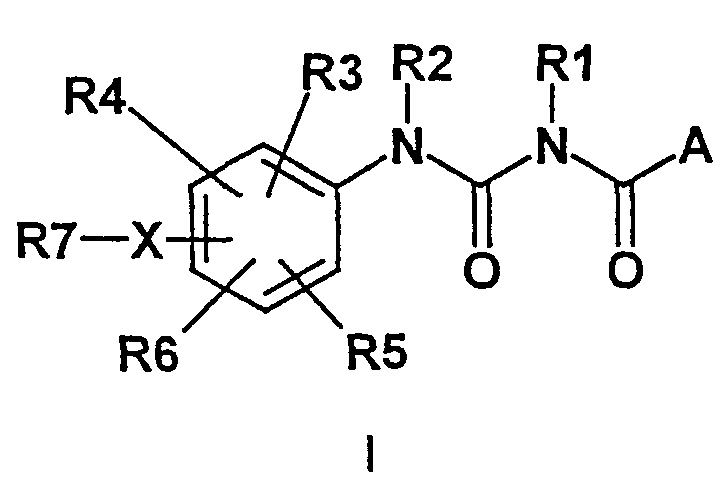
A означает фенил, причем фенильный остаток может быть вплоть до трехкратно замещен F, Cl, Br, CF3, NO2, O-(C1-C6)-алкилом, SO2-(C1-C6)-алкилом, (C1-C6)-алкилом,СООН; R1 означает H, (C1-C6)-алкил; R2 означает H, (C1-C6)-алкил,CO-(C1-C6)-алкил; R3, R4, R5, R6 независимо друг от друга означают H, F, Cl, Br, O-(C1-C6)-алкил, (C1-C6)-алкил, (C3-C7)-циклоалкил, COOH, COO(C1-C6)-алкил; X означает O, S; R7 означает (C1-C10)-алкилен-COOH, (C1-C10)-алкилен-COO-(C1-C6)-алкил, (C1-C10)-алкилен-NH2, (C1-C10)-алкилен-NH(C1-C6)-алкил, (C1-C10)-алкилен-N[(C1-C6)-алкил]2, (C1-C10)-алкилен-B; B означает пиперидинил или фурил. Изобретение также относится к фармацевтической композиции и к способу получения фармацевтической композиции.3 н. и 4 з.п. ф-лы, 2 табл.
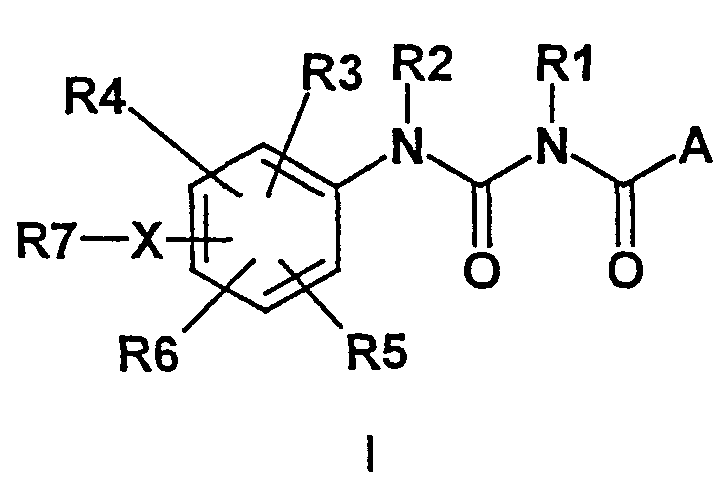
где A означает фенил, причем фенильный остаток может быть вплоть до трехкратно замещен F, Cl, Br, CF3, NO2, O-(C1-C6)-алкилом, SO2-(C1-C6)-алкилом, (C1-C6)-алкилом, СООН;
R1 означает H, (C1-C6)-алкил;
R2 означает H, (C1-C6)-алкил,CO-(C1-C6)-алкил;
R3, R4, R5, R6 независимо друг от друга означают H, F, Cl, Br, O-(C1-C6)-алкил, (C1-C6)-алкил, (C3-C7)-циклоалкил, COOH, COO(C1-C6)-алкил;
X означает O, S;
R7 означает (C1-C10)-алкилен-COOH, (C1-C10)-алкилен-COO-(C1-C6)-алкил, (C1-C10)-алкилен-NH2, (C1-C10)-алкилен-NH(C1-C6)-алкил, (C1-C10)-алкилен-N[(C1-C6)-алкил]2, (C1-C10)-алкилен-B;
B означает пиперидинил или фурил;
а также их физиологически приемлемые соли,
при этом исключаются соединения формулы
а также соединения формулы I, где остатки одновременно означают
A-фенил;
X-O;
R1-H;
R7-(C1-C4)-алкил-B;
B-(C3-C7)-циклоалкил, гетероарил.
A означает фенил, причем фенильный остаток может быть вплоть до трехкратно замещен F, Cl, Br, O-(C1-C6)-алкилом,
R1 означает H, (C1-C6)-алкил;
R2 означает H, (C1-C6)-алкил,CO-(C1-C6)-алкил;
R3, R4, R5, R6 независимо друг от друга означают H, F, Cl, O-(C1-C6)-алкил, (C1-C6)-алкил, COO(C1-C6)-алкил;
X означает O;
R7 означает (C1-C10)-алкилен-COOH, (C6-C10)-алкилен-COO-(C1-C6)-алкил;
а также их физиологически приемлемые соли, при этом исключается соединение формулы
| ПРОИЗВОДНЫЕ ТРИАЗИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, АНТИПРОТОЗОЙНАЯ КОМПОЗИЦИЯ, ДОБАВКА В ПИЩУ ЖИВОТНЫХ, СПОСОБ ИНГИБИРОВАНИЯ ПРОТОЗОИ У ЖИВОТНЫХ | 1994 |
|
RU2146674C1 |
Авторы
Даты
2006-03-10—Публикация
2001-05-26—Подача