Изобретение относится к клинической медицине, в частности к лабораторной диагностике, и может быть использовано для выбора тактики лечения больных с нарушением пуринового обмена.
В настоящее время для выбора тактики лечения больных с нарушением пуринового обмена необходимо проведение следующих исследований:
1. Исследование концентрации мочевой кислоты в крови и количества мочевой кислоты в суточной моче с расчетом клиренса мочевой кислоты [1, 4].
2. Определение концентрации мочевины и креатинина в крови и количества креатинина в суточной моче [1, 2, 3, 4].
3. Анализ суточной мочи по методу Зимницкого, позволяющий оценить концентрационную способность почек, включающий сбор суточной мочи каждые три часа (с 6 до 9 часов, с 9 до 12 часов, с 12 до 15 часов, с 15 до 18 часов, с 18 до 21 часа, с 21 до 24 часов, с 24 до 3 часов, с 3 до 6 часов) в отдельную посуду в течение суток при сохранении обычного пищевого и питьевого режима. При этом определяются суточный диурез, составляющий в норме 67-75% от количества выпитой жидкости, дневной диурез (от 6 до 18 часов), составляющий в норме 65-80% от количества мочи, выделенной за сутки, и колебания удельного веса мочи в каждой 3-часовой порции мочи в течение суток (в норме от 1005 до 1025) [1, 2, 6, 7].
4. Определение в моче рН [1, 2, 4].
5. Определение в моче суточной протеинурии [2, 3].
В монографии Э.Г.Пихлака "Подагра" [1] подробно рассматриваются методы лабораторной диагностики у больных подагрой, на основании которых определяют тактику лечения больных, что в целом является наиболее близким к предлагаемому способу и выбрано нами в качестве прототипа.
Используемая в настоящее время практика проведения лабораторного обследования больных, на основании которого осуществляют оценку состояния больного и выбор оптимальной схемы лечения, предполагает последовательное определение показателей, что занимает не одни сутки как при амбулаторном обследовании, так и в клинике. Однако поскольку урикемия и суточная урикозурия зависят от целого ряда причин (особенности питания и количество потребляемой жидкости, погодные условия, физические нагрузки, рН крови и мочи и др.), то расчет фракционного клиренса (который отражает способность почек к канальцевому транспорту мочевой кислоты и представляет собой отношение клиренсов мочевой кислоты и креатинина) становится корректным только тогда, когда клиренс мочевой кислоты и клиренс креатинина определяются в один день. Кроме этого, проведение указанных исследований в течение нескольких суток ведет к отсрочке получения данных врачом и как следствие задержке постановки диагноза, требует от больного больших затрат времени и определенных экономических издержек.
У больных с нарушением пуринового обмена целесообразно определять концентрацию кальция и фосфора в крови и в суточной моче, так как повышенная концентрация кальция и/или фосфора в суточной моче способствует образованию микрозародышей кристаллов этих соединений, которые, в свою очередь, могут вызывать образование и рост кристаллов кальция, фосфора, мочевой кислоты, а также и кристаллов смешанного состава. Также необходимо отметить, что периодически возникающие повышенные выделения с мочой кальция и фосфора встречаются у больных подагрой и входят в симптомокомплекс, получивший название "подагрического цикла" [1].
У больных подагрой также целесообразно определять связывающую способность альбумина. Повышение связывающей способности является фактором, увеличивающим растворимость уратов и тем самым препятствующим кристаллообразованию [8].
Определение количества креатинина в суточной моче дает возможность проверить полноту сбора суточной мочи, особенно при проведении серийных исследований у одного и того же больного [5].
Настоящее изобретение направлено на повышение эффективности выявления патологических изменений у больных с нарушением пуринового обмена и выбора оптимальной схемы лечения. Нами были проанализированы выписные эпикризы 126 больных подагрой, полученные из 32 медицинских учреждений. Ни в одном из случаев лабораторное обследование не было проведено в виде такого комплекса, который является основой предложенного нами метода выбора тактики лечения больных с нарушениями пуринового обмена.
Способ заключается в том, что выбор тактики лечения больного осуществляют на основании данных, полученных в результате лабораторного обследования, при котором указанные выше исследования проводятся одновременно в течение суток, при этом непосредственно после завершения сбора последней порции суточной мочи, натощак производят забор крови для биохимического анализа, в каждой порции мочи определяют рН, белок и относительную плотность, после чего порции объединяют и в общем объеме мочи определяют концентрацию и количество мочевой кислоты, креатинина и суточную протеинурию, рассчитывают клиренсы мочевой кислоты и креатинина и фракционный клиренс мочевой кислоты.
Такое лабораторное обследование позволяет подобрать оптимальную тактику лечения и, в первую очередь, решить вопрос о возможности проведения базисной терапии, включающей назначение аллопуринола. При выявлении повышения уровня креатинина и мочевины в крови на фоне приема аллопуринола делают вывод о нецелесообразности его использования. При выявлении нарушений пуринового обмена, включающих высокую концентрацию мочевой кислоты в моче при низком суточном диурезе, рекомендуют расширение питьевого режима. При выявлении нарушений пуринового обмена, включающих изменение реакции мочи в кислую сторону, назначают ощелачивающие средства. При этом в зависимости от показателей рН, определяемых в разных порциях мочи в течение суток, ощелачивающие средства могут быть назначены с использованием принципов хронотерапии. При выявлении выраженных нарушений пуринового обмена и тяжелой сопутствующей патологии проводят экстракорпоральную терапию. В зависимости от показаний и общего состояния больного может быть назначено проведение плазмафереза или других видов экстракорпоральной терапии.
Лабораторное обследование целесообразно проводить как на обычном пищевом режиме, так и после трехдневной низкопуриновой диеты.
Проведение повторного анализа на фоне низкопуриновой диеты, с одной стороны, открывает дополнительные возможности выявления метаболических нарушений у больного, а с другой стороны, определенное дублирование предыдущих результатов резко снижает вероятность получения ошибочных данных (неполный сбор больным суточной мочи, плохо обработанная посуда для сбора мочи, ошибки, возникающие при проведении лабораторных исследований, и т.д.).
При использовании предлагаемого способа возможно расширение набора исследуемых показателей, включенных в комплекс лабораторного обследования. Определение концентрации и количества мочевой кислоты в каждой трехчасовой порции мочи позволяет выявлять особенности суточного ритма выделения мочевой кислоты и на этом основании при выборе тактики лечения использовать принципы хронотерапии. Определение концентрации кальция и фосфора в крови и их количества в суточной моче открывает дополнительные возможности в лечении смешанных по составу мочевых конкрементов. Так, при выявлении гиперурикозурии на фоне высокой концентрации мочевой кислоты в моче, низкого рН мочи, гиперкальциурии целесообразно проведение дополнительных профилактических мероприятий, направленных на уменьшение вероятности появления в почках камней смешанного состава.
Определение связывающей способности альбумина у больных подагрой позволяет объективизировать контроль за динамикой заболевания, оценивать эффективность действия нестероидных противовоспалительных препаратов и экстракорпоральных методов лечения.
Необходима определенная подготовка больного к сбору суточной мочи. Больному выдается 8 пронумерованных чистых, сухих, нестерильных банок, с плотно закрывающимися крышками и прилагается памятка по методике сбора мочи. Предлагается перед сбором мочи проведение тщательного туалета наружных половых органов. Отмечается важность хранения мочи в темном и прохладном месте.
На основании результатов проведенных лабораторных исследований уточняется характер поражения и решается вопрос о тактике ведения больного. В дальнейшем осуществляется лабораторный контроль за его лечением.
Иллюстрациями выбора наиболее оптимальной схемы лечения на основании комплексного лабораторного обследования больных с нарушением пуринового обмена служат следующие клинические примеры.
Пример №1. Больной Г-в, 72 лет, находился на стационарном лечении с диагнозом:
подагра. Хронический подагрический полиартрит. Тофус с формированием свищевого хода. Подагрическая нефропатия: киста левой почки, уратовый уролитиаз, артериальная гипертензия.
Поступил в клинику с жалобами на боли в I плюснефаланговых суставах с обеих сторон, больше справа, усиливающиеся при движении, припухлость указанных суставов, покраснение кожи над ними, значительную боль и припухлость в области II пальца правой стопы, гиперемию кожи над пальцем и наличие белого содержимого, просвечивающегося через кожу в этой области, ноющие боли в обоих голеностопных суставах.
Больным себя считает с 1990 года, когда впервые в возрасте 60 лет, после обильного употребления мясной пищи появилась резкая боль в области I плюснефалангового сустава справа, припухлость его. Кожа над суставом стала горячей на ощупь, покраснела, а через несколько часов приобрела синюшно-багровую окраску. Диагностирована подагра, назначен вольтарен, на фоне приема которого приступ артрита был купирован полностью через 5 дней. В дальнейшем приступы артрита возникали 1-2 раза в год, провоцировались приемом алкоголя (даже в небольших количествах), обильным приемом мясной пищи, переохлаждением. Постепенно в процесс вовлекались I плюснефаланговый сустав слева, голеностопные, коленные, локтевые суставы. Лечился амбулаторно, назначали реопирин, вольтарен, индометацин. Прием нестероидных противовоспалительных препаратов позволял купировать артрит в течение 10-14 дней. С 1995 года стало повышаться АД, максимально до 170/110 мм рт.ст., гипотензивные препараты принимал нерегулярно. С 1999 года изменился характер течения артрита - боли в суставах не проходили полностью и обострения уже не достигали прежней интенсивности. В 2001 году впервые рекомендован прием аллопуринола. Аллопуринол принимал в течение месяца, затем прекратил из-за развития аллергического дерматита.
Причиной обращения послужило обострение артрита после переохлаждения.
Состояние при поступлении удовлетворительное. Повышенного питания. Отмечается дефигурация I плюснефаланговых и голеностопных суставов. Кожа над плюснефаланговыми суставами гиперемирована, горячая на ощупь. Отмечается дефигурация дистального межфалангового сустава II пальца правой стопы за счет экссудативных явлений, кожа над пальцем горячая на ощупь, гиперемирована, через кожу просвечиваются белые массы, периодически выделяющиеся через свищевой ход.
В легких дыхание везикулярное, хрипов нет, ЧДД 16 в минуту.
Границы относительной сердечной тупости расширены влево на 2 см. Тоны сердца ритмичные, приглушены, акцент II тона на аорте, ЧСС 56 в минуту, АД 160/100 мм рт.ст.
Общий клинический анализ крови: гемоглобин 138 г/л, лейкоциты 8,5·109/л, палочкоядерные нейтрофилы 4%, сегментоядерные нейтрофилы 56%, эозинофилы 1%, лимфоциты 30%, моноциты 9%, СОЭ 32 мм/час.
Общий анализ мочи: относительная плотность 1012, реакция кислая, белок 0,033 г/л, лейкоциты 2-4 в поле зрения, соли - ураты.
Биохимический анализ крови: мочевина 9,2 ммоль/л, креатинин 0,134 ммоль/л, холестерин 5,4 ммоль/л, триглицериды 2,28 ммоль/л, β-липопротеиды 61 оптич.ед., общий белок 70 г/л, альбумин 50%, глобулины: α1 1,3%, α2 2,17%, β 10%, γ 20%, ЦИК - 196 усл.ед., МСМ 0,42 оптич.ед.
На ЭКГ - синусовый ритм, отклонение электрической оси сердца влево. Признаки гипертрофии левого желудочка.
Динамическая сцинтиграфия почек: левая почка - инд. 43,3%, Tmax 6,7 мин, T1/2 22,3 мин, правая почка - инд. 56,7%, Тmax 4,9 мин, Т1/2 22,7 мин.
Рентгенографическое исследование суставов: стопы - в головках первых плюсневых костей и проксимальных фалангах с обеих сторон имеются кистевидные просветления, краевые узуры (справа более трети суставной поверхности), сужение суставной щели. Уплотнение мягких тканей в области I плюснефалангового сустава справа; коленные суставы - сужение суставной щели, краевые остеофиты, слева - увеличение мягких тканей.
УЗИ почек: правая почка расположена ниже обычного на 4 см. Форма почек обычная. Размеры: правая - 104·54·58 мм, левая - 96·48·55 мм. Обе почки имеют неровные, мелкобугристые контуры. Паренхима неравномерно (особенно слева) истончена до 8-12 мм, без корково-мозговой дифференциации. Эхогенность ткани повышена, есть мелкие высокоэхогенные включения (солевые кристаллы). Слева в области среднего сегмента медуллярная киста - 2,3 см. ЧЛС не дилатирована. Структура некоторых чашечек высокой эхогенности, видимо, за счет фиброза, нельзя исключить наличие единичных микролитов.
Больной был обследован по предложенному нами способу. Проведено исследование суточного количества мочи. Моча собиралась каждые 3 часа, начиная с 6 часов. По окончании сбора мочи у больного был произведен забор венозной крови. Результаты анализов представлены в таблицах №1(а) и №1(б).
Биохимический анализ крови
Анализ суточного количества мочи
При исследовании суточного количества мочи получены следующие результаты: общее количество 860 мл, дневной диурез 450 мл, ночной диурез 410 мл, минутный диурез 0,6 мл/мин, концентрация мочевой кислоты 4,77 ммоль/л, количество мочевой кислоты 4,1 ммоль/24 час, клиренс мочевой кислоты 5,7 мл/мин, концентрация креатинина 10,5 ммоль/л, количество креатинина 9,03 ммоль/24 час, клиренс креатинина 47,5 мл/мин, суточная протеинурия 0,2 г/24 час. Рассчитанный фракционный клиренс составил 12,0%.
Проведенное исследование предлагаемым способом показало низкий суточный диурез, что свидетельствует о недостаточном питьевом режиме данного пациента. Низкий суточный диурез привел к высокой концентрации мочевой кислоты в суточной моче.
Повторное исследование предложенным методом проведено после пребывания пациента на низкопуриновой диете в течение трех дней. Результаты исследования представлены в таблицах №2(а) и №2(б).
Биохимический анализ крови
Анализ суточного количества мочи
При исследовании суточного количества мочи получены следующие результаты: общее количество 1060 мл, дневной диурез 700 мл, ночной диурез 360 мл, минутный диурез 0,74 мл/мин, концентрация мочевой кислоты 4,39 ммоль/л, количество мочевой кислоты 4,65 ммоль/24 час, клиренс мочевой кислоты 6,58 мл/мин., концентрация креатинина 13,4 ммоль/л, количество креатинина 14,2 ммоль/24 час, клиренс креатинина 72,1 мл/мин, суточная протеинурия 0,18 г/24 час. Рассчитанный фракционный клиренс составил 9,13%.
То есть сохраняется низкое потребление жидкости, что, в свою очередь, ведет к низкому суточному диурезу и высокой концентрации мочевой кислоты в суточной моче. С учетом этого больному рекомендовано расширить питьевой режим до 2,5-3 литров в сутки. Наличие аллергической реакции на аллопуринол в анамнезе не позволило назначить базисную терапию данному пациенту. Лабораторное обследование, проведенное через месяц, показало следующие результаты (см. таблицы №3(а) и 3(б)):
Биохимический анализ крови
Анализ суточного количества мочи
При исследовании суточного количества мочи получены следующие результаты: общее количество 2280 мл, дневной диурез 1670 мл, ночной диурез 610 мл, минутный диурез 1,58 мл/мин, концентрация мочевой кислоты 2,14 ммоль/л, количество мочевой кислоты 4,88 ммоль/24 час, клиренс мочевой кислоты 8,11 мл/мин, концентрация креатинина 6,13 ммоль/л, количество креатинина 14,0 ммоль/24 час, клиренс креатинина 76,4 мл/мин. Рассчитанный фракционный клиренс составил 10,6%.
Как видно из результатов анализов, расширение питьевого режима привело к значительному (более чем в два раза) росту суточного диуреза, в результате чего отмечена нормализация уровня урикемии, снижение концентрации мочевой кислоты в суточной моче (более чем в два раза) на фоне повышения ее клиренса, отсутствие протеинурии. При повторном обследовании через 2 месяца уровень мочевой кислоты в крови оставался на верхней границе нормы. На этом фоне отмечено улучшение клинической картины - исчезли приступы артрита, значительно уменьшился в размерах тофус в области II пальца правой стопы, закрылся тофусный свищ. Больной вновь начал принимать аллопуринол, аллергической реакции не последовало.
Таким образом, выбранная на основании комплексного лабораторного обследования тактика ведения больного, заключавшаяся на данном этапе в расширении питьевого режима, привела к значительному улучшению состояния больного.
Пример №2. Больной К-й, 67 лет, инвалид Великой Отечественной войны, поступил в клинику с жалобами на боли в обоих голеностопных суставах в покое, усиливающиеся при движении, припухлость указанных суставов; боли в икроножных мышцах, появляющиеся при ходьбе, приблизительно через 100-120 метров, одышку при ходьбе, давящие боли в области сердца при ходьбе.
Больным себя считает с 1961 года, когда впервые в возрасте 37 лет, после обильного приема мясной пищи и алкоголя появилась резкая болезненность и припухлость I плюснефалангового сустава справа, гиперемия кожи над ним. К врачам не обращался, приступ прошел полностью через 5-7 дней. Повторный приступ артрита развился через год после переохлаждения, также с вовлечением правого I плюснефалангового сустава, самостоятельно купировался через 7 дней без приема лекарств. После этого приступы артрита возникали 1-2 раза в год, провоцировались приемом алкоголя и мясной пищи, переохлаждением. Постепенно в процесс вовлекались левый I плюснефаланговый сустав, голеностопные и коленные суставы, приступы становятся более длительными. С 1965 года лечился амбулаторно компрессами с мазью Вишневского и медицинской желчью без существенного эффекта. Диагноза подагры не ставили, соответственно и не получал базисных препаратов. С 1969 года при приступах артрита назначается бутадион. На фоне приема бутадиона приступы артрита купировались за 8-10 дней. В 1975 году во время приступа артрита возникает почечная колика с отхождением конкремента желто-бурого цвета. После этого почечные колики возникают еще дважды: в 1978 и 1984 году. С 1984 года фиксируются постоянные изменения в моче: протеинурия, лейкоцитурия, периодически гематурия. С 1985 года стал мочиться по ночам (2-3 раза), появилось затрудненное мочеиспускание. Урологом диагностирована аденома предстательной железы. С 1982 года отмечается повышение АД, максимально до 170/100 мм рт.ст. Гипотензивные препараты принимал нерегулярно, пользовался раунатином, адельфаном, коринфаром. С 1985 года стал замечать зябкость ног, боли в икроножных мышцах при ходьбе. Первоначально боли появлялись через 500-700 метров. Постепенно проходимое без боли расстояние уменьшалось, с 1990 года боли появлялись уже через 120-150 метров. С 1987 года стал замечать давящие боли в области сердца при ходьбе, а с 1989 появилась одышка при ходьбе. С 1985 года изменяется характер течения артрита: болевые ощущения в суставах сохраняются постоянно, несмотря на прием нестероидных противовоспалительных препаратов, а обострения не достигают прежней интенсивности. Тогда же отметил появление подкожных образований над локтевыми суставами величиной с вишню. Последнее ухудшение самочувствия с весны 1990 года, когда отметил усиление болей в голеностопных суставах, усиление болей в икроножных мышцах при ходьбе, снижение толерантности к физической нагрузке. Лечился стационарно, проводилась терапия нестероидными противовоспалительными препаратами, сосудистыми препаратами, однако эффект был непродолжительный. С августа 1990 года вновь отметил усиление болей в суставах. Самостоятельно принимал нестероидные противовоспалительные препараты в максимальных дозах, однако полностью купировать артрит не удалось.
Из анамнеза следует отметить частое обильное употребление мясной пищи и алкогольных напитков, осколочное ранение левой голени во время Великой Отечественной войны.
Состояние при поступлении средней тяжести. Отмечается дефигурация обоих голеностопных суставов за счет экссудативных и пролиферативных изменений. Пальпация суставов умеренно болезненна, имеется болевое ограничение движений. Отмечается деформация обеих стоп. Над обоими локтевыми суставами имеются тофусы величиной с грецкий орех, мелкие тофусы отмечаются на обеих ушных раковинах.
Пульсация на a. dorsalis pedis снижена, больше слева. Отмечается снижение пульсации на подколенной артерии слева.
Границы относительной сердечной тупости расширены влево на 2 см. Тоны сердца ритмичные, приглушены, акцент 2 тона на аорте. ЧСС 96 в минуту, АД 150/100 мм рт.ст.
Живот мягкий, безболезненный. Печень выступает на 2 см из-под края реберной дуги. Отеков нет.
В общем клиническом анализе крови: гемоглобин 150 г/л, лейкоциты 8,6·109/л, палочкоядерные нейтрофилы 1%, сегментоядерные нейтрофилы 66%, эозинофилы 2%, лимфоциты 23%, моноциты 8%, СОЭ 44 мм/час.
Биохимический анализ крови: мочевина 8,4 ммоль/л, протромбиновый индекс 91%, общий белок 81,7 г/л, альбумин 48%, глобулины: α1 1,5%, α2 15%, β 12%, γ 20%, фибриноген 9,1 г/л, СРБ 3+, холестерин 6,2 ммоль/л, триглицериды 2,32 ммоль/л, β-липопротеиды 62 оптич.ед.
Общий анализ мочи: относительная плотность 1010, реакция кислая, белок 0,29 г/л, лейкоциты 18-20 в поле зрения, эритроциты 2-3 в поле зрения, цилиндры гиалиновые 0-1 в поле зрения, соли - ураты.
Результаты предложенного способа лабораторного обследования представлены в таблицах №4(а) и №4(б).
Биохимический анализ крови
Анализ суточного количества мочи
При исследовании суточного количества мочи получены следующие результаты: общее количество 2030 мл, дневной диурез 750 мл, ночной диурез 1280 мл, минутный диурез 1,41 мл/мин, концентрация мочевой кислоты 1,88 ммоль/л, количество мочевой кислоты 3,82 ммоль/24 час, клиренс мочевой кислоты 6,16 мл/мин, концентрация креатинина 6,09 ммоль/л, количество креатинина 12,36 ммоль/24 час, клиренс креатинина 78,05 мл/мин. Рассчитанный фракционный клиренс составил 7,90%.
Рентгенография грудной клетки: эмфизема легких, умеренно выраженный пневмосклероз. Сердце расширено в поперечнике за счет левого желудочка. Аорта расширена, уплотнена.
ЭКГ: синусовый ритм, отклонение электрической оси сердца влево. Неполная блокада правой ножки пучка Гиса. Признаки гипертрофии левого желудочка. Дистрофические изменения миокарда.
Радиоизотопная ренография: левая почка - Тmax 7,5 мин, T1/2 14 мин; правая почка - Тmax 9 мин, T1/2 более 22 мин.
УЗИ: печень 12 см в поперечнике, структура ткани однородна. Желчный пузырь средних размеров, контуры ровные, стенки утолщены, в полости - конкременты. Поджелудочная железа - контуры ровные, размеры обычные, ткань железы однородной структуры. Почки с обеих сторон обычных размеров, контуры ровные. ЧЛС расширена, деформирована с обеих сторон. Справа конкрементов нет. Слева - в верхнем полюсе киста 1,0×0,9 см, в нижнем полюсе конкремент - 0,3×0,2 см в диаметре.
Уролог: доброкачественная гиперплазия предстательной железы I-II степени. Мочекаменная болезнь. Хронический пиелонефрит.
На основании данных обследования был впервые поставлен диагноз: "Подагра, тяжелое течение. Хронический подагрический полиартрит, обострение. Стадия III. Тофусы. Подагрическая нефропатия: уратовый уролитиаз, артериальная гипертензия. Вторичный деформирующий остеоартроз, ФН-III. ИБС. Стенокардия ФК-III. Атеросклеротический кардиосклероз. Н-II. Облитерирующий атеросклероз сосудов нижних конечностей. Хронический калькулезный холецистит. Ожирение II. Хронический пиелонефрит. Аденома предстательной железы".
Учитывая полученные результаты лабораторного обследования, отсутствие эффекта от предыдущей консервативной терапии в течение 6 месяцев, а также сопутствующую патологию - облитерирующий атеросклероз сосудов нижних конечностей и ИБС, гипер-фибриногенемию, больному решено провести курс экстракорпоральной терапии - плазмаферез (ПА).
Проведено 3 процедуры ПА с общей эксфузией плазмы 2200 мл за курс. Плазмоза-мещение проводилось физиологическим раствором и реополиглюкином.
В результате проведенного лечения состояние улучшилось (см. фиг.1) - купирован артрит, АД стабилизировалось в пределах 140/90-130/90 мм рт.ст., повысилась толерантность к физической нагрузке - увеличилось расстояние, проходимое без болей в ногах, до 230-250 метров, уменьшилась одышка при физической нагрузке, уредились боли в сердце, снизилось содержание фибриногена до 6,1 г/л и холестерина до 5,4 ммоль/л, протромбинового индекса до 80%, ЦИК, МСМ, снизился уровень СРБ, α2- и γ-глобулинов, нормализовалась СОЭ. Отмечено повышение СКФ и суточного диуреза. Улучшились показатели ренограммы: левая почка - Тmax 3,5 мин, T1/2 10 мин; правая почка - Тmax 4,5 мин, T1/2 17,5 мин.
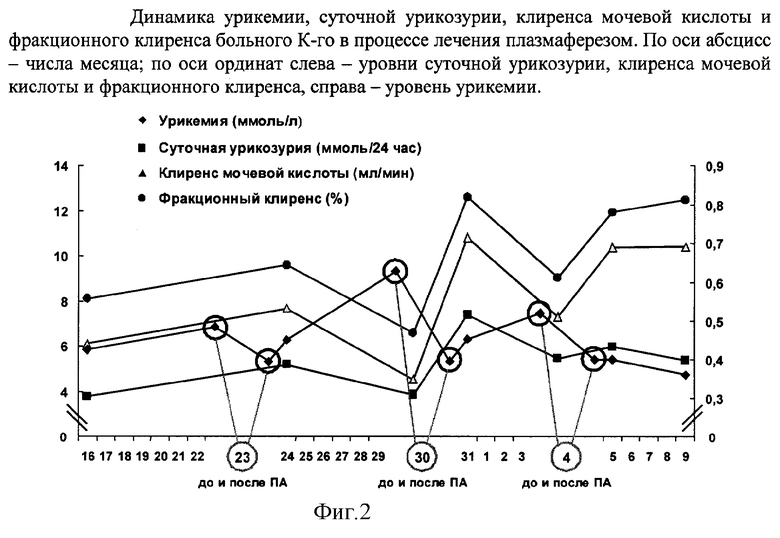
Динамика урикемии, суточной урикозурии, клиренса мочевой кислоты и фракционного клиренса в процессе проведения ПА представлена на фиг.2.
Как видно из фиг.2, отображающей результаты динамического обследования по предложенной методике, после первой процедуры отмечено существенное повышение урикемии (синдром "рикошета"), после второй процедуры повышение не было столь значительным, а после третьей процедуры отмечено снижение уровня мочевой кислоты в крови. В отличие от урикемии отмечался рост урикозурии на фоне проведения ПА и к окончанию курса она в 1,5 раза превышала исходный уровень. Отмечался также существенный рост клиренса мочевой кислоты и фракционного клиренса.
Результаты последнего лабораторного обследования больного предложенным способом представлены в таблицах №5(а) и №5(б).
Биохимический анализ крови
Анализ суточного количества мочи
При исследовании суточного количества мочи получены следующие результаты: общее количество 1410 мл, дневной диурез 1005 мл, ночной диурез 405 мл, минутный диурез 0,98 мл/мин, концентрация мочевой кислоты 3,83 ммоль/л, количество мочевой кислоты 5,40 ммоль/24 час, клиренс мочевой кислоты 10,42 мл/мин, концентрация креатинина 9,07 ммоль/л, количество креатинина 12,79 ммоль/24 час, клиренс креатинина 84,58 мл/мин. Рассчитанный фракционный клиренс составил 12,32%.
Данный клинический пример показывает, как у больных с тяжелым течением подагры и выраженной сопутствующей патологией предлагаемый способ позволяет оперативно выбрать эффективный метод лечения. При этом комплексное лабораторное обследование, проводимое в процессе лечения, дает возможность оценить его действие в динамике (выявлен существенный рост урикозурии, клиренса мочевой кислоты и фракционного клиренса, снижение уровня урикемии).
Пример №3. Больной Ч-й, 53 лет, наблюдается в клинике с диагнозом: подагра. Хронический подагрический полиартрит. Подагрическая нефропатия. Уратовый уролитиаз. Артериальная гипертензия. Вторичный деформирующий полиостеоартроз. ИБС. Атеросклеротический кардиосклероз с нарушением ритма по типу предсердной и желудочковой экстрасистолии H-I. Варикозное расширение вен нижних конечностей. Хроническая венозная недостаточность нижних конечностей.
Начало заболевания относится к 1971 году, когда в возрасте 25 лет после сильного переохлаждения (провалился под лед на зимней рыбалке) появилась боль и отечность голеностопных суставов. Боль усиливалась при малейшем движении. Обратился к участковому терапевту, диагностирован инфекционно-аллергический полиартрит. Лечился антибиотиками, явления артрита купированы приблизительно через 2 недели. После этого чувствовал себя удовлетворительно, боли в суставах не беспокоили. Повторно артрит развился через год, в 1972 году, после погрешности в питании появилась резкая боль и припухлость I плюснефаланговых суставов, гиперемия кожи над ними. Боль усиливалась при малейшем движении, отмечалось повышение температуры тела до субфебрильных цифр. К врачу не обращался. Боли самостоятельно прошли через 2 недели. После чего в течение года чувствовал себя удовлетворительно. В 1975 году ревматологом по месту жительства ставится диагноз "Ревматоидный артрит" и назначается бутадион. В 1976 году после после переохлаждения развивается острый артрит голеностопных и плюснефаланговых суставов. Больной обращается в артрологический центр, где впервые выявляется гиперурикемия, диагностируется подагра и назначаются аллопуринол и нестероидные противовоспалительные препараты (ортофен). Аллопуринол принимал нерегулярно. После этого приступы артрита повторяются до 3-4 раз в год. Постепенно в процесс вовлекаются коленные, локтевые, лучезапястные суставы, а также мелкие суставы кистей. При обострении артрита продолжает принимать нестероидные противовоспалительные препараты. Приблизительно с 1980 года меняется характер течения артрита - приступы уже не достигают прежней интенсивности и боли в суставах не проходят полностью, отмечается постепенное снижение мобильности. С 1987 года отметил появление подкожных образований в области локтевых суставов величиной с фасоль.
С 1988 года больной наблюдается в клинике. При обращении - снижение подвижности (передвигается с помощью костылей) из-за болей в коленных и голеностопных суставах. Отмечается дефигурация коленных, голеностопных суставов за счет экссудативных и пролиферативных явлений, гиперемия и гипертермия кожи над ними. Пальпация указанных суставов болезненна, движения ограничены из-за болей и вторичного остеоартроза. Имеется дефигурация плюснефаланговых суставов с обеих сторон и межфаланговых суставов обеих кистей. Движения в них сохранены, кожные покровы над суставами не изменены, пальпация незначительно болезненна. На разгибательных поверхностях локтевых суставов тофусы размером с фасоль. В области дистальных межфаланговых суставов II пальца справа и IV пальца слева тофусы размером с горошину. Мелкие тофусы на ушных раковинах.
В общем клиническом анализе крови ускорение СОЭ до 45 мм/час, лейкоцитарная формула не изменена.
В биохимическом анализе крови: СРБ 4+, фибриноген 844 мг %, мочевая кислота 0,66 ммоль/л.
УЗИ: почки расположены обычно, контуры ровные, обычных размеров. Паренхима уплотнена. Чашечно-лоханочная система не расширена, в чашечках мелкие кальцинаты.
Термография: повышение термогенной активности над голеностопными, правым коленным и I плюснефаланговым суставами (до 2,5°).
Больному проведено лабораторное исследование предлагаемым нами способом. Результаты анализов представлены в таблицах №6(а) и №6(б).
Биохимический анализ крови
Анализ суточного количества мочи
При исследовании суточного количества мочи получены следующие результаты: общее количество 1340 мл, дневной диурез 810 мл, ночной диурез 530 мл, минутный диурез 0,93 мл/мин, концентрация мочевой кислоты 4,8 ммоль/л, количество мочевой кислоты 6,3 ммоль/24 час, клиренс мочевой кислоты 6,7 мл/мин, концентрация креатинина 9,8 ммоль/л, количество креатинина 13,1 ммоль/24 час, клиренс креатинина 70,7 мл/мин, суточная протеинурия 0,13 г/24 час. Рассчитанный фракционный клиренс составил 9,6%.
Повторное исследование после проведения трехдневной низкопуриновой диеты: табл. №7(а) и №7(б):
Биохимический анализ крови
Анализ суточного количества мочи
При исследовании суточного количества мочи получены следующие результаты: общее количество 1220 мл, дневной диурез 710 мл, ночной диурез 510 мл, минутный диурез 0,8 мл/мин, концентрация мочевой кислоты 4,9 ммоль/л, количество мочевой кислоты 5,9 ммоль/24 час, клиренс мочевой кислоты 7,1 мл/мин, концентрация креатинина 10,0 ммоль/л, количество креатинина 12,2 ммоль/24 час, клиренс креатинина 67,8 мл/мин, суточная протеинурия 0,11 г/24 час. Рассчитанный фракционный клиренс составил 10,6%.
Как видно из результатов анализов, в ночное время отмечается стойко высокая концентрация мочевой кислоты в моче, изменения реакции мочи в кислую сторону. На основании полученных данных больному расширен питьевой режим во второй половине дня и назначены ощелачивающие средства, также во второй половине дня. Через две недели проведено повторное исследование суточного количества мочи, с забором крови после окончания сбора мочи. Результаты исследования представлены в таблицах №8(а) и №8(б).
Биохимический анализ крови
Анализ суточного количества мочи
При исследовании суточного количества мочи получены следующие результаты: общее количество 1730 мл, дневной диурез 860 мл, ночной диурез 870 мл, минутный диурез 1,2 мл/мин, концентрация мочевой кислоты 2,8 ммоль/л, количество мочевой кислоты 4,8 ммоль/24 час, клиренс мочевой кислоты 6,2 мл/мин, концентрация креатинина 8,1 ммоль/л, количество креатинина 14,0 ммоль/24 час, клиренс креатинина 83,1 мл/мин, суточная протеинурия 0,09 г/24 час. Рассчитанный фракционный клиренс составил 7,4%.
При изучении таблиц в порциях №№7 и 8 отмечается сдвиг реакции мочи в щелочную сторону и значительное снижение концентрации мочевой кислоты.
Таким образом, определение у данного больного концентрации мочевой кислоты в каждой трехчасовой порции позволило выявить ее высокий уровень в ночное время и с использованием принципов хронотерапии добиться коррекции этих нарушений. Назначение ощелачивающих средств, которое в данном случае было также проведено с использованием принципов хронотерапии, привело к нормализации рН мочи.
Пример №4. Больной Л-в, 32 лет, находился на лечении с диагнозом: подагра, интермиттирующий подагрический артрит. Ожирение II степени.
Поступил в клинику с жалобами на боли в правом лучезапястном суставе в покое, усиливающиеся при малейшем движении, припухлость его, гиперемию и гипертермию кожи над ним, умеренные боли в I плюснефаланговых и голеностопных суставах при ходьбе, их припухлость.
Больным себя считает с 1993 года, когда после избыточного употребления алкоголя и мясной пищи появилась резкая болезненность в области I плюснефалангового сустава справа, отечность его, покраснение и локальная гипертермия кожи над ним. Явления артрита сопровождались повышением температуры тела до 37,8°С. Боль усиливалась при малейшем движении, в связи с чем подвижность была резко ограничена. Участковым врачом назначен индометацин, на фоне приема которого явления артрита полностью купировались через 5 дней. Первоначально приступы артрита возникали приблизительно 2 раза в год, затем участились до 5-6 раз в год. Постепенно в процесс вовлекались I плюснефаланговый сустав слева, голеностопные и лучезапястные суставы. Приступы артрита провоцировались приемом алкоголя и мясной пищи, переохлаждением. Явления артрита купировались приемом индометацина или ортофена в течение 8-12 дней. Диагноза подагры не ставили, поэтому базисной терапии не получал.
Состояние при поступлении удовлетворительное. Повышенного питания. Отмечается дефигурация правого лучезапястного сустава за счет экссудативных явлений, гиперемия и гипертермия кожи над ним. Имеется болевое ограничение подвижности. Пальпация сустава резко болезненна. Менее выраженная дефигурация за счет экссудативных явлений обоих голеностопных суставов и менее выраженное ограничение подвижности в них.
Тоны сердца ритмичные, ясные, ЧСС 72 в минуту. АД 120/80 мм рт.ст.
Общий клинический анализ крови: гемоглобин 146 г/л, лейкоциты 6,5·109/л, палочкоядерные нейтрофилы 2%, сегментоядерные нейтрофилы 74%, эозинофилы 1%, лимфоциты 19%, моноциты 4%, СОЭ 31 мм/час.
Общий анализ мочи: относительная плотность 1016, реакция кислая, белок и глюкоза отрицательные, лейкоциты 1-2 в поле зрения.
Анализ мочи по Нечипоренко: лейкоциты 250 в 1 мл, эритроциты не обнаружены.
Биохимический анализ крови: мочевина 5,1 ммоль/л, протромбиновый индекс 85%, общий белок 70,0 г/л, альбумин 50%, глобулины: α1 5%, α2 16%, β 12%, γ 17%, СРБ 3+, холестерин 5,4 ммоль/л, триглицериды 2,2 ммоль/л, β-липопротеиды 54 оптич.ед., ЦИК 196,4 усл.ед., МСМ 0,56 оптич.ед.
ЭКГ: синусовый ритм. Преобладание левого желудочка.
УЗИ: печень незначительно увеличена за счет правой доли (157 мм), с ровными контурами. Паренхима однородна, повышенной эхогенности. Билиарная и сосудистая сеть не расширены. V. portae - 10 мм. Желчный пузырь нормальных размеров, стенки тонкие конкрементов нет. Поджелудочная железа нормальных размеров (2,6×1,5×2,0 см), ткань однородна, изоэхогенна. Почки обычного расположения, формы и размеров. Паренхима без структурных изменений. Чашечно-лоханочная система не расширена, без конкрементов. Мочевой пузырь и предстательная железа без особенностей.
Динамическая сцинтиграфия почек: левая почка - инд. 65,5%, Tmax 6,4 мин, T1/2 17,9 мин; правая почка - инд. 34,5%, Тmax 7,2 мин, Тmax 24,4 мин.
УЗ денситометрия: плотность кости значительно снижена, остеопороз (Т=-4,1). Полученные данные УЗ-денситометрии, выявившие остеопороз, явились основанием для исследования и фосфорно-кальциевого обмена. Результаты обследования по предложенному нами способу представлены в таблицах №9(а) и 9(б).
Биохимический анализ крови
Анализ суточного количества мочи
При исследовании суточного количества мочи получены следующие результаты: общее количество 1380 мл, дневной диурез 530 мл, ночной диурез 850 мл, минутный диурез 0,96 мл/мин, концентрация мочевой кислоты 4,21 ммоль/л, количество мочевой кислоты 5,81 ммоль/24 час, клиренс мочевой кислоты 7,77 мл/мин, концентрация креатинина 10,34 ммоль/л, количество креатинина 14,27 ммоль/24 час, клиренс креатинина 74,51 мл/мин, количество фосфора 39,0 ммоль/24 час, количество кальция 7,65 ммоль/24 час, суточная протеинурия 0,14 г/24 час. Рассчитанный фракционный клиренс составил 10,43%.
Полученные с помощью предлагаемого лабораторного обследования данные (гиперурикозурия на фоне высокой концентрации мочевой кислоты в моче, низкий рН мочи, гиперкальциурия) явились основанием для проведения дополнительных профилактических мероприятий, направленных на уменьшение вероятности появления в почках камней смешанного состава.
Пример №5. Больной Ц., 61 года, в течение 7 лет страдает подагрой. Поступил в клинику с жалобами на выраженные боли, отек и гиперемию левого лучезапястного сустава. Боль усиливалась при малейшем движении. В области левого лучезапястного сустава имелся свищ с белым творожистым отделяемым.
Ухудшение самочувствия в течение двух месяцев, когда возник острый артрит указанного сустава. Амбулаторно получал нестероидные противовоспалительные препараты per os и в/м без эффекта. При попытке добавления к терапии аллопуринола появилась и стала нарастать азотемия (креатинин крови 0,15 ммоль/л; мочевина крови 10,4 ммоль/л).
Результаты обследования по предложенному нами способу представлены в таблицах №10(а) и №10(б).
Биохимический анализ крови
Анализ суточного количества мочи
При исследовании суточного количества мочи получены следующие результаты: общее количество 950 мл, дневной диурез 400 мл, ночной диурез 550 мл, минутный диурез 0,66 мл/мин., концентрация мочевой кислоты 2,00 ммоль/л, количество мочевой кислоты 1,90 ммоль/24 час, клиренс мочевой кислоты 1,81 мл/мин, концентрация креатинина 15,02 ммоль/л, количество креатинина 14,27 ммоль/24 час, клиренс креатинина 50,05 мл/мин, суточная протеинурия 0,24 г/24 час. Рассчитанный фракционный клиренс составил 3,63%.
На основании полученных данных, учитывая отсутствие эффекта от предыдущей терапии, а также нарастающую почечную недостаточность, больному решено провести курс ПА. Одновременно были отменены нестероидные противовоспалительные препараты.
Проведено 7 процедур ПА с общей эксфузией плазмы 8900 мл за курс. Плазмозамещение проводилось реополиглюкином, изотоническим раствором хлорида натрия. Уже после двух процедур отмечен положительный эффект - значительно уменьшились боли и отечность левого лучезапястного сустава, увеличился объем движений в суставе.
После курса ПА полностью исчезли боли и отек, закрылся свищ в области пораженного сустава. Отмечена и положительная динамика лабораторных показателей: уменьшилась СОЭ с 55 до 25 мм/час, повысился уровень гемоглобина со 110 до 145 г/л, снизился уровень мочевой кислоты до 0,547 ммоль/л.
Таким образом, проведение экстракорпоральной терапии, назначенной на основании полученных данных о выраженных нарушениях пуринового обмена и нарастающей почечной недостаточности, позволило в короткие сроки добиться улучшения состояния больного.
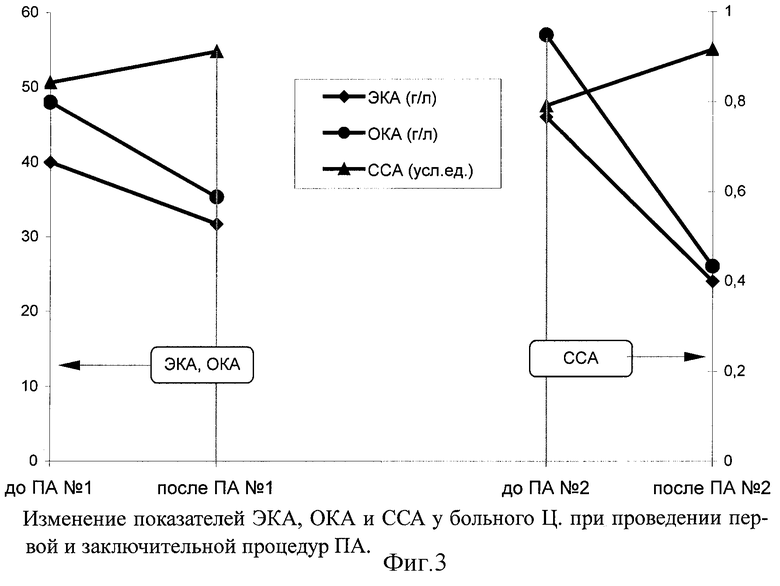
Кроме обследования по предложенной нами методике у больного Ц. была исследована динамика показателей эффективной концентрации альбумина (ЭКА, г/л), общей концентрации альбумина (ОКА, г/л) и связывающей способности альбумина (ССА, усл.ед.) при проведении первой и заключительной процедур ПА. Результаты представлены на фиг.3.
Как видно из фиг.3, проведение каждой процедуры ПА сопровождалось повышением связывающей способности альбумина при одновременном снижении как эффективной, так и общей его концентрации.
Комплексное лабораторное обследование по заявленному способу проведено в динамике у 320 больных с нарушением пуринового обмена как в стационарных, так и в амбулаторных условиях. Установлено, что обследование больных данным методом позволяет существенно улучшить качество диагностики. Это дает возможность подобрать наиболее оптимальные схемы лечения и осуществить необходимый стандартизированный контроль.
ЛИТЕРАТУРА
1. Пихлак Э.Г. Подагра, М., 1970.
2. Нефрология. Руководство для врачей. Под ред. И.Е.Тареевой, М., Медицина, 1992.
3. Справочник "Клинико-диагностическое значение лабораторных показателей" под ред. Долгова В.М., 1995.
4. Wyngaarden J.B,, Kelley W.N. Gout and hypemricemia. New York, Grune and Stratton,1976.
5. "Clinical guide to laboratory tests"; Third Edition. Edited by Norbert W.Tietz. W.B.Saunders Company, 1995.
6. Зимницкий С.С. Введение в функциональную диагностику болезней почек. Клин. мед. Том 5. №1, С.2, 1927.
7. Большая Медицинская Энциклопедия. Изд. 3. Том 8. М., 1978, С.445.
8. Пихлак А.Э, Рыжиков С.Б., Посошкова О.И., Терьянов М.Б., Логачев В.А., Ряпина Ж.Ю. Клиническая значимость определения связывающей способности альбумина у больных подагрой // Альбумин сыворотки крови в клинической медицине. Книга 2 / Под ред. Ю.А.Грызунова и Г.Е.Добрецова. - М.: ГЭОТАР, 1998. - С.371-378.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ ОПТИМАЛЬНОГО ВРЕМЕНИ ИНКУБИРОВАНИЯ ПЛАЗМЫ КРОВИ С СОРБЕНТОМ | 2001 |
|
RU2200027C1 |
| СПОСОБ ОЧИСТКИ ПЛАЗМЫ КРОВИ ОТ МОЧЕВОЙ КИСЛОТЫ, КРЕАТИНИНА И ХОЛЕСТЕРОЛА | 2001 |
|
RU2205036C2 |
| СПОСОБ ЛЕЧЕНИЯ ПОДАГРЫ С ПОМОЩЬЮ ПЛАЗМОСОРБЦИИ | 2001 |
|
RU2219957C2 |
| СПОСОБ ПОДГОТОВКИ И ПРОВЕДЕНИЯ ПЛАЗМАФЕРЕЗА У БОЛЬНЫХ ПОДАГРОЙ | 2001 |
|
RU2218158C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ОПТИМАЛЬНОГО ТИПА СОРБЕНТА И ВРЕМЕНИ СОРБЦИИ ДЛЯ ОЧИСТКИ ОРГАНИЗМА ПРИ ПЛАЗМОСОРБЦИИ | 2001 |
|
RU2188671C1 |
| СПОСОБ ДИАГНОСТИКИ ПОДАГРЫ | 2007 |
|
RU2343842C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ФУНКЦИОНАЛЬНОГО ПОЧЕЧНОГО РЕЗЕРВА | 2006 |
|
RU2308725C1 |
| Способ определения стадий хронической почечной недостаточности | 1986 |
|
SU1413529A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АКТИВНОСТИ ПРОЦЕССА ПРИ НЕФРИТЕ С СОХРАНЕННОЙ ФУНКЦИЕЙ ПОЧЕК | 2002 |
|
RU2214603C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ ХРОНИЧЕСКОЙ БОЛЕЗНЬЮ ПОЧЕК С3-С5 НА ДОДИАЛИЗНОМ ЭТАПЕ, ИСКЛЮЧАЯ ПИЕЛОНЕФРИТЫ, МОЧЕКАМЕННУЮ БОЛЕЗНЬ | 2017 |
|
RU2646467C1 |
Изобретение относится к клинической медицине, в частности к лабораторной диагностике. Для выбора тактики лечения больного проводят комплексное лабораторное обследование, включающее сбор суточной мочи по методу Зимницкого и забор крови для анализа непосредственно после завершения сбора последней порции мочи. В каждой порции мочи определяют рН, белок и относительную плотность, в общем объеме мочи определяют концентрацию и количество мочевой кислоты, креатинина и суточную протеинурию, рассчитывают клиренсы мочевой кислоты и креатинина и фракционный клиренс мочевой кислоты. При выявлении нарушений пуринового обмена, включающих высокую концентрацию мочевой кислоты в моче при низком суточном диурезе, рекомендуют расширение питьевого режима; при изменении реакции мочи в кислую сторону назначают ощелачивающие средства; при выраженных нарушениях пуринового обмена и тяжелой сопутствующей патологии проводят экстракорпоральную терапию. Способ позволяет существенно улучшить качество диагностики и подобрать наиболее оптимальные схемы лечения. 5 з.п. ф-лы, 10 табл., 3 ил.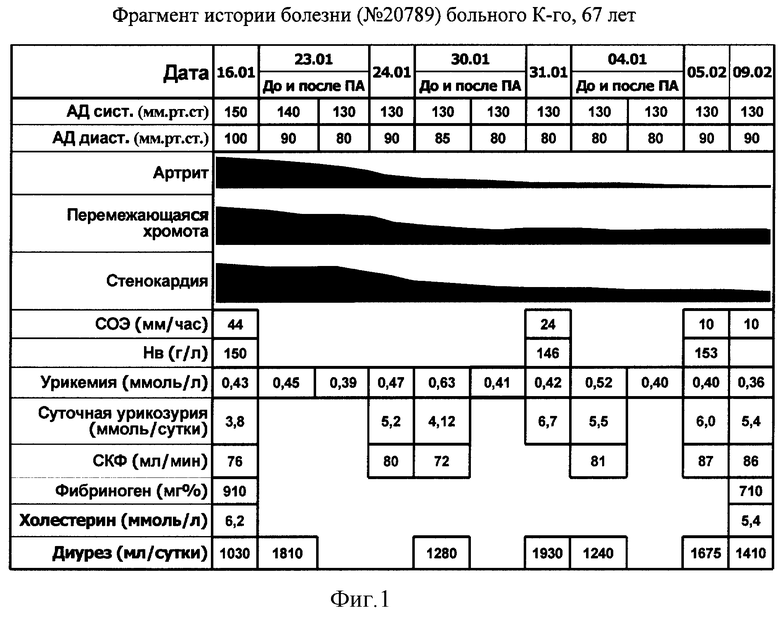
| ПИХЛАК Э.Г | |||
| Подагра | |||
| М., 1970 | |||
| RU 99100269 A, 10.10.2000 | |||
| КУРБАНОВ А.К | |||
| Пуриновый обмен при бронхиальной астме | |||
| Пульмонология, 2000, №2, с.13-19 | |||
| ЛЕБЕДЕВА М.В | |||
| и др | |||
| Микроальбуминурия как один из ранних признаков поражения почек у пациентов с нарушением пуринового обмена | |||
| Терапевт | |||
| Арх | |||
| Предохранительное устройство для паровых котлов, работающих на нефти | 1922 |
|
SU1996A1 |
| МАЛАЯ МЕДИЦИНСКАЯ ЭНЦИКЛОПЕДИЯ/ Гл | |||
| ред. | |||
Авторы
Даты
2006-03-27—Публикация
2003-06-05—Подача