Изобретение относится к медицинской микологии и клинической микробиологии, наиболее эффективно может быть использовано при выделении культур грибов-дерматофитов, например Microsporum canis, Trichophyton verrucosum, Trichophyton mentagrophytes var. gypseum, Trichophyton rubrum, из материала от больных.
Диагностика дерматомикозов проводится с помощью микроскопии и по результатам посевов материала от больного на различные питательные среды. Однако не при всех случаях, даже при соблюдении всех правил забора материала, удается идентифицировать возбудителя [1].
Известен способ выделения дерматофитов, который предусматривает посев материала на поверхность плотной среды Сабуро следующего состава, г/л:
Глюкоза или мальтоза - 40,0;
Пептон - 10,0;
Агар - 18,0-20,0;
Дистиллированная вода - остальное.
Инкубация посевов проводится при температуре 28-30°С в течение 30 дней [2].
Недостатком этого способа является то, что используемая питательная среда не подавляет рост сопутствующей микрофлоры, что затрудняет идентификацию дерматофитов.
Известен способ выделения дерматофитов на плотной среде Сабуро с селективными добавками - пенициллин (20000 ЕД) или стрептомицин (40000 ЕД), гентамицин (0,005 г/л), левомицетин (016 г/л):
Глюкоза или мальтоза - 40,0;
Пептон - 10,0;
Агар - 18,0-20,0;
Дистиллированная вода - остальное.
Инкубация посевов проводится при температуре 28-30°С в течение 30 дней [2].
Антибиотики вносят в среду для подавления роста сопутствующей микрофлоры и устранения таким образом ее антагонистического действия на дерматофиты. Недостатком этого способа является длительность процесса выделения чистой культуры [3].
В патенте [4] описан способ выделения грибов родов Microsporum и Trichophyton из клинического материала на селективной среде Сабуро с добавлением жидкой медицинской желчи, дрожжевого аутолизата и антибиотика из группы фторхинолонов, например ципрофлоксацина, при следующем соотношении компонентов, г/л:
Глюкоза - 40,0;
Пептон - 10,0;
Агар - 18,0-20,0;
Жидкая медицинская желчь - 1,0;
Аутолизат дрожжевой концентрированный - 5,0;
Ципрофлоксацин - 5,0;
Дистиллированная вода - до 1,0 л.
Посев инкубируют при температуре 37°С 5-7 дней и 15 дней при температуре 28-30°С с последующей идентификацией вида колоний.
В патенте [5] описан способ получения хитина и хитозана путем культивирования дерматофитов в жидкой среде, содержащий кератин. Однако доступность нерастворимого в воде кератина недостаточна в случае использования плотных питательных сред. К тому же содержащаяся в среде Сабуро глюкоза тормозит активность кератиназы - фермента, необходимого для усвоения кератина, кроме того, секреция фермента достигает максимальной величины только к 15 суткам инкубации [6].
Наиболее близким к заявляемому способу идентификации дерматофитов, с учетом состава и типа среды для их культивирования, является способ высева материала на плотную среду Сабуро с антибиотиками [2].
Целью изобретения является сокращение сроков выделения культуры грибов-дерматофитов из материала от больного, а также увеличение надежности идентификации дерматофитов.
Изобретение заключается в том, что питательная среда, содержащая глюкозу и микробиологический агар (среда Сабуро), дополнительно содержит гидролизат кератина определенного состава (см. пример 1) при следующих соотношениях ингредиентов, г/л:
Глюкоза - 40,0;
Пептон - 10,0;
Агар - 18,0-20,0;
Гидролизат кератина (в пересчете на сухое вещество) - 10,0-20,0;
Левомицетин - 50000 ЕД;
Дистиллированная вода - остальное.
Питательную среду готовили следующим образом:
в колбу насыпали 18,0-20,0 г мелко размельченного агара, доливали 900 мл дистиллированной воды и через 30 мин прибавляли 40,0 г глюкозы и 10,0 г пептона, после чего кипятили в течение 30 мин и фильтровали. Затем добавляли 40,0-80,0 мл 25% гидролизата кератина, доливали воду до 1,0 л, перемешивали и стерилизовали при давлении 1 атм (120°С) 20 мин. Левомицетин (50000 ЕД) добавляли в среду перед разливом в пробирки.
Посев исследуемого материала проводили на поверхность среды. Инкубацию проводили в течение 4-8 дней при 20-24°С. По характеру роста колоний, цвету и т.д. определяли вид дерматофитов.
Пример 1. Гидролизат кератина получали из куриного пера путем щелочного гидролиза в течение 72 ч при комнатной температуре, после чего гидролизат подвергали диализу против дистиллированной воды до достижения рН 7,0-7,6. Аминокислотный состав гидролизата кератина приведен в таблице 1. Содержание белка по биуретовой реакции в гидролизате - 25,0%.
Пример 2. Чистые культуры грибов дерматофитов М.canis, Т. verrucosum, Т.mentagrophytes var.gypseum, Т.rubrum, T.verrucosum высевали штрихом в чашки Петри на следующие питательные среды: Сабуро с гидролизатом кератина (предлагаемая) состава, г/л:
Глюкоза - 40,0;
Пептон - 10,0;
Агар - 18,0;
Гидролизат кератина - 10,0;
Левомицетин - 50000 ЕД;
Дистиллированная вода - до 1,0 л
и стандартную среду Сабуро, г/л:
Глюкоза или мальтоза - 40,0;
Пептон - 10,0;
Агар - 18,0;
Дистиллированная вода - остальное;
с добавлением левомицетина - 50000 ЕД;
Посевы помещали в термостате при 20°С. С интервалом в 1 сутки визуально отмечали появление и развитие колоний грибов.
Динамика проявления роста и развития грибов представлена в табл.2.
На среде с гидролизатом кератина (предлагаемая среда) рост дерматофитов отмечался на 1-5 сутки, идентификацию проводили на 4-8 день в зависимости от вида гриба. Плеоморфных изменений культур не зафиксировали.
Рост дерматофитов на стандартной среде Сабуро отмечался со 2-х по 7-е сутки инкубации. Культуры дерматофитов возможно было идентифицировать на 5-10 день в зависимости от вида гриба.
Пример 3. Материал от больного (волосы, чешуйки кожи и ногти) помещали в пробирки на следующие питательные среды: Сабуро с гидролизатом кератина, г/л:
Глюкоза - 40,0;
Пептон - 10,0;
Агар - 20,0;
Гидролизат кератина - 20,0;
Левомицетин - 50000 ЕД;
Дистиллированная вода - остальное
и стандартную среду Сабуро. Посевы помещали в термостат при 24°С. С интервалом в 1 сутки визуально отмечали появление и развитие грибов.
Динамика проявления роста и развития грибов представлена в табл.3.
На среде с гидролизатом кератина (предлагаемая среда) рост М.canis, и Т.mentagrophytes var. gypseum отмечался на 1-2 сутки, идентификация была возможна с 4-5 суток, Т.rubrum рост - на 3-4 сутки, идентификация - на 5-7 сутки, рост Т.verrucosum - на 4-5 сутки, идентификация на 7-8 сутки. Плеоморфных изменений культур не зафиксировали.
Рост дерматофитов на стандартной среде Сабуро отмечался с задержкой на 2-3 суток по сравнению с предлагаемой средой.
В ряде случаев не было роста на всех средах в связи с отсутствием фрагментов грибов в материале от больного.
Пример 4. Материал от больного (эпилированные из очага волосы) был помещен в одну пробирку на среду Сабуро, в другую - на предлагаемую среду Сабуро с гидрализатом кератина состава, г/л:
Глюкоза - 40,0;
Пептон - 10,0;
Агар - 18,0;
Гидролизат кератина - 15,0;
Левомицетин - 50000 ЕД;
Дистиллированная вода - остальное.
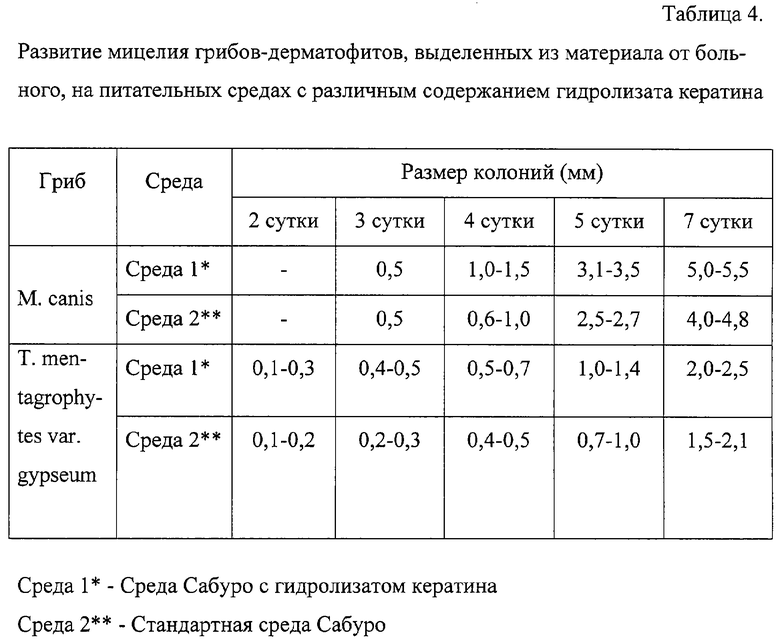
Инкубацию посевов проводили при 22°С. Появление колоний было отмечено примерно в одно время на обеих средах, но развитие колоний значительно быстрее шло на среде Сабуро с гидрализатом кератина, что проявлялось большим размером колоний (табл.4).
Пример 5. Материал от больного (волосы, чешуйки кожи и ногти) помещали в пробирки на среду Сабуро с гидролизатом кератина (предлагаемая), г/л:
Глюкоза - 40,0;
Пептон - 10,0;
Агар - 18,0;
Гидролизат кератина - 5,0; 10,0; 20,0; 30,0 или 40,0;
Левомицетин - 50000 БД;
Дистиллированная вода - остальное
и стандартную среду Сабуро. Посевы помещали в термостат при 24°С. С интервалом в 1 сутки визуально отмечали появление и развитие грибов. Плеоморфных изменений культур не наблюдали.
Результаты, представленные в табл.5, свидетельствуют о том, что содержание гидролизата кератина в питательной среде для высева дерматофитов должно быть больше 10 г/л.
Таким образом, предлагаемый нами способ диагностики дерматомикозов путем высева клинического материала на среду Сабуро с гидролизатом кератина позволяет сокращать сроки выделения и идентификации культур грибов-дерматофитов. Кроме того, при использовании предлагаемой среды не происходит плеоморфных изменений культур. Высев дерматофитов предлагаемым способом позволяет проводить идентификацию для Т.mentagrophytes var.gypseum и М.canis - на 4-5 день, для Т.rubrum - на 5-7 день, для Т.verrucosum - на 7-8 день. В то же время для идентификации дерматофитов по патенту [4] требуется 20-22 дня. Ускоренный рост дерматофитов в случае добавления в среду гидролизата кератина наблюдается также при сравнении со способом их выделения на стандартной среде Сабуро, что позволяет проводить инкубирование при температуре 20-24°С.
Предлагаемая нами среда Сабуро с гидролизатом кератина имеет следующие преимущества: простота приготовления и сокращение сроков выделения и идентификации культур грибов-дерматофитов из материала от больного. Увеличение скорости роста культур дерматофитов происходит при содержании в питательной среде гидролизата кератина выше 10,0 г/л, в то же время повышение содержания гидролизата более 20,0 г/л не приводит к дальнейшему увеличению скорости роста культур и поэтому нецелесообразно.
Источники информации
1. Разнатовский К.И., Родионов А.Н., Котрехова Л.П. Дерматомикозы: Руководство для врачей. - СПб.: Издательский дом СПбМАПО, 2003, 158 с.
2. Кашкин П.Н., Лисин В.В. Практическое руководство по медицинской микологии. Л.: Медицина, 1983.
3. Лещенко В.М. Лабораторная диагностика грибковых заболеваний. М., Медицина, 1977, 127 с.
4. Подхомутникова О.В., Воробьева О.Н., Коняхина И.Г., Лазарева Г.А., Типикина Л.М. Способ выделения дерматофитов из клинического материала. Патент РФ 2181144 (10.04.2002). МПК 7 С 12 N 1/14, С 12 Q 1/04.
5. Nakamura K., Yamada C. Process for producing chitin and chitisan from dermatophyte. WO 9314216, C 12 P 19/26 (22.07.1993).
6. Singh C.J. Characterization of an extracellular keratinase of Trichophyton simii and its role in keratin degradation. - Mycopathologia. - 1997. - V.137. - P.13-16.
| название | год | авторы | номер документа |
|---|---|---|---|
| Питательная среда для культивирования Microsporum canis | 2019 |
|
RU2695675C1 |
| СПОСОБ ВЫДЕЛЕНИЯ ДЕРМАТОФИТОВ ИЗ КЛИНИЧЕСКОГО МАТЕРИАЛА | 2000 |
|
RU2181144C1 |
| СПОСОБ СПЕЦИФИЧЕСКОЙ ДЕТЕКЦИИ Trichophyton mentagrophytes В КЛИНИЧЕСКОМ МАТЕРИАЛЕ ПРИ РАЗЛИЧНЫХ КЛИНИЧЕСКИХ ФОРМАХ ЗАБОЛЕВАНИЯ | 2014 |
|
RU2563619C1 |
| СПОСОБ СПЕЦИФИЧЕСКОЙ ДЕТЕКЦИИ TRICHOPHYTON VERRUCOSUM В КЛИНИЧЕСКОМ МАТЕРИАЛЕ ПРИ РАЗЛИЧНЫХ КЛИНИЧЕСКИХ ФОРМАХ ЗАБОЛЕВАНИЯ | 2014 |
|
RU2562540C1 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВЫРАЩИВАНИЯ МИЦЕЛИАЛЬНЫХ ГРИБОВ-ДЕРМАТОМИЦЕТОВ ИЗ КЛИНИЧЕСКОГО МАТЕРИАЛА | 2013 |
|
RU2527074C1 |
| СЕЛЕКТИВНАЯ ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВЫДЕЛЕНИЯ ВОЗБУДИТЕЛЕЙ ДЕРМАТОФИТОЗОВ | 2020 |
|
RU2745159C1 |
| СПОСОБ СПЕЦИФИЧЕСКОЙ ДЕТЕКЦИИ MICROSPORUM CANIS В КЛИНИЧЕСКОМ МАТЕРИАЛЕ ПРИ РАЗЛИЧНЫХ КЛИНИЧЕСКИХ ФОРМАХ ЗАБОЛЕВАНИЯ | 2014 |
|
RU2558927C1 |
| Способ трихоскопии с использованием искусственных нейронных сетей для диагностики поврежденных спорами дерматофитов волос у кошек | 2022 |
|
RU2796767C1 |
| ШТАММЫ МИЦЕЛИАЛЬНЫХ ГРИБОВ MICROSPORUM CANIS И TRICHOPHYTON MENTAGROPHYTES, ПРЕДНАЗНАЧЕННЫЕ ДЛЯ КОНТРОЛЯ РОСТОВЫХ СВОЙСТВ ПИТАТЕЛЬНЫХ СРЕД | 2020 |
|
RU2741097C1 |
| ШТАММ ГРИБА Eremothecium ashbyi - ПРОДУЦЕНТ ЭФИРНОГО МАСЛА С ЗАПАХОМ СВЕЖИХ ЦВЕТКОВ РОЗЫ | 2014 |
|
RU2567675C1 |
Изобретение относится к медицинской микологии и клинической микробиологии. Диагностику дерматомикозов осуществляют путем высева дерматофитов из клинического материала на плотную селективную среду Сабуро с добавлением антибиотика - левомицетина и гидролизата кератина, полученного из куриного пера. Питательная среда для выделения дерматофитов имеет следующий состав, г/л: глюкоза - 40,0; пептон - 10,0; агар - 18,0-20,0; гидролизат кератина (в пересчете на сухое вещество) - 10,0-20,0; левомицетин - 50000 ЕД; дистиллированная вода - остальное. Посев инкубируют при температуре 22-24°С в течение 4-8 дней с последующей идентификацией вида колоний. Способ наиболее эффективен при выделении из материала от больных культур грибов-дерматофитов, в частности Microsporum canis, Trichophyton vermcosum, Trichophyton mentagrophytes var. gypseum, Trichophyton rubrum. Использование питательной среды с гидролизатом кератина позволяет сократить сроки выделения и идентификации культур грибов-дерматофитов из клинического материала. 2 н.п. ф-лы, 5 табл.
при этом инкубируют посев при температуре 22-24°С в течение 4-8 дней, после чего проводят идентификацию вида колоний.
| Кашкин П.Н | |||
| и др | |||
| Практическое руководство по медицинской микологии | |||
| Л.: Медицина, 1983, с.152-153 | |||
| МИКРОБИОЛОГИЧЕСКАЯ СРЕДА ДЛЯ ВЫДЕЛЕНИЯ TRICHOPHYTON VERRUCOSUM | 2002 |
|
RU2237709C2 |
| СПОСОБ ВЫДЕЛЕНИЯ ДЕРМАТОФИТОВ ИЗ КЛИНИЧЕСКОГО МАТЕРИАЛА | 2000 |
|
RU2181144C1 |
| Асонов Н.Р | |||
| Микробиология | |||
| М.: Колос, 1997, с.248-255 | |||
| Jessup CJ et al | |||
| Antifungal susceptibility testing of dermatophytes: establishing a medium for inducing conidial growth and evaluation of | |||
Авторы
Даты
2006-04-27—Публикация
2004-10-14—Подача