Область техники
Настоящее изобретение относится к области молекулярной биологии, в частности к нуклеотидной последовательности гена, кодирующего цитокин GM-CSF лошади, к содержащим ее экспрессирующим векторам, к ее использованию в качестве адъюванта при вакцинации лошадей и в качестве неспецифического стимулятора иммунитета.
Сущность изобретения
Первое открытие гранулоцит-макрофаг колониестимулирующего фактора (Granulocyte-Macrophage Colony-Stimulating Factor, или GM-CSF) датировано 1977 г. (Burgess A.W. и др., J. Biol. Chem., 252, 1998-2003 (1977)). Речь идет о GM-CSF мыши, выделенном в чистом виде из культуральных супернатантов легких мышей.
Биологические активности GM-CSF были показаны при исследованиях и GM-CSF мыши и человека (Clark S.C. и др., 230, 1229 (1987); Grant S.M. и др., Drugs, 53, 516 (1992)).
GM-CSF принимает участие в различных физиологических процессах (Dy M. в книге "Cytokines" Cavaillon J. - M., 1996, изд. Masson, Париж, Франция, 43-56). В частности, GM-CSF стимулирует продуцирование, развитие и образование колоний гранулоцитов, макрофагов, эозинофилов и мегакариоцитов. GM-CSF индуцирует, в частности, макрофаговую цитотоксичность, стимулирует антителозависимую цитотоксическую активность (ADCC) и вызывает рекрутинг лейкоцитов на уровне зон воспаления.
В настоящее время идентифицированы GM-CSF различных видов животных.
Нуклеотидные последовательности, кодирующие GM-CSF различных видов, как правило имеют длину от 381 до 432 нуклеотидов. Гомология между нуклеотидными последовательностями GM-CSF мыши и человека составляет 69%. Гомология аминокислотных последовательностей составляет 54% (Cantrell М.А. и др., Proc/ Natl. Acad. Sci. USA, 82, 6250-6254 (1985)). Однако, несмотря на высокую гомологию, перекрестной физиологической активности между GM-CSF человека и мыши не обнаружено (Metcalf D. и др., Blood, 67, 37-45 (1986)).
Введение гетерологичного GM-CSF, то есть происходящего от другого, чем обрабатываемый вид, не позволяет достигать оптимального адъювантного действия, в особенности стимуляции активности гемопоэтиновых клеток, и существенного усиления иммунного ответа.
До настоящего времени GM-CSF лошади не был идентифицирован. Однако этот цитокин представляет значительный интерес для использования в терапии и вакцинации в случае лошадей.
Целью изобретения явилось выделение и секвенирование гена GM-CSF лошади. Этот ген был выделен с помощью ПЦР с использованием описанных в примерах олигонуклеотидов.
Длина гена GM-CSF лошади составляет 432 нуклеотида (последовательность №8 и фигура 1) и кодирует белок из 144 аминокислот (последовательность №9 и фигура 1). Кодируемый этим геном белок имеет гомологию по меньшей мере 75% с аминокислотными последовательностями GM-CSF других видов животных.
Следовательно, объектом настоящего изобретения является фрагмент ДНК, кодирующий GM-CSF лошади, например фрагмент, включающий последовательность № 8. Объектом настоящего изобретения также является фрагмент ДНК, включающий эту последовательность или по существу состоящий из нее.
Объектом настоящего изобретения также является фрагмент ДНК, кодирующий аминокислотную последовательность № 9.
Изобретение охватывает гомологичные нуклеотидные последовательности лошади или полученные синтетическим путем, то есть нуклеотидные последовательности, кодирующие белок с функциональной активностью и специфичностью, эквивалентыми таковым у лошадей. Разумеется, сюда входят и нуклеотидные последовательности, возникающие с учетом вырожденности генетического кода. В частности, эквивалентными являются последовательности ДНК, имеющие гомологию выше или равную 90%, предпочтительно 92%, более предпочтительно 95%, с идентифицированной последовательностью № 8.
Объектом настоящего изобретения также являются фрагменты ДНК, которые включают нуклеотидную последовательность, кодирующую GM-CSF лошади, например последовательность № 8, или последовательность, кодирующую аминокислотную последовательность № 9, связанную с нуклеотидной последовательностью, кодирующей по меньшей мере один иммуноген или по меньшей мере один его иммунологически активный фрагмент или по меньшей мере один эпитоп иммуногена. В этом случае фрагмент ДНК не содержит стоп-кодона между последовательностью, кодирующей GM-CSF, и кодирующей иммуноген последовательностью. Например, в случае последовательности № 8 встроенная кодирующая последовательность заканчивается нуклеотидом 432 и не включает стоп-кодона.
Объектом настоящего изобретения также является выделенный белок или фрагмент GM-CSF лошади, например такой, который кодируется нуклеотидной последовательностью № 8 или гомологичными последовательностями, такими, как указаны выше.
Объектом настоящего изобретения также является белок GM-CSF лошади, имеющий аминокислотную последовательность № 9.
Длина GM-CSF лошади составляет 144 аминокислоты. Тем не менее, настоящее изобретение относится также к белкам и их фрагментам, природного или синтетического происхождения, имеющим длину больше, равную или меньше 144 аминокислот, а также к рекомбинантным белкам (имеющим одну или несколько замен, делеций или инсерций) и к слитым белкам, пока их биологическая активность (для общей части с GM-CSF) по существу эквивалентна таковой природного GM-CSF лошади in vivo. В качестве эквивалентных включены аминокислотные последовательности, кодируемые любой из гомологичных нуклеотидных последовательностей, указанных выше.
Объектом настоящего изобретения также является выделение и очистка белка GM-CSF лошади.
Объектом настоящего изобретения также являются экспрессирующие векторы, включающие один из фрагментов ДНК или одну из нуклеотидных последовательностей, указанных выше, в частности ген GM-CSF лошади (последовательность № 8) или ее гомолог, такой, как указанный выше, а также любую нуклеотидную последовательность, кодирующую любую аминокислотную последовательность, такую, как указанная выше. Точно также вектор может, кроме того, включать нуклеотидную последовательность, кодирующую по меньшей мере один иммуноген, или по меньшей мере один его иммунологически активный фрагмент, или по меньшей мере один эпитоп иммуногена, который может необязательно быть ассоциирован путем слияния, как указано выше.
Нуклеотидная последовательность может быть встроена в классические системы экспрессии in vitro, например вирусного происхождения, такие как бакуловирус, размножающийся в клетках насекомых, или клетки прокариотического (например, Escherichia coli) или эукариотического происхождения, в частности дрожжи, предпочтительно Saccharomyces cerevisiae, клетки млекопитающих, предпочтительно клетки хомяка (например, СНО) и клетки лошадей. Изобретение, следовательно, относится также к системам экспрессии, трансформированным последовательностью согласно изобретению, таким образом продуцирующих GM-CSF лошади и их применению в качестве адъюванта при вакцинации и неспецифического стимулятора иммунитета.
Последовательность согласно изобретению предпочтительно встроена в экспрессирующие векторы, обеспечивающие экспрессию in vivo функционального GM-CSF лошади и экспрессию нуклеотидной последовательности, кодирующей по меньшей мере один иммуноген, или по меньшей мере один его иммунологически активный фрагмент, или по меньшей мере один эпитоп иммуногена. Экспрессирующие векторы могут представлять собой плазмидные векторы, вирусные векторы, такие как поксвирусы, например вирус коровьей оспы, вирусы оспы птиц (оспа канареек, куриная оспа), включая видоспецифичные поксвирусы (оспа свиней, оспа енотов и оспа верблюдов), аденовирусы и герпесвирусы, такие как герпесвирус лошадей.
Под термином "плазмида" понимают любую транскрипционную единицу ДНК в виде полинуклеотидной последовательности, включающей последовательность гена GM-CSF лошади и элементы, необходимые для его экспрессии in vivo. Форма плазмиды предпочтительно кольцевая, "суперскрученная" или нет. В рамки настоящего изобретения также входит линейная форма.
Каждая плазмида включает промотор, способный обеспечивать в клетке-хозяине экспрессию встроенного гена. Обычно речь идет о сильном эукариотическом промоторе и, в особенности, о раннем промоторе цитомегаловируса CMV-IE человека или мыши или другого вида, такого как крыса или морская свинка. По большей части выбирают промотор либо вирусного, либо клеточного происхождения. В качестве вирусного промотора, другого, чем CMV-IE, можно указать ранний или поздний промотор вируса SV40 или промотор области LTR вируса саркомы Рауса. Речь может также идти о промоторе вируса, который происходит от гена, например, о присущем гену промоторе. В качестве клеточного промотора можно указать промотор гена цитоскелета, такой как, например, десминовый промотор, или актиновый промотор. Когда в одной и той же плазмиде присутствуют несколько генов, они могут находиться в одной и той же транскрипционной единице или в двух разных транскрипционных единицах.
Плазмиды могут также включать другие элементы регуляции транскрипции, такие как, например, интроны, предпочтительно интрон II гена β-глобина кролика (van Ooyen и др. Science, 206, 337-344 (1979)), сигнальная последовательность белка, кодируемого геном тканевого плазминогенного активатора (tPA; Montgomery и др., Cell. Mol. Biol., 43б 285-292 (1997)), и сигнал полиаденилирования (полиА), предпочтительно сигнал полиаденилирования гена гормона роста быка (bGH) (заявка на патент США А-5122458) или ген β-глобина кролика.
Изобретение относится также к иммуногенным композициям и вакцинам, включающим GM-CSF лошади согласно изобретению и по меньшей мере один иммуногенный или вакцинирующий препарат патогена лошадей, приемлемый в области ветеринарии эксципиент или наполнитель. Понятие "иммуногенный препарат" здесь охватывает любой препарат, способный, при однократном введении лошади, индуцировать иммунный, направленный против рассматриваемого патогена ответ, который усиливается за счет присутствия белка GM-CSF. Речь идет предпочтительно о вакцинном препарате, способном индуцировать эффективную защиту или некоторую степень защиты против патогена, степень защиты, которая увеличивается в присутствии GM-CSF лошади. Иммуногенные и вакцинные препараты, предусматриваемые согласно изобретению, охватывают все известные типы, такие, как инактивированные, ослабленные живые, субъединичные и рекомбинантные вакцины (в которых используется экспрессируюший in vivo вектор, предпочтительно вирусного или плазмидного происхождения). Как было указано выше, GM-CSF может быть добавлен к иммуногенному или вакцинному препарату для получения, в присутствии приемлемого в ветеринарии эксципиента или наполнителя, готовой к употреблению иммуногенной или вакцинной композиции. Можно также предусмотреть сочетание GM-CSF с системой пролонгированного высвобождения, предназначенной для постепенного высвобождения белков.
Согласно более предпочтительному варианту изобретения, однако, предпочтительно экспрессируют GM-CSF in vivo, используя экспрессирующий in vivo вектор, такой, как описанный выше. В этом случае также является предпочтительным, чтобы иммуногенный или вакцинный препарат был также рекомбинантного типа, основанный на использовании экспрессирующего вектора in vivo, такого же или другого типа. Можно также предусмотреть использование одного и того же экспрессирующего in vivo вектора, включающего и экспрессирующего по меньшей мере один иммуноген патогена лошадей и GM-CSF лошадей.
Преимуществами использования GM-CSF при вакцинации является в особенности снижение дозы иммуногена или вектора или используемой ДНК. Более того, у некоторых животных, не реагирующих на введение обычной вакцины, использование GM-CSF позволяет стимулировать иммунный ответ и усилить его до уровня защиты.
Следовательно, настоящее изобретение предпочтительно относится к иммуногенным композициям и вакцинам, включающим:
- экспрессирующий in vivo вектор, содержащий нуклеотидную последовательность, кодирующую GM-CSF лошади, в условиях, позволяющих протекать экспрессии в организме лошади функционального белка GM-CSF;
- по меньшей мере один экспрессирующий in vivo вектор, содержащий по меньшей мере одну нуклеотидную последовательность, кодирующую по меньшей мере один иммуноген лошади, имея в виду, что вектор, или некоторые, или все векторы (когда имеется несколько векторов, кодирующих различные иммуногены) могут представлять собой также вектор GM-CSF (включающий по меньшей мере одну последовательность GM-CSF и иммуногенную последовательность); и
- наполнитель или эксципиент, приемлемый в ветеринарии.
Согласно предпочтительному варианту изобретения, изобретение относится к иммуногенным композициям и вакцинам на основе ДНК, включающим одну плазмиду, кодирующую и экспрессирующую GM-CSF лошади, согласно изобретению, и по меньшей мере одну другую плазмиду, кодирующую и экспрессирующую иммуноген лошади или его иммунологически активный фрагмент, происходящий от этого последнего. Примеры конструкций плазмид, используемых согласно изобретению, которые содержат иммуноген лошади, представлены в Международной заявке на патент WO-A-98/03198. Изобретение относится также к вакцинам на основе ДНК, включающим плазмиду, кодирующую и экспрессирующую одновременно GM-CSF лошади и по меньшей мере один иммуноген лошади.
Изобретение относится ко всем патогенам лошади. В особенности можно назвать: герпесвирус лошади типа 1 или типа 4 (предпочтительно изобретение относится к сочетанию этих двух типов); вирус гриппа лошадей, вирус столбняка; Borrelia burgdorferi; вирусы энцефалитов лошадей Est, Quest, Venezuela; вирус бешенства. Для субъединичных вакцин и рекомбинантных вакцин иммуногены предпочтительно выбирают из группы, состоящей из гликопротеинов gB, gC, gD герпесвируса лошадей типа 1 или типа 4, гемагглютинина (НА) и нуклеопротеина (NP) вируса гриппа лошадей, неполностью единичного фрагмента С столбнячного токсина, белка OspA Borrelia burgdorferi, генов Е2 и С вирусов энцефалитов лошадей Est, Quest, Venezuela; гена G вируса бешенства.
Еще одним объектом настоящего изобретения являются композиции, стимулирующие неспецифический иммунитет, то есть используемые в качестве общего стимулятора иммунитета у лошади. Такие композиции вводят как при наличии, так и в отсутствие явной патологии, обычно независимо от любой вакцины, чтобы усилить иммунную защиту лошади. Такие композиции включают GM-CSF, согласно изобретению, в любых вышеописанных формах - белковой или рекомбинантной, предпочтительно рекомбинантной (экспрессирующий in vivo, вирусный или плазмидный вектор), и наполнитель или эксципиент, приемлемый в ветеринарии. Характеристики этих векторов уже описаны.
Неспецифические стимулирующие композиции и иммуногенные композиции и вакцины согласно изобретению могут также включать один или несколько адъювантов, предпочтительно выбираемых среди таковых, обычно используемых для вакцинации лошадей против рассматриваемого или рассматриваемых патогенов (валентностей). Стимулирующие композиции и иммуногенные композиции и классические (инактивированные, ослабленные живые, субъединичные) вакцины также могут включать в качестве классического адъюванта соединения типа карбомера, оксида алюминия, или могут быть приготовлены в виде эмульсии масло-в-воде. Для стимулирующих композиций и иммуногенных композиций и рекомбинантных вакцин на основе экспрессирующего вирусного вектора предпочтительно использовать эмульсии масло-в-воде.
Согласно одному предпочтительному варианту изобретения, для стимулирующих композиций плазмидного типа и иммуногенных композиций и вакцин плазмидного типа плазмида, кодирующая и экспрессирующая GM-CSF лошади, и плазмида, кодирующая и экспрессирующая по меньшей мере один иммуноген лошадей, а также смеси этих плазмид, могут быть преимущественно получены принципиально новым образом с катионным липидом, содержащим соль четвертичного аммония формулы:
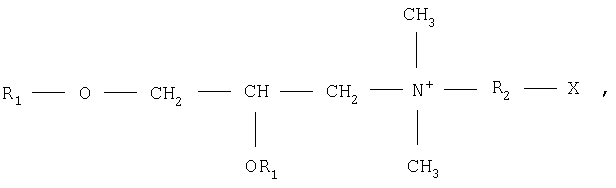
в которой
R1 означает линейный, насыщенный или ненасыщенный алифатический радикал с 12-18 атомами углерода;
R2 означает другой алифатический радикал с 2 или 3 атомами углерода; и
X означает гидроксил или аминогруппу.
Предпочтительно речь идет о DMRIE (N-(2-гидроксиэтил)-N,N-диметил-2,3-бис(тетрадецилокси)-1-пропанаммоний; WO-A-9634109), предпочтительно связанном с нейтральным липидом; DOPE (диолеоилфосфатидилэтаноламин), для образования предпочтительно DMRIE-DOPE. Смесь рекомбинантного вектора с этим адъювантом предпочтительно готовят перед самым употреблением и более предпочтительно перед ее введением животному, оставляют на некоторое время для образования комплекса, например, в течение времени от 10 до 60 минут, предпочтительно около 30 минут.
Когда DOPE присутствует, молярное соотношение DMRIE: DOPE составляет предпочтительно от 95:5 до 5:95, более предпочтительно 1:1.
Массовое соотношение плазмида: адъювант DMRIE или DMRIE-DOPE составляет от 50:1 до 1:10, предпочтительно от 10:1 до 1:5, более предпочтительно от 1:1 до 1:2.
Согласно другому предпочтительному варианту изобретения, для стимулирующих композиций рекомбинантного типа и иммуногенных композиций и вакцин рекомбинантного типа (вирусный или плазмидный вектор) в качестве адъюванта можно использовать полимеры акриловой кислоты или метакриловой кислоты или сополимеры малеинового ангидрида и алкенильного производного. Предпочтительно используют полимеры акриловой или метакриловой кислоты, в особенности сшитые с помощью простых полиалкенильных эфиров сахаров или многоатомных спиртов. Эти соединения известны под названием "карбомер" (Pharmeuropa, том 8, № 2, июнь 1996 г.). Специалист также может сослаться на заявку на патент США А-2909462 (включенную в настоящее описание в качестве ссылки), в которой описываются акриловые полимеры, сшитые с помощью полигидроксилированного соединения, содержащего по меньшей мере 3 гидроксильные группы, предпочтительно не больше 8, причем атомы водорода по меньшей мере трех гидроксильных групп заменены ненасыщенными алифатическими радикалами по меньшей мере с 2 атомами углерода. Предпочтительно радикалы содержат 2-4 атома углерода, как, например, винильные, аллильные и другие группы с этиленовой связью. Ненасыщенные радикалы могут содержать другие заместители, такие как метил. Особенно применимыми являются продукты, выпускаемые под названием Карбопол® (BF Goodrich, Огайо, США). Они сшиты с помощью аллилсахарозы или с помощью аллилпентаэритрита. В качестве примера можно привести Карбопол® 974Р, 934Р и 971Р.
Из сополимеров малеинового ангидрида и алкенильного производного предпочтительны ЕМ® (Monsanto), которые представляют собой линейные или сшитые сополимеры малеинового ангидрида и этилена, например, сшитые с помощью дивинилового эфира. Можно сослаться на J. Fields и др., Nature, 186, 778-780, июнь 1960 г. (включено в настоящее описание в виде ссылки). В плане их структуры, полимеры акриловой или метакриловой кислоты и ЕМА® образованы предпочтительно основными звеньями следующей формулы:
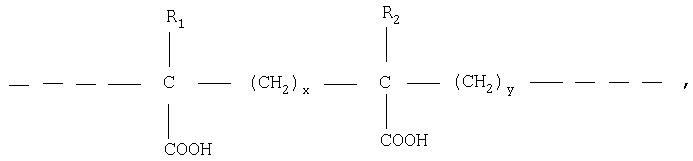
в которой:
R1 и R2, одинаковые или разные, означают Н или СН3;
х означает 0 или 1, предпочтительно х=1;
у означает 1 или 2;
причем (х+у)=2.
Для ЕМА® х=0 и у=2. Для карбомеров (х+у)=1.
Диссоциация этих полимеров в воде приводит к кислому раствору, который нужно нейтрализовать, предпочтительно вплоть до физиологических значений рН, для получения адъювантного раствора, в который и будет включена вакцина. Карбоксильные группы полимера тогда частично находятся в форме COO-.
Предпочтительно получают раствор карбомера или ЕМА® в дистиллированной воде, предпочтительно в присутствии хлорида натрия, причем полученный раствор имеет кислое значение рН. Раствор карбомера разводят раствором NaCl, предпочтительно физиологическим раствором (9 г/л NaCl), в один или несколько приемов, с одновременной или последующей нейтрализацией (рН от 7,3 до 7,4), предпочтительно с помощью NaOH. Полученный раствор с физиологическим значением рН используют для смешения с иммуногенным или вакцинным препаратом, предпочтительно сохраняемым в лиофилизированной, жидкой или замороженной форме.
Концентрация полимера в конечной вакцинной композиции составляет 0,01-2% масса/объем, более предпочтительно 0,06-1% масса/объем, предпочтительно 0,1-0,6% масса/объем.
Другим объектом изобретения является способ стимуляции иммунитета, и/или иммунизации, и/или вакцинации непарнокопытных, согласно которому непарнокопытным, и в частности лошадям, вводят стимулирующую, иммуногенную и/или вакцинную композицию согласно изобретению. Введение предпочтительно осуществляют парентерально, и в частности внутримышечно, внутрикожно или подкожно. Композицию вводят один или несколько раз. В частности, в случае вакцинации, введение осуществляют каждый раз вместе с вакциной.
Количество ДНК, используемое в стимулирующих композициях и иммуногенных композициях и вакцинах согласно изобретению, составляет от примерно 10 мкг до примерно 2000 мкг и предпочтительно от примерно 50 мкг до примерно 1000 мкг для данной плазмиды. Специалист обладает необходимыми знаниями для точного определения эффективной дозы ДНК, используемой для терапевтического протокола или вакцинации.
Если используют вектор, дозы могут составлять от 104 до 1010 БОЕ (бляшкообразующая единица), предпочтительно от 106 до 108 БОЕ.
В случае композиции, содержащей GM-CSF, дозы могут составлять от 1 мкг до 5 мг, предпочтительно от 50 мкг до 1 мг.
Объемы дозы предпочтительно могут составлять от 0,5 мл до 5 мл, предпочтительно 2-3 мл.
Перечень последовательностей
Последовательность № 1: олигонуклеотид JP705
Последовательность № 2: олигонуклеотид JP706
Последовательность № 3: олигонуклеотид JP729
Последовательность № 4: олигонуклеотид JP730
Последовательность № 5: олигонуклеотид JP731
Последовательность № 6: олигонуклеотид JP734
Последовательность № 7: олигонуклеотид JP735
Последовательность № 8: последовательность конского гена GM-CSF лошади (фигура 1)
Последовательность № 9: последовательность белка GM-CSF лошади (фигура 1)
Перечень фигур
Фигура 1: последовательности гена и белка GM-CSF лошади.
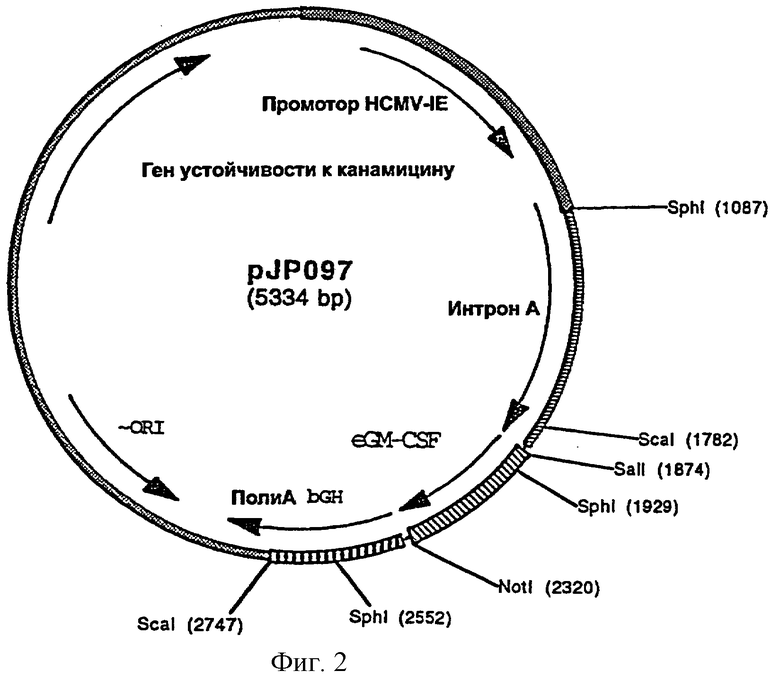
Фигура 2: рестрикционная карта плазмиды pJP097
Все плазмиды были сконструированы с помощью стандартных методов молекулярной биологии (клонирование, рестрикция, синтез однонитевой кДНК, ПЦР, элонгация олигонуклеотида с помощью ДНК-полимеразы...), описанных Sambrook J. и др. (Molecular Cloning: A Laboratory Manual, второе издание, Cold Spring Harbor Laboratory. Cold Spring Harbor, Нью-Йорк, 1989 г.). Все рестриктные фрагменты, а также фрагменты ДНК, полученные методом ПЦР были выделены и очищены с помощью набора "Geneclean®" (BI0101 Inc. La Jolla, Канада).
Сведения, подтверждающие возможность осуществления изобретения
Изобретение более подробно описывается с помощью вариантов осуществления, приводимых в качестве не ограничивающих объема охраны изобретения примеров и со ссылкой на фигуры.
Пример 1
Получение тотальной РНК лимфоцитов лошади, стимулированных in vitro митогенами
Кровь лошадей собирали в пробирку, содержащую этилендиамин-тетрауксусную кислоту (EDTA), путем взятия крови из яремной вены. Мононуклеарные клетки собирали путем центрифугирования в градиенте Ficoll, а затем культивировали в чашках Петри диаметром 60 мм. Мононуклеарные клетки лошади затем стимулировали либо с помощью конканавалина А (ConA) (конечная концентрация примерно 5 мкг/мл), либо с помощью фитогемагглютинина (РНА) (конечная концентрация примерно 10 мкг/мл). После стимуляции лимфобласты "ConA" и "РНА" соскабливали с культуральных чашек и тотальную РНК экстрагировали, используя набор "набор для выделения мРНК из лейкоцитов" (Boehringer Mannheim / Roche Cat # 1934325).
Пример 2
Выделение гена, кодирующего GM-CSF лошади
Были синтезированы олигонуклеотиды JP075 и JP076, имеющие следующую структуру:
JP705 (20 нт) (последовательность № 1)
5' TGGGCACTGTGGYCTGCAGC 3'
JP706 (17 нт) (последовательность № 2)
5' AGCATGTGRATGCCATC 3'.
Олигонуклеотиды использовали в наборе 5' / 3' RACE (Boehringer Mannheim / Roche Cat # 1734792) и получили клоны 3'RACE 6S4, 6W6 и 6W7. 3'-последовательность, составленная на основе этих структур клонов, была использована для синтеза олигонуклеотидов JP729, JP730 и JP731 для получения соответствующих клонов 5'RACE:
JP729 (21 нт) (последовательность № 3)
5' AGCTCCCAGGGCTAGCTCCTA 3'
JP730 (21 нт) (последовательность № 4)
5' CCCTGTTTGTACAGCTTCAGG 3'
JP731 (21 нт) (последовательность № 5)
5' TGTTGTTCAGAAGGCTCAGGG 3'.
Были получены 5'RACE клоны 7D2 и 7D10. Общие последовательности, синтезированные на основе 3'RACE и 5'RACE, клонов были использованы для амплификации последовательности гена GM-CSF лошади методом ПЦР с обратной транскриптазой. В качестве матрицы для синтеза первой нити комплементарной ДНК использовали тотальную РНК, экстрагированную из лимфоцитов лошади, стимулированных ConA или РНА (пример 1). Первую нить комплементарной ДНК получали путем элонгации олигонуклеотида p(dT)15 (Boehringer Mannheim /Roche Cat # 814270). Полученная однонитевая комплементарная ДНК затем была использована в качестве матрицы для ПЦР со следующими олигонуклеотидами:
JP734 (44 нт) (последовательность №6)
5' CATCATCATGTCGACGCCACCATGTGGCTGCAGAACCTGCTTCT 3' и
JP735 (41 нт) (последовательность №7)
5' CATCATCATGCGGCCGCTACTTCTGGGCTGCTGGCTTCCAG 3'
для амплификации фрагмента длиной примерно 500 пар оснований. Этот фрагмент очищали электрофорезом в агарозном геле (= фрагмент А).
Пример 3
Получение плазмиды pJP097 и последовательности гена GM-CSF лошади
Фрагмент А (пример 2) рестриктировали NotI и SalI и фрагмент NotI-SalI лигировали с плазмидой pVR1012 (Hartikka J. и др., Human Gene Therapy, 7, 1205-1217 (1996)), предварительно рестриктированной NotI и SalI, в результате чего была получена плазмида pJP097 (5334 пары оснований, фигура 2). Фрагмент NotI - SalI, клонированный в этой плазмиде, был полностью секвенирован. Эта последовательность (последовательность № 8) кодирует белок из 144 аминокислот (последовательность № 9), представляющий собой цитокин GM-CSF лошади (фигура 1).
Пример 4
Биологическая активность in vitro продукта, кодируемого геном GM-CSF лошади
Клетки СНО-К1 (клетки яичника хомяка, полученные из библиотеки Американской коллекции клеточных культур под номером CCL-61) культивировали в минимальной среде MEM (Gibco-BRL), в чашках Петри диаметром 60 мм и трансфицировали 5 мкг плазмиды pJP097 в виде предварительно полученного комплекса с 10 мкл LipofectAmine PLUS® (Cat # 10964-013, Gibco-BRL, Кливленд, Огайо, США). Образования комплексов ДНК/LipofectAmine® и трансфекцию клеток проводили согласно рекомендациям производителя (Gibco-BRL). Спустя 48 часов после трансфекции супернатанты культур собирали и замораживали.
Клетки костного мозга свиней культивировали в полутвердой среде Methocult (Cat # H4230 StremCell Technologies). К этим культурам затем добавляли (или не добавляли в случае отрицательного контроля) 10 мкл супернатанта клеток, трансфицированных плазмидой pJP097, культуру клеток независимо трансфицировали плазмидами pJP097 Т1 и pJP097 Т2. Каждый супернатант (10 мкл, разведенные в десять раз) тестировали параллельно в 3 культуральных чашках. Отрицательный контроль представлял собой супернатант культуры СНО. После культивирования в течение 14 дней чашки исследовали на образование колоний макрофагов и подсчитывали число образовавшихся колоний.
Для супернатантов клеток СНО, трансфицированных плазмидов pJP097, были получены следующие результаты:
Полученные результаты показывают, что продукт, кодируемый геном GM-CSF лошади, клонированным в плазмиде pJP097, обладает активностью GM-CSF типа в клетках in vitro.
Пример 5
Получение плазмид согласно изобретению
Для получения плазмид, предназначенных для вакцинации лошадей, можно использовать любой метод, позволяющий получать очищенные плазмиды.
Такие методы хорошо известны специалистам. Плазмиды получали путем культивирования бактерий Echerichia coli К12, трансформированных плазмидами согласно изобретению. Наиболее предпочтительно использовать метод щелочного лизиса с двумя последовательными ультрацентрифугированиями в градиенте плотности хлорида цезия в присутствии этидиумбромида как описано Sambrook J. и др. (Molecular Cloning: A Laboratory Manual, второе издание. Cold Spring Harbor Laboratory. Cold Spring Harbor, Нью-Йорк, 1989 г.). Можно также сослаться на Международные заявки WO-A-95/21250 и WO-A-96/02658, в которых описаны методы продуцирования в промышленном масштабе плазмид, используемых для вакцинации. Для получения вакцин, плазмиды готовили в виде высококонцентрированных растворов (>2 мг/мл), удобных для хранения. Для этого плазмиды растворяли либо в сверхчистой воде, либо в буфере ТЕ (10 мМ Трис-HCl, 1 мМ EDTA; рН 8,0).
Пример 6
Приготовление вакцин согласно изобретению и введение
Плазмиду pJP097 разводили в буфере ТЕ, физиологическом растворе или PBS и смешивали с различными вакцинными плазмидами, экспрессирующими защитные иммуногены. В качестве таких плазмид можно использовать, например, указанные в примерах Международной заявки РСТ WO-98/03198.
Лошадей вакцинировали 100 мкг, 250 мкг или 500 мкг, на плазмиду.
Для этого различные смеси "иммуногенных" плазмид и плазмиды pJP097 "GM-CSF лошадей" совместно вводили внутримышечно (шприц + игла) в мышцы шеи или груди. Объем вакцинных доз составлял 2 мл.
Для внутримышечных инъекций также можно использовать струйный жидкостный безыгольный инъектор, с помощью которого можно вводить дозу объемом примерно 0,5 мл. Если необходимо, одному и тому же животному может быть сделано несколько последовательных инъекций объемом 0,5 мл. Последовательные введения проводят путем смещения, чтобы зоны инъекции были отделены друг от друга примерно на 1-2 см.
Внутрикожные инъекции также можно проводить с использованием струйного жидкостного безыгольного инъектора, позволяющего вводить дозу 0,2 мл в 5 различных точек (0,04 мл на одну точку введения) (например, аппарат "PIGJET®" Endoscoptic, Лан, Франция).
Лошадей обычно вакцинируют путем двух инъекций смесей плазмид согласно изобретению, осуществляемых с интервалом 4-5 недель.
Пример 7
Приготовление лекарственного средства на основе плазмид согласно изобретению
Смесь "иммуногенных" плазмид и плазмиды pJP097 разводили в буфере ТЕ, физиологическом растворе или PBS таким образом, чтобы получить концентрацию 1 мг/мл. 0,75 мМ раствор DMRIE-DOPE готовили путем растворения лиофилизата DMRIE-DOPE в нужном объеме стерильной воды.
ДНК-липидые комплексы получали путем смешивания равных объемов 0,75 мМ раствора DMRIE-DOPE и раствора ДНК с концентрацией 1 мг/мл. Раствор ДНК добавляли медленно с помощью иглы 26G по внутренней стенке пробирки, содержащей раствор катионного липида для того, чтобы избежать образования пены. Полученный раствор медленно перемешивали. В результате получают раствор, содержащий 0,375 мМ DMRIE-DOPE и 500 мкг/мл ДНК.
Предпочтительно ДНК-липидные комплексы (ДНК / DMRIE-DOPE) получают при комнатной температуре в течение 30 минут перед иммунизацией животных, как это описано в примере 6.
Должно быть совершенно понятно, что изобретение, описанное в прилагаемых пунктах формулы изобретения, не ограничено отдельными вариантами осуществления, указанными в вышеприведенном описании, а охватывает варианты, которые не входят ни в рамки, ни в изобретательский уровень настоящего изобретения.



| название | год | авторы | номер документа |
|---|---|---|---|
| ДНК-ВАКЦИНА (ВАРИАНТЫ) И ИММУНОГЕННАЯ КОМПОЗИЦИЯ ПРОТИВ ЧУМКИ СОБАК | 2000 |
|
RU2283867C2 |
| ВАКЦИНА ПРОТИВ ВИРУСА ЗАПАДНО-НИЛЬСКОЙ ЛИХОРАДКИ | 2002 |
|
RU2283138C2 |
| РЕКОМБИНАНТНАЯ ВАКЦИНА ПРОТИВ ВИРУСА АФРИКАНСКОЙ КАТАРАЛЬНОЙ ЛИХОРАДКИ | 2007 |
|
RU2446823C2 |
| КОМПОЗИЦИИ РЕКОМБИНАНТНОГО CDV И ЕЕ ПРИМЕНЕНИЕ | 2011 |
|
RU2567337C2 |
| РЕКОМБИНАНТНАЯ ВАКЦИНА ОТ ПТИЧЬЕГО ГРИППА И ЕЁ ПРИМЕНЕНИЕ | 2009 |
|
RU2559527C2 |
| ВАКЦИНЫ ПРОТИВ FMDV НА ОСНОВЕ РЕКОМБИНАНТНОГО АДЕНОВИРУСНОГО ВЕКТОРА И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2725495C2 |
| РЕКОМБИНАНТНАЯ ВАКЦИНА ВИРУСА ЛЕЙКЕМИИ КОШЕК, СОДЕРЖАЩАЯ ОПТИМИЗИРОВАННЫЙ ГЕН ОБОЛОЧКИ ВИРУСА ЛЕЙКЕМИИ КОШЕК | 2012 |
|
RU2591817C2 |
| ДНК-ПЛАЗМИДЫ, ОБЛАДАЮЩИЕ ПОВЫШЕННОЙ ЭКСПРЕССИЕЙ И СТАБИЛЬНОСТЬЮ | 2007 |
|
RU2456346C2 |
| РЕКОМБИНАНТНЫЕ ВАКЦИНЫ ПРОТИВ ВИРУСА "СИНЕГО ЯЗЫКА", ИХ ПРИМЕНЕНИЕ | 2011 |
|
RU2575599C2 |
| РЕАССОРТАНТНЫЕ BTV И AHSV ВАКЦИНЫ | 2013 |
|
RU2656187C2 |

Изобретение относится к области молекулярной биологии. Предложен выделенный фрагмент ДИК, кодирующий GM-CSF лошади, а также сам выделенный белок GM-CSF лошади. Кроме того, предложены векторы и различные композиции, содержащие их. GM-CSF может быть использован в качестве адъюванта при вакцинации лошадей и в качестве неспецифического стимулятора иммунитета в ветеринарии. 12 н. и 6 з.п. ф-лы, 2 ил., 1 табл.
| MCINNES C.J | |||
| et al | |||
| Cloning and expression of a cDNA encoding ovine granulocyte-macrophage colony-stimulating factor | |||
| Gene | |||
| Циркуль-угломер | 1920 |
|
SU1991A1 |
| Прибор для нагревания перетягиваемых бандажей подвижного состава | 1917 |
|
SU15A1 |
| INUMARU S | |||
| et al | |||
| cDNA cloning of porcine granulocyte-macrophage colony-stimulating factor | |||
| Immunol Cell Biol | |||
| Топка с качающимися колосниковыми элементами | 1921 |
|
SU1995A1 |
Авторы
Даты
2006-07-10—Публикация
2000-06-08—Подача