Изобретение относится к замещенным 3-фенил-5-алкокси-1,3,4-оксадиазол-2-онам, которые проявляют ингибирующее действие на гормоночувствительную липазу, HSL.
Определенные 5-алкокси-1,3,4-оксадиазол-2-оны с орто-замещенным фенильным кольцом в качестве заместителя или сконденсированными пяти- или шестичленными циклами обладают противоглистным (патент DE-A 2604110) и инсектицидным действием (патенты DE-A 2603877, ЕР-В 0048040, ЕР-В 0067471).
Определенные 5-фенокси-1,3,4-оксадиазол-2-оны с орто-замещенным фенильным кольцом в качестве заместителя проявляют эндопаразитицидное действие (патент ЕР-А 0419918).
Целью изобретения теперь являлось найти соединения, которые проявляют ингибирующее действие на гормоночувствительную липазу, HSL.
Это было достигнуто с помощью замещенных 3-фенил-5-алкокси-1,3,4-оксадиазол-2-онов общей формулы 1
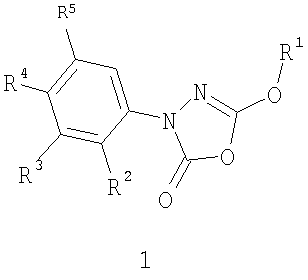
где
R1 означает C1-С6-алкил, С3-С9-циклоалкил, причем обе группы могут быть моно- или полизамещены фенилом, С1-С4-алкилоксигруппой, S-С1-С4-алкилом, N(С1-С4-алкил)2 и фенил в свою очередь может быть моно- или полизамещен галогеном, С1-С4-алкилом, С1-С4-алкилоксигруппой, нитрогруппой, CF3; и
R2, R3, R4 и R5 независимо друг от друга означают водород, галоген, нитрогруппу, С1-С4-алкил, С1-С9-алкилоксигруппу; С6-С10-арил-С1-С4-алкилокси-, С6-С10-арилоксигруппу, С6-С10-арил, С3-С8-циклоалкил или O-С3-С8-циклоалкил, которые могут быть моно-, ди- или тризамещены галогеном, CF3, С1-С4-алкилоксигруппой или С1-С4-алкилом; 2-оксо-пирролидин-1-ил, 2,5-диметилпиррол-1-ил или NR6-A-R7,
причем R2, R3, R4 и R5 не могут одновременно означать водород и по меньшей мере один остаток R2, R3, R4 или R5 является 2-оксо-пирролидин-1-илом, 2,5-диметилпиррол-1-илом или NR6-A-R7, где
R6 является водородом, С1-С4-алкилом или С6-С10-арил-С1-С4-алкилом, причем арил может быть замещен галогеном, CF3, C1-С8-алкилоксигруппой или С1-С4-алкилом;
А означает простую связь, COn, SOn или CONH;
n- 1 или 2;
R7 означает водород; C1-C18-алкил или С2-С18-алкенил, которые от одного до трех раз могут быть замещены С1-С4-алкилом, галогеном, CF3, C1-С4-алкилоксигруппой, N(С1-С4-алкил)2, -СООН, С1-С4-алкоксикарбонилом, С6-С12-арилом, С6-С12-арилоксигруппой, С6-С12-арилкарбонилом, С6-С10-арил-С1-С4-алкилоксигруппой или оксогруппой, причем арил в свою очередь может быть замещен галогеном, С1-С4-алкилом, аминосульфонилом или метилмеркаптогруппой;
С6-С10-арил-С1-С4-алкил, С5-С8-циклоалкил-С1-С4-алкил, C5-C8-циклоалкил, С6-С10-арил-С2-С6-алкенил, С6-С10-арил, дифенил, дифенил-С1-С4-алкил, инданил, которые могут быть моно- или дизамещены C1-C18-алкилом, C1-C18-алкилоксигруппой, С3-С8-циклоалкилом, СООН, гидроксигруппой, С1-С4-алкилкарбонилом, С6-С10-арил-С1-С4-алкилом, С6-С10-арил-С1-С4-алкилоксигруппой, С6-С10-арилоксигруппой, нитро-, цианогруппой, С6-С10-арилом, фторсульфонилом, C1-С6-алкилоксикарбонилом, С6-С10-арилсульфонилоксигруппой, пиридилом, NHSO2-С6-С10-арилом, галогеном, CF3 или OCF3, причем алкил может быть еще раз замещен С1-С4-алкилоксикарбонилом, CF3 или карбоксигруппой, а арил - галогеном, CF3 или С1-С4-алкилоксигруппой;
или группу Het-(CH2)r с
r=0, 1, 2 или 3 и Het означает насыщенный или ненасыщенный 5-7-членный гетероцикл, который может быть сконденсирован с бензолом и замещен С1-С4-алкилом, С6-С10-арилом, галогеном, С1-С4-алкилоксигруппой, С1-С4-алкилоксикарбонилом, С6-С10-арил-С1-С4-алкилом, С6-С10-арил-С1-С4-алкилмеркапто- или нитрогруппой, причем сконденсированный с бензолом арил в свою очередь может быть замещен галогеном, С1-С4-алкилоксигруппой или CF3 и алкил в арилалкиле - метоксигруппой или CF3,
а также их фармакологически приемлемые соли и аддитивные соли кислот.
Упомянутые арильные остатки в случае необходимости могут быть моно- или полизамещены C1-С9-алкилом, C1-C8-алкилоксигруппой, галогеном, трифторметилом. Упомянутые циклоалкильные остатки в случае необходимости могут быть моно- или полизамещены С1-С4-алкилом, С6-С10-арилом и упомянутые алкильные остатки могут быть замещены гидрокси-, ди-С1-С4-алкиламиногруппой и фтором. Галогеном является фтор, хлор, бром, предпочтительно фтор и хлор. Алкил, алкенил, алкилоксигруппа и т.д. могут быть разветвленными или неразветвленными.
Предпочтительными являются соединения формулы 1, где
R1 означает С1-С4-алкил; и/или
R5 означает водород; и/или
R2 означает водород, галоген, С1-С4-алкил, С1-С9-алкилокси- или аминогруппу.
Дополнительно предпочтительными соединениями формулы 1 являются те, в которых:
R3 означает водород, С1-С4-алкил, С6-С10-арил-С1-С4-алкилоксигруппа, которые в случае необходимости могут быть замещены в арильной части галогеном, или NR6-A-R7, где R6 означает водород или бензил,
А означает простую связь и
R7 означает С6-С10-арил-С1-С4-алкил, который может быть замещен галогеном, CF3, цианогруппой, фенил-С1-С4-алкилокси-, CF3-феноксигруппой, С5-С8-циклоалкилом или фторсульфонилоксигруппой;
С1-С12-алкил, который может быть замещен С1-С4-алкилоксигруппой, фенилом, CF3 или фенил-С1-С4-алкилоксигруппой;
С2-С12-алкенил или группу Het(CH2)r-, где r=0 или 1 и Het означает насыщенный или ненасыщенный 5-7-членный гетероцикл, который может быть сконденсирован с бензолом и замещен С1-С4-алкилом или галогеном.
Кроме того, предпочтительными соединениями формулы 1 являются те, где:
R4 означает водород, 2-оксо-пирролидин-1-ил, 2,5-диметилпиррол-1-ил или С6-С10-арил-С1-С4-алкилоксигруппу, которая может быть замещена галогеном, и/или
соединениями формулы 1, где:
R4 означает NR6-A-R7, где
R6 означает водород или метил,
А означает простую связь и
R7 означает водород;
С1-С12-алкил, который может быть моно- или дизамещен галогеном;
С2-С18-алкенил, который может быть моно- или дизамещен C1-С4-алкилом или С1-С4-алкилоксикарбонилом;
С6-С10-арил-С1-С4-алкил, который может быть замещен галогеном, C1-C6-алкилоксигруппой, CF3, цианогруппой, C5-С6-циклоалкилом, С1-С4-алкилоксикарбонилом, С6-С10-арил-С1-С4-алкилом, С6-С10-арил- С1-С4-алкилоксигруппой, причем арил может быть еще раз замещен галогеном или CF3;
С5-С8-циклоалкил-С1-С4-алкил;
или группу Het-(CH2)r-, где
r=1, 2 или 3 и Het означает насыщенный или ненасыщенный 5-7-членный гетероцикл, который может быть замещен галогеном, С1-С4-алкилоксигруппой или С1-С4-алкилоксикарбонилом, и/или
соединения формулы 1, где
R4 означает NR6-A-R7, где
R6 означает водород,
А означает -СО- и
R7 означает C1-C18-алкил, который может быть замещен галогеном, фенилом, феноксигруппой, фенилкарбонилом или С1-С4-алкилоксикарбонилом, причем феноксигруппа в свою очередь может быть замещена метилом, галогеном или метилмеркаптогруппой;
С2-С18-алкенил, который может быть замещен С6-С10-арилом;
С6-С10-арил, который может быть замещен галогеном, C1-C8-алкилом, фенил- С1-С4-алкилом, CF3, OCF3, фторсульфонилом, С1-С4-алкилоксикарбонилом, феноксигруппой, причем арил в свою очередь может быть замещен С1-С4-алкилоксигруппой;
С6-С10-арил-С1-С4-алкил, причем алкил может быть замещен метоксигруппой или CF3 и арил - галогеном;
или группу Het-(CH2)r-, где
r=0 и Het означает насыщенный или ненасыщенный 5-7-членный гетероцикл, который может быть сконденсирован с бензолом и замещен С1-С4-алкилом, галогеном, С1-С4-алкилоксигруппой, галогенофенилом или галогенобензилмеркаптогруппой, причем сконденсированный с бензолом арил в свою очередь может быть замещен галогеном или метоксигруппой, и/или
соединениями формулы 1, где:
R4 означает NR6-A-R7, где
R6 означает водород,
А означает -CO2- и
R7 означает C1-C18-алкил, который замещен CF3 или фенилом;
С6-С10-арил;
С6-С10-арил-С1-С4-алкил, который замещен С1-С4-алкилом, галогеном, CF3 или OCF3, бензилоксигруппой или фенилом;
или группу Het-(CH2)r-, где
r=0 или 1 и Het означает насыщенный или ненасыщенный 5-7-членный гетероцикл, который может быть сконденсирован с бензолом и замещен С1-С4-алкилом или бензилом, и/или
R4 означает NR6-A-R7, где
R6 означает водород,
А означает -SO2- и
R означает C1-С6-алкил, который может быть замещен CF3;
С2-С4-алкенил, который может быть замещен фенилом;
С6-С10-арил, который может быть замещен C1-С6-алкилом, галогеном, С1-С4-алкилоксигруппой или бензилом;
дифенил-С1-С4-алкил, замещенный галогеном;
или группу Het-(CH2)r-, где
r=0 и Het означает насыщенный или ненасыщенный 5-7-членный гетероцикл, и/или
соединениями формулы 1, где:
R4 означает NR6-A-R7, где
R6 означает водород,
А означает -CO-NH и
R7 означает С1-С10-алкил, который может быть замещен С1-С4-алкилоксикарбонилом, N((С1-С4)-алкил)2 или фенилом, который в свою очередь может быть замещен галогеном или аминосульфонилом;
С6-С10-арил, который может быть замещен C1-С6-алкилом, C1-С6-алкилоксигруппой, C1-С6-алкилоксикарбонилом, феноксигруппой, OCF3, бензилом или пиридилом, причем алкил может быть еще раз замещен С1-С4-алкилоксикарбонилом или карбоксигруппой;
С5-С8-циклоалкил, который может быть замещен гидроксигруппой, или инданил;
или группу Het-(CH2)r-, где
r=0 или 1, Het означает насыщенный или ненасыщенный 5-7-членный гетероцикл, который может быть замещен бензилом.
Особенно предпочтительны соединения формулы 1, где R1 означает метил.
Совершенно особенно предпочтительна группа соединений формулы 1, названная в примерах 21, 22, 27, 28, с 30 по 34, с 36 по 42, 53, 54, 58, 60, 62, 65, 69, 71, 74, 92, 97, 107, 116, 128, 130, 136, 139, 142, 152, 166 и 171.
Предложенные соединения общей формулы 1 обладают широким ингибирующим действием на гормоночувствительную липазу, HSL, аллостерический фермент в адипоцитах, который ингибируется инсулином и ответственен за разрушение жиров в жировых клетках и, таким образом, за перевод компонент жиров в кровяное русло. Ингибирование указанных ферментов соответствует, таким образом, инсулиноподобному действию предложенных соединений, которое в конечном счете ведет к уменьшению свободных жирных кислот в крови и сахара в крови. Они, таким образом, могут быть введены при нарушениях обмена веществ, как, например, при инсулиннезависимом сахарном диабете, при диабетическом синдроме и при непосредственном повреждении поджелудочной железы.
Получение предложенных соединений общей формулы 1 может осуществляться по известным способам различными путями.
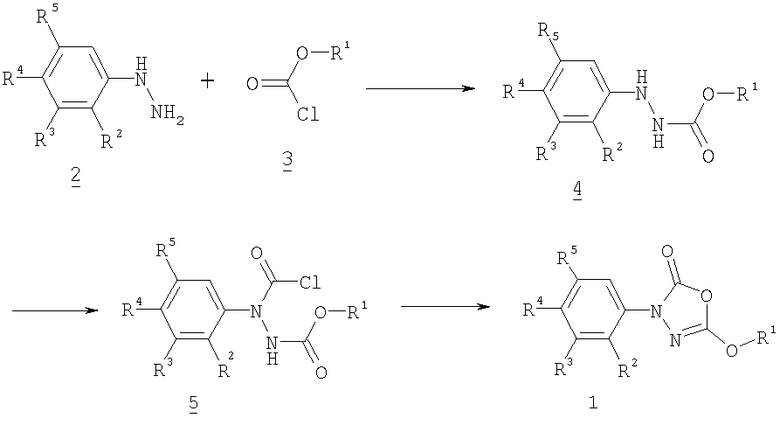
Например, получение замещенных 3-фенил-5-алкокси-1,3,4-оксадиазол-2-онов общей формулы 1 может производиться путем взаимодействия гидразинов общей формулы 2 с эфирами хлормуравьиной кислоты формулы 3 или другими реакционноспособными производными угольной кислоты, где R1, R2, R3, R4 и R5, как определены выше, с образованием соединений формулы 4, которые ацилируют фосгеном, карбонилдиимидазолом, дифосгеном или трифосгеном, циклизуют и в случае необходимости путем дальнейшего модифицирования остатков R2-R5, как, например, путем восстановления нитро- в аминогруппы известным способом и последующим ацилированием или алкилированием, превращают в соединения формулы 1. Так как при указанных реакциях, как правило, высвобождаются кислоты, для ускорения рекомендуется добавлять основания, такие как пиридин, триэтиламин, натронную щелочь или карбонат щелочного металла. Реакции можно проводить в широком диапазоне температур. Как правило, предпочтительно работать при температурах от 0°С до точки кипения использованного растворителя. В качестве растворителя используют, например, метиленхлорид, ТГФ, ДМФА, толуол, этилацетат, н-гептан, диоксан, диэтиловый эфир.
Гидразин формулы 2 можно получить известными способами, например диазотированием соответствующих анилинов

и последующим восстановлением известными способами или нуклеофильным замещением подходящим образом замещенных фенильных производных 6 (X=F, Cl, Br, I, OSO2CF3) гидразингидратом. Такими подходящими фенильными производными могут быть нитрозамещенные галогенобензолы, предпочтительно фтор- и хлорнитробензолы, из которых предложенные соединения удается получить на подходящей стадии синтеза путем восстановления и взаимодействия с ацилирующими или алкилирующими средствами, как, например, хлорангидридами кислот, ангидридами, изоцианатами, эфирами хлормуравьиной кислоты, хлорангидридами сульфокислот или алкил- и арилалкилгалогенидами, или путем восстановительного алкилирования альдегидами известными способами.
Действие предложенных соединений формулы 1 испытывали на следующей ферментной тестовой системе:
Подготовка фермента:
Получение частично очищенной HSL:
Изолированные жировые клетки крыс из жировой ткани придатка яичка необработанных крыс-самцов (Wistar, 220-250 г) получали обработкой коллагеназой согласно опубликованному способу (например, S.Nilsson and al., Anal. Biochem. 158, 1986, 399-407; G.Fredrikson., J. Biol. Chem. 256, 1981, 6311-6320; Н.Tornquist and al., J. Biol. Chem. 251, 1976, 813-819). Жировые клетки из 10 крыс трижды промывали флотацией каждый раз по 50 мл буферного раствора для гомогенизации (25 мл Tris (трис(гидроксиметил)аминометана)/HCl, рН 7,4, 0,25 М сахарозы, 1 мМ EDTA (этилендиаминтетрауксусной кислоты), 1 мМ DTT (трео-1,4-димеркапто-бутан-2,3-диола), 10 мкг/мл лейпептина, 10 мкг/мл антипаина, 20 мкг/мл пепстатина) и затем извлекали 10 мл буферного раствора для гомогенизации. Жировые клетки гомогенизировали в тефлоно-стеклянном гомогенизаторе (Braun-Melsungen) за 10 ходов при 1500 об/мин и 15°С. Гомогенизат центрифугировали (Sorvall SМ24-трубки, 5000 об/мин, 10 мин 4°С). Нижний слой между лежащим сверху жировым слоем и частицами отбирали и центрифугирование повторяли. Полученный нижний слой снова центрифугировали (Sorvall SМ24-трубки, 20000 об/мин, 45 мин, 4°С). Нижний слой отбирали и смешивали с 1 г гепарин-сефарозы (Pharmacia-Biotech, CL-6B, промывали 5 раз 25 мл Tris/HCl, pH 7,4, 150 мМ NaCl). После инкубирования 60 мин при 4°С (встряхивали с интервалом 15 мин) смесь центрифугировали (Sorvall SМ24-трубки, 3000 об/мин, 10 мин, 4°С). Верхний слой доводили до pH 5,2 путем прибавления ледяной уксусной кислоты и инкубировали 30 мин при 4°С. Осадок собирали центрифугированием (Sorvall SS34, 12000 об/мин, 10 мин, 4°С) и суспендировали в 2,5 мл 20 мМ Tris/HCl, pH 7,0, 1 мМ EDTA, 65 мМ NaCl, 13% сахарозы, 1 мМ DTT, 10 мкг/мл лейпептина/пепстатина/антипаина. Суспензию подвергали в течение ночи диализу при 4°С 25 мМ Tris/HCl, pH 7,4, 50% глицерина, 1 мМ DTT, 10 мкг/мл лейпептина, пепстатина, антипаина и затем вводили в гидроксиапатитовую колонку (0,1 г на 1 мл суспензии, приводили к равновесию 10 мМ фосфата калия, pH 7,0, 30% глицерина, 1 мМ DTT). Колонку промывали четырьмя объемами уравновешивающего буферного раствора при скорости потока от 20 до 30 мл/ч. HSL вымывали одним объемом уравновешивающего буфера, который содержал 0,5 М фосфата калия, затем диализовали (см. выше) и от 5- до 10-кратно концентрировали путем ультрафильтрования (фильтр Amicon Diaflo PM 10) при 4°С. Частично очищенная HSL может храниться от 4 до 6 недель при -70°С.
Образец:
Для получения субстрата перемешивали 25-50 мкКи [3Н] триолеоилглицерина (в толуоле), 6,8 мкмоля немеченого триолеоилглицерина и 0,6 мг фосфолипида (фосфатидилхолин/фосфатидилинозита 3:1 вес/объем), сушили в атмосфере N2 и затем поглощали 2 мл 0,1 М KPi (pH 7,0) путем обработки ультразвуком (Branson 250, микрошприц, установка 1-2,2×1 мин в 1-минутном интервале). После прибавления 1 мл KPi и повторной обработки ультразвуком (4×30 сек на льду с интервалами 30 сек) прибавляли 1 мл 20% BSA (N,O-бис(триметилсилил)ацетамида) (в KPi) (конечная концентрация триолеоилглицерина 1,7 мМ). Для реакции прибавляли пипеткой 100 мкл раствора субстрата к 100 мкл раствора HSL (HSL получали, как указано выше, разбавляли 20 мМ KPi, pH 7,0, 1 мМ EDTA, 1 мМ DTT, 0,02% BSA, 20 мкг/мл пепстатина, 10 мкг/мл лейпептина) и инкубировали 30 мин при 37°С. После прибавления 3,25 мл смеси метанол/хлороформ/гептана (10:9:7) и 1,05 мл 0,1 М К2СО3, 0,1 М борной кислоты (pH 10,5) хорошо перемешивали и наконец центрифугировали (800 × г, 20 мин). После разделения фаз отбирали один эквивалент верхней фазы (1 мл) и определяли радиоактивность жидкостным сцинтилляционным счетчиком.
Оценка:
Вещества обычно испытывали в четырех независимых композициях. Ингибирование ферментативной активности HSL тестовым веществом определяли путем сравнения с неингибированной контрольной реакцией. Расчет значения IC50 осуществляли по кривой ингибирования с минимум 10 концентрациями тестового вещества. Для анализа данных использовали пакет программного обеспечения GRAPHIT, Elsevier-BIOSOFT.
В указанной пробе соединения проявили следующее действие:
Следующие примеры лучше проясняют способы получения, не ограничивая их.
Примеры:
Пример 1:
3-Метил-4-нитро-фенилгидразин
К раствору 15,9 г 2-метил-4-фтор-нитробензола в 10 мл N-метилпирролидона медленно прибавляли по каплям при комнатной температуре 5 г гидразингидрата и смесь нагревали при перемешивании 4 часа до 65°С. Путем прибавления 70 мл воды продукт осаждали и перекристаллизовывали из изопропанола. Выход: 13,3 г, т. пл.: 138°С.
Аналогичным способом были получены следующие примеры:
Пример 2:
3-фтор-4-нитро-фенилгидразин
т.пл.: 130°С
Пример 3:
2-хлор-4-нитро-фенилгидразин
т.пл.: 144°С
Пример 4:
2-метил-4-нитро-фенилгидразин
т.пл.: 135°С
Пример 5:
(3-(4-фторбензилокси)-2-нитро-фенилгидразин
т.пл.: 164°С
Исходное соединение 2-фтор-4-(4-фторбензилокси)нитробензол (т.пл.: 99°С) было получено алкилированием 3-фтор-4-нитро-фенола 4-фторбензилхлоридом в ДМФА в присутствии поташа.
Пример 6:
3-(4-фторбензилокси)-4-нитро-фенилгидразин (промежуточный продукт)
т.пл.: 145°С
Пример 7:
4-(4-хлорфенокси)-3-нитро-анилин
К раствору 1,29 г 4-хлорфенола в 8 мл ДМФА добавляли 1,4 г поташа и через 30 минут перемешивания прибавляли 1,6 г 4-фтор-3-натро-анилина и смесь перемешивали 3 часа при 100°С. После охлаждения добавляли 80 мл воды и осадок после кратковременного перемешивания отсасывали и сушили в вакууме при 40°С. Выход: 2,0 г; т.пл.: 101°С.
Пример 8:
4-(4-хлорфенокси)-3-нитро-фенилгидразин
К охлажденной до 0°С перемешиваемой смеси, состоящей из 1,9 г 4-(4-хлорфенокси)-3-нитро-анилина, 25 мл конц. соляной кислоты и 25 мл этанола, прибавляли по каплям раствор 0,52 г нитрита натрия в 5 мл воды, смесь перемешивали при 0°С 60 мин и наконец к суспензии прибавляли по каплям 8,5 г дигидрата дихлорида олова в 8 мл конц. HCl. Осадок отсасывали, промывали водой, суспендировали в 200 мл воды под азотом и разлагали 100 мл 30%-ной натронной щелочи при 10-15°С. Образовавшееся масло встряхивали с ледяной уксусной кислотой, промывали водой, органическую фазу сушили сульфатом натрия. Затем продукт осаждали изопропанольным HCl, отсасывали и сушили в вакууме. Выход: 1,1 г; т.пл.: 221°С
Пример 9:
метиловый эфир N'-(4-нитро-2-метил-фенил)-гидразино-муравьиной кислоты
К смеси, состоящей из 0,84 г 2-метил-4-нитро-фенилгидразина, 15 мл NMP (N-метилпирролидона) и 2 мл пиридина осторожно при охлаждении льдом прибавляли по каплям 0,43 мл метилового эфира хлормуравьиной кислоты и затем перемешивали 2 часа при медленном нагревании до комнатной температуры. После разбавления 50 мл воды смесь перемешивали в течение ночи и твердое вещество сушили в вакууме при 40°С.
Выход 0,81 г; т.пл.: 153°С
Следующие примеры были получены подобным способом:
Пример 10:
метиловый эфир N'-(4-нитро-фенил)-гидразино-муравьиной кислоты (промежуточный продукт)
т.пл.: 179°С
Пример 11:
метиловый эфир N'-(3-фтор-4-нитро-фенил)-гидразино-муравьиной кислоты
т.пл.: 127,4°С
Пример 12:
метиловый эфир N'-(3-метил-4-нитро-фенил)-гидразино-муравьиной кислоты
т.пл.: 159°С
Пример 13:
метиловый эфир N'-(2-хлор-4-нитро-фенил)-гидразино-муравьиной кислоты
т.пл.: 156°С
Пример 14:
метиловый эфир N'-(3-(4-фторбензилокси)-4-нитро-фенил)-гидразино-муравьиной кислоты (промежуточный продукт)
т.пл.: 166°С
Пример 15:
метиловый эфир N'-(3-(4-фторбензилокси)-2-нитро-фенил)-гидразино-муравьиной кислоты
т.пл.: 193°С
Пример 16:
метиловый эфир N'-(4-(4-хлорфенокси)-3-нитро-фенил)-гидразино-муравьиной кислоты
т.пл.: 147°С
Пример 17:
метиловый эфир N'-(3-пиперидино-4-нитро-фенил)-гидразино-муравьиной кислоты (-)
т.пл.: 131°С
Указанное соединение и соединение примера 18 были получены взаимодействием метилового эфира N'-(3-фтор-4-нитро-фенил)-гидразино-муравьиной кислоты с пиперидином или N-бензил-пиперазином в NMP при 80°С.
Пример 18:
метиловый эфир N'-3-(N-бензил-пиперазино)-4-нитро-фенил)-гидразино-муравьиной кислоты
т.пл.: 156°С
Пример 19:
5-метокси-3-(4-нитрофенил)-3-Н-(1,3,4)оксадиазол-2-он
2,5 г метилового эфира N'-(4-нитро-фенил)-гидразино-муравьиной кислоты и 5 мл пиридина помещали в 15 мл метиленхлорида и прибавляли по каплям при перемешивании и охлаждении льдом 3 мл 20%-ного толуольного раствора фосгена. Смесь оставляли стоять в течение ночи при комнатной температуре, разбавляли еще 10 мл метиленхлорида и затем промывали 3 раза водой. После высушивания над сульфатом натрия смесь упаривали в вакууме и продукт очищали колоночной хроматографией (силикагель, растворитель: метанол:метиленхлорид = 2:98) и перекристаллизовывали из изопропанола.
Выход: 1,5 г; т.пл.: 151°С
Следующие примеры были получены аналогично примеру 4:
Пример 20:
5-метокси-3-(3-метил-4-нитро-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 112°С
Пример 21:
5-метокси-3-(4-(4-хлорфенокси-3-нитро-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: масло
Пример 22:
5-метокси-3-(3-(4-фторбензилокси)-2-нитро-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 99°С
Пример 23:
5-метокси-3-(2-метил-4-нитро-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 111°С
Пример 24:
5-метокси-3-(3-(4-фторбензилокси)-4-нитро-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 137°С
Пример 25:
5-метокси-3-(4-амино-фенил)-3-Н-(1,3,4)оксадиазол-2-он
Смесь, состоящую из 1,4 г 5-метокси-3-(4-нитро-фенил)-3-Н-(1,3,4)оксадиазол-2-она, 0,5 г Pd/C и 20 мл метанола, гидрировали при нормальном давлении при комнатной температуре до поглощения рассчитанного количества водорода. Затем отфильтровывали от катализатора и раствор упаривали в вакууме. Оставшийся полутвердый остаток перемешивали с изопропанолом и отсасывали.
Выход: 0,75 г; т.пл.: 85°С
Пример 26:
5-метокси-3-(2-амино-4-(4-фторбензилокси)-фенил-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: масло
Пример 27:
5-метокси-3-(3-амино-4-(4-хлорфенокси)-фенил-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 133°С
Пример 28:
5-метокси-3-(4-амино-3-метил-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 114°С
Пример 29:
5-метокси-3-(4-амино-3-(4-фторбензилокси)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 195°С
Пример 30:
5-метокси-3-(4-(4-хлорфенилацетамино)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
К охлаждаемой льдом смеси, состоящей из 200 мг 5-метокси-3-(4-амино-фенил)-3-Н-(1,3,4)оксадиазол-2-она, 20 мл метиленхлорида и 0,1 мл пиридина, прибавляли по каплям 201 мг хлорангидрида 4-хлорфенилуксусной кислоты и смесь перемешивали 5 часов при комнатной температуре. Летучие компоненты удаляли в вакууме, остаток перемешивали с водой, твердое вещество отсасывали и сушили в вакууме при 40°С.
Выход: 318 мг; т.пл.: 161°С
Аналогичным способом были получены следующие примеры:
Пример 31:
5-метокси-3-(4-(4-хлорфенилацетамино)-3-метил-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 190°С
Пример 32:
5-метокси-3-(4-октаноиламино-3-метил-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 110°С
Пример 33:
5-метокси-3-(4-(4-гептил-бензоиламино)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 155°С
Пример 34:
5-метокси-3-(4-(4-бутил-фенил-сульфониламино)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.:135°С
Пример 35:
5-метокси-3-(4-(4-хлорбутаноиламино)-3-метил-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 137°С
Пример 36:
5-метокси-3-(4-пивалоиламино-3-метил-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 157°С
Пример 37:
5-метокси-3-(4-(4-хлорфенилсульфониламино)-3-метил-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 147°С
Пример 38:
5-метокси-3-(4-(1-нафтилсульфониламино)-3-метил-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 123°С
Пример 39:
5-метокси-3-(4-(2-фенилэтенилсульфониламино)-3-метил-фенил)-3-Н-(1,3,4) оксадиазол-2-он
т.пл.: 129°С
Пример 40:
5-метокси-3-(4-(2,2,2-трифторэтил-сульфониламино)-3-метил-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 151°С
Пример 41:
5-метокси-3-(4-бензилоксикарбониламино)-3-метил-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 115°С
Пример 42:
5-метокси-3-(4-(3,4-дихлорфениламино-карбониламино)-3-метил-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 210°С
Это соединение было получено взаимодействием 5-метокси-3(4-амино-3-метил-фенил)-3-Н-(1,3,4)оксадиазол-2-она с эквимолярным количеством 3,4-дихлорфенилизоцианата в толуоле при 50°С.
Пример 43:
5-метокси-3-(4-(4-хлорфенилсульфониламино)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 169°С
Пример 44:
5-метокси-3-(4-(2-хлорфенилсульфониламино)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 171°С
Пример 45:
5-метокси-3-(4-(3-хлорфенилсульфониламино)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 141°С
Пример 46:
5-метокси-3-(4-(4-хлорфенилацетил-амино)-3-(4-фторбензилокси)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 167°С
Пример 47:
5-метокси-3-(4-бензилсульфониламино-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 153°С
Пример 48:
5-метокси-3-(4-(2-(4'-хлор-бифенил)-этил)-сульфониламино)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 165°С
Пример 49:
5-метокси-3-(4-изопропилсульфониламино-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 190°С
Пример 50:
5-метокси-3-(4-диметиламино-3-метил-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 71°С
Это соединение было получено взаимодействием 5-метокси-3-(4-амино-3-метил-фенил)-3-Н-(1,3,4)оксадиазол-2-она с параформальдегидом/муравьиной кислотой в ДМФА при комнатной температуре и очищено колоночной хроматографией (силикагель, этилацетат:н-гептан = 1:1).
Пример 51:
5-метокси-3-(4-(4-хлорбензиламино)-3-метил-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: масло
Это соединение было получено взаимодействием 5-метокси-3-(4-амино-3-метил-фенил)-3-Н-(1,3,4)оксадиазол-2-она с 4-хлорбензальдегидом/борогидридом натрия в метаноле/метиленхлориде при комнатной температуре и очищено колоночной хроматографией (силикагель, этилацетат:н-гептан = 1:1).
Пример 52:
5-метокси-3-(4-(2-оксо-пирролидин-1-ил)-3-метил-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: масло
Это соединение было получено взаимодействием 5-метокси-3-(4-(4-хлорбутаноиламино)-3-метил-фенил)-3-Н-(1,3,4)оксадиазол-2-она с боргидридом натрия в диоксане при комнатной температуре и очисткой сырого продукта колоночной хроматографией (силикагель, метиленхлорид:метанол = 98:2).
Пример 53:
5-метокси-3-(4-(4-оксо-пент-2-ен-2-ил-амино)-3-метил-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 143°С
Это соединение было получено взаимодействием 5-метокси-3-(4-амино-3-метил-фенил)-3-Н-(1,3,4)оксадиазол-2-она с эквимолярным количеством ацетилацетона в ледяной уксусной кислоте при 80°С и выделено осаждением путем добавления воды и фильтрованием.
Пример 54:
5-метокси-3-(4-(2,5-диметил-пиррол-1-ил)-3-метил-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: масло
Это соединение было получено взаимодействием 5-метокси-3-(4-амино-3-метил-фенил)-3-Н-(1,3,4)оксадиазол-2-она с эквимолярным количеством ацетонилацетона в ледяной уксусной кислоте при 80°С. Обработку осуществляли разбавлением водой, встряхиванием с этилацетатом и колоночной хроматографией (силикагель, метиленхлорид) сырого продукта, полученного после упаривания высушенной органической фазы.
Пример 55:
5-метокси-3-(3-(4-фторбензилокси)-4-метиламино-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 98°С
Это соединение было получено в качестве побочного продукта при гидрировании 5-метокси-3-(3-(4-фторбензилокси)-4-нитро-фенил)-3-Н-(1,3,4)оксадиазол-2-она с диоксидом платины в качестве катализатора в метаноле при комнатной температуре и нормальном давлении и после отфильтровывания катализатора, упаривания реакционной смеси и колоночной хроматографии (силикагель, метиленхлорид).
Соединения примеров 56-199 были получены аналогично предшествующим примерам.
Пример 56:
5-метокси-3-(3-амино-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 95°С
Пример 57:
5-метокси-3-(3-дибензиламино-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 71°С
Пример 58:
5-метокси-3-(3-бензиламино-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: масло
Пример 59:
5-метокси-3-(4-(пирид-2-ил)-амино-карбонил-амино-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 81°С
Пример 60:
5-метокси-3-(3-(4-фторбензил-окси)-4-бензилоксикарбониламино-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: масло
Пример 61:
5-метокси-3-(4-амино-2-метил-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: масло
Пример 62:
5-метокси-3-(3-метил-4-(2-хлорбензилоксикарбониламино)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 161°С
Пример 63:
5-метокси-3-(4-амино-2-хлор-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 126°С
Пример 64:
5-метокси-3-(2-хлор-4-нитро-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 92°С
Пример 65:
5-метокси-3-(2-метил-4-бензилоксикарбониламино-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 112°С
Пример 66:
5-метокси-3-(2-метил-4-(4-трифторметоксибензоиламино)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 150°С
Пример 67:
5-метокси-3-(2-хлор-4-бензилоксикарбониламино-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 150°С
Пример 68:
5-метокси-3-(3-фтор-4-нитро-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 127°С
Пример 69:
5-метокси-3-(4-(4-трет-бутил-бензоиламино)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 173°С
Пример 70:
5-метокси-3-(4-(4-хлор-бензилоксикарбониламино)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 177°С
Пример 71:
5-метокси-3-(2-хлор-4-(4-гептилбензоиламино)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 135°С
Пример 72:
5-метокси-3-(4-(3,4-дихлорбензоиламино)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 200°С
Пример 73:
5-метокси-3-(4-(2-(4-хлорфенокси)-2-метил-пропиониламино)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 153°С
Пример 74:
5-этокси-3-(3-метил-4-бензилоксикарбониламино-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 94°С
Пример 75:
5-изопропокси-3-(3-метил-4-бензилоксикарбониламино-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 119°С
Пример 76:
5-изопропокси-3-(3-метил-4-бутилоксикарбониламино-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 114°С
Пример 77:
5-изопропокси-3-(3-метил-4-(3-хлорфениламино-карбониламино)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 201°С
Пример 78:
5-трет-бутокси-3-(3-метил-4-бензилоксикарбониламино-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 113°С
Пример 79:
5-метокси-3-(3-метил-4-феноксикарбониламино-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 145°С
Пример 80:
5-метокси-3-(3-метил-4-(пирид-3-ил-карбониламино)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: масло
Пример 81:
5-метокси-3-(3-метил-4-(индан-2-ил-аминокарбониламино)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 206°С
Пример 82:
5-метокси-3-(3-метил-4-(пирид-3-ил-метиламинокарбониламино)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 229°С
Пример 83:
5-метокси-3-(3-метил-4-(пирид-3-ил-метоксикарбониламино)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 232°С
Пример 84:
5-метокси-3-(3-фтор-4-бензилоксикарбониламино-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: масло
Пример 85:
5-метокси-3-(3-фтор-4-(4-трифторметилбензоиламино)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: масло
Пример 86:
5-метокси-3-(3-бензилокси-4-(4-трифторметилбензоиламино)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 159°С
Пример 87:
5-метокси-3-(3-фтор-4-(4-трет-бутил-бензоиламино)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 144°С
Пример 88:
5-метокси-3-(3-метил-4-(2,2,2-трифторэтоксикарбониламино)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 141°С
Пример 89:
5-метокси-3-(3-метил-4-пиперидинокарбониламино-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 154°С
Пример 90:
5-метокси-3-(4-(6-метокси-бензофуран-2-ил-карбониламино)-фенил)-3-Н-(1,3,4)оксадиазол-2-он
т.пл.: 191°С
Дальнейшие примеры, которые получены по вышеописанному способу и охарактеризованы масс-спектроскопией (М+1):










| название | год | авторы | номер документа |
|---|---|---|---|
| ЗАМЕЩЕННЫЕ 3-ФЕНИЛ-5-АЛКОКСИ-1,3,4-ОКСАДИАЗОЛ-2-ОНЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ЛИПАЗЫ | 2000 |
|
RU2265600C2 |
| ПРОИЗВОДНЫЕ ОКСАДИАЗОЛА | 1997 |
|
RU2182905C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ОКСАЗОЛ-БЕНЗОИЗОТИАЗОЛДИОКСИДА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЯ | 2005 |
|
RU2377242C2 |
| МОЧЕВИНА И СУЛЬФАМИДНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ TAFIA | 2007 |
|
RU2459619C2 |
| СОЕДИНЕНИЕ, НАЦЕЛЕННОЕ НА БЕЛОК И ЕГО ДЕГРАДАЦИЮ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2021 |
|
RU2829459C1 |
| ПОЛУЧЕНИЕ ДИГИДРОТИЕНО[3,2-d]ПИРИМИДИНОВ И ПРОМЕЖУТОЧНЫХ ПРОДУКТОВ, ПРИМЕНЯЮЩИХСЯ ДЛЯ ИХ СИНТЕЗА | 2008 |
|
RU2528340C2 |
| ПРИМЕНЕНИЕ ИНГИБИТОРОВ IkB-КИНАЗЫ ПРИ ОБЕЗБОЛИВАЮЩЕМ ЛЕЧЕНИИ | 2003 |
|
RU2320338C2 |
| ЗАМЕЩЕННЫЕ ИЗОХИНОЛИНОВЫЕ И ИЗОХИНОЛИНОНОВЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ Rho-КИНАЗЫ | 2007 |
|
RU2455302C2 |
| НОВЫЕ ДИАМИДЫ ПИРИМИДИН-4,6-ДИКАРБОНОВОЙ КИСЛОТЫ ДЛЯ СЕЛЕКТИВНОГО ИНГИБИРОВАНИЯ КОЛЛАГЕНАЗ | 2003 |
|
RU2344129C2 |
| СПОСОБ ИНГИБИРОВАНИЯ ПРОДУЦИРОВАНИЯ ОСТАТОЧНЫХ ЛИПОПРОТЕИНОВ | 2004 |
|
RU2330682C2 |
Изобретение относится к соединениям общей формулы 1
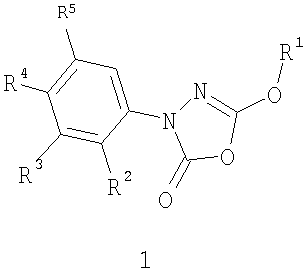
где R1 означает C1-С6-алкил, который может быть замещен фенилом; и R2, R3, R4 и R5 являются независимо друг от друга водородом, галогеном, нитрогруппой, C1-С4-алкилом, C6-С10-арил-C1-С4-алкилокси, C6-С10-арилоксигруппой, C6-С10-арилом, которые могут быть моно-, ди- или тризамещены галогеном; 2-оксо-пирролидин-1-илом, 2,5-диметилпиррол-1-илом или NR6-A-R7, при условии, что R2, R3, R4 и R5 не могут одновременно означать водород и, по меньшей мере, один остаток R2, R3, R4 или R5 является 2-оксо-пирролидин-1-илом, 2,5-диметилпиррол-1-илом или NR6-A-R7, при значении R6 - водород, C1-С4-алкил или C6-С10-арил-C1-С4-алкил; причем арил может быть замещен галогеном; А означает простую связь, COn, SOn или CONH; n равно 1 или 2; R7 означает водород, C1-С18-алкил или C2-С18-алкенил, которые могут быть замещены от одного до трех раз C1-С4-алкилом, C1-С4-алкилокси, N(C1-С4-алкил)2, -СООН, C1-С4-алкилоксикарбонилом, С6-С12-арилом, C6-С12-арилокси, C6-С12-арилкарбонилом, C6-С10-арил-C1-С4-алкилокси, галогеном, CF3 или оксогруппой, причем арил в свою очередь может быть замещен галогеном, C1-С4-алкилом, аминосульфонилом или метилмеркаптогруппой; C6-С10-арил-C1-С4-алкил, C5-С8-циклоалкил-C1-С4-алкил, C5-С8-циклоалкил, C6-С10-арил-C2-С6-алкенил, C6-С10-арил, дифенил, дифенил-C1-С4-алкил, инданил, которые могут быть моно- или дизамещены C1-С18-алкилом, C1-С18-алкилоксигруппой, C3-С8-циклоалкилом, гидроксигруппой, C1-С4-алкилкарбонилом, C6-С10-арил-C1-С4-алкилом, С6-С10-арил-C1-С4-алкилоксигруппой, C6-С10-арилоксигруппой, нитро-, цианогруппой, C6-С10-арилом, фторсульфонилом, C1-С6-алкилоксикарбонилом, C6-С10-арилсульфонилоксигруппой, пиридилом, NHSO2-C6-С10-арилом, галогеном, CF3 или OCFз, причем арил может быть еще раз замещен галогеном, CF3 или C1-С4-алкилоксигруппой; или группу Het-(CH2)r, где r=0, 1, 2 или 3 и Het - насыщенный или ненасыщенный 5-7-членный гетероцикл, который содержит атомы N, О или S и может быть сконденсирован с бензолом и замещен C1-С4-алкилом, C6-С10-арилом, галогеном, C1-С4-алкилоксигруппой, C6-С10-арил-C1-С4-алкилом, C6-С10-арил-C1-С4-алкилмеркапто - или нитрогруппой, причем сконденсированный с бензолом арил в свою очередь может быть замещен галогеном, C1-С4-алкилоксигруппой; а также к их фармакологически приемлемым солям и аддитивным солям кислот и к способу их получения. Соединения оказывают ингибирующее действие на гормоночувствительную липазу, HSL. 2 н. и 12 з.п. ф-лы.
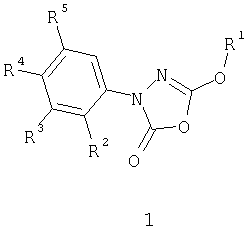
где R1 означает C1-С6-алкил, который может быть замещен фенилом;
R2, R3, R4 и R5 являются независимо друг от друга водородом, галогеном, нитрогруппой, C1-С4-алкилом, C6-С10-арил-C1-С4-алкилокси, C6-С10-арилоксигруппой, C6-С10-арилом, которые могут быть моно-, ди- или тризамещены галогеном;
2-оксо-пирролидин-1-илом, 2,5-диметилпиррол-1-илом или NR6-A-R7,
при условии, что R2, R3, R4 и R5 не могут одновременно означать водород и, по меньшей мере, один остаток R2, R3, R4 или R5 является 2-оксо-пирролидин-1-илом, 2,5-диметилпиррол-1-илом или NR6-A-R7, при значении
R6 - водород, C1-С4-алкил или C6-С10-арил-C1-С4-алкил; причем арил может быть замещен галогеном;
А означает простую связь, COn, SOn или CONH;
n равно 1 или 2;
R7 означает водород;
C1-С18-алкил или C2-С18-алкенил, которые могут быть замещены от одного до трех раз C1-С4-алкилом, C1-С4-алкилокси, N(C1-С4-алкил)2, -СООН, C1-С4-алкилоксикарбонилом, C6-С12-арилом, C6-С12-арилокси, C6-С12-арилкарбонилом, C6-С10-арил-С1-С4-алкилокси, галогеном, CF3 или оксогруппой, причем арил, в свою очередь, может быть замещен галогеном, С1-С4-алкилом, аминосульфонилом или метилмеркаптогруппой;
C6-С10-арил-С1-С4-алкил, С5-С8-циклоалкил-С1-С4-алкил, C5-С8-циклоалкил, C6-С10-арил-С2-С6-алкенил, C6-С10-арил, дифенил, дифенил-C1-С4-алкил, инданил, которые могут быть моно- или дизамещены C1-С18-алкилом, С1-С18-алкилоксигруппой, C3-С8-циклоалкилом, гидроксигруппой, C1-С4-алкилкарбонилом, C6-С10-арил-С1-С4-алкилом, C6-С10-арил-C1-С4-алкилоксигруппой, C6-С10-арилоксигруппой, нитро-, цианогруппой, C6-С10-арилом, фторсульфонилом, C1-С6-алкилоксикарбонилом, C6-С10-арилсульфонилоксигруппой, пиридилом, MHSO2-C6-С10-арилом, галогеном, CF3 или OCF3, причем арил может быть еще раз замещен галогеном, CF3 или С1-С4-алкилоксигруппой;
или группу Het-(CH2)r, где
r=0, 1, 2 или 3 и Het - насыщенный или ненасыщенный 5-7-членный гетероцикл, который содержит атомы N, О или S и может быть сконденсирован с бензолом и замещен C1-С4-алкилом, C6-С10-арилом, галогеном, С1-С4-алкилоксигруппой, C6-С10-арил-С1-С4-алкилом, C6-С10-арил-С1-С4-алкилмеркапто- или нитрогруппой, причем сконденсированный с бензолом арил, в свою очередь, может быть замещен галогеном, С1-С4-алкилоксигруппой;
а также их фармакологически приемлемые соли и аддитивные соли кислот.
R6 означает водород,
А означает простую связь, и
R7 означает C6-С10-арил-C1-С4-алкил, который может быть замещен галогеном, CF3, циано-, дифенил-C1-С4-алкил-, CF3-феноксигруппой, C5-С8-циклоалкилом или фторсульфонилоксигруппой;
C1-С12-алкил, который может быть замещен C1-С4-алкилоксигруппой, CF3;
C2-С12-алкенил или группу Het-(CH2)r-, где r=0 или 1 и Het означает насыщенный или ненасыщенный 5-7-членный гетероцикл, который может быть сконденсирован с бензолом и замещен C1-С4-алкилом или галогеном.
где R6 означает водород или метил; А означает простую связь, R7 означает водород; С1-С12-алкил, который может быть моно- или дизамещен галогеном;
С2-С18-алкенил, который может быть моно- или дизамещен С1-С4-алкилом или С1-С4-алкилоксикарбонилом;
С6-С10-арил-С1-С4-алкил, который может быть замещен галогеном, С1-С6-алкилоксигруппой, CF3, циано-, С5-С6-циклоалкилом, С1-С4-алкилоксикарбонилом, С6-С10-арил-С1-С4-алкилом, С6-С10-арил-С1-С4-алкилоксигруппой, причем арил может быть еще раз замещен галогеном или CF3; С5-С8-циклоалкил-С1-С4-алкил; или группу Het-(CH2)r,
где r=1, 2 или 3 и Het означает насыщенный или ненасыщенный 5-7-членный гетероцикл, который может быть замещен галогеном или С1-С4-алкилоксигруппой.
где R6 означает водород; А означает -СО- и R7 означает С1-С18-алкил, который может быть замещен галогеном, фенилом, феноксигруппой, фенилкарбонилом или С1-С4-алкилоксикарбонилом, причем феноксигруппа в свою очередь может быть замещена метилом, галогеном или метилмеркаптогруппой; С2-С18-алкенил, который может быть замещен С6-С10-арилом; С6-С10-арил, который может быть замещен галогеном, С1-С8-алкилом, фенил-С1-С4-алкилом, CF3, OCF3, фторсульфонилом, С1-С4-алкилоксикарбонилом, феноксигруппой, причем арил, в свою очередь, может быть замещен С1-С4-алкилоксигруппой; С6-С10арил-С1-С4-алкил, причем алкил может быть замещен метоксигруппой или CF3 и арил-галогеном;
или группу Het-(CH2)r- r,
где r=0 и Het означает насыщенный или ненасыщенный 5-7-членный гетероцикл, который может быть сконденсирован с бензолом и замещен С1-С4-алкилом, галогеном, С1-С4-алкилоксигруппой, галогенофенилом или галогено-бензилмеркаптогруппой, причем сконденсированный с бензолом арил, в свою очередь, может быть замещен галогеном или метоксигруппой.
где R6 означает водород; А означает -СО2- и R7 означает С1-С18-алкил, который замещен CF3 или фенилом; С6-С10-арил; С6-С10-арил-С1-С4-алкил, который замещен С1-С4алкилом, галогеном, CF3 или OCF3, бензилоксигруппой или фенилом; или группу Het-(СН2)r-,
где r=0 или 1 и Het означает насыщенный или ненасыщенный 5-7-членный гетероцикл, который может быть сконденсирован с бензолом и замещен С1-С4-алкилом или бензилом.
где R6 означает водород; А означает -SO2- и R7 означает С1-С6-алкил, который может быть замещен CF3; С2-С4-алкенил, который может быть замещен фенилом; С6-С10-арил, который может быть замещен С1-С6-алкилом, галогеном, С1-С4-алкилоксигруппой или бензилом; дифенил-С1-С4-алкил, замещенный галогеном; или группу Het-(СН2)r-,
где r=0 и Het означает насыщенный или ненасыщенный 5-7-членный гетероцикл.
где R6 означает водород; А означает -CO-NH- и R7 означает С1-С10-алкил, который может быть замещен С1-С4-алкилоксикарбонилом, N(С1-С4-алкил)2 или фенилом, который в свою очередь может быть замещен галогеном или аминосульфонилом; С6-С10-арил, который может быть замещен С1-С6-алкилом, С1-С6-алкилоксигруппой, С1-С6-алкилоксикарбонилом, феноксигруппой, OCF3, бензилом или пиридилом; С5-С8-циклоалкил, который может быть замещен гидроксигруппой, или инданил;
или группу Het-(CH2)r,
где r=0 или 1 и Het означает насыщенный или ненасыщенный 5-7-членный гетероцикл, который может быть замещен бензилом.
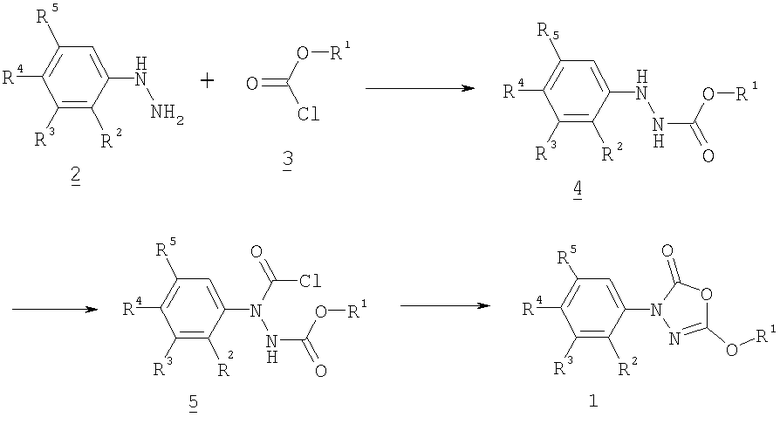
проводят взаимодействие гидразинов общей формулы 2 с эфирами хлормуравьиной кислоты формулы 3 или другими реакционноспособными производными угольной кислоты, где R1, R2, R3, R4 и R5 определены в пп.1 - 12, с образованием соединений формулы 4, которые ацилируют фосгеном, карбонилдиимидазолом, дифосгеном или трифосгеном, циклизуют и, в случае необходимости, путем дальнейших химических превращений остатков R2-R5, как, например, путем восстановления нитрогруппы в аминогруппы и последующим ацилированием или алкилированием, превращают в соединения формулы 1.
Приоритеты по пунктам:
| Приспособление в пере для письма с целью увеличения на нем запаса чернил и уменьшения скорости их высыхания | 1917 |
|
SU96A1 |
| Способ получения производных оксадиазолина | 1974 |
|
SU635870A3 |
Авторы
Даты
2006-08-10—Публикация
2001-02-20—Подача