ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
По настоящей заявке испрашивается приоритет по предварительной заявке U.S. №60/981105, поданной 18 октября 2007 г., содержание которой включено в настоящее изобретение в качестве ссылки.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Изобретение относится к улучшенным способам получения дигидротиенопиримидинов и промежуточных продуктов, применяющихся для их синтеза.
УРОВЕНЬ ТЕХНИКИ
Известно, что дигидротиенопиримидины обладают терапевтической активностью, которая делает их применимыми для лечения различных заболеваний и устранения их симптомов. Например, в патентах U.S. №3318881 и BE 663693 раскрыто получение дигидротиено[3,2-d]пиримидинов, которые воздействуют на сердечно-сосудистую систему и обладают седативной способностью. В публикации U.S. №2008/0096882 А1, которая включена в настоящее изобретение в качестве ссылки, раскрыты дигидротиенопиримидины, которые применимы для лечения респираторных или желудочно-кишечных нарушений или заболеваний, воспалительных заболеваний суставов, кожи или глаз, заболеваний периферической или центральной нервной системы или рака.
Синтез дигидротиенопиримидина включает несколько стадий и может сопровождаться затруднениями, связанными со стереоселективностью, региоселективностью и очисткой, в особенности при крупномасштабном синтезе. На первых стадиях этого синтеза можно использовать промежуточные продукты, такие как эфиры 3-оксотетрагидротиофен-2-карбоновой кислоты. Традиционный синтез эфиров 3-оксотетрагидротиофен-2-карбоновой кислоты включает регулируемую конденсацию типа Дикмана в щелочной среде, например NaH и NaOMe (Yamada et al., Tetrahedron Lett. 1981, 22, 1353). Однако сообщали, что использование обычных диэфиров при катализируемой основанием конденсацию по Дикману протекает неселективно и поэтому дает смесь региоизомеров (см. ниже уравнение 1).

Поэтому выделение отдельного региостереоизомера, использующегося в дополнительных стадиях синтеза, требует дополнительного разделения с помощью хроматографии на силикагеле. См., например, публикацию Liu et al., Can. J. С hem. 1982, 60, 437 и Li et al., Bioorg. Med. Chem. Lett. 2003, 13, 2591. Описано региоселектвиное образование а2 из a1 при воздействии TiCl4 в присутствии Et3N (Deshmukh, et al., Synth. Commun., 1996, 26, 1657). Однако это превращение приводит к одновременному образованию примесей вследствие хлорирования и дегидрогалогенирования, которые необходимо удалять с помощью хроматографии на силикагеле. Кроме того, любая методика обработки может привести к образованию больших количеств твердых веществ, которые необходимо удалять с помощью трудоемких стадий фильтрования. Аналогичным образом, использование избытка Et3N приводит к разложению продукта при крупномасштабном синтезе. Вследствие таких затруднений катализируемая посредством TiCl4 конденсация неэффективна для крупномасштабного производства. Поэтому необходима разработка эффективного и региоселективного синтеза эфира 3-оксотетрагидротиофен-2-карбоновой кислоты.
Таким образом, вся методика синтеза дигидротиенопиримидинов может быть трудоемкой вследствие необходимости проведения многократной очистки, обработки микроволновым излучением и регулирования сильно экзотермических реакций. Поэтому также необходимо оптимизировать условия реакции и уменьшить количество стадий синтеза дигидротиенопиримидинов, в особенности при крупномасштабном производстве.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
В настоящем изобретении решена задача региоселективности и устранены (а) очистка промежуточных продуктов, (б) применение микроволнового излучения на стадиях реакции и (в) сильно экзотермические реакции при получении дигидротиенопиримидинов. Одним объектом настоящего изобретения является уменьшение количества стадий синтеза для получения дигидротиенопиримидинов формулы 1:
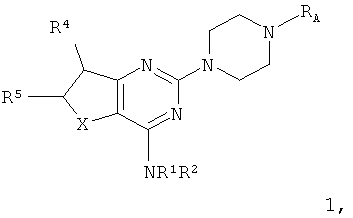
в которой:
RA обозначает остаток, выбранный из группы, включающей Het, гетероарил, и который необязательно замещен остатком, выбранным из группы, включающей галоген, С1-С3-фторалкил, CN, ОН, оксогруппу, -С1-С6-алкил, -O-R2.1, -COOR2.1, SO-R2.1, SO2-R2.1, С6-С10-арил, С1-С3-алкилен-С6-С10-арил, -C1-С3-алкилен-NR2.2R2.3, -NR2.2R2.3, С3-С10-циклоалкил, С1-С3-алкилен-С3-С10-циклоалкил, Het, гетероарил, C1-С3-алкиленгетероарил и С1-С3-алкилен-Het, который необязательно может быть замещен остатком, выбранным из группы, включающей ОН, галоген, -С1-С3-фторалкил, C1-С6-алкил, С6-С10-арил, СОО(С1-С3-алкил) и O-(С1-С3-алкил),
где
Het обозначает 3-11-членный моно- или бициклический насыщенный или частично насыщенный гетероцикл, который содержит 1, 2, 3 или 4 гетероатома, независимо выбранных из N, S и О,
гетероарил представляет собой 5-11-членный моно- или бициклический гетероарил, который содержит 1, 2, 3 или 4 гетероатома, независимо выбранных из N, S и О,
где
циклоалкил является насыщенным или частично насыщенным,
или в которой
RA обозначает

и где Х обозначает SO или SO2, предпочтительно SO;
R1 обозначает Н, C1-С6-алкил, С2-С6-алкенил, С2-С6-алкинил, С6-С10-арил, С6-С10-арил-С1-С6-алкилен или С5-С10-гетероарил-С1-С6-алкилен;
R2 обозначает Н или группу, выбранную из группы, включающей С1-С10-алкил, С2-С6-алкенил и С2-С6-алкинил, который необязательно может быть замещен галогеном, и которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей OR2.1, COOR2.1, CONR2.2R2.3, SR2.1, С6-С10-арил, моно- или бициклический С3-С10-гетероцикл, моно- или бициклический С5-С10-гетероарил, моно- или бициклический С3-С10-циклоалкил, СН2-NR2.2R2.3 и NR2.2R2.3, которая, в свою очередь, необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, галоген, OR2.1, оксогруппу, C1-С6-алкил, С6-С10-арил, COOR2.1, CH2-NR2.2R2.3 и NR2.2R2.3,
где R2.1 обозначает Н или группу, выбранную из группы, включающей C1-С6-алкил, C1-С6-алканол, C1-С3-галогеналкил, моно- или бициклический С3-С10-циклоалкил, С6-С10-арил-С1-С6-алкилен, моно- или бициклический С5-С10-гетероарил-С1-С6-алкилен, С3-С10-гетероцикл-С1-С6-алкилен, С3-С10-циклоалкил-С1-С6-алкилен, моно- или бициклический С5-С10-арил, моно- или бициклический С5-С10-гетероарил и моно- или бициклический, насыщенный или ненасыщенный гетероцикл, которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, галоген, С1-С6-алкил и С6-С10-арил,
где R2.2 и R2.3 независимо друг от друга обозначают Н или группу, выбранную из группы, включающей галоген, C1-С6-алкил, моно- или бициклический С3-С10-циклоалкил, С6-С10-арил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, моно- или бициклический С6-С10-арил, моно- или бициклический С3-С10-гетероцикл, моно- или бициклический С5-С10-гетероарил, CO-NH2, СО-NНСН3, СО-N(СН3)2, SO2(С1-С2-алкил), CO-R2.1 и COOR2.1, которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, галоген, C1-С6-алкил, С6-С10-арил и COOR2.1,
или
R2 обозначает моно- или полициклический С3-С10-циклоалкил, который необязательно может содержать мостик из одной или более С1-С3-алкильных групп и который необязательно может быть замещен группой, выбранной из группы, включающей разветвленный или неразветвленный С1-С6-алканол, OR2.1, COOR2.1, SO2NR2.2R2.3, С3-С10-гетероцикл, С6-С10-арил, С1-С6-алкил, С6-С10-арил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, моно- или бициклический С3-С10-циклоалкил и NR2.2R2.3, которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, галоген, C1-С6-алкил, С6-С10-арил и NR2.2R2.3,
или
R2 обозначает моно- или полициклический С6-С10-арил, который необязательно может быть замещен ОН, SH или галогеном или одной или более группой, выбранной из группы, включающей OR2.1, COOR2.1, NR2.1R2.3, СН2-NR2.2R2.3, С3-С10-циклоалкил, С3-С10-гетероцикл, С1-С6-алкил, С6-С10-арил-С1-С6-алкилен, С3-С10-гетероцикл-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, С6-С10-арил, SO2-СН3, SO2-СН2СН3 и SO2-NR2.2R2.3, которая, в свою очередь, необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, галоген, C1-С6-алкил, С6-С10-арил,
или
R2 обозначает группу, выбранную из группы, включающей моно- или бициклический насыщенный или ненасыщенный С3-С10-гетероцикл и моно- или бициклический С5-С10-гетероарил, который включает от 1 до 4 гетероатомов, выбранных из S, О и N, и необязательно может быть замещена одной или более группой, выбранной из группы, включающей галоген, ОН, оксогруппу и SH, или одной или более группой, выбранной из группы, включающей OR2.1, SR2.1, COOR2.1, COR2.1, C1-С6-алканол, С3-С10-циклоалкил, С6-С10-арил, C1-С6-алкил, С6-С10-арил-C1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, С5-С10-гетероцикл, С5-С10-гетероарил, C1-С6-алканол и NR2.2R2.3, которая, в свою очередь, необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, галоген, C1-С6-алкил, С6-С10-арил, CH2-NR2.2R2.3 и NR2.2R2.3;
или где
NR1R2 вместе обозначают гетероциклическое С4-С7-кольцо, которое необязательно может содержать мостик, которое содержит 1, 2 или 3 гетероатома, выбранных из N, О и S, и которое необязательно может быть замещено одной или более группой, выбранной из группы, включающей ОН, OR2.1, C1-С6-алканол, оксогруппу, галоген, C1-С6-алкил, С6-С10-арил, COOR2.1, CH2-NR2.2-COO-R2.1, CH2-NR2.2-CO-R2.1, CH2-NR2.2-CO-CH2-NR2.2R2.3, CH2-НR2.2-С1-С3-алкил, CH2-NR2.2-SO2-NR2.2R2.3, CH2-NR2.2-CO-NR2.2R2.3, СО-NR2.2R2.3 и NR2.2R2.3;
R3 выбран из группы, включающей фтор, хлор, бром, йод, гидроксигруппу, SO2-СН3, COOR2.1, нитрильную группу и С3-С10-гетероцикл-С1-С6-алкилен, где С3-С10-гетероцикл может быть моно- или бициклическим и необязательно может быть замещен группой, выбранной из группы, включающей ОН, галоген, оксогруппу, C1-С6-алкил и С6-С10-арил,
или
обозначает группу, выбранную из группы, включающей C1-С6-алкил, С2-С6-алкенил, С2-С6-алкинил, С6-С10-арил, С6-С10-арил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, С3-С10-гетероцикл и С3-С10-циклоалкил, который необязательно может быть замещен группой, выбранной из группы, включающей ОН, галоген, оксогруппу, С1-С6-алкил и С6-С10-арил,
или
R3 обозначает группу -CO-NR3.1R3.2,
в которой R3.1 и R3.2 независимо друг от друга обозначают Н или группу, выбранную из группы, включающей C1-С6-алкил, С2-С6-алкенил, С2-С6-алкинил, С6-С10-арил, С6-С10-арил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкинилен, С5-С10-гетероарил-С1-С6-алкенилен, моно- или бициклический С3-С10-гетероцикл, С3-С10-гетероцикл-С1-С6-алкилен и моно- или бициклический С5-С10-гетероарил, где в каждом случае группа необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, оксогруппу, галоген, С1-С6-алкил и O-C1-С6-алкил,
или
R3 обозначает группу -NR3.3-CO-R3.4,
в которой R3.3 обозначает Н или группу, выбранную из группы, включающей С1-С6-алкил, С2-С6-алкенил, С2-С6-алкинил, С6-С10-арил, С6-С10-арил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, С3-С10-гетероцикл и С5-С10-гетероарил, которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, NH2, NR2.2R2.3, галоген, C1-С6-алкил и С6-С10-арил, и
в которой R3.4 обозначает Н или группу, выбранную из группы, включающей C1-С6-алкил, С1-С6-алкенил, С2-С6-алкинил, C1-С6-алканол, OR2.1, СН2-О-СО-С1-С6-алкил, CH2-NR2.2R2.3, NR2.2R2.3, С6-С10-арил, С6-С10-арил-С1-С6-алкилен, C5-С10-гетероарил-С1-С6-алкилен, моно- или бициклический, насыщенный, частично насыщенный или ненасыщенный С3-С10-гетероцикл, содержащий 1, 2 или 3 гетероатома, выбранных из S, О и N, и моно- или бициклический С5-С10-гетероарил, содержащий 1, 2 или 3 гетероатома, выбранных из S, О и N, которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, NH2, NR2.2R2.3, галоген, C1-С6-алкил и С6-С10-арил,
или
R3 обозначает необязательно моно- или ди-Н-замещенную сульфонамидную группу SO2-NR3.5R3.6,
в которой R3.5 и R3.6 все независимо друг от друга могут обозначать C1-С6-алкил
или С6-С10-арил;
и
R4 и R5 независимо выбраны из группы, включающей Н, С1-С6-алкил, С2-С6-алкенил, С2-С6-алкинил, С6-С10-арил, С6-С10-арил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, С3-С10-гетероцикл и С5-С10-гетероарил, -О-С1-С6-алкил, -O-С6-С10-арил, -O-С3-С10-гетероцикл и -O-С5-С10-гетероарил, -NR'R", фтор, C1-С6-фторалкил и C1-С6-фторалкоксигруппу, где R' и R" независимо выбраны из группы, включающей Н и C1-С6-алкил, и где в каждом случае группа необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, оксогруппу, галоген, C1-С6-алкил и O-C1-С6-алкил.
Настоящее изобретение предпочтительно относится к способу получения соединения формулы 1, где
RA обозначает
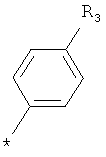
Z обозначает галоген;
Х обозначает SO;
R1 обозначает Н или метил;
R2 обозначает Н или группу, выбранную из группы, включающей С1-С10-алкил, С2-С6-алкенил и С2-С6-алкинил, который необязательно может быть замещен галогеном, и которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей OR2.1, COOR2.1, CONR2.2R2.3, SR2.1, С6-С10-арил, моно- или бициклический С3-С10-гетероцикл, моно- или бициклический С3-С10-гетероарил, моно- или бициклический С3-С10-циклоалкил, СН2-NR2.2R2.3 и NR2.2R2.3, которая, в свою очередь, необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, галоген, OR2.1, оксогруппу, C1-С6-алкил, С6-С10-арил, COOR2.1, СН2-НR2.2R2.3 и NR2.2R2.3,
где R2.1 обозначает Н или группу, выбранную из группы, включающей С1-С6-алкил, C1-С6-алканол, C1-С3-галогеналкил, моно- или бициклический С3-С10-циклоалкил, С6-С10-арил-С1-С6-алкилен, моно- или бициклический С5-С10-гетероарил-С1-С6-алкилен, С3-С10-гетероцикл-С1-С6-алкилен, С3-С10-циклоалкил-С1-С6-алкилен, моно- или бициклический С6-С10-арил, моно- или бициклический С5-С10-гетероарил и моно- или бициклический насыщенный или ненасыщенный гетероцикл, которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, галоген, С1-С6-алкил и С6-С10-арил,
где R2.2 и R2.3 независимо друг от друга обозначают Н или группу, выбранную из группы, включающей галоген, С1-С6-алкил, моно- или бициклический С3-С10-циклоалкил, С6-С10-арил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, моно- или бициклический С6-С10-арил, моно- или бициклический С3-С10-гетероцикл, моно- или бициклический С5-С10-гетероарил, CO-NH2, СО-NНСН3, СО-N(СН3)2, SO2(С1-С2-алкил), CO-R2.1 и COOR2.1, которая необязательно может быть замещена одной или более группой, выбранной из группы,
включающей ОН, галоген, С1-С6-алкил, С6-С10-арил и COOR2.1, или R2 обозначает моно- или полициклический С5-С10-циклоалкил, который необязательно может содержать мостик из одной или более C1-С3-алкильных групп и который необязательно может быть моно- или полизамещен ОН, или галогеном, или одной или более группой, выбранной из группы, включающей разветвленный или неразветвленный C1-С3-алканол, OR2.1, COOR2.1, SO2NR2.2R2.3, С5-С10-гетероцикл, фенил, С1-С6-алкил, фенил-С1-С6-алкилен, С5-С6-гетероарил-С1-С6-алкилен, моно- или бициклический С5-С10-циклоалкил и NR2.2R2.3, которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, галоген, C1-С6-алкил, фенил и NR2.2R2.3,
или где NR1R2 вместе обозначают гетероциклическое С4-С7-кольцо, которое необязательно может содержать мостик, которое содержит 1, 2 или 3 гетероатома, выбранных из N, О и S, и который необязательно может быть замещен одной или более группой, выбранной из группы, включающей ОН, OR2.1, С1-С6-алканол, оксогруппу, галоген, C1-С6-алкил, С6-С10-арил, COOR2.1, CH2-NR2.2-COO-R2.1, CH2-NR2.2-CO-R2.1, CH2-NR2.2-CO-CH2-NR2.2R2.3, СН3-NR2.2-SO2-C1-C3-aлкил, CH2-NR2.2-SO2-NR2.2R2.3, CH2-NR2.2-CO-NR2.2R2.3, СО-NR2.2R2.3 и NR2.2R2.3;
R3 обозначает фтор, хлор, бром, йод или CN; и
R4 и R5 независимо выбраны из группы, включающей Н и C1-С6-алкил.
В другом предпочтительном варианте осуществления настоящее изобретение относится к способу получения соединения формулы 1, где RA обозначает

R2 обозначает С1-С10-алкил, который необязательно может быть замещен одной или более группой, выбранной из группы, включающей OR2.1, COOR2.1 и С6-С10-арил, где R2.1 обозначает Н,
или R2 обозначает моноциклический С5-С10-циклоалкил,
или в которой NR1R2 вместе обозначают гетероциклическое С4-С7-кольцо.
В еще одном предпочтительном варианте осуществления настоящее изобретение относится к способу получения соединения формулы 1, где RA обозначает

Z обозначает хлорид;
Х обозначает SO;
R1 обозначает Н; и
R4 и R5 независимо обозначают Н или метил.
В еще одном предпочтительном варианте осуществления настоящее изобретение относится к способу получения соединения формулы 1, где RA обозначает

Z обозначает хлорид;
Х обозначает SO;
R1 обозначает Н;
R3 обозначает хлорид; и R и R независимо обозначают Н или метил.
В другом предпочтительном варианте осуществления настоящее изобретение относится к способу получения соединения формулы 1, где
RA обозначает моноциклическое 5- или 6-членное гетероарильное кольцо, которое необязательно замещено группой, выбранной из группы, включающей F, Сl, Вr, СF3, СНF3, CH2F, CN, ОН, -метил, этил, пропил, изопропил, -O-метил, O-этил, -СООметил, -СООэтил, SO2-(СН3), SO-(СН3), SO2-(СН2СН3), SO-(СН2СН3), фенил, -метиленфенил, -этиленфенил, -NH2, -NН(СН3), N(СН3)2, -метилен-NН2, -метилен-NН(СН3), -метилен-N(СН3)2, С3-С6-циклоалкил, -метилен-С3-С6-циклоалкил, насыщенный или частично насыщенный 5-6-членный гетероцикл, 5-6-членный гетероарил и -Het, который необязательно может быть замещен остатком, выбранным из группы, включающей ОН, F, Сl, Вr, СF3, СНF2, СН2F, метил, этил, пропил, изопропил, фенил, -СОО(СН3), -O-метил и -O-этил.
В еще одном предпочтительном варианте осуществления настоящее изобретение относится к способу получения соединения формулы 1, где
RA обозначает бициклический 9-11-членный насыщенный, ненасыщенный или частично насыщенный гетероцикл, который необязательно замещен остатком, выбранным из группы, включающей F, Сl, Вr, СF3, CHF2, СН2F, CN, ОН, -метил, этил, пропил, изопропил, -O-метил, O-этил, -СООметил, -СООэтил, SO2-(СН3), SO-(СН3), SO2-(СН2СН3), SO-(СН2СН3), фенил, -метиленфенил, -этиленфенил, -NH2, -NН(СН3), N(СН3)2, -метилен-NН2, -метилен-NН(СН3), -метилен-N(СН3)2, -С3-С6-циклоалкил, -метилен-С3-С6-циклоалкил, насыщенный, частично насыщенный или ненасыщенный, 5-6-членный гетероцикл, 5-6-членный гетероарил, метиленгетероарил и -метилен-Het,
который необязательно может быть замещен остатком, выбранным из группы, включающей ОН, F, Сl, Вr, СF3, CHF2, CH2F, метил, этил, пропил, изопропил, фенил, -СОО(СН3), -O-метил и -O-этил.
В еще одном предпочтительном варианте осуществления настоящее изобретение относится к способу получения соединения формулы 1, где
RA обозначает моноциклическое 5-6-членное гетероарильное кольцо, выбранное из группы, включающей пиррол, пиразол, фуран, тиофен, тиазол, имидазол, оксазол, пиридазин, пиримидин, пиразин, тиадиазол, оксадиазол, изооксазол, изотиазол и пиридин, которое необязательно замещено остатком, выбранным из группы, включающей F, Cl, Вr, СF3, CHF2, CH2F, CN, ОН, -метил, этил, пропил, изопропил, -O-метил, O-этил, -СООметил, -СООэтил, SO2-(СН3), SO2-(СН2СН3), фенил, -метиленфенил, -этиленфенил, -NH2, -NН(СН3), N(CH3)2, -метилен-NН2, -метилен-NН(СН3), -метилен-N(СН3)2, С3-С6-циклоалкил, метилен-С3-С6-циклоалкил, Het, гетероарил, -метиленгетероарил и -метилен-Het, где этот остаток также необязательно может быть замещен одним или большим количеством остатков, выбранных из группы, включающей ОН, F, Cl, Вr, СF3, CHF2, CH2F, метил, этил, пропил, изопропил, фенил, -СОО(СН3), -O-метил и -O-этил.
В еще одном предпочтительном варианте осуществления настоящее изобретение относится к способу получения соединения формулы 1, где
RA обозначает бициклический 9-11-членный гетероцикл, выбранный из группы, включающей бензоксазол, бензодиоксол, дигидробензодиоксин, бензодиоксин, бензизоксазол, бензотиазол, бензизотиазол, тиенопиримидин, фуропиримидин, тиенопиридин, фуропиридин, индол, изоиндол, хиноксалин, нафтиридин, пиридопиразин, пиридопиримидин, хинолин, изохинолин, бензимидазол, 6, 7, 8, 9-тетрагидро-5Н-пиразино[2,3-d]азепин, бензотиофен, бензофуран, хиназолин, индазол, изобензофуран и птеридин, и этот остаток необязательно может быть замещен другим остатком, выбранным из группы, включающей F, Cl, Вr, СF3, CHF2, CH2F, CN, ОН, -метил, этил, пропил, изопропил, -O-метил, O-этил, -СООметил, -СООэтил, SO2-(СН3), SO2-(СН2СН3), фенил, -метиленфенил, -этиленфенил, -NH2, -NH(CH3), N(CH3)2, -метилен-NН2, -метилен-NН(СН3), -метилен-N(СН3)2, С3-С6-циклоалкил, метилен-С3-С6-циклоалкил, Het, гетероарил, -метиленгетероарил и -метилен-Het, и этот остаток также необязательно может быть замещен другим остатком, выбранным из группы, включающей ОН, F, Cl, Вr, СF3, CHF2, CH2F, метил, этил, пропил, изопропил, фенил, -СОО(СН3), -O-метил и -O-этил.
Способ, предлагаемый в настоящем изобретении, относится к получению дигидротиенопиримидинов формулы I:

и включает стадии:
а) галогенирования, сульфонирования или присоединения отщепляющейся группы промежуточного продукта формулы 4:

с получением промежуточного продукта формулы 3:

б) стереоселективного окисления промежуточного продукта формулы 3 с получением промежуточного продукта формулы 2:

в) взаимодействия промежуточного продукта формулы 2 с реагентом формулы HNR1R2 с получением соединения формулы 1;
в которой Z обозначает галоген, предпочтительно Сl, сульфонильную или сульфонатную отщепляющуюся группу, выбранную из группы, включающей тозилат, мезилат, безилат, брозилат, трифлат и нозилат, или отщепляющуюся группу, выбранную из группы, включающей F, NO2 или N2, R1-R5 и Х являются такими, как определено в настоящем изобретении, и стадии реакции проводят без необходимости хроматографической очистки промежуточных продуктов.
Альтернативно, настоящее изобретение относится к способу получения дигидротиенопиримидинов формулы 1:

который включает стадии:
а) галогенирования, сульфонирования или присоединения отщепляющейся группы промежуточного продукта формулы 4:

с получением промежуточного продукта формулы 3:

б) взаимодействия промежуточного продукта формулы 3 с реагентом формулы HNR1R2 с получением соединения формулы 8;

в) стереоселективного окисления промежуточного продукта формулы 8 с получением соединения формулы 1;
в которой RA, R1-R5, Z, Het, гетероарил, циклогексил и Х являются такими, как определено в настоящем изобретении, и стадии реакции проводят без необходимости хроматографической очистки промежуточных продуктов.
В предпочтительном варианте осуществления стадию галогенирования (а) проводят в присутствии РОСl3, SOCl2, SO2Cl2, (СОСl)2, PCl5, РОСl3/РСl5, Cl2 или NCS (N-хлорсукцинимид) в растворителе. Предпочтительно, если растворителем является ацетонитрил, метиленхлорид, толуол или хлороформ.
В другом предпочтительном варианте осуществления стадии окисления (б) или (в) в описанных выше способах проводят в присутствии системы хиральный лиганд/металл, стехиометрического количества окислительного реагента и растворителя. Предпочтительно, если системой хиральный лиганд/металл является Ti/BINOL (1,1'-бинафтол), замещенный BINOL, WО3/хиральный лиганд, оксазиридин Дэвиса, D-эпоксон/оксон, Mn/Salen, Ti/варианты гидробензоина, Ti/миндальная кислота, Ti/DET, V(acac)2 или Fе(асас)3/хиральный лиганд и использующимся в стехиометрическом количестве окислительным реагентом является гидропероксид кумола, пероксид водорода, раствор трет-бутилгидропероксида, МСРВА (м-хлорпербензойная кислота), пероксибензойные кислоты, оксон или диоксираны. Предпочтительно, если растворителем является толуол, метиленхлорид, хлороформ, ацетонитрил, ТГФ (тетрагидрофуран) или фторбензол.
В другом предпочтительном варианте осуществления стадии реакции (в) или (б) в описанных выше способах проводят в присутствии основания и растворителя. Предпочтительно, если основание выбрано из группы, включающей: амины, NaOH, NaH, t-BuONa, t-BuOK, DBU (1,8-диазабицикло[5.4.0]ундец-7-ен), KN(TMS)2, NaN(TMS)2, LiN(TMS)2 и LDA (диизопропиламид лития), и предпочтительно, если растворитель выбран из группы, включающей: ТГФ, диглим, ДМСО (диметилсульфоксид), NMP (N-метилпирролидон), DMAc, ацетонитрил и воду.
Настоящее изобретение также относится к промежуточным продуктам формулы 4:

в которой R3 является таким, как определено в настоящем изобретении, и при условии, что R4 и R5 оба не могут обозначать Н.
Настоящее изобретение также относится к промежуточным продуктам формулы 4:

в которой R3 является таким, как определено в настоящем изобретении, и при условии, что R4 и R5 не обозначают Н.
Настоящее изобретение также относится к способу получения промежуточных продуктов формулы 4, который включает взаимодействие промежуточного продукта формулы 5:

с промежуточным продуктом формулы 6:

в присутствии основания с получением промежуточного продукта формулы 4, в которой Ra обозначает алкил и более предпочтительно метил и RA, R4-R5 являются такими, как определено в настоящем изобретении.
Другим объектом настоящего изобретения является способ получения промежуточных продуктов формулы 4, который включает взаимодействие промежуточного продукта формулы 5:

с промежуточным продуктом формулы 6:

в присутствии основания с получением промежуточного продукта формулы 4, в которой Ra обозначает алкил и RA, R4 и R5 являются такими, как определено в настоящем изобретении. В предпочтительном варианте осуществления основанием является алкоксид или гидрид натрия в комбинации с растворителем, где алкоксидом предпочтительно является t-BuOK, t-BuONa, NaOMe, NaOEt, n-BuLi или t-BuLi и гидрид натрия используют в комбинации с МеОН, NaOH, i-РrОН или f-BuOH.
В предпочтительном варианте осуществления R4 и R5 независимо обозначают Н или метил. В другом предпочтительном варианте осуществления Ra обозначает метил. Более предпочтительно, если R4 и R5 обозначают H и Ra обозначает метил.
Другим объектом настоящего изобретения является практический региоселективный синтез эфиров 3-оксотетрагидротиофен-2-карбоновой кислоты без образования нежелательных региоизомеров, таких как а3 в уравнении 1. Например, настоящее изобретение относится к способу получения промежуточных продуктов формулы 6:

включающему стадии:
а) взаимодействия реагентов формул HS-CH2-CO2Ra и CHR5=CR4-СО2Ra с получением промежуточного продукта формулы 7:

б) циклизации промежуточного продукта формулы 7 в растворителе с получением промежуточного продукта формулы 6, в которой Ra, R4-R5 являются такими, как определено в настоящем изобретении; и в которой промежуточный продукт формулы 6 можно использовать на следующей стадии реакции без необходимости проведения хроматографической очистки на этой стадии или необязательно на всех последующих стадиях.
Сложный тиоэфир и α,β-ненасыщенный сложный эфир формул HS-CH2-CO2Ra и CHR5=CR4-CO2Ra соответственно можно ввести в реакцию при условиях, известных в данной области техники, например, с пиперидином с получением промежуточного продукта формулы 7.
В предпочтительных вариантах осуществления указанную выше стадию реакции (а) проводят в присутствии основания и стадию циклизации (б) проводят в присутствии TiCl4, TiCl2(OiPr)2, ТiСl(OiРr)3, ТiСl3(OiРr) или их хиральных вариантов и в присутствии амина-основания, такого как диизопропилэтиламин или триэтиламин. В предпочтительном варианте осуществления хиральным вариантом является BINOL, замещенный BINOL, хиральные диолы, BINAP (2,2'-бис(дифенилфосфино)-1,1'-бинафтил), DuPhos, Taddols или тартраты.
В еще одном предпочтительном варианте осуществления указанную выше стадию циклизации (б) проводят в присутствии SnХ4, СuХ2 или NiX2, где Х обозначает Сl, Вr или OTf, и необязательно в присутствии основания. Растворителем может быть спиртовый или неспиртовый растворитель, предпочтительно - неспиртовый растворитель. Стадию циклизации (б) можно провести при температуре в диапазоне от 0 до -78ºС.
В одном варианте осуществления настоящего изобретения соединениями, полученными с помощью указанных выше способов, являются:
метиловый эфир (R)-2-{(R)-2-[4-(4-хлорфенил)пиперазин-1-ил]-5-оксо-6,7-дигидро-5Н-5λ4-тиено[3,2-d]пиримидин-4-иламино}-3-метилмасляной кислоты;
(R)-2-{(R)-2-[4-(4-хлорфенил)пиперазин-1-ил]-5-оксо-6,7-дигидро-5Н-5λ4-тиено[3,2-d]пиримидин-4-иламино}-3-метилбутан-1-ол;
{(R)-2-[4-(4-хлорфенил)пиперазин-1-ил]-5-оксо-6,7-дигидро-5Н-5λ4-тиено[3,2-d]пиримидин-4-ил}-((S)-1-фенилэтил)амин;
{(R)-2-[4-(4-хлорфенил)пиперазин-1-ил]-5-оксо-6,7-дигидро-5Н-5λ4-тиено[3,2-d]пиримидин-4-ил}циклогексиламин; и
(R)-2-[4-(4-хлорфенил)пиперазин-1-ил]-4-пиперидин-1-ил-6,7-дигидротиено[3,2-d]-пиримидин-5-оксид.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Определения терминов и использующиеся обозначения
Терминам, специально не определенным в настоящем изобретении, следует придавать значения, которые им придал бы специалист в данной области техники с учетом описания и контекста. Однако при использовании в настоящей заявке и прилагаемой формуле изобретения, если не указано иное, приведенные ниже термины обладают указанными значениями и используются указанные ниже обозначения.
А. Химическая номенклатура, термины и обозначения
Если не указано иное, все заместители не зависят друг от друга. Если, например, может быть несколько С1-С6-алкильных групп в качестве заместителей одной группы, то в случае трех C1-С6-алкильных заместителей один может означать метил, один н-пропил и один трет-бутил.
В объеме настоящей заявки в определениях возможных заместителей они также могут быть приведены в виде структурной формулы. Звездочка (*) в структурной формуле заместителя означает положение присоединения к остальной части молекулы. Кроме того, атом заместителя, расположенный после положения присоединения, означает атом в положении 1. Так, например, группы N-пиперидинил (I), 4-пиперидинил (II), 2-толил (III), 3-толил (IV) и 4-толил (V) имеют вид:





Если в структурной формуле заместителя звездочка (*) отсутствует, то каждый атом в заместителе водорода может быть удален и образовавшаяся таким образом свободная валентность может использоваться для присоединения к остальной части молекулы. Так, например, VI может означать 2-толил, 3-толил, 4-толил и бензил.

Термин "С1-С10-алкил" (включая являющиеся частями других групп) означает разветвленные и неразветвленные алкильные группы, содержащие от 1 до 10 атомов углерода, термин "С1-С6-алкил" соответственно означает разветвленные и неразветвленные алкильные группы, содержащие от 1 до 6 атомов углерода. "С1-С4-алкил" соответственно означает разветвленные и неразветвленные алкильные группы, содержащие от 1 до 4 атомов углерода. Алкильные группы, содержащие от 1 до 4 атомов углерода, являются предпочтительными. Примеры включают: метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, изопентил, неопентил или гексил. Для указанных выше групп также необязательно могут использоваться аббревиатуры Me, Et, n-Рr, i-Рr, n-Вu, i-Bu, t-Bu и т.п. Если не указано иное, то определения пропила, бутила, пентила и гексила включают все изомерные формы указанных групп. Так, например, пропил включает н-пропил и изопропил, бутил включает изобутил, втор-бутил и трет-бутил и т.п.
Термин "C1-С6-алкилен" (включая являющиеся частями других групп) означает разветвленные и неразветвленные алкиленовые группы, содержащие от 1 до 6 атомов углерода, и термин "С1-С4-алкилен" означает разветвленные и неразветвленные алкиленовые группы, содержащие от 1 до 4 атомов углерода. Алкиленовые группы, содержащие от 1 до 4 атомов углерода, являются предпочтительными. Примеры включают: метилен, этилен, пропилен, 1-метилэтилен, бутилен, 1-метилпропилен, 1,1-диметилэтилен, 1,2-диметилэтилен, пентилен, 1,1-диметилпропилен, 2,2-диметилпропилен, 1,2-диметилпропилен, 1,3-диметилпропилен и гексилен. Если не указано иное, определения пропилена, бутилена, пентилена и гексилена включают все изомерные формы указанных групп с таким же количеством атомов углерода. Так, например, пропил также включает 1-метилэтилен и бутилен включает 1-метилпропилен, 1,1-диметилэтилен, 1,2-диметилэтилен.
Если углеродная цепь должна быть замещена группой, которая вместе с одним или двумя атомами углерода алкиленовой цепи образует карбоциклическое кольцо, содержащее 3, 5 или 6 атомов углерода, то она включает, в частности, следующие примеры колец:


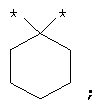


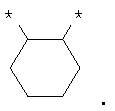
Термин "С2-С6-алкенил" (включая являющиеся частями других групп) означает разветвленные и неразветвленные алкенильные группы, содержащие от 2 до 6 атомов углерода, и термин "С2-С4-алкенил" означает разветвленные и неразветвленные алкенильные группы, содержащие от 2 до 4 атомов углерода при условии, что они содержат по меньшей мере одну двойную связь. Алкенильные группы, содержащие от 2 до 4 атомов углерода, являются предпочтительными. Примеры включают: этинил или винил, пропенил, бутенил, пентенил и гексенил. Если не указано иное, определения пропенил, бутенил, пентенил и гексенил включают все изомерные формы указанных групп. Так, например, пропенил включает 1-пропенил и 2-пропенил, бутенил включает 1-, 2- и 3-бутенил, 1-метил-1-пропенил, 1-метил-2-пропенил и т.п.
Термин "С2-С6-алкенилен" (включая являющиеся частями других групп) означает разветвленные и неразветвленные алкениленовые группы, содержащие от 2 до 6 атомов углерода, и термин "С2-С4-алкенилен" означает разветвленные и неразветвленные алкиленовые группы, содержащие от 2 до 4 атомов углерода.
Алкениленовые группы, содержащие от 2 до 4 атомов углерода, являются предпочтительными. Примеры включают: этенилен, пропенилен, 1-метилэтенилен, бутенилен, 1-метилпропенилен, 1,1-диметилэтенилен, 1,2-диметилэтенилен, пентенилен, 1,1-диметилпропенилен, 2,2-диметилпропенилен, 1,2-диметилпропенилен, 1,3-диметилпропенилен или гексенилен. Если не указано иное, определения пропенилен, бутенилен, пентенилен и гексенилен включают все изомерные формы указанных групп с таким же количеством атомов углерода. Так, например, пропенил также включает 1-метилэтенилен и бутенилен включает 1-метилпропенилен, 1,1-диметилэтенилен, 1,2-диметилэтенилен.
Термин "С2-С6-алкинил" (включая являющиеся частями других групп) означает разветвленные и неразветвленные алкинильные группы, содержащие от 2 до 6 атомов углерода, и термин "С2-С4-алкинил" означает разветвленные и неразветвленные алкинильные группы, содержащие от 2 до 4 атомов углерода при условии, что они содержат по меньшей мере одну тройную связь. Алкинильные группы, содержащие от 2 до 4 атомов углерода, являются предпочтительными. Примеры включают: этинил, пропинил, бутинил, пентинил и гексинил. Если не указано иное, определения пропинил, бутинил, пентинил и гексинил включают все изомерные формы указанных групп. Так, например, пропинил включает 1-пропинил и 2-пропинил, бутинил включает 1-, 2- и 3-бутинил, 1-метил-1-пропинил, 1-метил-2-пропинил и т.п.
Термин "С2-С6-алкинилен" (включая являющиеся частями других групп) означает разветвленные и неразветвленные алкиниленовые группы, содержащие от 2 до 6 атомов углерода, и термин "С2-С4-алкинилен" означает разветвленные и неразветвленные алкиленовые группы, содержащие от 2 до 4 атомов углерода. Алкиниленовые группы, содержащие от 2 до 4 атомов углерода, являются предпочтительными. Примеры включают: этинилен, пропинилен, 1-метилэтинилен, бутинилен, 1-метилпропинилен, 1,1-диметилэтинилен, 1,2-диметилэтинилен,пентинилен, 1,1-диметилпропинилен, 2,2-диметилпропинилен, 1,2-диметилпропинилен, 1,3-диметилпропинилен и гексинилен. Если не указано иное, определения пропинилен, бутинилен, пентинилен и гексинилен включают все изомерные формы указанных групп с таким же количеством атомов углерода. Так, например, пропинил также включает 1-метилэтинилен и бутинилен включает 1-метилпропинилен, 1,1-диметилэтинилен, 1,2-диметилэтинилен.
Термин "арил" (включая являющиеся частями других групп) означает ароматические кольцевые системы, содержащие от 6 до 10 атомов углерода. Примеры включают: фенил или нафтил, предпочтительной арильной группой является фенил. Если не указано иное, то ароматические группы могут быть замещены одной или более группой, выбранной из группы, включающей метил, этил, изопропил, трет-бутил, гидроксигруппу, фтор, хлор, бром и йод.
Термин "арил-С1-С6-алкилен" (включая являющиеся частями других групп) означает разветвленные и неразветвленные алкиленовые группы, содержащие от 1 до 6 атомов углерода, которые замещены ароматической кольцевой системой, содержащей 6 или 10 атомов углерода. Примеры включают: бензил, 1- или 2-фенилэтил или 1- или 2-нафтилэтил. Если не указано иное, то ароматические группы могут быть замещены одной или более группой, выбранной из группы, включающей метил, этил, изопропил, трет-бутил, гидроксигруппу, фтор, хлор, бром и йод.
Термин "гетероарил-С1-С6-алкилен" (включая являющиеся частями других групп) означает - хотя уже включенные в термин "арил-С1-С6-алкилен" - разветвленные и неразветвленные алкиленовые группы, содержащие от 1 до 6 атомов углерода, которые замещены гетероарилом.
Гетероарил такого типа включает 5- или 6-членные гетероциклические ароматические группы или 5-10-членные бициклические гетероарильные кольца, которые могут содержать 1, 2 или 3 гетероатома, выбранных из группы, включающей кислород, серу и азот, и содержит количество сопряженных двойных связей, достаточное для образования ароматической системы. Ниже приведены примеры 5- или 6-членных гетероциклических ароматических групп:
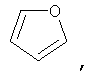
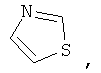






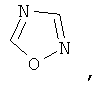
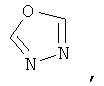


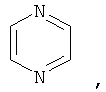


Если не указано иное, то эти гетероарилы могут быть замещены одной или более группой, выбранной из группы, включающей метил, этил, изопропил, трет-бутил, гидроксигруппу, фтор, хлор, бром и йод.
Ниже приведены примеры гетероарил-С1-С6-алкиленов:

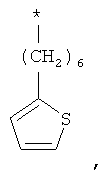



Термин "С1-С6-галогеналкил" (включая являющиеся частями других групп) означает разветвленные и неразветвленные алкильные группы, содержащие от 1 до 6 атомов углерода, которые замещены одним или большим количеством атомов галогенов. Термин "С1-С4-алкил" означает разветвленные и неразветвленные алкильные группы, содержащие от 1 до 4 атомов углерода, которые замещены одним или большим количеством атомов галогенов. Алкильные группы, содержащие от 1 до 4 атомов углерода, являются предпочтительными. Примеры включают: СF3, СНF2, СН2F, СН2СF3.
Термин "С3-С7-циклоалкил" (включая являющиеся частями других групп) означает циклические алкильные группы, содержащие от 3 до 7 атомов углерода. Примеры включают: циклопропил, циклобутил, циклопентил, циклогексил или циклогептил. Если не указано иное, то циклические алкильные группы могут быть замещены одной или более группой, выбранной из группы, включающей метил, этил, изопропил, трет-бутил, гидроксигруппу, фтор, хлор, бром и йод.
Термин "С3-С10-циклоалкил", кроме того, означает моноциклические алкильные группы, содержащие от 3 до 7 атомов углерода, и также бициклические алкильные группы, содержащие от 7 до 10 атомов углерода, или также моноциклические алкильные группы, которые содержат по меньшей мере один С1-С3-углеродный мостик.
Термин "гетероциклические кольца" или также "гетероциклы" означает 5-, 6- или 7-членные насыщенные или ненасыщенные гетероциклические кольца, которые могут содержать 1, 2 или 3 гетероатома, выбранных из группы, включающей кислород, серу и азот, и одновременно это кольцо может быть связано с молекулой через атом углерода или, если он имеется, через атом азота.
Хотя и включенный в термин "гетероциклические кольца" или "гетероцикл", термин "гетероциклические неароматические кольца" означает 5-, 6- или 7-членные ненасыщенные кольца. Примеры включают:


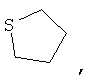








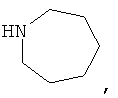

Хотя и включенный в термин "гетероциклические кольца" или "гетероцикл", термин "гетероциклические ароматические кольца" или "гетероарил" означает 5- или 6-членные гетероциклические ароматические группы или 5-10-членные бициклические гетероарильные кольца, которые могут содержать 1, 2, 3 или 4 гетероатома, выбранных из группы, включающей кислород, серу и азот, и содержит количество сопряженных двойных связей, достаточное для образования ароматической системы. Ниже приведены примеры 5- или 6-членных гетероциклических ароматических групп:











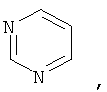



Если не указано иное, то гетероциклическое кольцо (или "гетероцикл") может содержать кетогруппу. Ниже приведены примеры таких колец.

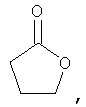


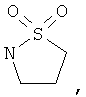


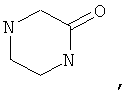

Хотя и включенный в термин "циклоалкил", термин "бициклические циклоалкилы" обычно означает 8-, 9- или 10-членные бициклические углеродные кольца. Приведенные ниже указаны в качестве примера:








Хотя и включенный в термин "гетероцикл", термин "бициклические гетероциклы" обычно обозначает 8-, 9- или 10-членные бициклические кольца, которые могут содержать один или большее количество гетероатомов, предпочтительно 1-4, более предпочтительно 1-3, еще более предпочтительно 1-2, еще более предпочтительно 1 гетероатом, выбранный из группы, включающей кислород, серу и азот. Одновременно это кольцо может быть связано с молекулой через атом углерода или, если он имеется, через атом азота. Приведенные ниже гетероциклы указаны в качестве примера;
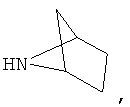



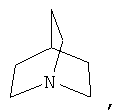

Хотя и включенный в термин "арил", термин "бициклический арил" означает 5-10-членное бициклическое арильное кольцо, которое содержит количество сопряженных двойных связей, достаточное для образования ароматической системы. Одним примером бициклического арила является нафтил.
Хотя и включенный в термин "гетероарил", термин "бициклический гетероарил" означает 5-10-членное бициклическое гетероарильное кольцо, которое может содержать 1, 2, 3 или 4 гетероатома, выбранных из группы, включающей кислород, серу и азот, и содержит количество сопряженных двойных связей, достаточное для образования ароматической системы.
Хотя и включенный в термин "бициклические циклоалкилы" или "бициклический арил", термин "конденсированный циклоалкил" или "конденсированный арил" означает бициклические кольца, в которых мостиком, разделяющим кольца, является непосредственная двойная связь. Ниже приведены примеры конденсированных бициклических циклоалкилов:



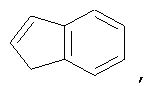


Хотя и включенный в термин "бициклические гетероциклы" или "бициклические гетероарилы", термин "конденсированные бициклические гетероциклы" или "конденсированные бициклические гетероарилы" означает бициклические 5-10-членные гетероциклы, которые содержат 1, 2 или 3 гетероатома, выбранных из группы, включающей кислород, серу и азот, в которых мостиком, разделяющим кольца, является непосредственная ординарная связь. "Конденсированные бициклические гетероарилы" также содержат количество сопряженных двойных связей, достаточное для образования ароматической системы. Примеры включают пирролизин, индол, индолизин, изоиндол, индазол, пурин, хинолин, изохинолин, бензимидазол, бензофуран, бензопиран, бензотиазол, бензотиазол, бензоизотиазол, пиридопиримидин, птеридин, пиримидопиримидин,


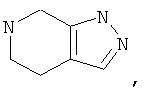





Термин "гетероциклические спироциклические кольца" (спираны) означает 5-10-членные спироциклические кольца, которые необязательно могут содержать 1, 2 или 3 гетероатома, выбранных из группы, включающей кислород, серу и азот, и одновременно это кольцо может быть связано с молекулой через атом углерода или, если он имеется, через атом азота. Если не указано иное, то спироциклическое кольцо может содержать оксогруппу, метильную или этильную группу. Их примеры включают:
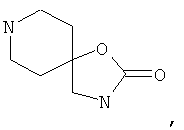




"Галоген" в объеме настоящего изобретения обозначает фтор, хлор, бром или йод. Если не указано иное, то фтор, хлор и бром рассматриваются как предпочтительные галогены.
Соединения общей формулы 1, полученные способом, предлагаемым в настоящем изобретении, могут содержать кислотные группы, преимущественно карбоксигруппы, и/или основные группы, такие как, например, аминогруппы. Поэтому соединения общей формулы 1 могут существовать в виде внутренних солей, в виде солей с фармацевтически применимыми неорганическими кислотами, такими как хлористоводородная кислота, серная кислота, фосфорная кислота, сульфоновая кислота, или органическими кислотами (такими как, например, малеиновая кислота, фумаровая кислота, лимонная кислота, винная кислота или уксусная кислота) или в виде солей с фармацевтически применимыми основаниями, таких как гидроксиды или карбонаты щелочных или щелочноземельных металлов, гидроксиды цинка или алюминия, или органическими аминами, такими как, например, в частности, диэтиламин, триэтиламин, триэтаноламин.
В. Соли, диастереоизомеры, энантиомеры, рацематы, гидраты и сольваты
Соединения формулы 1 и эквивалентные выражения включают соединения формулы 1 по отдельности, в некоторой комбинации или их все в соответствии с контекстом. В соответствии с определением, приведенным в настоящем изобретении, соединения формулы 1 включают их фармацевтически приемлемые соли, диастереоизомеры, энантиомеры, рацематы, гидраты или сольваты.
Как указано выше в настоящем изобретении, соединения формулы 1, полученные способом, предлагаемым в настоящем изобретении, можно превратить в их соли, в особенности предназначенные для применения в фармацевтике в их физиологически и фармакологически приемлемые соли. С одной стороны, эти соли могут находиться в форме физиологически и фармакологически приемлемых солей присоединения с кислотами соединений формулы 1 с неорганическими или органическими кислотами. С другой стороны, если R обозначает водород, соединение формулы 1, полученное способом, предлагаемым в настоящем изобретении, с помощью дополнительной реакции с неорганическими основаниями также можно превратить в физиологически и фармакологически приемлемые соли, содержащие в качестве противоиона катионы щелочных или щелочноземельных металлов. Соли присоединения с кислотами можно получить, например, с использованием хлористоводородной кислоты, бромистоводородной кислоты, серной кислоты, фосфорной кислоты, метансульфоновой кислоты, уксусной кислоты, фумаровой кислоты, янтарной кислоты, молочной кислоты, лимонной кислоты, винной кислоты или малеиновой кислоты. Также можно использовать смеси указанных выше кислот. Соли щелочных или щелочноземельных металлов и соединения формулы 1 предпочтительно получают с использованием гидроксидов и гидридов щелочных или щелочноземельных металлов, из которых предпочтительными являются гидроксиды и гидриды щелочных металлов, в особенности натрия и калия, и особенно предпочтительными являются гидроксиды натрия и калия. Соединения, предлагаемые в настоящем изобретении, применимы в форме и свободных оснований, и солей, и на практике применение соли означает применение основания. Перечни подходящих солей приведены, например, в публикации S.M. Birge et al., J. Pharm. Sci., 1977, 66, 1-19, которая во всей своей полноте включена в настоящее изобретение в качестве ссылки.
При необходимости соединения общей формулы 1, полученные способом, предлагаемым в настоящем изобретении, можно превратить в их соли, в особенности предназначенные для применения в фармацевтике в их фармакологически приемлемые соли присоединения с неорганическими или органическими кислотами. Подходящие кислоты включают, например, янтарную кислоту, бромистоводородную кислоту, уксусную кислоту, фумаровую кислоту, малеиновую кислоту, метансульфоновую кислоту, молочную кислоту, фосфорную кислоту, хлористоводородную кислоту, серную кислоту, винную кислоту и лимонную кислоту. Также можно использовать смеси указанных выше кислот.
Настоящее изобретение относится к соединениям, полученным способом, предлагаемым в настоящем изобретении, необязательно в виде отдельных оптических изомеров, смесей отдельных оптических изомеров, смесей отдельных энантиомеров или рацематов, в виде таутомеров, а также в виде свободных оснований или соответствующих солей присоединения с фармакологически приемлемыми кислотами, таких как, например, соли присоединения с галогенводородными кислотами, например с хлористоводородной или бромистоводородной кислотой, или органическими кислотами, такими как, например, щавелевая, фумаровая, дигликолевая или метансульфоновая кислота. Термин "энантиомеры" означает пару стереоизомеров, которые представляют собой не налагающиеся друг на друга зеркальные изображения. Термин "диастереоизомеры" означает оптические изомеры, которые не являются зеркальными отображениями друг друга. Термин "рацемическая смесь" или "рацемат" означает смесь, содержащую одинаковые количества отдельных энантиомеров. Термин "нерацемическая смесь" означает смесь, содержащую неодинаковые количества отдельных энантиомеров.
Соединения, полученные способом, предлагаемым в настоящем изобретении, необязательно могут представлять собой рацематы, но они также могут получаться в виде чистых энантиомеров, т.е. в (R)- или (S)-форме. В одном варианте осуществления соединения, полученные способом, предлагаемым в настоящем изобретении, находятся в виде рацематов или в (S)-форме. В другом варианте осуществления соединения, полученные способом, предлагаемым в настоящем изобретении, находятся в (R)-форме.
Настоящее изобретение относится к соединениям, полученным способом, предлагаемым в настоящем изобретении, необязательно в виде отдельных оптических изомеров, смесей отдельных энантиомеров или рацематов, в виде таутомеров, а также в виде свободных оснований или соответствующих солей присоединения с фармакологически приемлемыми кислотами, таких как, например, соли присоединения с галогенводородными кислотами, например с хлористоводородной или бромистоводородной кислотой, или органическими кислотами, такими как, например, щавелевая, фумаровая, дигликолевая или метансульфоновая кислота.
Термин "сольват" означает физическое объединение соединения с одной или большим количеством молекул растворителя или комплекс переменной стехиометрии, образованный растворенным веществом (например, соединением формулы 1) и растворителем, например водой, этанолом или уксусной кислотой. В некоторых случаях сольват можно выделить, например, когда одна или большее количество молекул растворителя включены в кристаллическую решетку кристаллического твердого вещества. Обычно выбранные растворители не препятствуют биологической активности растворенного вещества. Сольваты включают растворенную фазу и выделенные сольваты. Типичные сольваты включают гидраты, этаноляты, метаноляты и т.п.
Типичные дигидротиенопиримидины
Настоящее изобретение относится к стадиям синтеза, предназначенным для получения дигидротиенопиримидинов формулы 1:

в которой:
RA обозначает остаток, выбранный из группы, включающей Неt, гетероарил и который необязательно замещен остатком, выбранным из группы, включающей галоген, C1-С3-фторалкил, CN, ОН, оксогруппу, -С1-С6-алкил, -O-R2.1, -COOR2.1, SO-R2.1, SO2-R2.1, С6-С10-арил, С1-С3-алкилен-С6-С10-арил, -С1-С3-алкилен-NR2.2R2.3, NR2.2R2.3, С3-С10-циклоалкил, C1-С3-алкилен-С3-С10-циклоалкил, Het, гетероарил, С1-С3-алкиленгетероарил и С1-С3-алкилен-Неt, который необязательно может быть замещен остатком, выбранным из группы, включающей ОН, галоген, -C1-С3-фторалкил, С1-С6-алкил, С6-С10-арил, -СОО(С1-С3-алкил) и O-(С1-С3-алкил),
где
Het обозначает 3-11-членный моно- или бициклический, насыщенный или частично насыщенный гетероцикл, который содержит 1, 2, 3 или 4 гетероатома, независимо выбранных из N, S и О,
гетероарил представляет собой 5-11-членный моно- или бициклический гетероарил, который содержит 1, 2, 3 или 4 гетероатома, независимо выбранных
из N, S и О,
где
циклоалкил является насыщенным или частично насыщенным,
или в которой
RA обозначает

и где Х обозначает SO или SO2, предпочтительно SO;
R1 обозначает Н, C1-С6-алкил, С2-С6-алкенил, С2-С6-алкинил, С6-С10-арил, С6-С10-арил-С1-С6-алкилен или С5-С10-гетероарил-С1-С6-алкилен;
R2 обозначает Н или группу, выбранную из группы, включающей С1-С10-алкил,
С2-С6-алкенил и С2-С6-алкинил, который необязательно может быть замещен галогеном, и которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей OR2.1, COOR2.1, CONR2.2R2.3, SR2.1, С6-С10-арил, моно- или бициклический С3-С10-гетероцикл, моно- или бициклический С3-С10-гетероарил, моно- или бициклический С3-С10-циклоалкил, CH2-NR2.2R2.3 и NR2.2R2.3, которая, в свою очередь, необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, галоген, OR2.1, оксогруппу, C1-С6-алкил, С6-С10-арил, COOR2.1, CH2-NR2.2R2.3 и NR2.2R2.3,
где R2.1 обозначает Н или группу, выбранную из группы, включающей C1-С6-алкил, C1-С6-алканол, C1-С3-галогеналкил, моно- или бициклический С3-С10-циклоалкил, С6-С10-арил-С1-С6-алкилен, моно- или бициклический С5-С10-гетероарил-С1-С6-алкилен, С3-С10-гетероцикл-C1-С6-алкилен, С3-С10-циклоалкил-С1-С6-алкилен, моно- или бициклический С6-С10-арил, моно- или бициклический С3-С10-гетероарил и моно- или бициклический, насыщенный или ненасыщенный гетероцикл, которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, галоген, C1-С6-алкил и С6-С10-арил,
где R2.2 и R2.3 независимо друг от друга обозначают Н или группу, выбранную из группы, включающей галоген, С1-С6-алкил, моно- или бициклический С3-С10-циклоалкил, С6-С10-арил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, моно- или бициклический С6-С10-арил, моно- или бициклический С3-С10-гетероцикл, моно- или бициклический С5-С10-гетероарил, CO-NH2, СО-NНСН3, СО-N(СН3)2, SO2(С1-С2-алкил), CO-R2.1 и COOR2.1, которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, галоген, С1-С6-алкил, С6-С10-арил и COOR2.1,
или
R2 обозначает моно- или полициклический С3-С10-циклоалкил, который необязательно может содержать мостик из одной или более C1-С3-алкильных групп и который необязательно может быть замещен группой, выбранной из группы, включающей разветвленный или неразветвленный С1-С6-алканол, OR2.1, COOR2.1, SO2NR2.2R2.3, С3-С10-гетероцикл, С6-С10-арил, C1-С6-алкил, С6-С10-арил-C1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, моно- или
бициклический С3-С10-циклоалкил и NR2.2R2.3, которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, галоген, C1-С6-алкил, С6-С10-арил и NR2.2R2.3, или
R2 обозначает моно- или полициклический С6-С10-арил, который необязательно может быть замещен ОН, SH или галогеном или одной или более группой, выбранной из группы, включающей OR2.1, COOR2.1, NR2.2R2.3, СН2-NR2.2R2.3, С3-С10-циклоалкил, С3-С10-гетероцикл, С1-С6-алкил, С6-С10-арил-С1-С6-алкилен, С3-С10-гетероцикл-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, С6-С10-арил, SO2-СН3, SO2-СН2СН3 и SO2-NR2.2R2.3, которая, в свою очередь, необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, галоген, C1-С6-алкил, С6-С10-арил и NR2.2R2.3, или
R2 обозначает группу, выбранную из группы, включающей моно- или бициклический насыщенный или ненасыщенный С3-С10-гетероцикл и моно- или бициклический С5-С10-гетероарил, который включает от 1 до 4 гетероатомов, выбранных из S, О и N, и необязательно может быть замещена одной или более группой, выбранной из группы, включающей галоген, ОН, оксогруппу и SH, или одной или более группой, выбранной из группы, включающей OR2.1, SR2.1, COOR2.1, COR2.1, C1-С6-алканол, С3-С10-циклоалкил, С6-С10-арил, С1-С6-алкил, С6-С10-арил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, С5-С10-гетероцикл, С5-С10-гетероарил, C1-С6-алканол и NR2.2R2.3, которая, в свою очередь, необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, галоген, С1-С6-алкил, С6-С10-арил, CH2-NR2.2R2.3 и NR2.2R2.3;
или где
NR1R2 вместе обозначают гетероциклическое С4-С7-кольцо, которое необязательно может содержать мостик, которое содержит 1, 2 или 3 гетероатома, выбранных из N, О и S, и которое необязательно может быть замещено одной или более группой, выбранной из группы, включающей ОН, OR2.1, C1-С6-алканол, оксогруппу, галоген, С1-С6-алкил, С6-С10-арил, COOR2.1, CH2-NR2,2-COO-R2.1, CH2-NR2.2-CO-R2.1, CH2-NR2.2-CO-CH2-NR2.2R2.3, СН2-NR2.2-SO2-C1-C3-aлкил, CH2-NR2.2-SO2-NR2.2R2.3, CH2-NR2.2-CO-NR2.2R2.3, СО-NR2.2R2.3 и NR2.2R2.3;
R3 выбран из группы, включающей фтор, хлор, бром, йод, гидроксигруппу, SO2-СН3, COOR2.1, нитрильную группу и С3-С10-гетероцикл-С1-С6-алкилен, где С3-С10-гетероцикл может быть моно- или бициклическим и необязательно может быть замещен группой, выбранной из группы, включающей ОН, галоген, оксогруппу, С1-С6-алкил и С6-С10-арил,
или
обозначает группу, выбранную из группы, включающей C1-С6-алкил, С2-С6-алкенил, С2-С6-алкинил, С6-С10-арил, С6-С10-арил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, С3-С10-гетероцикл и С3-С10-циклоалкил, которая необязательно может быть замещена группой, выбранной из группы, включающей ОН, галоген, оксогруппу, С1-С6-алкил и С6-С10-арил,
или
R3 обозначает группу -CO-NR3.1R3.2,
в которой R3.1 и R3.2 независимо друг от друга обозначают Н или группу, выбранную из группы, включающей С1-С6-алкил, С2-С6-алкенил, С2-С6-алкинил, С6-С10-арил, С6-С10-арил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкинилен, С5-С10-гетероарил-С1-С6-алкенилен, моно- или бициклический, С3-С10-гетероцикл, С3-С10-гетероцикл-С1-С6-алкилен и моно- или бициклический С5-С10-гетероарил, где в каждом случае группа необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, оксогруппу, галоген, C1-С6-алкил и O-C1-С6-алкил, или
R3 обозначает группу -NR3.3 -CO-R3.4,
в которой R3.3 обозначает Н или группу, выбранную из группы, включающей С1-С6-алкил, С2-С6-алкенил, С2-С6-алкинил, С6-С10-арил, С6-С10-арил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, С3-С10-гетероцикл и С5-С10-гетероарил, которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, NH2,
NR2.2R2.3, галоген, C1-С6-алкил и С6-С10-арил, и
где R3.4 обозначает Н или группу, выбранную из группы, включающей C1-С6-алкил, С2-С6-алкенил, С2-С6-алкинил, C1-С6-алканол, OR2.1, СН2-О-СО-С1-С6-алкил, CH2-NR2.2R2.3, NR2.2R2.3, С6-С10-арил, С6-С10-арил-С1-С6-алкилен, C5-С10-гетероарил-С1-С6-алкилен, моно- или бициклический насыщенный, частично насыщенный или ненасыщенный С3-С10-гетероцикл, содержащий 1, 2 или 3 гетероатома, выбранных из S, О и N, и моно- или бициклический С5-С10-гетероарил, содержащий 1, 2 или 3 гетероатома, выбранных из S, О и N, который необязательно может быть замещен одной или более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, NН2, NR2.2R2.3, галоген, С1-С6-алкил и С6-С10-арил,
или
R3 обозначает необязательно моно- или ди-N-замещенную сульфонамидную группу
SO2-NR3.5R3.6,
в которой R3.5 и R3.6 все независимо друг от друга могут обозначать С1-С6-алкил
или С6-С10-арил;
и
R4 и R5 независимо выбраны из группы, включающей Н, C1-С6-алкил, С2-С6-алкенил, С2-С6-алкинил, С6-С10-арил, С6-С10-арил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, С3-С10-гетероцикл и С5-С10-гетероарил, -О-С1-С6-алкил, -O-С6-С10-арил, -O-С3-С10-гетероцикл и -O-С5-С10-гетероарил, -NR'R", фтор, C1-С6-фторалкил и C1-С6-фторалкоксигруппу, где R' и R" независимо выбраны из группы, включающей Н и С1-С6-алкил, и где в каждом случае группа необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, оксогруппу, галоген, С1-С6-алкил и O-C1-С6-алкил, а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Настоящее изобретение предпочтительно относится к способу получения соединений формулы 1, в которой:
Х обозначает SO;
R1 обозначает Н, С1-С6-алкил, С6-С10-арил, С6-С10-арил-С1-С6-алкилен или С5-С10-гетероарил-С1-С6-алкилен;
R2 обозначает Н или С1-С6-алкил, который необязательно может быть замещен галогеном и который необязательно может быть замещен одной или более группой, выбранной из группы, включающей OR2.1, COOR2.1, CONR2.2R2.3, SR2.1, С6-С10-арил, моно- или бициклический С3-С10-гетероцикл, моно- или бициклический С5-С10-гетероарил, моно- или бициклический С3-С10-циклоалкил, CH2-NR2.2R2.3 и NR2.2R2.3, которая, в свою очередь, необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, галоген, OR2.1, оксогруппу, С1-С6-алкил, С6-С10-арил, COOR2.1, CH2-NR2.2R2.3 и NR2.2R2.3,
в которой R2.1 обозначает Н или группу, выбранную из группы, включающей С1-С6-алкил, C1-С6-алканол, С1-С3-галогеналкил, моно- или бициклический С3-С10-циклоалкил, С6-С10-арил-С1-С6-алкилен или С5-С10-гетероарил-С1-С6-алкилен, С3-С10-гетероцикл-С1-С6-алкилен, С3-С10-циклоалкил-С1-С6-алкилен, моно- или бициклический С6-С10-арил, моно- или бициклический С5-С10-гетероарил и моно- или бициклический насыщенный или ненасыщенный С3-С10-гетероцикл, которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, галоген, C1-С6-алкил, С6-С10-арил, в которой R2.2 и R2.3 независимо друг от друга обозначают Н или выбраны из группы, включающей галоген, C1-С6-алкил, моно- или бициклический С3-С10-циклоалкил, С6-С10-арил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, моно- или бициклический С6-С10-арил, моно- или бициклический насыщенный или ненасыщенный С3-С10-гетероцикл, моно- или бициклический С5-С10-гетероарил, CO-NH2, СО-NНСН3, СО-N(СН3)2, SO2(С1-С2-алкил), CO-R2.1 и COOR2.1, которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, галоген, C1-С6-алкил, С6-С10-арил и COOR2.1,
или
R2 обозначает моно- или полициклический С3-С10-циклоалкил, который необязательно может содержать мостик из одной или более С1-С3-алкильных групп и который необязательно может быть моно- или полизамещен ОН или галогеном или одной или более группой, выбранной из группы, включающей разветвленный или неразветвленный C1-С6-алканол, OR2.1, COOR2.1, SO2NR2.2R2.3, С3-С10-гетероцикл, С6-С10-арил, C1-С6-алкил, С6-С10-арил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, моно- или бициклический С3-С10-циклоалкил и NR2.2R2.3, которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, галоген, C1-С6-алкил, С6-С10-арил и NR2.2R2.3,
или
R2 обозначает моно- или полициклический С6-С10-арил, который необязательно может быть замещен ОН, SH или галогеном или одной или более группой, выбранной из группы, включающей OR2.1, COOR2.1, NR2.2R2.3, СН2-NR2.2R2.3,С3-С10-циклоалкил, С3-С10-гетероцикл, C1-С6-алкил, С6-С10-арил-C1-С6-алкилен, С3-С10-гетероцикл-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, С6-С10-арил, SO2-СН3, SО2-СН2СН3 и SO2-NR2.2R2.3, которая, в свою очередь, необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, галоген, C1-С6-алкил, С6-С10-арил и NR2.2R2.3,
или
R2 обозначает группу, выбранную из группы, включающей моно- или бициклический насыщенный или ненасыщенный С3-С10-гетероцикл и моно- или бициклический С3-С10-гетероарил, который включает от 1 до 4 гетероатомов, выбранных из S, О и N, и необязательно может быть замещена одной или более группой, выбранной из группы, включающей галоген, ОН, оксогруппу и SH, или одной или более группой, выбранной из группы, включающей OR2.1, SR2.1, COOR2.1, COR2.1, C1-С6-алканол, С3-С10-циклоалкил, С6-С10-арил, C1-С6-алкил, С6-С10-арил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, С5-С10-гетероцикл, С5-С10-гетероарил, С1-С6-алканол и NR2.2R2.3, которая, в свою очередь, необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, галоген, С1-С6-алкил, С6-С10-арил и NR2.2R2.3,
или
NR1R2 вместе обозначают гетероциклическое C4-С7-кольцо, которое необязательно может содержать мостик, который содержит 1, 2 или 3 гетероатома, выбранных из N, О и S, и которое необязательно может быть замещено одной или более группой, выбранной из группы, включающей ОН, OR2.1, C1-С6-алканол, оксогруппу, галоген, С1-С6-алкил, С6-С10-арил, COOR2.1, CH2-NR2.2-COO-R2.1, СН2-NR2.2-СО-R2.1, CH2-NR2.2-CO-CH2-NR2.2R2.3, СН2-NR2.2-SO2-C1-C3-алкил, CH2-NR2.2-SO2-NR2.2R2.3, CH2-NR2.2-CO-NR2.2R2.3, СО-NR2.2R2.3, CH2-NR2.2R2.3 и NR2.2R2.3; и
R4 и R5 независимо выбраны из группы, включающей Н, С1-С6-алкил, С6-С10-арил, -O-C1-С6-алкил, -NR'R", фтор, C1-С6-фторалкил и С1-С6-фторалкоксигруппу, где R' и R" независимо выбраны из группы, включающей Н и C1-С6-алкил,
а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Также предпочтительным является способ получения соединений формулы 1, в которой:
Х обозначает SO;
R1 обозначает Н, C1-С6-алкил, С6-С10-арил, С6-С10-арил-С1-С6-алкилен или C5-С10-гетероарил-С1-С6-алкилен;
R2 обозначает Н или C1-С6-алкил, который необязательно может быть замещен галогеном и который необязательно может быть замещен одной или более группой, выбранной из группы, включающей OR2.1, COOR2.1, CONR2.2R2.3, SR2.1, фенил, моно- или бициклический С5-С10-гетероцикл, С5-С6-гетероарил, моно- или бициклический С5-С10-циклоалкил, СН2-NR2.2R2.3 и NR2.2R2.3, которая, в свою очередь, необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, галоген, OR2.1, оксогруппу, C1-С6-алкил, фенил, COOR2.1, CH2-NR2.2R2.3 и NR2.2R2.3,
в которой R2.1 обозначает Н или группу, выбранную из группы, включающей C1-С6-алкил, C1-С6-алканол, C1-С3-галогеналкил, моно- или бициклический С5-С10-циклоалкил, фенил-С1-С6-алкилен, С5-С6-гетероарил-С1-С6-алкилен, c5-c10-гетероцикл-С1-С6-алкилен, С5-С10-циклоалкил-С1-С10-алкилен, фенил, моно- или бициклический С5-С10-гетероарил и моно- или бициклический насыщенный или ненасыщенный С5-С10-гетероцикл, которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, галоген, C1-С6-алкил и фенил,
в которой R2.2 и R2.3 независимо друг от друга обозначают Н или группу, выбранную из группы, включающей галоген, C1-С6-алкил, моно- или бициклический С5-С10-циклоалкил, фенил-С1-С6-алкилен, С5-С6-гетероарил-С1-С6-алкилен, фенил, моно- или бициклический С5-С10-гетероцикл, моно- или бициклический С5-С6-гетероарил, CO-NH2, СО-NНСН3, СО-N(СН3)2, SO2(C1-C2-алкил), CO-R2.1 и COOR2.1, которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, галоген, С1-С6-алкил, фенил и COOR2.1,
или
R2 обозначает моно- или полициклический С5-С10-циклоалкил, который необязательно может содержать мостик из одной или более C1-С3-алкильных групп и который необязательно может быть моно- или полизамещен ОН или галогеном или одной или более группой, выбранной из группы, включающей разветвленный или неразветвленный С1-С3-алканол, OR2.1, COOR2.1, SO2NR2.2R2.3, С5-С10-гетероцикл, фенил, C1-С6-алкил, фенил-С1-С6-алкилен, C5-С6-гетероарил-С1-С6-алкилен, моно- или бициклический С5-С10-циклоалкил и NR2.2R2.3, которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, галоген, C1-С6-алкил, фенил и NR2.2R2.3,
или
R2 обозначает фенил, который необязательно может быть замещен ОН, SH или галогеном или одной или более группой, выбранной из группы, включающей OR2.1, COOR2.1, NR2.2R2.3, СН2-NR2.2R2.3, С5-С10-циклоалкил, С5-С10-гетероцикл, C1-С6-алкил, фенил-С1-С6-алкилен, С5-С10-гетероцикл-С1-С6-алкилен, С5-С6-гетероарил-С1-С6-алкилен, фенил, SO2-СН3, SО2-СН2СН3 и SO2-NR2.2R2.3, которая, в свою очередь, необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, галоген, С1-С6-алкил, С6-С10-арил и NR2.2R2.3,
или
R2 обозначает группу, выбранную из группы, включающей моно- или бициклический насыщенный или ненасыщенный С5-С10-гетероцикл и моно- или бициклический С5-С6-гетероарил, который содержит от 1 до 4 гетероатомов, выбранных из S, О и N, и необязательно может быть замещен одной или более группой, выбранной из группы, включающей галоген, ОН, оксогруппу и SH, или одной или более группой, выбранной из группы, включающей OR2.1, SR2.1, COOR2.1, COR2.1, C1-С6-алканол, С3-С10-циклоалкил, фенил, C1-С6-алкил, фенил-C1-С6-алкилен, С5-С6-гетероарил-С1-С6-алкилен, С5-С10-гетероцикл, C5-C6-гетероарил, C1-С6-алканол и NR22.2R2.3, которая, в свою очередь, необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, галоген, C1-С6-алкил, фенил и NR2.2R2.3; и
R4 и R5 независимо выбраны из группы, включающей Н, С1-С6-алкил, С6-С10-арил, -O-C1-С6-алкил, -NR'R", фтор, C1-С6-фторалкил и C1-С6-фторалкоксигруппу, где R' и R" независимо выбраны из группы, включающей Н и C1-С6-алкил,
а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Также особенно предпочтительным является способ получения соединений формулы 1, в которой:
NR1R2 вместе обозначают гетероциклическое С4-С7-кольцо, которое необязательно может содержать мостик, который содержит 1, 2 или 3 гетероатома, выбранных из N, О и S, и которое необязательно может быть замещено одной или более группой, выбранной из группы, включающей ОН, OR2.1, C1-С6-алканол, оксогруппу, галоген, С1-С6-алкил, С6-С10-арил, COOR2.1, CH2-NR2.2-COO-R2.1, CH2-NR2.2-CO-R2.1, CH2-NR2.2-CO-CH2-NR2.2R2.3, CH2-НR2.2-С1-С3-алкил, CH2-NR2.2-SO2-NR2.2R2.3, CH2-NR2.2-CO-NR2.2R2.3, CO-NR2.2R2.3, CH2-NR2.2R2.3 и NR2.2R2.3,
а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Настоящее изобретение предпочтительно относится к способу получения соединений формулы 1, в которой RA обозначает

Также предпочтительным является способ получения соединений формулы 1, в которой
RA обозначает моноциклическое 5- или 6-членное гетероарильное кольцо, которое необязательно замещено группой, выбранной из группы, включающей F, Сl, Вr, СF3, CHF2, CH2F, CN, ОН, -метил, этил, пропил, изопропил, -O-метил, O-этил, -СООметил, -СООэтил, SO2-(СН3), SO-(СН3), SО2-(СН2СН3), SO-(СН2СН3), фенил, -метиленфенил, -этиленфенил, -NH2, -NH(CH3), N(СН3)2, -метилен-NН2, -метилен-NН(СН3), -метилен-N(СН3)2, С3-С6-циклоалкил, -метилен-С3-С6-циклоалкил, насыщенный или частично насыщенный 5-6-членный гетероцикл, 5-6-членный гетероарил и -Het, которая необязательно может быть замещена остатком, выбранным из группы, включающей ОН, F, Сl, Вr, СF3, CHF2, CH2F, метил, этил, пропил, изопропил, фенил, -СОО(СН3), -O-метил и -O-этил;
или
RA обозначает бициклический 9-11-членный насыщенный, ненасыщенный или частично насыщенный гетероцикл, который необязательно замещен остатком, выбранным из группы, включающей F, Cl, Вr, СF3, CHF2, CH2F, CN, ОН, -метил, этил, пропил, изопропил, -O-метил, O-этил, -СООметил, -СООэтил, SO2-(СН3), SO-(СН3), SO2-(СН2СН3), SО-(СН2СН3), фенил, -метиленфенил, -этиленфенил, -NH2, -NН(СН3), N(CH3)2,
-метилен-NН2, -метилен-NН(СН3), -метилен-N(СН3)2, -С3-С6-циклоалкил, -метилен-С3-С6-циклоалкил, насыщенный, частично насыщенный или ненасыщенный, 5-6-членный гетероцикл, 5-6-членный гетероарил, метиленгетероарил и -метилен-Het,
который необязательно может быть замещен остатком, выбранным из группы, включающей ОН, F, Cl, Вr, СF3, CHF2, CH2F, метил, этил, пропил, изопропил, фенил, -СОО(СН3), -O-метил и -O-этил;
или
RA обозначает моноциклическое 5-6-членное гетероарильное кольцо, выбранное из группы, включающей пиррол, пиразол, фуран, тиофен, тиазол, имидазол, оксазол, пиридазин, пиримидин, пиразин, тиадиазол, оксадиазол, изооксазол, изотиазол и пиридин, которое необязательно замещено остатком, выбранным из группы, включающей F, Cl, Вr, СF3, CHF2, СН2F, CN, ОН, -метил, этил, пропил, изопропил, -O-метил, O-этил, -СООметил, -СООэтил, SO2-(СН3), SO2-(СН2СН3), фенил, -метиленфенил, -этиленфенил, -NH2, -NН(СН3), N(СН3)2, -метилен-NН2, -метилен-NН(СН3), -метилен-N(СН3)2, С3-С6-циклоалкил, метилен-С3-С6-циклоалкил, Het, гетероарил, -метиленгетероарил и -метилен-Het, где этот остаток также необязательно может быть замещен одним или более остатком, выбранным из группы, включающей ОН, F, Cl, Вr, СF3, CHF2, CH2F, метил, этил, пропил, изопропил, фенил, -СОО(СН3), -O-метил и -O-этил; или
RA обозначает бициклический 9-11-членный гетероцикл, выбранный из группы, включающей бензоксазол, бензодиоксол, дигидробензодиоксин, бензодиоксин, бензизоксазол, бензотиазол, бензизотиазол, тиенопиримидин, фуропиримидин, тиенопиридин, фуропиридин, индол, изоиндол, хиноксалин, нафтиридин, пиридопиразин, пиридопиримидин, хинолин, изохинолин, бензимидазол, 6, 7, 8, 9-тетрагидро-5Н-пиразино[2,3-d]азепин, бензотиофен, бензофуран, хиназолин, индазол, изобензофуран и птеридин, и этот остаток необязательно может быть замещен другим остатком, выбранным из группы, включающей F, Cl, Вr, СF3, CHF2, СН2F, CN, ОН, -метил, этил, пропил, изопропил, -O-метил, O-этил, -СООметил, -СООэтил, SO2-(СН3), SO2-(CH2CH3), фенил, -метиленфенил, -этиленфенил, -NH2, -NН(СН3), N(СН3)2, -метилен-NН2, -метилен-NН(СН3), -метилен-N(СН3)2, С3-С6-циклоалкил, метилен-С3-С6-циклоалкил, Het, гетероарил, -метиленгетероарил и -метилен-Het, и этот остаток также необязательно может быть замещен другим остатком, выбранным из группы, включающей ОН, F, Cl, Вr, СF3, CHF2, CH2F, метил, этил, пропил, изопропил, фенил, -СОО(СН3), -O-метил и -O-этил.
Настоящее изобретение предпочтительно также относится к способу получения соединений формулы 1, в которой R1 обозначает Н или метил, а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Настоящее изобретение предпочтительно также относится к способу получения соединений формулы 1, в которой R4 и R5 обозначают Н или метил, а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Настоящее изобретение предпочтительно также относится к способу получения соединений формулы 1, в которой R4 и R5 обозначают Н, а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Настоящее изобретение предпочтительно также относится к способу получения соединений формулы 1, в которой:
NR1R2 вместе образуют пирролидиновое кольцо, которое необязательно может быть замещено одной или более группой, выбранной из группы, включающей ОН, OR2.1, СН2-ОН, СН2-СН2-ОН, оксогруппу, Cl, F, Вr, метил, этил, пропил, фенил, COOR2.1, CH2-NR2.2-COO-R2.1, CH2-NR2.2-CO-R2.1, CH2-NR2.2-CO-CH2-NR2.2R2.3, СН2-НR2.2-SО2-С1-С3-алкил, CH2-NR2.2SO2-NR2.2R2.3, CH2-NR2.2-CO-NR2.2R2.3, CO-NR2.2R2.3, CH2-NR2.2.R2.3 и NR2.2R2.3,
а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Настоящее изобретение предпочтительно также относится к способу получения соединений формулы 1, в которой:
R2 обозначает фенил, который моно- или полизамещен ОН, SH или галогеном и/или одной или более группой, выбранной из группы, включающей OR2.1, COOR2.1, NR2.2R2.3, СН2-NR2.2R2.3, С5-С10-циклоалкил, С5-С10-гетероцикл, С1-С6-алкил, фенил-С1-С6-алкилен, С5-С10-гетероцикл-С1-С6-алкилен, С5-С6-гетероарил-С1-С6-алкилен, фенил, SO2-СН3, SO2-СН2СН3 и SO2-NR2.2R2.3 в любом положении, которая, в свою очередь, необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, галоген, C1-С6-алкил, фенил и NR2.2R2.3,
а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Настоящее изобретение предпочтительно также относится к способу получения соединений формулы 1, в которой:
R2 обозначает фенил, который может быть замещен по меньшей мере в одном из двух мета-положений ОН, SH или галогеном или одной или более группой, выбранной из группы, включающей OR2.1, COOR2.1, NR2.2R2.3, CH2-NR2.2R2.3, C5-С10-циклоалкил, С5-С10-гетероцикл, C1-С6-алкил, фенил-С1-С6-алкилен, С5-С10-гетероцикл-С1-С6-алкилен, С5-С6-гетероарил-С1-С6-алкилен, фенил SO2-СН3, SO2-СН2СН3 и SO2-NR2.2R2.3, которая, в свою очередь, необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, галоген, С1-С6-алкил, фенил и NR2.2R2.3, а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Настоящее изобретение предпочтительно также относится к способу получения соединений формулы 1, в которой:
R обозначает фенил, который замещен по меньшей мере в одном из двух мета-положений одной или более группой, выбранной из группы, включающей метил, F, Cl, ОН, OR2.1, COOR2.1, NH2 и N(СН3)2, а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Настоящее изобретение предпочтительно также относится к указанному выше способу получения соединений формулы 1, в которой:
R2 обозначает С1-С6-алкил, который необязательно может быть замещен галогеном и который необязательно может быть замещен одной или более группой, выбранной из группы, включающей OR2.1, COOR2.1, CONR2.2R2.3, SR2.1, фенил, моно- или бициклический С5-С10-гетероцикл, С5-С6-гетероарил, моно- или бициклический С5-С10-циклоалкил, CH2-NR2.2R2.3 и NR2.2R2.3, которая, в свою очередь, может быть замещена одной или более группой, выбранной из группы, включающей ОН, галоген, OR2.1, оксогруппу, С1-С6-алкил, фенил, COOR2.1, CH2-NR2.2R2.3 и NR2.2R2.3, а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Настоящее изобретение предпочтительно также относится к указанному выше способу получения соединений формулы 1, в которой:
R2 обозначает метил, этил или пропил,
а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Настоящее изобретение предпочтительно также относится к указанному выше способу получения соединений формулы 1, в которой:
R2 обозначает С1-С6-алкил, который необязательно замещен одной или более группой, выбранной из группы, включающей ОН, COOR2.1, СON(СН3)2, C1-С6-алкил, фенил, циклопропил и NR2.2R2.3, которая, в свою очередь, необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, фтор, хлор, бром, йод, OR2.1, оксогруппу, C1-С6-алкил, фенил, С1-С3-алканол, CH2-NR2.2R2.3 и NR2.2R2.3, а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Настоящее изобретение предпочтительно также относится к указанному выше способу получения соединений формулы 1, в которой:
R2 обозначает С1-С6-алкил, который замещен одной или более группой, выбранной из группы, включающей ОН, фенил, COOR2.1, NH2, где фенил, в свою очередь, необязательно может быть замещен одной или более группой, выбранной из группы, включающей ОН, фтор, хлор, бром, йод, OR2.1, C1-С6-алкил, CH2-NH2, СН2(СН3)2, NH2 и N(СН3)2.
а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Настоящее изобретение предпочтительно также относится к способу получения соединений формулы 1, в которой:
R2 обозначает группу формулы 9

в которой
R7 обозначает ОН или NH2; и
R6 обозначает группу, выбранную из группы, включающей С1-С6-алкил, С5-С10-гетероарил и С6-С10-арил, предпочтительно фенил, который необязательно может быть замещен одной или более группой, выбранной из группы, включающей галоген, ОН, COOR2.1, OR2.1, NH2, C1-С6-алкил, С1-С6-галогеналкил и С1-С6-алканол,
а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Настоящее изобретение предпочтительно также относится к способу получения соединений формулы 1, в которой:
R2 обозначает группу формулы 9
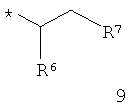
в которой
R7 обозначает ОН или NH2; и
R6 обозначает метил, этил, пропил, изопропил.
Настоящее изобретение предпочтительно также относится к способу получения соединений формулы 1, в которой
R2 обозначает моноциклическое С3-С7-циклоалкильное кольцо, которое может быть замещено в спиро-положении группой, выбранной из группы, включающей -ОН, -СН2-ОН, -СН2-СН2-ОН, разветвленный или неразветвленный С3-С6-алканол, -OR2.1, метил, этил, пропил, изопропил, бутил, изобутил и галоген, где R2.1 может быть выбран из группы, включающей метил, этил, пропил, изопропил, бутил, изобутил.
Настоящее изобретение предпочтительно также относится к способу получения соединений формулы 1, в которой:
R2 обозначает группу, выбранную из группы, включающей моноциклический насыщенный 3-, 4-, 5-, 6- или 7-членный гетероцикл, содержащий 1, 2 или 3 гетероатома, в каждом случае выбранных из N, О и S, который необязательно может быть замещен одной или более группой, выбранной из группы, включающей фтор, хлор, бром, ОН, оксогруппу и SH, или одной или более группой, выбранной из группы, включающей OR2.1, SR2.1, COOR2.1, COR2.1, C1-С6-алканол, С3-С10-циклоалкил, фенил, С1-С6-алкил, фенил-C1-С6-алкилен, C5-С10-гетероарил-С1-С6-алкилен, С5-С10-гетероцикл, С5-С10-гетероарил и NR2.2R2.3, которая, в свою очередь, необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, галоген, C1-С6-алкил, фенил и NR2.2R2.3,
в которой R2.1 обозначает Н или группу, выбранную из группы, включающей C1-С6-алкил, C1-С6-алканол, C1-С3-галогеналкил, моно- или бициклический С3-С10-циклоалкил, фенил-С1-С6-алкилен, моно- или бициклический С5-С10-гетероарил-С1-С6-алкилен, С3-С10-гетероцикл-С1-С6-алкилен, С3-С7-циклоалкил-С1-С6-алкилен, фенил, моно- или бициклический С5-С10-гетероарил и моноциклический насыщенный или ненасыщенный 5-, 6- или 7-членный гетероцикл, содержащий 1, 2 или 3 гетероатома, выбранных из N, О и S, который необязательно может быть замещен одной или более группой, выбранной из группы, включающей ОН, галоген, C1-С6-алкил и фенил, в которой R2.2 и R2.3 независимо друг от друга обозначают Н или группу, выбранную из группы, включающей галоген, С1-С6-алкил, моно- или бициклический С3-С10-циклоалкил, фенил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, фенил, моно- или бициклический С3-С10-гетероцикл, моно- или бициклический С5-С10-гетероарил, CO-NH2, CO-NHCH3, СО-N(СН3)2, SO2(C1-С2-алкил), CO-R2.1 и COOR2.1, которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, галоген, С1-С6-алкил, фенил и COOR2.1.
Настоящее изобретение предпочтительно также относится к способу получения соединений формулы 1, в которой:
R3 обозначает фтор, хлор, бром, йод или CN,
а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Настоящее изобретение предпочтительно также относится к указанному выше способу получения соединений формулы 1, в которой:
R3 обозначает группу -CO-NR3.1R3.2,
в которой R3.1 и R3.2 независимо друг от друга обозначают Н или группу, выбранную из группы, включающей С1-С6-алкил, С2-С6-алкенил, С2-С6-алкинил, С6-С10-арил, С6-С10-арил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкинилен, С5-С10-гетероарил-С1-С6-алкенилен, моно- или бициклический, С5-С10-гетероцикл, С5-С10-гетероцикл-С1-С6-алкилен и моно- или бициклический С5-С10-гетероарил, где группа в каждом случае необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, оксогруппу, галоген, C1-С6-алкил и O-C1-С6-алкил, а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Настоящее изобретение предпочтительно также относится к способу получения соединений формулы 1, в которой:
R3 обозначает группу -CO-NR3.1R3.2,
в которой R3.1 обозначает водород или метил, и
R3.2 обозначает группу, выбранную из группы, включающей С1-С6-алкил, С2-С6-алкенил, С2-С6-алкинил, С6-С10-арил, С6-С10-арил-С1-С6-алкилен, С5-С10-гетероарил-C1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкинилен, С5-С10-гетероарил-С1-С6-алкенилен, моно- или бициклический С5-С10-гетероцикл, C5-С10-гетероцикл-С1-С6-алкилен и моно- или бициклический С5-С10-гетероарил, где группа в каждом случае необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, оксогруппу, галоген, C1-С6-алкил и O-C1-С6-алкил,
а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Настоящее изобретение предпочтительно также относится к способу получения соединений формулы 1, в которой:
R3 обозначает группу -CO-NR3.1R3.2,
в которой R3.1 и R3.2 независимо друг от друга обозначают Н или группы, выбранные из группы, включающей C1-С6-алкил, фенил, фенил-C1-С6-алкилен, С5-С6-гетероарил-С1-С6-алкилен, С5-С6-гетероарил-С1-С6-алкинилен, С5-С6-гетероарил-С1-С6-алкенилен, моно- или бициклический С5-С10-гетероцикл, C5-С10-гетероцикл-C1-С6-алкилен и моно- или бициклический С5-С10-гетероарил, где группа в каждом случае необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, оксогруппу, галоген, C1-С6-алкил и O-С1-С6-алкил,
а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Настоящее изобретение предпочтительно также относится к способу получения соединений формулы 1, в которой:
R3 обозначает группу -NR3.3-CO-R3.4,
в которой R3.3 обозначает Н или группу, выбранную из группы, включающей С1-С6-алкил, С2-С6-алкенил, С2-С6-алкинил, С6-С10-арил, С6-С10-арил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, С3-С10-гетероцикл и С5-С10-гетероарил, которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, NH2, NR2.2R2.3, галоген, C1-С6-алкил и С6-С10-арил может быть замещенным, и
в которой R3.4 обозначает Н или группу, выбранную из группы, включающей С1-С6-алкил, С2-С6-алкенил, С2-С6-алкинил, C1-С6-алканол, OR2.1, СН2-O-СО-С1-С6-алкил, CH2NR2.2R2.3, NR2.2R2.3, С6-С10-арил, С6-С10-арил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, моно- или бициклический насыщенный или ненасыщенный С3-С10-гетероцикл, содержащий 1, 2 или 3 гетероатома, выбранных из О, S и N и моно- или бициклический С5-С10-гетероарил, содержащий 1, 2 или 3 гетероатома, выбранных из О, S и N, которая необязательно может быть замещена одной иди более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, NH2, NR2.2R2.3, галоген, С1-С6-алкил и С6-С10-арил,
а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Настоящее изобретение предпочтительно также относится к указанному выше способу получения соединений формулы 1, в которой:
R3 обозначает группу -NR3.3-CO-R3.4, в которой R3.3 обозначает водород или метил, и
в которой R3.4 обозначает группу, выбранную из группы, включающей С1-С6-алкил, С2-С6-алкенил, С2-С6-алкинил, C1-С6-алканол, OR2.1, СН2-О-СО-С1-С6-алкил, CH2NR2.2R2.3, NR2.2R2.3, С6-С10-арил, С6-С10-арил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, моно- или бициклический насыщенный или ненасыщенный С3-С10-гетероцикл, содержащий 1, 2 или 3 гетероатома, выбранных из N, S и О, и моно- или бициклический С5-С10-гетероарил, содержащий 1, 2 или 3 гетероатома, выбранных из N, S и О, которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, NH2, NR2.2R2.3, галоген, С1-С6-алкил и С6-С10-арил,
а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Настоящее изобретение предпочтительно также относится к способу получения соединений формулы 1, в которой:
R обозначает группу -NR3.3-CO-R3.4,
в которой R3.3 обозначает Н или группу, выбранную из группы, включающей С1-С6-алкил, фенил, фенил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, C5-С10-гетероцикл и С5-С10-гетероарил, которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, NH2, N(СН3)2, галоген, C1-С6-алкил и фенил, и в которой R3.4 обозначает Н или группу, выбранную из группы, включающей С1-С6-алкил, C1-С6-алканол, OR2.1, СН2-О-СО-С1-С6-алкил, CH2-NH2, СН2-N(СН3)2, NH2, N(СН3)2, фенил, фенил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, моно- или бициклический насыщенный или ненасыщенный С3-С10-гетероцикл, содержащий 1, 2 или 3 гетероатома, выбранных из N, S и О, и моно- или бициклический С5-С10-гетероарил, содержащий 1, 2 или 3 гетероатома, выбранных из N, S и О, которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, NH2, N(CH3)2, галоген, С1-С6-алкил и фенил, а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Настоящее изобретение предпочтительно также относится к указанному выше способу получения соединений формулы 1, в которой R4 и R5 обозначают Н или метил.
Настоящее изобретение предпочтительно относится к способу получения соединения формулы 1, в которой RA обозначает

Z обозначает галоген;
Х обозначает SO;
R1 обозначает Н или метил;
R2 обозначает Н или группу, выбранную из группы, включающей C1-С10-алкил, С2-С6-алкенил и С2-С6-алкинил, который необязательно может быть замещен галогеном, и которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей OR2.1, COOR2.1, CONR2.2R2.3, SR2.1, С6-С10-арил, моно- или бициклический С3-С10-гетероцикл, моно- или бициклический С5-С10-гетероарил, моно- или бициклический С3-С10-циклоалкил, CH2-NR2.2R2.3 и NR2.2R2.3, которая, в свою очередь, необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, галоген, OR2.1, оксогруппу, C1-С6-алкил, С6-С10-арил, COOR2.1, CH2-NR2.2R2.3 и NR2.2R2.3,
где R2.1 обозначает Н или группу, выбранную из группы, включающей С1-С6-алкил, C1-С6-алканол, C1-С3-галогеналкил, моно- или бициклический С3-С10-циклоалкил, С6-С10-арил-С1-С6-алкилен, моно- или бициклический С5-С10-гетероарил-C1-С6-алкилен, С3-С10-гетероцикл-С1-С6-алкилен, С3-С10-циклоалкил-С1-С6-алкилен, моно- или бициклический С6-С10-арил, моно- или бициклический С3-С10-гетероарил и моно- или бициклический, насыщенный или ненасыщенный гетероцикл, которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, галоген, С1-С6-алкил и С6-С10-арил,
где R2.2 и R2.3 независимо друг от друга обозначают Н или группу, выбранную из группы, включающей галоген, С1-С6-алкил, моно- или бициклический С3-С10-циклоалкил, С6-С10-арил-С1-С6-алкилен, С5-С10-гетероарил-С1-С6-алкилен, моно- или бициклический С6-С10-арил, моно- или бициклический С3-С10-гетероцикл, моно- или бициклический С5-С10-гетероарил, CO-NH2, СО-NНСН3, CO-N(CH3)2, SO2(С1-С2-алкил), CO-R2.1 и COOR2.1, которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, галоген, C1-С6-алкил, С6-С10-арил и COOR2.1,
или R2 обозначает моно- или полициклический С5-С10-циклоалкил, который необязательно может содержать мостик из одной или более C1-С3-алкильных групп и который необязательно может быть моно- или полизамещен ОН или галогеном или одной или более группой, выбранной из группы, включающей разветвленный или неразветвленный C1-С3-алканол, OR2.1, COOR2.1, SO2NR2.2R2.3, С5-С10-гетероцикл, фенил, C1-С6-алкил, фенил-С1-С6-алкилен, C5-С6-гетероарил-С1-С6-алкилен, моно- или бициклический С5-С10-циклоалкил и NR2.2R2.3, которая необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, OR2.1, оксогруппу, галоген, C1-С6-алкил, фенил и NR2.2R2.3,
или где NR1R2 вместе обозначают гетероциклическое С4-С7-кольцо, которое необязательно может содержать мостик, которое содержит 1, 2 или 3 гетероатома, выбранных из N, О и S, и которое необязательно может быть замещено одной или более группой, выбранной из группы, включающей ОН, OR2.1, C1-С6-алканол, оксогруппу, галоген, С1-С6-алкил, С6-С10-арил, COOR2.1, CH2-NR2.2-COO-R2.1, CH2-NR2.2-CO-R2.1, CH2-NR2.2-CO-CH2-NR2.2R2.3, CH2-NR2.2-SO2-C1-C3-алкил, CH2-NR2.2-SO2-NR2.2R2.3, CH2-NR2.2-CO-NR2.2R2.3, CO-NR2.2R2.3HNR2.2R2.3;
R3 обозначает фтор, хлор, бром, йод или CN; и R4 и R5 независимо выбраны из группы, включающей Н и C1-С6-алкил.
В другом предпочтительном варианте осуществления настоящее изобретение относится к способу получения соединения формулы 1, в которой RA обозначает

R2 обозначает С1-С10-алкил, который необязательно может быть замещен одной или более группой, выбранной из группы, включающей OR2.1, COOR2.1 и С6-С10-арил, где R2.1 обозначает Н,
или R2 обозначает моноциклический С5-С10-циклоалкил,
или в которой NR1R2 вместе обозначают гетероциклическое С4-С7-кольцо.
В еще одном предпочтительном варианте осуществления настоящее изобретение относится к способу получения соединения формулы 1, в которой
RA обозначает
 ;
;
Z обозначает хлорид;
Х обозначает SO;
R1 обозначает Н; и R4 и R5 независимо обозначают Н или метил.
В еще одном предпочтительном варианте осуществления настоящее изобретение относится к способу получения соединения формулы 1, в которой RA обозначает
 ;
;
Z обозначает хлорид;
Х обозначает SO;
R1 обозначает Н;
R3 обозначает хлорид; и
R4 и R5 независимо обозначают Н или метил.
Настоящее изобретение предпочтительно также относится к указанному выше способу получения соединений формулы 1, в которой:
R1 обозначает Н;
R2 выбран из группы, включающей Н, метил, этил, пропил,





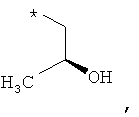
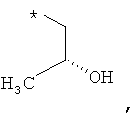



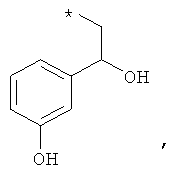




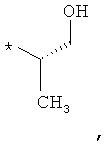
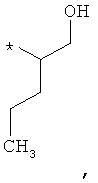




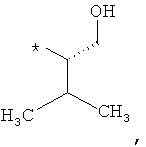
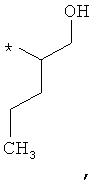






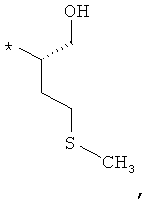


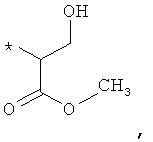



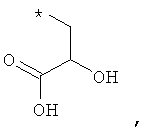




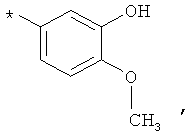

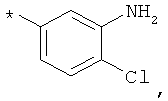






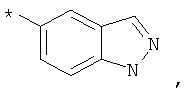






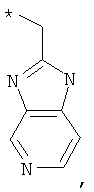
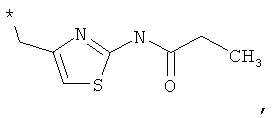





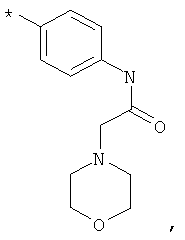
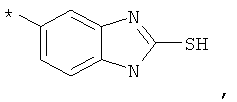
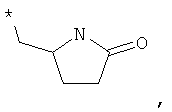





























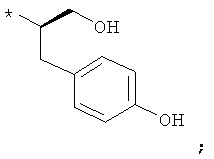


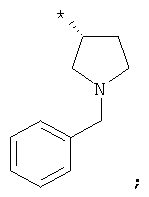


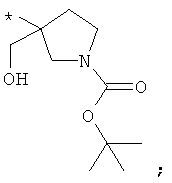





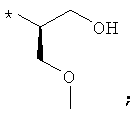











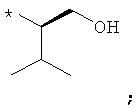






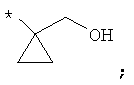



и 
RA обозначает

и
R3 выбран из группы, включающей хлорид, цианид,






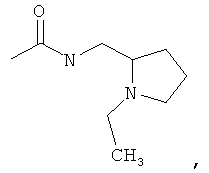












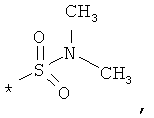


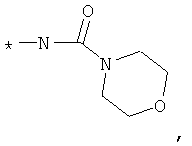
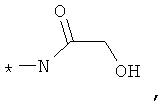






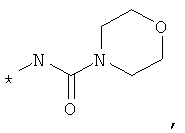
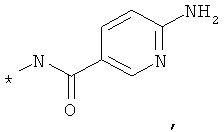






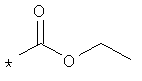 и бромид,
и бромид,
а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Настоящее изобретение предпочтительно также относится к указанному выше способу получения соединений формулы 1, в которой:
R1 обозначает Н;
NR1R2 выбран из группы, включающей





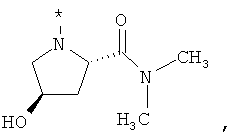







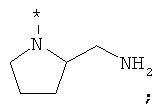









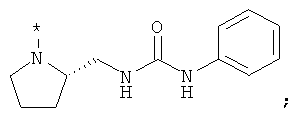



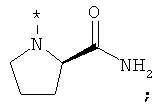






 и
и 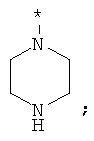
RA обозначает

R3 обозначает фторид, хлорид, бромид, нитрил или гидроксигруппу, а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Настоящее изобретение предпочтительно также относится к указанному выше способу получения соединений формулы 1, в которой:
R1 обозначает Н, R2 выбран из группы, включающей



 и
и 
RA выбран из группы, включающей
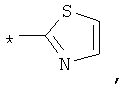
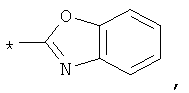








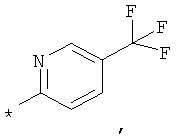
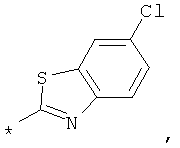





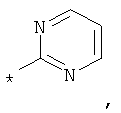







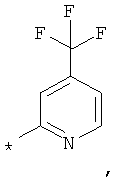

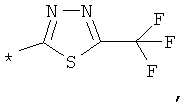
 и
и 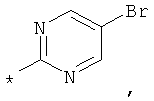
а также их фармакологически приемлемых солей, диастереоизомеров, энантиомеров, рацематов, гидратов или сольватов.
Способы получения соединений формулы 1 и промежуточных продуктов, применяющихся для их синтеза
Настоящее изобретение относится к способу получения соединений формулы 1, дигидротиенопиримидинов, и промежуточных соединений, используемых для их синтеза. Способ, предлагаемый в настоящем изобретении, является особенно подходящим для крупномасштабного синтеза дигидротиенопиримидинов, поскольку промежуточное соединение формулы 6 (см. схему 1) можно получить из исходного тиоэфира и αβ-ненасыщенного сложного эфира без необходимости проведения хроматографической очистки на последующих стадиях реакции. Другим преимуществом способа, предлагаемого в настоящем изобретении, является то, что промежуточное соединение формулы 4 уже содержит замещенный 4-фенилпиперазин-1-ильный фрагмент в положении 2, поэтому 4-гидроксильную группу можно превратить в галогенидную группу и затем аминировать и получить искомый 4-замещенный 2-(4-фенилпиперазин-1-ил)дигидротиенопиримидин. В способе, предлагаемом в настоящем изобретении, по существу устранены ограничения способа предшествующего уровня техники, в котором раскрыто получение промежуточного 2,4-дигалогендигидротиенопиримидина, который затем аминируют по двум различным заместителям. Способ предшествующего уровня техники приводит к образованию нежелательных региоизомеров, что делает необходимым проведение очистки с помощью хроматографии, что, в свою очередь, (а) препятствует проведению крупномасштабного синтеза и (б) значительно уменьшает общий выход искомого продукта. В отличие от этого, в способе, предлагаемом в настоящем изобретении, промежуточное соединение формулы 4 можно превратить в соответствующий 4-галогенид, и алкилировать его подходящим амином и получить искомый продукт (соединение формулы 1) без необходимости проведения хроматографической очистки. И в заключение, можно успешно осуществить стереоселективное окисление соединения формулы 3 с образованием соединения формулы 2 или соединения формулы 8 с образованием соединения формулы 1. Ни одну из стадий реакции способа синтеза, предлагаемого в настоящем изобретении, не требуется проводить при чрезвычайно высоких или низких температурах, использование которых может быть сложным, дорогостоящим и потенциально опасным при проведении крупномасштабного синтеза. Также ни одну из реакций, раскрытых в настоящем изобретении, не требуется проводить с использованием микроволнового излучения, применение которого невозможно при крупномасштабном синтезе.
Общий синтез




На схеме 1 описан общий способ синтеза соединений формулы 1, в которой RA, Ra, R1-R5, Z и X являются такими, как определено в настоящем изобретении.
Диалкил-3-тиаадипат получают по реакции соответствующего алкил-2-тиоэтилового эфира с αβ-ненасыщенным алкиловым эфиром в присутствии основания. Предпочтительно, если основанием является органическое основание, и его предпочтительно используют только в каталитических количествах. Специалисту в данной области техники должны быть известны многие органические основания, подходящие для этой реакции. Предпочтительные основания включают третичные и вторичные амины, такие как триэтиламин и пиперидин, наиболее предпочтительным основанием является пиперидин.
Без необходимости проведения перегонки или хроматографической очистки диалкил-3-тиаадипат можно циклизовать с образованием алкил-3-оксотетрагидротиофен-2-карбоксилата в присутствии амина-основания и металлоорганического катализатора или кислоты Льюиса, такой как TiCl4, (i-PrO)2TiCl2, (i-РrО)3ТiСl и (i-PrO)TiCl3. Например, можно использовать Ti(OR)nClm, где R обозначает алкил, n=1-3 и m+n=4. Предпочтительной кислотой Льюиса является ТiСl3(ОiРr). Также можно использовать хиральные варианты вышеуказанных катализаторов, полученных путем добавления хиральных лигандов, таких как BINOL, замещенный BINOL, хиральные диолы, BINAP, DuPhos, Taddols и тартраты. Другими возможными реагентами, известными для проведения региоселективной конденсации Дикмана, являются соединения или кислоты Льюиса следующих формул: SnX4, CuX2 и NiX2, в которых Х выбран из группы, включающей Сl, Вr и -OTf. Этот список не является исчерпывающим, и специалист в данной области техники должен быть знаком с другими подходящими металлоорганическими катализаторами. Подходящие амины-основания известны специалисту в данной области техники. Однако предпочтительными являются третичные амины-основания, например триэтиламин и диизопропилэтиламин (ДИПЭА). Предпочтительным растворителем является дихлорметан. Также можно использовать другие растворители, такие как толуол, хлороформ и CCl4. Если для остановки реакции используют кислоту, то можно использовать кислоты, такие как, но не ограничиваясь только ими, НСl или H2SO4. Фильтрование через MgSO4 можно не проводить или заменить фильтрованием через другие среды, такие как Na2SO4, целит, древесный уголь и т.д. Эту реакцию проводят при температуре в диапазоне от 0 до -78ºС. Этот способ получения промежуточных соединений формулы 6 обеспечивает возможность проведения последующей стадии или всего синтеза без необходимости какой-либо хроматографической очистки.
Без проведения какой-либо перегонки в высоком вакууме или хроматографической очистки алкил-3-оксотетрагидротиофен-2-карбоксилат можно ввести в реакцию с промежуточным гуанидином и получить промежуточное соединение формулы 4. Эту реакцию проводят в присутствии основания. Специалисту в данной области техники должны быть известны основания, подходящие для этой реакции. Предпочтительным основанием является металлоорганическое основание, такое как t-BuOK, t-BuONa, NaOCH3, NaOEt, n-BuLi, t-BuLi, NaOH или NaH, и его можно использовать в комбинации с другими растворителями (например, МеОН, i-PrOH, t-BuOH). Наиболее предпочтительным основанием является NаОСН3. Также можно использовать другие органические амины-основания, такие как пиридин, пирролидин, триэтиламин или ДИПЭА. В этой реакции можно использовать многие различные органические растворители. Специалисту в данной области техники должно быть известно, какие растворители могут быть подходящими для этой реакции, в частности, принимая во внимание выбранное основание. Если в качестве основания используют NаОСН3, то в качестве растворителя предпочтительно использовать метанол. Обычно реакцию проводят при нагревании до температуры выше комнатной, и более предпочтительно, если реакцию проводят при нагревании примерно до 60ºС или выше, или в случае использования метанола в качестве растворителя предпочтительно, если реакцию проводят при кипячении с обратным холодильником. Если для остановки реакции используют кислоту, то остановку реакции можно проводить с использованием таких кислот, как НСl, H2SO4 или АсОН. Циклоконденсация протекает с образованием различных солей гуанидина и его свободного основания.
Без проведения хроматографической очистки промежуточное соединение формулы 4 можно превратить в промежуточное соединение формулы 3. Например, гидроксильную группу можно превратить в сульфонильную или сульфонированную отщепляющуюся группу, такую как тозилат, мезилат, безилат, брозилат, трифлат или нозилат. Спирты можно превратить в соответствующие галогениды с использованием многих различных реагентов и условий проведения реакций, и они должны быть известны специалисту в данной области техники, поскольку в литературе описано множество примеров. Одной из возможностей является использование реагента формулы POZ3, в которой Z обозначает галоген. Предпочтительной методикой является превращение гидроксильной группы в галогенидную группу. Наиболее предпочтительным галогенидом является такой, в котором Z обозначает Сl. Предпочтительными реагентами для этой реакции являются РОСl3, SOCl2, SO2Cl2, (СОСl)2, РСl5, РОСl3/РСl5, Сl2 и NCS. Другой возможностью является присоединение отщепляющейся группы в положение гидроксильной группы. Подходящие отщепляющиеся группы включают F и отщепляющиеся группы, не содержащие галогены, включая, но не ограничиваясь только ими, NO2 и N2. В зависимости от выбранных реагентов можно использовать различные растворители, но в случае использования РОСl3 наилучшим является апротонный органический растворитель, такой как CH3CN, СН2Сl2, толуол, СНСl3 и диэтиловый эфир. Для крупномасштабного синтеза в качестве растворителя предпочтительно использовать СН3СН. Эту реакцию можно проводить при комнатной температуре, но предпочтительно проводить реакцию при нагревании примерно до 50ºС или выше, и более предпочтительно проводить реакцию при нагревании примерно до 60ºС или выше. Специалисту в данной области техники также должны быть известны реагенты и условия проведения реакций для превращения гидроксильной группы в сульфонильную отщепляющуюся группу. Обычно реакцию проводят с использованием соответствующего сульфонилгалогенида, например, для образования тозилата можно использовать тозилхлорид.
Без проведения хроматографической очистки промежуточное соединение формулы 3 можно аминировать необходимым замещенным амином (NR1R2) в щелочной среде и получить дигидротиенопиримидин формулы 8. Подходящие для этой реакции основания включают такие, как, но не ограничиваясь только ими, амины, NaH, t-BuONa, t-BuOK, DBU, KN(TMS)2, NaN(TMS)2, LiN(TMS)2 и LDA. Другие основания включают i-Pr2NEt, Et3N, морфолин и пиридин.
Предпочтительными основаниями для этой реакции являются третичные амины-основания, такие как триэтиламин и диизопропилэтиламин. Специалисту в данной области техники должны быть известны подходящие для этой реакции растворители, например ТГФ, диглим, ДМСО, NMP, DMAc, ацетонитрил и вода. Предпочтительным растворителем является ДМСО. Эту реакцию можно проводить при комнатной температуре, но предпочтительно проводить реакцию при нагревании примерно до 60ºС или выше, и более предпочтительно - примерно до 80ºС.
Дигидротиенопиримидин формулы 8 можно окислить. Окисление с образованием сульфидов можно осуществить с использованием многих реагентов и условий проведения реакций, и они должны быть известны специалисту в данной области техники, поскольку в литературе описано множество примеров. Кроме того, специалисту в данной области техники должны быть известны хиральные катализаторы, которые можно использовать в реакции окисления для обеспечения энантиоселективности. Например, стереоселективное окисление можно провести в присутствии системы хиральный лиганд/металл или стехиометрического количества окислительного реагента и растворителя. Системой хиральный лиганд/металл может являться Ti/BINOL, замещенный BINOL, WО3/хиральный лиганд, оксазиридин Дэвиса, D-эпоксон/оксон, Mn/Salen, Ti/варианты гидробензоина, Ti/миндальная кислота, Ti/DET, V(acac)2 или Fе(асас)3/хиральный лиганд, тогда как использующимся в стехиометрическом количестве окислительным реагентом может являться гидропероксид кумола, пероксид водорода, раствор трет-бутилгидропероксида, МСРВА, пероксибензойные кислоты, оксон или диоксираны. Растворы гидропероксида можно приготовить в растворителях, например в декане, нонане, толуоле и воде. Подходящие для этой реакции растворители включают, например, толуол, метиленхлорид, хлороформ, ацетонитрил, ТГФ и фторбензол. Окисление предпочтительно проводить с использованием трет-бутилгидропероксида, и более предпочтительно проводить окисление с использованием трет-бутилгидропероксида, Ti(i-PrO)4 и (S)-гидробензоина и получить большой избыток R-энантиомера.
Альтернативно, без проведения хроматографической очистки промежуточное соединение формулы 3 можно окислить, как описано выше, и получить промежуточное соединение формулы 2. Затем промежуточное соединение формулы 2 можно аминировать замещенным амином, как описано выше, и получить искомое соединение формулы 1
Примеры синтеза
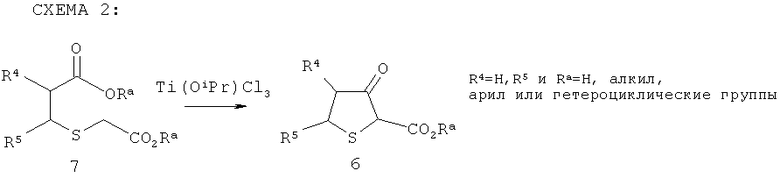
На схеме 2 описан эффективный и региоселективный синтез эфиров 3-оксотетрагидротиофен-2-карбоновой кислоты. Использование в качестве катализатора кислоты Льюиса, например Ti(OiPr)Cl3, вместо основания, такого как NaOMe, NaH, R3N и т.п., обеспечивает селективное образование соединения формулы 6 и исключает образование нежелательного региоизомера (см., например, а3 в уравнении 1). Такое региоселективное образование исключает необходимость трудоемкого хроматографического разделения и увеличивает общий выход желательного изомера формулы 6. Кроме того, отказ от использования щелочной среды при проведении реакции и обработки предотвращает последующее разложение продукта. Использование Тi(OiРr)Сl3 является особенно подходящим для предотвращения образования продуктов хлорирования и элиминирования, которые образуются при использовании других кислот Льюиса, таких как TiCl4.
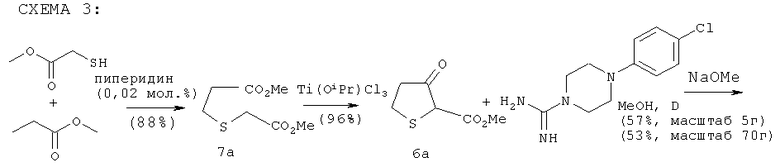



Приведенные ниже экспериментальные методики относятся к конкретному синтезу, описанному на схеме 3.
4-(4-Хлорфенил)пиперазин-1-карбоксамид(5а):
К суспензии 20,01 г 1-(4-хлорфенил)пиперазина в 60 мл этанола добавляют 10,44 г пиразол-1-карбоксамидингидрохлорида и 55 мл диизопропилэтиламина. Затем реакционную смесь перемешивают при кипячении с обратным холодильником. Через 6 ч добавляют еще 1,50 г пиразола (0,14 г). После кипячения с обратным холодильником в течение еще 1 ч реакционной смеси дают охладиться до комнатной температуры. Мутную смесь концентрируют до объема, равного примерно половине исходного. Добавляют воду (30 мл) и смесь перемешивают в течение ночи. Белое твердое вещество отфильтровывают, промывают водой (2×10 мл) и сушат при пониженном давлении при 50ºС и получают 11,88 г 4-(4-хлорфенил)пиперазин-1-карбоксамида в виде белого твердого вещества. Затем мутный фильтрат дополнительно концентрируют, и вторая порция продукта осаждается, и ее сушат и получают 5,13 г 4-(4-хлорфенил)-пиперазин-1-карбоксамида (общий выход 99%).
Метил-3-оксотетрагидротиофен-2-карбоксилат (6а):
В сухой реактор с рубашкой с инертной атмосферой объемом 2 л, снабженный датчиком температуры, механической мешалкой и капельной воронкой, помещают TiCl4 (668 мл 1,0 М раствора в CH2Cl2). Раствор охлаждают до -10ºС. При -10ºС добавляют изопропанол (51 мл) и смесь перемешивают в течение 30 мин. В течение 1 ч медленно добавляют раствор диметил-3-тиаадипата (метил-3-[(2-метокси-2-оксоэтил)тио]пропаноат (7а, 120 г)) и CH2Cl2 (500 мл), поддерживая внутреннюю температуру равной -10°С или ниже. Реакционную смесь перемешивают при -10ºС в течение 30 мин. В течение 1 ч по каплям добавляют Et3N (287 мл), поддерживая внутреннюю температуру равной -10ºС или ниже. После завершения добавления смесь перемешивают в течение 1-2 ч, затем смесь охлаждают до -10ºС и добавляют 3 н. раствор НСl (примерно 800 мл). Смесь нагревают до 30ºС и энергично перемешивают в течение не менее 1 ч. Органический слой собирают и водный слой дважды экстрагируют дихлорметаном (примерно по 500 мл). Объединенную органическую порцию дважды промывают водой (примерно 500 мл). Раствор фильтруют через тонкий слой MgSO4 и промывают дихлорметаном. Летучие компоненты удаляют путем отгонки (температура =25ºС, давление =35 Торр) и получают коричневое масло (116 г, по данным анализа содержание 75%, выход 87%). Неочищенное вещество сразу используют или хранят под слоем азота или аргона и до использования держат в холодильнике. По данным ЯМР (ядерный магнитный резонанс) продукт представляет собой смесь кетонный таутомер/енольный таутомер состава, равного примерно 12:1. 1Н ЯМР (400 МГц, CDCl3) кетонный таутомер: δ 4,03 (s, 1Н), 3,77 (s,3H), 3,31 (ddd, J=7,5, 8,0, 11,5 Гц, 1Н), 3,05 (ddd, J=3,5, 8,0, 11,5 Гц, 1Н), 2,84 (ddd, J=3,5, 7,5, 18,0 Гц, 1Н), 2,66 (ddd, J=8,5, 8,5, 18,0 Гц, 1Н); енольный таутомер: 10,47 (s, 1Н), 3,80 (s, 3Н), 3,13 (dd, J=8,5, 8,5 Гц, 2Н), 2,95 (dd, J=8,5, 8,5 Гц, 2Н); ГХМС (газовая хроматография-масс-спекроскопия) для C6H8O3S (M+): рассчитано 160, найдено 160.
Кроме того, по описанной выше экспериментальной методике получают приведенные ниже аналоги:

2-[4-(4-Хлорфенил)пиперазин-1-ил]-6,7-дигидротиено[3,2-d]пиримидин-4-ол (4а):
В реактор с инертной атмосферой, снабженный охлаждающей рубашкой, термометром с термопарой, механической мешалкой и линией подачи N2, помещают гуанидин (5, 70 г). Добавляют метанол (140 мл). Добавляют 25% раствор NaOMe в метаноле (224 мл). В реактор добавляют метил-3-оксотетрагидротиофен-2-карбоксилат (6а, 62,1 г). Смесь перемешивают при кипячении с обратным холодильником в течение 3-7 ч. Смесь охлаждают до 22-25ºС. Реакционную смесь медленно нейтрализуют до рН=6 2 М раствором НСl (примерно 250 мл). Смесь перемешивают при 22-25ºС в течение 3 ч (не менее). Полученное твердое вещество собирают фильтрованием. Отфильтрованное твердое вещество 2 раза промывают изопропанолом (примерно по 50 мл) и 2-5 раз водой (примерно по 50 мл). Твердое вещество сушат на воздухе на воронке для фильтрования в течение не менее 2 ч. Твердое вещество сушат в вакуумном сушильном шкафу при пониженном давлении при 50°С в течение ночи и получают 56,2 г (55%) продукта в виде почти белого твердого вещества. 1Н ЯМР (400 МГц, CDCl3) δ 11,51 (s, 1H), 7,25-7,35 (m, 2H), 6,95-7,05 (m, 2H), 3,70-3,76 (m, 2H), 3,16-3,24 (m, 4H), 3,25(dd, J=8,0, 8,0 Гц, 2H), 3,07 (dd, J=8,5, 8,5 Гц, 2H); 13С ЯМР (400 МГц, СDСl3) δ 150,5, 129,6, 123,7, 118,1, 48,6, 45,3, 38,5, 28,9 (8 сигналов отсутствуют вследствие перекрывания). ЖХМС (жидкостная хроматография-масс-спектроскопия) (ИЭР (ионизация электрораспылением)) для C16H18ClN4OS (M+H)+: рассчитано 349,1, найдено 349,1.
4-Хлор-2-[4-(4-хлорфенил)пиперазин-1-ил]-6,7-дигидротиено[3,2-d]пиримидин (3а):
В сухой реактор с рубашкой с инертной атмосферой, снабженный механической мешалкой, термометром с термопарой, капельной воронкой и линией подачи N2, помещают 2-[4-(4-хлорфенил)-пиперазин-1-ил]-6,7-дигидротиено[3,2-d]пиримидин-4-ол (4а, 50,4 г). В реактор добавляют ацетонитрил (250 мл), затем РОСl3 (14,8 мл), поддерживая температуру равной 25-35ºС. Смесь перемешивают при 60ºС в течение 4-6 ч и затем устанавливают внутреннюю температуру равной 23±2ºС. В другом реакторе готовят 2 н. водный раствор NaOH (примерно 250 мл). Содержимое первого реактора выливают в реактор, содержащий 2 н. раствор NaOH, поддерживая температуру ниже 20ºС. Полученную выше смесь перемешивают при 23±2ºС в течение 16 ч и твердое вещество собирают фильтрованием. Отфильтрованное твердое вещество 3-5 раз промывают водой (примерно по 50 мл), отфильтрованное твердое вещество сушат на воздухе (с отсасыванием) в течение 3-4 ч и затем сушку продолжают в вакуумном сушильном шкафу при 50ºС в течение не менее 16 ч. Полученное твердое вещество (96,0 г, 95%) переносят в подходящий сосуд и хранят в атмосфере азота или аргона. ЯМР (400 МГц, CDCl3) δ 7,18-7,26 (m, 2H), 6,82-6,93 (m, 2H), 3,88-3,94 (m, 4Н), 3,22-3,36 (m, 4Н), 3,15-3,21 (m, 4H); 13С ЯМР (400 МГц, СDСl3) δ 172,8, 160,4, 152,9, 150,1, 129,4, 125,4, 119,8, 118,1, 77,6, 49,6, 44,4, 38,0, 29,3 (4 сигнала отсутствуют вследствие перекрывания); ЖХМС (ИЭР) для C16H17Cl2N4S (М+Н)+: рассчитано 367,1, найдено 367,0.
(R)-4-Хлор-2-[4-(4-хлорфенил)пиперазин-1-ил]-6,7-дигидротиено[3,2-d]пиримидин 5-оксид (2а):
В реактор с рубашкой при механическом перемешивании со скоростью 400 об/мин, помещают (S)-гидробензоин (292 мг) и толуол (50 мл), затем Ti(i-PrO)4 (0,20 мл) и воду (0,25 мл). Смесь перемешивают при 20ºС в течение 30 мин. Затем добавляют 4-хлор-2-[4-(4-хлорфенил)-пиперазин-1-ил]-6,7-дигидротиено[3,2-d]пиримидин (За. 5,00 г) и смесь перемешивают при 20ºС в течение 15 мин, затем охлаждают до 0ºС (для этого требуется 20 мин). К реакционной смеси добавляют ТБГП (трет-бутилгидропероксид) (70% водный раствор) (0,75 мл) и перемешивают при 0ºС в течение 23 ч. Степень превращения составляет 96% при энантиомерном избытке (ЭИ) 89%. Реакцию останавливают 5% раствором Na2SO3 (20 мл). Слои разделяют и водный слой экстрагируют дихлорметаном (50 мл). Органические слои объединяют и промывают водой (20 мл), сушат (MgSO4), фильтруют и концентрируют и получают искомый сульфоксид (4,6 г, выход 88%, 89% ЭИ). Продукт можно перекристаллизовать из смеси ТГФ/вода (5:1) с хорошим выходом и получить вещество с ЭИ>96%. ЯМР (400 МГц, СDСl3) δ 7,16-7,26 (m, 2H), 6,80-6,90 (m, 2H), 3,90-4,20 (m, 4Н), 3,75-3,90 (m, 1H), 3,00-3,30 (m, 7 H); 13С ЯМР (400 МГц, CDCl3) δ 177,5, 162,5, 160,7, 149,8, 129,4, 125,7, 123,9, 118,2, 49,6, 46,5, 44,7, 44,4, 33,7 (3 сигнала отсутствуют вследствие перекрывания); ЖХМС (ИЭР) для C16H17Cl2N4OS (M+H)+: рассчитано 383,1, найдено 383,0.
Дополнительные примеры
Приведенные ниже соединения получают путем аминирования полученного выше (R)-4-хлор-2-[4-(4-хлорфенил)-пиперазин-1-ил]-6,7-дигидротиено[3,2-d]пиримидин-5-оксида (2) различными аминами или аминокислотами так, как подробно описано ниже.
Метиловый эфир (R)-2-{(R)-2-[4-(4-хлорфенил)пиперазин-1-ил]-5-оксо-6,7-дигидро-5Н-5λ4-тиено[3,2-d]пиримидин-4-иламино}-3-метилмасляной кислоты:

Получают по методике получения (R)-2-{(R)-2-[4-(4-хлорфенил)пиперазин-1-ил]-5-оксо-6,7-дигидро-5Н-5λ4-тиено[3,2-d]пиримидин-4-иламино}-3-метилбутан-1-ола (за исключением того, что не проводят перекристаллизацию из ИПС (изопропиловый спирт)) из (R)-4-хлор-2-[4-(4-хлорфенил)пиперазин-1-ил]-6,7-дигидротиено[3,2-d]пиримидин-5-оксида и метилового эфира D-валина (1,3 экв.). Получают неочищенный продукт с выходом 85%. 1Н ЯМР (500 МГц, CDCl3) δ 7,18-7,26 (m, 2Н). 6,82-6,90 (m, 2H), 5,78 (d, J=6,5 Гц, 1Н), 4,59 (dd, J=7,0, 7,0 Гц, 1Н), 3,98 (bs, 4H), 3,72 (s, 3H), 3,62 (ddd, J=7,5, 7,5, 15,0 Гц, 1Н), 3,36 (ddd, J=8,0, 8,0, 15,0 Гц, 1Н), 3,10-3,20 (m, 4H), 2,95-3,10 (m 2H), 2,23 (m, 1Н), 1,00-1,07 (m, 6H); 13С ЯМР (500 МГц, СDCl3) δ 174,8, 172,8, 163,1, 159,8, 150,2, 129,4, 125,4, 118,0, 109,0, 59,6, 59,5, 52,3, 50,4, 49,7, 44,1, 33,0, 31,3, 19,4, 19,1 (3 сигнала отсутствуют вследствие перекрывания); ЖХМС (ИЭР) для С22Н29СlN5O3S (М+Н)+: рассчитано 478,2, найдено 478,1.
(R)-2-{(R)-2-[4-(4-Хлорфенил)пиперазин-1-ил]-5-оксо-6,7-дигидро-5Н-5λ4-тиено[3,2-d]пиримидин-4-иламино}-3-метилбутан-1-ол:

В 3-горлую круглодонную колбу, снабженную датчиком температуры, патрубком для подачи азота и мешалкой, помещают (R)-4-хлор-2-[4-(4-хлорфенил)пиперазин-1-ил]-6,7-дигидротиено[3,2-d]пиримидин-5-оксид (0,10 г), D-валинол (46,8 мг) и ДМСО (2 мл). Добавляют диизопропилэтиламин (0,1 мл) и смесь при перемешивании нагревают при 80ºС в течение 2 ч. Смесь охлаждают до температуры окружающей среды и медленно добавляют воду (3-5 мл), что приводит осаждению продукта в виде почти белого твердого вещества. Твердое вещество отфильтровывают и промывают водой. Твердое вещество сушат в вакууме при 50ºС в течение 12 ч и получают (R)-2-{(R)-2-[4-(4-хлорфенил)-пиперазин-1-ил]-5-оксо-6,7-дигидро-5Н-5λ4-тиено[3,2-d]пиримидин-4-иламино}-3-метилбутан-1-ол (0,21 г, выход 92%) в виде почти белого твердого вещества. Это вещество перекристаллизовывают из смеси ИПС/Н2О (15 об./0,5 об.) и получают вещество, обладающее чистотой>99%. 1Н ЯМР (400 МГц, СDСl3) δ 7,16-7,26 (m, 2Н), 7,00 (bs, 1Н), 6,80-6,90 (m, 2H), 4,02-4,12 (m, 1H), 3,90-4,00 (m, 4H), 3,68-3,85 (m, 3Н), 3,55-3,65 (m, 1H), 3,35-3,45 (m, 1H), 3,12-3,20 (m, 4H), 2,94-3,08 (m, 2H), 1,92-2,06 (m, 1H), 0,95 (d, J=6,5 Гц, 3Н), 0,90 (d, J=6,5 Гц, 3Н); 13С ЯМР (400 МГц, CDCl3) δ 174,6, 163,1, 160,4, 150,1, 129,4, 125,3, 118,0, 107,6, 63,9, 58,6, 49,6, 44,1, 33,0, 29,7, 20,2, 19,8 (5 сигналов отсутствуют вследствие перекрывания); ЖХМС (ИЭР) для C21H29ClN5O2S (М+Н)+: рассчитано 450,2, найдено 450,1.
{(R)-2-[4-(4-Хлорфенил)пиперазин-1-ил]-5-оксо-6,7-дигидро-5Н-5λ4-тиено[3,2-d]пиримидин-4-ил}-((S)-1-фенилэтил)амин:

Получают по методике получения (R)-2-{(R)-2-[4-(4-хлорфенил)-пиперазин-1-ил]-5-оксо-6,7-дигидро-5Н-5λ4-тиено[3,2-d]пиримидин-4-иламино}-3-метилбутан-1-ола (перекристаллизацию из смеси ИПС/Н2О заменяют на промывку смесью ИПС/Н2О) из (R)-4-хлор-2-[4-(4-хлорфенил)-пиперазин-1-ил]-6,7-дигидротиено[3,2-d]пиримидин-5-оксида и (S)-метилбензиламина. Получают очищенный продукт с выходом 57%. 1Н ЯМР (400 МГц, CDCl3) δ 7,18-7,28 (m, 4Н), 7,05-7,17 (m, 3Н), 6,80-6,90 (m, 2H), 6,52 (d, J=5,6 Гц, 1Н), 5,19 (dddd, J=7,0, 7,0, 7,0, 7,0 Гц, 1Н), 3,80-4,00 (m, 4Н), 3,58 (ddd, J=8,0, 8,0, 16,0 Гц, 1Н), 3,34 (ddd, J=8,0, 8,0, 16,0 Гц, 1Н), 2,90-3,20 (m, 6H), 1,55 (d, J=7,2 Гц, 3Н); 13С ЯМР (400 МГц, CDCl3) δ 174,6, 163,2, 159,2, 150,2, 144,4, 129,4, 128,6, 127,1, 126,3, 125,3, 118,0, 108,5, 51,1, 50,2, 49,6, 44,1, 33,0, 23,2 (6 сигналов отсутствуют вследствие перекрывания); ЖХМС (ИЭР) для C24H27ClN5OS (М+Н)+: рассчитано 468,2, найдено 468,3.
{(R)-2-[4-(4-Хлорфенил)пиперазин-1-ил]-5-оксо-6,7-дигидро-5Н-5λ4-тиено[3,2-d]пиримидин-4-ил}циклогексиламин:

Получают по методике получения (R)-2-{(R)-2-[4-(4-хлорфенил)-
пиперазин-1-ил]-5-оксо-6,7-дигидро-5Н-5λ4-тиено[3,2-d]пиримидин-4-иламино}-3-метилбутан-1-ола (перекристаллизацию из смеси ИПС/Н2О заменяют на промывку смесью ИПС/Н2О) из (R)-4-хлор-2-[4-(4-хлорфенил)-пиперазин-1-ил]-6,7-дигидротиено[3,2-d]пиримидин-5-оксида и циклогексиламина. Получают очищенный продукт с выходом 77%. 1Н ЯМР (400 МГц, СDСl3) δ 7,18-7,24 (m, 2H), 6,80-6,90 (m, 2H), 5,77 (d, J=7,2 Гц, 1Н), 3,88-4,02 (m, 5H), 3,58 (ddd, J=7,5, 7,5, 15,0 Гц, 1Н), 3,31 (ddd, J=8,0, 8,0, 15,5 Гц, 1Н), 3,12-3,22 (m, 4H), 2,90-3,06 (m, 2H), 1,10-2,00 (m, 10Н); 13С ЯМР (400 МГц, CDCl3) δ 174,3, 163,4, 159,3, 150,2, 129,3, 125,3, 118,0, 108,5, 50,1, 50,0, 49,6, 44,1, 33,1, 33,0, 32,8, 25,9, 25,4, 25,3 (4 сигнала отсутствуют вследствие перекрывания); ЖХМС (ИЭР) для C22H29ClN5OS (М+Н)+: рассчитано 446,2, найдено 446,2.
(R)-2-[4-(4-Хлорфенил)пиперазин-1 -ил]-4-пиперидин-1 -ил-6,7-дигидротиено[3,2-d]-пиримидин-5-оксид:

Получают по методике получения (R)-2-{(R)-2-[4-(4-хлорфенил)-пиперазин-1-ил]-5-оксо-6,7-дигидро-5Н-5λ4-тиено[3,2-d]пиримидин-4-иламино}-3-метилбутан-1-ол (перекристаллизацию из смеси ИПС/Н2О заменяют на промывку смесью ИПС/Н2О) из (R)-4-хлор-2-[4-(4-хлорфенил)-пиперазин-1-ил]-6,7-дигидротиено[3,2-d]пиримидин-5-оксида и пиперидина. Получают очищенный продукт с выходом 61%. 1Н ЯМР (400 МГц, CDCl3) δ 7,18-7,24 (m, 2H), 6,80-6,90 (m, 2H), 3,95-4,00 (m, 4H), 3,80-3,95 (m, 4H), 3,68 (ddd, J=8,0, 8,0, 16,0 Гц, 1Н), 3,13-3,20 (m, 4H), 2,96-3,13 (m, 3H), 1,60-1,80 (m, 6H); 13С ЯМР (400 МГц, CDCL3) δ 177,7, 162,3, 159,9, 150,2, 129,4, 125,3, 118,0, 109,8, 49,7, 48,3, 48,0, 44,1, 32,8, 26,1, 24,9 (6 сигналов отсутствуют вследствие перекрывания); ЖХМС (ИЭР) для C21H27ClN5OS (M+H)+: рассчитано 432,2, найдено 432,3.
Другие примеры дигидротиенопиримидинов, которые можно получить по методикам синтеза, аналогичным описанным в настоящем изобретении, описаны в публикации U.S. №2008/0096882 А1, которая включена в настоящее изобретение в качестве ссылки. Эти соединения являются подходящими в качестве ингибиторов PDE4 и обладают значениями IС50, меньшими или равными 1 мкмоль.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОНДЕНСИРОВАННОЕ ГЕТЕРОЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ | 2009 |
|
RU2480473C2 |
| ЗАМЕЩЕННЫЕ ГЕТЕРОЦИКЛОМ ПИПЕРАЗИНОДИГИДРОТИЕНОПИРИМИДИНЫ | 2008 |
|
RU2500681C2 |
| ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ В КАЧЕСТВЕ ИНГИБИТОРОВ АДГЕЗИИ ЛЕЙКОЦИТОВ И VLA-4-АНТАГОНИСТОВ | 1997 |
|
RU2229296C2 |
| СОЕДИНЕНИЕ, НАЦЕЛЕННОЕ НА БЕЛОК И ЕГО ДЕГРАДАЦИЮ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2021 |
|
RU2829459C1 |
| АРИЛЬНЫЕ, ГЕТЕРОАРИЛЬНЫЕ И ГЕТЕРОЦИКЛИЧЕСКИЕ ФАРМАЦЕВТИЧЕСКИЕ СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ МЕДИЦИНСКИХ НАРУШЕНИЙ | 2018 |
|
RU2801278C2 |
| ДИГИДРОБЕНЗОДИАЗЕПИНЫ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2000 |
|
RU2247115C2 |
| АМИНОПИРИМИДИНЫ И ПИРИДИНЫ | 2002 |
|
RU2308455C2 |
| ЗАМЕЩЕННЫЕ ИЗОХИНОЛИНОВЫЕ И ИЗОХИНОЛИНОНОВЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ Rho-КИНАЗЫ | 2007 |
|
RU2455302C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ИМИДАЗОЛИДИНА, СПОСОБ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ | 1998 |
|
RU2239641C2 |
| НОВЫЕ ЗАМЕЩЕННЫЕ 8-ГЕТЕРОАРИЛКСАНТИНЫ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2004 |
|
RU2357969C2 |
Изобретение относится к улучшенному способу получения соединений формулы 6


Соединения формулы 6, являются промежуточными продуктами для получения дигидротиено[3,2-d]пиримидинов, обладающих действием на сердечно-сосудистую систему, седативным действием, или могут быть использованы при лечении воспалительных заболеваний суставов, кожи, глаз или заболеваний периферической или центральной нервной системы, респираторных или желудочно-кишечных нарушений. Способ включает стадии: а) взаимодействия реагентов формул HS-CH2-CO2Ra и CHR5=CR4-CO2Ra с получением промежуточного продукта формулы 7; и б) циклизации промежуточного продукта формулы 7 в растворителе и в присутствии TiCl2(O-iPr)2, TiCl(O-iPr)3, TiCl3(O-iPr) и в присутствии основания-амина, с получением продукта формулы 6. При этом Ra обозначает алкил, R4 и R5 независимо выбраны из группы, включающей H, C1-C6-алкил, C2-C6-алкенил, C2-C6-алкинил, C6-C10-арил, C6-C10-арил-C1-C6-алкилен, C5-C10-гетероарил-C1-C6-алкилен, C3-C10-гетероцикл и C5-C10-гетероарил, -O-C1-C6-алкил, -O-C6-C10-арил, -O-C3-C10-гетероцикл и -O-C5-C10-гетероарил, -NR′R″, фтор, C1-C6-фторалкил и C1-C6-фторалкоксигруппу, где R′ и R″ независимо выбраны из группы, включающей H и C1-C6-алкил, и где в каждом случае группа необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, оксогруппу, галоген, C1-C6-алкил и O-C1-C6-алкил. Способ позволяет получить промежуточные продукты 6, которые не требуют проведения перегонки и хроматографической очистки между стадиями при осуществлении процессов, подходящих для крупномасштабного синтеза дигидротиено[3,2-d]пиримидинов. В итоге это приводит к более высокому суммарному выходу конечных продуктов, чем при осуществлении способов предшествующего уровня техники. 5 з.п. ф-лы.
1. Способ получения соединений формулы 6

включающий стадии:
а) взаимодействия реагентов формул HS-CH2-CO2Ra и CHR5=CR4-CO2Ra с получением промежуточного продукта формулы 7:
 и
и
б) циклизации промежуточного продукта формулы 7 в растворителе и в присутствии TiCl2(O-iPr)2, TiCl(O-iPr)3, TiCl3(O-iPr) и в присутствии основания-амина с получением промежуточного продукта формулы 6, где
Ra обозначает алкил, и где
R4 и R5 независимо выбраны из группы, включающей H, C1-C6-алкил, C2-C6-алкенил, C2-C6-алкинил, C6-C10-арил, C6-C10-арил-C1-C6-алкилен, C5-C10-гетероарил-C1-C6-алкилен, C3-C10-гетероцикл и C5-C10-гетероарил, -O-C1-C6-алкил, -O-C6-C10-арил, -O-C3-C10-гетероцикл и -O-C5-C10-гетероарил, -NR′R″, фтор, C1-C6-фторалкил и C1-C6-фторалкоксигруппу, где R′ и R″ независимо выбраны из группы, включающей H и C1-C6-алкил, и где в каждом случае группа необязательно может быть замещена одной или более группой, выбранной из группы, включающей ОН, оксогруппу, галоген, C1-C6-алкил и O-C1-C6-алкил.
2. Способ по п.1, в котором R4 и R5 оба обозначают H.
3. Способ по п.1 или 2, в котором стадию реакции (а) проводят в присутствии основания.
4. Способ по любому из пп.1-3, в котором стадию циклизации (б) проводят в присутствии SnX4, CuX2 или NiX2, где X обозначает Cl, Br или OTf.
5. Способ по любому из пп.1-4, в котором растворителем является спиртовый или неспиртовый растворитель.
6. Способ по любому из пп.1-5, в котором стадию циклизации (б) проводят при температуре в диапазоне от 0 до -78°C.
| WO2006111549 A1, 26.10.2006 | |||
| US3318881A ,09.05.1967 | |||
| DE19540737 A1, 07.05.1997 | |||
| US4974609 A1, 04.12.1990 | |||
| ТЕПЛООБМЕННИК | 2016 |
|
RU2700215C2 |
| Deshmukh M N et al.Regioselective titanium tetrachloride mediated five membered hetero-cyclisations ,SYNTHETIC COMMUNICATIONS, 19960101Vol:26,Nr:9,Page(s):1657 " 1661 | |||
| Плечевой упор для стрельбы из ручного оружия | 1926 |
|
SU5889A1 |
| БИЦИКЛИЧЕСКИЕ ГЕТЕРОАРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ LH АГОНИСТОВ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2000 |
|
RU2248979C2 |
| RU2010119645А, 27.01.2012, приоритет 19.10.2007 | |||
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
Авторы
Даты
2014-09-10—Публикация
2008-10-15—Подача