Изобретение относится к области офтальмологии, а именно к офтальмоонкологии и предназначено для повышения эффективности лечения внутриглазных опухолей.
Среди новообразований органа зрения внутриглазные опухоли занимают второе место, уступая по частоте лишь опухолям век [Клиническая онкология органа зрения. Пачес А.И., Бровкина А.Ф., Зиангирова А.Ф. - М. - Медицина. - 1980 - С.323]. Существуют различные способы лечения внутриглазных опухолей. Выбор способа лечения зависит от стадии неопластического процесса и размеров опухоли. На стадиях Т1-3N0M0 и толщине опухоли до 7 мм возможно органосохранное лечение. К органосохранным способам лечения относят брахитерапию, фотодеструкцию, эндорезекцию. Каждый из перечисленных методов имеет свои показания и противопоказания, и все они обладают ограниченными возможностями.
Фотодеструкция, которая проводится на аргоновых и криптоновых лазерах, эффективна при меланомах, не превышающих по высоте 1,5 мм - 2,0 мм [Офтальмоонкология. - под ред. Бровкиной А.Ф. - Москва. - Медицина. - 2001 - стр.116-120]. Столь узкий спектр показаний объясняется механизмом лазерного воздействия, вызывающего лечебный эффект, а также глубиной проникновения лазерного излучения. Глубина проникновения излучения, находящегося в диапазоне длин волн 488 нм (аргон) и 514 нм (криптон) в ткани не превышает 2 мм. В основе фотодеструкции лежит эффект коагуляции опухолевых тканей.
Брахитерапия представляет собой способ локального разрушения опухоли с помощью строго дозированного, направленного излучения бета-частиц, испускаемых офтальмоаппликаторами (стронциевыми или рутениевыми), подшиваемыми к основанию опухоли на склеру. Она предназначена для внутриглазных опухолей, толщиной до 5 мм и диаметром не более 14 мм, задний край опухоли должен отстоять от диска зрительного нерва на 3 мм; при юкстапапиллярной локализации опухоль не должна окружать диск зрительного нерва более 120° его окружности [Офтальмоонкология. - под ред. Бровкиной А.Ф. - Москва. - Медицина. - 2001 - стр.130]. Как видно из показаний, а также по собственным и литературным данным, эффективность брахитерапии значительно превосходит эффективность фотодеструкции: она позволяет разрушить опухоли толщиной до 5 мм. Вместе с тем, способ не лишен недостатков. Так, брахитерапия - инвазивный метод, при котором офтальмоаппликатор подшивают под наркозом. Далее, как видим из приведенных показаний, метод имеет ограничение по локализации и по размерам опухоли. Наряду с этим, в ходе проведения самой процедуры подшивания радиоактивной пластинки могут возникнуть технические трудности, существенно снижающие эффективность лечения. Так, в случаях амеланотичных опухолей фиксировать аппликатор приходится практически "вслепую", то есть ориентируясь только на офтальмоскопические данные о положении опухоли, поскольку определить истинные границы опухоли на склере не представляется возможным. Беспигментная опухоль при трансиллюминации (способ определения границ опухоли на склере) не отбрасывает тень на склеру.
Далее, при подшивании возможно смещение пластинки или отстояние ее от склеры; несвоевременное распознавание этого фактора или недоучет его существенно снижают эффективность метода. Известно, что увеличение расстояния на какую-либо величину х между радиоактивной пластинкой и опухолью, ограничивают длину пробега бета частиц в собственно тканях опухоли точно на эту же величину х. Следовательно, в конечном итоге размеры регрессии опухоли значительно уменьшатся, по сравнению с планируемыми ожидаемыми показателями [Бровкина А.Ф. с соавт. "Об эффективности брахитерапии при увеальных меланомах." // Офтальмологический журнал. - 1993 - №1 - С.1-4].
Далее, выбор радиоактивных пластинок, используемых для этих целей весьма невелик: минимальные размеры диаметра офтальмоаппликатора составляют 17 мм, а максимальные - 22 мм [Офтальмоонкология. - под ред. Бровкиной А.Ф. - Москва. - Медицина. - 2001 - стр.125]. Порой мы сталкиваемся с проблемой неадекватного индивидуального подбора аппликатора к опухоли. Диаметр основания аппликатора намного перекрывает истинные размеры опухоли. Таким образом, большая часть здоровой, функционирующей сетчатки, расположенной вокруг опухоли, облучается напрасно, а следовательно, выбывает из акта зрения. Это сопровождается формированием большого дефекта в поле зрения, который сводит к нулю шансы пациента на удовлетворительные зрительные функции, а также существенно ухудшает его качество жизни.
Наряду с этим, при высоких лучевых дозах на склеру порой развивается склеромаляция, при которой дальнейшие попытки спасти глаз, как орган, становятся невозможны. Безальтернативной тактикой в этом случае становится энуклеация [Зарубей Г.Д. Радиотерапия опухолей глаза. - Диссертация на соискание ученой степени доктора медицинских наук. - Москва. - 1982 г.].
Термотерапия - один из новых способов органосохранного лечения внутриглазных опухолей, появившийся на рубеже XX-XXI столетия. Она основана на принципе локального лазерного воздействия на опухоль. Механизмом опухолевой деструкции является комбинированный эффект гипертермии опухолевой ткани (нагревание до 42°-65°) и объемной коагуляции опухолевых сосудов. Различают транспупиллярную и транссклеральную термотерапию [Denis Robertson, Helmut Buettner, Steven Bennet Traspupillary Thermotherapy as primary treatment for small choroidal melanomas. // Arch Ophthalmol - 1999 - vol.117 - nov. - pp.1512-1519].
Транпупиллярная термотерапия проводится под визуальным контролем путем лазерного воздействия через зрачковую диафрагму. Трансклеральная термотерапия проводится аналогично брахитерапии путем подведения лазерного излучения к основанию опухоли через склеру. Каждый метод имеет свои показания и противопоказания.
Транссклеральная термотерапия показана при опухолях, расположенных на средней и крайней периферии, которые недоступны или частично доступны для транспупиллярной термотерапии. Речь идет о том, что при транспупиллярной термотерапии продолжительное воздействие квазинепрерывным лазерным лучом с диаметром пятна излучения в фокальной плоскости >1 мм на поверхность опухоли, расположенной на крайней периферии глазного дна, через зрачок сопряжено с высоким риском развития лучевой катаракты (опухоли, расположенные в цилиохориоидальной зоне) и/или с риском развития иридоциклита, поскольку край радужки попадает в зону облучения [Oosterhuis JA, Joumee-de Korver JG. Transpupillary thermotherapy: results in 50 patients with chotoidal melanoma. // Arch Ophthalmol. - 1998 - vol.116 - pp.157-162].
Однако, несмотря на указанные недостатки, транспупиллярная термотерапия признана перспективным высокоэффективным методом. Она имеет явные преимущества перед брахитерапией и фотодеструкцией. Во-первых, она может быть проведена в амбулаторных условиях, поскольку не является инвазивным методом. Во-вторых, при этом способе устранены проблемы маркировки границ для точного подведения лучевого воздействия к опухоли. Транспупиллярная термотерапия проводится под визуальным контролем врача, проводящего процедуру термотерапии. Облучают исключительно саму опухоль и небольшой участок окружающих здоровых тканей, для предотвращения роста опухоли из-под рубца, поэтому соблюдается принцип избирательного, дозированного воздействия на патологический очаг. Этот принцип значительно повышает шансы пациента на сохранность зрительных функций.
Для термотерапии используются диодные лазеры, работающие в инфракрасном диапазоне волн: 810 нм. Эффект гипертермии и/или термотерапии достигается благодаря квазинепрерывному режиму лазерного воздействия при экспозиции в 1 минуту. Продолжительность воздействия основана на законах физики, согласно которым температура, в зоне воздействия инфракрасных лазеров достигает 65° при квазинепрерывном режиме и подобрана эмпирическим путем при разработке диодных лазеров разработчиками. Она заложена в технические характеристики приборов, предназначенных для термотерапии и является величиной постоянной - константой. Диаметр светового пятна и мощности подбираются индивидуально, согласно рекомендациям, представленным в литературе, разработанным на основании аккумуляции и анализа международного опыта. Адекватность проведения термотерапии в целом оценивается по цвету опухолевой ткани на момент завершения сеанса облучения. Контролем качества служит равномерно белый цвет поверхности опухоли [Journee-de Korver JG. Transpupillary thermotherapy: a new treatment of choroidal melanoma. The Haque. - The Netherlands: Kugier Publications; 1998 - P.125].
Классический способ транпупиллярной термотерапии, описанный выше, мы и взяли за ближайший аналог нашего изобретения.
Наш собственный опыт показал, что опухолевая ткань обретает белый цвет при воздействии лазерным излучением не только в зоне непосредственного облучения, но и на небольшом участке вокруг нее (перифокально) благодаря теплоотдаче. При этом температура (65°), необходимая для полной деструкции опухолевых клеток, достигается только в зоне прямого воздействия. В перифокальной зоне температура не поднимается выше 45°С, а при ней полного разрушения опухоли на всю ее толщину не происходит. Хотя поверхностные участки перифокальной ткани в зоне воздействия достигают аналогичного белого цвета, на который ориентируется врач при проведении термотерапии. Мы заметили, что на четвертые сутки после сеанса облучения опухолевые ткани, которые подверглись истинному воздействию, еще сохраняют белый цвет, а перифокальные, получившие свой "белый" цвет к концу сеанса термотерапии благодаря теплоотдаче, возвращаются к исходному серовато-аспидному цвету и восстанавливают исходную структуру с соответствующим этому сохранением жизнеспособности.
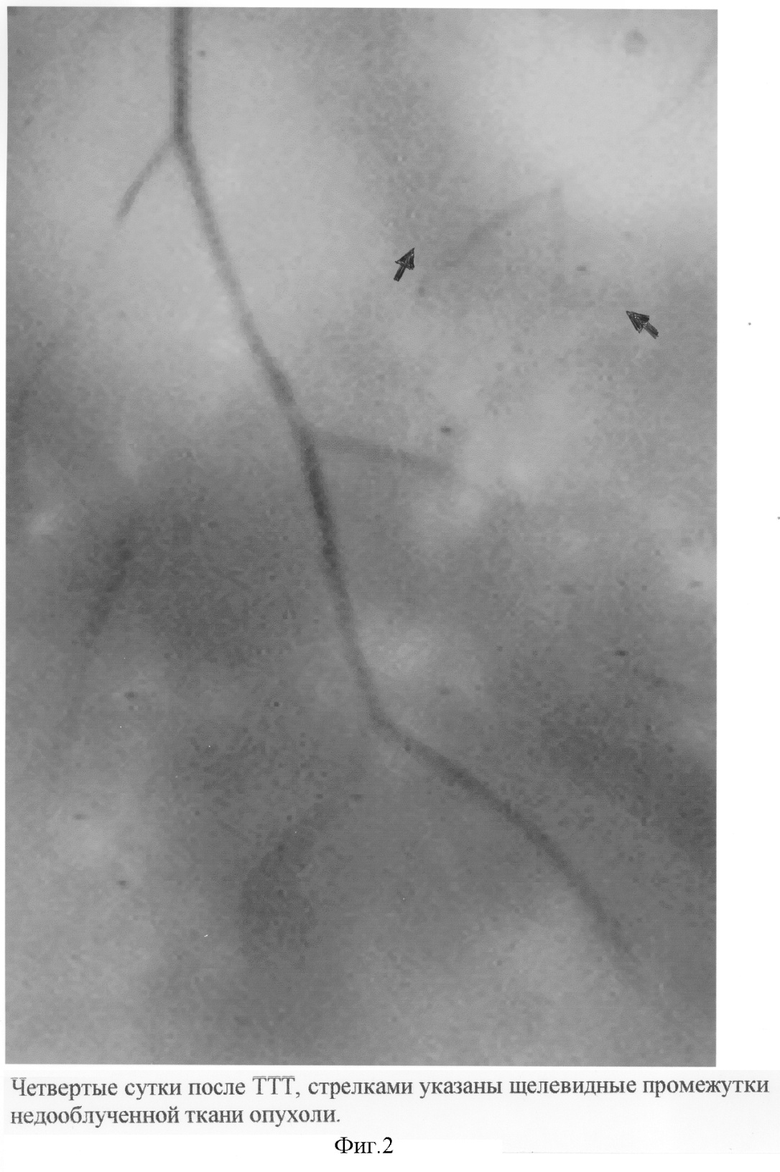
В связи с этим эти "недооблученные" участки опухоли могут стать причиной неполной регрессии или недостаточно быстрой регрессии или в ряде случаев источником рецидива опухолевого роста. Таким образом, истинный визуальный контроль качества проведения термотерапии становится возможным или, точнее, более информативным и достоверным только на 4-е сутки. Именно в эти сроки "недооблученные" ткани на фоне белых пятен облученной опухоли проявляются в виде сероватых щелевидных участков.
Мы предприняли попытку улучшить качество проведения самой термотерапии, а соответственно, и оптимизировать эффективность лечения. Мы предположили, что достичь цели можно путем нанесения дополнительных аппликаций лазерным лучом, сфокусированным прицельно в зону недооблученных тканей, которые как показали наши наблюдения, начинают визуализироваться в виде сероватых щелевидных участков к четвертым суткам. Эмпирически были подобраны оптимальные режимы для первого и второго этапов лечения.
Задачей предлагаемого изобретения является разработка адекватного способа термотерапии внутриглазных опухолей, позволяющего добиться полной деструкции опухоли.
Техническим результатом данного способа является полноценное разрушение опухоли, что и является основным критерием оценки эффективности транспупиллярной термотерапии как органосохранного способа лечения внутриглазных опухолей.
Технический результат достигается за счет двухэтапности воздействия с определенными режимами воздействия на каждом этапе.
Способ осуществляют следующим образом.
Первым этапом на лазере с длиной волны 810 нм, с экспозицией 60 секунд наносят аппликации в черепицеобразном порядке. При этом мощность излучения подбирают в начале сеанса, ориентируясь на факт побеления облученного участка опухоли по завершении 60-секундного лазерного воздействия от 200 до 1700 мВт. Если ткань опухоли белеет ранее 60 секунд, мощность лазерного воздействия уменьшают. Если эффект отсутствует по истечении 60-секунд, то мощность увеличивают.
Используют диаметры фокального пятна 1 мм, или 1,8 мм, или 3 мм, или 5 мм, в зависимости от размера опухоли, ее конфигурации и близости к центральным отделам сетчатки. При меланомах парапапиллярных, юкстапапиллярных и макулярных локализациях из-за опасности повреждения диска зрительного нерва используют меньший диаметр пятна. При обширных опухолях, расположенных на средней периферии глазного дна, для снижения общей продолжительности сеанса облучения используют большие диаметры пятна фокального изучения - 3 и 5 мм. Неправильная конфигурация опухоли предполагает использование аппликаций различного диаметра: 1,0 или 1,8 или 3,0 или 5,0 мм, для максимального сохранения здоровых тканей. По периферии опухоли используют меньший диаметр фокального пятна, в центре больший. Кроме того, при "ригидном" зрачке, когда достичь мидриаза не удается его диаметр уменьшают до 1,8 мм. Подбор осуществляют индивидуально, ориентируясь на указанные моменты.
Второй этап проводят через 4 суток, используя уменьшенный диаметр фокального пятна: 0,6 мм или 0,8 мм, при этом облучают только те участки опухолевой ткани, которые восстановили исходный цвет, существовавший до первого этапа воздействия.
По указанному способу проведено лечение 22 больных, из них 5 - с гемангиомами хориоидеи и 17 - с меланомами хориоидеи.
Пример №1. Больной М, 57 лет. Диагноз юкстапапиллярная меланома хориоидеи левого глаза. Размеры опухоли до лечения составили в высоту - 3,5 мм, диаметр основания - 11 мм.
Диагноз меланомы подтвержден данными флуоресцентной ангиографии и ультразвуковыми методами.
Проведена транспупиллярная термотерапия в квазинепрерывном режиме излучения на инфракрасном лазере с длиной волны 810 нм Iridex (США) с мощностью 950 мВт с диаметром светового пятна 1,8 мм в плоскости фокального воздействия, экспозиция каждой аппликации составляла 60 секунд. При подборе мощности ориентировались на факт приобретения опухолью белого цвета в месте облучения точно по истечении 60 секунд лазерного воздействия. По завершении сеанса визуально вся поверхность опухоли обрела равномерно белый цвет (фиг.1). Общее время облучения составило 17 минут. На четвертые сутки после облучения по мере нивелирования отека проявились щелевидные пространства недооблученной ткани (фиг.2). Отдаленные наблюдения показали, что, несмотря на, казалось бы, адекватный режим лучевого воздействия, ориентиром которого являлся белый цвет опухоли к концу сеанса термотерапии, полного эффекта в виде разрушения опухоли мы не достигли. Так, к четвертому месяцу высота опухоли оставалась на уровне 1,8 мм, а диаметр был 11,5 мм. Мы вынуждены были повторить термотерапию дважды на протяжении последующих шести месяцев в том же режиме. Причиной недостаточного эффекта мы считаем побочный эффект теплоотдачи, который стушевывает офтальмоскопическую картину и не позволяет адекватно провести лечение.
Пример №2. Пациентка М, 42 г. Диагноз: узловая гемангиома хориоидеи правого глаза. Левый глаз здоров.
Диагноз подтвержден с помощью ультразвуковых методов и флуоресцентной ангиографии. Исходные размеры опухоли составили: высота опухоли - 4,5 мм, диаметр основания - 15,5 мм.
На первом этапе лечения проведена термотерапия в режиме квазинепрерывного излучения на диодном лазере с длиной волны 810 нм Index (США) с мощностью 1140 мВт диаметром светового пятна 3,0 мм в плоскости фокального воздействия. Размер диаметра обусловлен большой площадью облучения поверхности опухоли и отдаленностью от макулы и диска зрительного нерва. Экспозиция в каждой точке воздействия составила 60 секунд. По завершении сеанса визуально достигли полного равномерного побеления всей поверхности опухоли. Общее время облучения составило 18 минут. На четвертые сутки по мере уменьшения отека в поверхности опухоли проявились щелевидные пространства недооблученной ткани. Проведен второй этап. При этом облучали только недооблученные ткани, используя тот же режим облучения, но с меньшим диаметром светового пятна в зоне воздействия - 0,6 мм. По мере выравнивания цвета опухоли на ее поверхности сеанс завершили. Динамическое наблюдение показало, что в течение 4 месяцев произошла полная регрессия опухоли с формированием плоского хориоретинального рубца.
Таким образом, полученный клинический опыт свидетельствует о том, что проведение на четвертые сутки дополнительного сеанса термотерапии, в ходе которого облучают участки ткани опухоли, которые восстановили исходный цвет, существовавший до первого этапа воздействия, существенно повышает эффективность способа.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОРГАНОСОХРАНЯЮЩЕГО ЛЕЧЕНИЯ ВНУТРИГЛАЗНЫХ ОПУХОЛЕЙ | 2010 |
|
RU2452444C1 |
| Способ комбинированного одноэтапного лазерного лечения беспигментной меланомы хориоидеи малых размеров юкстапипиллярной локализации | 2023 |
|
RU2805827C1 |
| СПОСОБ ЛЕЧЕНИЯ МЕЛАНОМЫ ХОРИОИДЕИ | 2006 |
|
RU2359648C2 |
| СПОСОБ ЛЕЧЕНИЯ ВНУТРИГЛАЗНЫХ ОПУХОЛЕЙ | 2005 |
|
RU2295944C1 |
| СПОСОБ ЛЕЧЕНИЯ ВНУТРИГЛАЗНЫХ ОПУХОЛЕЙ | 2005 |
|
RU2294780C1 |
| СПОСОБ ЛЕЧЕНИЯ ВНУТРИГЛАЗНЫХ ОПУХОЛЕЙ | 2005 |
|
RU2290905C1 |
| СПОСОБ ОРГАНОСОХРАННОГО ЛЕЧЕНИЯ МЕЛАНОМЫ ХОРИОДЕИ НЕБОЛЬШОЙ ЭЛЕВАЦИИ | 2006 |
|
RU2329020C1 |
| СПОСОБ ЛЕЧЕНИЯ ВНУТРИГЛАЗНЫХ НОВООБРАЗОВАНИЙ БОЛЬШОГО РАЗМЕРА | 2005 |
|
RU2303965C2 |
| ЭЛЕКТРОДЫ ДЛЯ ЭЛЕКТРОХИМИЧЕСКОЙ ДЕСТРУКЦИИ ВНУТРИГЛАЗНЫХ НОВООБРАЗОВАНИЙ И СПОСОБ ИХ ВВЕДЕНИЯ | 2008 |
|
RU2375020C1 |
| СПОСОБ КОМБИНИРОВАННОЙ ОБРАБОТКИ СКЛЕРАЛЬНОГО ЛОЖА ПОСЛЕ ЭНДОРЕЗЕКЦИИ ВНУТРИГЛАЗНОГО НОВООБРАЗОВАНИЯ | 2013 |
|
RU2532879C1 |
Изобретение относится к медицине, а именно к офтальмоонкологии. Транспупиллярно воздействуют лазерным излучением с длиной волны 810 нм, экспозицией 60 секунд в каждой точке воздействия с нанесением аппликаций в виде черепицы до полного равномерного побеления опухоли. Воздействие осуществляют с мощностью 200-1700 мВт в два этапа. На первом этапе, в зависимости от размера опухоли, ее конфигурации и близости к сенсорным отделам сетчатки используют диаметр фокального пятна размером 1,0 или 1,8 или 3,0 или 5,0 мм. На втором этапе через 4 суток используют диаметр фокального пятна размером 0,6 или 0,8 мм. При этом облучают только те участки ткани опухоли, которые восстановили исходный цвет, существовавший до первого этапа воздействия. Способ позволяет полноценно разрушить опухоль, что существенно повышает эффективность способа. 2 ил.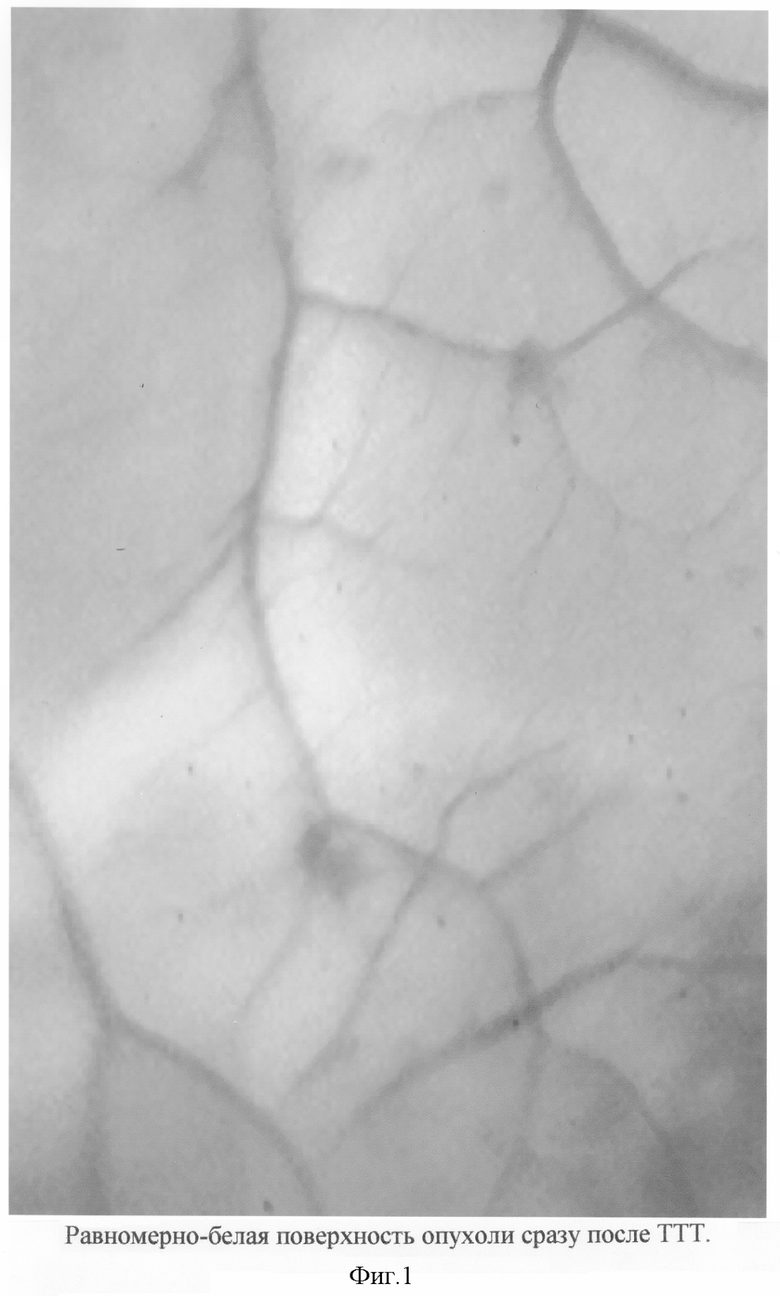
Способ транспупиллярной термотерапии внутриглазных опухолей, включающий локальное воздействие лазерным излучением с длиной волны 810 нм, экспозицией 60 с в каждой точке воздействия с нанесением аппликаций в виде черепицы до полного равномерного побеления опухоли, отличающийся тем, что воздействие осуществляют с мощностью 200-1700 мВт в два этапа: на первом этапе в зависимости от размера опухоли, ее конфигурации и близости к сенсорным отделам сетчатки используют диаметр фокального пятна размером 1,0, или 1,8, или 3,0, или 5,0 мм, а на втором этапе через 4 сут используют диаметр фокального пятна размером 0,6 или 0,8 мм, при этом облучают только те участки ткани опухоли, которые восстановили исходный цвет, существовавший до первого этапа воздействия.
| SHIELDS C.L | |||
| et al | |||
| Облицовка комнатных печей | 1918 |
|
SU100A1 |
| Ophthalmology | |||
| Способ и аппарат для получения гидразобензола или его гомологов | 1922 |
|
SU1998A1 |
| ГУСЕВ Г.А | |||
| Особенности методики лазерной коагуляции меланомы хориоидеи с использованием диодного лазера | |||
| VII Съезд офтальмологов России | |||
| Тезисы докладов | |||
| - М., 2000, ч.2, с.108. | |||
Авторы
Даты
2006-10-10—Публикация
2005-01-26—Подача