Область применения настоящего изобретения
Настоящее изобретение касается использования псевдомицинов в качестве эффективных фунгицидов при заболеваниях растений и сельскохозяйственных культур; более конкретно оно касается использования фунгицидов против определенных классов грибков, вызывающих заболевания растений и сельскохозяйственных культур.
Предпосылки настоящего изобретения
Псевдомицины - класс новых противогрибковых средств, которые демонстрируют хорошую перспективу лечения грибковых инфекций у различных пациентов (см., например, Harrison L. et al. "Pseudomycins, a family of novel peptides from Pseudomonas syringae possessing broad-spectrum antifungal activity", J.Gen. Microbiology, 137 (12), 2857-65 (1991), а также патенты США №5,576,298 и №5,837,685). Псевдомицины представляют собой природные продукты, полученные из изолятов Pseudomonas syringae. P. syrlngae - это большая группа сопутствующих растениям бактерий, которые являются источником нескольких биологически активных веществ, типа бакитрацина и сирингомицинов. Природные штаммы, а также полученные с помощью транспозона мутанты Р. syringae продуцируют соединения, обладающие противогрибковой активностью. Генерированный транспозоном регуляторый мутант обширного класса Р. syringae MSU 174, известный как MSU 16H (АТСС 67028), продуцирует несколько псевдомицинов. Были выделены и химически проидентифицированы псевдомицины А, В, С и С' и было показано, что они обладают широким спектром противогрибковой активности, включая активность в отношении важных патогенных грибков как человека, так и растений. Структурно эти псевдомицины относятся к сирингомицинам, но отличаются от них и других противогрибковых средств, выделенных из Р. syringae. Пептидный фрагмент псевдомицинов А, В, С и С' соответствует L-Ser-D-Dab-L-Asp-L-Lys-L-Dab-L-aThr-Z-Dhb-L-Asp(3-OH)-L-Thr-(4-Cl) с концевой карбоксильной группой, замыкающей ОН-группой N-концевой макроцикл серина (Ser). Аналоги различаются N-ацилированной боковой цепью, а именно псевдомицин А N-ацилирован 3,4-дигидрокситетрадеканоатом, псевдомицин В - 3-гидрокситетрадеканоатом, псевдомицин С - 3,4-дигидроксинексадексадеканоатом, а псевдомицин С' - 3-гидроксигексадеканоатом (см., например, Ballio A. et al. "Novel bioactive lipodepsipeptides from Pseudomonas syringae: the pseudomycins, FEBS Letters, 355 (1), 96-100 (1994), а также Coiro V.M. et al. "Solution conformation of the Pseudomonas syringae MSU 16H phytotoxic lipodepsipeptides Pseudomycin A determined by computer simulation using distance geometry and molecular dynamics from NMR data", Eur. J. Biochem., 257 (2), 449-456 (1998).
Настоящее изобретение обеспечивает группу псевдомицинов, которые, в частности, особенно пригодны для защиты растений и животных от грибковых заболеваний.
Краткое содержание настоящего изобретения
Предметом настоящего изобретения является обеспечение способа лечения заболеваний растений и сельскохозяйственных культур или защиты от них.
Другим предметом настоящего изобретения является обеспечение способа лечения или защиты растений и сельскохозяйственных культур путем применения определенных пседомицинов.
Еще одним предметом настоящего изобретения является применение определенных псевдомицинов для защиты растений и сельскохозяйственных культур от заболеваний, вызванных грибками, или лечения этих заболеваний.
Другие предметы и преимущества настоящего изобретения станут очевидными из дальнейшего описания.
Удовлетворяя вышеупомянутым предметам и преимуществам, настоящее изобретение обеспечивает способ защиты растений и сельскохозяйственных культур от заболеваний, имеющих отношение к грибкам, или лечения этих заболеваний; этот способ включает нанесение на указанные растения или сельскохозяйственные культуры эффективного количества одного или более псевдомицинового продукта.
Описание предпочтительных вариантов настоящего изобретения.
Описание настоящего изобретения касается обнаружения нового, неожиданного применения класса липопептидов, известных как псевдомицины, в качестве фунгицидов или противогрибковых средств. В одном предпочтительном варианте настоящего изобретения псевдомицины, каждый в отдельности и в виде группы, особенно полезны для лечения или защиты растений, прошедших проверку иммунности к группе грибков Ascomyceteous, относящихся к Mycosphaerella asp. (совершенная или половая фаза развития этих грибков), а также практически на все известные несовершенные (бесполые) фазы этих грибков, включая Septoria sp. и Cercospora sp. Помимо этого, псевдомицины уничтожают ряд других важных для растений патогенных грибков, включая Tapesia yallundae, Ustilago maydis, Penicillium roqueforti, Monilinia sp., а также Geotrichum candldum. Таким образом, псевдомицины сами по себе используются при обработке растений для их защиты от вреда, причиняемого указанными грибками.
Диапазон заболеваний, вызываемых этими организмами, охватывает от заболеваний растений, находящихся на хранении, до очень значительных заболеваний плантаций типа черной сигатоки (Black Sigatoka) бананов и пятнистости пшеницы.
Настоящее изобретение касается ранее не предполагаемого ряда очень важных для растений патогенных грибков, считавшихся биологически родственными, они чувствительны к одному или более псевдомицинам и подавляются и уничтожаются ими. Эти грибки, а также некоторые остальные, не выявленные прежде, являются причиной одних из самых серьезных на планете заболеваний растений. В настоящее время с грибками, вызывающими эти заболевания, борются с помощью простых или сложных искусственных фунгицидов, которые наносят вред окружающей среде, и могут также создать неожиданную опасность здоровью человека. С другой стороны, псевдомицины представляют собой безопасную и эффективную альтернативу применения искусственных химикатов для борьбы с определенными заболеваниями растений. Помимо этого, использование псевдомицинов для борьбы с заболеваниями растений имеет определенные преимущества, поскольку применение для этой цели природных продуктов даст возможность производителю заявить о том, что урожай выращен в биологически/экологически чистых условиях, и это позволит получить от продукта больший доход. Следует заметить, что в мире в настоящее время в целях борьбы с заболеваниями растений ни для одной из важных сельскохозяйственных культур не использовался ни один из природных фунгицидов. Псевдомицины предлагают значительную выгоду как производителям сельскохозяйственной продукции, так и ее потребителям.
Примером того, как и по какой причине псевдомицины могут быть полезными для сельского хозяйства, является то, что минимальные ингибирующие концентрации некоторых псевдомицинов (например, пседомицинов А, В, В', С и С') находятся в диапазоне от 1 мг/мл или ниже. Такая концентрация особенно желательна для эффективного применения в сельском хозяйстве. При тестировании в отношении М. fijiensis, изолят 8088/88, эти соединения дают еще больший эффект (менее 1,0 мг). М. fijiensis является тем организмом, который вызывает заболевание бананов и подорожника черной сигатокой (Black Sigatoka). В настоящее время производители этих культур во всем мире для того, чтобы получить урожай бананов, должны распылять смесь трех фунгицидов (искусственных) с частотой 30 раз в год. В мире только при одном этом заболевании требуется самый большой расход фунгицида на каждую сельскохозяйственную культуру. Недостатками применения этих трех синтетических фунгицидов являются следующие: 1. их очень высокая стоимость (миллионы долларов); 2. неспособность производителя продать выращенный продукт как экологически чистый, т.к. при этом применялись фунгициды; 3. опасность причинения риска здоровью человека, а также окружающей среде при постоянном применении фунгицидов на протяжении десятилетий. Почва под бананами на плантациях становится непригодной для жизни живых организмов и оказывается построенной из остатков фунгицидов. С другой стороны, выявилось, что продуцированные естественным способом псевдомицины более эффективны в борьбе против заболевания сигатокой, причем одновременно извлекается выгода для окружающей среды и здоровья человека.
Помимо этого, псевдомицины эффективны в отношении ряда других заболеваний растений, вызываемых грибками, включая грибки, разрушающие растения при их хранении, например Penicillium sp., Monilinia sp. и Geotrichum sp. Смесь псевдомицинов, нанесенная на собранный урожай фруктов, должна предотвратить грибковые инфекции и гниение в процессе хранения.
Другие возможности применения псевдомицинов включают их нанесение для борьбы с заболеваниями, вызванными на пшенице Seproria sp., в частности S. nodurum и S. tritici; но они также основаны на биологической активности этих молекул - фактически любого представителя вида Seproria sp., вызывающего любое заболевание растений в мире. Аналогичным образом воздействуют другие грибки, относящиеся к Mycosphaeella sp., в их число входит Cercospora sp., вызывающий заболевания растений, в частности пятнистость листьев сахарной свеклы и многих других сельскохозяйственных культур. Другие заболевания растений, вызываемые организмами, включая Dreschslera portulaceae, также подвергаются воздействию псевдомицинов.
В соответствии с настоящим изобретением было обнаружено, что описываемые в этом документе пседомицины обладают очень сильной противогрибковой активностью в отношении группы патогенных грибков, непосредственно родственных грибкам растений, хотя ранее этого не ожидалось. Эту основную группу представляют половая фаза развития грибков Mycosphaeella sp., а также каждый из ее представителей в бесполой фазе своего развития (типа Septoria sp. и Cercospora sp). Обычно псевдомицины можно использовать в чистом виде или в виде смеси в составе рецептуры для защиты растений от грибковых инфекций. В качестве потенциального использования этих соединений рассматривается применение для сельскохозяйственных культур на поле, а также для культур, находящихся на хранении.
Таким образом, целью настоящего изобретения является продемонстрировать, что некоторые особенно важные для растений патогенные грибки чувствительны к воздействию одного или более псевдомицинов, первоначально выделенных из растений, связанных с бактериями Pseudomonas syringae.
Псевдомицинами, пригодными в способе по настоящему изобретению, предпочтительно являются псевдомицины, идентифицированные как псевдомицин А, псевдомицин А', псевдомицин В, псевдомицин B', псевдомицин С и псевдомицин С', а также их производные, такие как фосфатное производное псевдомицин А-PO4 и псевдомицин A-FB (они оба известны).
Эти псевдомицины применяют в отношении разнообразных растений и сельскохозяйственных культур, чувствительных к паразитическим заболеваниям, вызываемым грибками. В этой связи псевдомициновые составы по настоящему изобретению в первую очередь пригодны для предотвращения начала паразитических заболеваний, вызванных грибками, поэтому обработку растений и сельскохозяйственных культур предпочтительно проводить до начала указанных заболеваний. Однако псевдомициновые составы пригодны также для лечения инфицированных растений.
Псевдомициновые составы по настоящему изобретению эффективны при очень низких концентрациях, составляющих от приблизительно 1 до 100 мкг псевдомицина на 1 мл водного раствора. Поэтому предпочтительным способом нанесения псевдомицинового состава по настоящему изобретению является его распыление непосредственно над растениями или сельскохозяйственными культурами, нуждающимися в лечении, при этом используются указанные выше концентрации. Псевдомициновые составы по настоящему изобретению могут представлять собой составы в виде растворов, суспензий или эмульсий или в любой другой форме, пригодной для распыления над растениями или сельскохозяйственными культурами.
Предпочтительные псевдомицины, используемые в настоящем изобретении, а также способы их получения известны или они полностью раскрываются и описываются в совместно сделанных заявках на патенты PCT/US 00/08728 от 14 апреля 2000 года и PCT/US 00/08727 от 14 апреля 2000 года, обе заявки поданы США. Раскрытие обоих этих заявок включено здесь в виде ссылок во всей их полноте.
Термином «псевдомицины» согласно использованию в настоящем документе называют соединения, имеющие следующую формулу I:
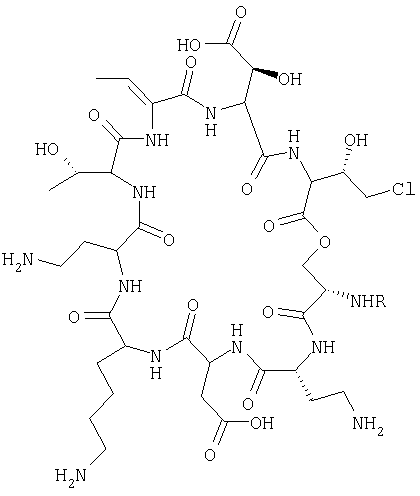
в которой R представляет собой липофильный фрагмент. Соединения псевдомицинов А, А', В, В', С и С' представлены приведенной выше формулой I, в которой R имеет следующие значения:
для псевдомицина A R=3,4-дигидрокситетрадеканоил
для псевдомицина A' R=3,4-дигидроксипентадеканоат
для псевдомицина В R=3-гидрокситетрадеканоил
для псевдомицина В' R=3-гидроксидодеканоат
для псевдомицина С R=3,4-дигидроксигексадеканоил
для псевдомицина С' R=3-гидроксигексадеканоил
Согласно использованию в настоящем документе псевдомицинами называют один или более членов группы противогрибковых средств, выделенных из бактерий Pseudomonas syringae. Псевдомицин представляет собой липодепсипептид, циклический пептид, содержащий одну или более редкую (нестандартную) аминокислоту с присоединенными одной или более гидрофобными боковыми цепями или жирными кислотами в боковых цепях. В частности, псевдомицины представляют собой липодепсинонапептиды, циклическая пептидная часть которых замкнута лактоновой связью и содержащие редкие (нестандартные) аминокислоты: 4-хлортреонин, 3-гидроксиаспарагиновую кислоту, дегидро-2-аминомасляную кислоту, а также 2,4-диаминомасляную кислоту. Предполагается, что эти редкие (нестандартные) аминокислоты определяют биологические характеристики указанных псевдомицинов, такие как стабильность в сыворотке и смертоносное воздействие. Указанные псевдомицины включают псевдомицин А, псевдомицин А', псевдомицин В, псевдомицин В', псевдомицин С и псевдомицин С'. Каждый из этих псевдомицинов имеет одно и то же циклическое пептидное ядро, а различаются они гидрофобными боковыми цепями, присоединенными к этому ядру.
Псевдомицины А, А', В, В', С, и С' были выделены и очищены и их структуры определялись способами, включающими секвенирование аминокислот, ЯМР и масс-спектрометрию. Псевдомицины А, А', В, В', С и С' раскрыты в патенте США №5,576,298 от 19 ноября 1996, принадлежащем G.Strobel et al.; Harrison et al. "Pseudomicins, a family of novel peptides from Pseudomonas syringae possessing broad-spectrum antifungal activity", J.Gen.Microbiology, 137, 2857-2865 (1991); а также Ballio A. et al. "Novel bioactive lipodepsipeptides from Pseudomonas syringae: the pseudomycins, FEBS Letters, 355 (1), 96-100, (1994). Псевдомицины А' и В' описаны в заявке на патент США PCT/US 00/08727, принадлежащем Palaniappan Kulanthaivel et al. и озаглавленном "Pseudomicins Natural Products" и предложенном тогда же на рассмотрение, описаны в примерах и включены в настоящий документ во всей своей полноте. Противогрибковая активность за счет нескольких псевдомицинов была зафиксирована у Р. syringae, несущего транспозон, известный как Tn 903; последний кодирует факторы, включающие стойкость к канамицину. Последовательность и способы манипулирования транспозоном Tn 903 известны (Oka et al. "Nucleotide sequence of the kanamycin resistance transposon Tn 903", J.Mol.Biol, 147, 217-226 (1981). Каждая из ссылок, указанных в этом параграфе, включена в перечень ссылок.
Псевдомицины отличаются по своей структуре и свойствам. Предпочтительные псевдомицины А, А', В, В', С и С' демонстрируют активность в отношении разнообразных грибков и они обладают вполне приемлемой токсичностью. По сравнению с другими предпочтительными псевдомицинами псевдомицин В обладает более высокой результативностью в отношении определенных грибков и более низким уровнем токсичности. Следовательно, для современных способов более предпочтителен псевдомицин В. Каждый псевдомицин обладает нонапептидным циклом, содержащим последовательность Ser-Dab-Asp-Lys-Dab-aThr-Dhb-HOAsp-ClThr (серин; 2,4-диаминомасляная кислота; аспарагиновая кислота; лизин; 2,4-диаминомасляная кислота; аллотреонин; дегидро-2-аминомасляная кислота; 3-гидроксиаспарагиновая кислота; 4-хлоротреонин), в частности L-Ser-D-Dab-L-Asp-L-Lys-L-Dab-L-aThr-Z-Dhb-L-Asp(3-OH)-L-Thr-(4-Cl), причем карбоксильная группа ClThr и карбоксильная группа серина замыкают этот цикл лактоновой связью. Псевдомицины различаются природой липофильного фрагмента, прикрепленного к аминной группе N-концевого серина. Эта аминная группа серина образует аминную связь с карбоксилом 3,4-дигидрокситетрадеканоилового фрагмента (в псевдомицине А), 3,4-дигидроксигексадеканоилового фрагмента (в псевдомицине С) и 3-моногидроксигексадеканоилового фрагмента (в псевдомицине С'). Карбоксильная группа серина образует аминную связь с 2,4-диаминомасляной кислотой цикла.
Псевдомицины, применяемые в настоящем изобретении, можно использовать в виде их приемлемых солей. Используемый здесь термин «приемлемые соли» относится к солям описанных выше соединений, являющимся в существенной степени нетоксичными в отношении живых организмов. Типичные приемлемые соли включают соли, полученные взаимодействием соединений по настоящему изобретению с минеральной или органической кислотой или с неорганическим основанием. Такие соли известны как аддитивные кислые или основные соли.
Кислотами, обычно используемыми для образования кислых аддитивных солей, являются минеральные кислоты (типа соляной кислоты, бромистоводородной кислоты, иодистоводородной кислоты, серной кислоты и фосфорной кислоты), а также органических кислот (типа п-толуолсульфоновой кислоты, метансульфоновой кислоты, щавелевой кислоты, п-бромфенилсульфоновой кислоты, угольной кислоты, янтарной кислоты, лимонной кислоты, бензойной кислоты и уксусной кислоты). Примерами таких фармацевтически приемлемых солей являются сульфаты, пиросульфаты, бисульфаты, сульфиты, бисульфиты, фосфаты, моногидрофосфаты, дигидрофосфаты, метафосфаты, пирофосфаты, хлориды, бромиды, иодиды, ацетаты, пропионаты, деканоаты, каприлаты, акрилаты, формиаты, изобутираты, капроаты, гептаноаты, пропиолаты, оксалаты, малонаты, сукцинаты, субераты, себакаты, фумараты, малеаты, бутин-1,4-диоаты, гексин-1,4-диоаты, бензоаты, хлорбензоаты, метилбензоаты, динитробензоаты, гидроксибензоаты, метоксибензоаты, фталаты, сульфонаты, ксилолсульфонаты, фенилацетаты, фенилпропионаты, фенилбутираты, цитраты, лактаты, γ-гидпоксибутираты, гликоллаты, тартраты, метансульфонаты, пропансульфонаты, нафталин-1-сульфонаты и манделаты. Предпочтительными фармацевтически приемлемыми кислыми аддитивными солями являются соли, образованные такими минеральными кислотами, как соляная кислота и бромистоводородная кислота, а также такими органическими кислотами, как малеиновая кислота и метансульфоновая кислота.
Основные аддитивные соли включают соли, являющиеся производными неорганических оснований, таких как гидроксиды, карбонаты и бикарбонаты алюминия или щелочных или щелочноземельных металлов. Таким образом, основания, пригодные для получения солей по настоящему изобретению, включают гидроксид натрия, гидроксид калия, гидроксид аммония, карбонат калия, карбонат натрия, бикарбонат натрия, бикарбонат калия, гидроксид кальция и карбонат кальция. Особенно предпочтительны натриевые и калиевые соли.
Следует понимать, что конкретный противоион, образующий часть любой соли по настоящему изобретению, не является существенным при условии, если эта соль в целом является фармакологически приемлемой, и при условии, что этот противоион не придает соли в целом нежелательных свойств.
Настоящее изобретение можно лучше понять с помощью приведенных далее примеров. Эти примеры предназначены представить специфические варианты настоящего изобретения и не имеют целью ограничить сущность настоящего изобретения.
Депонированные биологические материалы
P. syringae MSU 16H доступен для определенного круга лиц из Американской Коллекции Культур (American Type Culture Collection, Parklawn Drive, Rockville, MD, USA) под инвентарным номером АТСС 67028. Штаммы P. syringae 25-B1, 7H9-1 и 67Н1 были депонированы Американской Коллекцией Культур 23 марта 2000 г. и им были присвоены следующие инвентарные номера:
25-В1 Инвентарный номер РТА-1622
7H9-1 Инвентарный номер РТА-1623
67Н1 Инвентарный номер РТА-1621
Псевдомицины были выделены из жидких культур Pseudomonas syringae. Pseudomonas syringae является бактерией, связанной с растениями, которая продуцирует множество фитотоксинов и других сложных пептидов1-3. В конце 80-х годов 20 века было показано, что Р. syringae продуцирует противогрибковые средства. Общая идея состояла в том, что эндосимбионты, выросшие на растении, продуцируют противогрибковые средства для защиты указанного растения от грибковых заболеваний. Псевдомицины идентифицировались как биологически активные противогрибковые средства. Было показано, что генерирующий транспозон мутант дикого типа Р. syringae является гиперпродуцентом этих природных продуктов. Мутантные штаммы транспозона4, разработанные В Университете штата Монтана, с успехом использовались для инокуляции вязов в целях борьбы с болезнью голландских вязов5-6. Кроме того, эти природные продукты продемонстрировали селективную противогрибковую активность в борьбе с заболеваниями, обнаруженными на полевых культурах, фруктах и других растениях (таблица 1-3). Например, псевдомицины демонстрируют многообещающую активность в отношении М. fijensis, которая вызывает черную сигатоку бананов, что требует большего количества фунгицидов и аппликаций фунгицидами, чем другие заболевания растений в современном мире. Псевдомицины, как было показано, предотвращают преждевременное гниение манго.
ПРИМЕР 1
Широкомасштабное воспроизводимое продуцирование (кг) этих природных продуктов было с успехом продемонстрировано. Были приготовлены очищенные образцы свободной основной и альтернативной форм солей. Для оценки противогрибковых свойств псевдомицинов А, В, В', С и С' использовалось приблизительно 34 грибка, патогенных для растений. Ингибиторную концентрацию измеряли дважды, на 2 и на 5 день.
Противогрибковая активность, испытанная с помощью представляющих интерес патогенов:
Материалы и способы
Грибки, приготовленные для испытаний, размножали при комнатной температуре на чашке Петри с картофельно-декстрозным агаром (КДА). Объединенные растворы псевдомицинов и депсипептида суспендировали в диметилсульфоксиде (Sigma) при концентрации 5 мг/мл и сохраняли при -20°С. В день эксперимента проводились серийные разбавления соединений. Все серийные разбавления осуществляли в диметилсульфоксиде. Замечание: первичный эксперимент с псевдомицинами В и В' в метаноле проводилсь на некоторых грибках и было продемонстрировано, что в присутствии метанола рост нескольких грибков подавляется. Это отмечено в разделе предварительных данных.
Анализ проводили в коллекторах клеточной культуры на 24 ячейки (Costar 3524), при этом каждая ячейка содержала 990 мкл картофельно-декстрозного бульона (PDB, Difco) и 10 мкл испытуемого соединения. Исходные анализируемые концентрации составляли 50-1,56 мкг/мл (конечная концентрация псевдомицина). Фактические концентрации испытуемых псевдомицинов составляли 50; 25; 12,5; 6,25; 3,12 и 1,56 мкг/мл. Каждую ячейку инокулировали соответствующим грибком. Если особо это не оговорено, то грибковый инокулят содержал приблизительно 4 мм2 фрагмент картофельно-декстрозного агара (КДА) с грибковым мицелием. Ниже приведены исключения. Ustilago maydis: эти грибки размножались на картофельно-декстрозном агаре, во многом как дрожжи, их клетки счищали с чашки Петри с КДА, повторно суспендировали в картофельно-декстрозном бульоне и в каждую ячейку добавили 10 мкл инокулята. Monilinia sp.: этот грибковый мицелий разрастался на верхней части картофельно-декстрозного агара в виде очень рыхлой пленки и не прилипал к блокам агара. Грибковый мицелий измельчали в 500 мкл картофельно-декстрозного бульона с помощью металлического прутка и в каждую ячейку добавили 10 мкл инокулята. Mycosphaeella fijiensis, Septoria passerinil, Septoria triticik: все эти грибки росли очень медленно и, если в качестве инокулята использовали небольшой фрагмент агара с помещенным на нем мицелием грибка, то результаты было очень трудно зафиксировать. Мицелий этих грибков измельчали в 500 мкл картофельно-декстрозного бульона с помощью металлического прутка и в каждую ячейку добавили 10 мкл инокулята.
Рост грибков в ячейках отмечали за 2 дня и за 5 дней. У некоторых очень медленно размножающихся грибков замеры делали в более поздние сроки, поскольку не было возможности за 2 или за 5 дней сделать оценку. Рост грибков измерялся в сравнении с контрольным образцом, который включал грибки, инокулированные в 990 мкл картофельно-декстрозного бульона, а также 10 мкл диметилсульфоксида. Дополнительный контроль, включающий только грибковый инокулят в картофельно-декстрозном бульоне, осуществлялся для того, чтобы гарантировать, что диметилсульфоксид не обладает ингибиторным действием на размножение грибков. Диметилсульфоксид не оказывал воздействия ни на один из испытуемых грибков за исключением Drechslera portulacae, где было отмечено некоторое ингибирование.
Все грибки, подавление размножения которых было отмечено, протестировали повторно. Для повторных анализов из второй партии псевдомицинов приготовили новые объединенные растворы. Заметим, что объединенные растворы псевдомицина В' и депсипептида были заново приготовлены из первой партии материалов, потому что вторая партия их не содержала. У некоторых грибков не наблюдалось никакого роста даже при самых низких концентрациях добавленных псевдомицинов и их снова, в третий раз, протестировали, используя более низкие концентрации псевдомицинов (конечная концентрация псевдомицина 2-0,0625 мкг/мл. Фактические концентрации псевдомицинов составляли 2,1; 0,5; 0,25; 0,125 и 0,0625 мкг/мл. А-PO4 и А-FB представляют собой соответственно фосфатную соль псевдомицина А и его свободное основание.
Результаты, полученные за 2 дня, - приведенная концентрация является самой низкой концентрацией соединения (мкг/мл), которая не приводит ни к какому размножению. «NI» - отсутствие ингибирования; «р» - частичное, по крайней мере 50% ингибирование; знак «-» означает «не определено». Если количество сделанных на грибках анализов было больше 1, то это количество указано в круглых скобках. Для некоторых медленноразмножающихся грибков отмечены дни, прошедшие до наблюдения (если их количество не равно 2).
Результаты, полученные за 5 дней, - приведенная концентрация является самой низкой концентрацией соединения (мкг /мл), которая не приводит ни к какому размножению. «NI» отсутствие ингибирования; «р» - частичное, по крайней мере 50% ингибирование; знак «-» означает «не определено» (медленное размножение). Если количество сделанных на грибках анализов было больше 1, то это количество указано в круглых скобках. Для некоторых медленно размножающихся грибков отмечены дни, прошедшие до наблюдения (если их количество не равно 5).
Обзор приведенных выше экспериментов показал, что испытанные грибки сильнее, чем все остальные соединения ингибировал один или несколько псевдомицинов. Шесть грибков не продемонстрировали размножения даже при самой низкой концентрации первоначально испытанных псевдомицинов, составляющей 1,56 мкг/мл. Например, оказалось, что Drecshslera portulacae не размножались даже при концентрации псевдомицина А (PO4), В и С, составляющей 0,0625 мкг/мл (9 дней). Два разных изолята Mycospaella fijiensis по-разному реагировали на более низкие дозы псевдомицинов. Оказалось, что каждый псевдомицин (в концентрации до приблизительно 1 мкг/мл) подавлял рост изолята сигатока. Однако изолят 8088/88 сильнее всего подавлялся псевдомицином В, при этом в случае концентрации 0,125 мкг/мл не было никакого роста в течение 21 дня. Septoria tritici и Septoria passerinii сильно ингибировались всеми псевдомицинами, причем S. tritici не продемонстрировали никакого размножения за 5 дней при концентрации псевдомицина В, составляющей 0,0625 мкг/мл, a S. passerinii не продемонстрировали никакого размножения за 5 дней при концентрации 0,0625 мкг/мл псевдомицина А (свободное основание). В, С и С'. Ustilago maydis сильнее всего ингибировался или псевдомицином С, или псевдомицином С', причем при концентрации 0,25 мкг/мл не было никакого размножения в течение 5 дней. Некоторые грибки (например, Alternaria helianti, Aphanomyces sp., Botrytis alii, Sclerotinia sclerotiorum, Tapesia acuformis, Tapesia yallundae, а также Verticillium dahliae) продемонстрировали лишь незначительное подавление роста даже при самых высоких концентрациях испытываемых псевдомицинов. Некоторые грибки показали сильное ингибирование одним или более псевдомицинами, однако не всеми. К таким грибкам относятся Rhizoctonia solani, который сильнее всего ингибировался псевдомицином В' (при концентрации 6,25 мкг/мл размножение отсутствует в течение 5 дней), Monilinia sp. сильнее всего ингибировался псевдомицинами В и С' (при концентрации 6,25 мкг/мл размножение отсутствует в течение 5 дней), Geotrichim candidum сильнее всего ингибировался псевдомицином В (при концентрации 3,12 мкг/мл размножение отсутствует в течение 5 дней), а Penicillium roqueforti сильнее всего ингибировался псевдомицином В' (при концентрации 1, 56 мкг/мл размножение отсутствует в течение 5 дней).
Из этих данных можно сделать вывод, что псевдомицины представляют собой группу природных селективных фунгицидов. Некоторые грибки, вызывающие инфекции сельскохозяйственных культур после сбора урожая и других видов растений, оказались чувствительны к псевдомицинам (например, Penicillium и Geotrichim). Псевдомицины продемонстрировали существенную активность в отношении М. fijiensis (бананы). Неочищенные препараты, а также очищенные вещества обладают скрытыми возможностями для борьбы с заболеваниями растений. Широкомасштабное продуцирование псевдомицинов реально и относительно недорого. По всей видимости, природные продукты совместимы с окружающей средой и потенциально безопасны.
Источники информации
1. A.Ballio, F.Bossa, D.DiGiorgio, P.Ferranti, M.Paci, P.Pucci, A.Scaloni, A.Serge, G.A.Strobel. FEBS Letters, 1994, 355, 96-100.
2. C.Potera. Science, 1994, 265/605.
3. L.Harrision, D.B.Teplow, M.Rinaldi, G.A.Strobel. J.General Microbiology, 1991, 137/2857-2865.
4. В.Lam, G.Strobel, L. Harrison, S.Lam. Proc. Nat.Acad.Sci., 1987, 84, 6447-6451.
5. R.Scheffer, D.Elgersma, G.Strobel. Neth. J.Pl.Path., 1989, 95, 293-304.
6. R.Scheffer, D.Elgersma, L.A.DeWeger, G.Strobel. Neth. J.Pl.Path., 1989, 95, 281-292.
Изобретение относится к сельскому хозяйству, в частности к способу защиты и лечения растений и сельскохозяйственных культур. Наносят на растение эффективное количество одного или более составов псевдомицинов. Изобретение позволяет эффективно бороться с заболеваниями растений, которые вызываются грибками группы Ascomyceteous, относящихся к Mycosphaerella. 4 з.п. ф-лы, 3 табл.
| US 5576298, 19.11.1996 | |||
| US 5602097, 11.02.1997 | |||
| US 5885782, 23.03.1999 | |||
| СПОСОБ ЗАЩИТЫ РАСТЕНИЙ ОТ ГАЛЛОВЫХ НЕМАТОД | 1994 |
|
RU2062578C1 |
Авторы
Даты
2006-10-20—Публикация
2001-08-17—Подача