Настоящее изобретение относится к новым производным пиридина, к их получению и применению в качестве лекарственных средств. Изобретение прежде всего относится к соединениям формулы (I)
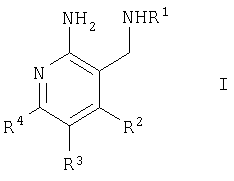
где
R1 означает водород или (низш.)алкил,
R2 означает гетероциклил, гетероциклил, независимо моно-, ди- или тризамещенный группой (низш.)алкил, (низш.)алкокси, перфтор(низш.)алкил, амино или галоген, арил или арил, независимо моно-, ди- или тризамещенный группой галоген, (низш.)алкил, (низш.)алкокси, амино или перфтор(низш.)алкил,
R3 и R4 вместе с атомами углерода, к которым они присоединены, образуют фенил, необязательно и независимо моно-, ди- или тризамещенный группой галоген, (низш.)алкил, перфтор(низш.)алкил или (низш.)алкокси, или 5-, 6-или 7-членный насыщенный цикл, необязательно содержащий гетероатом, выбранный из N, О и S, и необязательно и независимо моно-, ди- или тризамещенный группой галоген, (низш.)алкил, перфтор(низш.)алкил или (низш.)алкокси, причем указанный насыщенный цикл конденсирован в ортоположении с 5- или 6-членным ароматическим циклом, необязательно содержащим гетероатом, выбранный из N, О и S, а указанный ароматический цикл необязательно и независимо моно-, ди- или тризамещен заместителем, выбранным из группы, включающей галоген, (низш.)алкил, перфтор(низш.)алкил или (низш.)алкокси,
и к их фармацевтически приемлемым солям.
Фермент дипептидилпептидаза IV (ЕС.3.4.14.5, сокращенно DPP-IV) принимает участие в регуляции активности ряда гормонов. DPP-IV прежде всего эффективно и быстро гидролизует глюкагон-подобный пептид 1 (GLP-1), который является одним из наиболее активных стимуляторов продуцирования и секреции инсулина. При ингибировании DPP-IV происходит стимуляция действия эндогенного GLP-1 и повышение концентрации инсулина. У пациентов с нарушенной толерантностью к глюкозе и сахарным диабетом типа 2 при повышении концентрации инсулина снижается интенсивность гипергликемии и соответственно снижается риск повреждения ткани. Таким образом, ингибиторы DPP-IV предлагается использовать в качестве перспективных лекарственных средств для лечения нарушенной толерантности к глюкозе и сахарного диабета типа 2 (например, Vilhauer, WO 98/19998). Другие документы, относящиеся к уровню техники, включают WO 99/38501, DE 19616486, DE 19834591, WO 01/40180, WO 01/55105, US 6110949, WO 00/34241 и US 6011155.
Нами разработаны новые ингибиторы DPP-IV, которые чрезвычайно эффективно снижают уровень глюкозы в плазме (крови). Следовательно, соединения по настоящему изобретению могут применяться для лечения и/или профилактики диабета, прежде всего инсулиннезависимого сахарного диабета и/или нарушенной толерантности к глюкозе, а также других состояний, при которых лечебное действие оказывается благодаря усилению действия пептида, обычно инактивируемого ферментом DPP-IV. Неожиданно установлено, что соединения по настоящему изобретению могут также применяться для лечения и/или профилактики заболевания пищеварительного тракта, неспецифического язвенного колита, болезни Крона, ожирения и/или метаболического синдрома. Кроме того, соединения по настоящему изобретению можно использовать в качестве мочегонных агентов и для лечения и/или профилактики гипертензии. Неожиданно оказалось, что соединения по настоящему изобретению проявляют улучшенные терапевтические и фармакологические свойства по сравнению с другими ингибиторами DPP-IV, известными из уровня техники, например, в контексте фармакокинетических свойств и биодоступности.
Если не указано иное, термины, используемые в описании с целью иллюстрации и определения сущности и объема изобретения, имеют следующие значения.
Термин "низш.", используемый в описании, означает группу, содержащую от одного до шести, предпочтительно от одного до четырех атомов углерода.
Термин "галоген" означает фтор, хлор, бром и иод, предпочтительно фтор, бром и хлор, наиболее предпочтительно хлор.
Термин "алкил", используемый отдельно или в комбинации с другими группами, означает разветвленный или прямой одновалентный насыщенный алифатический углеводородный радикал, содержащий от 1 до 20, предпочтительно от 1 до 16 атомов углерода, более предпочтительно от 1 до 10 атомов углерода. Термин "(низш.)алкил", используемый отдельно или в комбинации с другими группами, означает разветвленный или прямой одновалентный алкильный радикал, содержащий от 1 до 6 атомов углерода, предпочтительно от 1 до 4 атомов углерода. Примеры (низш.)алкильных радикалов включают метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил, трет-бутил, н-пентил, 3-метилбутил, н-гексил, 2-этилбутил и т.п. Предпочтительно (низш.)алкильные остатки означают метил и этил, прежде всего предпочтителен метил.
Термин "перфтор(низш.)алкил" означает (низш.)алкильную группу, где все атомы водорода (низш.)алкильной группы заменены на фтор. Предпочтительные перфтор(низш.)алкильные группы включают трифторметил, пентафторэтил и гептафторпропил, прежде всего предпочтителен трифторметил.
Термин "алкокси" означает группу R'-O-, где R' означает алкил. Термин "(низш.)алкокси" означает группу R'-O-, где R' означает (низш.)алкил. Примерами (низш.)алкоксигрупп являются, например, метокси, этокси, пропокси, изопропокси, бутокси, изобутокси и гексилокси, прежде всего предпочтителен метокси.
Термин "гетероциклил" означает насыщенный, ненасыщенный или ароматический одновалентный циклический радикал, содержащий по мере один гетероатом, выбранный из атомов азота, серы и кислорода, или их комбинацию. Примерами гетероциклильных остатков являются пиридил, пиримидинил, фурил, тиенил, индолил, бензо[1,3]диоксолил, бензофуранил, бензотиофенил, дибензофуранил, оксазолил, имидазолил, тиазолил, изоксазолил, пиразолил, изотиазолил, оксадиазолил, тиадиазолил, триазолил, тетразолил, оксатриазолил, тиатриазолил, пиридазил, пиразинил, пирролидинил, азепанил и морфолино. Указанные гетероциклильные остатки независимо моно-, ди- или тризамещены группой галоген, амино, перфтор(низш.)алкил, (низш.)алкил или (низш.)алкокси, предпочтительно (низш.)алкил или (низш.)алкокси.
Термин "арил" означает ароматический одновалентный моно- или поликарбоциклический радикал, такой как фенил или нафтил, предпочтительно фенил, необязательно и независимо моно-, ди- или тризамещенный группой (низш.)алкил, (низш.)алкокси, галоген, амино или перфтор(низш.)алкил, предпочтительно (низш.)алкил, (низш.)алкокси и галоген.
Термин "фармацевтически приемлемые соли" включает соли соединений формулы (I) неорганических или органических кислот, таких как хлористоводородная кислота, бромистоводородная кислота, азотная кислота, серная кислота, фосфорная кислота, лимонная кислота, муравьиная кислота, малеиновая кислота, уксусная кислота, фумаровая кислота, янтарная кислота, винная кислота, метансульфоновая кислота, салициловая кислота, паратолуолсульфоновая кислота и т.п., которые являются нетоксичными в организме пациента. Предпочтительными солями являются формиаты, малеаты, цитраты, гидрохлориды, гидробромиды, метансульфонаты, более предпочтительны гидрохлориды.
В одном варианте настоящего изобретения R означает (низш.)алкил, предпочтительно метил.
В другом варианте R2 означает гетероциклил, необязательно и независимо моно-, ди- или тризамещенный группой (низш.)алкил, (низш.)алкокси или галоген. Предпочтительными гетероциклильными остатками R2 являются незамещенный тиенил и незамещенный бензо[1,3]диоксолил. В предпочтительном варианте R означает арил, предпочтительно фенил, необязательно и независимо орто-, мета- или пара-, предпочтительно орто- и паразамещенный группой (низш.)алкил, (низш.)алкокси, галоген, амино или перфтор(низш.)алкил, предпочтительно галоген, (низш.)алкил, перфтор(низш.)алкил или (низш.)алкокси. Наиболее предпочтительно R2 означает 2,4-дихлорфенил.
В другом варианте R3 и R4 вместе с атомами углерода, к которым они присоединены, образуют фенил, необязательно и независимо моно-, ди- или тризамещенный группой галоген, (низш.)алкил, перфтор(низш.)алкил или (низш.)алкокси. Предпочтительно указанный фенильный остаток незамещен или монозамещен галогеном, предпочтительно хлором, или перфтор(низш.)алкилом, предпочтительно трифторметилом.
В еще одном варианте R3 и R4 вместе с атомами углерода, к которым они присоединены, образуют 5-, 6- или 7-членный насыщенный цикл (цикл А), необязательно содержащий гетероатом, выбранный из N, О и S, и необязательно и независимо моно-, ди- или тризамещенный группой галоген, (низш.)алкил, перфтор(низш.)алкил или (низш.)алкокси, причем указанный насыщенный цикл конденсирован в ортоположении с 5- или 6-членным ароматическим циклом (циклом В), необязательно содержащим гетероатом, выбранный из N, О и S, а указанный ароматический цикл необязательно и независимо моно-, ди- или тризамещен группой галоген, такой как фтор, хлор и бром, (низш.)алкил, такой, как метил, перфтор(низш.)алкил, такой как трифторметил, или (низш.)алкокси, такой как метокси.
Указанный цикл А предпочтительно незамещен или замещен группой (низш.)алкил, такой как метил, цикл В предпочтительно означает фенил или тиенил, прежде всего предпочтителен фенил, необязательно и независимо моно-, ди- или тризамещенный группой галоген, (низш.)алкил, перфтор(низш.)алкил или (низш.)алкокси.
Предпочтительными примерами этого варианта являются следующие группы:
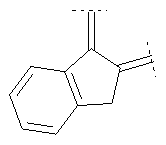
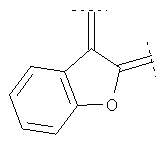
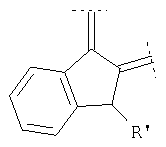
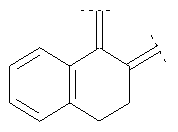
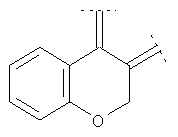
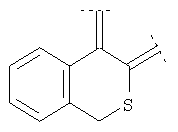
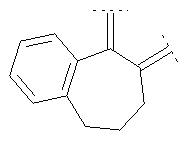
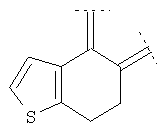
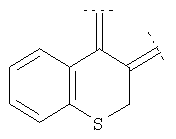
где фенил необязательно замещен, как указано выше, a R' означает (низш.)алкил, предпочтительно метил. Более предпочтительны




где фенил необязательно замещен, как указано выше, а R' означает (низш.)алкил, предпочтительно метил.
Предпочтительными соединениями по настоящему изобретению являются соединения формулы I, где R1 означает водород, R2 означает фенил, необязательно и независимо орто-, мета- или пара-, предпочтительно орто- и паразамещенный группой (низш.)алкил, такой как метил, галоген, такой как хлор и фтор, (низш.)алкил, такой как метил, перфтор(низш.)алкил, такой как трифторметил, или (низш.)алкокси, такой как метокси, прежде всего предпочтителен 2,4-дихлорфенил, a R3 и R4 вместе с атомами углерода, к которым они присоединены, образуют 5-, 6- или 7-членный насыщенный цикл, необязательно и независимо ди- или тризамещенный группой галоген, (низш.)алкил, перфтор(низш.)алкил или (низш.)алкокси, причем указанный насыщенный цикл конденсирован в ортоположении с 5- или 6-членным ароматическим циклом, необязательно содержащим гетероатом, выбранный из N, О и S, причем ароматический цикл необязательно и независимо моно-, ди- или тризамещен группой галоген, такой как фтор, хлор и бром, (низш.)алкил, такой как метил, перфтор(низш.)алкил, такой как трифторметил, или (низш.)алкокси, такой, как метокси.
Предпочтительными соединениями общей формулы (I) являются соединения, выбранные из группы, включающей
3-аминометил-4-(2,4-дихлорфенил)-5,6-дигидробензо[h]хинолин-2-иламин,
3-аминометил-4-(2,4-дихлорфенил)-5Н-индено[1,2-b]пиридин-2-иламин,
3-аминометил-4-(2,4-дихлорфенил)-6,7-дигидро-5Н-бензо[6,7]циклогепта[1,2-b]пиридин-2-иламин,
3-аминометил-4-(2,4-дихлорфенил)-7-метокси-5Н-индено[1,2-b]пиридин-2-иламин,
3-аминометил-4-(2,4-дихлорфенил)-7,8-диметокси-5Н-индено[1,2-b]пиридин-2-иламин,
3-аминометил-4-(2,4-дихлорфенил)бензо[4,5]фуро[3,2-b]пиридин-2-иламин,
2-аминометил-1-(2,4-дихлорфенил)-10Н-9-окса-4-азафенантрен-3-иламин,
3-аминометил-4-(2,4-дихлорфенил)-5,6-дигидротиено[2,3-h]хинолин-2-иламин,
2-аминометил-1-(2,4-дихлорфенил)-6-фтор-10Н-9-окса-4-азафенантрен-3-иламин,
2-аминометил-1-(2,4-дихлорфенил)-10Н-9-тиа-4-азафенантрен-3-иламин,
3-аминометил-4-(2,4-дихлорфенил)-5-метил-5Н-индено[1,2-b]пиридин-2-иламин,
2-аминометил-1-(2,4-дихлорфенил)-9Н-10-тиа-4-азафенантрен-3-иламин,
3-аминометил-4-(2,4-дихлорфенил)-10-фтор-6,7-дигидро-5Н-бензо[6,7]циклогепта[1,2-b]пиридин-2-иламин,
2-аминометил-1-(2,4-дихлорфенил)-10Н-9-тиа-4-азафенантрен-3-иламин,
3-аминометил-4-(2,4-дихлорфенил)-5-метил-5Н-индено[1,2-b]пиридин-2-иламин,
2-аминометил-1-(2,4-дихлорфенил)-9Н-10-тиа-4-азафенантрен-3-иламин,
3-аминометил-4-(2,4-дихлорфенил)-10-фтор-6,7-дигидро-5Н-бензо[6,7]циклогепта[1,2-b]пиридин-2-иламин,
3-аминометил-4-(2,4-дихлорфенил)-7-фтор-5Н-индено[1,2-b]пиридин-2-иламин,
3-аминометил-4-(2,4-дихлорфенил)-8-метил-5Н-индено[1,2-b]пиридин-2-иламин,
3-аминометил-4-(2,4-дихлорфенил)-9-метокси-5,6-дигидро-бензо[b]хинолин-2-иламин,
2-аминометил-6-хлор-1-(2,4-дихлорфенил)-10Н-9-тиа-4-азафенантрен-3-иламин,
3-аминометил-4-(2,4-дихлорфенил)-7,9-диметил-5,6-дигидробензо[b]хинолин-2-иламин,
2-аминометил-1-(2,4-дихлорфенил)-6-метил-10Н-9-окса-4-азафенантрен-3-иламин,
3-аминометил-7-бром-4-(2,4-дихлорфенил)-5Н-индено[1,2-b]пиридин-2-иламин,
3-аминометил-4-паратолилхинолин-2-иламин,
3-аминометил-6-хлор-4-(2-фторфенил)хинолин-2-иламин,
3-аминометил-6-хлор-4-(2-фторфенил)хинолин-2-иламин,
3-аминометил-4-фенил-6-трифторметилхинолин-2-иламин,
3-аминометил-4-(2-метоксифенил)хинолин-2-иламин,
3-аминометил-4-(2,4-дихлорфенил)хинолин-2-иламин,
3-аминометил-4-(2-хлорфенил)хинолин-2-иламин,
3-аминометил-4-(4-хлорфенил)хинолин-2-иламин,
3-аминометил-4-фенилхинолин-2-иламин, и их фармацевтически приемлемые соли.
Соединения формулы I, где R означает ортозамещенный фенил могут существовать в виде оптически чистых энантиомров или рацематов. Изобретение включает все указанные формы.
Предпочтительными вариантами настоящего изобретения являются соединения формулы (I), а также фармацевтически приемлемые соли соединений формулы (I).
Предполагается, что соединения общей формулы (I) по настоящему изобретению можно модифицировать по функциональным группам с образованием производных, которые могут превращаться в исходные соединения in vivo.
Соединения по настоящему изобретению получают, как показано ниже на схемах I и II.
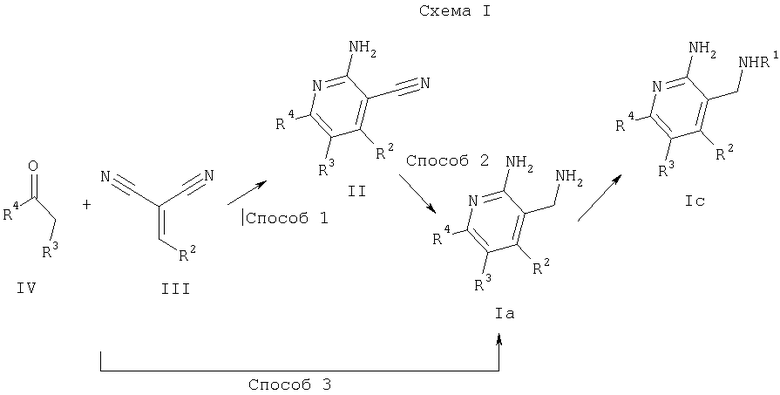
На схеме I R3 и R4 вместе с атомами углерода, к которым они присоединены, образуют 5-, 6- или 7-членный насыщенный цикл, необязательно содержащий гетероатом, выбранный из N, О и S, и необязательно и независимо моно-, ди- или тризамещенный группой галоген, (низш.)алкил, перфтор(низш.)алкил или (низш.)алкокси, причем указанный насыщенный цикл конденсирован в ортоположении с 5- или 6-членным ароматическим циклом, необязательно содержащим гетероатом, выбранный из N, О и S, и необязательно и независимо моно-, ди- или тризамещеннным группой галоген, (низш.)алкил, перфтор(низш.)алкил или (низш.)алкокси, а R1 и R2 имеют значения, указанные выше.
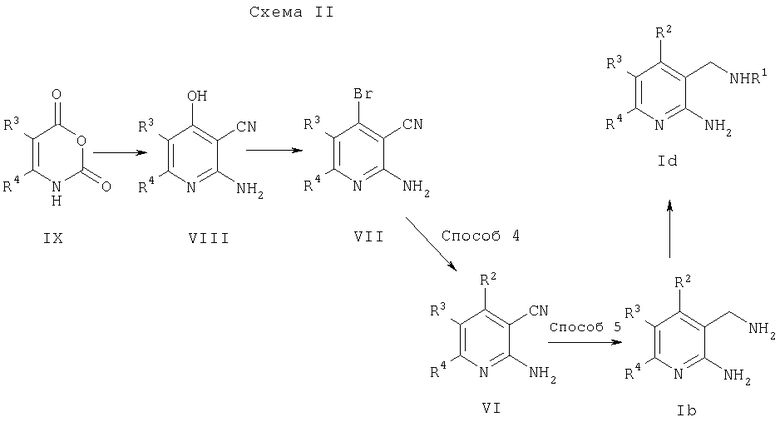
На схеме II R3 и R4 вместе с атомами углерода, к которым они присоединены, образуют фенильный цикл, необязательно и независимо моно-, ди- или тризамещенный группой галоген, (низш.)алкил, перфтор(низш.)алкил или (низш.)алкокси, а R1 и R2 имеют значения, указанные выше.
Настоящее изобретение относится также к способу получения соединений формулы I и V. Эти способы включают восстановление нитрилов формулы II и VI с образованием аминов формулы Ia и Ib соответственно. Восстановление проводят известными методами. Например, восстановление можно проводить гидридом металла, таким как гидрид литияалюминия, в инертном растворителе.
Нитрилы формулы II получают известными способами. Одним из таких способов является реакция арилиденмалононитрила III, такого как 2-(2,4-дихлорбензилиден)малононитрил, с кетоном IV, таким как альфа-тетралон. Например, реакцию можно проводить при нагревании в присутствии ацетата аммония в инертном растворителе, таком как метанол.
Нитрилы формулы VI можно получить из 2-амино-4-бромхинолин-3-карбонитрила и арилбороновых кислот способом, известным как "конденсация Сузуки". Например, реакцию проводят при нагревании в присутствии соединения палладия, такого как Pd(OAc)2, основания, такого как К3PO4, и необязательно в присутствии добавок, таких как фосфины, например, 2-дициклогексилфосфино-2'-(N,N-диметиламино)дифенил, в инертном растворителе. 2-Амино-4-бромхинолин-3-карбонитрил можно получить в несколько стадий из ангидрида изатовой кислоты известными методами.
Соединения формул Ic и Id можно получить из соответствующих соединений формулы Ia и Ib соответственно известным методом алкилирования (например, см. Bar-Haim G., Kol M., Tetrahedron Lett., 39, 2663 (1998)).
Кроме того, изобретение относится к соединениям формулы (I), указанным выше и полученным описанным выше способом.
Как указано выше, соединения формулы (I) по настоящему изобретению можно использовать в качестве лекарственных средств для лечения и/или профилактики заболеваний, ассоциированных с DPP IV, таких как диабет, прежде всего инсулиннезависимый сахарный диабет, нарушенная толерантность к глюкозе, заболевание пищеварительного тракта, неспецифический язвенный колит, болезнь Крона, ожирение и/или метаболический синдром, предпочтительно инсулиннезавимый сахарный диабет и/или нарушенная толерантность к глюкозе. Кроме того, соединения по настоящему изобретению можно использовать в качестве мочегонных агентов и для лечения и/или профилактики гипертензии.
Изобретение также относится к фармацевтическим композициям, включающим соединение, указанное выше, и фармацевтически приемлемый носитель и/или адъювант.
Кроме того, изобретение относится к вышеуказанным соединениям для применения в качестве терапевтически активных веществ, прежде всего в качестве терапевтически активных веществ для лечения и/или профилактики заболеваний, ассоциированных с DPP IV, таких как диабет, прежде всего инсулиннезависимый сахарный диабет, нарушенная толерантность к глюкозе, заболевание пищеварительного тракта, неспецифический язвенный колит, болезнь Крона, ожирение и/или метаболический синдром, предпочтительно для применения в качестве терапевтически активных веществ для лечения и/или профилактики инсулиннезавимого сахарного диабета и/или нарушенной толерантности к глюкозе. Кроме того, изобретение относится к соединениям, указанным выше, для применения в качестве мочегонных агентов или для применения в качестве терапевтически активных веществ для лечения и/или профилактики гипертензии.
В другом варианте изобретение относится к способу лечения и/или профилактики заболеваний, ассоциированных с DPP IV, таких как диабет, прежде всего инсулиннезависимый сахарный диабет, нарушенная толерантность к глюкозе, заболевание пищеварительного тракта, неспецифический язвенный колит, болезнь Крона, ожирение и/или метаболический синдром, предпочтительно для лечения и/или профилактики инсулиннезависимого сахарного диабета и/или нарушенной толерантности к глюкозе, причем указанный способ включает введение соединения, указанного выше, человеку или животному. Кроме того, изобретение относится к способу лечения и/или профилактики, указанному выше, где заболевание означает гипертензию, где лечебное действие достигается благодаря применению мочегонного агента.
Кроме того, изобретение относится к применению вышеуказанных соединений для лечения и/или профилактики заболеваний, ассоциированных с DPP IV, таких как диабет, прежде всего инсулиннезависимый сахарный диабет, нарушенная толерантность к глюкозе, заболевание пищеварительного тракта, неспецифический язвенный колит, болезнь Крона, ожирение и/или метаболический синдром, предпочтительно для лечения и/или профилактики инсулиннезависимого сахарного диабета и/или нарушенной толерантности к глюкозе. Кроме того, изобретение относится к применению, указанному выше, где заболевание означает гипертензию, или к применению в качестве мочегонного агента.
Кроме того, изобретение относится к применению вышеуказанных соединений для получения лекарственных средств, предназначенных для лечения и/или профилактики заболеваний, ассоциированных с DPP IV, таких как диабет, прежде всего инсулиннезависимый сахарный диабет, нарушенная толерантность к глюкозе, заболевание пищеварительного тракта, неспецифический язвенный колит, болезнь Крона, ожирение и/или метаболический синдром, предпочтительно для лечения и/или профилактики инсулиннезавимого сахарного диабета и/или нарушенной толерантности к глюкозе. Такие лекарственные средства включают соединение, указанное выше. Кроме того, изобретение относится к применению, указанному выше, где заболевание означает гипертензию, или к применению для получения мочегонных агентов.
В связи с вышеуказанными способами и применениями предпочтительными заболеваниями являются: диабет, прежде всего инсулиннезависимый сахарный диабет, нарушенная толерантность к глюкозе, ожирение и/или метаболический синдром, предпочтительно инсулиннезависимый сахарный диабет и/или нарушенная толерантность к глюкозе.
Соединения формулы (I) получают по нижеописанным методам, по методам, приведенным в примерах или аналогичными методами. Оптимальные условия отдельных стадий реакции известны специалисту в данной области. Исходные материалы являются коммерческими препаратами или их получают аналогично тому, как описано ниже, указано в примерах или известными методами.
Активность соединений формулы (I) определяют по следующей методике.
Активность ингибиторов DPP-IV определяют при использовании нативного DPP-IV человека, выделенного из плазмы (крови) человека, или рекомбинантного DPP-IV человека. Обработанную цитратом плазму (крови) человека, полученную от различных доноров, объединяют, фильтруют через мембрану с диаметром пор 0,2 мкм в стерильных условиях, аликвотные части объемом 1 мл быстро замораживают и хранят при -120°С до проведения анализа. При колориметрическом анализе в качестве источника фермента DPP-IV используют от 5 до 10 мкл плазмы (крови) человека, а при флуориметрическом анализе 1,0 мкл плазмы (крови) человека, при этом общий объем смеси составляет 100 мкл. кДНК, кодирующую аминокислотную последовательность DPP-IV (31-766), не содержащую N-концевого фрагмента и трансмембранного домена, клонируют в дрожжах (pichia pastoris). DPP-IV человека экспрессируют и выделяют из культуральной среды хроматографией на колонке, включая гельпроникающую, анионо- и катионообменную хроматографию. Степень очистки полученного препарата фермента по результатам электрофореза в ДДС-ПААГ при окрашивании кумаси составляет >95%. При колориметрическом анализе DPP-IV в качестве источника фермента используют 20 нг рекомбинантного DPP-IV человека, а при флуориметрическом анализе 2 нг рекомбинантного DPP-IV человека в общем объеме 100 мкл.
При флуорогенном анализе в качестве субстрата используют ала-про-7-амидо-4-трифторметилкумарин (фирма Calbiochem, кат.№125510). Исходный 20 мМ раствор субстрата в 10% ДМФА/Н2О хранят при -20°С. При определении IC50 конечная концентрация субстрата составляет 50 мкМ. При определении кинетических параметров, таких как Km, Vmax, Ki, концентрация субстрата составляет от 10 до 500 мкМ.
При колориметрическом анализе в качестве субстрата используют ала-про-pNA·HCl (фирма Bachem L-1115). Исходный 10 мМ раствор субстрата в 10% MeOH/H2O хранят при -20°С. При определении IC50 конечная концентрация субстрата составляет 200 мкМ. При определении кинетических параметров, таких как Кm, Vmax, Кi, концентрация субстрата составляет от 100 до 2000 мкМ.
Флуоресценцию измеряют на спектрофлуориметре LS 50 В (фирма Perkin Elmer) при волне возбуждения 400 нм и волне испускания 505 нм, причем измерение проводят каждые 15 с в течение от 10 до 30 мин. Константы исходной скорости рассчитывают методом оптимальной линейной регрессии.
Поглощение pNA, высвождающегося из колориметрического сустрата, определяют на спектрофотометре SrectraCount (фирма Packard) при 405 нм, причем измерение проводят каждые 2 мин в течение от 30 до 100 мин. Константы исходной скорости рассчитывают методом оптимальной линейной регрессии.
Активность DPP-IV определяют в 96-луночных планшетах при 37°С в объеме реакционной смеси 100 мкл. Буферный раствор для анализа включает 50 мМ трис/HCl, рН 7,8, содержащий 0,1 мг/мл БСА и 100 мМ NaCl. Анализируемые соединения растворяют в 100% ДМСО и разбавляют до требуемой концентрации в 10% ДМСО/H2O. Конечная концентрация ДМСО в реакционной смеси составляет 1% (об./об.). При этой концентрации инактивация фермента под действием ДМСО составляет <5%. Соединения анализируют с использованием предварительной инкубации с ферментом (37°С, 10 мин) и без предварительной инкубации. Реакцию инициируют добавлением субстрата с последующим перемешиванием.
Величины IC50 анализируемых соединений рассчитывают методом нелинейной регрессии по результатам ингибирования DPP-IV по меньшей мере при пяти различных концентрациях анализируемого соединения. Кинетические параметры ферментативной реакции рассчитывают по меньшей мере при пяти различных концентрацих субстрата и по меньшей мере при пяти различных концентрациях анализируемого соединения.
Как показано в таблице, предпочтительные соединения по настоящему изобретению характеризуются значениями IC50 от 1 нМ до 10 мкМ, более предпочтительно 1-100 нМ.
Соединения формулы (I) и/или их фармацевтически приемлемые соли могут использоваться в качестве лекарственных средств, например, в форме фармацевтических препаратов для энтерального, парентерального и местного введения. Соединения можно вводить, например, пероральным способом, например, в форме таблеток, таблеток с покрытием, драже, твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий, ректальным способом в форме суппозиториев, парентеральным способом, например, в форме инъекционных растворов или растворов для вливания, или местным способом, например, в форме мазей, кремов или масел. Предпочтителен пероральный способ введения.
Фармацевтические препараты получают известным способом, например переработкой указанных соединений формулы I и/или их фармацевтически приемлемых солей, необязательно в комбинации с другими терапевтически ценными соединениями, в смеси с пригодными, нетоксичными, инертными и терапевтически приемлемыми твердыми или жидкими носителями и при необходимости фармацевтическими адъювантами, в готовую галеновую форму.
Пригодные носители включают как неорганические, так и органические материалы. Так, например, при получении таблеток, таблеток в оболочке, драже и твердых желатиновых капсул в качестве носителей используются лактоза, кукурузный крахмал или его производные, тальк, стеариновая кислота или ее соли. Пригодными носителями для мягких желатиновых капсул являются, например, растительные масла, воски, жиры и полутвердые или жидкие полиолы (причем в зависимости от природы активного соединения в случае мягких желатиновых капсул обычно не требуется никаких носителей). Пригодными носителями для получения растворов и сиропов являются, например, вода, полиолы, сахароза, инвертированный сахар и т.п. Пригодными носителями для инъекционных растворов являются, например, вода, спирты, полиолы, глицерин и растительные масла. Пригодными носителями для суппозиториев являются, например, твердые или отвержденные масла, воски, жиры и полужидкие или жидкие полиолы. Пригодными носителями для препаратов местного применения являются глицериды, полусинтетические и синтетические глицериды, гидрогенированные масла, жидкие воски, жидкие парафины, жидкие жирные спирты, стеролы, полиэтиленгликоли и производные целлюлозы.
В качестве фармацевтических адъювантов используются различные стабилизаторы, консерванты, смачивающие и эмульгирующие агенты, агенты, улучшающие консистенцию, ароматизаторы, соли для регуляции осмотического давления, буферные вещества, солюбилизирующие агенты, красители, маскирующие агенты и антиоксиданты.
Дозы соединения формулы I могут варьировать в зависимости от излечиваемого заболевания, возраста и относительного состояния здоровья пациента, способа введения, и должны соответствовать индивидуальным требованиям в каждом конкретном случае. Для взрослых пациентов суточная доза составляет от приблизительно 1 до 1000 мг, предпочтительно от приблизительно 1 до 100 мг. В зависимости от тяжести заболевания и конкретного фармакокинетического профиля соединение можно вводить в виде одной или нескольких стандартных доз, например, от 1 до 3 стандартных доз.
Фармацевтические препараты обычно содержат приблизительно 1-500 мг, предпочтительно 1-100 мг соединения формулы I.
Изобретение иллюстрируется следующими примерами, не ограничивающими его объем.
Примеры
Сокращения:
ЯМР - спектроскопия ядерно-магнитного резонанса, МС - масс-спектрометрия, ТГФ - тетрагидрофуран, ДМФА - диметилформамид, ДМСО - диметилсульфоксид, ТФУ - трифторуксуная кислота, КТ - комнатная температура, tfp.температура возгорания.
Пример 1
Синтез арилметилиденмалононитрилов.
2-(2,4-Дихлорбензилиден)малононитрил
2,4-Дихлорбензальдегид (30,00 г, 171 ммоль) и малононитрил (13,59 г, 206 ммолей) суспендировали в 1-бутаноле (350 мл) в атмосфере аргона и перемешивали в течение 15 мин. Затем при КТ добавляли 8 капель пиперидина и перемешивали в течение еще 3 ч, после чего добавляли диэтиловый эфир. Осадок отделяли фильтрованием и промывали диэтиловым эфиром и гексаном, при этом получали указанное в заголовке соединение в виде бесцветного твердого вещества (35,34 г, 92%). МС: m/е 222,8 (М+).
1Н ЯМР (300 МГц, ДМСО-d6, 25°С): (7,45 (m, 1Н), 7,59 (m, 1Н), 8,18 (m, 2Н).
Пример 2
Синтез 2-аминоникотинонитрилов (схема I, способ 1)
2-Амино-4-(2,4-дихлорфенил)-5,6-дигидробензо[h]хинолин-3-карбонитрил
Смесь 2-(2,4-дихлорбензилиден)малононитрила (1,125 г, 5 ммолей), альфа-тетралона (735 мг, 5 ммолей), ацетата аммония (578 мг, 7,5 ммоля) и толуола (5 мл) перемешивали при кипячении с обратным холодильником в течение 3 ч. После охлаждения до комнатной температуры, смесь переносили в этилацетат, экстрагировали насыщенным раствором NaHCO3, водой и насыщенным раствором NaCl, сушили над Na2SO4 и выпаривали растворитель. Остаток очищали хроматографией на колонке с силикагелем (элюент: гексан, этлацетат), при этом получали указанное в заголовке соединение (868 мг, 47%). МС: m/е 365,9 (М+Н+).
Следующие 2-аминоникотинонитрилы получали аналогично тому, как описано выше:
2-амино-4-(2,4-дихлорфенил)-5Н-индено[1,2-b]пиридин-3-карбонитрил получали из 1-инданона в виде твердого вещества (322 мг, 18%), МС: m/е 352,0 (M+H+),
2-амино-4-(2,4-дихлорфенил)-6,7-дигидро-5Н-бензо[6,7]циклогепта[1,2-b]пиридин-3-карбонитрил получали из 1-бензосуберона в виде твердого вещества (730 мг, 38%), МС: m/е 379,9 (М+),
2-амино-4-(2,4-дихлорфенил)-7-метокси-5Н-индено[1,2-b]пиридин-3-карбонитрил получали из 5-метокси-1-инданона в виде твердого вещества (715 мг, 37%), МС: m/е 381,8 (М+),
2-амино-4-(2,4-дихлорфенил)-7,8-диметокси-5Н-индено[1,2-b]пиридин-3-карбонитрил получали из 5,6-диметокси-1-инданона в виде твердого вещества (180 мг, 9%), МС: m/е 412,0 (М+Н+),
2-амино-4-(2,4-дихлорфенил)бензо[4,5]фуро[3,2-b]пиридин-3-карбонитрил получали из бензофуран-3(2Н)-она в виде твердого вещества (128 мг, 13%), МС: m/е 354,0 (М+Н+).
Пример 3
Синтез 3-аминометилпиридин-2-иламинов (схема I, способ 2)
3-Аминометил-4-(2,4-дихлорфенил)-5,6-дигидробензо[h]хинолин-2-иламин
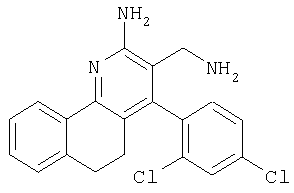
К суспензии LiAlH4 (162 мг, 4,26 ммоля) в ТГФ (1 мл) в атмосфере аргона медленно добавляли раствор 2-амино-4-(2,4-дихлорфенил)-5,6-дигидробензо[h]хинолин-3-карбонитрила (200 мг, 0,58 ммоля) в ТГФ (1 мл). Реакционную смесь перемешивали при комнатной температуре в течение 2 ч, охлаждали до -20°С и добавляли 0,2 мл воды. Через 15 мин к смеси добавляли этилацетат и фильтровали через декалит. Органическую фазу отделяли, промывали водой и сушили над сульфатом натрия. Продукт очищали экспресс-хроматографией на силикагеле (элюент: метанол, дихлорметан), при этом получали указанное в заголовке соединение в виде твердого вещества желтого цвета (53 мг, 26%). МС: m/е 369,9 (М+Н+).
Пример 4
3-Аминометил-4-(2,4-дихлорфенил)-5Н-индено[1,2-b]пиридин-2-иламин
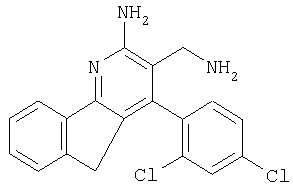
Указанное в заголовке соединение получали в виде твердого вещества (64 мг, 67%) из 2-амино-4-(2,4-дихлорфенил)-5Н-индено[1,2-b]пиридин-3-карбонитрила аналогично тому, как описано в примере 3. МС: m/е 355,8 (М+).
Пример 5
3-Аминометил-4-(2,4-дихлорфенил)-6,7-дигидро-5Н-бензо[6,7]циклогепта[1,2-b]пиридин-2-иламин
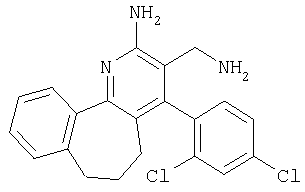
Указанное в заголовке соединение получали в виде твердого вещества (40 мг, 25%) из 2-амино-4-(2.4-дихлорфенил)-6,7-дигидро-5Н-бензо[6,7]циклогепта[1,2-b]пиридин-3-карбонитрила аналогично тому, как описано в примере 3. МС: m/е 383,9 (М+).
Пример 6
3-Аминометил-4-(2,4-дихлорфенил)-7-метокси-5Н-индено[1,2-b]пиридин-2-иламин
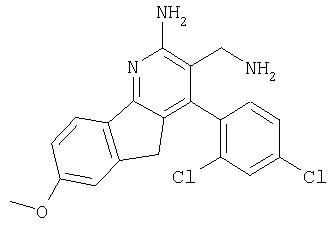
Указанное в заголовке соединение получали в виде твердого вещества (14 мг, 9%) из 2-амино-4-(2,4-дихлорфенил)-7-метокси-5Н-индено[1,2-b]пиридин-3-карбонитрила аналогично тому, как описано в примере 3. МС: m/е 385,9 (М+).
Пример 7
3-Аминометил-4-(2,4-дихлорфенил)-7,8-диметокси-5Н-индено[1,2-b] пиридин-2-иламин
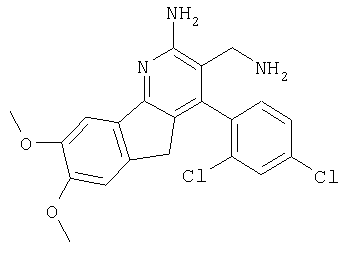
Указанное в заголовке соединение получали в виде твердого вещества (9 мг, 6%) из 2-амино-4-(2,4-дихлорфенил)-7,8-диметокси-5Н-индено[1,2-b]пиридин-3-карбонитрила аналогично тому, как описано в примере 3. МС: m/е 415,9 (М+).
Пример 8
3-Аминометил-4-(2,4-дихлорфенил)бензо[4,5]фуро[3,2-b]пиридин-2-иламин
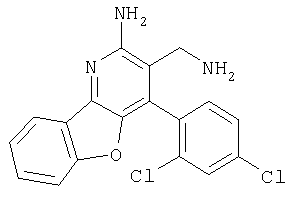
Указанное в заголовке соединение получали в виде твердого вещества (0,8 мг, 62%) из 2-амино-4-(2,4-дихлорфенил)бензо[4,5]фуро[3,2-b]пиридин-3-карбонитрила аналогично тому, как описано в примере 3. МС: m/е 357,8 (М+).
Пример 9
Препаративный синтез 3-аминометилпиридин-2-иламинов из арилметилиденмалононитрилов (схема I, способ 3)
2-Аминометил-1-(2,4-дихлорфенил)-10Н-9-окса-4-азафенантрен-3-иламин
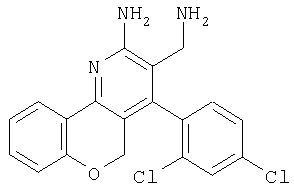
2-(2,4-Дихлорбензилиден)малононитрил (95 мг, 0,4 ммоля), хроман-4-он (59 мг, 0,4 ммоля), ацетат аммония (78 мг, 1,2 ммоля) и толуол (4 мл) помещали в реакционный сосуд и встряхивали при 118°С в течение ночи. Затем смесь охлаждали и фильтровали, фильтрат упаривали в вакуумной центрифуге (45°С), остаток очищали с использованием автоматизированной системы для препаративной ЖХВР (колонка YMC CombiPrep С18, 50×20 мм, элюент: градиент СН3CN/вода + 0,1% ТФУ, от 5 до 95%, скорость элюирования 40 мл/мин, время 6,0 мин, λ 230 нм). Полученное твердое вещество (28 мг) растворяли в ТГФ (1 мл) и при охлаждении (0°С) в атмосфере аргона добавляли в реакционный сосуд с суспензией 100 мг гидрида литияалюминия в 1 мл ТГФ. Реакционную смесь встряхивали при КТ в течение 2 ч, а затем при 40°С в течение 4 ч. После охлаждения к смеси осторожно добавляли воду и смесь фильтровали. Фильтрат выпаривали в вакуумной центрифуге (45°С), остаток растворяли в 1 мл ДМФА и очищали с использованием системы для препаративной ЖХВР (колонка YMC CombiPrep С18, 50×20 мм, элюент: градиент СН3CN/вода + 0,1% ТФУ, от 5 до 95%, скорость элюирования 40 мл/мин, время 6,0 мин, λ 230 нм), при этом получали 11 мг (7%) указанного в заголовке соединения в виде твердого вещества. МС: m/е 371,9 (М+Н).
Пример 10
3-Аминометил-4-(2,4-дихлорфенил)-5,6-дигидротиено[2,3-h]хинолин-2-иламин
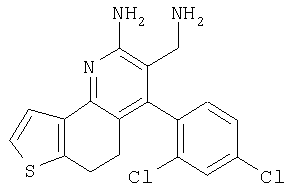
Указанное в заголовке соединение получали в виде твердого вещества из 6,7-дигидро-5Н-бензо[b]тиофен-4-она аналогично тому, как описано в примере 9. МС: m/е 376 (М+Н+).
Пример 11
2-Аминометил-1-(2,4-дихлорфенил)-6-фтор-10Н-9-окса-4-азафенантрен-3-иламин
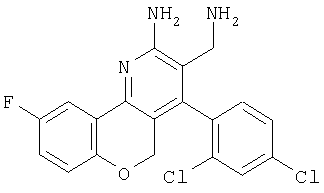
Указанное в заголовке соединение получали в виде твердого вещества из 6-фторхроман-4-она аналогично тому, как описано в примере 9. МС: m/е 390,2 (М+Н+).
Пример 12
2-Аминометил-1-(2,4-дихлорфенил)-10Н-9-тиа-4-азафенантрен-3-иламин
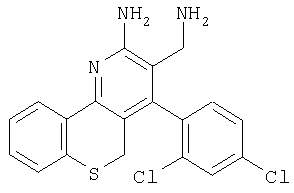
Указанное в заголовке соединение получали в виде твердого вещества из тиохроман-4-она аналогично тому, как описано в примере 9. МС: m/е 388,2 (М+Н+).
Пример 13
3-Аминометил-4-(2,4-дихлорфенил)-5-метил-5Н-индено[1,2-h]пиридин-2-иламин
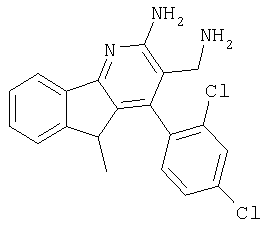
Указанное в заголовке соединение получали в виде твердого вещества из 3-метилиндан-1-она аналогично тому, как описано в примере 9. МС: m/е 370,1 (М+Н+).
Пример 14
2-Аминометил-1-(2,4-дихлорфенил)-9Н-10-тиа-4-азафенантрен-3-иламин
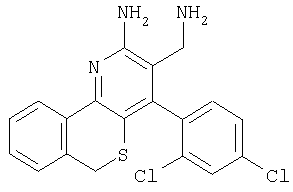
Указанное в заголовке соединение получали в виде твердого вещества из изотиохроман-4-она аналогично тому, как описано в примере 9. МС: m/е 388,2 (М+Н+).
Пример 15
3-Аминометил-4-(2,4-дихлорфенил)-10-фтор-6,7-дигидро-5Н-бензо[6,7]циклогепта[1,2-b]пиридин-2-иламин
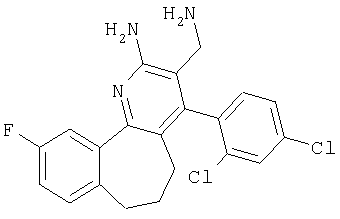
Указанное в заголовке соединение получали в виде твердого вещества из 3-фтор-6,7,8,9-тетрагидробензоциклогептен-5-она аналогично тому, как описано в примере 9. МС: m/е 402,0 (М+Н+).
Пример 16
3-Аминометил-4-(2,4-дихлорфенил)-7-фтор-5Н-индено[1,2-b]пиридин-2-иламин
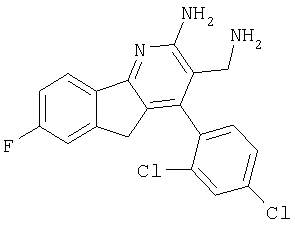
Указанное в заголовке соединение получали в виде твердого вещества из 5-фтор-1-инданона аналогично тому, как описано в примере 9. МС: m/е 374,3 (М+Н+).
Пример 17
3-Аминометил-4-(2,4-дихлорфенил)-8-метил-5Н-индено[1,2-b]пиридин-2-иламин
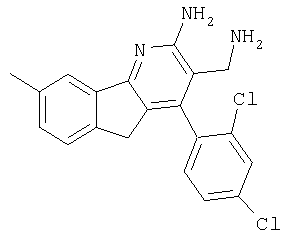
Указанное в заголовке соединение получали в виде твердого вещества из 6-метилиндан-1-она аналогично тому, как описано в примере 9. МС: m/е 370,0 (М+Н+).
Пример 18
3-Аминометил-4-(2,4-дихлорфенил)-9-метокси-5,6-дигидробензо[h]хинолин-2-иламин
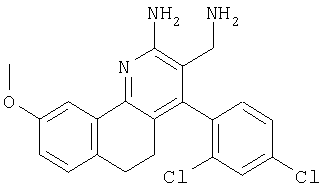
Указанное в заголовке соединение получали в виде твердого вещества из 7-метокси-3,4-дигидро-2Н-нафталин-1-она аналогично тому, как описано в примере 9. МС: m/е 400,3 (М+Н+).
Пример 19
2-Аминометил-6-хлор-1-(2,4-дихлорфенил)-10Н-9-тиа-4-азафенантрен-3-иламин
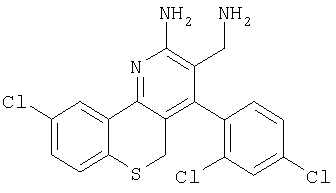
Указанное в заголовке соединение получали в виде твердого вещества из 6-хлортиохроман-4-она аналогично тому, как описано в примере 9. МС: m/е 422,0 (М+).
Пример 20
3-Аминометил-4-(2,4-дихлорфенил)-7,9-диметил-5,6-дигидробензо[h]хинолин-2-иламин
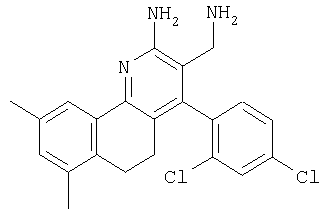
Указанное в заголовке соединение получали в виде твердого вещества из 5,7-диметил-3,4-дигидро-2Н-нафталин-1-она аналогично тому, как описано в примере 9. МС: m/е 398,0 (М+Н+).
Пример 21
2-Аминометил-1-(2,4-дихлорфенил)-6-метил-10Н-9-окса-4-азафенантрен-3-иламин
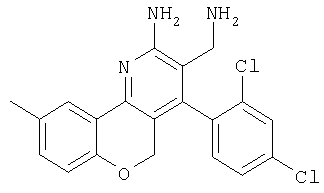
Указанное в заголовке соединение получали в виде твердого вещества из 6-метилхроман-4-она аналогично тому, как описано в примере 9. МС: m/е 386,2 (М+Н+).
Пример 22
3-Аминометил-7-бром-4-(2,4-дихлорфенил)-5Н-индено[1,2-b]пиридин-2-иламин
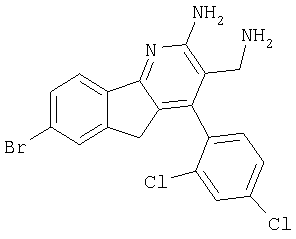
Указанное в заголовке соединение получали в виде твердого вещества из 5-броминдан-1-она аналогично тому, как описано в примере 9. МС: m/е 435,0 (М+Н+).
Пример 23
Синтез хинолин-3-карбонитрилов
а) 2-Амино-4-гидроксихинолин-3-карбонитрил
К раствору малононитрила (10 г, 151,4 ммоля) в ДМФА (210 мл) добавляли раствор гидрида натрия (60%, 6,05 г, 151,3 ммоля) и смесь перемешивали при КТ в течение 30 мин. Затем добавляли изатовый ангидрид (22,2 г, 136,1 ммоля) и смесь перемешивали при 60°С в течение 30 мин. Смесь выливали в 1,4 л смеси лед/вода и фильтровали. Фильтрат подкисляли 37% HCl, перемешивали в течение 1 ч и отделяли осадок. Продукт высушивали при 40°С в вакууме, твердое вещество желтого цвета растворяли в ДМФА (100 мл) и нагревали при 120°С в течение 10 мин. Затем смесь охлаждали до КТ и выливали в воду (1,5 л), осадок отделяли фильтрованием и высушивали при 50°С при пониженном давлении, при этом получали указанное в заголовке соединение в виде твердого вещества желтого цвета (24,33 г, 96%). МС: m/е 185,1 (М+).
б) 2-Амино-4-бромхинолин-3-карбонитрил
2-Амино-4-гидроксихинолин-3-карбонитрил (6 г, 32,4 ммоля) суспендировали в ацетонитриле (2 л), добавляли трибромид фосфора (33 г, 11,5 мл, 122 ммоля) и бром (19,15 г, 6,15 мл, 120 ммолей) и смесь кипятили с обратным холодильником в течение ночи. Растворитель выпаривали при пониженном давлении и смесь переносили в 1 н. NaOH. Продукт отделяли фильтрованием, промывали водой и высушивали, при этом получали указанное в заголовке соединение (5,05 г, 62%). МС: m/е 248,2 (М+).
Пример 24
Синтез 2-амино-4-арилхинолин-3-карбонитрилов (схема II, способ 4)
2-Амино-4-пара-толилхинолин-3-карбонитрил
2-Амино-4-бромхинолин-3-карбонитрил (248 мг, 1 ммоль), 4-метилфенилбороновую кислоту (204 мг, 1,5 ммоля), ацетат палладия (II) (11 мг, 0,05 ммоля), 2-дициклогексилфосфино-2'-(N,N-диметиламино)дифенил (39 мг, 0,10 ммоля) и К3РО4 (425 мг, 2 ммоля) суспендировали в 4 мл толуола (в атмосфере аргона) и нагревали при 100°С в течение 21 ч. Затем реакционную смесь переносили в диэтиловый эфир, промывали раствором NaOH, солевым раствором и сушили над Na2SO4. Растворитель выпаривали, остаток очищали хроматографией на колонке с силикагелем (элюент: градиент дихлометан/метанол, от 100:0 до 85:15), при этом получали указанное в заголовке соединение (46 мг, 18%). МС: m/е 259,9 (М++Н).
Следующие 2-амино-4-арилхинолин-3-карбонитрилы получали аналогично тому, как описано выше:
2-амино-6-хлор-4-(2-фторфенил)хинолин-3-карбонитрил получали в виде твердого вещества (54 мг, 10%) при взаимодействии 2-фторфенилбороновой кислоты и 2-амино-4-бром-6-хлорхинолин-3-карбонитрила, МС: m/е 298,2 (М++Н),
2-амино-6-хлор-4-фенилхинолин-3-карбонитрил получали в виде твердого вещества (60 мг, 11%) при взаимодействии фенилбороновой кислоты и 2-амино-4-бром-6-хлорхинолин-3-карбонитрила, МС: m/е 279,8 (М++Н),
2-амино-6-хлор-4-(2-хлорфенил)хинолин-3-карбонитрил получали в виде твердого вещества (33 мг, 5%) при взаимодействии 2-хлорфенилбороновой кислоты и 2-амино-4-бром-6-хлорхинолин-3-карбонитрила, МС: m/е 313,7 (М++Н),
2-амино-4-(2-фторфенил)-6-фенилхинолин-3-карбонитрил получали в виде твердого вещества (72 мг, 12%) при взаимодействии 2-фторфенилбороновой кислоты и 2-амино-4-бром-6-фенилхинолин-3-карбонитрила, МС: m/е 339,8 (М++Н),
2-амино-4-фенил-6-трифторметилхинолин-3-карбонитрил получали в виде твердого вещества (47 мг, 6%) при взаимодействии фенилбороновой кислоты и 2-амино-4-бром-6-трифторметилхинолин-3-карбонитрила, МС: m/e 313,8 (M++Н),
2-амино-4-(2-метоксифенил)хинолин-3-карбонитрил получали в виде твердого вещества (35 мг, 5%) из 2-метоксифенилбороновой кислоты, МС: m/e 275,5 (М++Н),
2-амино-4-(2,4-дихлорфенил)хинолин-3-карбонитрил получали в виде твердого вещества (8 мг, 2,4%) из 2,4-дихлорфенилбороновой кислоты, МС: m/e 314,0 (М++Н),
2-амино-4-(2-хлорфенил)хинолин-3-карбонитрил получали в виде твердого вещества (61 мг, 11%) из 2-хлорфенилбороновой кислоты, МС: m/e 279,9 (M++Н),
2-амино-4-(4-хлорфенил)хинолин-3-карбонитрил получали в виде твердого вещества (52 мг, 9%) из 4-хлорфенилбороновой кислоты, МС: m/e 279,9 (М++Н).
Пример 25
Синтез 3-аминометил-4-арилхинолин-2-иламинов (схема II, способ 5)
3-Аминометил-4-паратолилхинолин-2-иламин
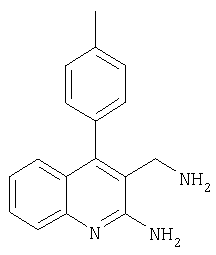
К суспензии LiAlH4 (67,3 мг, 1,77 ммоля) в ТГФ (1 мл) в атмосфере аргона медленно добавляли раствор 2-амино-4-паратолилхинолин-3-карбонитрила (46 мг, 0,177 ммоля) в ТГФ (0,5 мл) и смесь перемешивали при 40°С в течение 2 ч. Затем смесь охлаждали до -20°С, добавляли 0,3 мл воды и перемешивали при КТ течение 15 мин. Смесь переносили в этилацетат и фильтровали через декалит. Фильтрат промывали водой и солевым раствором, сушили (Na2SO4) и упаривали. Остаток растворяли в 1 мл ДМФА и очищали с использованием автоматихированной системы для препаративной ЖХВР (колонка YMC CombiPrep C18, 50×20 мм, элюент: градиент СН3CN/вода + 0,1% ТФУ, от 5 до 95%, скорость элюирования 40 мл/мин, время 6,0 мин, (230 нм), при этом получали 5 мг (11%) указанного в заголовке соединения в виде твердого вещества.
Пример 26
3-Аминометил-6-хлор-4-(2-фторфенил)хинолин-2-иламин
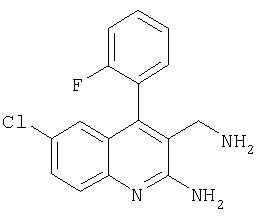
Указанное в заголовке соединение получали в виде твердого вещества (4 мг, 8%) из 2-амино-6-хлор-4-(2-фторфенил)хинолин-3-карбонитрила аналогично тому, как описано в примере 25. МС: m/е 302,0 (М++Н).
Пример 27
3-Аминометил-6-хлор-4-фенилхинолин-2-иламин
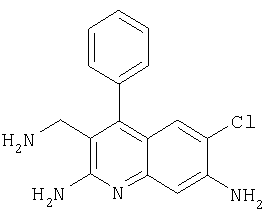
Указанное в заголовке соединение получали в виде твердого вещества (4 мг, 7%) из 2-амино-6-хлор-4-фенилхинолин-3-карбонитрила аналогично тому, как описано в примере 25. МС: m/е 283,1 (М++Н).
Пример 28
3-Аминометил-6-хлор-4-(2-хлорфенил)хинолин-2-иламин
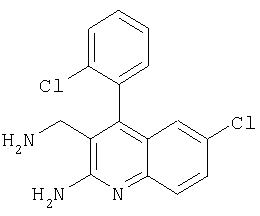
Указанное в заголовке соединение получали в виде твердого вещества (3 мг, 10%) из 2-амино-6-хлор-4-(2-хлорфенил)хинолин-3-карбонитрила аналогично тому, как описано в примере 25. МС: m/е 316,9 (М++Н).
Пример 29
3-Аминометил-4-фенил-6-трифторметилхинолин-2-иламин
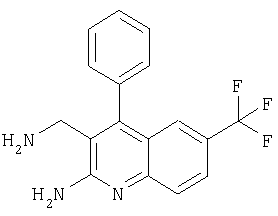
Указанное в заголовке соединение получали в виде твердого вещества (4 мг, 9%) из 2-амино-4-фенил-6-трифторметилхинолин-3-карбонитрила аналогично тому, как описано в примере 25. МС: m/е 317,3 (М++Н).
Пример 30
3-Аминометал-4-(2-метоксифенил)хинолин-2-иламин
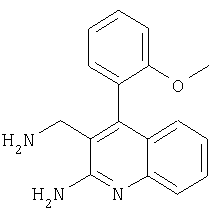
Указанное в заголовке соединение получали в виде твердого вещества (1 мг, 2%) из 2-амино-4-(2-метоксифенил)хинолин-3-карбонитрила аналогично тому, как описано в примере 25. МС: m/е 279,1 (М++Н).
Пример 31
3-Аминометил-4-(2,4-дихлорфенил)хинолин-2-иламин
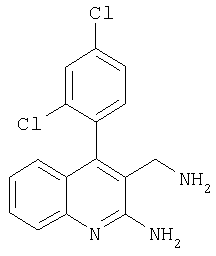
Указанное в заголовке соединение получали в виде твердого вещества (6 мг, 14%) из 2-амино-4-(2,4-дихлорфенил)хинолин-3-карбонитрила аналогично тому, как описано в примере 25. МС: m/е 317,1 (М++Н).
Пример 32
3-Аминометил-4-(2-хлорфенил)хинолин-2-иламин
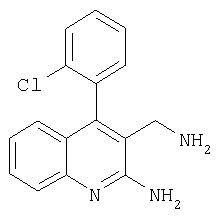
Указанное в заголовке соединение получали в виде твердого вещества (3 мг, 2%) из 2-амино-4-(2-хлорфенил)хинолин-3-карбонитрила аналогично тому, как описано в примере 25. МС: m/е 284,0 (М++Н).
Пример 33
3-Аминометил-4-(4-хлорфенил)хинолин-2-иламин
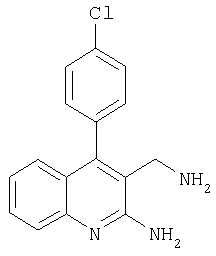
Указанное в заголовке соединение получали в виде твердого вещества (2 мг, 6%) из 2-амино-4-(4-хлорфенил)хинолин-3-карбонитрила аналогично тому, как описано в примере 25. МС: m/е 284,0 (М++Н).
Пример 34
3-Аминометил-4-фенилхинолин-2-иламин
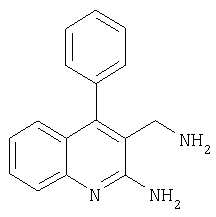
Указанное в заголовке соединение получали в виде твердого вещества светло-желтого цвета (0,56 г, 12%) из 2-амино-4-фенилбензопиридин-3-карбонитрила аналогично тому, как описано в примере 3. tfp.225-226°C
Примеры галеновых препаратов
Пример А
Таблетки с покрытием следующего состава получают стандартным способом:
Активное соединение просеивали и смешивали с микрокристаллической целлюлозой, затем смесь гранулировали в смеси с раствором поливинилпирролидона в воде. Гранулят смешивали с натрий гликолятом крахмала и стеаратом магния, прессовали для образования ядер таблеток массой 120 или 350 мг соответственно. Ядра покрывали водным раствором/суспензией указанного состава.
Пример Б
Капсулы следующего состава получают стандартным способом:
Компоненты просеивали, смешивали и смесью заполняли капсулы размера 2.
Пример В
Растворы для инъекций следующего состава получают стандартным способом:
Активный компонент растворяли в смеси полиэтиленгликоля 400 и порции воды для инъекции. Добавляли уксусную кислоту до рН 5,0 и доводили до 1,0 мл добавлением остального количества воды. Раствор фильтровали, разливали во флаконы и стерилизовали.
Пример Г
Мягкие желатиновые капсулы следующего состава получают стандартным способом:
Состав капсулы, мг:
Желатиновая капсула:
Активный компонент растворяли в теплой расплавленной смеси других ингредиентов и смесь разливали в мягкие желатиновые капсулы пригодного размера. Заполненные мягкие желатиновые капсулы обрабатывали стандартным способом.
Пример Д
Пакетики следующего состава получают стандартным способом, мг:
Активный компонент смешивали с лактозой, микрокристаллической целлюлозой и натриевой солью карбоксиметилцеллюлозы, гранулировали в смеси с раствором поливинилпирролидона в воде. Гранулят смешивали со стеаратом магния и ароматизаторами, а затем расфасовывали в пакетики.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ПИРИДИНА И ПИРИМИДИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ), ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ПРИМЕНЕНИЕ | 2003 |
|
RU2293731C2 |
| МОДУЛЯТОРЫ АДЕНОЗИНОВЫХ РЕЦЕПТОРОВ | 2001 |
|
RU2277911C2 |
| ПРОИЗВОДНЫЕ ПИРИДО(2,1-А)ИЗОХИНОЛИНА В КАЧЕСТВЕ ИНГИБИТОРОВ DPP-IV | 2002 |
|
RU2297417C2 |
| ПРОИЗВОДНЫЕ АЗАБИЦИКЛООКТАНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ ДИПЕПТИДИЛПЕПТИДАЗЫ IV | 2007 |
|
RU2447063C2 |
| ИНГИБИТОРЫ JAK | 2010 |
|
RU2538204C2 |
| N-ГИДРОКСИ-БЕНЗАМИДЫ ДЛЯ ЛЕЧЕНИЯ РАКА | 2011 |
|
RU2577861C2 |
| ПРОИЗВОДНЫЕ БЕНЗОТИАЗОЛА | 2001 |
|
RU2251419C2 |
| ПРОИЗВОДНЫЕ ДИЦИКЛОАЗААЛКАНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ В МЕДИЦИНЕ | 2008 |
|
RU2487866C2 |
| 5-ЧЛЕННОЕ ГЕТЕРОЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ И ЕГО ПРИМЕНЕНИЕ ДЛЯ ЛЕКАРСТВЕННЫХ ЦЕЛЕЙ | 2008 |
|
RU2515968C2 |
| ПРОИЗВОДНЫЕ ЦИКЛОАЛКИЛАМИНА | 2005 |
|
RU2402526C2 |
Описываются соединения формулы (I)
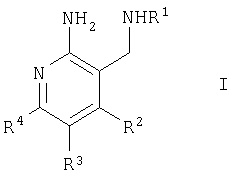
где R1 означает водород; R2 означает фенил или фенил, независимо моно-, дизамещенный группой галоген, (низш.)алкил, (низш.)алкокси, перфтор(низш.)алкил; R3 и R4 вместе с атомами углерода, к которым они присоединены, образуют фенил, необязательно и независимо моно-, ди- или тризамещенный галогеном, или перфтор(низш.)алкилом, или образуют 5-, 6- или 7-членный насыщенный цикл, необязательно содержащий гетероатом, выбранный из О и S, и необязательно и независимо монозамещенный (низш.)алкилом, причем указанный насыщенный цикл конденсирован в ортоположении с 5-членным ароматическим циклом, необязательно содержащим S в качестве гетероатома, или с фенилом, необязательно и независимо моно-, дизамещенный группой галоген, (низш.)алкил, перфтор(низш.)алкил или (низш.)алкокси, и их фармацевтически приемлемые соли. Описывается также способ получения соединений, фармацевтическая композиция и применение соединений для лечения и/или профилактики заболеваний, ассоциированных с DPP-IV. Соединения используются для лечения таких заболеваний, как диабет, прежде всего инсулиннезависимый сахарный диабет, и нарушенная толерантность к глюкозе. 4 н. и 12 з.п. ф-лы, 1 табл.
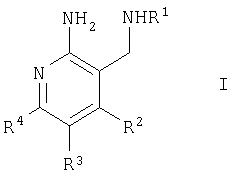
где R1 означает водород;
R2 означает незамещенный фенил или фенил, независимо моно- или дизамещенный группой галоген, (низш.)алкил, (низш.)алкокси, перфтор(низш.)алкил;
R3 и R4 вместе с атомами углерода, к которым они присоединены, образуют фенил, необязательно и независимо моно-, ди- или тризамещенный галогеном, или перфтор(низш.)алкилом, либо образуют 5-, 6- или 7-членный насыщенный цикл, необязательно содержащий гетероатом, выбранный из О и S, и необязательно и независимо монозамещенный (низш.)алкилом, причем указанный насыщенный цикл конденсирован в орто-положении с 5-членным ароматическим циклом, необязательно содержащим S в качестве гетероатома, или с фенилом, необязательно и независимо моно-, ди-замещенный группой галоген, (низш.)алкил, перфтор(низш.)алкил или (низш.)алкокси,
и их фармацевтически приемлемые соли.
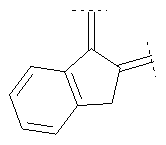
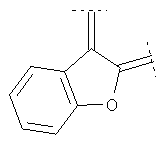
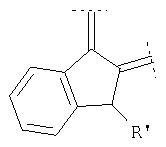
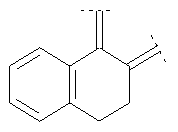
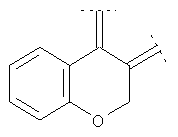
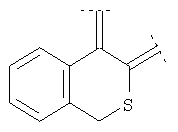
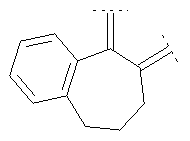
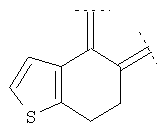
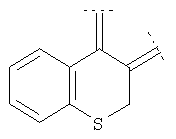
где фенильный остаток необязательно и независимо моно-, дизамещен группой галоген, (низш.)алкил, перфтор(низш.)алкил или (низш.)алкокси, а R' означает (низш.)алкил.




где фенильный остаток необязательно и независимо моно-, дизамещен группой галоген, (низш.)алкил, перфтор(низш.)алкил или (низш.)алкокси, а R' означает (низш.)алкил.
3-аминометил-4-(2,4-дихлорфенил)-5,6-дигидробензо[h]хинолин-2-иламин,
3-аминометил-4-(2,4-дихлорфенил)-5Н-индено[1,2-b]пиридин-2-иламин,
3-аминометил-4-(2,4-дихлорфенил)-6,7-дигидро-5Н-бензо[6,7]циклогепта[1,2-b]пиридин-2-иламин,
3-аминометил-4-(2,4-дихлорфенил)-7-метокси-5Н-индено[1,2-b]пиридин-2-иламин,
3-аминометил-4-(2,4-дихлорфенил)-7,8-диметокси-5Н-индено[1,2-b]пиридин-2-иламин,
3-аминометил-4-(2,4-дихлорфенил)бензо[4,5]фуро[3,2-b]пиридин-2-иламин,
2-аминометил-1-(2,4-дихлорфенил)-10Н-9-окса-4-азафенантрен-3-иламин,
3-аминометил-4-(2,4-дихлорфенил)-5,6-дигидротиено[2,3-b]хинолин-2-иламин,
2-аминометил-1-(2,4-дихлорфенил)-6-фтор-10Н-9-окса-4-азафенантрен-3-иламин,
2-аминометил-1-(2,4-дихлорфенил)-10Н-9-тиа-4-азафенантрен-3-иламин,
3-аминометил-4-(2,4-дихлорфенил)-5-метил-5Н-индено[1,2-b]пиридин-2-иламин,
2-аминометил-1-(2,4-дихлорфенил)-9Н-10-тиа-4-азафенантрен-3-иламин,
3-аминометил-4-(2,4-дихлорфенил)-10-фтор-6,7-дигидро-5Н-бензо[6,7]циклогепта[1,2-b]пиридин-2-иламин,
2-аминометил-1-(2,4-дихлорфенил)-10Н-9-тиа-4-азафенантрен-3-иламин,
3-аминометил-4-(2,4-дихлорфенил)-5-метил-5Н-индено[1,2-b]пиридин-2-иламин,
2-аминометил-1-(2,4-дихлорфенил)-9Н-10-тиа-4-азафенантрен-3-иламин,
3-аминометил-4-(2,4-дихлорфенил)-10-фтор-6,7-дигидро-5Н-бензо[6,7]циклогепта[1,2-b]пиридин-2-иламин,
3-аминометил-4-(2,4-дихлорфенил)-7-фтор-5Н-индено[1,2-b]пиридин-2-иламин,
3-аминометил-4-(2,4-дихлорфенил)-8-метил-5Н-индено[1,2-b]пиридин-2-иламин,
3-аминометил-4-(2,4-дихлорфенил)-9-метокси-5,6-дигидро-бензо[b]хинолин-2-иламин,
2-аминометил-6-хлор-1-(2,4-дихлорфенил)-10Н-9-тиа-4-азафенантрен-3-иламин,
3-аминометил-4-(2,4-дихлорфенил)-7,9-диметил-5,6-дигидро-бензо[b]хинолин-2-иламин,
2-аминометил-1-(2,4-дихлорфенил)-6-метил-10Н-9-окса-4-азафенантрен-3-иламин,
3-аминометил-7-бром-4-(2,4-дихлорфенил)-5Н-индено[1,2-b]пиридин-2-иламин,
3-аминометил-4-пара-толилхинолин-2-иламин,
3-аминометил-6-хлор-4-(2-фторфенил)хинолин-2-иламин,
3-аминометил-6-хлор-4-фенилхинолин-2-иламин,
3-аминометил-6-хлор-4-(2-хлорфенил)хинолин-2-иламин,
3-аминометил-4-фенил-6-трифторметилхинолин-2-иламин,
3-аминометил-4-(2-метоксифенил)хинолин-2-иламин,
3-аминометил-4-(2,4-дихлорфенил)хинолин-2-иламин,
3-аминометил-4-(2-хлорфенил)хинолин-2-иламин,
3-аминометил-4-(4-хлорфенил)хинолин-2-иламин,
3-аминометил-4-фенилхинолин-2-иламин,
и их фармацевтически приемлемые соли.
(а) восстановление нитрила формулы
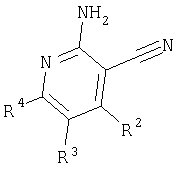
где R2, R3 и R4 имеют значения, указанные в пп.1-11, с образованием амина формулы
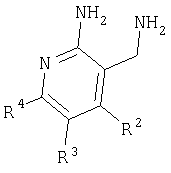
где R2, R3 и R4 имеют значения, указанные в пп.1-11, или (б) алкилирование амина формулы

где R2, R3 и R4 имеют значения, указанные в пп.1-11, с обазованием соединения формулы
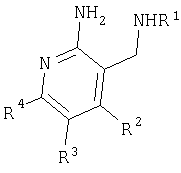
где R1, R2, R3 и R4 имеют значения, указанные в пп.1-11.
| Машина для изготовления дратвы | 1932 |
|
SU33839A1 |
| Способ прокатки | 1983 |
|
SU1088818A1 |
| СПОСОБ ПОЛУЧЕНИЯ N-AЛKИЛЗAMEШ,EHHЫX 1,2,3,4,5б,9б-ГЕКСАГИДРО-5Н-ИНДЕИО-[1,2-й]-ПИРИДИНОВ | 0 |
|
SU327193A1 |
Авторы
Даты
2006-10-20—Публикация
2003-02-05—Подача