Область техники, к которой относится изобретение
Настоящее изобретение относится к 5-членным гетероциклическим соединениям, применимым в качестве лекарственных средств.
Более конкретно, настоящее изобретение относится к 5-членным гетероциклическим соединениям, обладающим ингибирующим ксантиноксидазу активностью и применимым в качестве агентов для профилактики или лечения заболевания, связанного с отклонением от нормы уровня мочевой кислоты в сыворотке, их пролекарствам или фармацевтически приемлемым солям.
Уровень техники
Мочевая кислота является конечным продуктом метаболизма пурина в организме человека. У многих млекопитающих, в отличие от человека, мочевая кислота дополнительно разрушается уратоксидазой (уриказой) в печени, превращаясь в аллантоин, который экскретируется через почки. У людей основным путем экскреции мочевой кислоты являются почки, в которых приблизительно две трети мочевой кислоты экскретируется в моче. Остальная часть экскретируется в испражнениях. Когда имеет место избыточное продуцирование или пониженная экскреция мочевой кислоты, появляется гиперурикемия. Гиперурикемию классифицируют на тип избыточного продуцирования мочевой кислоты, тип недостаточной экскреции мочевой кислоты и их смешанный тип. Эта классификация гиперурикемии является клинически важной. С целью снижения отрицательных действий терапевтических агентов, терапевтические агенты выбирают согласно каждому классу (см., например, непатентную ссылку 1).
При гиперурикемии типа избыточного продуцирования мочевой кислоты мочевыделение мочевой кислоты увеличивается и, когда мочевыделение мочевой кислоты дополнительно увеличивается в результате применения лекарственного средства, способствующего выведению мочевой кислоты, возможным является развитие осложнения, проявляющегося в образовании мочевых конкрементов. Поэтому, по существу, аллопуринол, ингибитор продуцирования мочевой кислоты (или иногда называемый ингибитором синтеза мочевой кислоты, далее называемый “ингибитором продуцирования мочевой кислоты”), применяют при гиперурикемии типа избыточного продуцирования мочевой кислоты.
Мочевая кислота образуется из пуриновых веществ, которые происходят из пищевых продуктов и синтезируются эндогенно, и наконец, окислением ксантина ксантиноксидазой. Аллопуринол разработан в качестве ингибитора ксантиноксидазы и является единственным ингибитором продуцирования мочевой кислоты, применяемого в медицинской практике. Однако, хотя описано, что аллопуринол является эффективным при гиперурикемии и различных заболеваниях, вызванных теми же самыми причинами, описаны также (см., например, непатентную ссылку 2) серьезные отрицательные действия, такие как синдром отравления (аллергический васкулит), синдром Стевенса-Джонсона, эксфолиативный дерматит, анапластическая анемия, дисфункция печени и тому подобное (см., например, непатентную ссылку 2). В качестве одной из причин этого указывается, что аллопуринол имеет структуру, подобную нуклеиновой кислоте, и ингибирует путь метаболизма пиримидина (см., например, непатентную ссылку 3).
С другой стороны, при гиперурикемии типа недостаточной экскреции мочевой кислоты, экскреция мочевой кислоты снижается. Было описано, что когда применяют аллопуринол, который метаболизируется в оксипуринол, который экскретируется через почки таким же механизмом в мочевую кислоту, экскреция оксипуринола также уменьшается и это увеличивает частоту заболеваний печени (см., например, непатентную ссылку 4). Поэтому, по существу, лекарственные средства, способствующие выведению мочевой кислоты, такие как пробеницид, бензбромарон и тому подобное, применяют при гиперурикемии типа недостаточной экскреции мочевой кислоты. Однако эти лекарственные средства, способствующие выведению мочевой кислоты, также обнаруживают отрицательные действия, такие как желудочно-кишечные нарушения, мочевые конкременты или тому подобное. В частности, бензбромарон известен как возможно вызывающий фульминантный гепатит в случае идиосинкразических пациентов (см., например, непатентную ссылку 5).
Таким образом, показано, что как существующий ингибитор продуцирования мочевой кислоты, так и лекарственное средство, способствующее выведению мочевой кислоты, имеют ограничения при применении для пациентов или серьезные отрицательные действия. Поэтому желательным является разработка легкого для применения агента для лечения гиперурикемии.
Мочевая кислота в основном экскретируется почками, и динамики образования уратов в почках исследовали до сих пор в нескольких экспериментах с применением везикул мембран каемчатого эпителия (BBMV), полученных из коркового вещества почки (см., например, непатентные ссылки 6 и 7). Известно, что у человека мочевая кислота свободно проходит через клубочки почек, и имеются механизмы реабсорбции и секреции мочевой кислоты в проксимальном почечном канальце (см., например, непатентную ссылку 8).
В последние годы был идентифицирован ген (SLC22A12), кодирующий переносчик урата почек человека (см., например, непатентную ссылку 9). Переносчик, кодированный этим геном (переносчик 1 урата, в дальнейшем обозначаемый “УРАТ1”), является молекулой 12-трансмембранного типа, относящейся к семейству ОАТ. мРНК УРАТ1 специфически экспрессируется в почке, и локализацию УРАТ1 в апикальной стороне проксимального почечного канальца наблюдали на разрезе ткани почки человека. В эксперименте с применением системы экспрессии овоцита xenopus было показано поглощение мочевой кислоты посредством УРАТ1. Кроме того, было показано, что поглощение мочевой кислоты происходит посредством обмена с органическими анионами, такими как анионы молочной кислоты, пиразинкарбоновой кислоты (PZA), никотиновой кислоты и тому подобное, и поглощение мочевой кислоты посредством УРАТ1 ингибируется лекарственными средствами, способствующими выведению мочевой кислоты, пробенецидом и бензбромароном. Таким образом, как и ожидалось в эксперименте с применением мембранных везикул, было сделано убедительное предположение, что УРАТ1 является ионообменником урат/анион. То есть было показано, что УРАТ1 является переносчиком, который играет важную роль в реабсорбции мочевой кислоты в почке (см., например, непатентную ссылку 9).
Кроме того, становится ясной связь между URAT1 и заболеваниями. Идиопатическая почечная гипоурикемия является заболеванием, при котором экскреция мочевой кислоты повышается вследствие аномальных динамик урата в почке и уровень мочевой кислоты в сыворотке становится низким. Известно, что заболевание часто ассоциировано с мочевым конкрементом или острой почечной недостаточностью после физической нагрузки. Ген URAT1 был идентифицирован как ген, вызывающий почечную гипоурекимию (см, например, непатентную ссылку 9). Эти факты убедительно позволяют предположить, что URAT1 является ответственным за регулирование уровня мочевой кислоты в крови.
Следовательно, вещество, обладающее ингибирующей URAT1 активностью, является применимым в качестве агента для лечения или профилактики заболеваний, связанных с высокими уровнями мочевой кислоты в крови, т.е. гиперурикемии, подагрических узлов, подагрического артрита, почечного заболевания, связанного с гиперурикемией, мочевых конкрементов или тому подобное.
Описано, что при лечении гиперурикемии применение комбинации аллопуринола, ингибитора продуцирования мочевой кислоты, и агента, обладающего активностью по выведению мочевой кислоты из организма, снижает уровень мочевой кислоты в сыворотке сильнее, чем применение только одного аллопуринола (см., например, непатентные ссылки 10 и 11). Поэтому, когда лечение только одним существующим агентом не может оказывать достаточное действие, более сильное терапевтическое действие можно ожидать при применении комбинации ингибитора продуцирования мочевой кислоты и агента, способствующего выведению мочевой кислоты из организма. Кроме того, в случае гиперурикемии типа недостаточной экскреции мочевой кислоты считается, что поскольку мочевыделение мочевой кислоты можно уменьшить снижением уровня мочевой кислоты в крови, риск образования мочевых конкрементов, вызванных монотерапией агентом, способствующим выведению мочевой кислоты из организма, может быть снижен. Кроме того, предполагается сильное терапевтическое действие в случае гиперурикемии смешанного типа. Поэтому предполагается, что агент, обладающий как ингибирующей активностью в отношении продицирования мочевой кислоты, так и активностью, способствующей выведению мочевой кислоты из организма, станет в высшей степени пригодным агентом для профилактики или лечения гиперурикемии или тому подобное.
В качестве соединения, обладающего как ингибирующей ксантиноксидазу активностью, так и ингибирующей URAT1 активностью, известен морин, природный продукт (см. непатентную ссылку 12). Кроме того, в качестве соединения, обладающего активностью, способствующей выведению мочевой кислоты из организма, известны также соединения биарилы и диариловые простые эфиры (см. патентную ссылку 1).
В качестве 1-фенилзамещенных 5-членных гетероциклических соединений известны производные 1-фенилпиррола и производные 1-фенилпиразола (см., например, патентные ссылки 2 и 3). Однако, в любой из этих ссылок 5-членное гетероциклическое соединение настоящего изобретения конкретно не описано и ничего не указано, не предположено относительно того, что оно обладает ингибирующей ксантиноксидазу активностью или является применимым для профилактики или лечения заболевания, связанного с аномальным уровнем мочевой кислоты в сыворотке, такого как подагра, гиперурикемия или тому подобное.
Патентная ссылка 1: Tokkai 2000-001431 (JPA2000-001431).
Патентная ссылка 2: Международная публикация проспекта 2006/012642.
Патентная ссылка 3: Международная публикация проспекта 2006/021462.
Непатентная ссылка 1: Atsuo Taniguchi and 1 person, Modern Physician, 2004, Vol.24, No.8, pp.1309-1312.
Непатентная ссылка 2: Kazuhide Ogino and 2 persons, Nihon Rinsho (Japan Clinical), 2003, Vol.61, Extra edition 1, pp.197-201.
Непатентная ссылка 3: Hideki Horiuchi and 6 persons, Life Science, 2000, Vol.66, No.21, pp.2051-2070.
Непатентная ссылка 4: Hisashi Yamanaka and 2 persons, Konyosankessyo to Tsufu (Hyperuricemia and gout), issued by Medical Review Co., 1994, Vol.2, No.1, pp.103-111.
Непатентная ссылка 5: edited by Konyosankessyo, tsufu no Chiryo guideline sakuseiiinkai (The Committee establishing a guideline for the treatment of hyperuricemia and gout), The guideline for the treatment of hyperuricemia и gout, Edition 1, issued by Nihon tsuhu kakusan taisya gakkai (Japanese society of gout и nucleic acid metabolism), 2002, pp.32-33.
Непатентная ссылка 6: Francoise Roch-Ramel and 2 persons, Am. J. Physiol., 1994, Vol. 266 (Renal Fluid Electrolyte Physiol., Vol.35), F797-F805.
Непатентная ссылка 7: Francoise Roch-Ramel and 2 persons, J. Pharmacol. Exp. Ther., 1997, Vol. 280, pp.839-845.
Непатентная ссылка 8: Hiroaki Kimura and 3 persons, Nihon rinsyo (Japan Clinical), 2003, Vol. 61, Extra Edition 1, pp.119-123.
Непатентная ссылка 9: Atsushi Enomoto and 18 persons, Nature, 2002, Vol.417, pp.447-452.
Непатентная ссылка 10: S Takahashi and 5 persons, Ann. Rheum. Dis., 2003, Vol. 62, pp.572-575.
Непатентная ссылка 11: M. D. Feher and 4 persons, Rheumatology, 2003, Vol.42, pp.321-325.
Непатентная ссылка 12: Zhifeng Yu and 2 persons, J. Pharmacol. Exp. Ther., 2006, Vol.316, pp.169-175.
Описание изобретения
Проблема, которая должна быть решена изобретением
Настоящее изобретение относится к агенту, который обладает ингибирующей активностью в отношении продуцирования мочевой кислоты и применим для профилактики или лечения заболевания, связанного с аномальным уровнем мочевой кислоты в сыворотке.
Способ решения проблемы
Авторы настоящего изобретения убедительно решили указанную выше проблему. В результате этого было обнаружено, что 5-членные гетероциклические соединения, представленные нижеследующей общей формулой (I), проявляют превосходную ингибирующую ксантиноксидазу активностью и очень эффективно снижают уровни мочевой кислоты в сыворотке, и поэтому они могут быть агентами для профилактики или лечения заболеваний, связанных с аномальным уровнем мочевой кислоты в сыворотке, таким образом образуется основа настоящего изобретения.
То есть настоящее изобретение относится к
[1] 5-членному гетероциклическому соединению, представленному общей формулой (I)
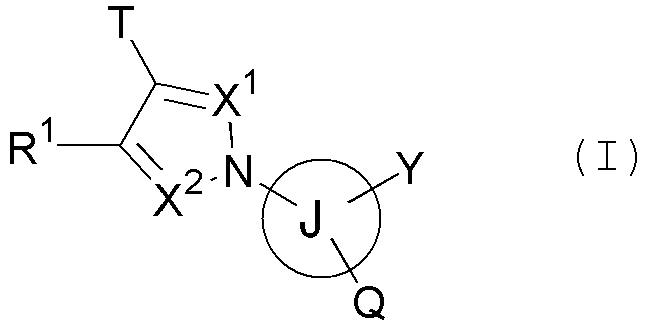
где
Т представляет собой нитро, циано, трифторметил или атом галогена;
кольцо J представляет собой кольцо арила или кольцо гетероарила;
Q представляет собой карбокси, низший алкоксикарбонил, карбамоил, моно(ди)(низший алкил)карбамоил, сульфо, сульфамоил или 5-тетразолил;
Х1 и Х2 независимо представляют собой CR2 или N, при условии, что оба из Х1 и Х2 одновременно не представляют собой N и, когда присутствуют два или более R2, эти R2 необязательно являются одинаковыми или отличными друг от друга;
R2 представляет собой атом водорода или необязательно замещенный низший алкил;
Y представляет собой атом водорода, гидрокси, амино, атом галогена, перфтор(низший алкил), необязательно замещенный низший алкил, необязательно замещенный низший алкокси, нитро, (низший алкил)карбониламино или (низший алкил)сульфониламино, при условии, что два или более Y присутствуют на кольце J необязательно, и эти Y необязательно являются одинаковыми или отличными друг от друга;
R1 представляет собой циано, перфтор(низший алкил), -AA, -A-D-L-M, -A-D-E-G-L-M или -N(-D-L-M)2, при условии, что два (-D-L-M) являются необязательно отличными друг от друга;
в формуле AA представляет собой атом водорода, тиол, -CHO, карбокси, -CONHR3, амино, -N(R3)CHO, -N=CR3NHR4, -COCOOH, -COCONHR3, -SO2NHR3, -N(R3)CONHR4 или -N(R3)SO2NHR4;
A представляет собой простую связь, -O-, -S-, -CO-, -COO-, -CON(R3)-, -SO2-, -NH-, -N(R3)CO-, -N(R3)COO-, -N(R3)SO2-, -N=CR3N(R4)-, -COCOO-, -COCON(R3)-, -SO2N(R3)-, -N(R3)CON(R4)- или -N(R3)SO2N(R4)-, где R3 и R4 независимо представляют собой атом водорода или низший алкил;
D представляет собой необязательно замещенный низший алкилен, необязательно замещенный низший алкенилен, необязательно замещенный низший алкинилен, необязательно замещенный циклоалкилен, необязательно замещенный гетероциклоалкилен, необязательно замещенный арилен или необязательно замещенный гетероарилен, при условии, что D необязательно дополнительно замещен -L-M или -E-G-L-M;
E представляет собой простую связь, -O-, -S-, -CO-, -COO-, -CON(R5)-, -SO2-, -N(R5)-, -N(R5)CO-, -N(R5)COO-, -N(R5)SO2-, -OCON(R5)-, -OCOO-, -COCOO-, -COCON(R5)-, -SO2N(R5)-, -N(R5)CON(R6)- или -N(R5)SO2N(R6)-, где R5 и R6 независимо представляют собой атом водорода или низший алкил;
G представляет собой необязательно замещенный низший алкилен, необязательно замещенный низший алкенилен, необязательно замещенный низший алкинилен, необязательно замещенный циклоалкилен, необязательно замещенный гетероциклоалкилен, необязательно замещенный арилен или необязательно замещенный гетероарилен;
L представляет собой простую связь, -O-, -S-, -CO-, -COO-, -CON(R8)-, -SO2-, -N(R8)-, -N(R8)CO-, -N(R8)COO-, -N(R8)SO2-, -OCO-, -OCON(R8)-, -OCOO-, -COCOO-, -COCON(R8)-, -SO2N(R8)-, -N(R8)CON(R9)- или -N(R8)SO2N(R9)-, где R8 и R9 независимо представляют собой атом водорода или низший алкил и
M представляет собой атом водорода, необязательно замещенный низший алкил, необязательно замещенный низший алкенил, необязательно замещенный низший алкинил, необязательно замещенный циклоалкил(низший алкил), необязательно замещенный гетероциклоалкил(низший алкил), необязательно замещенный арил(низший алкил), необязательно замещенный гетероарил(низший алкил), необязательно замещенный циклоалкил, необязательно замещенный гетероциклоалкил, необязательно замещенный арил или необязательно замещенный гетероарил при условии, что, когда M представляет собой атом водорода, L представляет собой простую связь, -O-, -S-, -CO-, -COO-, -CON(R8)-, -N(R8)-, -N(R8)CO-, -OCO-, -OCON(R8)-, -COCOO-, -COCON(R8)-, -SO2N(R8)-, -N(R8)CON(R9)- или -N(R8)SO2N(R9)-; при условии, что, когда присутствуют R1 и R2, связанные с соседними атомами, эти R1 и R2 необязательно связываются вместе с образованием кольца; соответственно; или его пролекарству или его фармацевтически приемлемой соли;
[2] 5-членному гетероциклическому соединению, описываемому выше в [1], где Y представляет собой атом водорода, гидрокси, амино, атом галогена, перфтор(низший алкил), необязательно замещенный низший алкил или необязательно замещенный низший алкокси, при условии, что на кольце J необязательно присутствую два или более Y и эти Y необязательно являются одинаковыми или отличными друг от друга, или его пролекарству или его фармацевтически приемлемой соли;
[3] 5-членному гетероциклическому соединению, описываемому выше в [2], где
Т представляет собой нитро, циано или трифторметил;
Q представляет собой карбокси, карбамоил или 5-тетразолил;
Y представляет собой атом водорода, гидрокси, амино, атом галогена, перфтор(низший алкил), необязательно замещенный низший алкил или низший алкокси, который необязательно имеет 1-3 одинаковых или разных заместителя, выбранные из группы, состоящей из атома фтора, гидрокси и амино, при условии, что два или более Y необязательно присутствуют на кольце J и эти Y необязательно являются одинаковыми или отличными друг от друга;
R1 представляет собой перфтор(низший алкил), -AA, -A-D-L-M, -A-D-E-G-L-M или -N(-D-L-M)2, при условии, что два (-D-L-M) необязательно являются отличными друг от друга;
в формуле AA представляет собой тиол, -CHO, -CONHR3, амино, -N(R3)CHO, -N=C(R3)NHR4, -COCOOH, -COCONHR3, -SO2NHR3, -N(R3)CONHR4 или -N(R3)SO2NHR4;
A представляет собой простую связь, -O-, -S-, -CO-, -CON(R3)-, -SO2-, -NH-, -N(R3)CO-, -N(R3)COO-, -N(R3)SO2-, -N=CR3N(R4)-, -COCOO-, -COCON(R3)-, -SO2N(R3)-, -N(R3)CON(R4)- или -N(R3)SO2N(R4)-, где R3 и R4 независимо представляют собой атом водорода или низший алкил;
D представляет собой необязательно замещенный низший алкилен, необязательно замещенный низший алкенилен, необязательно замещенный низший алкинилен, необязательно замещенный циклоалкилен, необязательно замещенный гетероциклоалкилен, необязательно замещенный арилен или необязательно замещенный гетероарилен, при условии, что D необязательно дополнительно замещен -L-M или -E-G-L-M;
E представляет собой простую связь, -O-, -S-, -CO-, -COO-, -CON(R5)-, -SO2-, -N(R5)-, -N(R5)CO-, -N(R5)COO-, -N(R5)SO2-, -OCON(R5)-, -OCOO-, -COCOO-, -COCON(R5)-, -SO2N(R5)-, -N(R5)CON(R6)- или -N(R5)SO2N(R6)-, где R5 и R6 независимо представляют собой атом водорода или низший алкил;
G представляет собой необязательно замещенный низший алкилен, необязательно замещенный низший алкенилен, необязательно замещенный низший алкинилен, необязательно замещенный циклоалкилен, необязательно замещенный гетероциклоалкилен, необязательно замещенный арилен или необязательно замещенный гетероарилен;
L представляет собой простую связь, -O-, -S-, -CO-, -COO-, -CON(R8)-, -SO2-, -N(R8)-, -N(R8)CO-, -N(R8)COO-, -N(R8)SO2-, -OCO-, -OCON(R8)-, -OCOO-, -COCOO-, -COCON(R8), -SO2N(R8)-, -N(R8)CON(R9)- или -N(R8)SO2N(R9)-, где R8 и R9 независимо представляют собой атом водорода или низший алкил; и
M представляет собой атом водорода, необязательно замещенный низший алкил, необязательно замещенный низший алкенил, необязательно замещенный низший алкинил, необязательно замещенный циклоалкил(низший алкил), необязательно замещенный гетероциклоалкил(низший алкил), необязательно замещенный арил(низший алкил), необязательно замещенный гетероарил(низший алкил), необязательно замещенный циклоалкил, необязательно замещенный гетероциклоалкил, необязательно замещенный арил или необязательно замещенный гетероарил, при условии, что когда M представляет собой атом водорода, L представляет собой простую связь, -O-, -S-, -CO-, -COO-, -CON(R8)-, -N(R8)-, -N(R8)CO-, -OCO-, -OCON(R8)-, -COCOO-, -COCON(R8)-, -SO2N(R8)-, -N(R8)CON(R9)- или -N(R8)SO2N(R9)-, при условии, что когда присутствуют R1 и R2, связанные с соседними атомами, эти R1 и R2 необязательно связываются вместе с образованием кольца, соответственно, или его пролекарству или его фармацевтически приемлемой соли;
[4] 5-членному гетероциклическому соединению, описываемому выше в [2] или [3], где X1 представляет собой N и X2 представляет собой CR11, где R11 представляет собой атом водорода или необязательно замещенный низший алкил, или его пролекарству или его фармацевтически приемлемой соли;
[5] 5-членному гетероциклическому соединению, описываемому выше в [2] или [3], где X1 представляет собой СН и X2 представляет собой N, или его пролекарству или его фармацевтически приемлемой соли;
[6] 5-членному гетероциклическому соединению, описываемому выше в [2] или [3], где X1 и Х2 независимо представляют собой CR11, где эти R11 являются необязательно отличными друг от друга и представляют собой атом водорода или необязательно замещенный низший алкил, или его пролекарству или его фармацевтически приемлемой соли;
[7] 5-членному гетероциклическому соединению, описываемому выше в [6], где X1 и Х2 представляют собой CH, или его пролекарству или его фармацевтически приемлемой соли;
[8] 5-членному гетероциклическому соединению, описываемому выше в любом из [1]-[7], где Т представляют собой циано, или его пролекарству или его фармацевтически приемлемой соли;
[9] 5-членному гетероциклическому соединению, описываемому выше в любом из [1]-[8], где Q представляют собой карбокси, или его пролекарству или его фармацевтически приемлемой соли;
[10] 5-членному гетероциклическому соединению, описываемому выше в [9], где группа, представленная общей формулой

является группой, представленной следующей общей формулой (IIa) или (IIb)
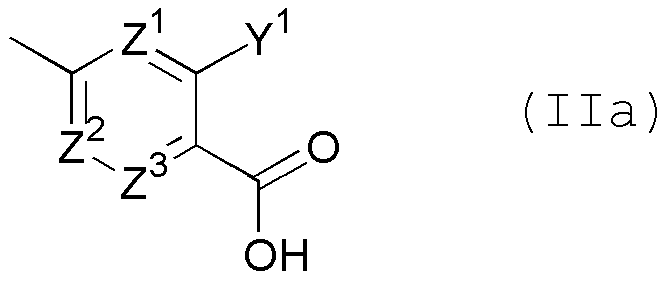
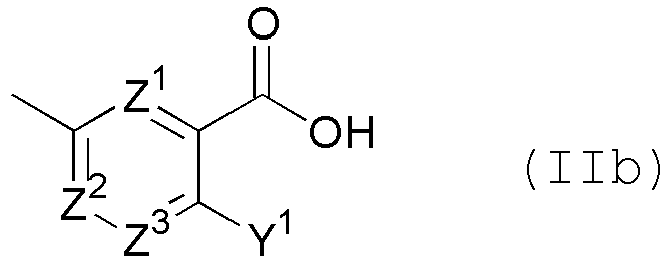
в формулах
Z1, Z2 и Z3 независимо представляют собой CR12 или N; и
Y1 и R12 независимо представляют собой атом водорода, гидрокси, амино, атом галогена, необязательно замещенный низший алкил или низший алкокси, который необязательно имеет 1-3 одинаковых или разных заместителей, выбранных из группы, состоящей из атома фтора, гидрокси и амино, при условии, что когда присутствуют два или более R12, эти R12 необязательно являются одинаковыми или отличными друг от друга, или его пролекарству или его фармацевтически приемлемой соли;
[11] 5-членному гетероциклическому соединению, описываемому выше в [10], где группа, представленная общей формулой (II), является группой, представленной общей формулой (IIa), где Z1, Z2 и Z3 независимо представляют собой CR13, где R13 представляет собой атом водорода или атом галогена, и Y1 представляет собой атом водорода, гидрокси или амино, или его пролекарству или его фармацевтически приемлемой соли;
[12] 5-членному гетероциклическому соединению, описываемому выше в [10], где группа, представленная общей формулой (II) является группой, представленной общей формулой (IIb), где Z1, Z2 и Z3 независимо представляют собой CR13, где R13 представляет собой атом водорода или атом галогена, и Y1 представляет собой атом водорода, гидрокси или амино, или его пролекарству или его фармацевтически приемлемой соли;
[13] 5-членному гетероциклическому соединению, описываемому выше в [10], где группа, представленная общей формулой (II), является группой, представленной общей формулой (IIa), где один из Z1 и Z2 представляет собой N, другой представляет собой СН; Z3 представляет собой CH и Y1 представляет собой атом водорода, гидрокси или амино, или его пролекарству или его фармацевтически приемлемой соли;
[14] 5-членному гетероциклическому соединению, описываемому выше в [10], где группа, представленная общей формулой (II), является группой, представленной общей формулой (IIb), где Z1 и Z3 независимо представляют собой CR13, где R13 представляет собой атом водорода или атом галогена; Z2 представляет собой N и Y1 представляет собой атом водорода, гидрокси или амино, или его пролекарству или его фармацевтически приемлемой соли;
[15] 5-членному гетероциклическому соединению, описываемому выше в [9], где кольцо J представляет собой 5-членное гетероарильное кольцо, имеющее 1-3 разных или одинаковых гетероатомов, выбранных из группы, состоящей из атома кислорода, атома азота и атома серы в кольце, или его пролекарству или его фармацевтически приемлемой соли;
[16] 5-членному гетероциклическому соединению, описываемому выше в [15], где группа, представленная общей формулой

является группой, представленной следующей общей формулой (IIc)
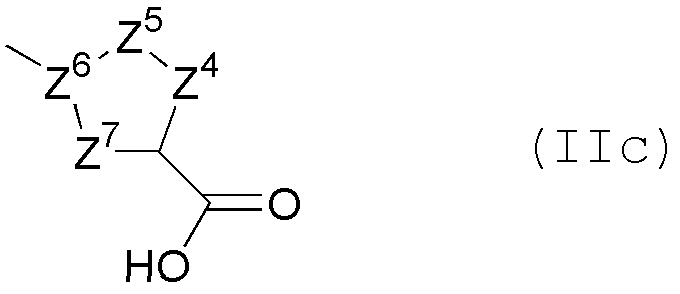
в формуле
Z4, Z5 и Z7 независимо представляют собой атом кислорода, атом азота, атом серы, при условии, что оба из Z4 и Z5 не являются одновременно атомами, выбранными из атома кислорода и атома серы, или CR14, где R14 представляет собой атом водорода, гидрокси, амино, атом галогена, необязательно замещенный низший алкил или необязательно замещенный низший алкокси, который необязательно имеет 1-3 одинаковых или разных заместителей, выбранных из группы, состоящей из атома фтора, гидрокси и амино, при условии, что когда присутствуют два или более R14, эти R14 являются необязательно одинаковыми или отличными друг от друга; Z6 представляет собой атом углерода и Z4, Z5, Z6 и Z7 связаны вместе с атомом углерода, связанным с карбоксильной группой, с образованием 5-членного гетероарильного кольца, или его пролекарству или его фармацевтически приемлемой соли;
[17] 5-членному гетероциклическому соединению, описываемому выше в любом из [1]-[8], где группа, представленная общей формулой (II) является группой, представленной следующей общей формулой (IIx) или (IIy)
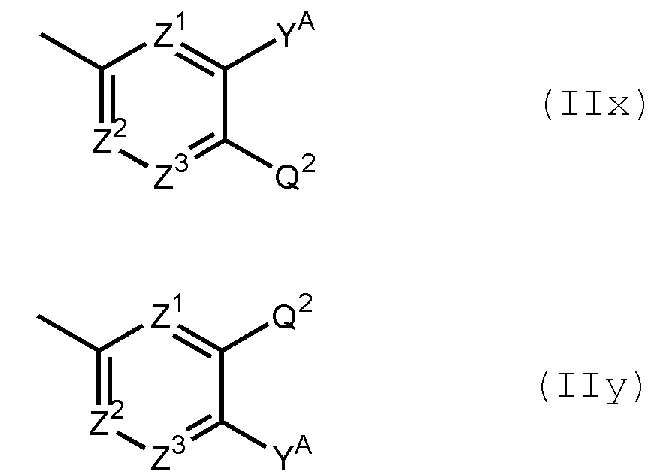
в формулах Z1, Z2 и Z3 независимо представляют собой CR15 или N и Q2 представляет собой карбамоил; YA и R15 независимо представляют собой атом водорода, гидрокси, амино или атом галогена, при условии, что когда присутствуют два или более R15, эти R15 являются необязательно одинаковыми или отличными друг от друга, или его пролекарству или его фармацевтически приемлемой соли;
[18] 5-членному гетероциклическому соединению, описываемому в любом из указанных выше [1]-[17], где R1 представляет собой -A1-D-L-M или -A1-D-E-G-L-M, в формуле A1 представляет собой простую связь и D, E, G, L и M имеют такие же значения, как указано выше в [1], или его пролекарству или его фармацевтически приемлемой соли;
[19] 5-членному гетероциклическому соединению, описываемому выше в [18], где R1 представляет собой -A1-D-L-M, в формуле A1 представляет собой простую связь и D, L и M имеют такие же значения, как указано выше в [1], или его пролекарству или его фармацевтически приемлемой соли;
[20] 5-членному гетероциклическому соединению, описываемому выше в [18], где R1 представляет собой -A1-D-Е-G-L-M, в формуле A1 представляет собой простую связь и D, E, G, L и M имеют такие же значения, как указано выше в [1], или его пролекарству или его фармацевтически приемлемой соли;
[21] 5-членному гетероциклическому соединению, описываемому выше в любом из [1]-[17], где R1 представляет собой -A2-D-L-M или -A2-D-E-G-L-M, в формуле A2 представляет собой -O- и D, E, G, L и M имеют такие же значения, как указаны выше в [1], или его пролекарству или его фармацевтически приемлемой соли;
[22] 5-членному гетероциклическому соединению, описываемому выше в любом из [1]-[17], где R1 представляет собой -A3-D-L-M или -A3-D-E-G-L-M, в формуле A3 представляет собой -CO- или -CON(R3)- и D, E, G, L, M и R3 имеют такие же значения, как указаны выше в [1], или его пролекарству или его фармацевтически приемлемой соли;
[23] 5-членному гетероциклическому соединению, описываемому выше в любом из [1]-[17], где R1 представляет собой -A4-D-L-M, -A4-D-E-G-L-M или -N(-D-L-M)2, при условии, что два (-D-L-M) являются необязательно отличными друг от друга, в формуле A4 представляет собой -N(R3)CO, -N(R3)SO2- или -N=CR3N(R4)- и D, E, G, L, M, R3 и R4 имеют такие же значения, как указаны выше в [1], или его пролекарству или его фармацевтически приемлемой соли;
[24] 5-членному гетероциклическому соединению, описываемому выше в любом из [1]-[23], где необязательно замещенный низший алкил, необязательно замещенный низший алкенил, необязательно замещенный низший алкинил, необязательно замещенный циклоалкил и необязательно замещенный гетероциклоалкил представляют собой низший алкил, который необязательно имеет 1-3 одинаковых или разных заместителя, выбранные из нижеследующей группы заместителей α, низший алкенил, который необязательно имеет 1-3 одинаковых или разных заместителя, выбранные из нижеследующей группы заместителей α, низший алкинил, который необязательно имеет 1-3 одинаковых или разных заместителя, выбранные из нижеследующей группы заместителей α, циклоалкил, который необязательно имеет 1-3 одинаковых или разных заместителя, выбранные из нижеследующей группы заместителей α, и гетероциклоалкил, который необязательно имеет 1-3 одинаковых или разных заместителя, выбранные из нижеследующей группы заместителей α, соответственно; и необязательно замещенный арил и необязательно замещенный гетероарил представляют собой арил, который необязательно имеет 1-3 одинаковых или разных заместителя, выбранные из нижеследующей группы заместителей β, и гетероарил, который необязательно имеет 1-3 одинаковых или разных заместителя, выбранные из нижеследующей группы заместителей β;
[группа заместителей α]
атом фтора, перфтор(низший алкил), -OW1, -SW1, карбокси, сульфо, низший алкил, низший алкилсульфонил, низший алкоксикарбонил, -OCOW2, -N(W2)COW3, -OCOOW4, -N(W2)COOW4, -NHC(=NH)-NW2W3, -NW2W3, -CONW2W3, -N(W5)CONW6W7, -N(W2)SO2W5, -SO2NW2W3, -SO2W4; арил, который необязательно имеет любые 1-3 заместителя, выбранные из группы, состоящей из атома галогена, гидрокси, низшего алкила, низшего алкокси и трифторметила; и гетероарил, который необязательно имеет любые 1-3 заместителя, выбранные из группы, состоящей из атома галогена, гидрокси, низшего алкила, низшего алкокси и трифторметила;
[группа заместителей β]
атом галогена, перфтор(низший алкил), циано, нитро, -OW8, -SW8, карбокси, низший алкил, низший алкилсульфонил, низший алкоксикарбонил, -OCOW2, -N(W2)COW3, -OCOOW4, -N(W2)COOW4, -NHC(=NH)-NW2W3, -NW2W3, -CONW2W3, -N(W5)CONW6W7, -N(W2)SO2W5, -SO2NW2W3, -SO2W4; арил, который необязательно имеет любые 1-3 заместителя, выбранные из группы, состоящей из атома галогена, гидрокси, низшего алкила, низшего алкокси и трифторметила; и гетероарил, который необязательно имеет любые 1-3 заместителя, выбранные из группы, состоящей из атома галогена, гидрокси, низшего алкила, низшего алкокси и трифторметила;
в указанных выше формулах W1 представляет собой атом водорода, низший алкил, перфтор(низший алкил); арил, который может иметь любые 1-3 группы, выбранные из группы, состоящей из атома галогена, гидрокси, алкила, низшего алкокси и трифторметила; арил(низший алкил) или низший алкил, имеющий 2-6 атомов углерода, который имеет группу, выбранную из группы, состоящей из амино, моно(ди)(низший алкил)амино и низший алкилсульфонамидо, при условии, что атом кислорода или серы, связанный с W1, и атом азота в W1 связаны с разными атомами углерода;
W2, W3, W5, W6 и W7 независимо представляют собой атом водорода, низший алкил, арил(низший алкил) или W2 и W3 и W5 и W6 или W6 и W7 могут образовывать алициклическую амино со связывающим атомом азота;
W4 представляет собой низший алкил или W2 и W4 могут образовывать алициклическую амино со связывающим атомом азота;
и W8 представляет собой атом водорода, низший алкил, перфтор(низший алкил); арил, который может иметь любые 1-3 группы, выбранные из группы, состоящие из атома галогена, гидрокси, алкила, низшего алкокси и трифторметила; арил(низший алкил) или низший алкил, имеющий 2-6 атомов углерода, который имеет группу, выбранную из группы, состоящей из амино, моно(ди)(низший алкил)амино и низшего алкилсульфонамида, при условии, что атом кислорода или серы, связанный с W8, и атом азота в W8 связываются с разными атомами углерода, и, когда два -OW8 присутствуют у соседних атомов углерода в арильном кольце, эти W8 могут связываться вместе с образованием метиленовой цепи, которая может быть замещена 1 или 2 атомами фтора, или этиленовой цепи, которая может быть замещена 1-4 атомами фтора, соответственно, или его пролекарству или его фармацевтически приемлемой соли;
[25] ингибитору ксантиноксидазы, содержащему в качестве активного ингредиента 5-членное гетероциклическое соединение, описываемое в любом указанном выше [1]-[24], его пролекарству или фармацевтически приемлемой соли;
[26] фармацевтической композиции, содержащей в качестве активного ингредиента 5-членное гетероциклическое соединение, описываемое в любом указанном выше [1]-[24], или его пролекарству или фармацевтически приемлемой соли;
[27] фармацевтической композиции, описываемой выше в [26], которая является агентом для профилактики или лечения заболевания, выбранного из группы, состоящей из гиперурикемии, подагрических узлов, подагрического артрита, почечного нарушения, связанного с гиперурикемией и мочевыми конкрементами;
[28] фармацевтической композиции, описываемой выше в [27], которая является агентом для профилактики или лечения гиперурикемии;
[29] фармацевтической композиции, описываемой выше в [26], которая является агентом для снижения уровня мочевой кислоты в сыворотке;
[30] фармацевтической композиции, описываемой выше в [26], которая является ингибитором продуцирования мочевой кислоты;
[31] фармацевтической композиции, описываемой выше в любом из [26]-[30], которая содержит дополнительно комбинацию по меньшей мере с одним лекарственным средством, выбранным из группы, состоящей из колхицинов, нестероидного противовоспалительного лекарственного средства, стероида и агента ощелачивания мочи в качестве активного ингредиента и тому подобное.
В 5-членных гетероциклических соединениях, представленных указанной выше общей формулой (I) настоящего изобретения, каждый термин имеет нижеследующие значения.
Термин “атом галогена” означает атом фтора, атом хлора, атом брома или атом иода.
Термин “низший” означает неразветвленную или разветвленную углеводородную группу, имеющую 6 или менее атомов углерода. Например, в качестве низшего алкила можно указать метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил, изопентил, неопентил, трет-пентил, гексил и тому подобное, в качестве низшего алкенила можно указать винил, аллил, 1-пропенил, изопропенил, 1-бутенил, 2-бутенил, 2-метилаллил и тому подобное и в качестве низшего алкинила можно указать этинил, 2-пропинил и тому подобное. В качестве низшего алкилена можно указать метилен, метилметилен, диметилметилен, этилен, 1-метилэтилен, 2-метилэтилен, пропан-1,3-диил, 1-метилпропан-1,3-диил, 1,1-диметилпропан-1,3-диил, 2-метилпропан-1,3-диил, 2,2-диметилпропан-1,3-диил, 3-метилпропан-1,3-диил, 3,3-диметилпропан-1,3-диил, бутан-1,4-диил, 1-метилбутан-1,4-диил, 1,1-диметилбутан-1,4-диил, 2,2-диметилбутан-1,4-диил, 3,3-диметилбутан-1,4-диил, 4-метилбутан-1,4-диил, 4,4-диметилбутан-1,4-диил, пентан-1,5-диил, 1-метилпентан-1,5-диил, 2-метилпентан-1,5-диил, 3-метилпентан-1,5-диил, 4-метилпентан-1,5-диил, 5-метилпентан-1,5-диил, гексан-1,5-диил и тому подобное, в качестве низшего алкенилена можно указать винилен, пропен-1,3-диил, 1-бутен-1,4-диил, 2-бутен-1,4-диил, 1,3-бутадиен-1,4-диил, 1-пентен-1,5-диил, 2-пентен-1,5-диил, 1,3-пентадиен-1,5-диил, 1-гексен-1,6-диил, 2-гексен-1,6-диил, 3-гексен-1,6-диил, 1,3-гексадиен-1,6-диил, 1,3,5-гексатриен-1,6-диил и тому подобное и в качестве низшего алкинилена можно указать этинилен, 2-пропинилен и тому подобное. В качестве низшего алкокси можно указать метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, втор-бутокси, трет-бутокси, пентилокси, изопентилокси, неопентилокси, трет-пентилокси, гексилокси и тому подобное и в качестве низшего алкоксикарбонила можно указать метоксикарбонил, этоксикарбонил, пропоксикарбонил, изопропоксикарбонил, бутоксикарбонил, изобутоксикарбонил, втор-бутоксикарбонил, трет-бутоксикарбонил, пентилоксикарбонил, изопентилоксикарбонил, neoпентилоксикарбонил, трет-пентилоксикарбонил, гексилоксикарбонил и тому подобное.
Термин “перфтор(низший алкил)” означает указанный выше низший алкил, который замещен атомом фтора, и предпочтительно метил, замещенный 1-3 атомами фтора, или этил, замещенный 1-5 атомами фтора.
Термин “циклоалкил” означает циклопропил, циклобутил, циклопентил, циклогексил, циклогексенил, циклогептил или циклооктил и термин “циклоалкилен” означает двухвалентную группу, образованную из указанного выше циклоалкила.
Термин “гетероциклоалкил” означает 3-8-членную алифатическую моноциклическую углеводородную группу, имеющую любые 1 или 2 гетероатома, выбранные из группы, состоящей из атома кислорода, атома серы и атома азота в кольце, и необязательно имеющую 1 или 2 оксогруппы, такую как азиридино, азетидино, морфолино, 2-морфолинил, тиоморфолино, 1-пирролидинил, пиперидино, 4-пиперидинил, 1-пиперазинил, 1-пирролил и тому подобное, или 5-6-членную алифатическую моноциклическую углеводородную группу, указанную выше, которая конденсирована с кольцом бензола, например, 1,3-диоксоизоиндолин-2-ил и тому подобное. Термин “гетероциклоалкилен” означает двухвалентную группу, образованную из указанного выше гетероциклоалкила.
Термин “арил” означает фенил или нафтил и термин “арилен” означает двухвалентную группу, образованную из указанного выше арила.
Термин “циклоалкил(низший алкил)” означает указанный выше низший алкил, замещенный указанным выше циклоалкилом, термин “гетероциклоалкил(низший алкил)” означает указанный выше низший алкил, замещенный указанным выше гетероциклоалкилом, термин “арил(низший алкил)” означает указанный выше низший алкил, замещенный указанным выше арилом, термин “гетероарил(низший алкил)” означает указанный выше низший алкил, замещенный указанным выше гетероарилом. Заместителем необязательно замещенного циклоалкил(низшего алкила) может быть либо циклоалкил, либо низший алкил. Он является почти сходным с необязательно замещенным гетероциклоалкил(низшим алкилом), необязательно замещенным арил(низшим алкилом) и необязательно замещенным гетероарил(низшим алкилом).
Термин “гетероарил” означает 5- или 6-членную ароматическую гетероциклическую группу, имеющую любые 1-4 гетероатома, выбранные из группы, состоящей из атома кислорода, атома серы и атома азота в кольце, которая образована из тиазола, оксазола, изотиазола, изоксазола, пиридина, пиримидина, пиразина, пиридазина, пиррола, фурана, тиофена, имидазола, пиразола, оксадиазола, тиадиазола, триазола, тетразола, фуразана или тому подобное, или 5- или 6-членную ароматическую гетероциклическую группу, конденсированную с 6-членным кольцом, имеющую любые 1-4 гетероатома, выбранные из группы, состоящей из атома кислорода, атома серы и атома азота в кольце, которая образована из индола, изоиндола, бензофурана, изобензофурана, бензотиофена, бензоксазола, бензотиазола, бензоизоксазола, бензизотиазола, индазола, бензимидазола, хинолина, изохинолина, фталазина, хиноксалина, хиназолина, синолина, индолизина, нафтиридина, птеридина или тому подобное. Термин “гетероарилен” означает двухвалентную группу, образованную из указанного выше гетероарила.
Термин “необязательно замещенный” означает группу, которая может иметь 1-3 одинаковых или разных заместителя.
В качестве заместителя необязательно замещенного низшего алкила, необязательно замещенного низшего алкенила, необязательно замещенного низшего алкинила, необязательно замещенного циклоалкила и необязательно замещенного гетероциклоалкила можно указать, например, атом фтора, перфтор(низший алкил), -OW1, -SW1, карбокси, сульфо, низший алкил, низший алкилсульфонил, низший алкоксикарбонил, -OCOW2, -N(W2)COW3, -OCOOW4, -N(W2)COOW4, -NHC(=NH)-NW2W3, -NW2W3, -CONW2W3, -N(W5)CONW6W7, -N(W2)SO2W5, -SO2NW2W3, -SO2W4; арил, который может иметь любые 1-3 группы, выбранные из группы, состоящей из атома галогена, гидрокси, низшего алкила, низшего алкокси и трифторметила; и гетероарил, который может иметь любые 1-3 группы, выбранные из группы, состоящие из атома галогена, гидрокси, низшего алкила, низшего алкокси и трифторметила.
В качестве заместителя необязательно замещенного низшего алкокси предпочтительно можно указать атом фтора, перфтор(низший алкил), низший алкил, гидроксильную группу и низший алкокси.
В качестве заместителя необязательно замещенного арила и необязательно замещенного гетероарила можно указать, например, атом галогена, перфтор(низший алкил), циано, нитро, -OW8, -SW8, карбокси, низший алкил, низший алкилсульфонил, низший алкоксикарбонил, -OCOW2, -N(W2)COW3, -OCOOW4, -N(W2)COOW4, -NHC(=NH)-NW2W3, -NW2W3, -CONW2W3, -N(W5)CONW6W7, -N(W2)SO2W5, -SO2NW2W3, -SO2W4; арил, который может иметь любые 1-3 группы, выбранные из группы, состоящей из атома галогена, гидрокси, низшего алкила, низшего алкокси и трифторметила; и гетероарил, который может иметь любые 1-3 группы, выбранные из группы, состоящей из атома галогена, гидрокси, низшего алкила, низшего алкокси и трифторметила.
В указанных выше формулах W1 представляет собой атом водорода, низший алкил, перфтор(низший алкил); арил, который может иметь любые 1-3 группы, выбранные из группы, состоящей из атома галогена, гидрокси, алкила, низшего алкокси и трифторметила; арил(низший алкил) или низший алкил, имеющий 2-6 атомов углерода, который имеет группу, выбранную из группы, состоящей из амино, моно(ди)(низший алкил)амино и низший алкилсульфонамида, при условии, что атом кислорода или серы, связанный с W1, и атом азота в W1 связываются с разными атомами углерода.
W2, W3, W5, W6 и W7 независимо представляют собой атом водорода, низший алкил, арил(низший алкил) или W2 и W3 и W5 и W6 или W6 и W7 могут образовывать алициклическую амино со связывающим атомом азота;
W4 представляет собой низший алкил, W2 и W4 могут образовывать алициклическую амино со связывающим атомом азота;
и W8 представляет собой атом водорода, низший алкил, перфтор(низший алкил); арил, который может иметь любые 1-3 группы, выбранные из группы, состоящей из атома галогена, гидрокси, алкила, низшего алкокси и трифторметила; арил(низший алкил) или низший алкил, имеющий 2-6 атомов углерода, который имеет группу, выбранную из группы, состоящей из амино, моно(ди)(низший алкил)амино и низший алкилсульфонамида, при условии, что атом кислорода или серы, связанный с W8, и атом азота в W8 связываются с разными атомами углерода, и, когда в арильном кольце два -OW8 присутствуют у соседних атомов углерода, эти W8 могут связываться вместе с образованием метиленовой цепи, которая может быть замещена 1 или 2 атомами фтора, или этиленовой цепи, которая может быть замещена 1-4 атомами фтора, соответственно.
Термин “моно(ди)(низший алкил)амино” означает амино, моно- или дизамещенный указанным выше низшим алкилом, и термин “моно(ди)(низший алкил)карбамоил” означает карбамоил, моно- или дизамещенный указанным выше низшим алкилом. Две низшие алкильные группы в дизамещенной группе могут быть отличными друг от друга.
Термин “алициклический амино” означает 3-8-членный циклический амино, необязательно имеющий гетероатом, выбранный из группы, состоящей из атома кислорода, атома серы и атома азота, другого, чем атом азота у связывающего положения в кольце, такой как азиридино, азетидино, морфолино, тиоморфолино, 1-пирролидинил, пиперидино, 1-пиперазинил, 1-пирролил и тому подобное, необязательно имеющий 1 или 2 оксогруппы и необязательно имеющий 1 или 2 двойные связи в кольце, например, 2-оксо-1-пирролидинил и тому подобное.
Когда кольцо J представляет собой 5-членное гетероарильное кольцо, термин “5-членный гетероарил” означает указанный выше 5-членный гетероарил, такой как тиазол, оксазол, фуран, тиофен, пиррол, пиразол, имидазол и тому подобное.
Термин “кольцо, в котором R1 и R2 необязательно связываются вместе с образованием”, означает 3-8-членную алифатическую моноциклическую углеводородную группу, имеющую любые 1 или 2 гетероатома, выбранные из группы, состоящей из атома кислорода, атома серы и атома азота в кольце, и необязательно имеющую 1 или 2 оксогруппы, такую как азиридин, азетидин, морфолин, тиоморфолин, пирролидин, пиперидин, пиперазин, пирролин или тому подобное, предпочтительным является соединение, имеющее 1 или 2 гетероатома в кольце.
В 5-членных гетероциклических соединениях, представленных формулой (I), когда R1 представляет собой -A-D-L-M или -A-D-E-G-L-M, в каждой комбинации A и L, A и E или E и L, оба представляют собой группу, выбранную из группы, состоящей из -O-, -S-, -SO2-, -N(R16)-, -N(R17)CO-, -N(R17)COO-, -N(R17)SO2-, -N=CR17N(R18)-, -SO2N(R17)-, -N(R17)CON(R18)- и -N(R17)SO2N(R18)-, где R16 представляет собой атом водорода в A; атом водорода или низший алкил в L, E или G, и R17 и R18 независимо представляют собой атом водорода или низший алкил и D или G между ними представляет собой необязательно замещенный низший алкил, низшее алкильное звено D или G имеет 2-6 атомов углерода и A и L, A и E или E и L предпочтительно связываются с разными атомами углерода низшей алкильной цепи D или G, при условии, что когда A или E в E и G представляют собой -N(R17)CO-, это не обязательно так. Аналогично этому, когда R1 представляет собой -N(-D-L-M)2, и L представляет собой группу, выбранную из указанной выше группы, N и L предпочтительно связываются с разными атомами углерода низшей алкильной цепи D. В формуле M имеет такие же значения, как указаны выше. Например для целей иллюстрации в качестве -A-D-L-M включен-O-CH2-CH2-O-M и тому подобное, в качестве -A-D-E-G-L-M включен -A-D-O-CH(CH3)-CH2-N(R16)CO-M и тому подобное и в качестве -N(-D-L-M)2 включен -N(-CH2-CH2-O-M)(-D-L-M) и тому подобное.
В 5-членных гетероциклических соединениях, представленных формулой (I), группа, представленная группой формулы (II), в некотором случае является группой, представленной формулой (IId)
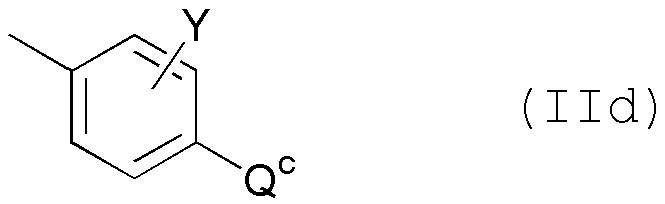
где QC представляет собой карбокси или 5-тетразолил и R1 представляет собой -A-D-L-M, при условии, что A представляет собой простую связь; D представляет собой арилен, необязательно замещенный заместителем, выбранным из группы, состоящей из низшего алкила, атома галогена, низшего алкила, замещенного атомом галогена, и низшего алкокси; или гетероарилен, необязательно замещенный заместителем, выбранным из группы, состоящей из низшего алкила, низшего алкокси и атома галогена, при условии, что когда гетероарилен представляет собой группу, выбранную из тиофена, пиррола или тиазола; L представляет собой простую связь; M представляет собой атом водорода; Y предпочтительно представляет собой гидрокси, амино или атом галогена.
Предпочтительное соединение среди 5-членных гетероциклических соединений, представленных указанной выше формулой (I) настоящего изобретения, обладает также ингибирующей URAT1 активностью. Согласно этому, такое соединение может обнаруживать действие, способствующее выведению мочевой кислоты, помимо ингибирующего действия в отношении синтеза мочевой кислоты и проявляет превосходное действие в отношении снижения уровня мочевой кислоты в сыворотке. В качестве соединения, которое обладает также ингибирующей URAT1 активностью, можно указать, например, соединения, представленные нижеследующими общими формулами от (IIIa) до (IIIc)
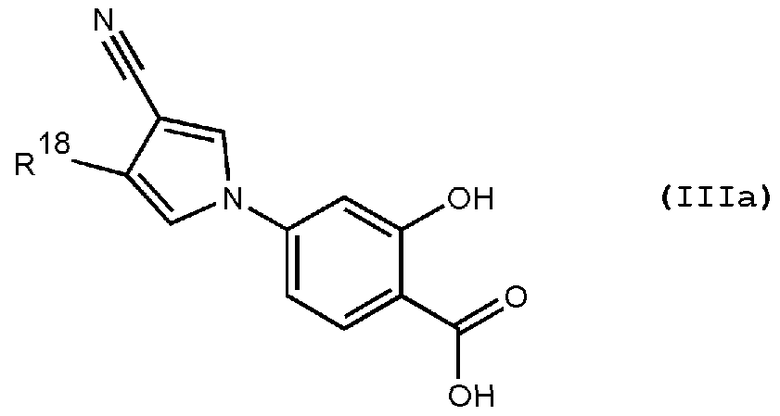
В формуле R18 представляет собой -A-D-L-M или -A-D-E-G-L-M, при условии, что A представляет собой простую связь и D, E, G, L и M имеют такие же значения, как указаны выше.
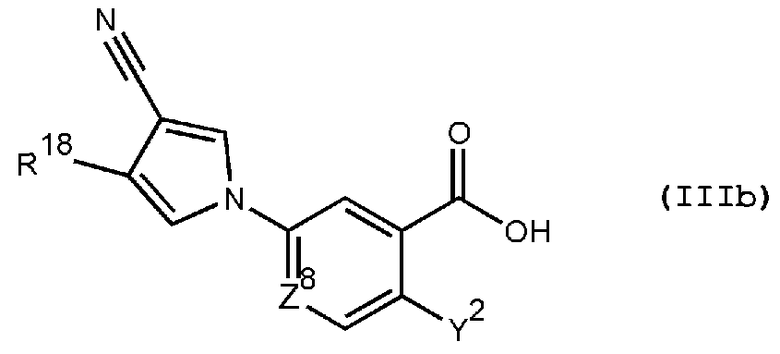
В формуле R18 имеет такие же значения, как указаны выше, Y2 представляет собой атом водорода, гидрокси или амино и Z8 представляет собой N или CR19, где R19 представляет собой атом водорода, атом галогена или низший алкил.
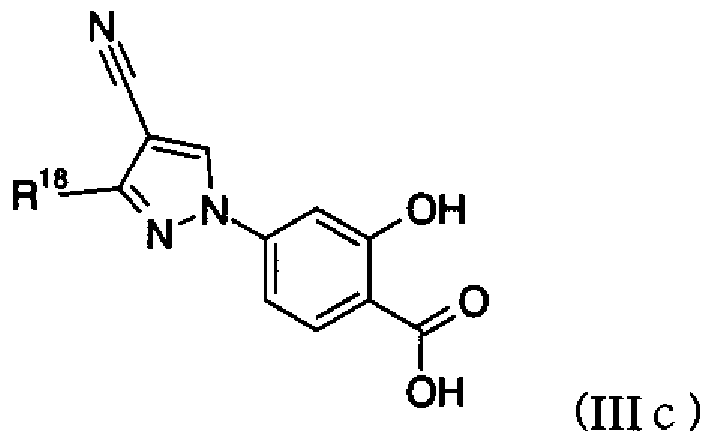
В формуле R18 имеет такие же значения, как указаны выше.
5-членные гетероциклические соединения, представленные указанной выше общей формулой (I) настоящего изобретения, можно получить, например, способом, описанным ниже или аналогичным ему способом, или способом, описанным в других литературных источниках, или способом, аналогичным ему, или тому подобное. Кроме того, когда необходима защитная группа, операции введения и удаления защитной группы можно проводить необязательно в сочетании согласно общему способу.
[Синтетический способ 1]
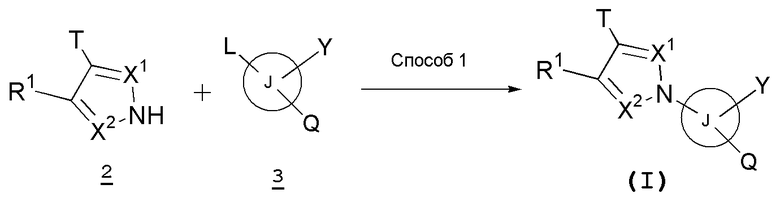
В формулах L представляет собой атом галогена и Т, кольцо J, Q, Y, X1, X2 и R1 имеют такие же значения, как указаны выше.
Способ 1
5-членное гетероциклическое соединение, представленное указанной выше общей формулой (I) настоящего изобретения, можно получить проведением реакции сочетания соединения (2) и соединения (3) в инертном растворителе или без какого-либо растворителя в присутствии основания и необязательно удалением защитной группы. В качестве инертного растворителя можно указать N,N-диметилформамид, тетрагидрофуран, N-метилпиролидон, 1,2-диметоксиэтан, диметилсульфоксид, 1,2-диэтоксиэтан, 1,4-диоксан, их смешанные растворители и тому подобное. В качестве основания можно указать гидрид натрия, карбонат калия, карбонат цезия, гидроксид натрия, гидроксид калия, метоксид натрия и тому подобное. Температура реакции обычно составляет от комнатной температуры до температуры кипения с обратным холодильником и время реакции обычно составляет от 30 минут до 7 дней, варьируя в зависимости от исходного соединения, растворителя и температуры реакции или тому подобное. Помимо этого, в настоящем способе реакцию можно необязательно проводить с применением устойчивого к давлению реакционного сосуда.
5-членное гетероциклическое соединение, представленное указанной выше общей формулой (I) настоящего изобретения, можно также получить проведением реакции сочетания соединения (2) и соединения (3) в инертном растворителе в присутствии основания, каталитического или эквивалентного количества иодида меди и лиганда и необязательно удалением защитной группы. В качестве инертного растворителя можно указать N,N-диметилформамид, тетрагидрофуран, N-метилпирролидон, 1,2-диметоксиэтан, их смешанный растворитель и тому подобное. В качестве основания можно указать фосфат калия, карбонат калия, карбонат цезия и тому подобное. В качестве лиганда можно указать N,N-диметилэтилендиамин, (1R,2R)-(-)-N,N′-диметилциклогексан-1,2-диамин, (1S,2S)-(+)-N,N′-диметилциклогексан-1,2-диамин, пролин, N,N-диметиламиноглицин и тому подобное. Температура реакции обычно составляет от комнатной температуры до температуры кипения с обратным холодильником и время реакции обычно составляет от 30 минут до 7 дней, варьируя в зависимости от применяемого исходного вещества, растворителя и температуры реакции или тому подобное. Помимо этого, в настоящем способе реакцию можно необязательно проводить с применением устойчивого к давлению реакционного сосуда.
Указанную выше реакцию можно также проводить способом, описанным в следующем литературном источнике (а).
(a) Hui Zhang,; Qian Cai,; и Dawei Ma, J. Org. Chem, Vol. 70, No. 13, 2005, 5173.
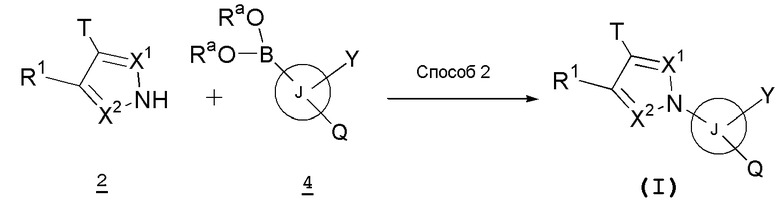
В формуле Ra представляет собой атом водорода или низший алкил, при условии, что два Ra могут быть разными и оба Ra могут связываться вместе с образованием кольца и Т, кольцо J, Q, Y, X1, X2 и R1 имеют такие же значения, как указано выше.
Способ 2
5-членное гетероциклическое соединение, представленное указанной выше общей формулой (I) настоящего изобретения, можно также получить проведением реакции сочетания соединения (2) и соединения (4) в инертном растворителе в присутствии основания и каталитического количества ацетата меди и необязательно удалением защитной группы. В качестве инертного растворителя можно указать дихлорметан, 1,2-дихлорэтан, N,N-диметилформамид, тетрагидрофуран, N-метилпирролидон, 1,2-диметоксиэтан, воду, их смешанный растворитель и тому подобное. В качестве основания можно указать триэтиламин, N,N-диизопропилэтиламин, пиридин, 2,6-лутидин, 1,8-диазабицикло[5,4,0]ундецен и тому подобное. Имеются случаи, когда в данной реакции лучше применять дегидратирующий агент, такой как молекулярные сита. Температура реакции обычно составляет от комнатной температуры до температуры кипения с обратным холодильником и время реакции обычно составляет от 30 минут до 7 дней, варьируя в зависимости от применяемого исходного вещества, растворителя и температуры реакции или тому подобное. Помимо этого, в настоящем способе реакцию можно необязательно проводить с применением устойчивого к давлению реакционного сосуда.
Указанную выше реакцию можно также проводить способом, описанным в следующем литературном источнике (b).
(b) Hartwi, John F.; Kawatsura, Motoi; Hauck, Sheila I. et al. Journal of Organic Chemistry, 1999, 64 (15), 5575-5580.
[Синтетический способ 2]
Среди 5-членных гетероциклических соединений, представленных указанной выше общей формулой (I) настоящего изобретения, соединение (Ia), где Т представляет собой циано, можно также получить, например, синтетическим способом 2.
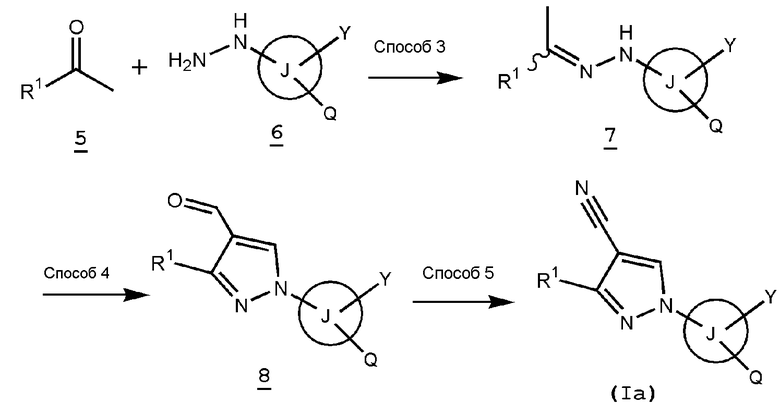
В формуле кольцо J, Q, R1 и Y имеют такие же значения, как указаны выше.
Способ 3
Соединение 7 можно также получить конденсацией соединения (5) с соединением (6) в инертном растворителе или без какого-либо растворителя в присутствии или в отсутствие кислоты. В качестве инертного растворителе можно указать метанол, этанол, изопропанол, бутанол, диэтиловый эфир, тетрагидрофуран, 1,4-диоксан, 1,2-диметоксиэтан, N,N-диметилформамид, ацетонитрил, бензол, толуол, ксилол, N-метилпирролидон, дихлорэтан, хлороформ, уксусную кислоту, воду, их смешанный растворитель и тому подобное. В качестве кислоты можно указать хлористоводородную кислоту, серную кислоту, уксусную кислоту, трифторуксусную кислоту и тому подобное. Температура реакции обычно составляет от 0°С до температуры кипения с обратным холодильником и время реакции обычно составляет от 30 минут до 7 дней, варьируя в зависимости от применяемого исходного вещества, растворителя и температуры реакции или тому подобное.
Способ 4
Производное формилпиразола (8) можно также получить предоставлением возможности для реакции соединения (7) в инертном растворителе в присутствии N,N-диметилформамида и фосфорилхлорида. В качестве инертного растворителя можно указать N,N-диметилформамид, ацетонитрил, бензол, толуол, ксилол, хлорбензол, дихлорметан, 1,2-дихлорэтан, хлороформ, их смешанный растворитель и тому подобное. Температура реакции обычно составляет от 0°С до температуры кипения с обратным холодильником и время реакции обычно составляет от 30 минут до 7 дней, варьируя в зависимости от применяемого исходного вещества, растворителя и температуры реакции или тому подобное.
Способ 5
5-членное гетероциклическое соединение (Ia) настоящего изобретения можно получить реакцией цианирования производного формилпиразола (8) и гидроксиламина или его гидрохлоридной соли в инертном растворителе в присутствии или в отсутствие основания и в присутствии или отсутствие дегидратирующего агента. В качестве инертного растворителя указываются N,N-диметилформамид, ацетонитрил, бензол, толуол, хлорбензол, дихлорметан, 1,2-дихлорэтан, хлороформ, N-метилпирролидон, их смешанный растворитель и тому подобное. В качестве основания можно указать триэтиламин, N-N-диизопропилэтиламин, пиридин, 2,6-лутидин, 1,8-диазабицикло[5,4,0]ундецен, карбонат калия, карбонат натрия и тому подобное. В качестве дегидратирующего агента можно указать уксусный ангидрид, тионилхлорид, пятихлористый фосфор, N,N′-дициклогексилкарбодиимид, N,N′-карбонилдиимидазол и тому подобное. Температура реакции обычно составляет от 0°С до температуры кипения с обратным холодильником и время реакции обычно составляет от 30 минут до 7 дней, варьируя в зависимости применяемого исходного вещества, растворителя и температуры реакции или тому подобное.
Указанную выше реакцию цианирования можно также проводить предоставлением возможности производному формилпиразола (8) и гидроксиламину или его гидрохлоридной соли реагировать с формиатом натрия в растворителе, таком как муравьиная кислота. Температура реакции обычно составляет от 0°С до температуры кипения с обратным холодильником и время реакции обычно составляет от 30 минут до 7 дней, варьируя в зависимости от применяемого исходного вещества, растворителя и температуры реакции или тому подобное.
[Синтетический способ 3]
Среди 5-членных гетероциклических соединений, представленных указанной выше формулой (I) настоящего изобретения, соединение (Ib), у которого R1 представляет собой -A-D-L-M или -A-D-E-G-L-M, при условии, что A представляет собой простую связь и D представляет собой необязательно замещенный низший алкенилен, при условии, что следом за A присутствует двойная связь, необязательно замещенный арилен или необязательно замещенный гетероарилен и E, G, L и M имеют такие же значения, как указаны выше, можно также получить, например, синтетическим способом 3. В синтетическом способе 3 в качестве примера описано применение соединения, у которого R1 представляет собой -Aa-Da-L-M, где Aa представляет собой простую связь, Da представляет собой необязательно замещенный низший алкенилен, необязательно замещенный арилен или необязательно замещенный гетероарилен и L и M имеют такие же значения, как указаны выше.
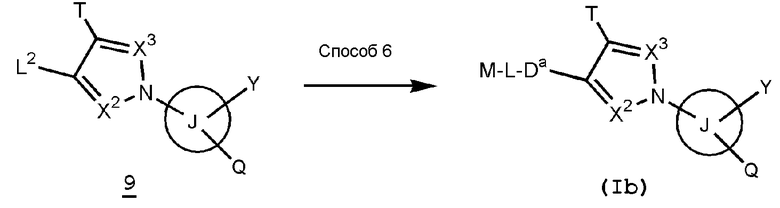
В формуле L2 представляет собой атом галогена или трифторметансульфонил, Da представляет собой необязательно замещенный низший алкенилен, необязательно замещенный арилен или необязательно замещенный гетероарилен и L, M, T, кольцо J, Q, X1, X2 и Y имеют такие же значения, как указаны выше.
Способ 6 [метод 1]
5-членное гетероциклическое соединение (Ib) настоящего изобретения можно также получить проведением реакции сочетания Сузуки-Миаура соединения (9) с применением реагента, соответствующей арилбороновой кислоты, или реагента, гетероарилбороновой кислоты, в инертном растворителе в присутствии основания и палладиевого катализатора. В качестве инертного растворителя можно указать бензол, толуол, ксилол, диэтиловый эфир, тетрагидрофуран, 1,4-диоксан, 1,2-диметоксиэтан, дихлорметан, 1,2-дихлорэтан, хлороформ, метанол, этанол, 2-пропанол, бутанол, N,N-диметилформамид, N-метилпирролидон, диметилсульфоксид, воду, их смешанный растворитель и тому подобное. В качестве основания можно указать карбонат натрия, карбонат калия, гидроксид натрия, гидроксид калия, этоксид натрия, метоксид натрия, фторид калия, бромид цезия, триэтиламин, N,N-диизопропилэтиламин, пиридин, 2,6-лутидин, 1,8-диазабицикло[5,4,0]-7-ундецен и тому подобное. В качестве палладиевого катализатора можно указать тетракис(трифенилфосфин)палладий, дихлорбис(трифенилфосфин)палладий, [1,1′-бис(дифенилфосфино)ферроцен]дихлорпалладий и тому подобное. Температура реакции обычно составляет от 0°С до температуры кипения с обратным холодильником и время реакции обычно составляет от 30 минут до 7 дней, варьируя в зависимости от применяемого исходного вещества, растворителя и температуры реакции или тому подобное. Помимо этого, в настоящем способе реакцию можно необязательно проводить с применением устойчивого к давлению реакционного сосуда.
Способ 6 [метод 2]
5-членное гетероциклическое соединение (Ib) настоящего изобретения можно также получить проведением реакции Мизороги-Хека соединения (9) с применением соответствующего алкена в инертном растворителе в присутствии основания и палладиевого катализатора. В качестве инертного растворителя можно указать бензол, толуол, ксилол, диэтиловый эфир, тетрагидрофуран, 1,4-диоксан, 1,2-диметоксиэтан, дихлорметан, 1,2-дихлорэтан, хлороформ, метанол, этанол, 2-пропанол, бутанол, N,N-диметилформамид, N-метилпирролидон, диметилсульфоксид, воду, их смешанный растворитель и тому подобное. В качестве основания можно указать триэтиламин, N,N-диизопропилэтиламин, пиридин, 2,6-лутидин, 1,8-диазабицикло[5,4,0]-7-ундецен и тому подобное. В качестве палладиевого катализатора можно указать ацетат палладия, хлорид палладия, тетракис(трифенилфосфин)палладий, дихлорбис(трифенилфосфин)палладий, [1,1′-бис(дифенилфосфино)ферроцен]дихлорпалладий и тому подобное. Кроме того, настоящую реакцию можно также проводить с применением лиганда в зависимости от типа палладиевого катализатора и в качестве лиганда можно указать трифенилфосфин, три-о-толилфосфин, тетрафторборат три-трет-бутилфосфония и тому подобное. Температура реакции обычно составляет от 0°С до температуры кипения с обратным холодильником и время реакции обычно составляет от 30 минут до 7 дней, варьируя в зависимости от применяемого исходного вещества, растворителя и температуры реакции или тому подобное. Помимо этого, в настоящем способе реакцию можно необязательно проводить с применением устойчивого к давлению реакционного сосуда.
Соединение, представленное вышеуказанной общей формулой (2), применяемое в качестве исходного вещества в указанных выше способах, может быть коммерчески доступным или его получают известным способом или аналогичным ему способом. Например, соединение (2а), где Х1 представляет собой СН и Х2 представляет собой CRb, где Rb представляет собой атом водорода или низший алкил, можно также получить способом, показанным в нижеследующем синтетическом способе 4.
[Синтетический способ 4]
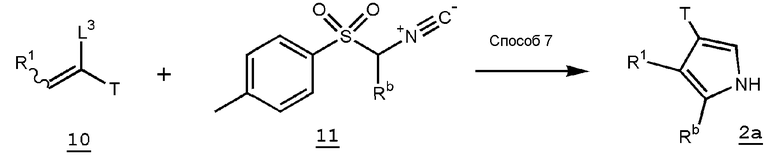
В формуле L3 представляет собой атом водорода или электроноакцепторную группу, такую как алкоксикарбонил и тому подобное, Rb представляет собой атом водород или низший алкил и Т и R1 имеют такие же значения, как указаны выше.
Способ 7
Производное пиррола (2а) можно также получить предоставлением возможности соединению (10) и изоцианидному соединению (11) реагировать в инертном растворителе в присутствии основания. В качестве инертного растворителя можно указать дихлорметан, дихлорэтан, диэтиловый простой эфир, тетрагидрофуран, 1,4-диоксан, 1,2-диметоксиэтан, ацетонитрил, метанол, этанол, N,N-диметилформамид, диметилсульфоксид, бензол, толуол, ксилол, воду, их смешанный растворитель и тому подобное. В качестве основания можно указать гидрид натрия, метоксид натрия, этоксид натрия, трет-бутоксид калия, трет-бутоксид натрия, н-бутиллитий, втор-бутиллитий, трет-бутиллитий и тому подобное. Температура реакции обычно составляет от 0°С до температуры кипения с обратным холодильником и время реакции обычно составляет от 30 минут до 7 дней, варьируя в зависимости от применяемого исходного вещества, растворителя и температуры реакции или тому подобное.
[Синтетический способ 5]
Среди соединений (10), применяемых в качестве исходных соединений в указанном выше способе 4, соединение (10а), где R1 представляет собой -A-D-L-M или -A-D-E-G-L-M, при условии, что А представляет собой простую связь, можно также получить способом, показанным в следующем синтетическом способе 5.
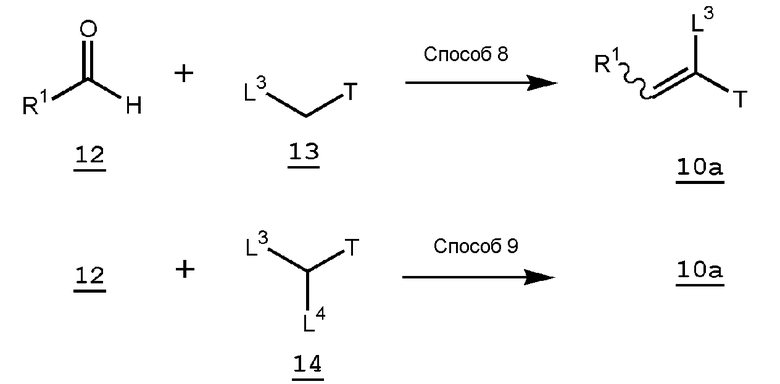
В формуле L4 представляет собой реагент Хорнера-Вадсворта-Эммонса, такой как диметиловый эфир фосфорной кислоты, диэтиловый эфир фосфорной кислоты и тому подобное, или реагент Виттига, такой как трифенилфосфоний, трибутилфосфоний и тому подобное, и L3, T и R1 имеют такие же значения, как указаны выше.
Способ 8
Соединение (10а) можно также получить предоставлением возможности альдегидному соединению (12) и соединению (13) реагировать в инертном растворителе в присутствии или в отсутствие каталитического или эквивалентного количества основания. В качестве инертного растворителя можно указать метанол, этанол, изопропанол, тетрагидрофуран, 1,4-диоксан, толуол, N-метилпирролидон, их смешанный растворитель и тому подобное. В качестве основания можно указать пиперидин, пирролидин, морфолин, триэтиламин, пиридин, 2,6-лутидин, 1,8-диазабицикло[5,4,0]-7-ундецен, карбонат калия, карбонат натрия, гидроксид натрия, гидроксид калия, метоксид натрия, этоксид натрия и тому подобное. Имеются случаи, когда в этой реакции лучше применять дегидратирующий агент, такой как молекулярные сита. Температура реакции обычно составляет от 0°С до температуры кипения с обратным холодильником и время реакции обычно составляет от 30 минут до 7 дней, варьируя в зависимости от применяемого исходного вещества, растворителя и температуры реакции или тому подобное.
Способ 9
Соединение (10а) можно также получить реакцией Хорнера-Вадсворта-Эммонса или реакцией Виттига альдегидного соединения (12) и соединения (14) в инертном растворителе в присутствии или в отсутствие основания. В качестве инертного растворителя можно указать диэтиловый простой эфир, тетрагидрофуран, 1,4-диоксан, 1,2-диметоксиэтан, N,N-диметилформамид, диметилсульфоксид, N-метилпирролидон, ацетонитрил, дихлорметан, дихлорэтан, гексан, гептан, бензол, толуол, ксилол, воду, их смешанный растворитель и тому подобное. В качестве основания можно указать гидрид натрия, метоксид натрия, этоксид натрия, трет-бутоксид калия, трет-бутоксид натрия, н-бутиллития, втор-бутиллитий, трет-бутиллитий, гидроксид натрия, гидроксид лития, гексаметилдисилазид калия, гексаметилдисилазид, гексаметилдисилазид лития и тому подобное. Температура реакции обычно составляет от -20°С до температуры кипения с обратным холодильником и время реакции обычно составляет от 30 минут до 7 дней, варьируя в зависимости от применяемого исходного вещества, растворителя и температуры реакции или тому подобное.
Среди соединений, представленных вышеуказанной общей формулой (2), применяемых в качестве исходных веществ в указанных выше способах, производное пиразола (2b), где R1 представляет собой -A-D-L-M или -A-D-G-L-M, при условии, что А представляет собой простую связь, Х1 представляет собой СН, Х2 представляет собой N и Т представляет собой циано, можно также получить способом, показанным в следующем синтетическом способе 6.
[Синтетический способ 6]
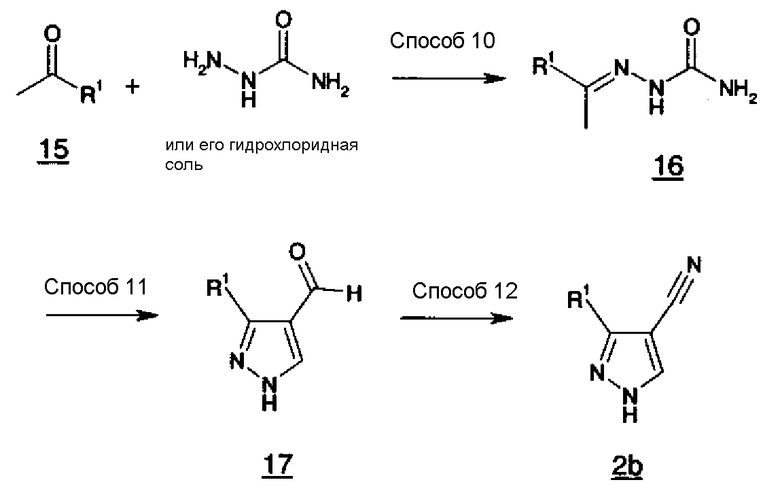
В формуле R1 имеет такие же значения, как указаны выше.
Способ 10
Семикарбазон (16) можно также получить предоставлением возможности ацетилсоединению (15) и семикарбазиду или его гидрохлоридной соли реагировать в инертном растворителе или без какого-либо растворителя в присутствии основания или кислоты. В качестве инертного растворителя можно указать метанол, этанол, н-бутанол, трет-бутанол, уксусную кислоту, тетрагидрофуран, N,N-диметилформамид, ацетонитрил, воду, их смешанный растворитель и тому подобное. В качестве основания можно указать ацетат натрия, ацетат калия, гидрокарбонат натрия, карбонат натрия, карбонат калия, метоксид натрия, гидроксид лития, пиридин, имидазол и тому подобное. В качестве кислоты можно указать уксусную кислоту, трифторуксусную кислоту и тому подобное. Температура реакции обычно составляет от 0°С до температуры кипения с обратным холодильником и время реакции обычно составляет от 1 час до 7 дней, варьируя в зависимости от применяемого исходного вещества, растворителя и температуры реакции или тому подобное.
Способ 11
Производное формилпиразола (17) можно получить предоставлением возможности соединению (16) реагировать в инертном растворителе в присутствии N,N-диметилформамида и фосфорилхлорида. В качестве инертного растворителя можно указать N,N-диметилформамид, ацетонитрил, бензол, толуол, ксилол, хлорбензол, дихлорметан, 1,2-дихлорэтан, хлороформ, их смешанный растворитель и тому подобное. Температура реакции обычно составляет от 0°С до температуры кипения с обратным холодильником и время реакции обычно составляет от 30 минут до 7 дней, варьируя в зависимости от применяемого исходного вещества, растворителя и температуры реакции или тому подобное.
Способ 12
Производное цианопиразола (2b) можно получить реакцией цианирования производного формилпиразола (17) и гидроксиламина или его гидрохлоридной соли в инертном растворителе в присутствии или отсутствии основания и в присутствии или отсутствие дегидратирующего агента. В качестве инертного растворителя можно указать N,N-диметилформамид, ацетонитрил, бензол, толуол, хлорбензол, дихлорметан, 1,2-дихлорэтан, хлороформ, N-метилпирролидон, их смешанный растворитель и тому подобное. В качестве основания можно указать триэтиламин, N,N-диизопропилэтиламин, пиридин, 2,6-лутидин, 1,8-диазабицикло[5,4,0]-7-ундецен, карбонат калия, карбонат натрия и тому подобное. В качестве дегидратирующего агента можно указать уксусный ангидрид, тионилхлорид, пятихлористый фосфор, N,N′-дициклогексилкарбодиимид, N,N′-карбонилимидазол и тому подобное. Температура реакции обычно составляет от 0°С до температуры кипения с обратным холодильником и время реакции обычно составляет от 30 минут до 7 дней, варьируя в зависимости от применяемого исходного вещества, растворителя и температуры реакции или тому подобное.
Указанную выше реакцию цианирования можно проводить предоставлением возможности производному формилпиразола (17) и гидроксиламину или его гидрохлоридной соли реагировать с формиатом натрия в растворителе, таком как муравьиная кислота. Температура реакции обычно составляет от 0°С до температуры кипения с обратным холодильником и время реакции обычно составляет от 30 минут до 7 дней, варьируя в зависимости от применяемого исходного вещества, растворителя и температуры реакции или тому подобное.
В качестве защитных групп, которые применяют в настоящем изобретении, можно применять различные защитные группы, обычно применяемые в органических реакциях. Например, в качестве защитных групп гидроксильной группы помимо п-метоксибензильной группы, бензильной группы, метоксиметильной группы, ацетильной группы, пивалоильной группы, бензоильной группы, трет-бутилдиметилсилильной группы, трет-бутилдифенилсилильной группы, аллильной группы и тому подобное, когда две гидроксильные группы являются соседними, можно указать изопропилиденовую группу, циклопентилиденовую группу, циклогексилиденовую группу и тому подобное. В качестве защитных групп тиольной группы можно указать п-метоксибензильную группу, бензильную группу, ацетильную группу, пивалоильную группу, бензоильную группу, бензилоксикарбонильную группу и тому подобное. В качестве защитных групп аминогруппы можно указать бензилоксикарбонильную группу, трет-бутоксикарбонильную группу, бензильную группу, п-метоксибензильную группу, трифторацетильную группу, ацетильную группу, фталоильную группу и тому подобное. В качестве защитных групп карбоксигруппы можно указать метильную группу, этильную группу, бензильную группу, трет-бутилдиметилсилильную группу, аллильную группу и тому подобное.
Соединение, представленное выше общей формулой (I) настоящего изобретения, можно выделить или очистить общепринятыми методиками выделения, такими как фракционированная перекристаллизация, очистка хроматографией, экстракция растворителем, экстракция в системе твердое тело-жидкость и тому подобное.
5-членные гетероциклические соединения, представленные выше общей формулой (I) настоящего изобретения, можно превратить в их фармацевтически приемлемые соли обычным путем. В качестве такой соли можно указать кислотно-аддитивную соль с минеральной кислотой, такой как хлористоводородная кислота, бромистоводородная кислота, иодистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота и тому подобное, кислотно-аддитивную соль с органической кислотой, такой как муравьиная кислота, уксусная кислота, метансульфоновая кислота, бензолсульфоновая кислота, п-толуолсульфоновая кислота, пропионовая кислота, лимонная кислота, янтарная кислота, винная кислота, фумаровая кислота, масляная кислота, щавелевая кислота, малоновая кислота, малеиновая кислота, молочная кислота, яблочная кислота, угольная кислота, бензойная кислота, глутаминовая кислота, аспарагиновая кислота и тому подобное, неорганическую соль, такую как соль натрия, соль калия, соль магния, соль цинка, соль лития, соль алюминия и тому подобное, соль с органическим амином, таким как N-метил-D-глюкамин, N,N′-дибензилэтилендиамин, 2-аминоэтанол, трис(гидроксиметил)аминометан, аргинин, лизин, пиперидин, холин, диэтиламин, 4-фенилциклогексиламин и тому подобное.
Среди 5-членных гетероциклических соединений, представленных указанной выше общей формулой (I) настоящего изобретения, в соединении, имеющем ненасыщенную связь, имеются два геометрических изомера, соединение цис-(Z)-формы и соединение транс-(Е)-формы. В настоящем изобретении можно применять любое из соединений и можно также применять их смесь.
Среди 5-членных гетероциклических соединений, представленных указанной выше общей формулой (I) настоящего изобретения, в соединении, имеющем хиральный атом углерода, имеются соединение R-формы и соединение S-формы для каждого хирального атома углерода. В настоящем изобретении можно применять любой из оптических изомеров и можно также применять смесь оптических изомеров.
Среди 5-членных гетероциклических соединений, представленных указанной выше общей формулой (I) настоящего изобретения, могут быть некоторые таутомеры, соединения настоящего изобретения включают в себя также эти таутомеры.
В настоящем изобретении термин “пролекарство” означает соединение, представляющее собой “исходное соединение”, модифицированное фармацевтически приемлемой группой, обычно применяемой в пролекарстве, например, группой, которая придает такие свойства, как повышенная стабильность, достаточная защита, пероральная абсорбционная способность или тому подобное, и как можно предположить, это соединение для оказания действия превращается в исходное соединение в организме (в печени, кишечнике и тому подобное). Пролекарство соединения, представленного вышеуказанной общей формулой (I) настоящего изобретения, можно получить введением подходящей группы, образующей пролекарство, в любую одну или несколько групп, выбранных из гидроксигруппы, аминогруппы и других групп, которые могут образовывать пролекарство соединения, представленного вышеуказанной общей формулы (I), и применением соответствующего реагента для получения пролекарства, такого как галогенидное соединение или тому подобное, обычным путем и затем подходящим образом выделением и очисткой обычным путем, в зависимости от требований каждого случая. Gekkan-Yakuji iyakuhin tekiseisiyou no tameno rinsyou yakubutudoutai (monthly pharmaceutical, clinical pharmacokinetics for the proper use of pharmaceutical products), 2003.3. extra number Vol.42, No.4, p.669-707, New drug Drug delivery system Published by CMC Co., Ltd., 2000.1.31., p.67-173.
В качестве применяемой группы, образующей пролекарство в гидроксигруппе или аминогруппе можно указать, например, (низший алкил)-CO-, такую как ацетил, пропионил, бутирил, изобутирил, пивалоил и тому подобное; арил-CO-, такую как бензоил; (низший алкил)-O-(низший алкилен)-CO-; (низший алкил)-OCO-(низший алкилен)-CO-; (низший алкил)-OCO-, такой как метилоксикарбонил, этилоксикарбонил, пропилоксикарбонил, изопропилоксикарбонил, трет-бутилоксикарбонил и тому подобное; (низший алкил)-O-(низший алкилен)-OCO-; (низший алкил)-COO-(низший алкилен), такую как ацетилоксиметил, пивалоилоксиметил, 1-(ацетилокси)этил, 1-(пивалоилокси)этил и тому подобное; (низший алкил)-OCOO-(низший алкилен), такую как метоксикарбонилоксиметил, 1-(метоксикарбонилокси)этил, этоксикарбонилоксиметил, 1-(этоксикарбонилокси)этил, изопропилоксикарбонилоксиметил, 1-(изопропилоксикарбонилокси)этил, трет-бутилоксикарбонилоксиметил, 1-(трет-бутилоксикарбонилокси)этил и тому подобное; циклоалкил-OCOO-(низший алкилен), такую как циклогексилоксикарбонилоксиметил, 1-(циклогексилоксикарбонил)этил и тому подобное; сложный эфир или амид с аминокислотой, такой как глицин и тому подобное; и тому подобное.
В качестве применяемой группы, образующей пролекарство в карбоксигруппе, можно указать, например, низший алкил, такой как метил, этил, пропил, изопропил, бутил, трет-бутил и тому подобное; (низший алкил)-COO-(низший алкилен), такой как пивалоилоксиметил, ацетилоксиметил, 1-(пивалоилокси)этил, 1-(ацетилокси)этил и тому подобное; (низший алкил)-OCOO-(низший алкилен), такой как этилоксикарбонилоксиметил, 1-(этилоксикарбонилокси)этил, изопропилоксикарбонилоксиметил, 1-(изопропилоксикарбонилокси)этил, трет-бутилоксикарбонилоксиметил, 1-(трет-бутилоксикарбонилокси)этил и тому подобное; циклоалкил-OCOO-(низший алкилен), такой как циклогексилоксикарбонилметил, 1-(циклогексилоксикарбонил)этил и тому подобное; и тому подобное.
5-членное гетероциклическое соединение, представленное общей формулой (I), или его пролекарство, или фармацевтически приемлемая соль может быть иногда получена в виде его гидрата или сольвата в ходе очистки или получения его солей. 5-членное гетероциклическое соединение, представленное общей формулой (I) настоящего изобретения, или его пролекарство, или его фармацевтически приемлемая соль включает его гидрат или его сольват с фармацевтически приемлемым растворителем. В качестве фармацевтически приемлемых растворителей можно указать этанол и тому подобное.
Фармацевтическая композиция настоящего изобретения является применимой в качестве агента для профилактики или лечения заболеваний, связанных с высокими уровнями мочевой кислоты в крови, таких как гиперурикемия, подагрические узлы, подагрический артрит, почечное нарушение, связанное с гиперурикемией, мочевыми конкрементами или тому подобное, особенно гиперурикемия.
Когда фармацевтические композиции настоящего изобретения применяют на практике при профилактике или лечении, дозу соединения, представленного выше общей формулой (I), или его пролекарства, или его фармацевтически приемлемой соли в качестве активного ингредиента подходящим образом выбирают в зависимости от возраста, пола, массы тела и тяжести симптомов и лечения каждого пациента, например, доза находится приблизительно в диапазоне от 1 до 2000 мг в день для взрослого человека в случае перорального введения, и суточную дозу можно разделить на несколько доз и вводить их в течение суток.
Когда фармацевтические композиции настоящего изобретения применяют на практике при профилактике или лечении, различные дозированные формы вводят перорально или парентерально, в зависимости от их применений, например, предпочтительными для перорального введения являются такие препараты, как порошки, мелкие гранулы, гранулы, таблетки, капсулы, сухие сиропы или тому подобное.
Эти фармацевтические композиции можно получить необязательно смешиванием с применением подходящей фармацевтической добавки, такой как эксципиенты, дезинтеграторы, лубриканты, смазывающие вещества и тому подобное, и обработкой смеси согласно общепринятым способам.
Например, порошки можно изготовить, если необходимо, эффективным смешиванием активного ингредиента с подходящими эксципиентами, лубрикантами и тому подобное. Например, таблетки можно изготовить таблетированием активного ингредиента с подходящими эксципиентами, дезинтеграторами, лубрикантами, смазывающими веществами и тому подобное согласно общепринятым способам, далее, если необходимо, таблетки можно покрыть подходящим образом для получения таблеток, покрытых пленкой, таблеток, покрытых сахаром, таблеток с энтеросолюбильным покрытием и тому подобное. Например, капсулы можно изготовить эффективным смешиванием активного ингредиента с подходящими эксципиентами, лубрикантами и тому подобное или изготовлением мелких гранул, гранул согласно общепринятым способам и заполнением ими подходящих капсул. Кроме того, в случае такого лекарственного средства для перорального введения, его можно также изготовить в форме препарата для быстрого высвобождения или замедленного высвобождения, в зависимости от способов профилактики или лечения.
Соединение, представленное выше общей формулой (I) настоящего изобретения, его пролекарство, или фармацевтически приемлемую соль можно применять далее в комбинации с любым другим лекарственным средством для лечения гиперурикемии или лекарственным средством для лечения подагры. В качестве лекарственного средства для лечения гиперурикемии, которое можно применять в настоящем изобретении, можно указать, например, средства ощелачивания мочи, такие как гидрокарбонат натрия, цитрат калия и цитрат натрия и тому подобное. Кроме того, в качестве лекарственного средства для лечения подагры можно указать колхицин или нестероидные противовоспалительные лекарственные средства, такие как индометацин, напроксен, фенбуфен, пранопрофен, оксапрозин, кетопрофен, эторикоксиб, теноксикам и тому подобное, и стероиды и тому подобное. В настоящем изобретении активный ингредиент настоящего изобретения можно также применять далее в комбинации по меньшей мере с одним из этих лекарственных средств, и фармацевтическая композиция, содержащая комбинацию по меньшей мере с одним из этих лекарственных средств, включает любые дозированные формы не только в виде одного препарата, содержащего указанное лекарственное средство вместе с активным ингредиентом настоящего изобретения, но также препарат-комбинацию, состоящую из фармацевтической композиции, содержащей активный ингредиент настоящего изобретения, и отдельно полученную фармацевтическую композицию для одновременного введения или введения через различные интервалы времени. Кроме того, при применении в комбинации с любым лекарственным средством, иным, чем активный ингредиент настоящего изобретения, дозу соединения настоящего изобретения можно уменьшить, в зависимости от дозы другого лекарственного средства, применяемого в комбинации, в этом случае можно получить более эффективное благоприятное действие, чем аддитивное действие, при профилактике или лечении указанных выше заболеваний, или можно избежать или уменьшить отрицательное действие другого лекарственного средства, применяемого в комбинации.
ЭФФЕКТ ИЗОБРЕТЕНИЯ
5-членные гетероциклические соединения, представленные вышеуказанной общей формулой (I) настоящего изобретения проявляют превосходную ингибирующую ксантиноксидазу активность и подавляют продуцирование мочевой кислоты. Кроме того, предпочтительное соединение настоящего изобретения может также проявлять превосходную ингибирующую URAT1 активность и усиливать экскрецию мочевой кислоты. Поэтому 5-членные гетероциклические соединения, представленные вышеуказанной общей формулой (I) настоящего изобретения, или их пролекарства, или их фармацевтически приемлемые соли могут сильно подавлять повышение уровня мочевой кислоты в сыворотке и являются применимыми в качестве агента для профилактики или лечения заболеваний, связанных с аномальным уровнем мочевой кислоты в сыворотке, таких как гиперурикемия или тому подобное.
НАИЛУЧШИЙ ВАРИАНТ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Настоящее изобретение далее иллюстрируется более подробно путем нижеследующих ссылочных примеров, примеров и примеров испытаний. Однако, настоящее изобретение не ограничивается ими.
Ссылочный пример 1
Этиловый эфир 4-фтор-2-метоксиметоксибензойной кислоты
К раствору 4-фтор-2-гидроксибензойной кислоты (3,0 г) в этаноле (40 мл) добавляли тионилхлорид (5,61 мл) при 0°C и эту смесь нагревали при кипячении с обратным холодильником в течение 24 часов. Эту реакционную смесь концентрировали и образовавшийся остаток выливали в воду и смесь экстрагировали этилацетатом. Органический слой промывали водой и насыщенным раствором соли, сушили над безводным сульфатом магния. Растворитель удаляли при пониженном давлении, получая при этом этиловый эфир 4-фтор-2-гидроксибензойной кислоты (3,5 г). К раствору этилового эфира 4-фтор-2-гидроксибензойной кислоты (3,5 г) в дихлорметане (30 мл) добавляли N,N-диизопропилэтиламин (5,0 г) и (хлорметил)метиловый простой эфир (2,3 г) при 0°C и эту реакционную смесь перемешивали при комнатной температуре на протяжении ночи. Данную реакционную смесь выливали в воду и образовавшуюся смесь экстрагировали этилацетатом. Полученный органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом магния. Растворитель удаляли при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (элюент: этилацетат/н-гексан), получая при этом указанное в заголовке соединение (2,8 г).
Ссылочный пример 2
1-(Толуол-4-сульфонил)этилизоцианид
К раствору толуол-4-сульфонилметилизоцианида (15 г), метилиодида (109 г), хлорида бензилтриметиламмония (3,5 г) в дихлорметане (300 мл) добавляли водный раствор 5 моль/л гидроксида натрия (307 мл) при охлаждении льдом и полученную смесь перемешивали при такой же температуре в течение 2 часов. К этой реакционной смеси добавляли воду и такую смесь экстрагировали диэтиловым эфиром. Полученный органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом магния. Растворитель удаляли при пониженном давлении, получая при этом указанное в заголовке соединение (16 г).
Ссылочный пример 3
2-Гептеннитрил
К суспензии гидрида натрия (60%, 0,48 г) в тетрагидрофуране (15 мл) добавляли раствор диэтилового эфира цианометанфосфоновой кислоты (1,9 г) в тетрагидрофуране (3 мл) при охлаждении смесью лед-насыщенный раствор соли. Данную реакционную смесь перемешивали при такой же температуре в течение 5 минут, к этой реакционной смеси добавляли пентаналь (0,86 г). После перемешивания при такой же температуре в течение 45 минут к этой реакционной смеси добавляли воду. Реакционную смесь экстрагировали диэтиловым эфиром и полученный органический слой промывали насыщенным раствором соли и сушили над безводным сульфатом магния. Растворитель удаляли при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (элюент: гексан/этилацетатом = 5/1), получая при этом указанное в заголовке соединение (0,56 г).
Ссылочный пример 4
4-Бутил-5-метил-1H-пиррол-3-карбонитрил
К суспензии гидрида натрия (60%, 0,096 г) в диэтиловом эфире (3 мл) добавляли раствор 1-(толуол-4-сульфонил)этилизоцианида (0,42 г) и 2-гептеннитрила (0,22 г) в смешанном растворителе диэтилового эфира (3 мл) и диметилсульфоксида (3 мл) при комнатной температуре и смесь перемешивали при комнатной температуре в течение 1 часа. К этой реакционной смеси добавляли воду (15 мл). Указанную смесь экстрагировали этилацетатом и органический слой промывали насыщенным раствором соли и сушили над безводным сульфатом магния. Растворитель удаляли при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (элюент: этилацетат/н-гексан), получая при этом указанное в заголовке соединение (0,19 г).
Ссылочный пример 5
Этиловый эфир 2-циано-3-(3-фторфенил)акриловой кислоты
Раствор этилового эфира цианоуксусной кислоты (1,1 г), 3-фторбензальдегида (1,5 г) и пирролидина (0,043 г) в этаноле (10 мл) перемешивали при комнатной температуре в течение 2 часов. Осажденное твердое вещество собирали фильтрованием и указанное полученное твердое вещество промывали этанолом (40 мл), получая при этом указанное в заголовке соединение (2,1 г).
Ссылочный пример 6
4-(3-Фторфенил)-1H-пиррол-3-карбонитрил
К раствору этилового эфира 2-циано-3-(3-фторфенил)акриловой кислоты (2,1 г) в метаноле (20 мл) добавляли метоксид натрия (28% раствор в метаноле, 2,2 мл) при 0°C, эту смесь перемешивали при такой же температуре в течение 15 минут. К этой реакционной смеси добавляли по каплям на протяжении 10 минут при 0°С раствор толуол-4-сульфонилметилизоцианида (2,0 г) в дихлорметане (20 мл) и смесь перемешивали при такой же температуре в течение 30 минут. К этой реакционной смеси добавляли 1 моль/л хлористоводородной кислоты, смесь экстрагировали дихлорметаном. Полученный органический слой промывали насыщенным раствором соли и сушили над безводным сульфатом магния. Растворитель удаляли при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (элюент: этилацетат/н-гексан), получая при этом указанное в заголовке соединение (0,60 г).
Ссылочный пример 7
4-Циано-1H-пиррол-3-карбоновая кислота
К раствору этилового эфира 4-циано-1H-пиррол-3-карбоновой кислоты (1,1 г) в метаноле (65 мл) добавляли водный раствор 1 моля/л гидроксида натрия (65 мл) и эту смесь перемешивали при 50°С в течение 5 часов. К реакционной смеси добавляли 1 моль/л хлористоводородной кислоты и эту смесь экстрагировали этилацетатом. Органический слой промывали насыщенным раствором соли и сушили над безводным сульфатом магния. Растворитель удаляли при пониженном давлении. Полученный остаток промывали диэтиловым эфиром, получая при этом указанное в заголовке соединение (0,72 г).
Ссылочный пример 8
Метиламид 4-циано-1Н-пиррол-3-карбоновой кислоты
К раствору 4-циано-1H-пиррол-3-карбоновой кислоты (0,034 г), гидрохлорида метиламина (0,034 г), триэтиламина (0,084 г) и 1-гидроксибензотриазола (0,034 г) в тетрагидрофуране (2,5 мл) добавляли N-этил-N′-3-диметиламинопропилкарбодиимид (0,058 г) при комнатной температуре и полученную смесь перемешивали при такой же температуре на протяжении ночи. Эту реакционную смесь выливали в 1 моль/л хлористоводородной кислоты и смесь экстрагировали этилацетатом. Полученный органический слой промывали насыщенным водным раствором бикарбоната натрия и насыщенным раствором соли и сушили над безводным сульфатом натрия. Растворитель удаляли при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (элюент: этилацетат/н-гексан), получая при этом указанное в заголовке соединение (0,035 г).
Ссылочный пример 9
Этиловый эфир 3-бензилокси-1H-пиразол-4-карбоновой кислоты
Суспензию этилового эфира 1-ацетил-3-oxo-2,3-дигидро-1H-пиразол-4-карбоновой кислоты (2,7 г, указанное соединение получали способом, аналогичным способу, описанному в Bioorganic & Medicinal Chemistry Letters (2002), 12 (16), 2105-2108), бензилбромида (2,5 г), карбоната калия (2,1 г) в N,N-диметилформамиде (20 мл) перемешивали при 40°С в течение 20 часов. К данной реакционной смеси добавляли 1 моль/л хлористоводородной кислоты и полученную смесь экстрагировали этилацетатом. Органический слой промывали насыщенным раствором соли и сушили над безводным сульфатом магния. Растворитель удаляли при пониженном давлении. Остаток очищали колоночной хроматографией на аминопропилсиликагеле (элюент: этилацетат/н-гексан), получая при этом указанное в заголовке соединение (1,6 г).
Ссылочный пример 10
Этиловый эфир 3-бензилокси-1-бензилоксиметил-1H-пиразол-4-карбоновой кислоты
Суспензию этилового эфира 3-бензилокси-1H-пиразол-4-карбоновой кислоты (0,74 г), бензилхлорметилового простого эфира (0,56 г) и N,N-диизопропилэтиламина (0,78 г) в N,N-диметилформамиде (15 мл) перемешивали при 90°C в течение 20 часов. К этой реакционной смеси добавляли 2 моль/л хлористоводородной кислоты при охлаждении льдом и полученную смесь экстрагировали этилацетатом. Органический слой промывали насыщенным раствором соли и сушили над безводным сульфатом магния. Растворитель удаляли при пониженном давлении. Остаток очищали колоночной хроматографией на аминопропилсиликагеле (элюент: этилацетат/н-гексан), получая при этом указанное в заголовке соединение (0,65 г).
Ссылочный пример 11
(3-Бензилокси-1-бензилоксиметил-1H-пиразол-4-ил)метанол
К суспензии литийалюминийгидрида (0,13 г) в тетрагидрофуране (5 мл) добавляли этиловый эфир 3-бензилокси-1-бензилоксиметил-1H-пиразол-4-карбоновой кислоты (0,65 г) при комнатной температуре и смесь перемешивали при такой же температуре в течение 3 час. К этой реакционной смеси добавляли воду и нерастворимое вещество удаляли фильтрованием. Фильтрат сушили над безводным сульфатом магния и указанный растворитель удаляли при пониженном давлении, получая при этом указанное в заголовке соединение (0,57 г).
Ссылочный пример 12
(3-Бензилокси-1-бензилоксиметил-1H-пиразол-4-ил)карбальдегид
К раствору (3-бензилокси-1-бензилоксиметил-1H-пиразол-4-ил)метанола (0,57 г) в дихлорметане (20 мл) добавляли оксид магния (0,77 г) и смесь перемешивали при 50°С в течение 20 часов. Нерастворимое вещество удаляли фильтрованием с отсасыванием через подушку целита и полученный фильтрат концентрировали при пониженном давлении, получая при этом указанное в заголовке соединение (0,57 г).
Ссылочный пример 13
3-Бензилокси-1H-пиразол-4-карбонитрил
К раствору (3-бензилокси-1-бензилоксиметил-1H-пиразол-4-ил)карбальдегида (0,57 г) в муравьиной кислоте (5 мл) добавляли гидрохлорид гидроксиламина (0,13 г) и формиат натрия (0,24 г) и данную смесь нагревали при кипячении с обратным холодильником в течение 5 часов. К этой реакционной смеси добавляли воду и смесь экстрагировали этилацетатом. Полученный органический слой промывали насыщенным раствором соли и сушили над безводным сульфатом магния. Растворитель удаляли при пониженном давлении, получая при этом указанное в заголовке соединение (0,045 г).
Ссылочный пример 14
3-Ацетил[b]бензотиофен-4-карбоксифенилгидразон
Суспензию 3-ацетил[b]бензотиофена (1,5 г) и 4-гидразинобензойной кислоты (1,3 г) в этаноле (20 мл) нагревали при кипячении с обратным холодильником в течение 30 часов. К этой реакционной смеси добавляли воду при комнатной температуре и полученную смесь экстрагировали этилацетатом. Органический слой промывали насыщенным раствором соли и сушили над безводным сульфатом магния. Растворитель удаляли при пониженном давлении. Полученный остаток промывали смесью 1:1 н-гексан/диэтиловый эфир и это нерастворимое вещество собирали фильтрованием, получая при этом указанное в заголовке соединение (1,7 г).
Ссылочный пример 15
4-(3-Бензо[b]тиофен-3-ил-4-формилпиразол-1-ил)бензойная кислота
Фосфорилхлорид (3,0 г) добавляли к N,N-диметилформамиду при охлаждении льдом и полученную смесь перемешивали при такой же температуре в течение 0,5 часа. К этой реакционной смеси добавляли 3-ацетил[b]бензотиофен-4-карбоксифенилгидразон (1,7 г) и смесь перемешивали при комнатной температуре в течение 30 час. К указанной реакционной смеси добавляли воду и эту смесь перемешивали в течение 0,5 часа. И затем нерастворимое вещество собирали фильтрованием и сушили при пониженном давлении, получая при этом указанное в заголовке соединение (0,3 г).
Ссылочный пример 16
Этиловый эфир 3-(2-бензилоксифенил)-2-цианоакриловой кислоты
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в ссылочном примере 5, с применением соответствующих исходных веществ.
Ссылочный пример 17
4-(2-Бензилоксифенил)-1Н-пиррол-3-карбонитрил
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в ссылочном примере 6, с применением соответствующих исходных веществ.
Ссылочный пример 18
Этиловый эфир 5-бром-2-метоксиметоксибензойной кислоты
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в ссылочном примере 1, с применением соответствующих исходных веществ.
Ссылочные примеры 19-25
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в ссылочном примере 6, с применением соответствующих исходных веществ.
Ссылочные примеры 26-32
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в ссылочном примере 8, с применением соответствующих исходных веществ.
Ссылочные примеры 33-51
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в ссылочном примере 6, с применением соответствующих исходных веществ.
Ссылочные примеры 52-61
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в ссылочном примере 4, с применением соответствующих исходных веществ.
Ссылочный пример 62
2-(1-Циклогексилэтилиден)-1-гидразинкарбоксамид
К смеси циклогексилметилкетона (1,5 г), гидрохлорида семикарбазида (1,86 г) и воды (23 мл) добавляли ацетат натрия (3,75 г) и полученную смесь перемешивали при комнатной температуре на протяжении ночи. Нерастворимое вещество собирали фильтрованием, промывали водой, сушили при пониженном давлении, получая при этом указанное в заголовке соединение (1,9 г).
Ссылочный пример 63
3-Циклогексил-1H-пиразол-4-карбальдегид
К раствору 2-(1-циклогексилэтилиден)-1-гидразинкарбоксамида (1,92 г) в N,N-диметилформамиде (46 мл) добавляли фосфорилхлорид (4,82 г) при охлаждении льдом и образовавшуюся смесь перемешивали при 80°С на протяжении ночи. Указанную реакционную смесь выливали в воду и смесь экстрагировали этилацетатом. Полученный органический слой сушили над безводным сульфатом магния. Растворитель удаляли при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (элюент: этилацетат/н-гексан), получая при этом указанное в заголовке соединение (1,2 г).
Ссылочный пример 64
3-Циклогексил-1H-пиразол-4-карбонитрил
К смеси 3-циклогексил-1H-пиразол-4-карбальдегида (1,2 г), гидрохлорида гидроксиламина (1,4 г) и тетрагидрофурана (12 мл) добавляли пиридин (2,66 г) и образованную смесь нагревали при кипячении с обратным холодильником на протяжении ночи. К этой реакционной смеси добавляли уксусный ангидрид (2,75 г) и смесь нагревали при кипячении с обратным холодильником в течение 12 час. К указанной реакционной смеси добавляли водный раствор 1 моль/л гидроксида натрия. После перемешивания 30 минут к данной смеси добавляли 2 моль/л хлористоводородной кислоты до тех пор, пока значение рН не достигло 1. Полученное твердое вещество собирали фильтрованием и это твердое вещество промывали водой, сушили при пониженном давлении, получая при этом указанное в заголовке соединение (1,2 г).
Ссылочный пример 65
2-Бром-5-фторизоникотиновая кислота
К раствору 2-бром-5-фторпиридина (5,0 г) в тетрагидрофуране (100 мл) способом прикапывания при -70°С добавляли раствор 2,6 моль/л н-бутиллития в тетрагидрофуране (12 мл) и эту смесь перемешивали при такой же температуре в течение 2 час. К этой реакционной смеси добавляли избыточное количество сухого льда при -70°С и смесь перемешивали при комнатной температуре в течение 12 часов. Эту смесь выливали в воду и смесь экстрагировали диэтиловым эфиром. К полученному водному слою добавляли 1 моль/л хлористоводородной кислоты (2 мл) и полученную смесь экстрагировали этилацетатом. Органический слой концентрировали, получая при этом указанное в заголовке соединение (5,2 г).
Ссылочный пример 66
Этиловый эфир 2-бром-5-фторизоникотиновой кислоты
К раствору 2-бром-5-фторизоникотиновой кислоты (5,2 г) в N,N-диметилформамиде (100 мл) добавляли карбонат калия (9,8 г) и иодэтан (7,4 г) при комнатной температуре и эту смесь перемешивали при такой же температуре в течение 24 часов. Реакционную смесь выливали в воду и полученную смесь экстрагировали этилацетатом. Органический слой промывали водой и насыщенным раствором соли, сушили над безводным сульфатом магния. Растворитель удаляли при пониженном давлении, получая при этом указанное в заголовке соединение (2,9 г).
Ссылочный пример 67
Этиловый эфир 5-бензилокси-2-бромизоникотиновой кислоты
К раствору бензилового спирта (1,5 г) в тетрагидрофуране (30 мл) добавляли гидрид натрия (55%, 0,3 г) при охлаждении льдом и полученную смесь перемешивали при такой же температуре в течение 5 минут. К этой реакционной смеси добавляли раствор этилового эфира 2-бром-5-фторизоникотиновой кислоты (2,9 г) в тетрагидрофуране (30 мл) и смесь перемешивали при комнатной температуре в течение 2 час. Эту реакционную смесь выливали в воду и смесь экстрагировали этилацетатом. Полученный органический слой промывали водой и насыщенным раствором соли, сушили над безводным сульфатом магния. Растворитель удаляли при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (элюент: этилацетат/н-гексан), получая при этом указанное в заголовке соединение (2,4 г).
Ссылочный пример 68
4-(трет-Бутилдифенилсиланилоксиметил)-1H-пиррол-3-карбонитрил
К суспензии гидрида натрия (60%, 0,12 г) в диэтиловом эфире (5 мл) добавляли раствор 4-(трет-бутилдифенилсиланилокси)бута-2-еннитрила (0,81 г) и п-толуолсульфонилметилизоцианида (0,49 г) в диэтиловом эфире (5 мл) и диметилсульфоксиде (5 мл). После перемешивания при комнатной температуре в течение 5 час к этой реакционной смеси добавляли воду и реакционную смесь экстрагировали этилацетатом. Полученный органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния. Растворитель удаляли при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (элюент: смесь н-гексан/этилацетат от 60/40 до 39/61), получая при этом указанное в заголовке соединение (0,50 г).
Ссылочный пример 69
4-Тиофен-2-ил-1H-пиразол-3-карбонитрил
После добавления триметилсилилдиазометана в гексане (0,6 моль/л, 5 мл) к тетрагидрофурану (20 мл) в атмосфере аргона к этой реакционной смеси способом прикапывания в течение 5 минут при -78°С добавляли раствор н-бутиллития в гексане (2,6 моль/л, 1,08 мл) и смесь перемешивали при такой же температуре в течение 20 минут. И затем к указанной реакционной смеси способом прикапывания на протяжении 20 минут добавляли раствор 2-тиофен-2-илметиленмалононитрила (0,32 г) в тетрагидрофуране (5 мл). К реакционной смеси добавляли насыщенный водный раствор хлорида аммония и смесь экстрагировали этилацетатом. Полученный органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали при пониженном давлении. Полученный остаток промывали гексаном, получая при этом 4-тиофен-2-ил-5-триметилсиланил-1Н-пиразол-3-карбонитрил (0,496 г). К 4-тиофен-2-ил-5-триметилсиланил-1Н-пиразол-3-карбонитрилу добавляли метанол (20 мл) и 1,0 моль/л водного раствора гидроксида натрия (20 мл) и эту смесь нагревали при кипячении с обратным холодильником в течение 2 час. Указанную реакционную смесь подкисляли (рН 1) добавлением 1,0 моль/л хлористоводородной кислоты, осажденное твердое вещество собирали фильтрованием. Полученное твердое вещество промывали водой, сушили при пониженном давлении при 50°С, получая при этом указанное в заголовке соединение (0,154 г).
Ссылочный пример 70
1-(2-Хлорпиридин-4-ил)-4-фенил-1H-пиррол-3-карбонитрил
К раствору 4-фенил-1H-пиррол-3-карбонитрила (0,168 г), иодида меди(I) (0,019 г), N,N-диметилглицина (0,021 г) и карбоната цезия (0,325 г) в диметилсульфоксиде (10 мл) добавляли 2-хлор-4-иодпиридин (0,287 г) при комнатной температуре и эту смесь выдерживали при 180°С в запаянной трубке при микроволновом облучении в течение 5 минут. После охлаждения до температуры окружающей среды данную реакционную смесь разбавляли дихлорметаном и водой и нерастворимое вещество удаляли фильтрованием через подушку целита. Полученный органический слой отделяли и указанный органический растворитель удаляли при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (элюент: этилацетат/гексан = 80/20), получая при этом указанное в заголовке соединение (0,16 г).
Ссылочные примеры 71-74
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в ссылочном примере 4, с применением соответствующих исходных веществ.
Ссылочные примеры 75-91
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в ссылочном примере 6, с применением соответствующих исходных веществ.
Ссылочные примеры 92-96
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в ссылочном примере 64, с применением соответствующих исходных веществ.
Ссылочные примеры 97-98
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в ссылочном примере 69, с применением соответствующих исходных веществ.
Пример 1
Этиловый эфир 4-(3-бутил-4-циано-2-метилпиррол-1-ил)бензойной кислоты
Суспензию 4-бутил-5-метил-1Н-пиррол-3-карбонитрила (0,081 г), этилового эфира 4-фторбензойной кислоты (0,10 г) и карбоната цезия (0,21 г) в N,N-диметилформамиде (3 мл) перемешивали при 70°С на протяжении ночи. Эту реакционную смесь выливали в воду и образовавшуюся смесь экстрагировали этилацетатом. Органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния. Растворитель удаляли при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (элюент: этилацетат/н-гексан = 1/6), получая при этом указанное в заголовке соединение (0,032 г).
Пример 2
4-(3-Бутил-4-циано-2-метилпиррол-1-ил)бензойная кислота
Суспензию этилового эфира 4-(3-бутил-4-циано-2-метилпиррол-1-ил)бензойной кислоты (0,030 г) и моногидрата гидроксида лития (0,041 г) в этаноле (2 мл) и воде (1 мл) перемешивали при 50°С в течение 2 часов. К этой реакционной смеси добавляли 1 моль/л хлористоводородной кислоты (5 мл) и смесь перемешивали при комнатной температуре в течение 30 минут. Реакционную смесь экстрагировали этилацетатом и образовавшийся органический слой промывали водой, сушили над безводным сульфатом магния. Растворитель удаляли при пониженном давлении, получая при этом указанное в заголовке соединение (0,027 г).
Пример 3
Этиловый эфир 4-(4-бром-3-цианопиразол-1-ил)бензойной кислоты
Суспензию 4-бром-1H-пиразол-3-карбонитрила (0,52 г), этилового эфира 4-фторбензойной кислоты (0,56 г) и карбоната цезия (1,5 г) в N,N-диметилформамиде (10 мл) перемешивали при 100°С в течение 2 час. После охлаждения до температуры окружающей среды эту реакционную смесь выливали в воду и смесь экстрагировали этилацетатом. Образовавшийся органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния. Органический слой пропускали через аминопропилсиликагель и полученный фильтрат концентрировали при пониженном давлении. Полученный остаток промывали смешанным растворителем н-гексан/диэтиловый эфир = 5/1, получая при этом указанное в заголовке соединение (0,25 г).
Пример 4
Этиловый эфир 4-[3-циано-4-(3,4-метилендиоксифенил)пиразол-1-ил]бензойной кислоты
Суспензию этилового эфира 4-(4-бром-3-цианопиразол-1-ил)бензойной кислоты (0,17 г), (3,4-метилендиоксифенил)бороновой кислоты (0,11 г), тетракис(трифенилфосфин)палладия (0,12 г) и карбоната натрия (0,17 г) в смешанном растворителе воды (0,5 мл) и N,N-диметилформамида (5 мл) перемешивали при 70°С в течение 12 часов. К этой реакционной смеси добавляли разбавленную хлористоводородную кислоту и смесь экстрагировали этилацетатом. Образовавшийся органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния. Растворитель удаляли при пониженном давлении. Остаток очищали колоночной хроматографией на аминопропилсиликагеле (элюент: этилацетат/н-гексан = 1/5), получая при этом указанное в заголовке соединение (0,05 г).
Пример 5
4-[3-Циано-4-(3,4-метилендиоксифенил)пиразол-1-ил]бензойная кислота
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 2, с применением соответствующих исходных веществ.
Пример 6
Этиловый эфир 4-(3-бензилокси-4-цианопиразол-1-ил)бензойной кислоты
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 1, с применением соответствующих исходных веществ.
Пример 7
4-(3-Бензилокси-4-цианопиразол-1-ил)бензойная кислота
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 2, с применением соответствующих исходных веществ.
Пример 8
4-(3-Бензо[b]тиофен-3-ил-4-цианопиразол-1-ил)бензойная кислота
Раствор 4-(3-бензо[b]тиофен-3-ил-4-формилпиразол-1-ил)бензойной кислоты (0,26 г), гидрохлорида гидроксиламина (0,058 г) и формиата натрия (0,10 г) в муравьиной кислоте (5 мл) нагревали при кипячении с обратным холодильником в течение 24 час. К этой реакционной смеси добавляли воду при комнатной температуре и смесь экстрагировали этилацетатом. Образовавшийся органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния. Растворитель удаляли при пониженном давлении. Полученный остаток растворяли в пиридине (5 мл), к раствору способом прикапывания при охлаждении добавляли трифторуксусный ангидрид (0,48 г) и эту смесь перемешивали при комнатной температуре в течение 5 часов. К реакционной смеси добавляли 2 моль/л хлористоводородной кислоты и смесь экстрагировали этилацетатом. Образовавшийся органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния. Растворитель удаляли при пониженном давлении. Полученный остаток промывали смесью н-гексан/диэтиловый эфир = 1/1, получая при этом указанное в заголовке соединение (0,13 г).
Пример 9
Этиловый эфир 4-[4-(2-бензилоксифенил)-3-цианопиррол-1-ил]-2-метоксиметоксибензойной кислоты
К раствору 4-(2-бензилоксифенил)-1H-пиррол-3-карбонитрила (1,5 г), этилового эфира 4-фтор-2-метоксиметоксибензойной кислоты (1,4 г) в N,N-диметилформамиде (25 мл) добавляли карбонат цезия и эту смесь перемешивали при 65°С в течение 15 час. Реакционную смесь выливали в воду, осажденное твердое вещество собирали фильтрованием и промывали водой и н-гексаном, сушили при пониженном давлении при 50°С, получая при этом указанное в заголовке соединение (2,3 г).
Пример 10
Этиловый эфир 4-[3-циано-4-(2-гидроксифенил)пиррол-1-ил]-2-метоксиметоксибензойной кислоты
К раствору этилового эфира 4-[4-(2-бензилоксифенил)-3-цианопиррол-1-ил]-2-метоксиметоксибензойной кислоты (2,3 г) в смешанном растворителе этилацетата (20 мл) и метанола (20 мл) добавляли палладий на порошке угля в атмосфере аргона и эту смесь перемешивали при комнатной температуре в атмосфере водорода в течение 5 часов. Нерастворимое вещество удаляли фильтрованием и полученный фильтрат концентрировали при пониженном давлении, получая при этом указанное в заголовке соединение (1,4 г).
Пример 11
Этиловый эфир 4-[3-циано-4-(2-гидроксифенил)пиррол-1-ил]-2-гидроксибензойной кислоты
К раствору этилового эфира 4-[3-циано-4-(2-гидроксифенил)пиррол-1-ил]-2-метоксиметоксибензойной кислоты (0,12 г) в смешанном растворителе тетрагидрофурана (3 мл) и этанола (5 мл) добавляли 2 моль/л хлористоводородной кислоты (2 мл) и эту смесь перемешивали при 70°С в течение 18 час. К этой реакционной смеси добавляли воду, осажденное твердое вещество собирали фильтрованием и это твердое вещество промывали водой, сушили при пониженном давлении и 50°С, получая при этом указанное в заголовке соединение (0,054 г).
Пример 12
4-[3-Циано-4-(2-гидроксифенил)пиррол-1-ил]-2-гидроксибензойная кислота
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 2, с применением соответствующих исходных веществ.
Пример 13
Этиловый эфир 4-{3-циано-4-[2-(2-метоксиэтокси)фенил]пиррол-1-ил}-2-метоксиметоксибензойной кислоты
К раствору этилового эфира 4-[4-(2-гидроксифенил)-3-цианопиррол-1-ил]-2-метоксиметоксибензойной кислоты (0,12 г) и карбоната калия (0,10 г) в N,N-диметилформамиде (1 мл) добавляли 1-бром-3-метоксипропан (0,092 г) и эту смесь перемешивали при 70°С в течение 18 час. Указанную реакционную смесь выливали в воду и смесь экстрагировали этилацетатом. Полученный органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и концентрировали при пониженном давлении, получая при этом указанное в заголовке соединение (0,12 г).
Пример 14
Этиловый эфир 4-{3-циано-4-[2-(2-метоксиэтокси)фенил]пиррол-1-ил}-2-гидроксибензойной кислоты
Указанное в заголовке соединение (0,072 г) получали способом, аналогичным способу, описанному в примере 11, с применением соответствующих исходных веществ.
Пример 15
4-{3-Циано-4-[2-(2-метоксиэтокси)фенил]пиррол-1-ил}-2-гидроксибензойная кислота
К раствору этилового эфира 4-{3-циано-4-[2-(2-метоксиэтокси)фенил]пиррол-1-ил}-2-гидроксибензойной кислоты (0,072 г) в смешанном растворителе этанола (9 мл) и тетрагидрофурана (3 мл) добавляли 1 моль/мл водного раствора гидроксида лития (2,7 мл) и эту смесь перемешивали при комнатной температуре в течение 48 час. Данную реакционную смесь выливали в 1 моль/л хлористоводородной кислоты (2,7 мл) и к этой смеси добавляли воду (30 мл). Осажденное твердое вещество собирали фильтрованием. Это полученное твердое вещество промывали водой, сушили при пониженном давлении и 50°С, получая при этом указанное в заголовке соединение (0,051 г).
Пример 16
Этиловый эфир 4-(3-циано-4-метоксипиррол-1-ил)бензойной кислоты
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 1, с применением соответствующих исходных веществ.
Пример 17
Этиловый эфир 4-(3-бензилокси-4-цианопиррол-1-ил)бензойной кислоты
К раствору этилового эфира 4-(3-циано-4-метоксипиррол-1-ил)бензойной кислоты (0,081 г) в дихлорметане (3 мл) добавляли трибромид бора (0,33 мл, раствор 1 моль/л в дихлорметане) при охлаждении льдом и эту смесь перемешивали при такой же температуре в течение 2 час. К указанной смеси добавляли воду и смесь экстрагировали диэтиловым эфиром. Органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния. Растворитель удаляли при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (элюент: этилацетат/н-гексан = 1/1), получая при этом этиловый эфир 4-(3-циано-4-гидроксипиррол-1-ил)бензойной кислоты (0,052 г). К раствору этилового эфира 4-(3-циано-4-гидроксипиррол-1-ил)бензойной кислоты (0,052 г) в N,N-диметилформамиде (4 мл) добавляли бензилбромид (0,038 г) и карбонат цезия (0,13 г) при комнатной температуре и эту смесь перемешивали при 80°С в течение 5 час. К этой реакционной смеси добавляли воду при комнатной температуре и осажденное твердое вещество собирали фильтрованием и промывали метанолом (5 мл), получая при этом указанное в заголовке соединение (0,016 г).
Пример 18
4-(3-Циано-4-бензилоксипиррол-1-ил)бензойная кислота
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 2, с применением соответствующих исходных веществ.
Пример 19
Этиловый эфир 2-(3-циано-4-фенилпиррол-1-ил)изоникотиновой кислоты
К раствору 4-фенил-1H-пиррол-3-карбонитрила (0,1 г) в толуоле (0,70 мл) добавляли этиловый эфир 2-бромизоникотиновой кислоты (0,19 г), фосфат калия (0,31 г), (1R,2R)-(-)-N,N′-диметилциклогексан-1,2-диамин (0,02 г) и иодид меди (0,007 г) при комнатной температуре и эту смесь перемешивали при 110°C в течение 24 час. Нерастворимое вещество удаляли фильтрованием через целит и фильтрат концентрировали. Полученный остаток очищали колоночной хроматографией на силикагеле (элюент: этилацетат/н-гексан, 10/90 - 66/34), получая при этом указанное в заголовке соединение (0,066 г).
Пример 20
2-(3-Циано-4-фенилпиррол-1-ил)изоникотиновая кислота
Указанное в заголовке соединение (0,041 г) получали способом, аналогичным способу, описанному в примере 2, с применением соответствующих исходных веществ.
Пример 21
Этиловый эфир 5-(3-циано-4-фенилпиррол-1-ил)-2-метоксиметоксибензойной кислоты
Смесь 4-фенил-1H-пиррол-3-карбонитрила (0,2 г), этиловый эфир 5-бром-2-метоксиметоксибензойной кислоты (0,36 г), иодида меди (0,023 г), N,N-диметилглицина (0,025 г), карбоната цезия (0,39 г) и диметилсульфоксида (3 мл) перемешивали при 75°C в течение 12 час. После охлаждения до температуры окружающей среды нерастворимое вещество удаляли фильтрованием через подушку целита и полученный фильтрат концентрировали. Полученный таким образом остаток очищали колоночной хроматографией на силикагеле (элюент: этилацетат/н-гексан = 10/90 - 66/34), получая при этом указанное в заголовке соединение (0,27 г).
Пример 22
5-(3-Циано-4-фенилпиррол-1-ил)-2-гидроксибензойная кислота
Указанное в заголовке соединение (0,16 г) получали способом, аналогичным способу, описанному в примере 2 и примере 11, с применением соответствующих исходных веществ.
Пример 23
Этиловый эфир 3-(3-циано-4-фенилпиррол-1-ил)бензойной кислоты
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 21, с применением соответствующих исходных веществ.
Пример 24
3-(3-Циано-4-фенилпиррол-1-ил)бензойная кислота
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 15, с применением соответствующих исходных веществ.
Пример 25
Этиловый эфир 4-(3-амино-4-цианопиразол-1-ил)бензойной кислоты
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 1, с применением соответствующих исходных веществ.
Пример 26
Этиловый эфир 4-(3-ацетиламино-4-цианопиразол-1-ил)бензойной кислоты
К раствору этилового эфира 4-(3-амино-4-цианопиразол-1-ил)бензойной кислоты (0,1 г) в тетрагидрофуране (4 мл) добавляли ацетилхлорид (0,12 г) и пиридин (0,15 г) и эту смесь перемешивали при комнатной температуре в течение 12 часов. Эту реакционную смесь выливали в воду и осажденное твердое вещество собирали фильтрованием. Полученное таким образом твердое вещество промывали этилацетатом, сушили при пониженном давлении и 50°С, получая при этом указанное в заголовке соединение (0,088 г).
Пример 27
4-(3-Ацетиламино-4-цианопиразол-1-ил)бензойная кислота
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 2, с применением соответствующих исходных веществ.
Пример 28
1-(5-Формилфуран-2-ил)-4-фенил-1H-пиррол-3-карбонитрил
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 1, с применением 5-бромфуран-2-карбальдегида вместо этилового эфира 4-фторбензойной кислоты.
Пример 29
5-(3-Циано-4-фенилпиррол-1-ил)фуран-2-карбоновая кислота
К раствору 1-(5-формилфуран-2-ил)-4-фенил-1H-пиррол-3-карбонитрила (0,14 г) в тетрагидрофуране (4 мл) добавляли оксид серебра (0,15 г) и водный раствор гидроксида натрия (2 моль/л, 0,4 мл) и эту смесь перемешивали при комнатной температуре в течение 6 часов. Нерастворимое вещество удаляли фильтрованием и полученный фильтрат концентрировали. К остатку добавляли воду (15 мл) и хлористоводородную кислоту (2 моль/л, 2 мл), эту смесь экстрагировали этилацетатом. Полученный органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (элюент: метанол/дихлорметан = 1/10 - 1/5), получая при этом указанное в заголовке соединение (0,040 г).
Примеры 30-32
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 1, с применением соответствующих исходных веществ.
Примеры 33-35
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 10, с применением соответствующих исходных веществ.
Примеры 36-52
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 13, с применением соответствующих исходных веществ.
Примеры 53-54
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 1, с применением соответствующих исходных веществ.
Пример 55
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 10, с применением соединения примера 54 вместо этилового эфира 4-[4-(2-бензилоксифенил)-3-цианопиррол-1-ил]-2-метоксиметоксибензойной кислоты.
Примеры 56-60
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 1, с применением соответствующих исходных веществ.
Примеры 61-62
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 13, с применением соответствующих исходных веществ.
Пример 63
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 1, с применением соответствующих исходных веществ.
Пример 64
Этиловый эфир 4-[3-циано-4-(3-гидроксиметилфенил)пиррол-1-ил]бензойной кислоты
3-Циано-5-[1-(4-этоксикарбонилфенил)-1H-пиррол-3-ил]бензойную кислоту получали способом, аналогичным способу примера 10, с применением этилового эфира 4-[3-циано-4-(3-бензилоксиметилфенил)пиррол-1-ил]бензойной кислоты. К раствору полученной карбоновой кислоты (1,0 г) в тетрагидрофуране (30 мл) добавляли комплекс боран-тетрагидрофуран (1,2 моль/л раствора тетрагидрофурана, 3,75 мл) при 0°С и эту смесь перемешивали при комнатной температуре в течение 2 час. К этой реакционной смеси добавляли насыщенный водный раствор бикарбоната натрия и эту смесь экстрагировали диэтиловым эфиром. Органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (элюент: метанол/дихлорметан = 1/20), получая при этом указанное в заголовке соединение (0,21 г).
Примеры 65-73
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 1, с применением соответствующих исходных веществ.
Примеры 74-75
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 17, с применением соответствующих исходных веществ.
Примеры 76-90
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 1, с применением соответствующих исходных веществ.
Примеры 91-92
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 55, с применением соответствующих исходных веществ и разделяли колоночной хроматографией на силикагеле (элюент: этилацетат/н-гексан = 10/90 - 66/34).
Примеры 93-94
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 26, с применением соответствующих исходных веществ.
Примеры 95-116
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 9, с применением соответствующих исходных веществ.
Пример 117
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 55, с применением соответствующих исходных веществ.
Примеры 118-123
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 9, с применением соответствующих исходных веществ.
Пример 124
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 55, с применением соответствующих исходных веществ.
Пример 125
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 9, с применением соответствующих исходных веществ.
Пример 126
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 55, с применением соответствующих исходных веществ.
Примеры 127-134
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 9, с применением соответствующих исходных веществ.
Примеры 135-136
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 10, с применением соответствующих исходных веществ.
Пример 137
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 13, с применением соответствующих исходных веществ.
Примеры 138-142
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 9, с применением соответствующих исходных веществ.
Примеры 143-263
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 2, с применением соответствующих исходных веществ.
Пример 264
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 29, с применением соответствующих исходных веществ.
Примеры 265-359
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 11 и примере 12, с применением соответствующих исходных веществ.
Примеры 360-370
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 2, с применением соответствующих исходных веществ.
Примеры 371-375
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 2, с применением соответствующего сложного эфира, который получали способом, аналогичным способу, описанному в примере 1, с применением этилового эфира 6-хлорникотиновой кислоты вместо этилового эфира 4-фтор-2-метоксиметоксибензойной кислоты.
Пример 376
4-(3-Циано-4-фенилпиррол-1-ил)бензамид
К раствору 4-(3-циано-4-фенилпиррол-1-ил)бензойной кислоты (0,14 г) в тетрагидрофуране (2,5 мл) добавляли 1,1′-карбонилдиимидазол (0,16 г). После перемешивания в течение 30 минут к этой реакционной смеси добавляли водный аммиак (28% раствор, 0,75 мл) и эту смесь перемешивали 2 час. К этой реакционную смеси добавляли воду (10 мл), осажденное белое твердое вещество собирали фильтрованием и промывали метанолом, сушили, получая при этом указанное в заголовке соединение (0,13 г).
Пример 377
Этиловый эфир 5-(3-циано-4-фенилпиррол-1-ил)пиридин-2-карбоновой кислоты
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 19, с применением соответствующих исходных веществ.
Пример 378
Этиловый эфир 4-(3-циано-4-фенилпиррол-1-ил)-2-нитробензойной кислоты
Указанное в заголовке соединение 0,137 г) получали способом, аналогичным способу, описанному в примере 1, с применением этилового эфира 4-фтор-2-нитробензойной кислоты вместо этилового эфира 4-фторбензойной кислоты.
Пример 379
Этиловый эфир 2-амино-4-(3-циано-4-фенилпиррол-1-ил)бензойной кислоты
К раствору этилового эфира 4-(3-циано-4-фенилпиррол-1-ил)-2-нитробензойной кислоты (0,090 г) в смешанном растворителе метанола (2,5 мл) и этилацетата (2,5 мл) добавляли 10% палладия на порошке угля (0,016 г) в атмосфере аргона и эту смесь перемешивали при 40°С в атмосфере водорода в течение 3 час. После этого атмосферу водорода реакционной смеси заменяли атмосферой аргона, нерастворимое вещество удаляли фильтрованием с отсасыванием через подушку целита. Полученный фильтрат концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на аминопропилсиликагеле (элюент: этилацетат/гексан = 50/50), получая при этом указанное в заголовке соединение (0,070 г).
Пример 380
Этиловый эфир 4-(3-циано-4-фенилпиррол-1-ил)-2-метансульфониламинобензойной кислоты
К раствору этилового эфира 2-амино-4-(3-циано-4-фенилпиррол-1-ил)бензойной кислоты (0,050 г) и триэтиламина (0,046 г) в дихлорметане (2 мл) добавляли метансульфонилхлорид (0,043 г) при охлаждении льдом и эту смесь перемешивали при комнатной температуре в течение 3 дней. Эту реакционную смесь концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (элюент: этилацетат/н-гексан = 75/25), получая при этом указанное в заголовке соединение (0,015 г).
Пример 381
Этиловый эфир 2-ацетиламино-4-(3-циано-4-фенилпиррол-1-ил)бензойной кислоты
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 380, с применением ацетилхлорида вместо метансульфонилхлорида.
Пример 382
4-Фенил-1-[4-(1H-тетразол-5-ил)пиридин-2-ил]-1H-пиррол-3-карбонитрил
К раствору 2-(3-циано-4-фенилпиррол-1-ил)изоникотинамида (0,058 г) и азида натрия (0,039 г) в смешанном растворителе ацетонитрила (1,0 мл) и тетрагидрофурана (0,5 мл) добавляли тетрахлорсилан (0,068 г) при комнатной температуре и эту смесь перемешивали при 80°С на протяжении ночи. К реакционной смеси добавляли воду, полученное твердое вещество собирали фильтрованием. После промывания водой указанное твердое вещество сушили при 50°С при пониженном давлении, получая при этом указанное в заголовке соединение (0,051 г).
Пример 383
Этиловый эфир 5-бензилокси-2-(3-циано-4-фенилпиррол-1-ил)изоникотиновой кислоты
К раствору 3-циано-4-фенилпиррола (0,20 г) в диметилсульфоксиде (2 мл) добавляли этиловый эфир 5-бензилокси-2-бромизоникотиновой кислоты (0,30 г), карбонат цезия (0,30 г), иодид меди (0,010 г) и N,N-диметилглицин (0,020 г) при комнатной температуре и эту смесь перемешивали при 110°С в течение 8 час. Нерастворимое вещество удаляли фильтрованием с отсасыванием через подушку целита. Полученный фильтрат выливали в воду и смесь экстрагировали этилацетатом. Полученный органический слой промывали водой и насыщенным раствором соли, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (элюент: этилацетат/н-гексан = 10/90-60/40), получая при этом указанное в заголовке соединение (0,20 г).
Пример 384
Этиловый эфир 2-(3-циано-4-фенилпиррол-1-ил)-5-гидроксиизоникотиновой кислоты
К раствору этилового эфира 5-бензилокси-2-(3-циано-4-фенилпиррол-1-ил)изоникотиновой кислоты в смешанном растворителе метанола (2 мл) и этилацетата (2 мл) добавляли палладий на порошке угля (0,020 г) и эту смесь перемешивали при комнатной температуре в атмосфере водорода в течение 30 минут. Нерастворимое вещество удаляли фильтрованием с отсасыванием через подушку целита. Полученный фильтрат концентрировали при пониженном давлении. Полученное твердое вещество промывали диэтиловым эфиром, сушили, получая при этом указанное в заголовке соединение (0,040 г).
Пример 385
2-(3-Циано-4-фенилпиррол-1-ил)-5-гидроксиизоникотиновая кислота
К раствору этилового эфира 2-(3-циано-4-фенилпиррол-1-ил)-5-гидроксиизоникотиновой кислоты (0,050 г) в смешанном растворителе тетрагидрофурана (3,6 мл) и этанола (1,2 мл) добавляли водный раствор 1 моль/л гидроксида лития (1,2 мл) при комнатной температуре и эту смесь перемешивали при такой же температуре в течение 5 часов. Эту смесь выливали в воду и смесь промывали диэтиловым эфиром. К полученному водному слою добавляли 1 моль/л хлористоводородной кислоты (1,2 мл) и осажденное твердое вещество собирали фильтрованием и промывали водой и н-гексаном. Это твердое вещество сушили при пониженном давлении и 50°C, получая при этом указанное в заголовке соединение (0,030 г).
Пример 386
Этиловый эфир 4-(3-циано-4-гидроксиметилпиррол-1-ил)бензойной кислоты
Суспензию 4-(трет-бутилдифенилсиланилоксиметил)-1H-пиррол-3-карбонитрила (0,3 г), этилового эфира 4-фторбензойной кислоты (0,35 г) и карбоната цезия (0,81 г) в N,N-диметилформамиде (2 мл) перемешивали при 70°C на протяжении ночи. К этой реакционной смеси добавляли воду и смесь экстрагировали этилацетатом. Полученный органический слой промывали водой и насыщенным раствором соли, концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (элюент: гексан/этилацетат = 80/20 - 30/70), получая при этом указанное в заголовке соединение (0,0310 г).
Пример 387
4-(3-Циано-4-этоксиметилпиррол-1-ил)бензойная кислота
К раствору этилового эфира 4-(3-циано-4-гидроксиметилпиррол-1-ил)бензойной кислоты (0,022 г) в тетрагидрофуране (1 мл) добавляли триэтиламин (0,0082 г) и метансульфонилхлорид (0,0093 г) при охлаждении льдом. После нагревания до температуре окружающей среды эту смесь перемешивали в течение 30 минут. Нерастворимое вещество этой реакционной смеси удаляли фильтрованием и полученный фильтрат добавляли к смеси этанола (1,125 г) и гидрида натрия (60%, 0,13 г), и эту смесь перемешивали в течение 5 часов. К реакционной смеси добавляли воду и эту смесь перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси добавляли 2 моль/л хлористоводородной кислоты (3 мл), эту смесь экстрагировали этилацетатом. Полученный органический слой промывали насыщенным раствором соли, концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (элюент: дихлорметан/метанол = 88/12 - 81/19), получая при этом указанное в заголовке соединение (0,010 г).
Пример 388
Метиловый эфир 4-(3-циано-4-фенилпиррол-1-ил)пиридин-2-карбоновой кислоты
К раствору 1-(2-хлорпиридин-4-ил)-4-фенил-1H-пиррол-3-карбонитрила (0,070 г), ацетата палладия (II) (0,006 г) и триэтиламина (0,056 г) в метаноле (1 мл) и диметилсульфоксиде (1 мл) добавляли 1,3-бис(дифенилфосфино)пропан (0,025 г) в атмосфере аргона при комнатной температуре и эту смесь перемешивали в атмосфере монооксида углерода при 75°C в течение 1 дня. После охлаждения до температуры окружающей среды эту реакционную смесь разбавляли дихлорметаном и водой. После удаления нерастворимого вещества фильтрованием с отсасыванием через подушку целита полученный органический слой отделяли и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (элюент: этилацетат/гексан = 67/33), получая при этом указанное в заголовке соединение (0,053 г).
Примеры 389-392
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 1, с применением соответствующих исходных веществ.
Пример 393
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 11, с применением соответствующих исходных веществ.
Примеры 394-397
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 1, с применением соответствующих исходных веществ.
Примеры 398-401
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 9, с применением соответствующих исходных веществ.
Примеры 402-403
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 55, с применением соответствующих исходных веществ и разделяли колоночной хроматографией на силикагеле (элюент: этилацетат/н-гексан = 25/75).
Примеры 404-407
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 9, с применением соответствующих исходных веществ.
Примеры 408-412
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 21, с применением метилового эфира 4-иод-2-метоксиметоксибензойной кислоты и соответствующих исходных веществ.
Примеры 413-414
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 9, с применением соответствующих исходных веществ.
Примеры 415-416
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 9, с применением соответствующих исходных веществ и этилового эфира 2,4-дифтор-6-метоксиметоксибензойной кислоты вместо этилового эфира 4-фтор-2-метоксиметоксибензойной кислоты.
Пример 417
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 378, с применением соответствующих исходных веществ.
Пример 418
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 379, с применением соответствующих исходных веществ.
Примеры 419-432
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 21, с применением этилового эфира 2-бромизоникотиновой кислоты и соответствующих исходных веществ.
Примеры 433-435
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 384, с применением соответствующих исходных веществ.
Примеры 436-441
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 13, с применением соответствующих исходных веществ.
Примеры 442-449
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 383, с применением соответствующих исходных веществ.
Пример 450
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 19, с применением этилового эфира 2-бром-5-фторизоникотиновой кислоты и соответствующих исходных веществ.
Примеры 451-467
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 2, с применением соответствующих исходных веществ.
Пример 468
После получения производного карбоновой кислоты по способу, аналогичному способу, описанному в примере 2, к этому соединению добавляли 2 моль/л хлористоводородной кислоты (0,165 мл) и смесь перемешивали при 50°С на протяжении ночи. Осажденное твердое вещество собирали фильтрованием и промывали метанолом, получая при этом указанное в заголовке соединение (0,080 г).
Примеры 469-487
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 468, с применением соответствующих исходных веществ.
Примеры 488-489
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 2, с применением соответствующих исходных веществ.
Примеры 490-491
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 379, с применением соответствующих исходных веществ.
Примеры 492-498
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 2, с применением соответствующих исходных веществ.
Пример 499
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 55, с применением соответствующих исходных веществ.
Примеры 500-521
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 2, с применением соответствующих исходных веществ.
Примеры 522-524
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 385, с применением соответствующих исходных веществ.
Примеры 525-526
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 2, с применением соответствующих исходных веществ.
Примеры 527-528
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 376, с применением соответствующих исходных веществ.
Пример 529
Указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 55, с применением соединения примера 528.
Примеры 530-531
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 529, с применением соответствующих исходных веществ.
Примеры 532-548
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 376, с применением соответствующих исходных веществ.
Пример 549
После получения производного амида способом, аналогичным способу, описанному в примере 376, с применением соединения примера 461, указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 11.
Примеры 550-552
Указанные в заголовке соединения получали способом, аналогичным способу, описанному в примере 549, с применением соответствующих исходных веществ.
Пример 553
После получения производного амида способом, аналогичным способу, описанному в примере 376, с применением соединения примера 488, указанное в заголовке соединение получали способом, аналогичным способу, описанному в примере 379.
В таблицах 1-9 и 68 показаны химические структуры и данные 1Н-ЯМР указанных выше соединений ссылочных примеров 1-61, исключая соединения примеров 3 и 62-70, в таблице 69 показаны химические структуры соединений ссылочных примеров 71-98, в таблицах 10-67, 70-71 и 76-90 показаны химические структуры и данные 1Н-ЯМР, включающие некоторые данные масс-спектров указанных выше соединений примеров 1-376, исключая соединения примеров 11 и 14, 377-388 и 451-553, в таблицах 72-75 показаны химические структуры соединений примеров 389-450, соответственно.
Аббревиатуры в этих таблицах “ссыл. пр.”, “№ пр.”, ”Струк.”, “Раств.” и “МС” представляют собой номер ссылочного примера, номер примера, химическую структуру, данные измерения 1Н-ЯМР и масс-спектров в растворителе, соответственно.
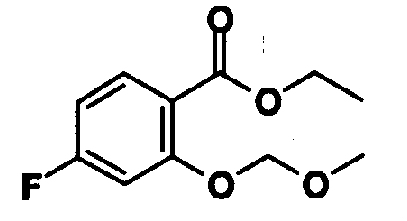
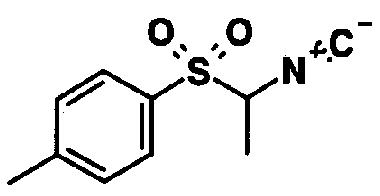
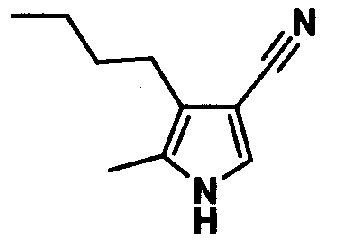
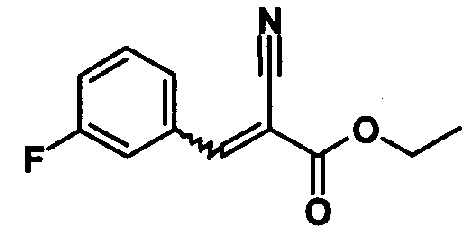
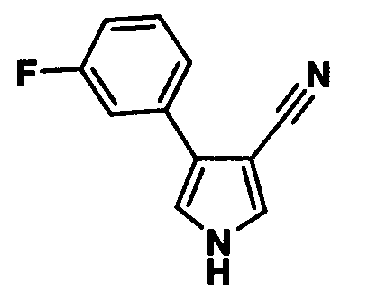
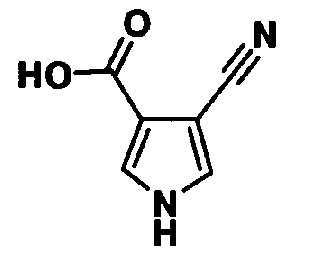
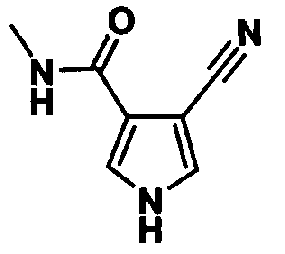
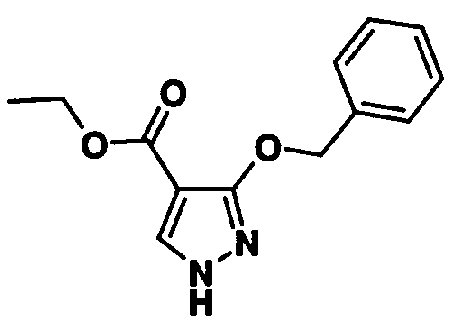
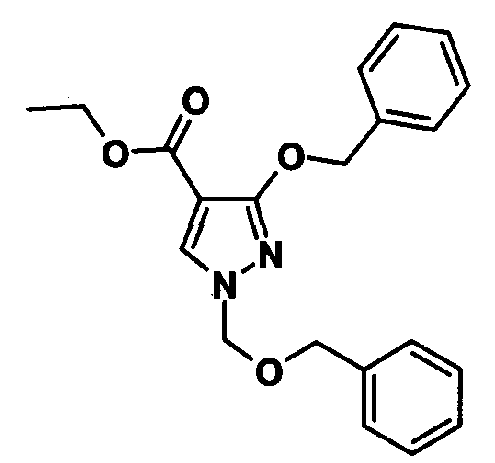
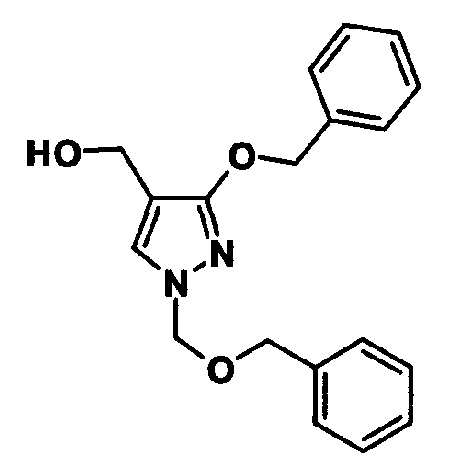
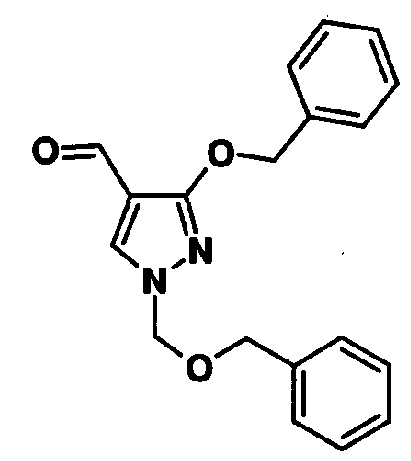
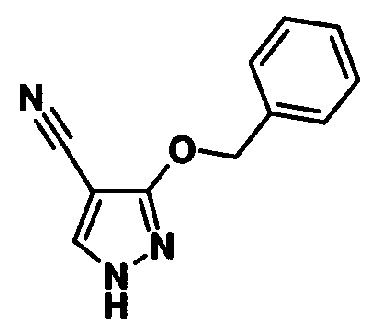
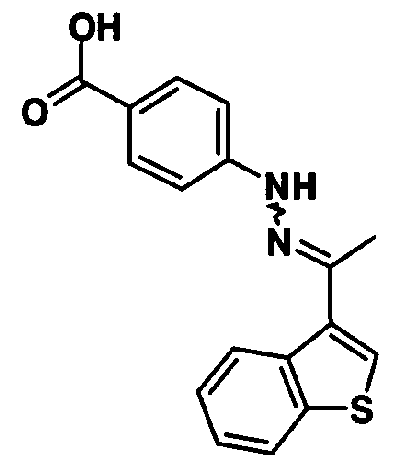
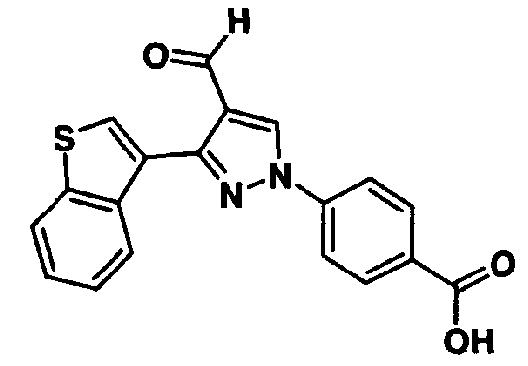
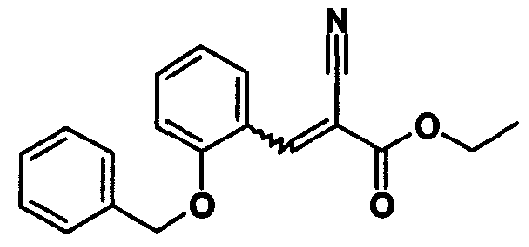
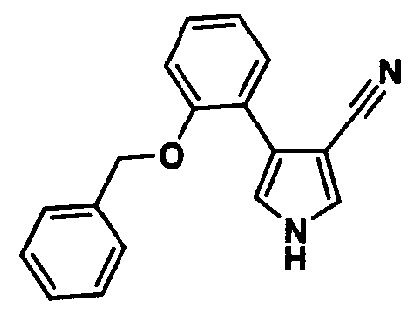
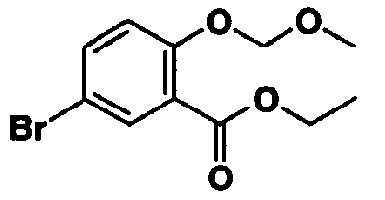
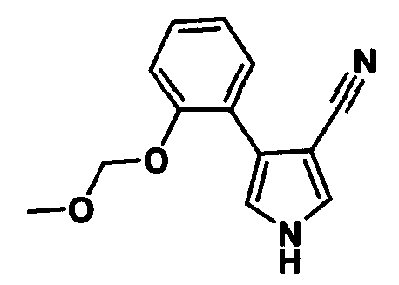
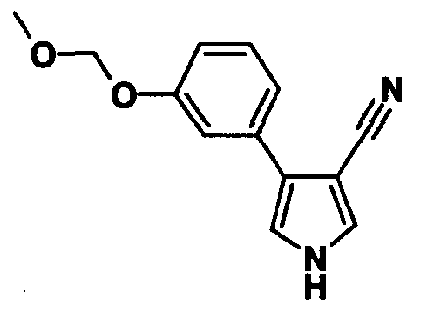
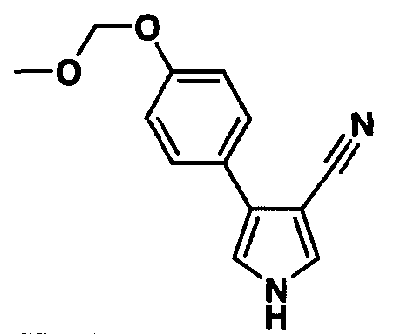
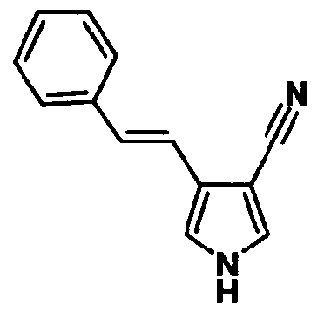
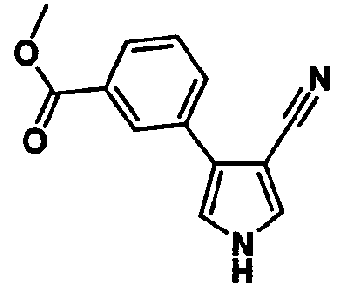
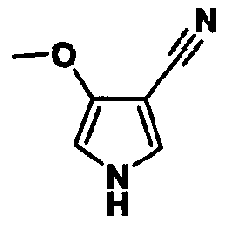
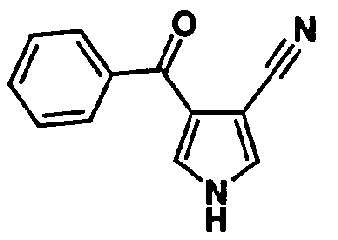
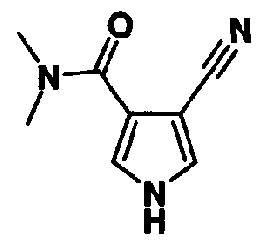
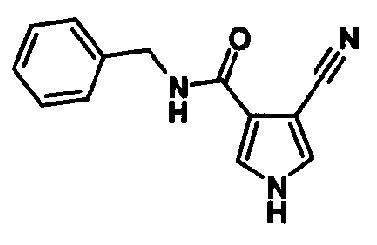
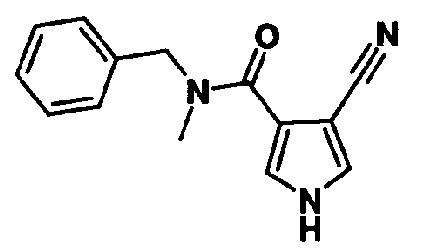
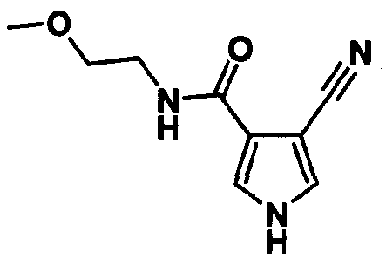
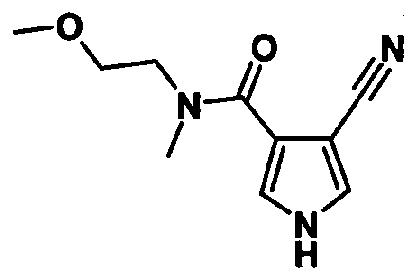
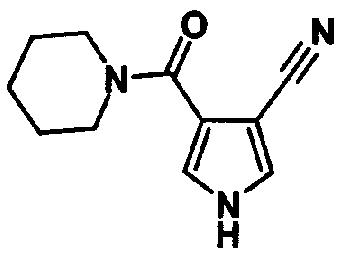
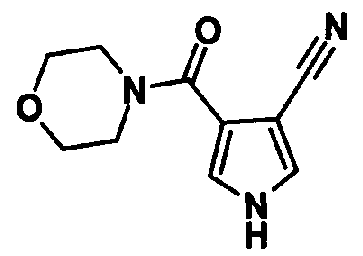
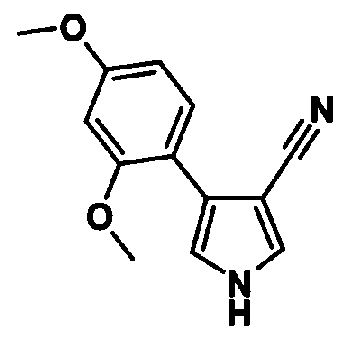
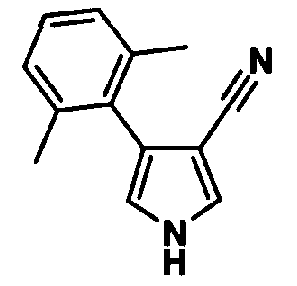
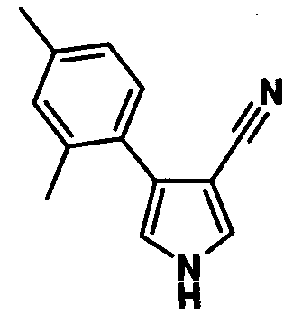
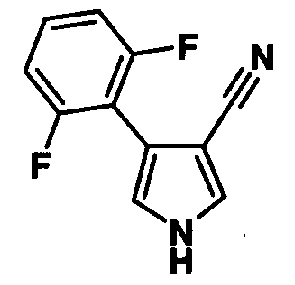
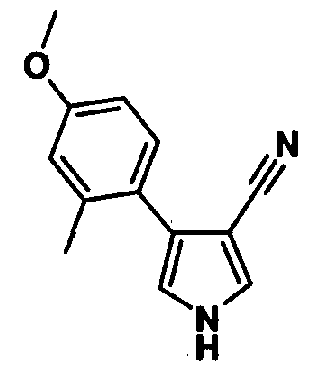
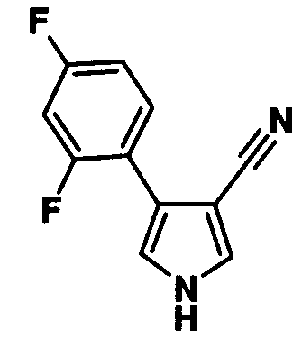
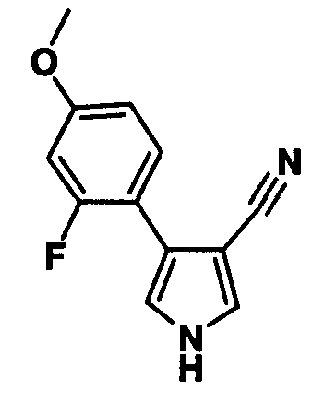
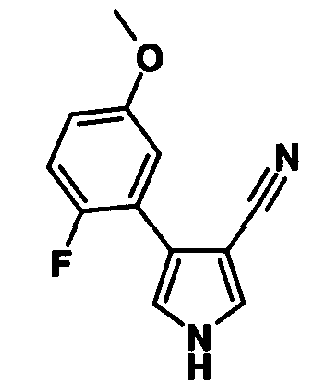
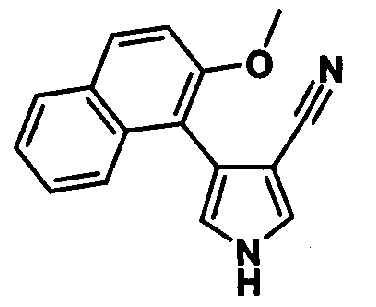
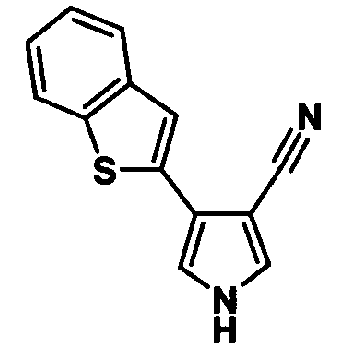
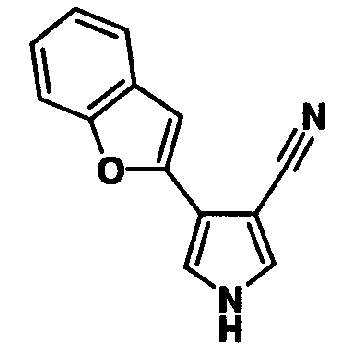
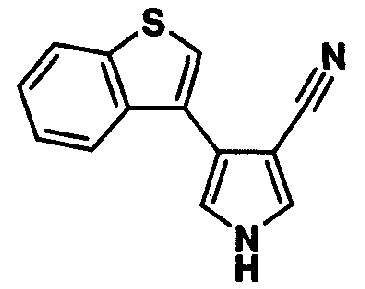
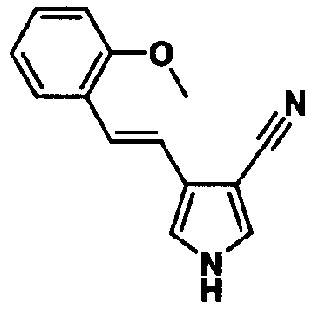
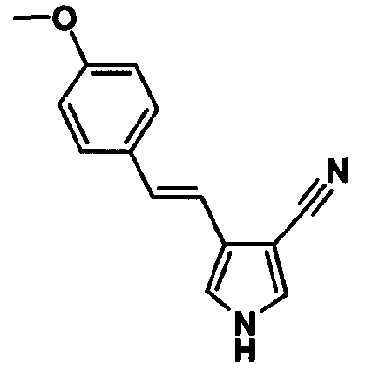
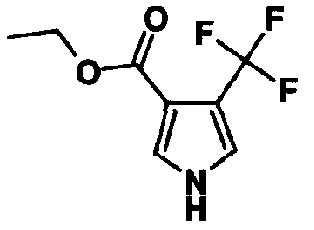
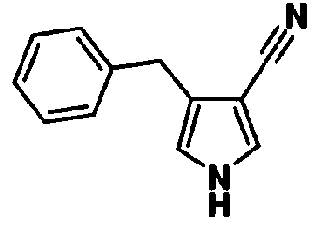
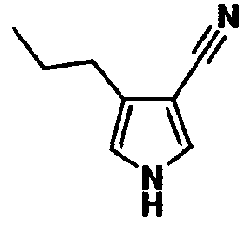
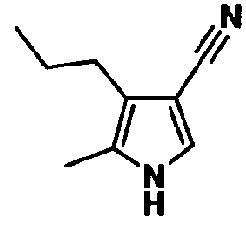
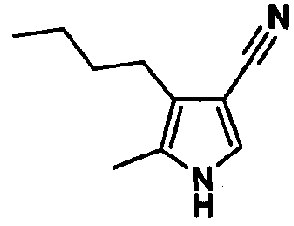
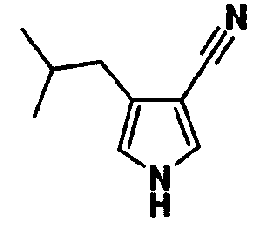
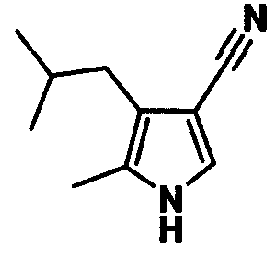
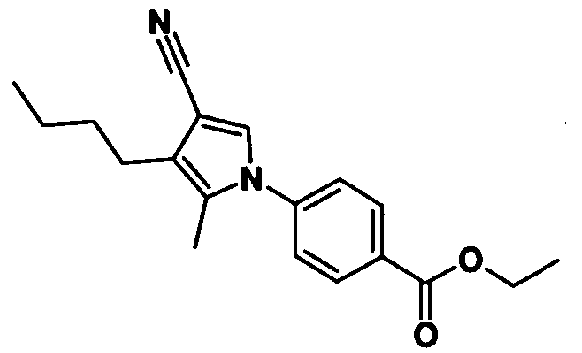
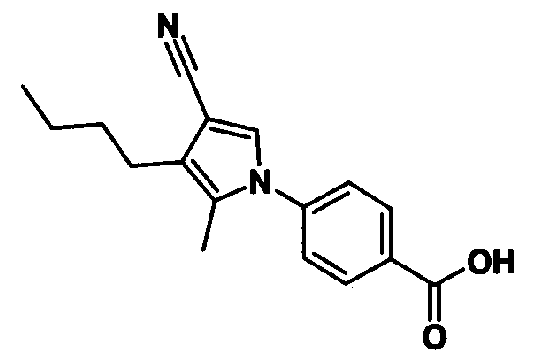
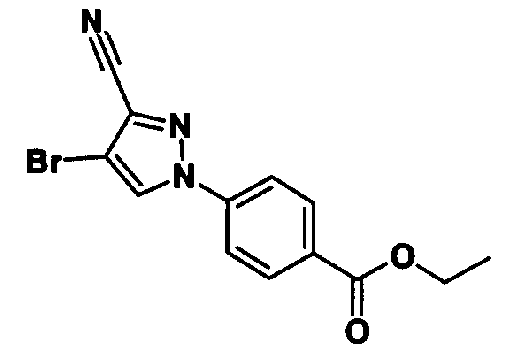
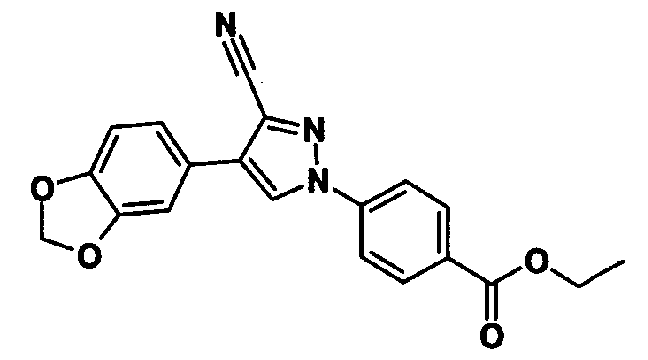
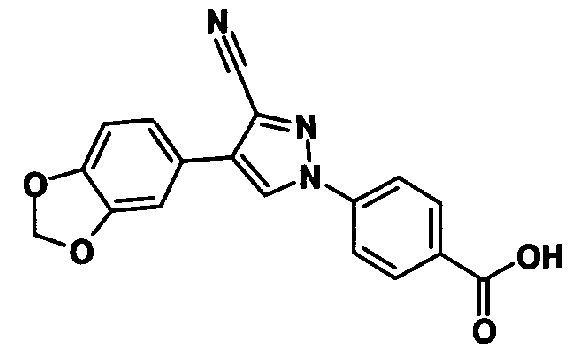
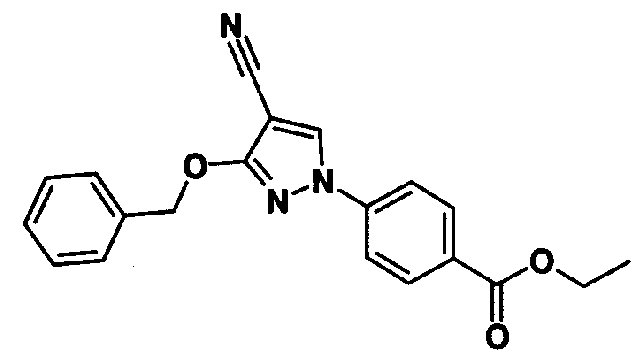

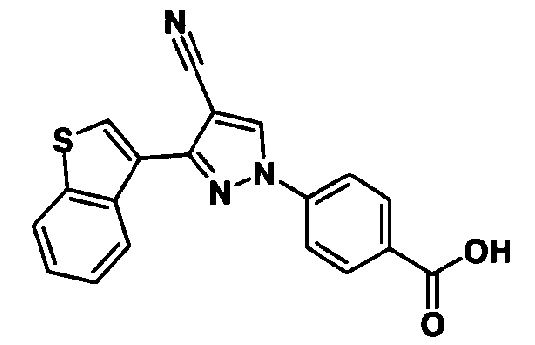
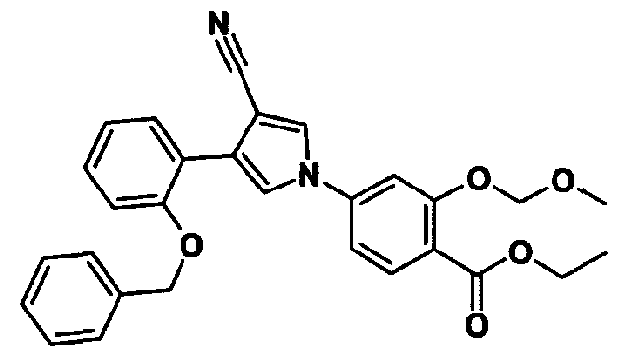
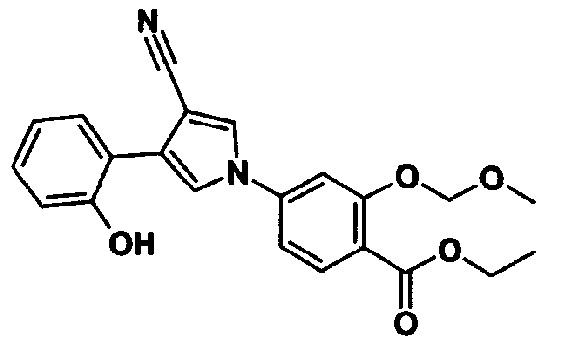
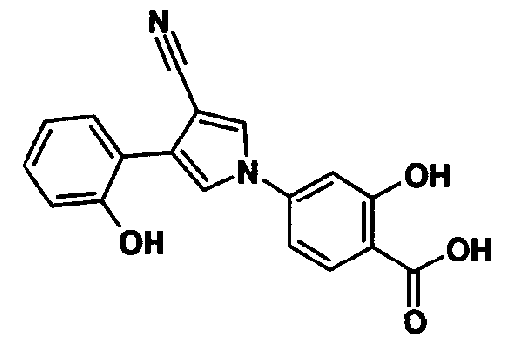
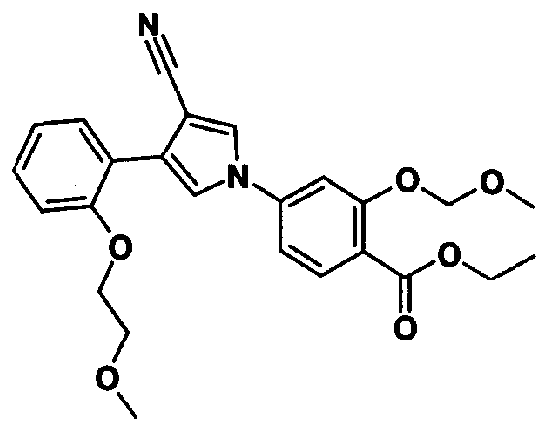
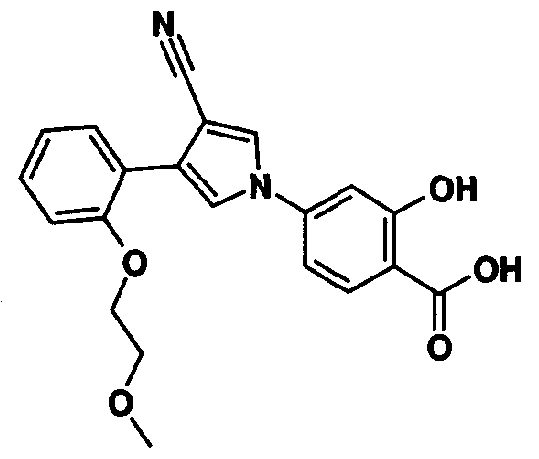
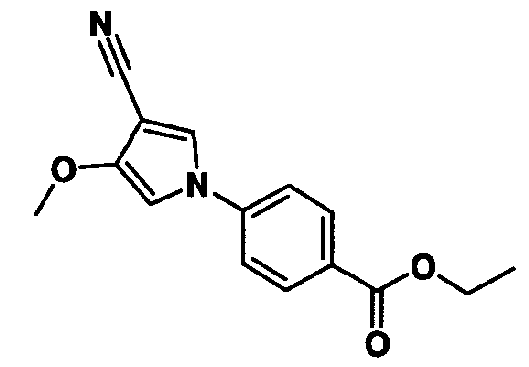
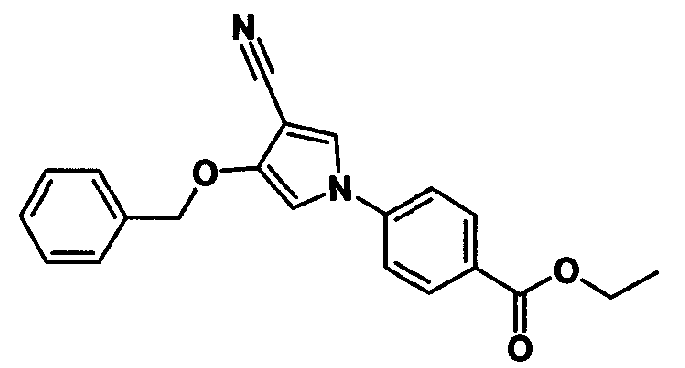
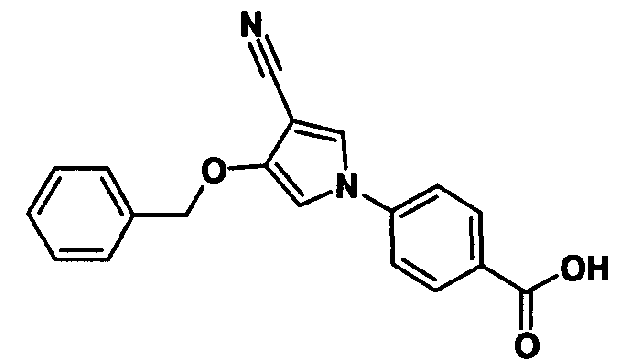
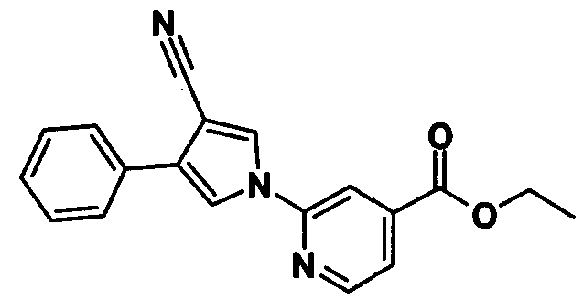
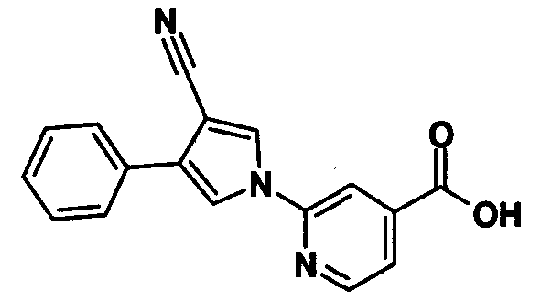
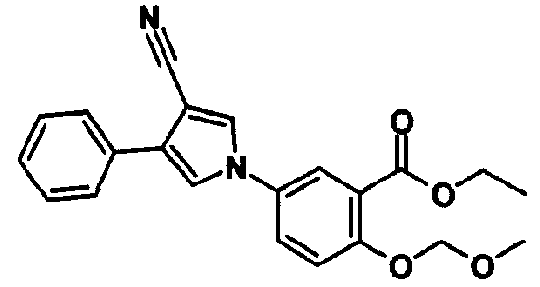
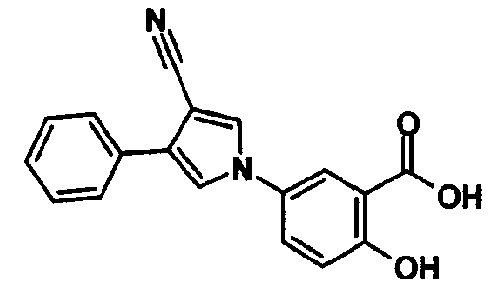
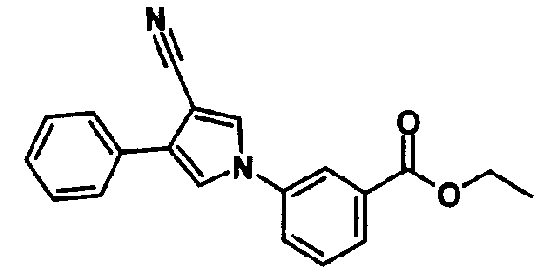
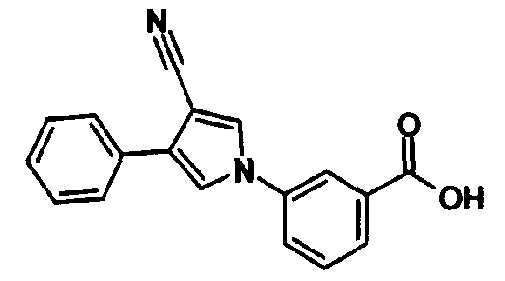
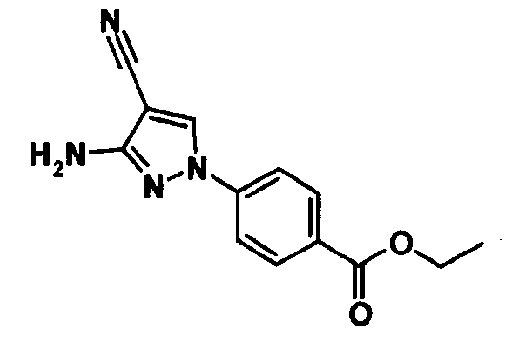
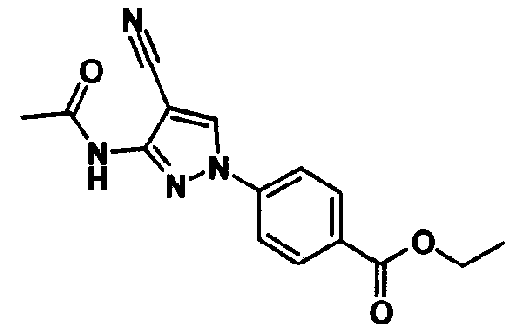
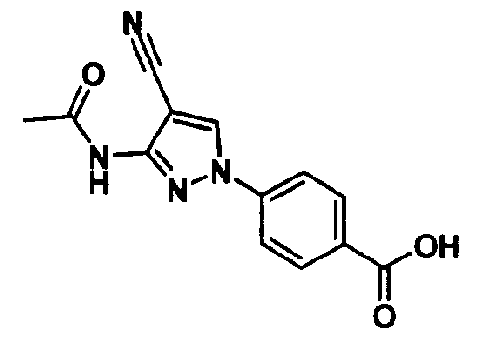
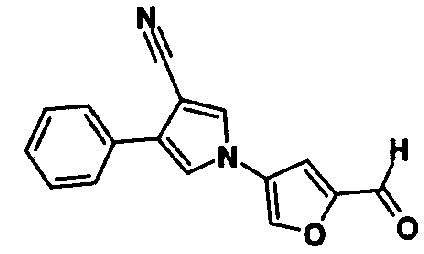
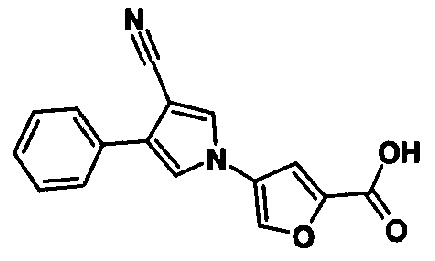
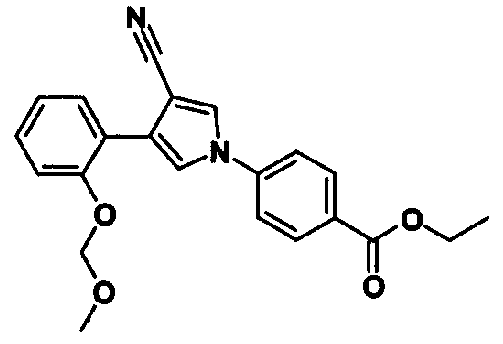
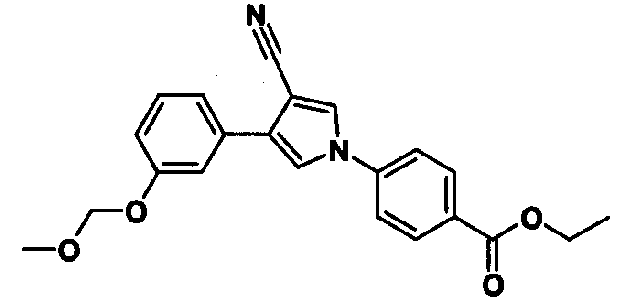
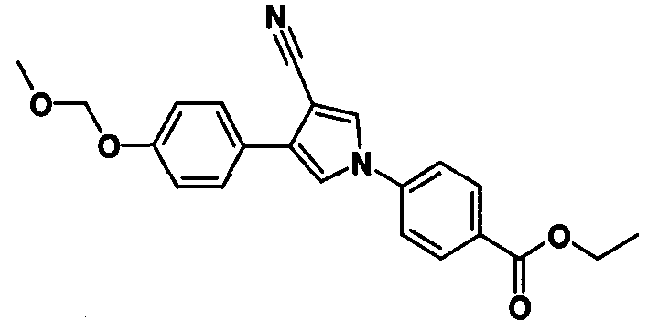
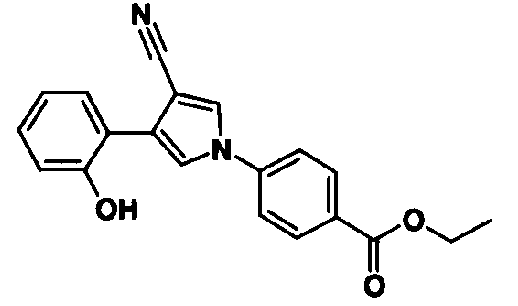
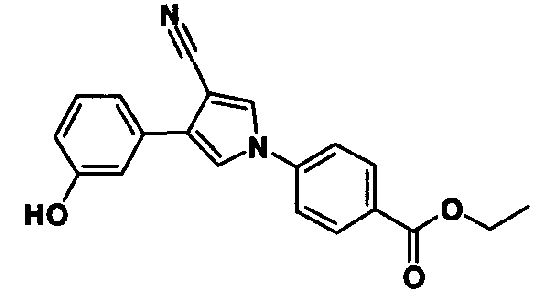
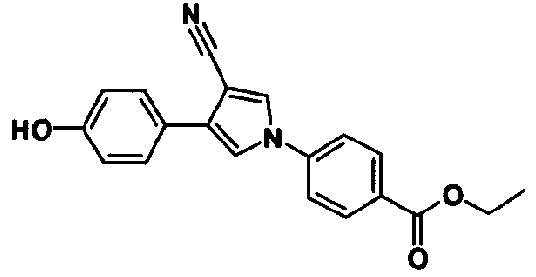


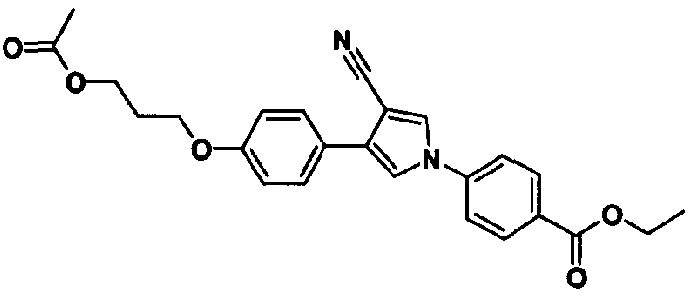
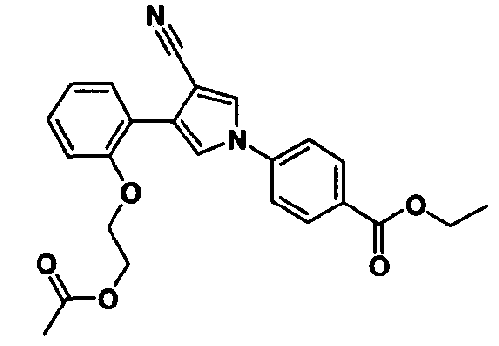
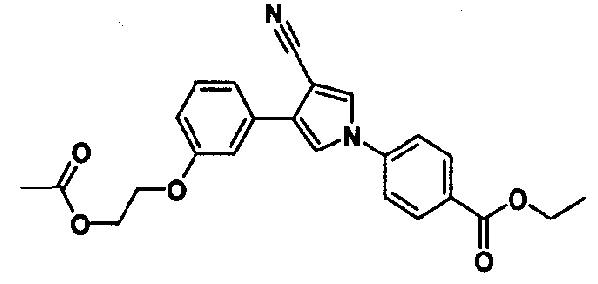
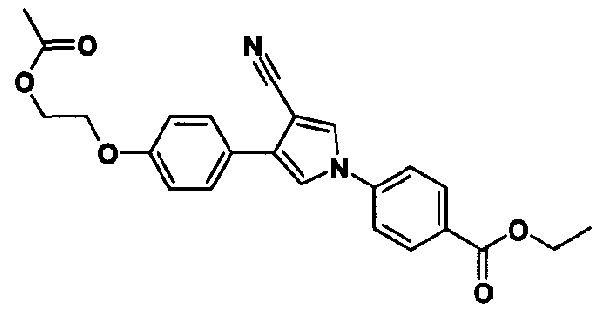
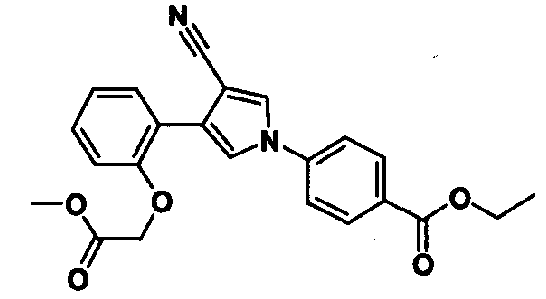
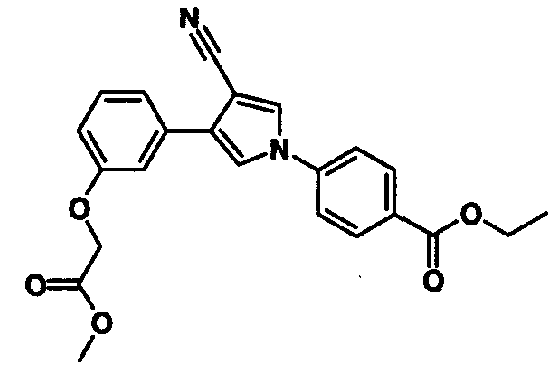
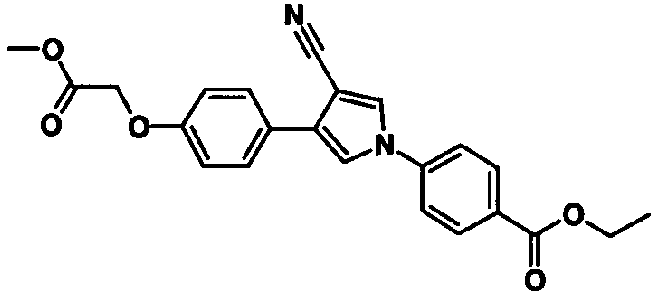
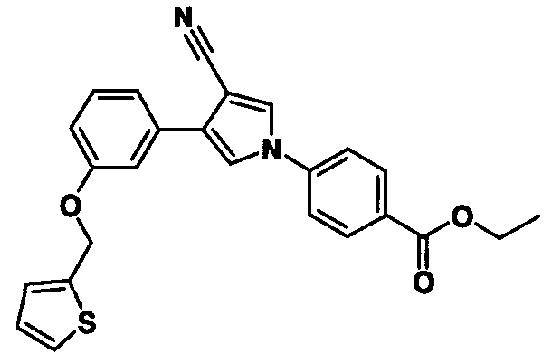
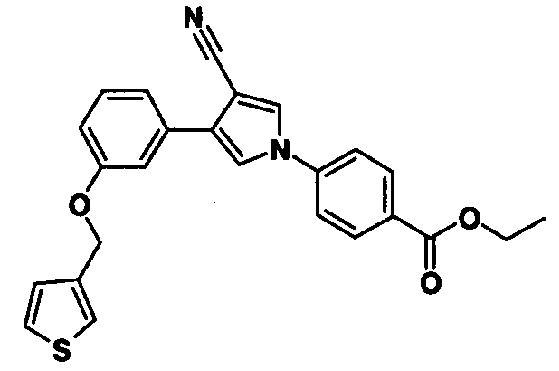
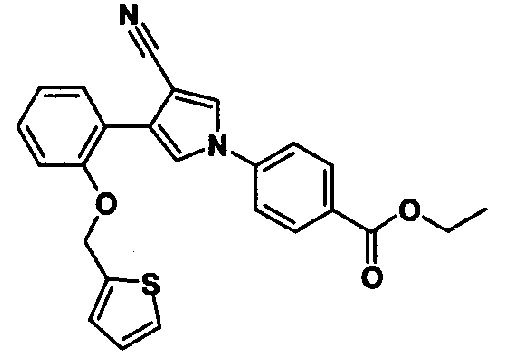
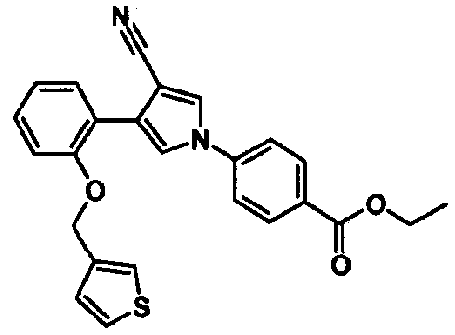
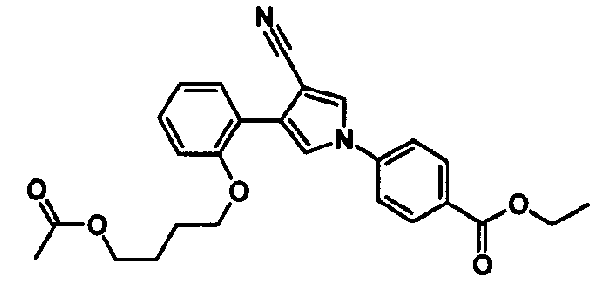
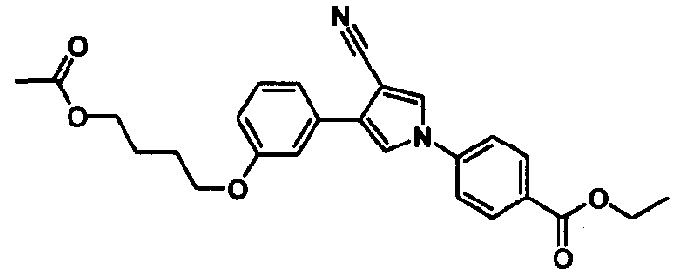
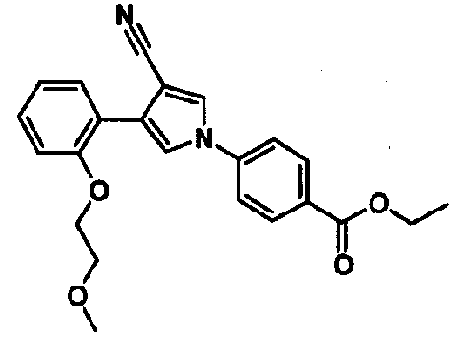
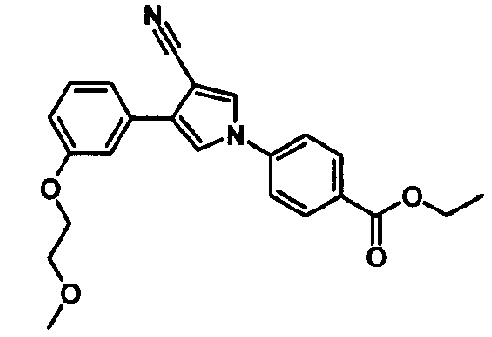
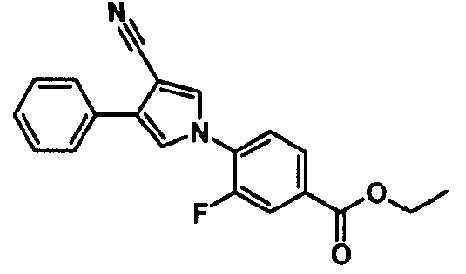
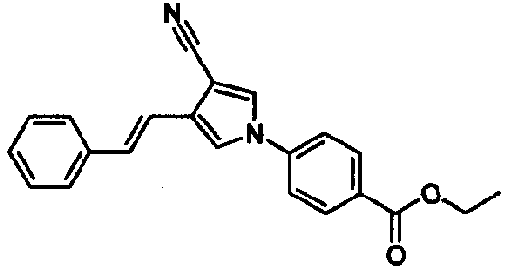
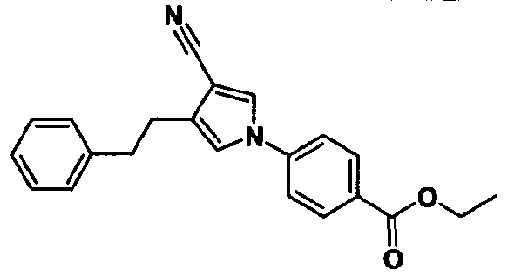
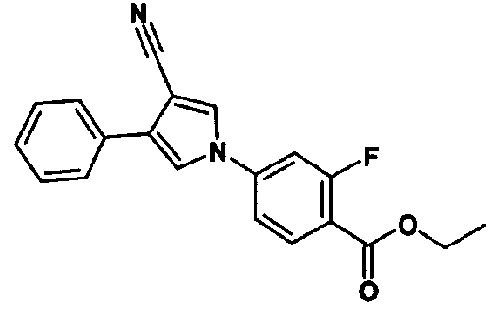
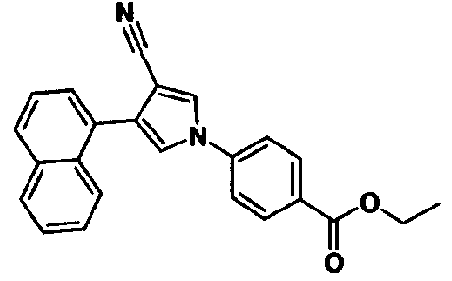
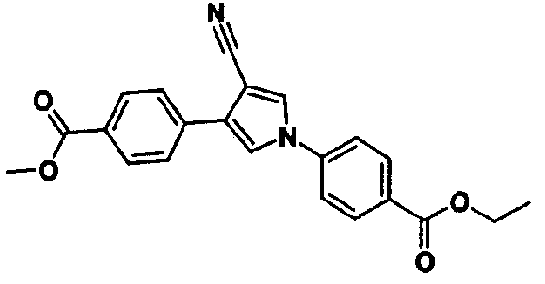
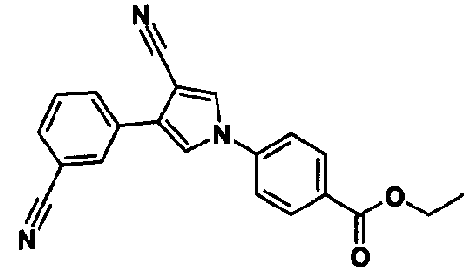
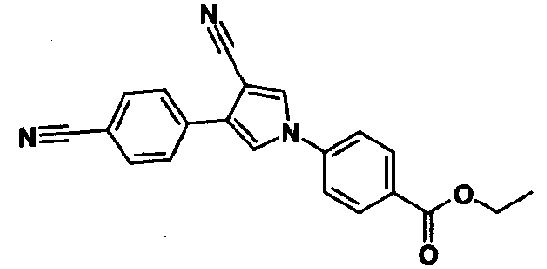
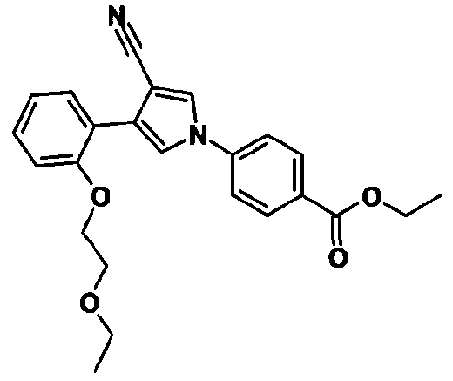
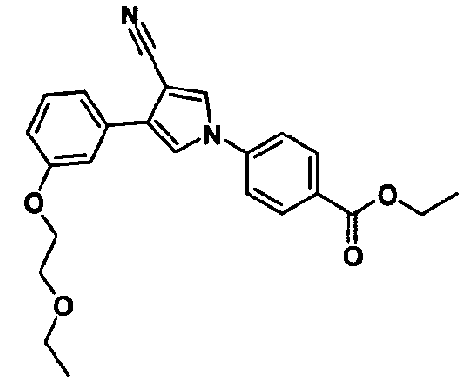

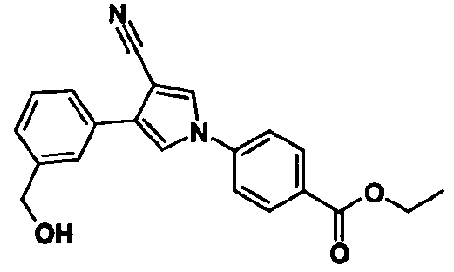
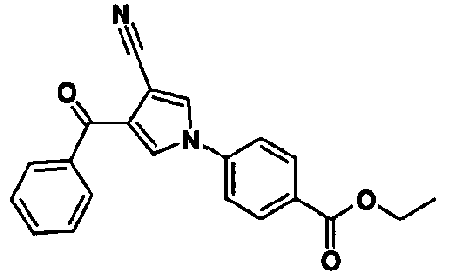
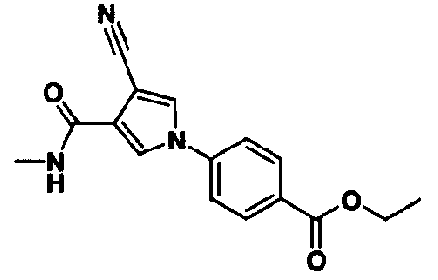
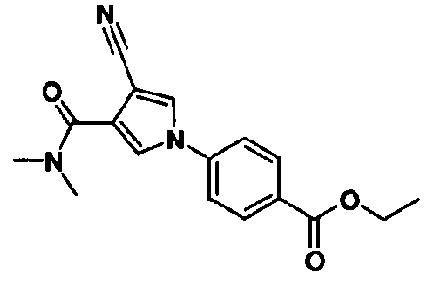
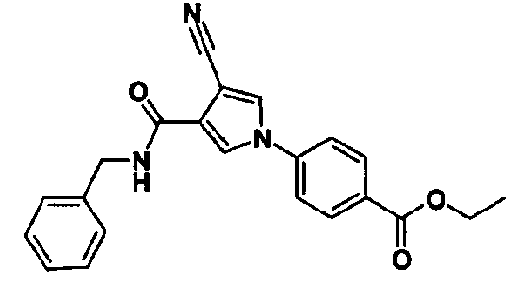
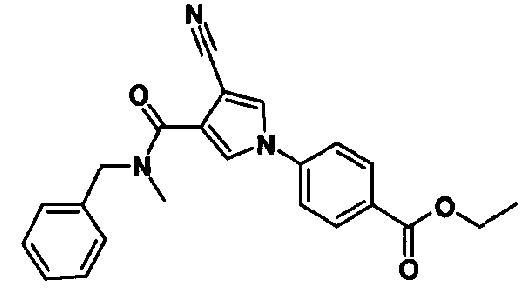
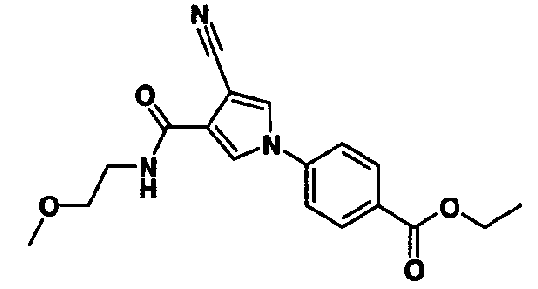
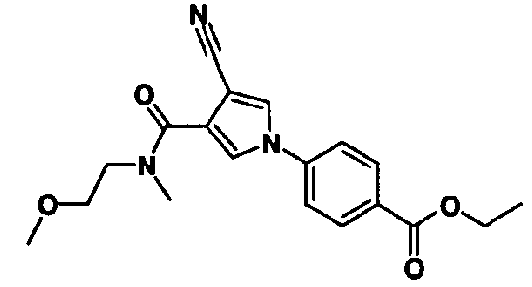
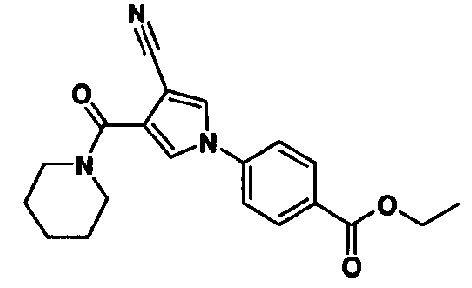
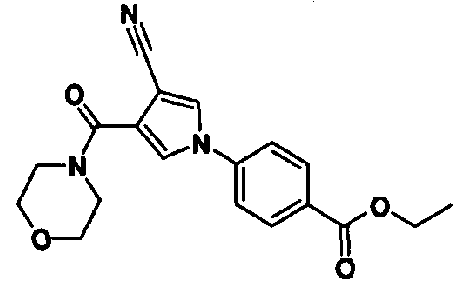
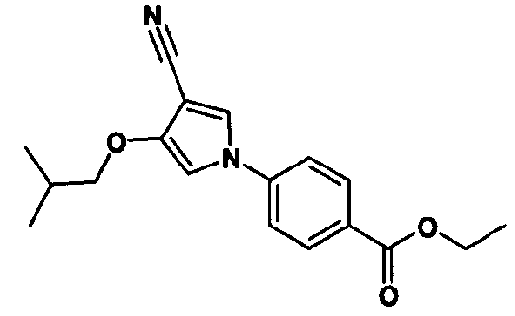
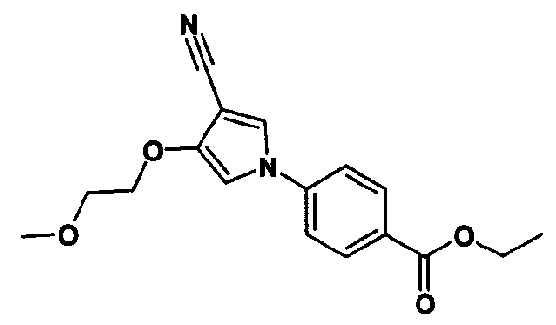
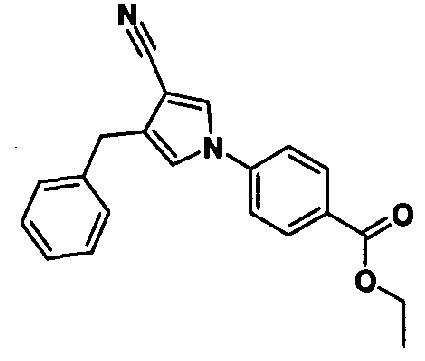
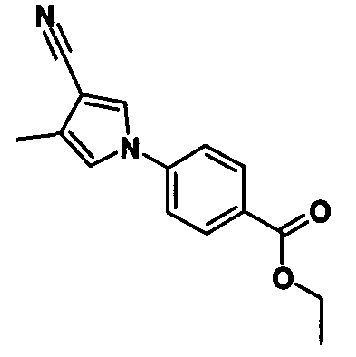
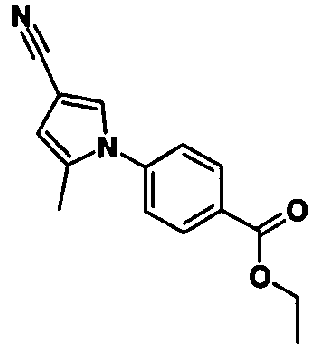
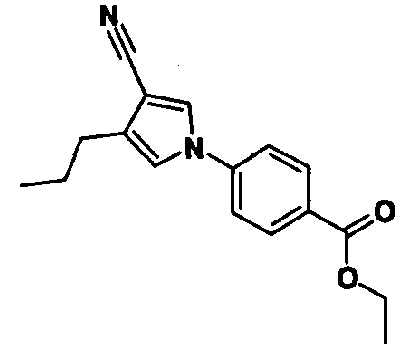
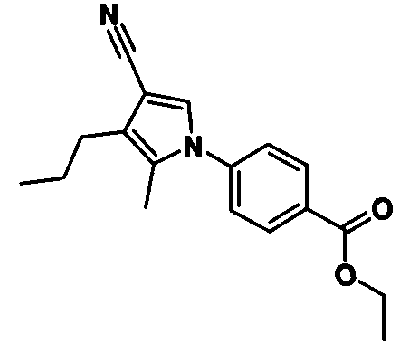
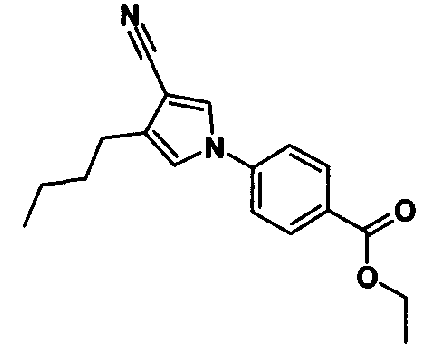
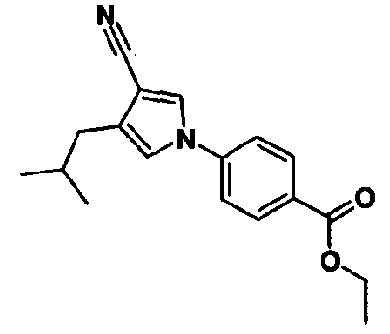
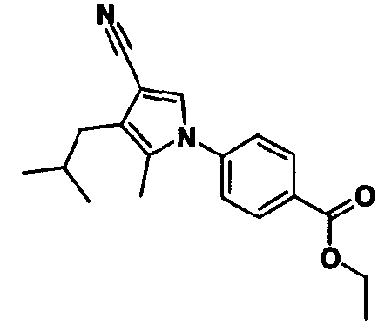
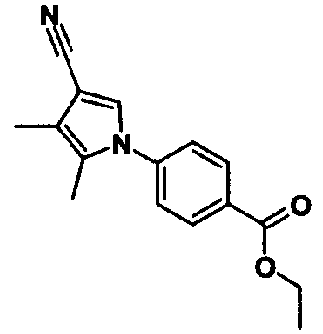
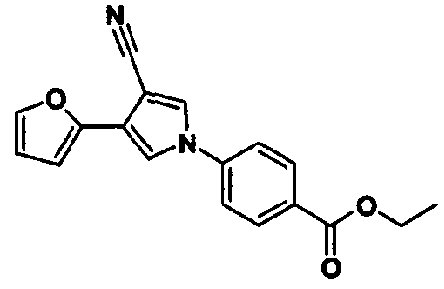
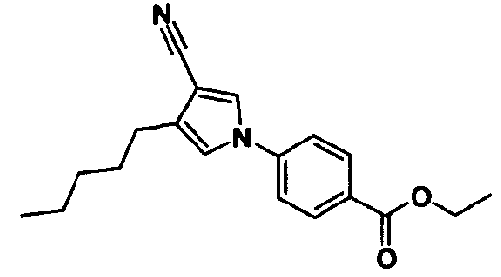
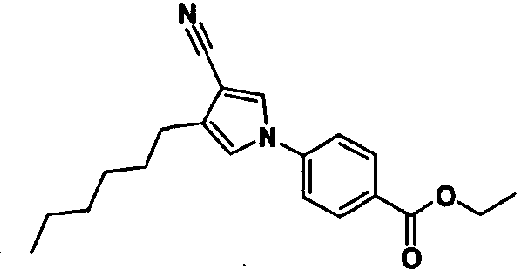
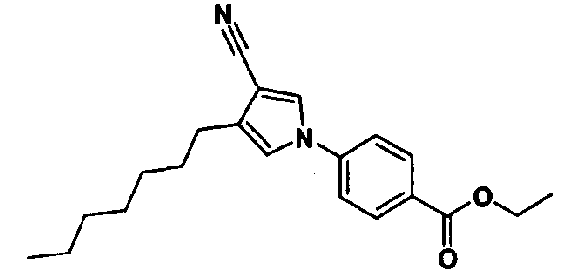
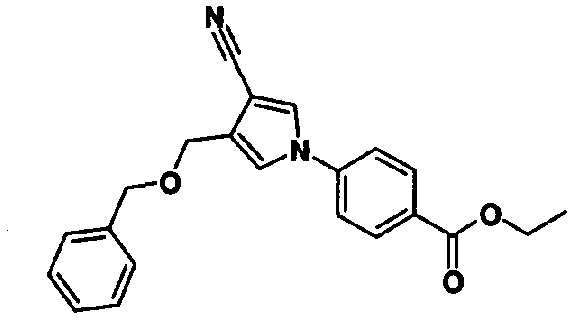
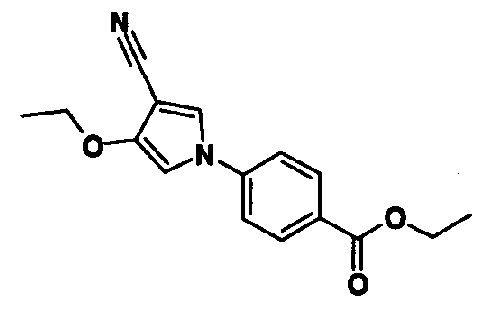
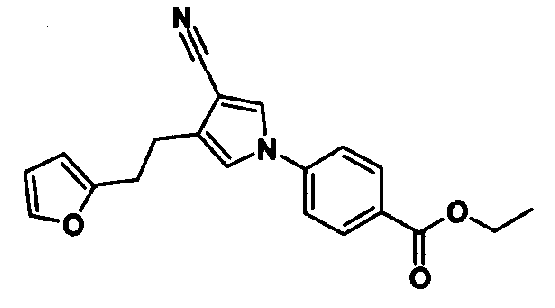
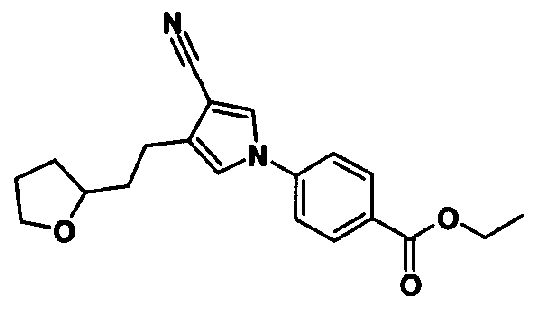
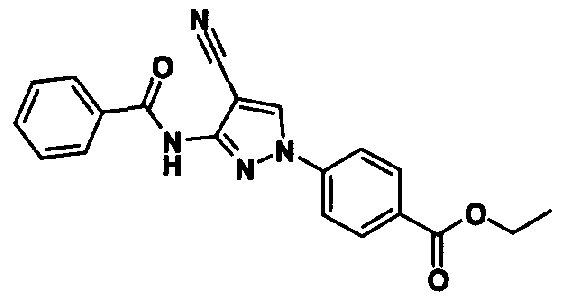

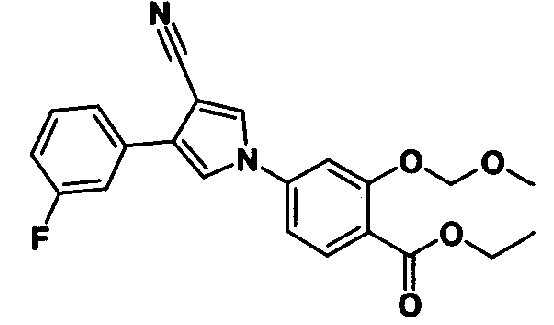
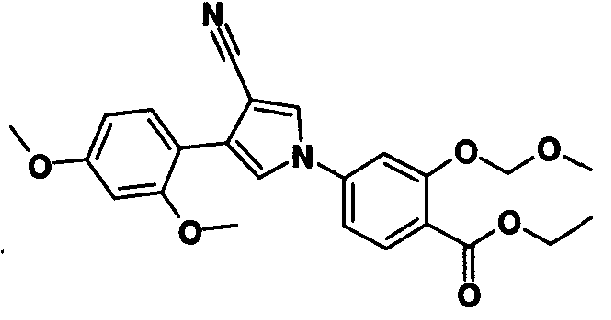
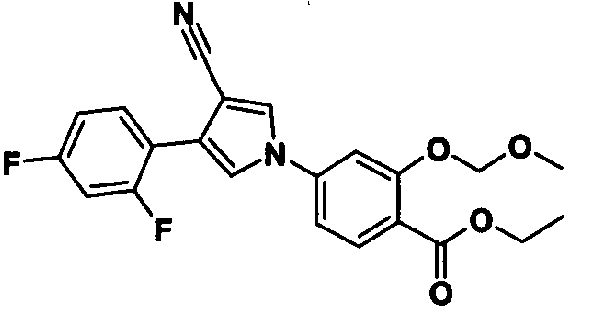
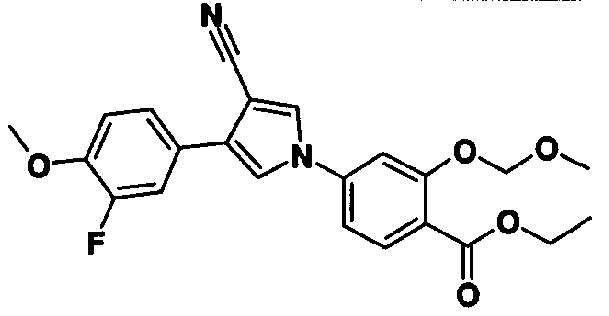
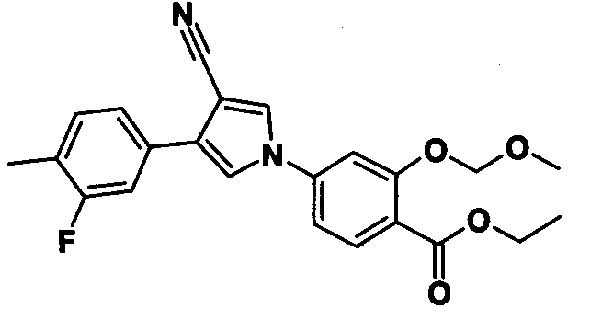
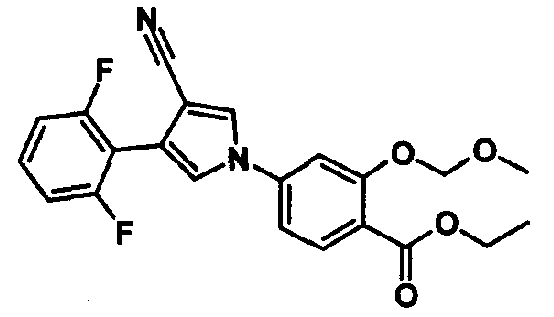
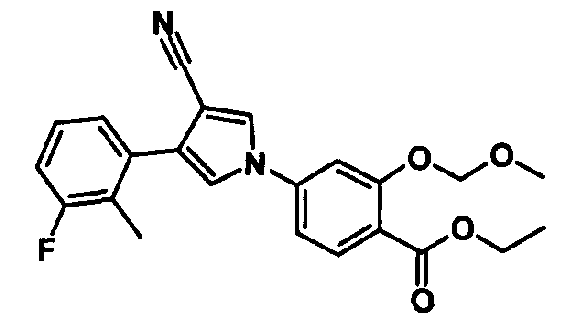
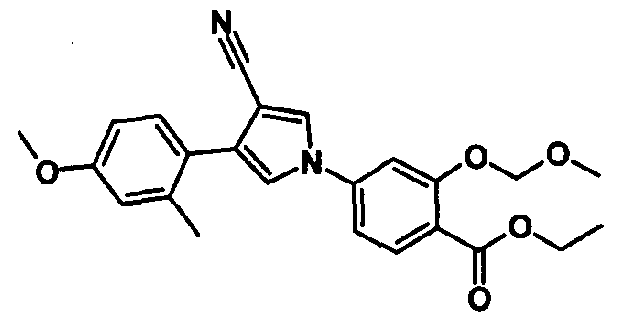
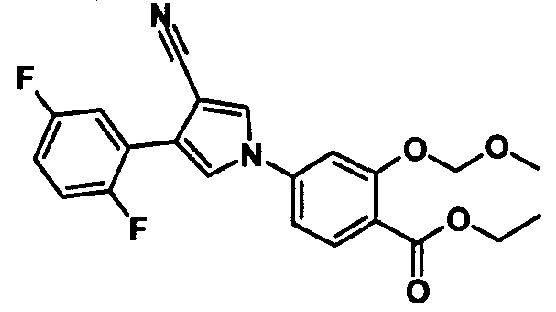
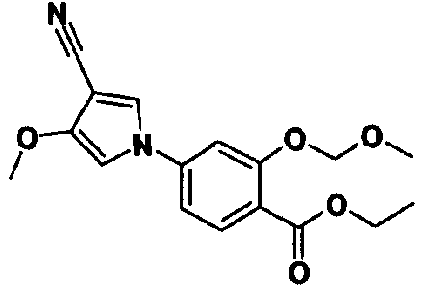
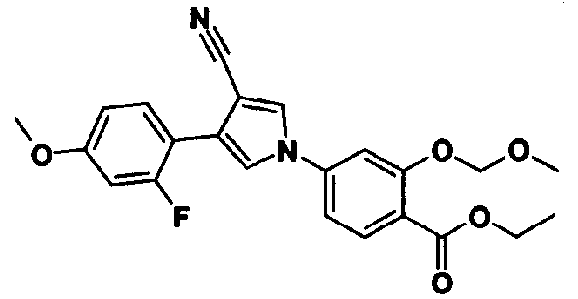
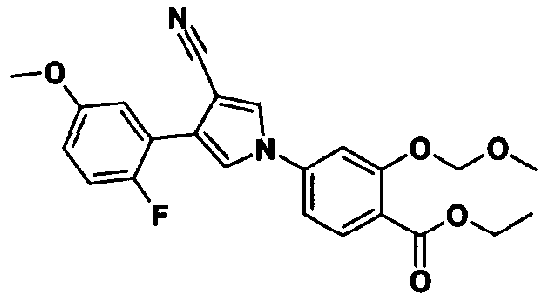
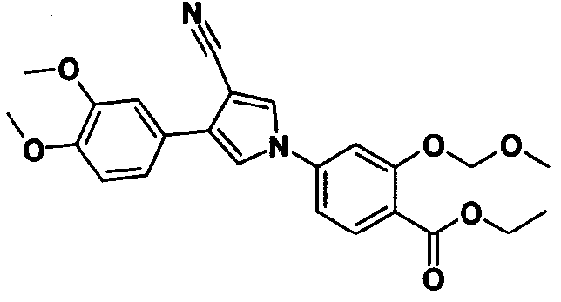
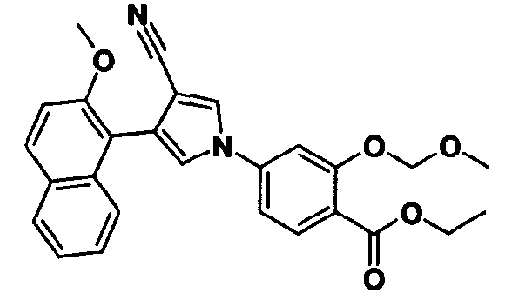
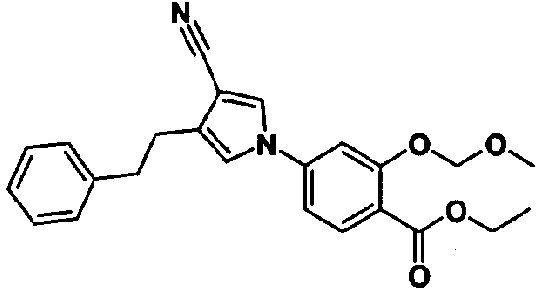
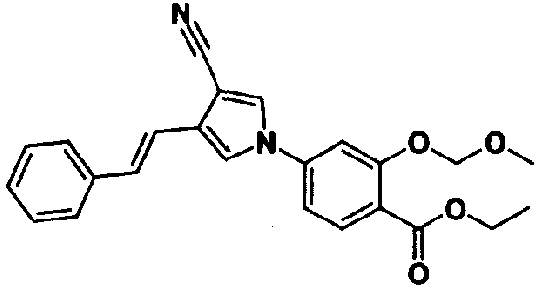
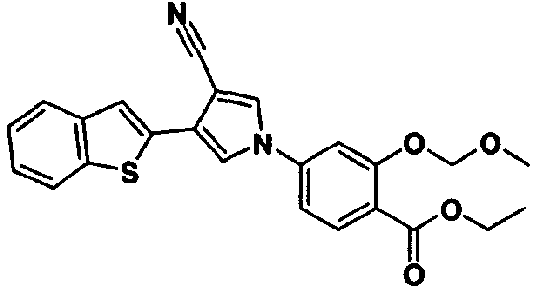
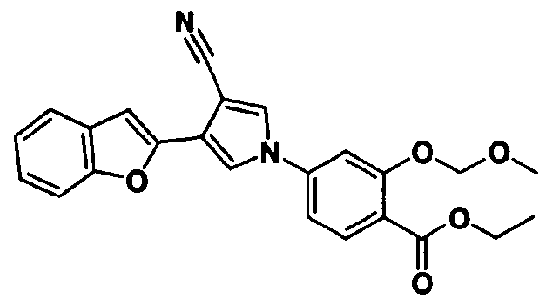
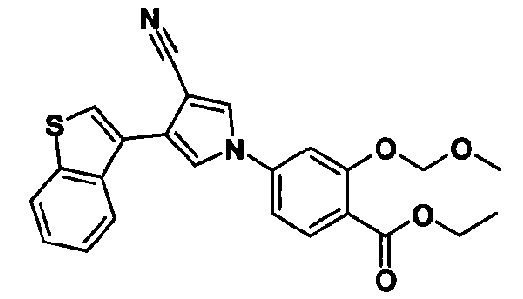
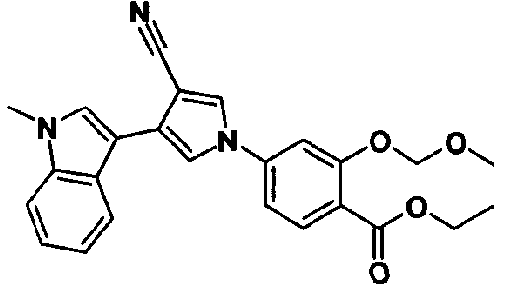
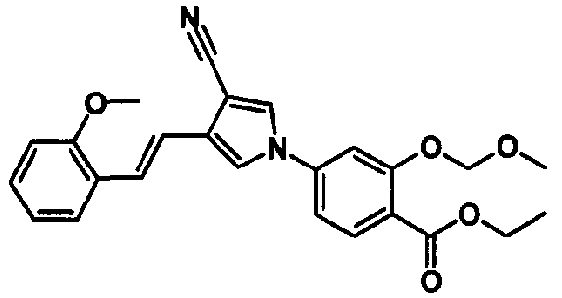
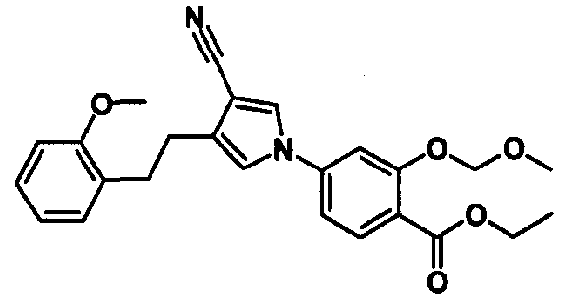
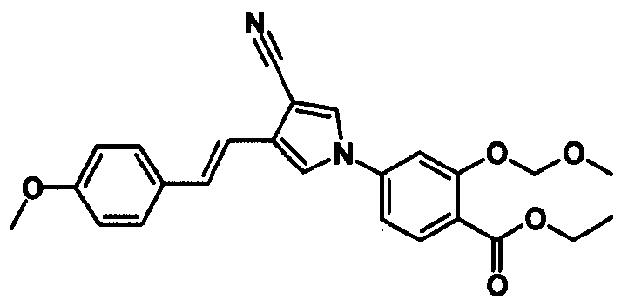
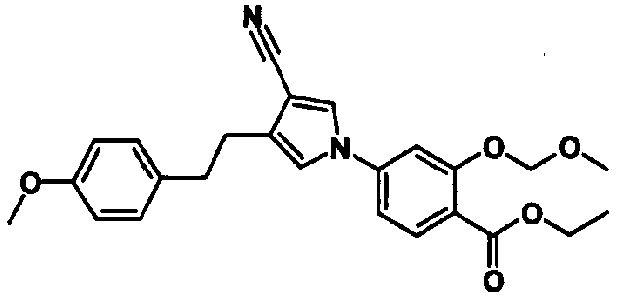
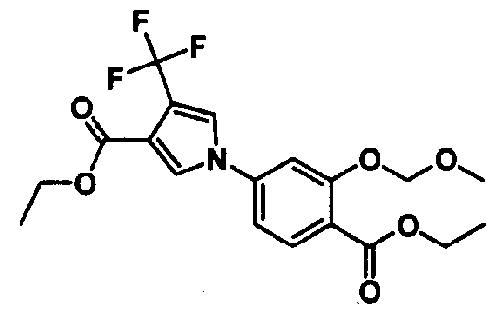
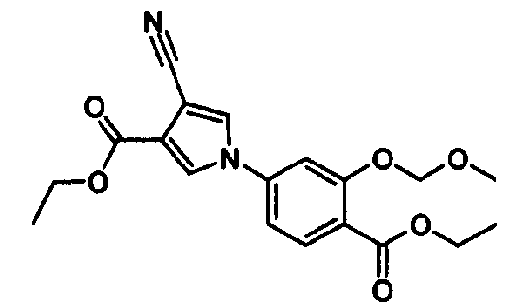
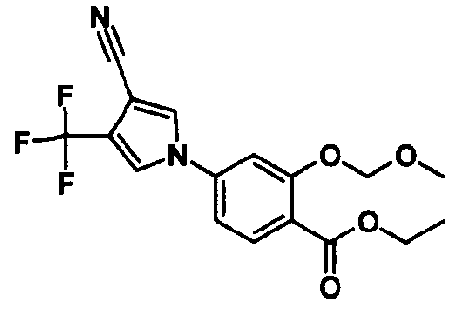
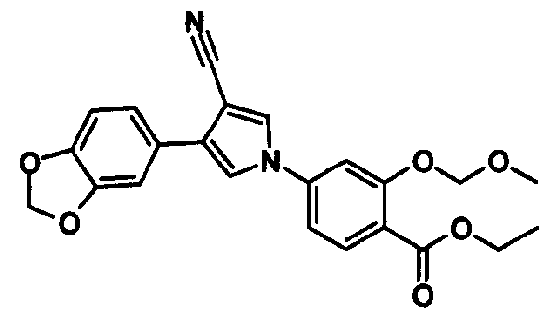
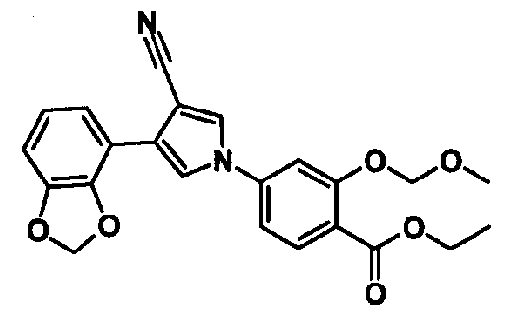
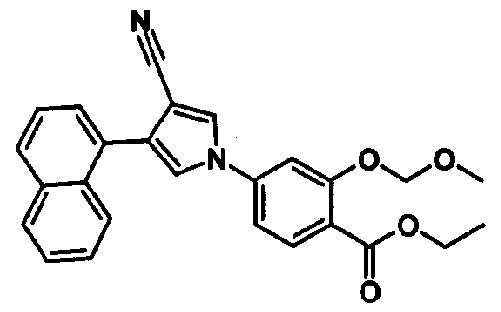
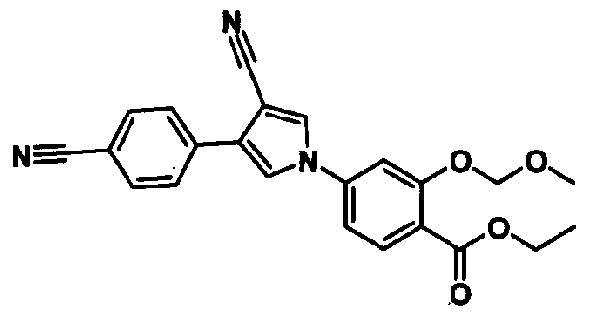
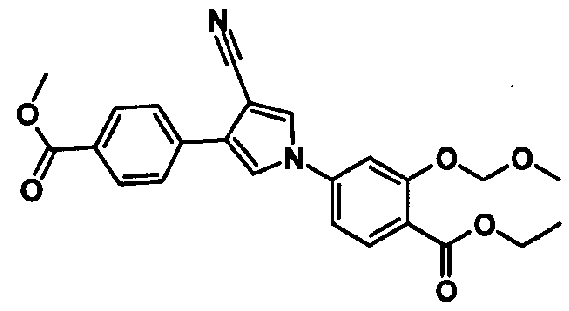
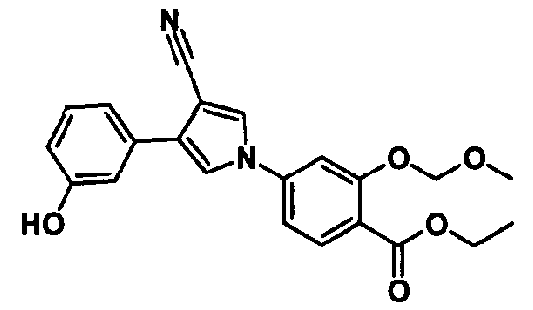
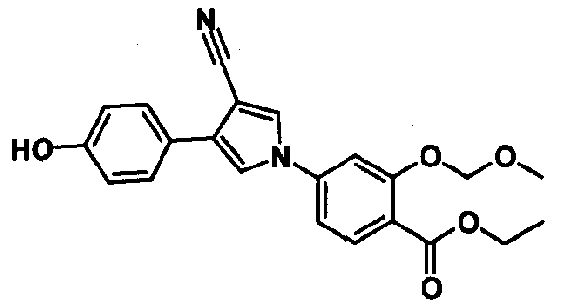
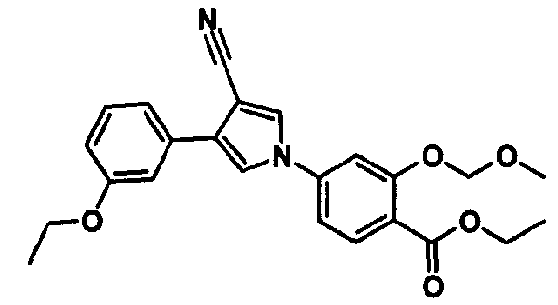
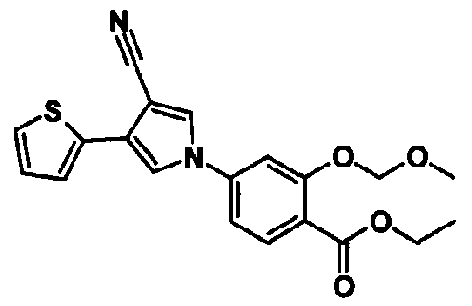
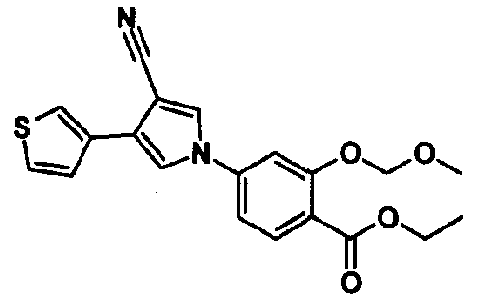
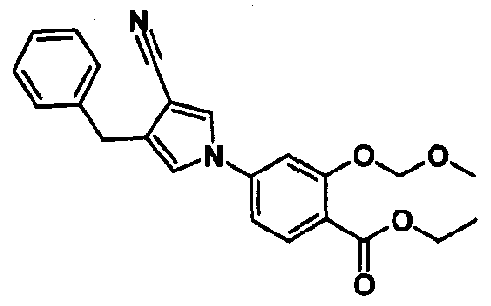
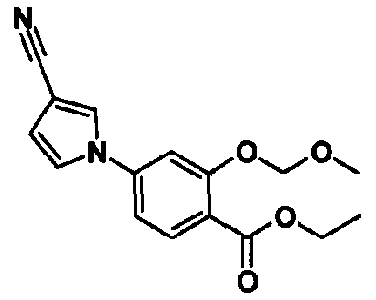
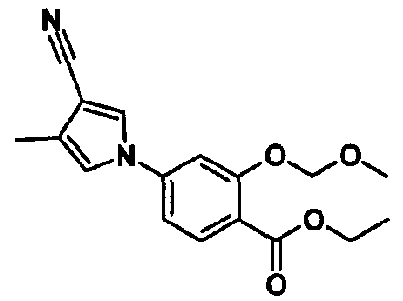
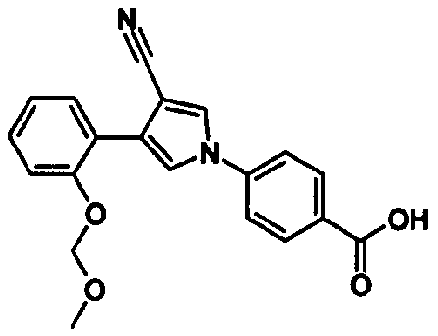
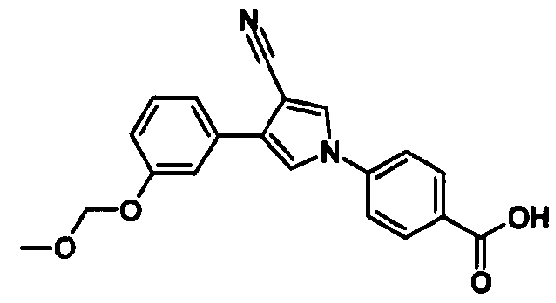
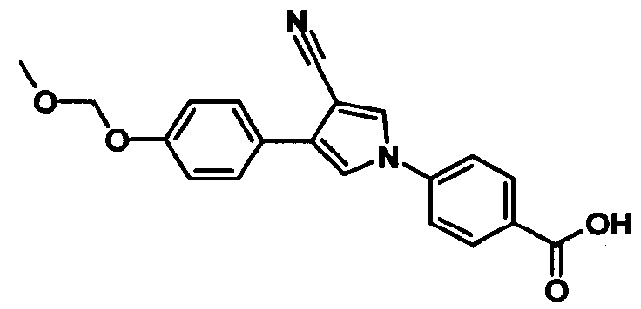
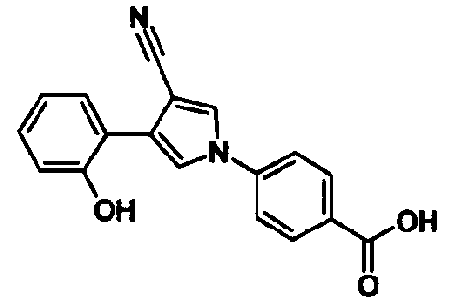
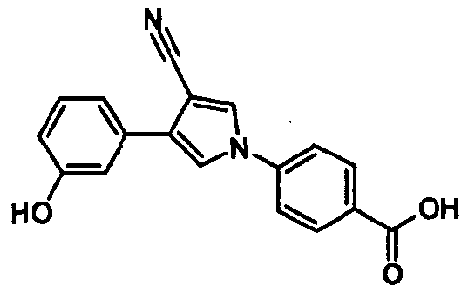
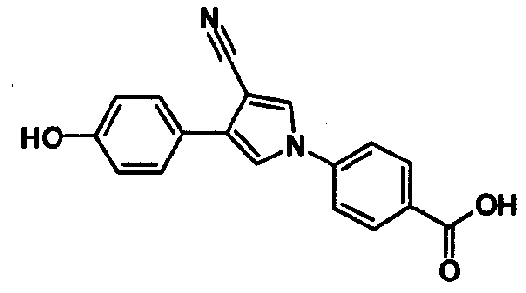
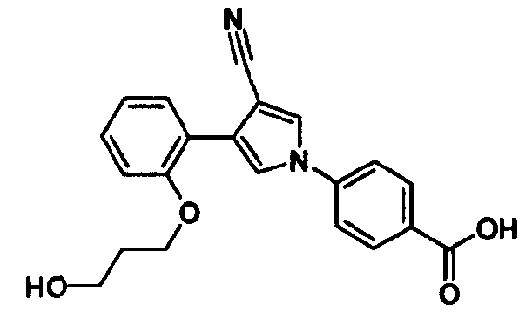
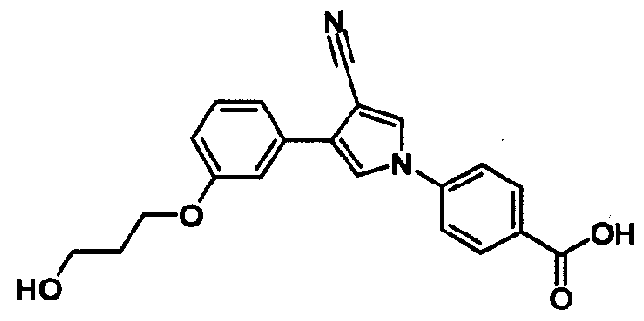
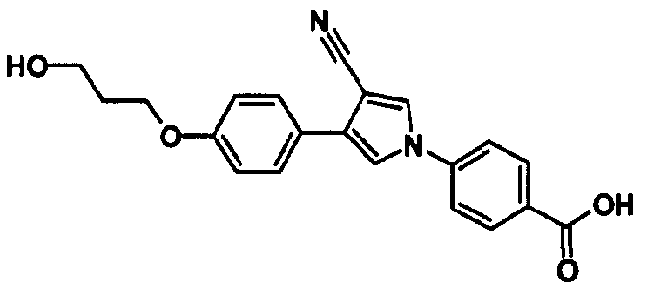
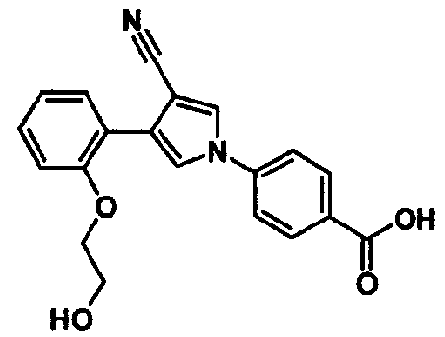
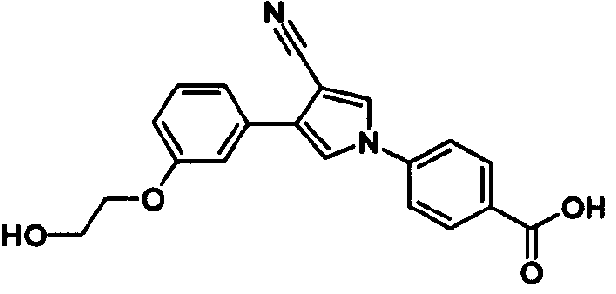
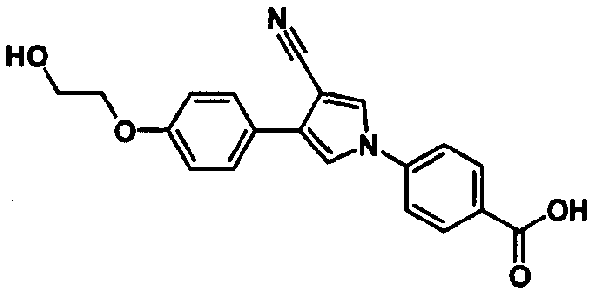
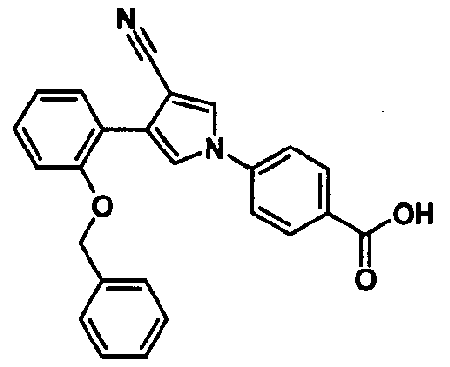
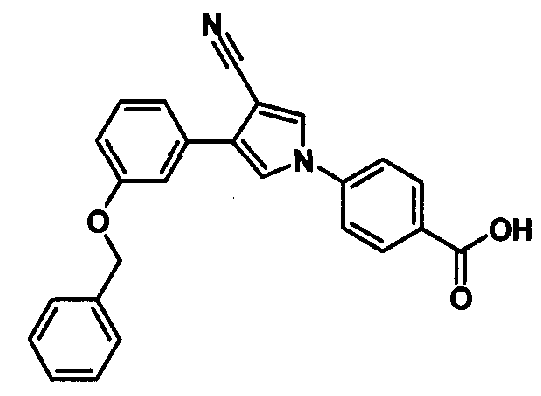
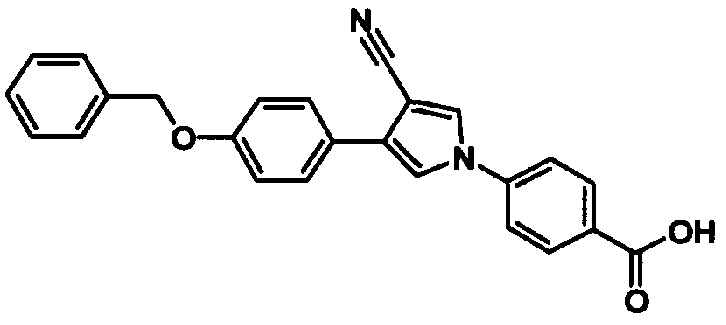
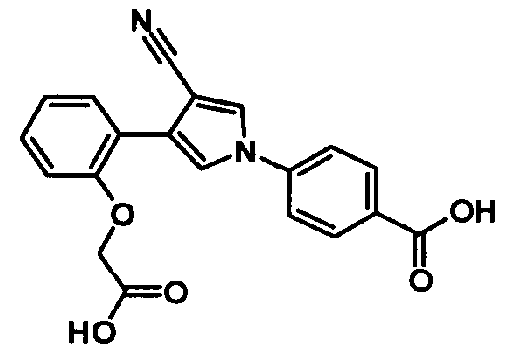
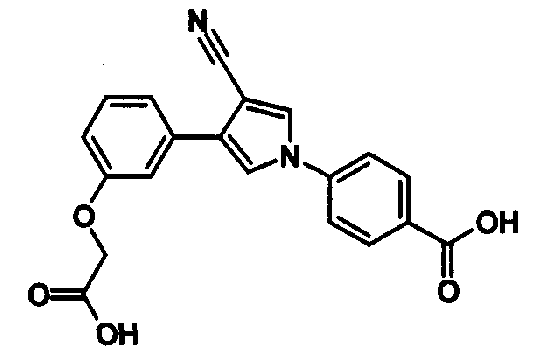
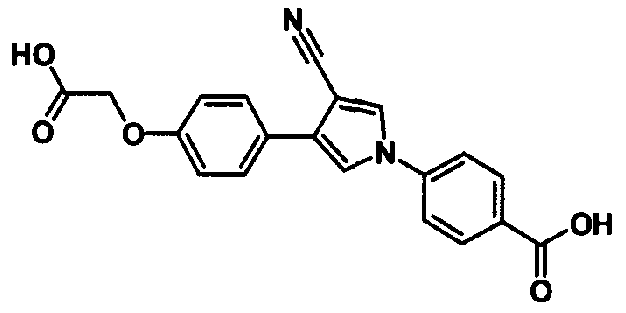
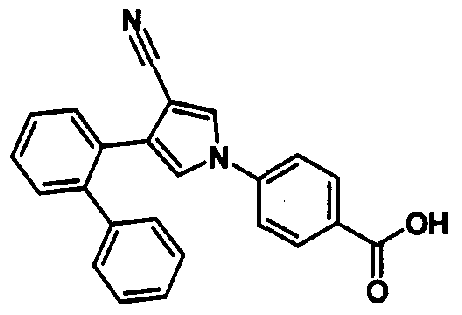
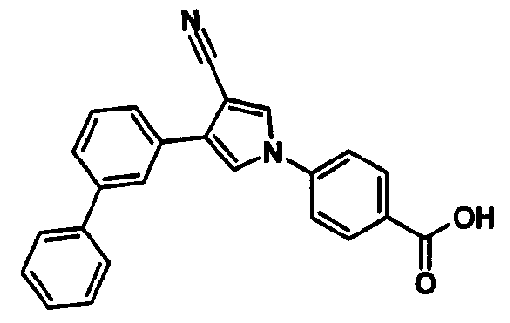
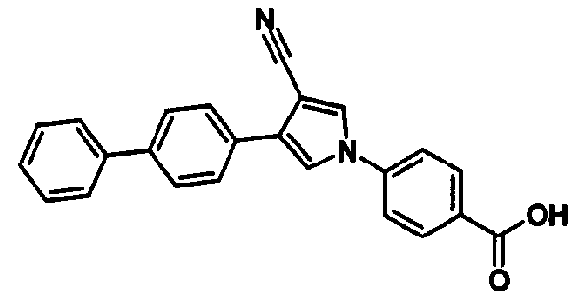
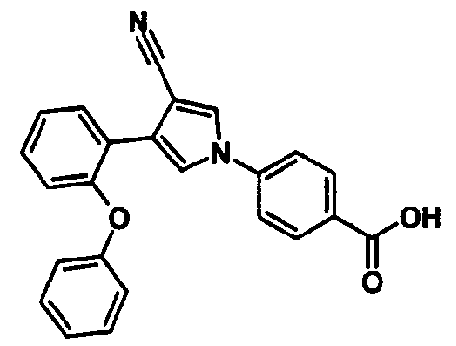
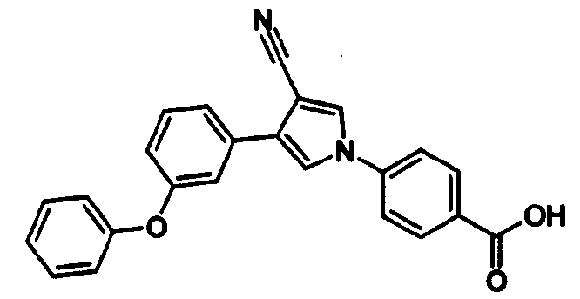
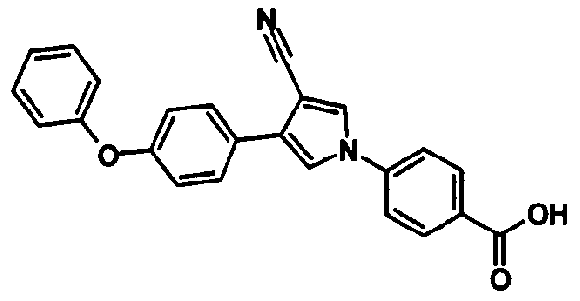
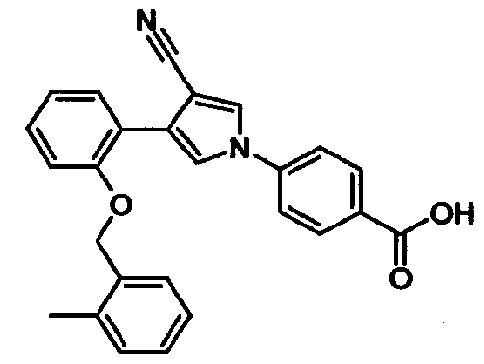
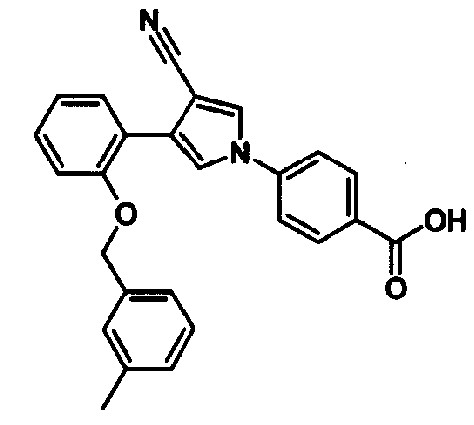
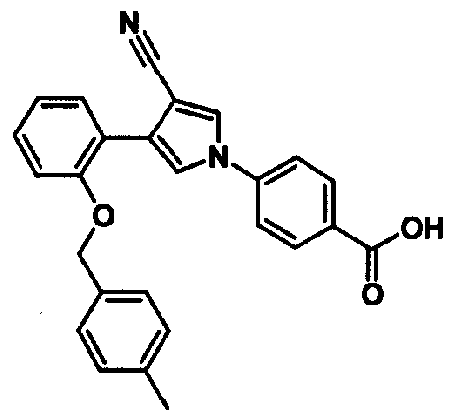
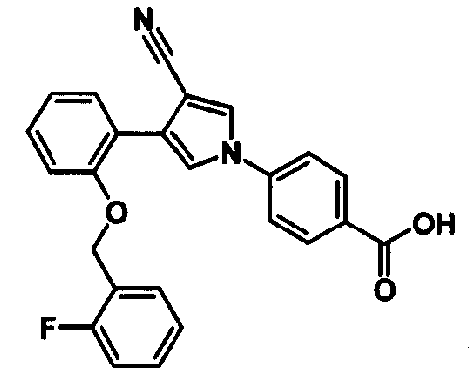
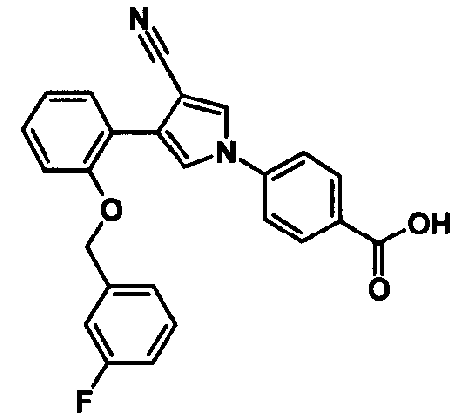
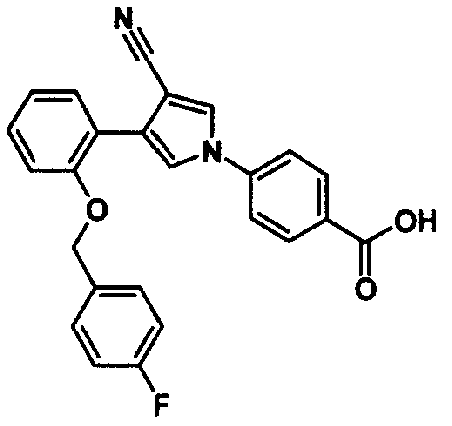
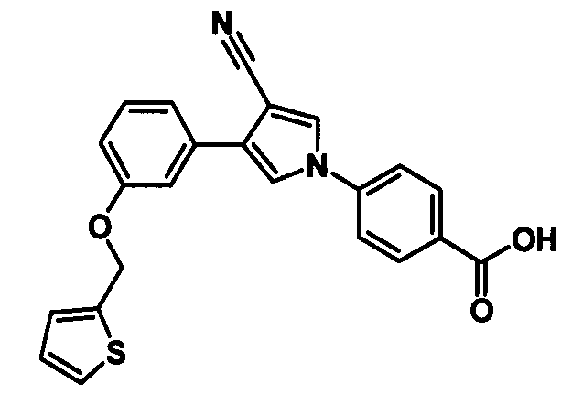
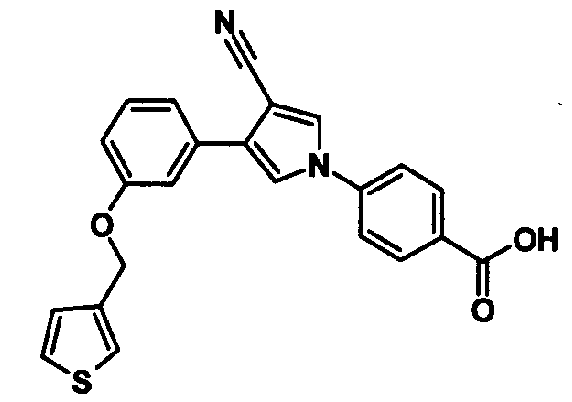
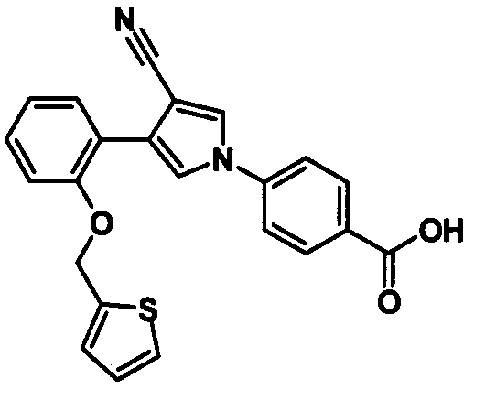
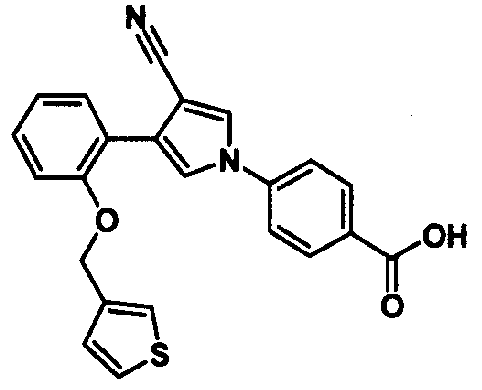
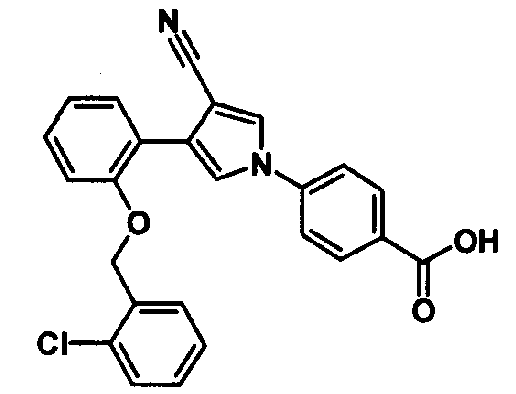
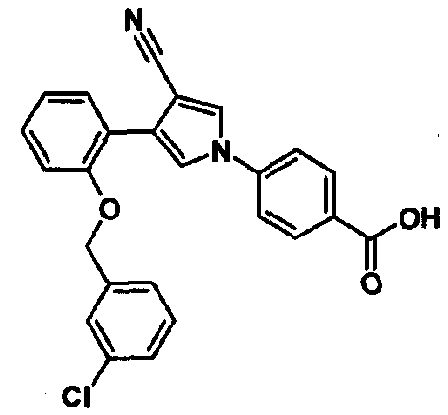
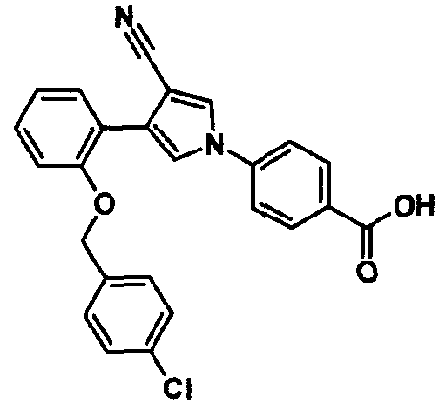
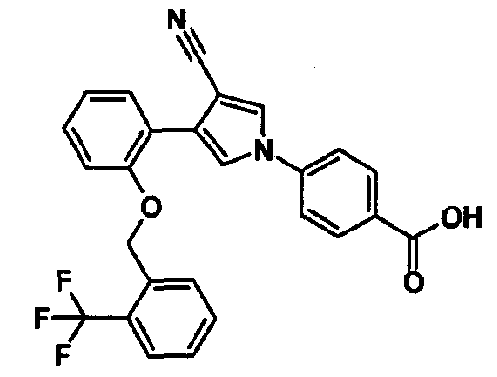
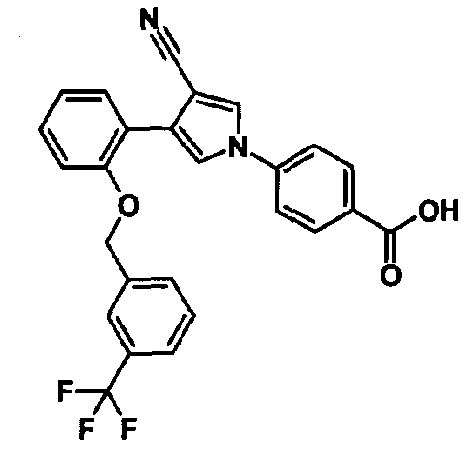
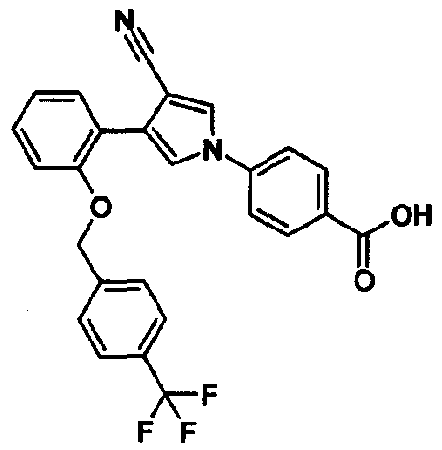
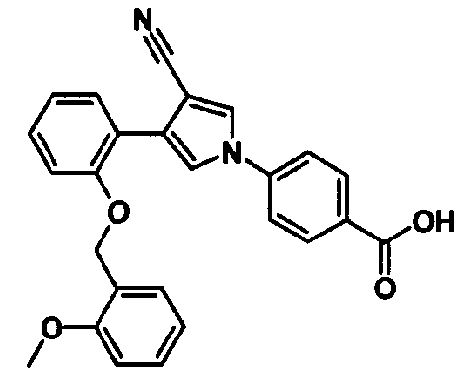
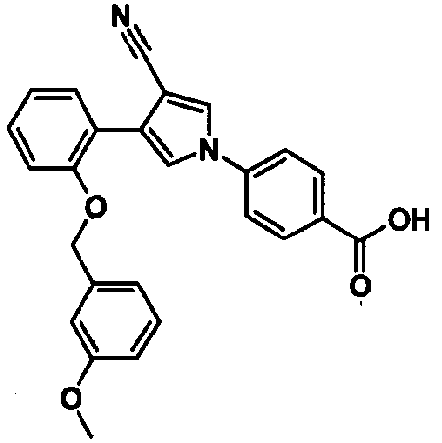
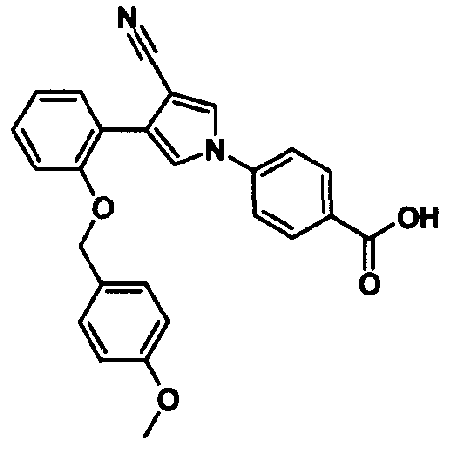
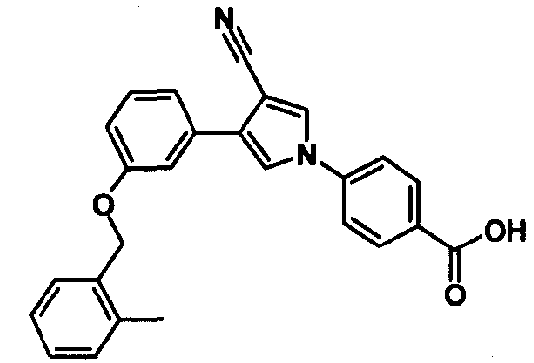
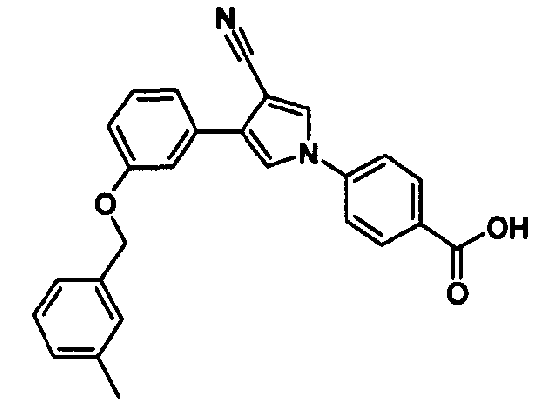
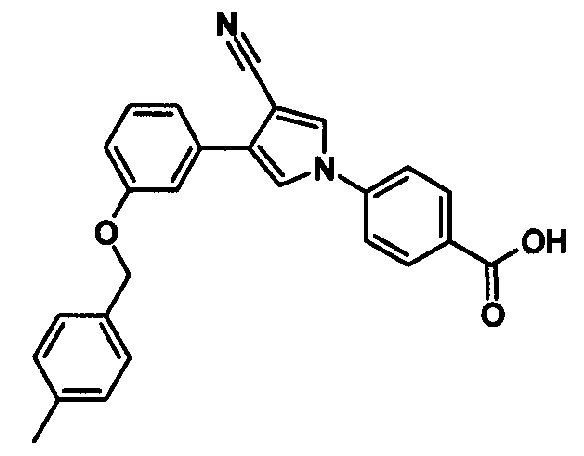
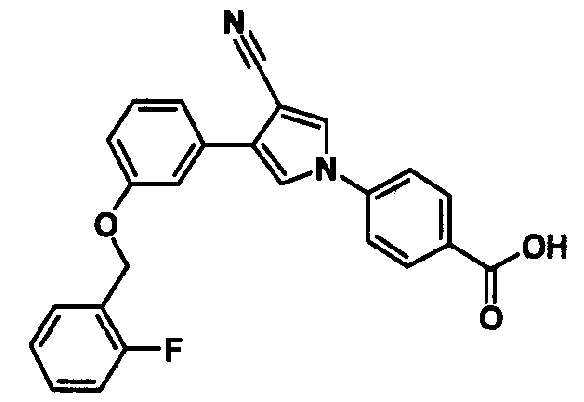
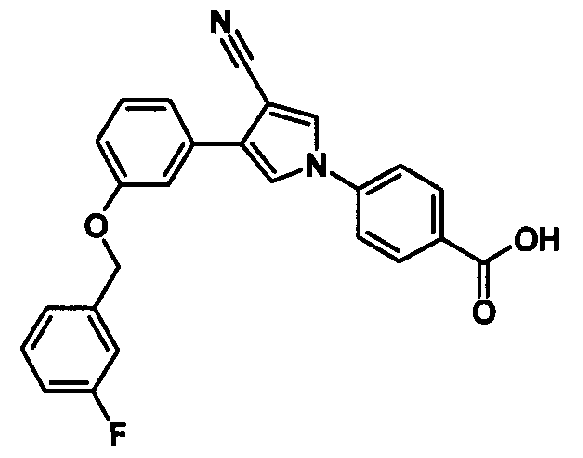
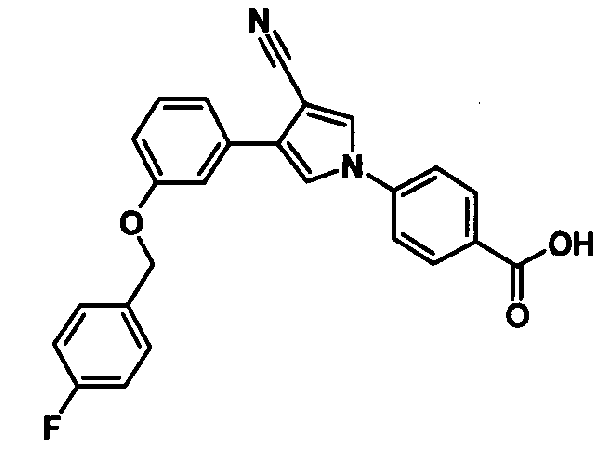
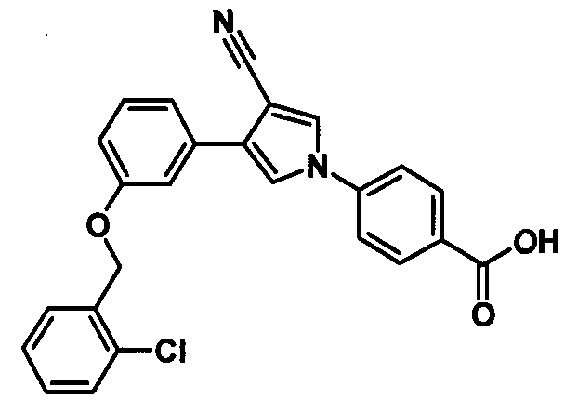
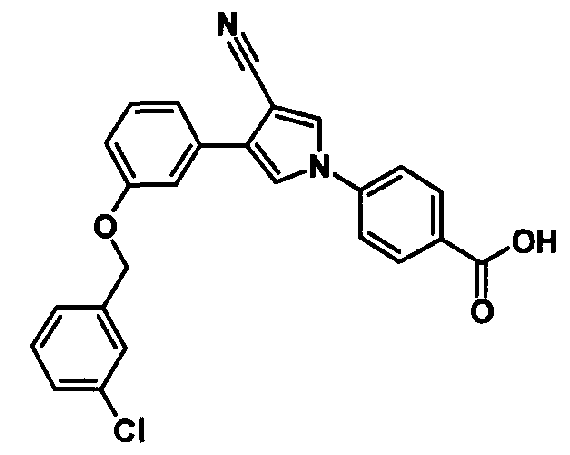
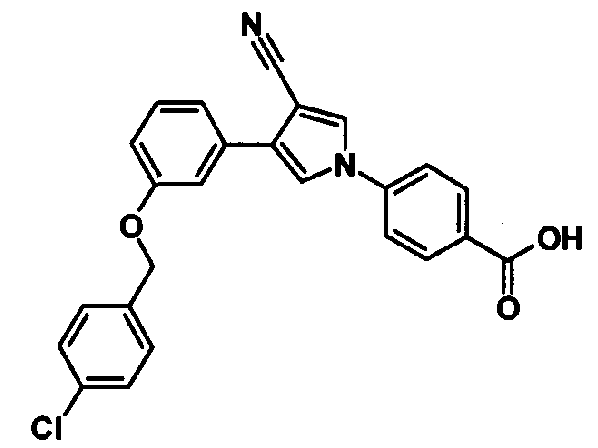
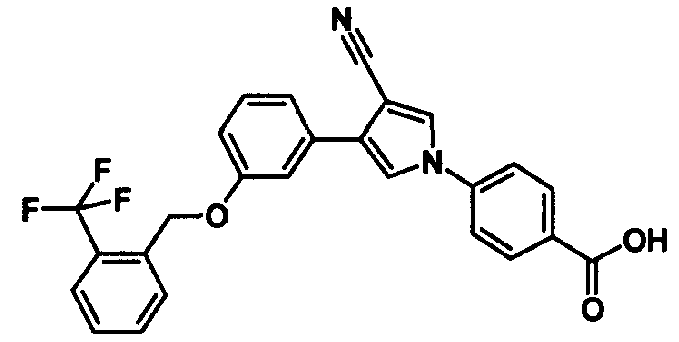
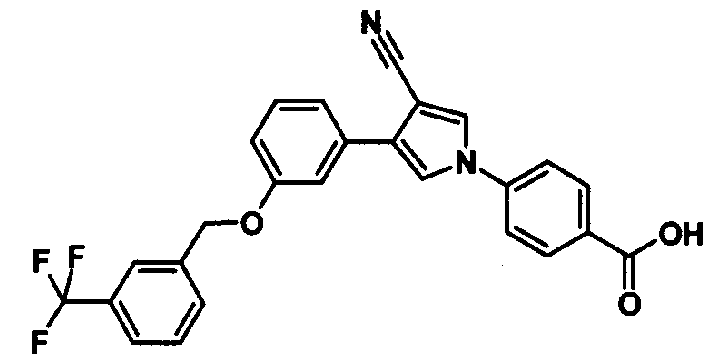
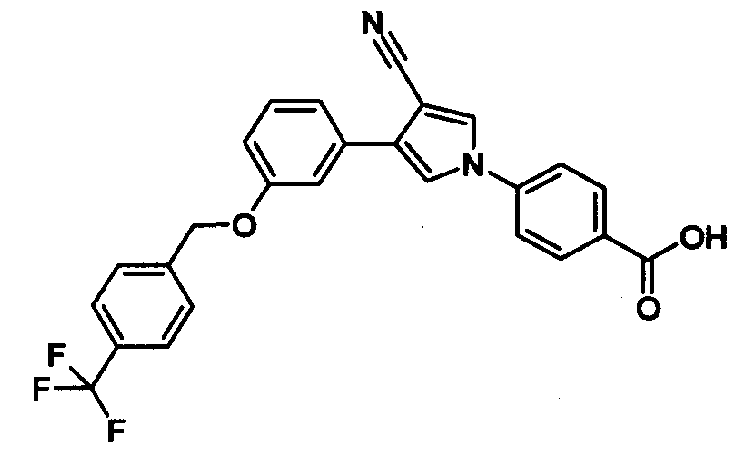
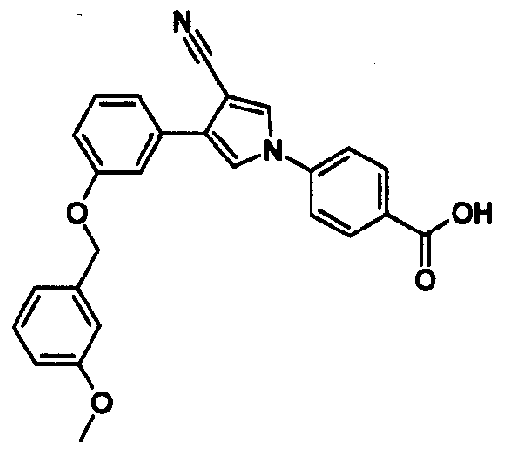
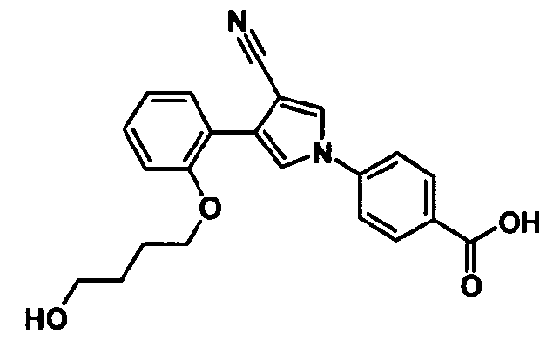
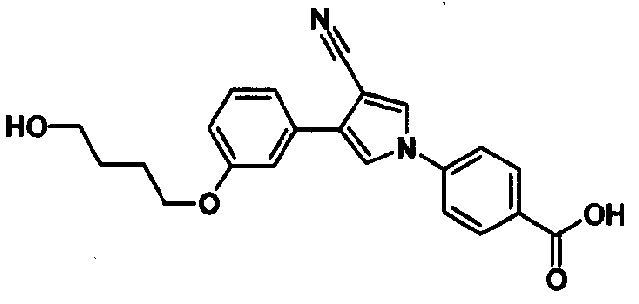
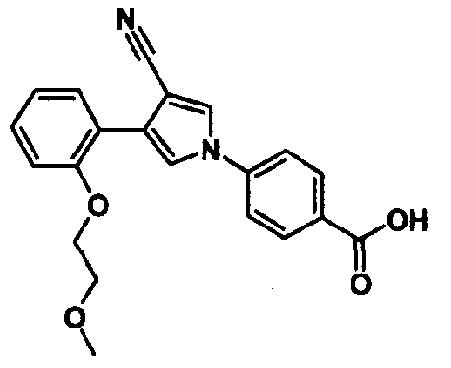
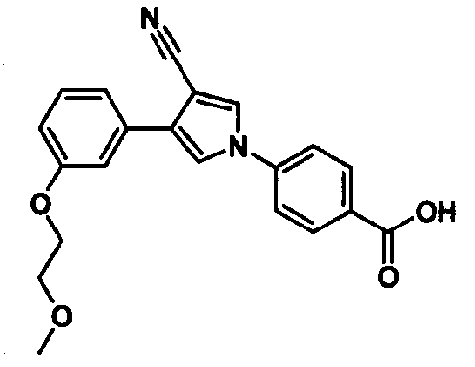
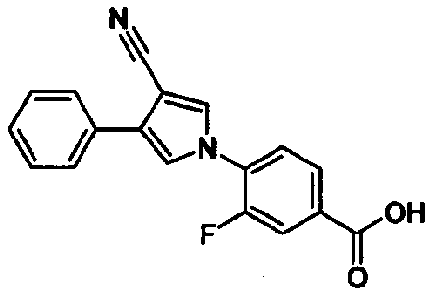
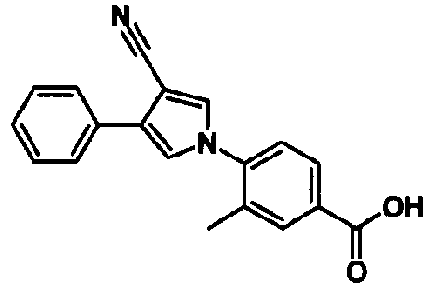
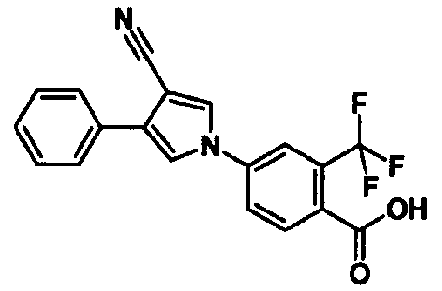
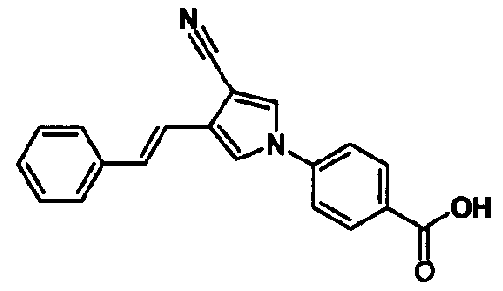
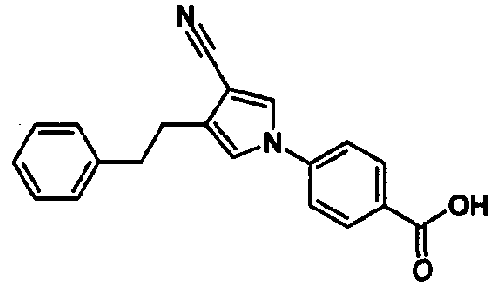
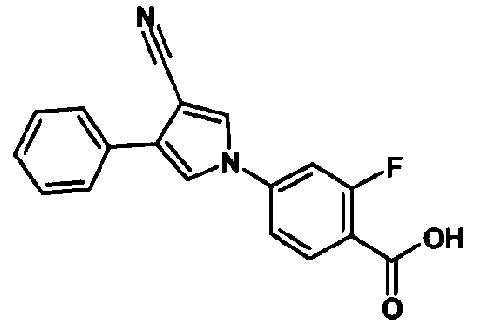
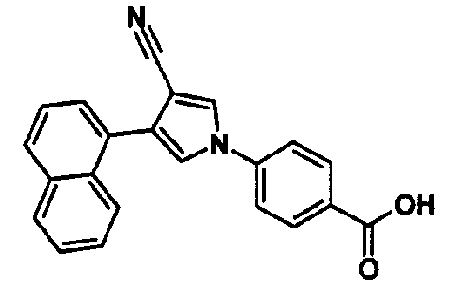
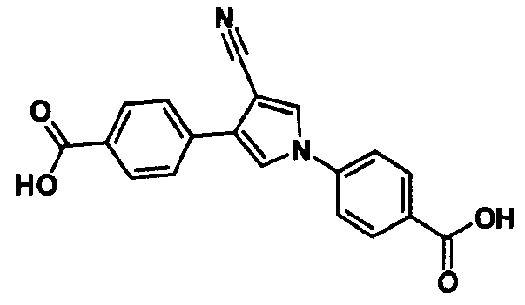
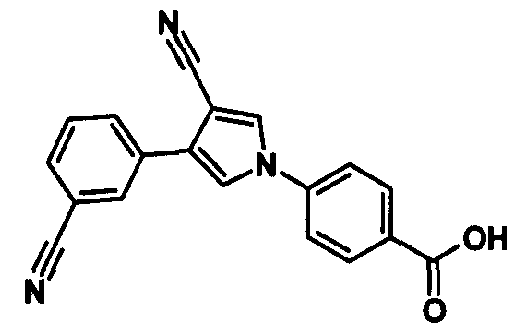
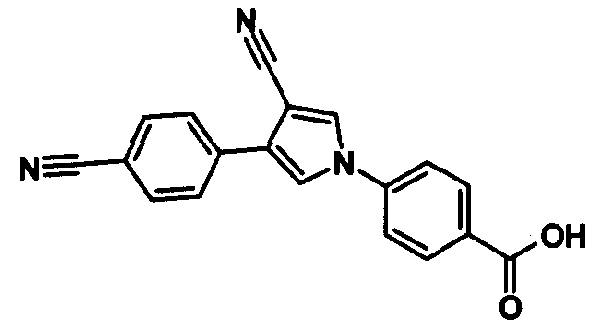
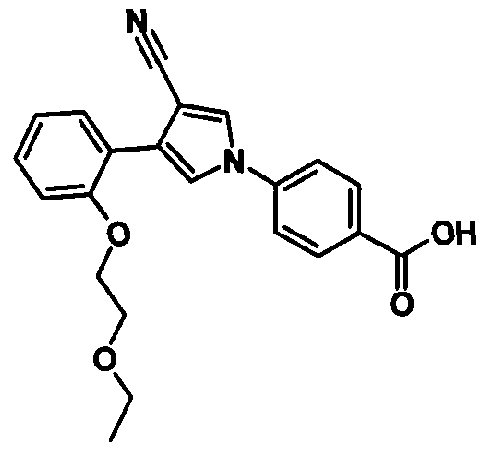
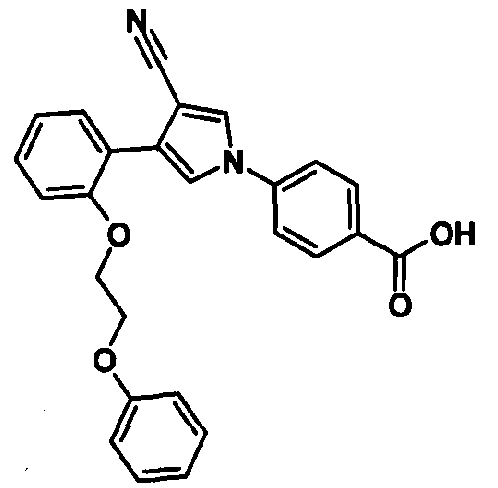
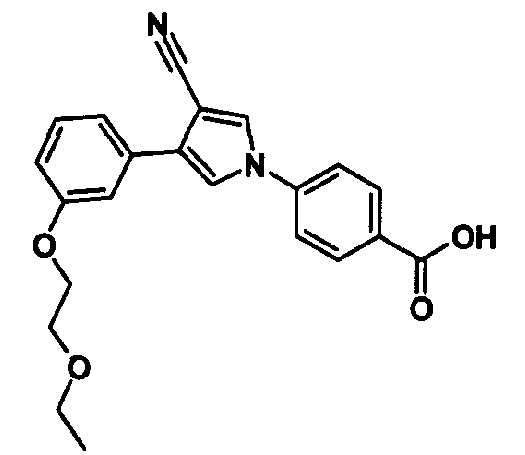
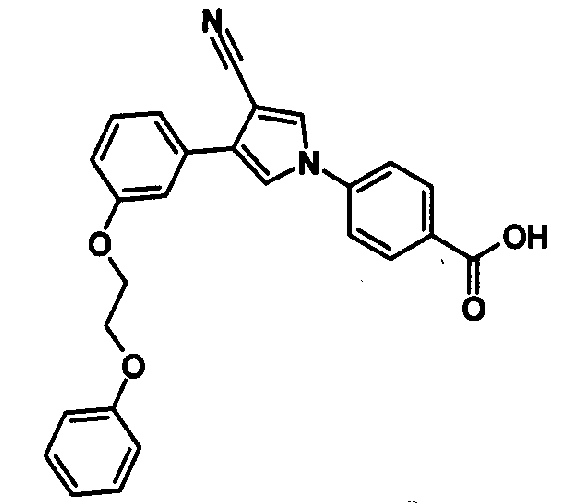
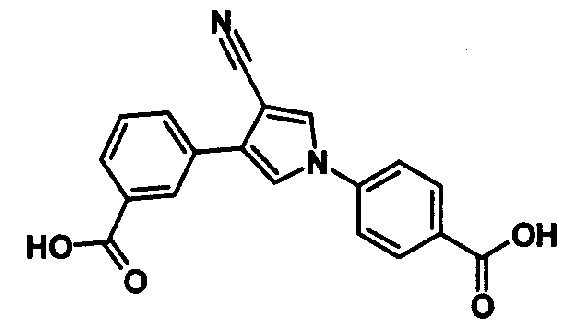
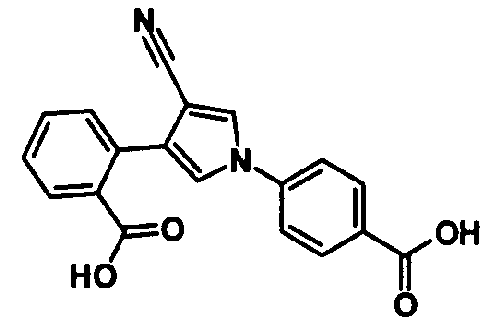
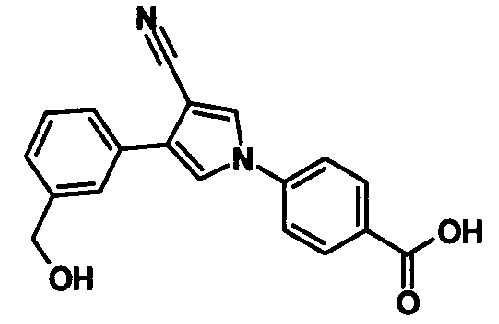
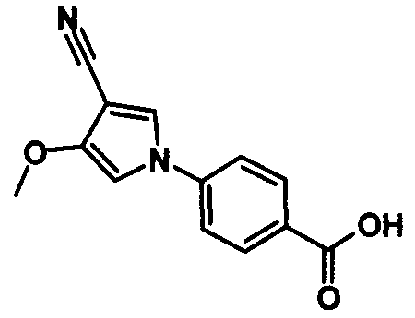
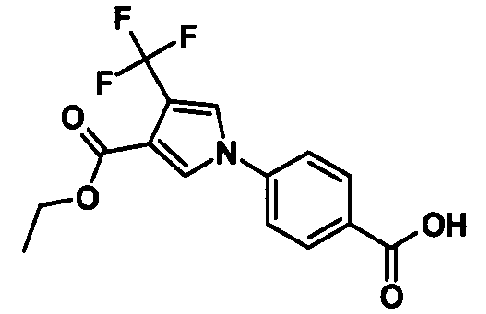
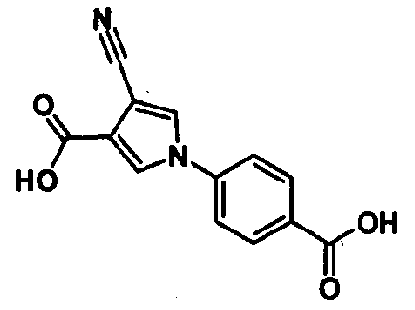
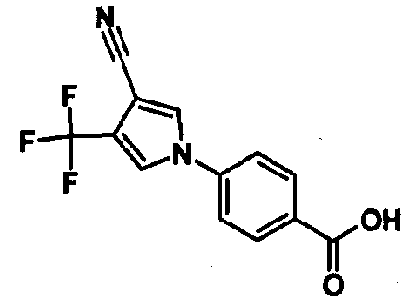
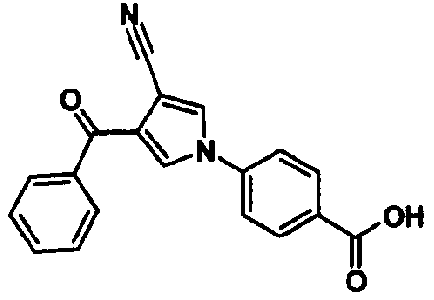
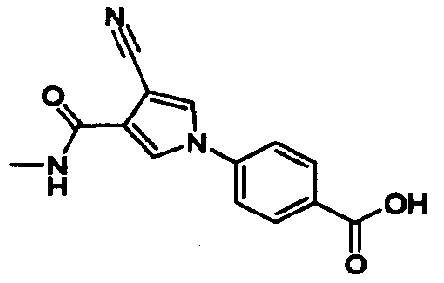
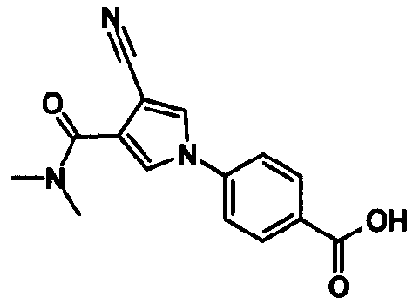
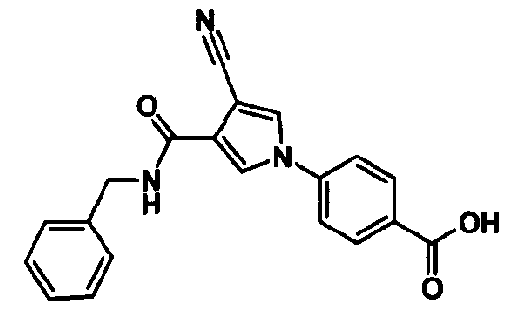
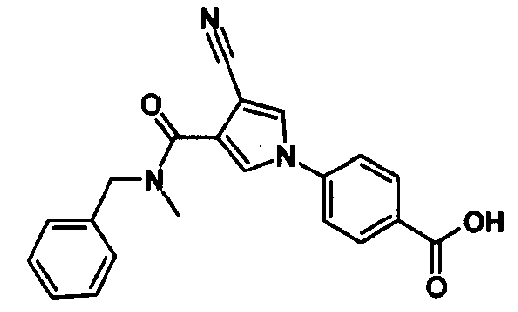
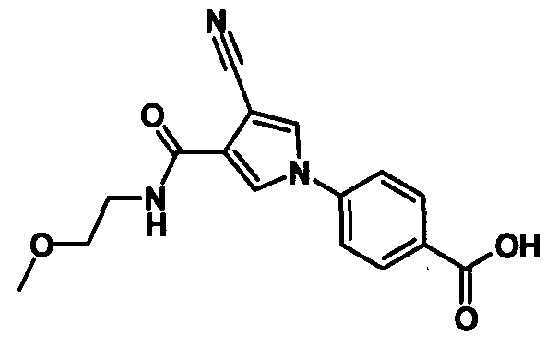
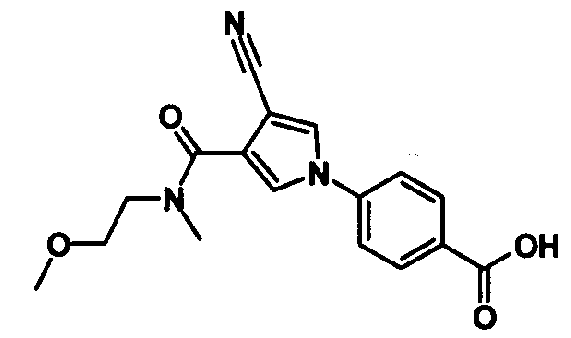
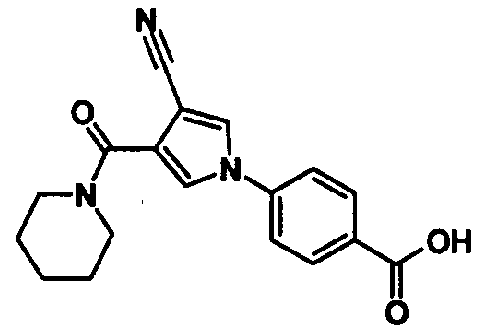
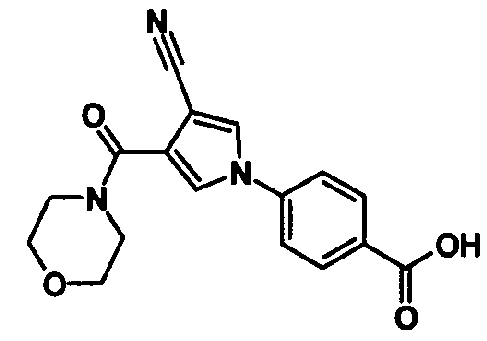
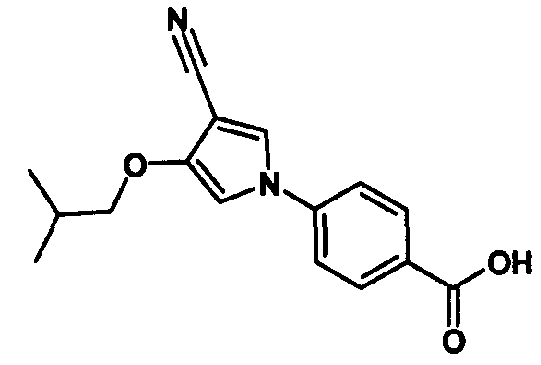
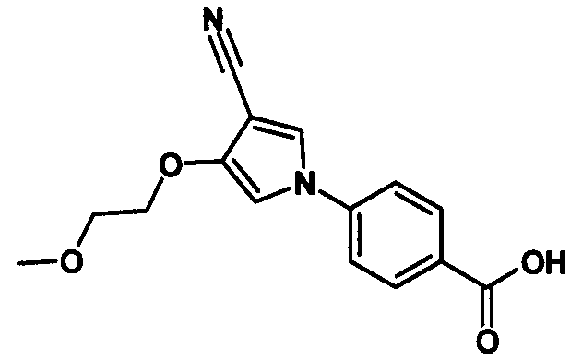
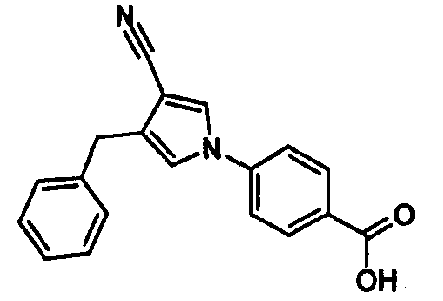
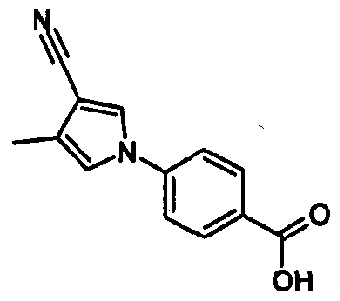
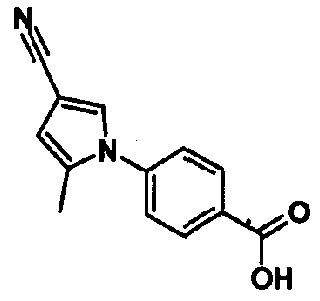
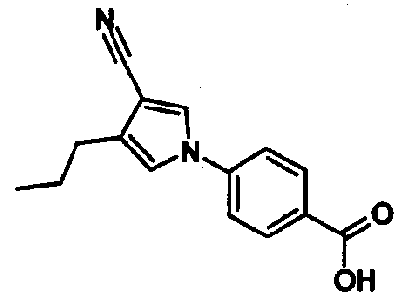
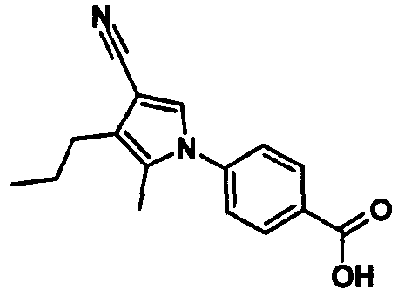
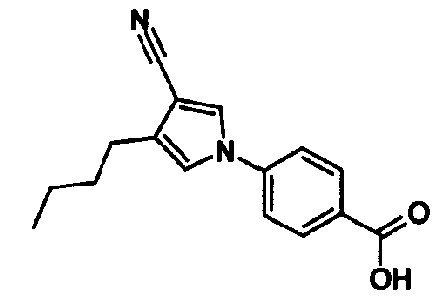
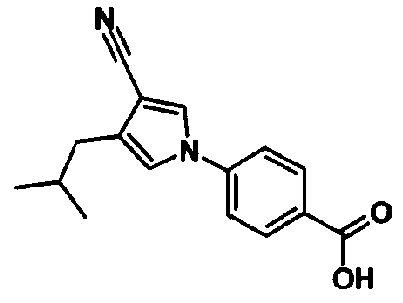
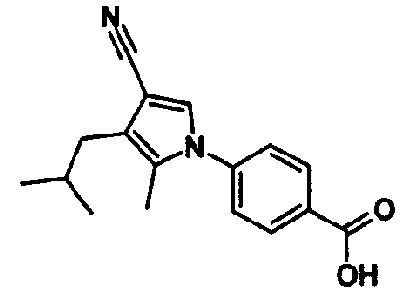
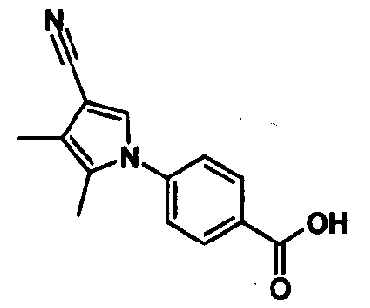
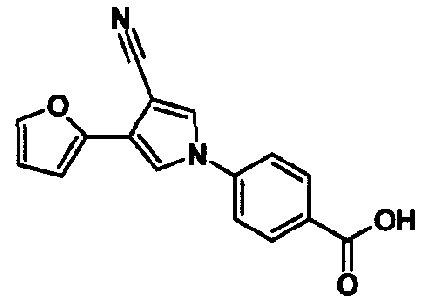
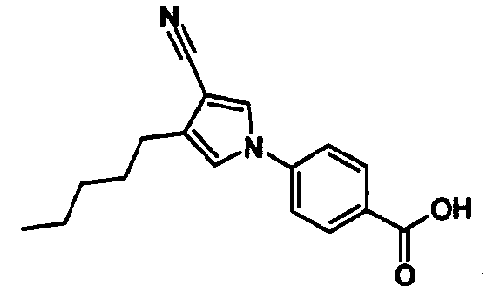
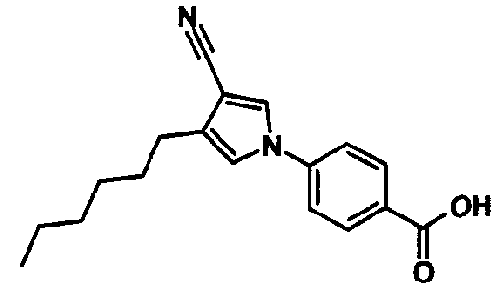
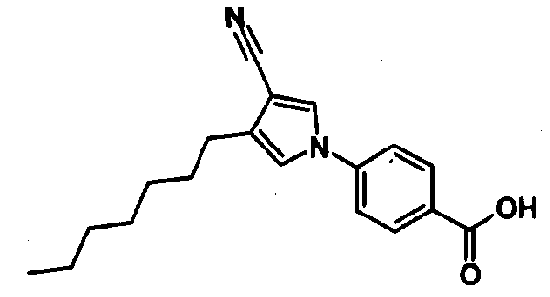
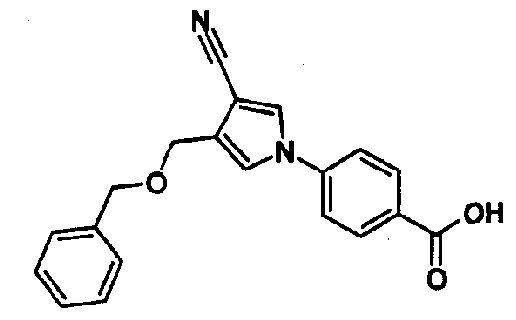
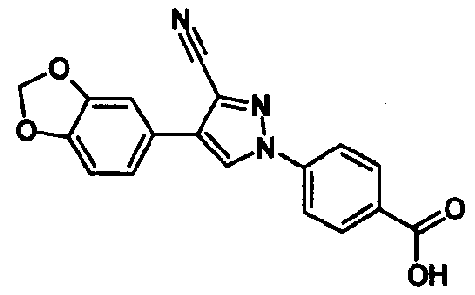
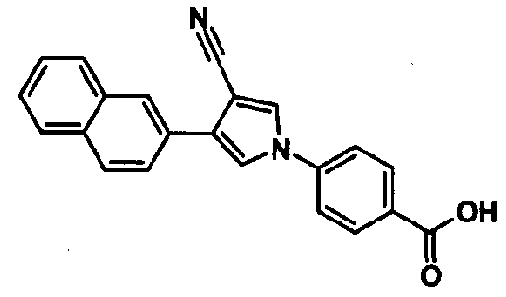
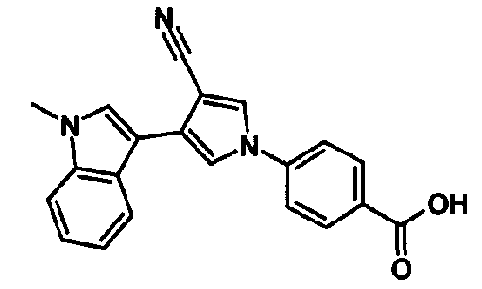
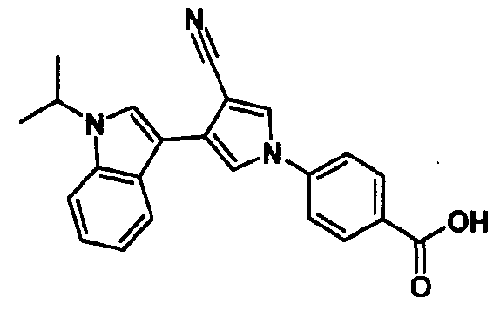
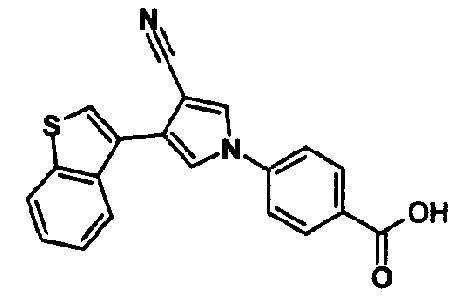
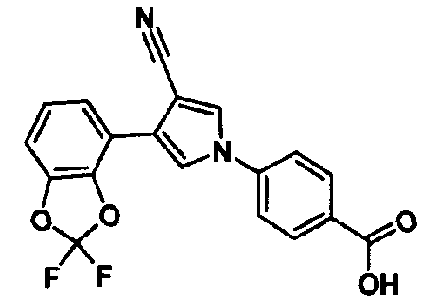
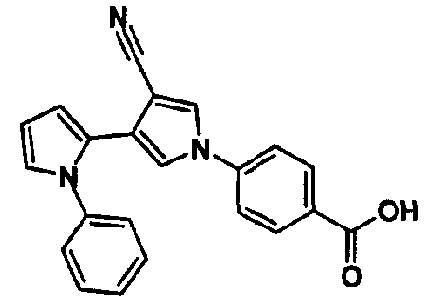
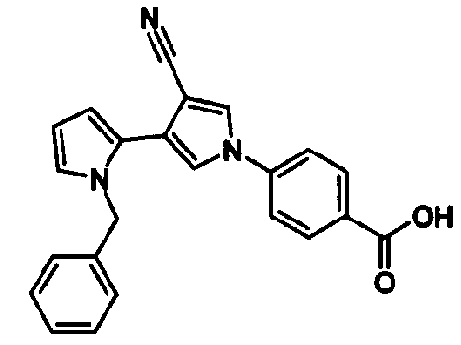
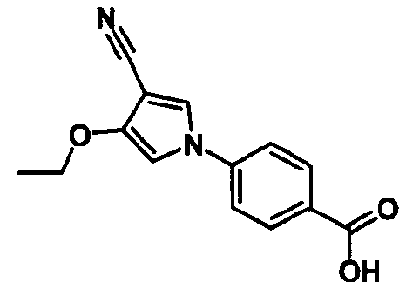
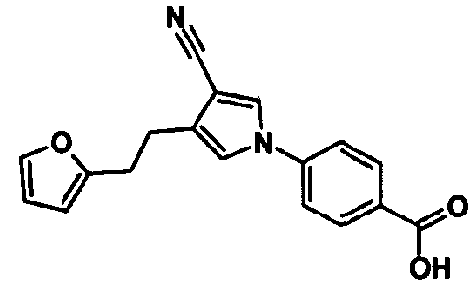
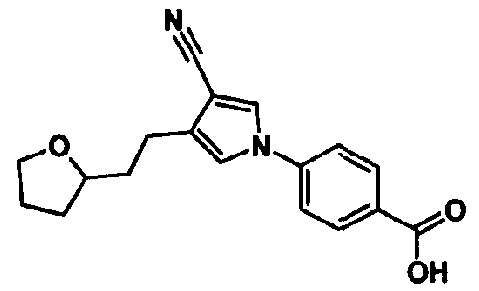
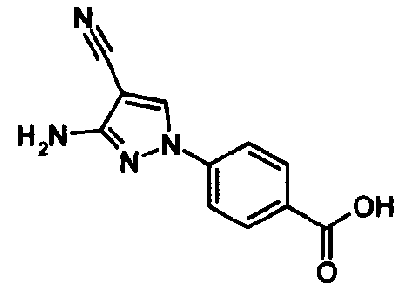
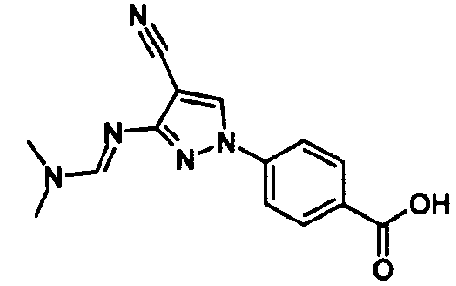
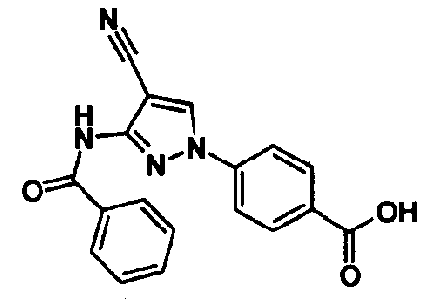
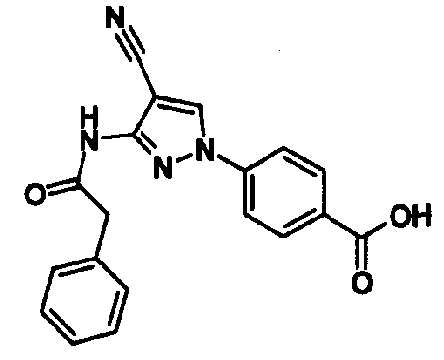
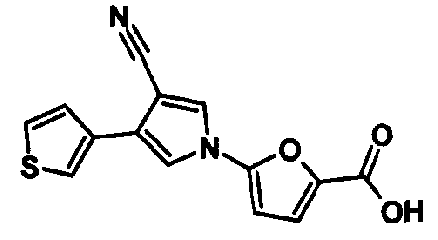
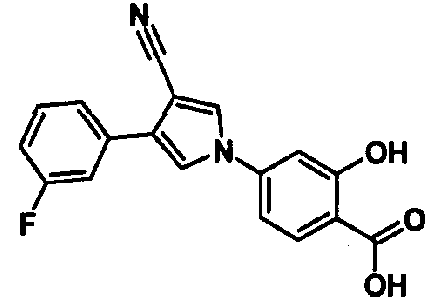
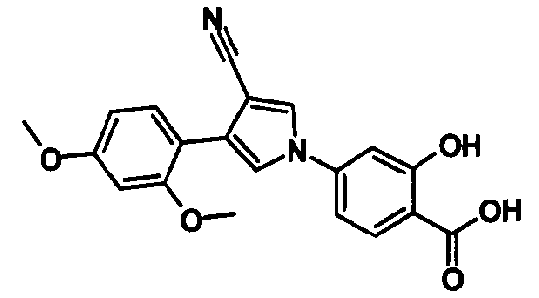
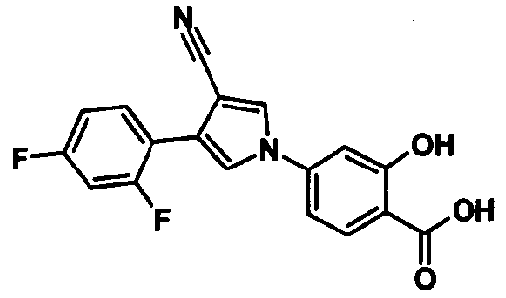
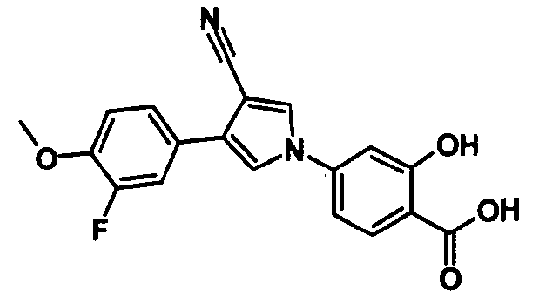
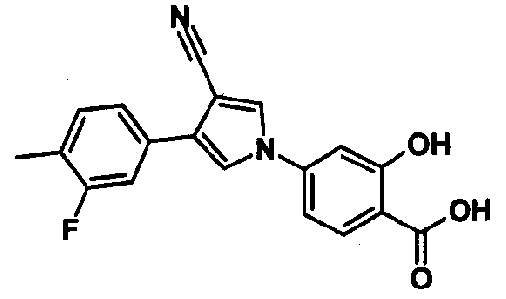
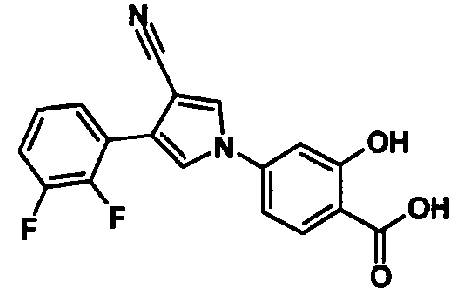
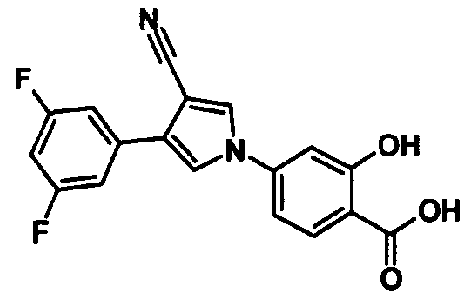
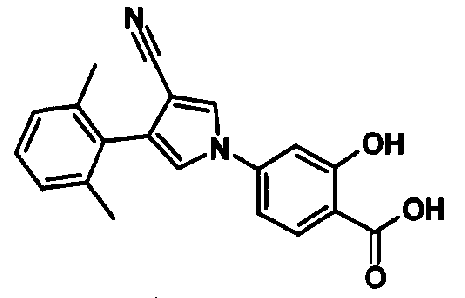
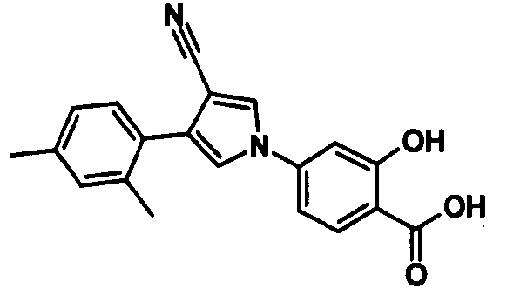
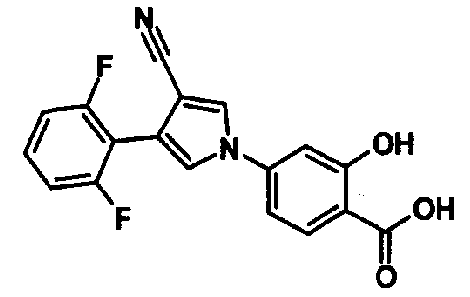
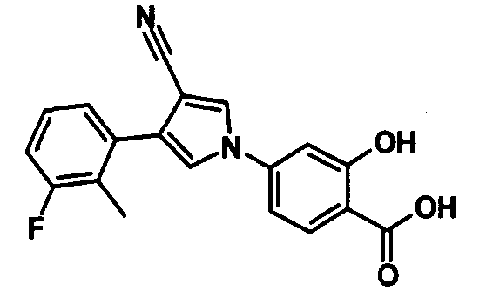
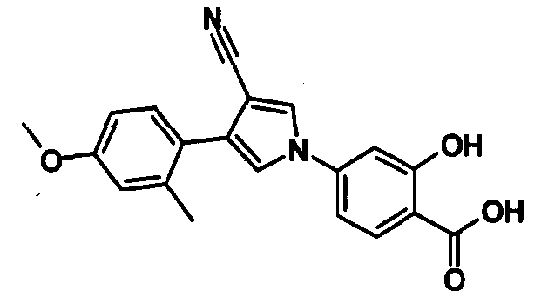
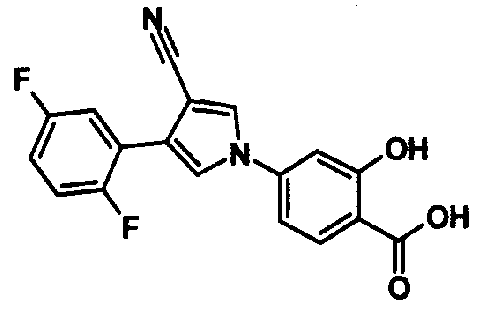
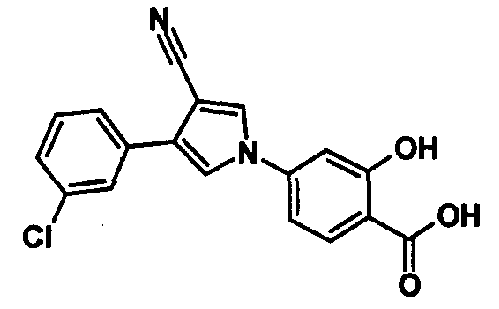
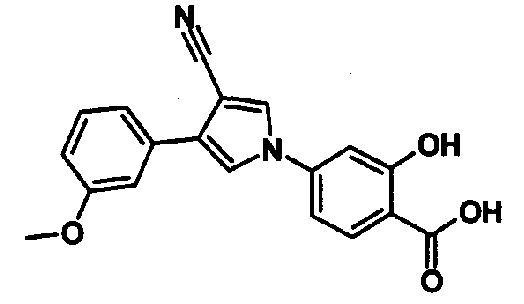
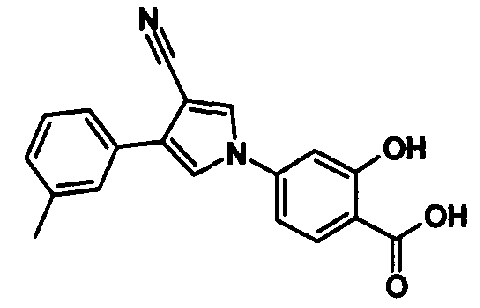
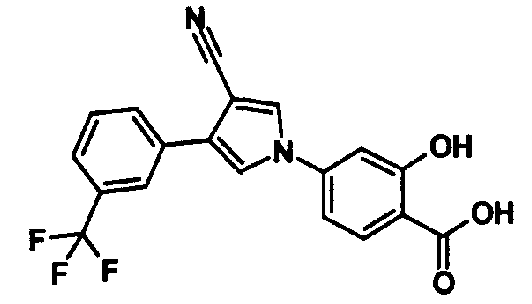
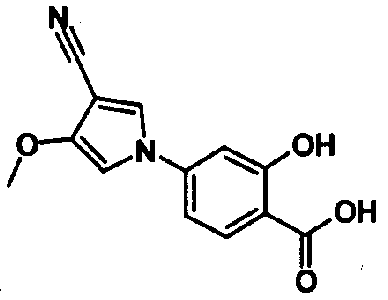
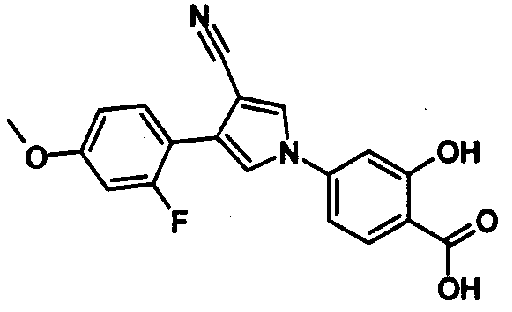
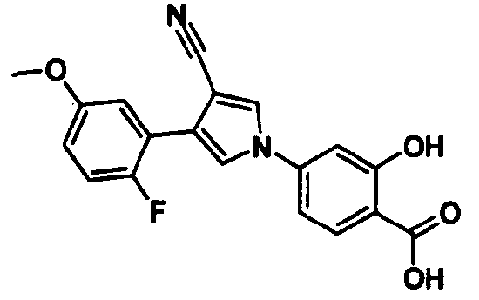
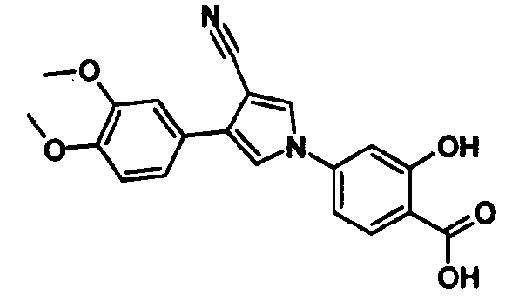
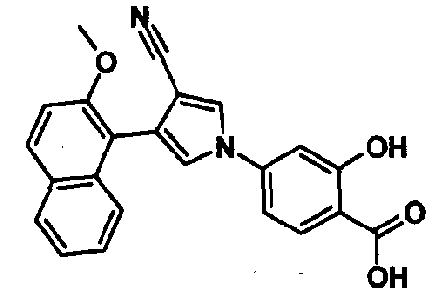
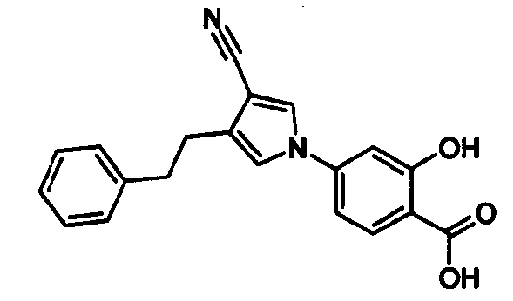
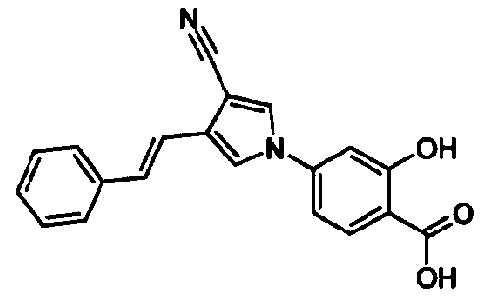
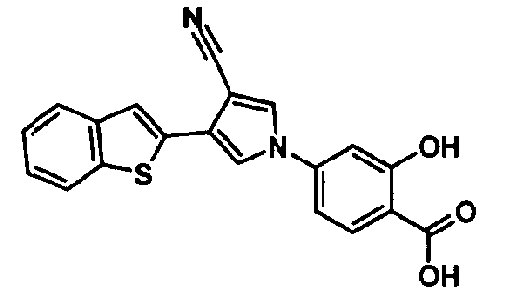

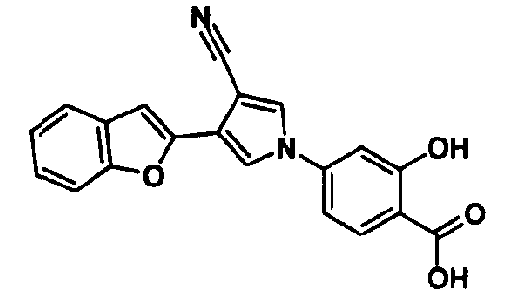
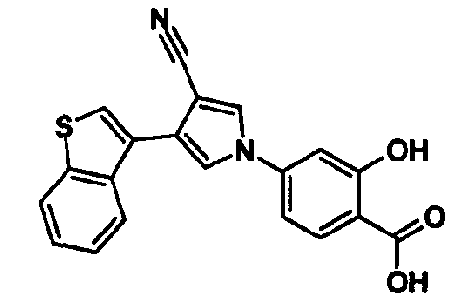
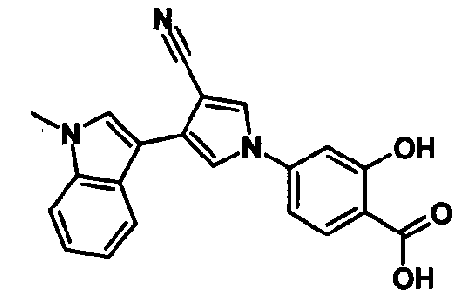
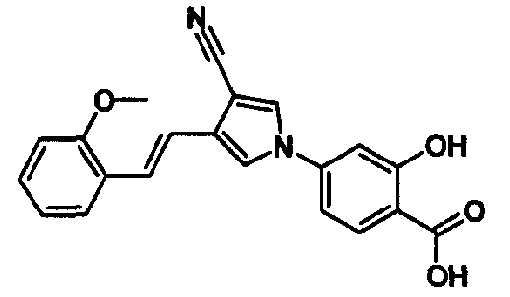
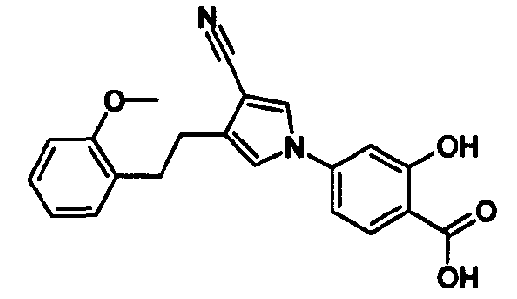
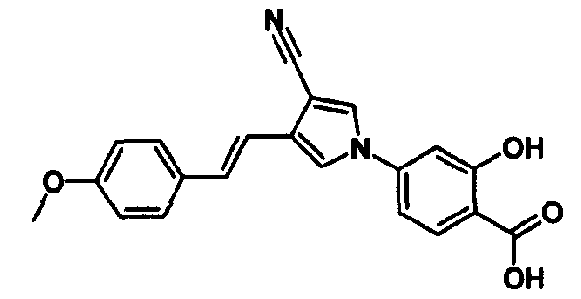
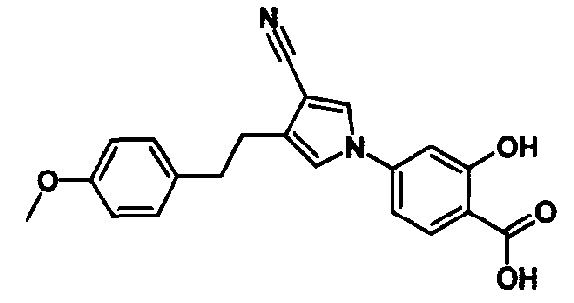
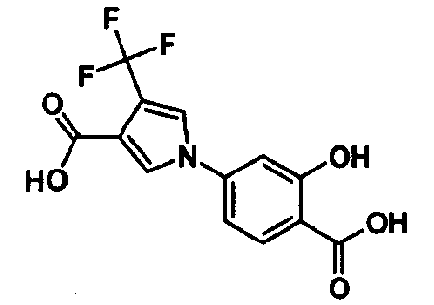
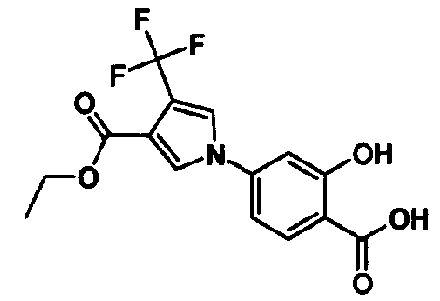
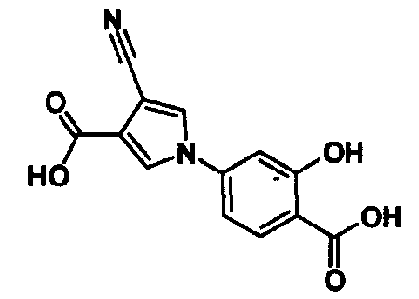
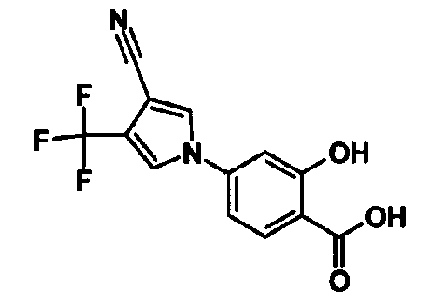
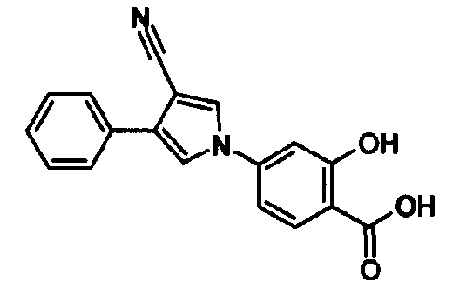
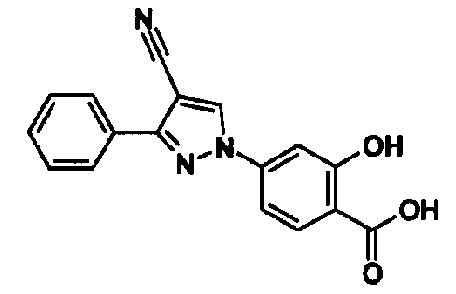
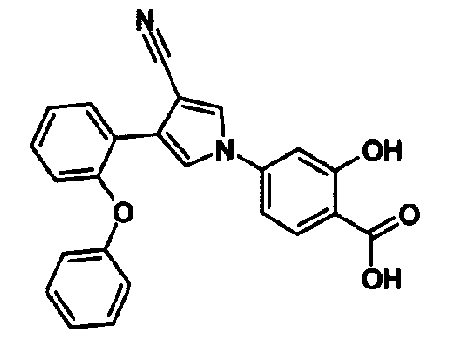
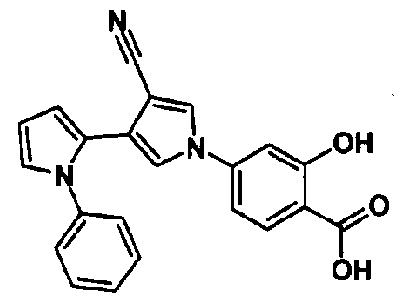
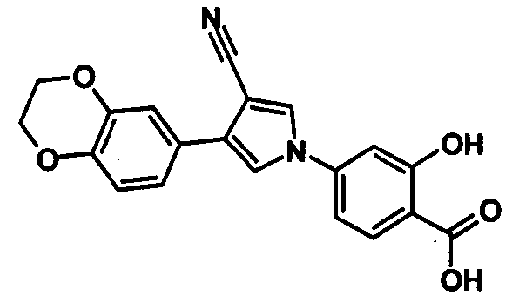
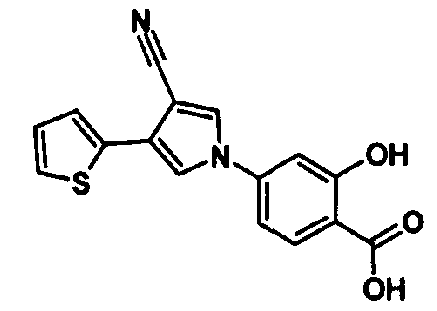
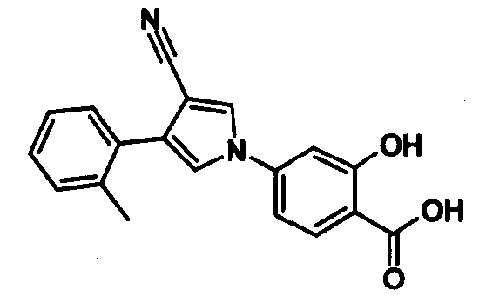
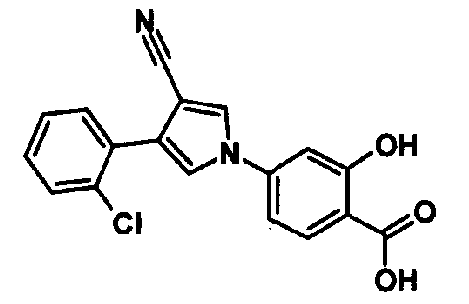
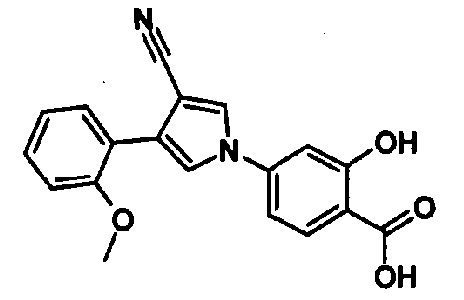
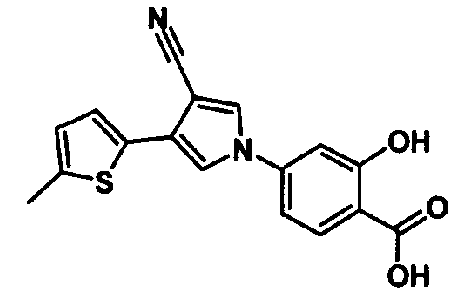
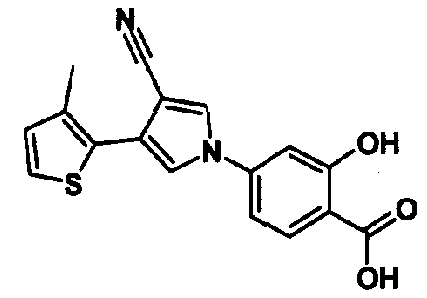
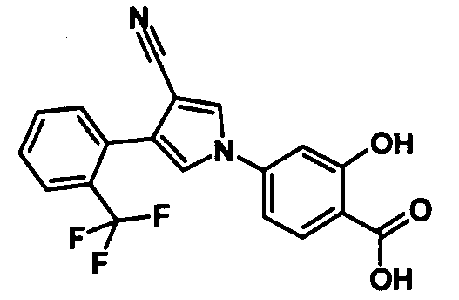
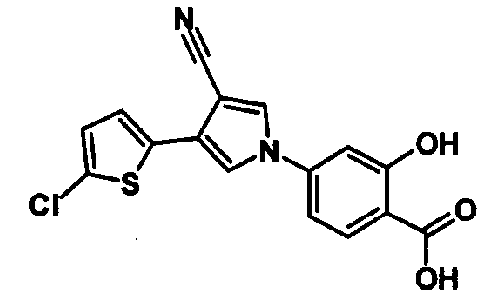
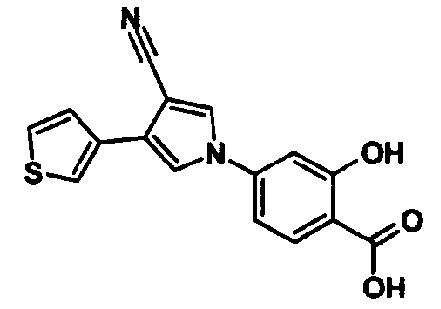
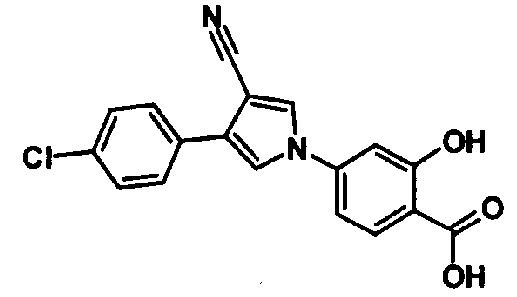
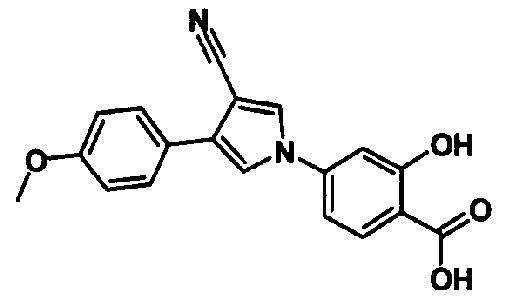
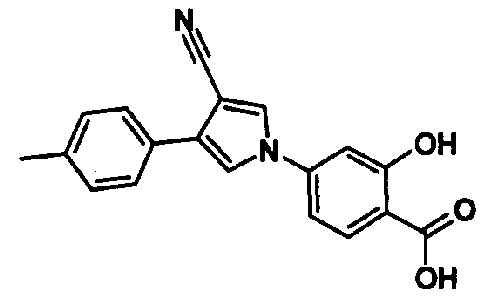
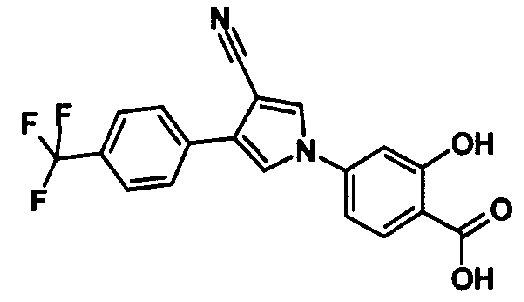
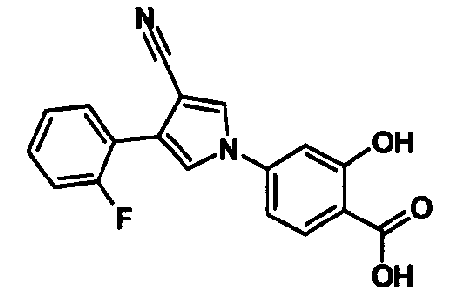
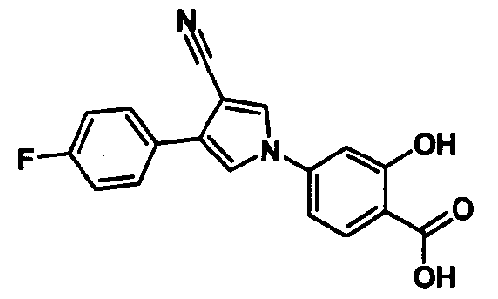
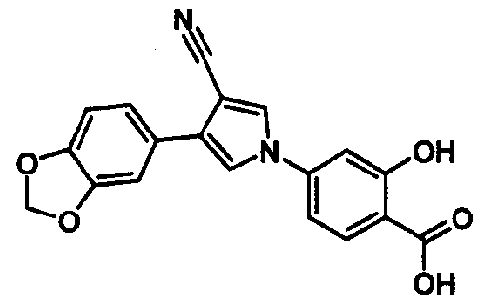
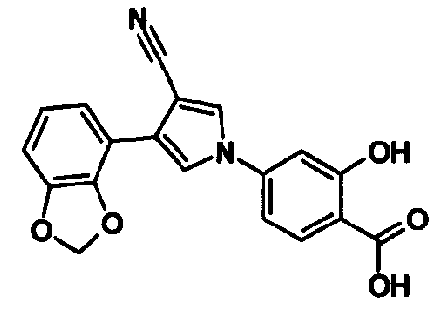
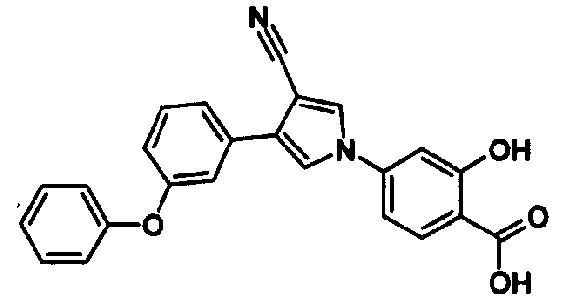
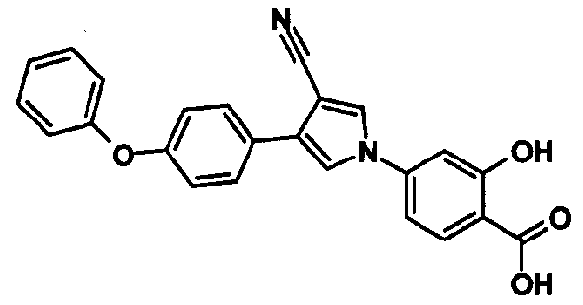
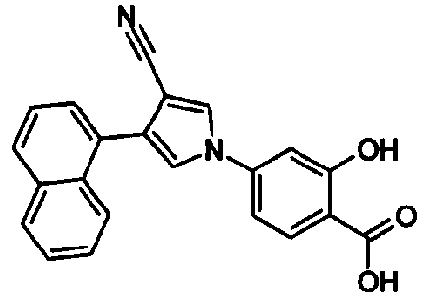
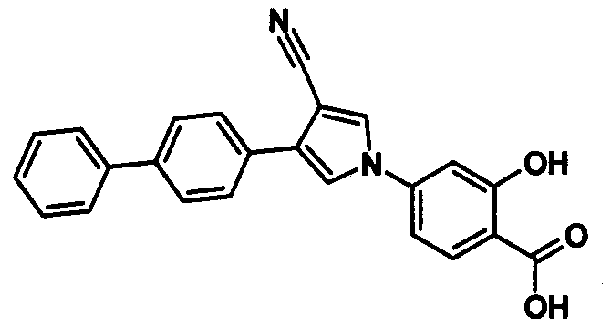
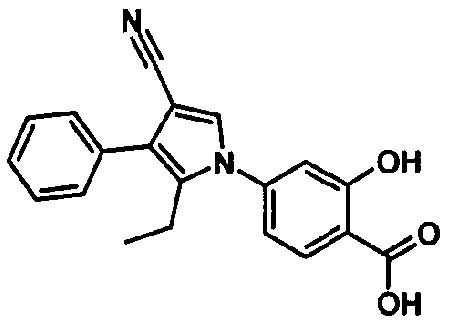
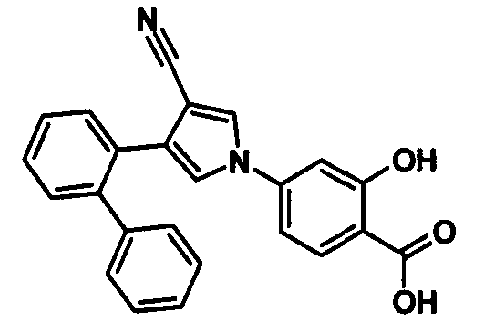
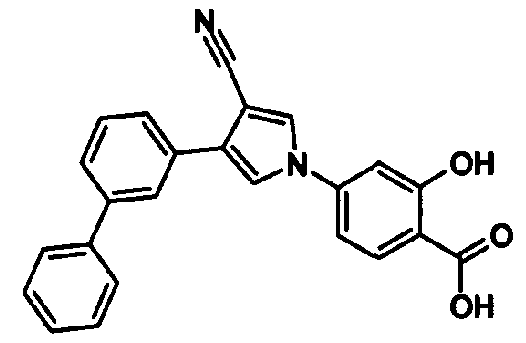
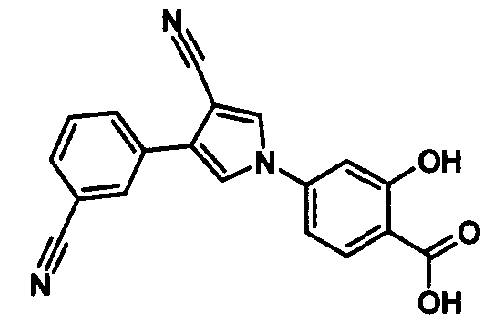
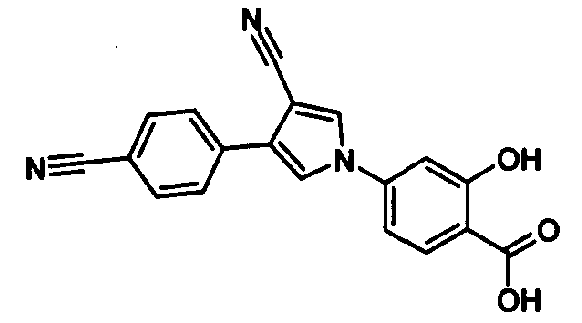
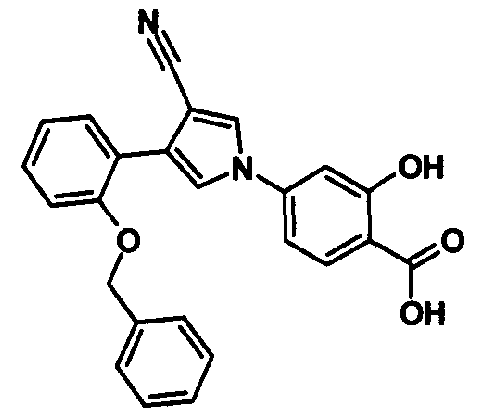
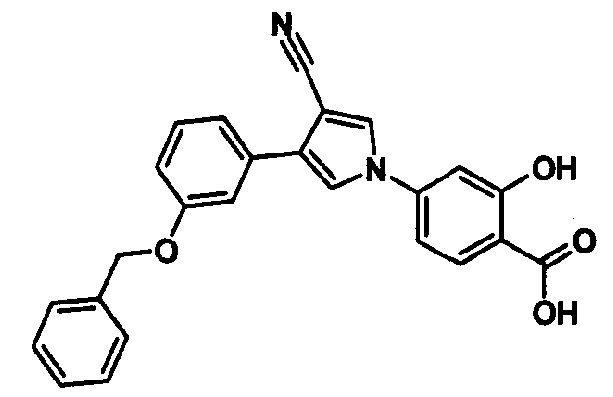
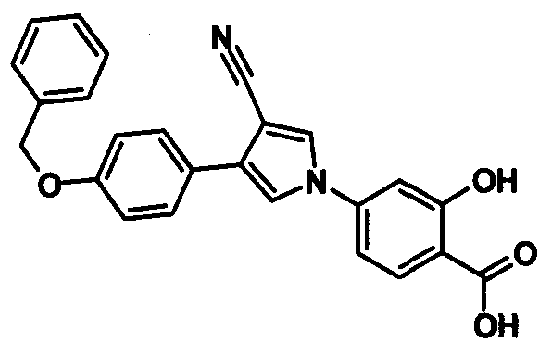
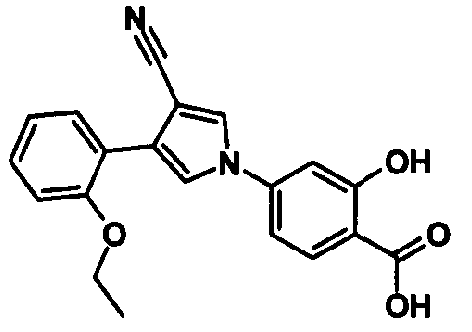

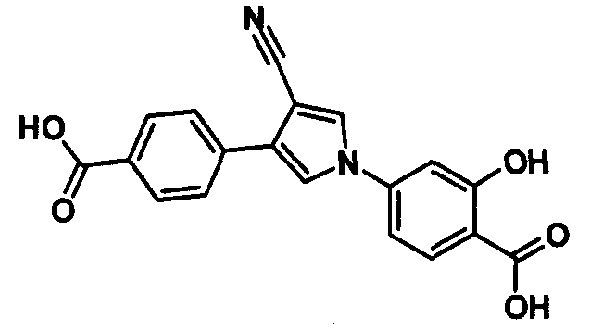
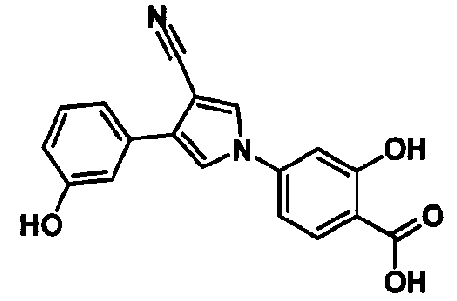
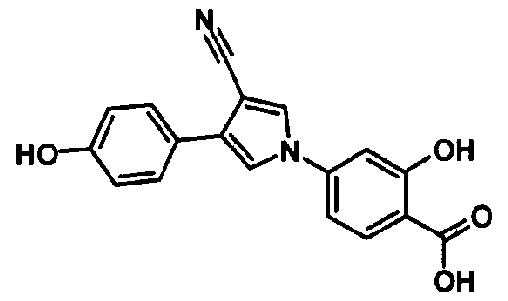
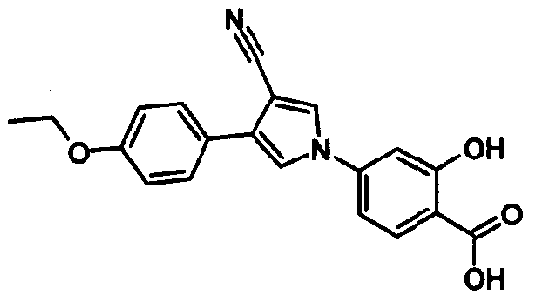
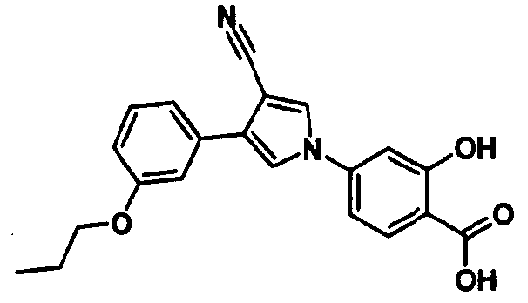
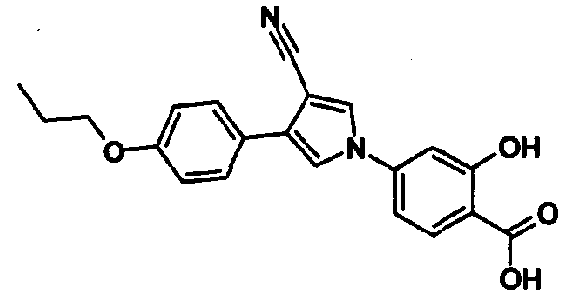
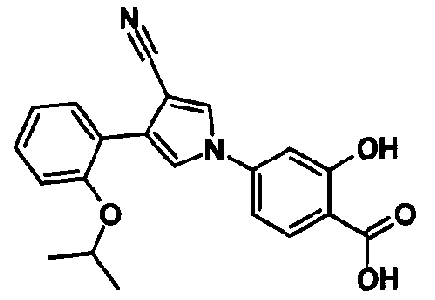
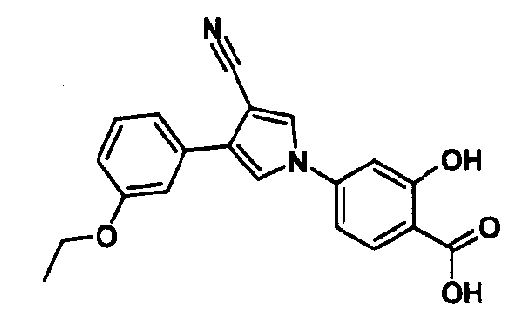
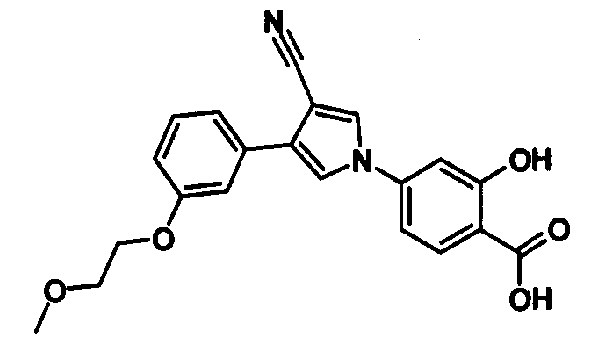
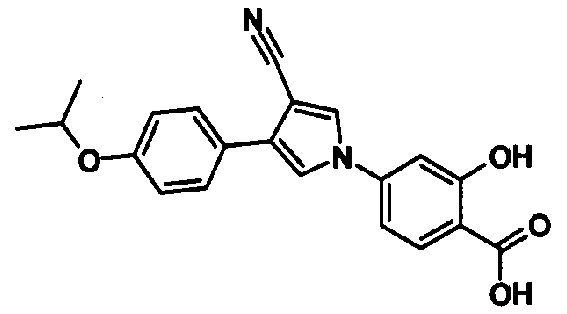
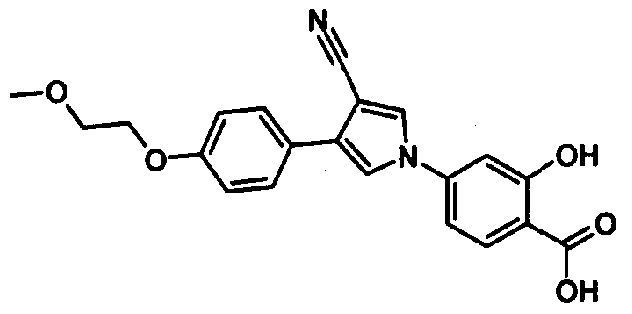
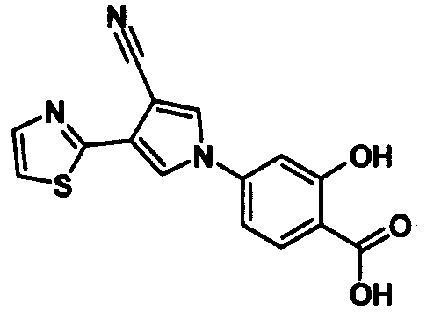
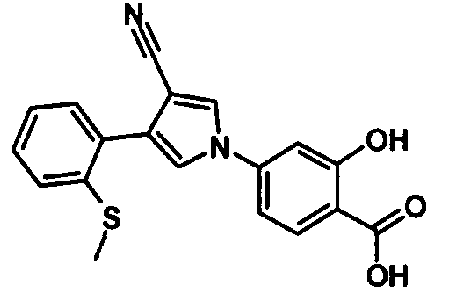
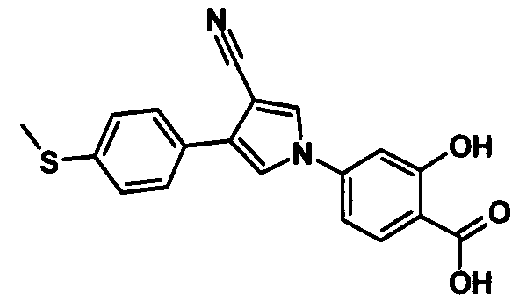
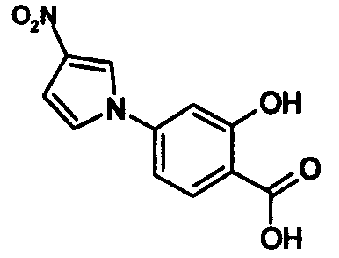
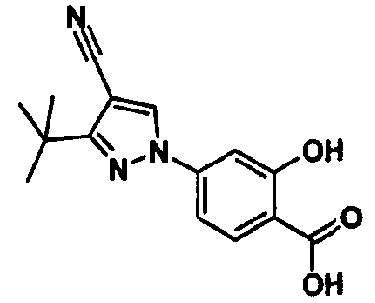
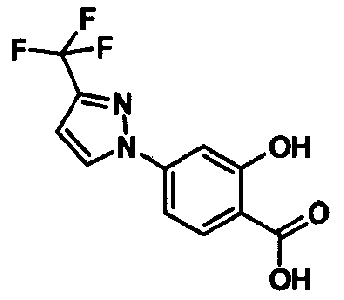
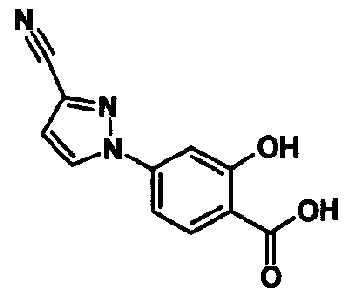
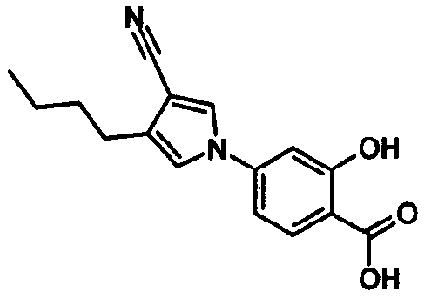
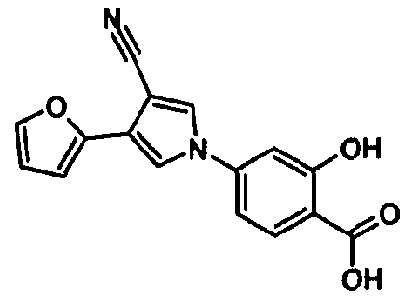
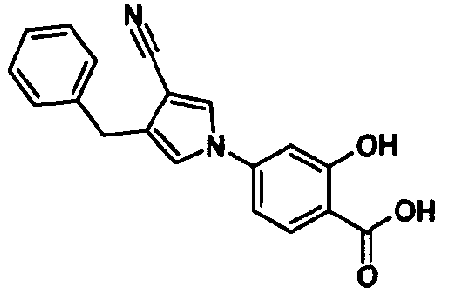
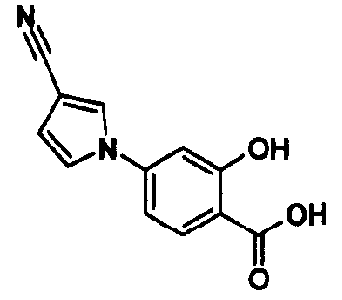
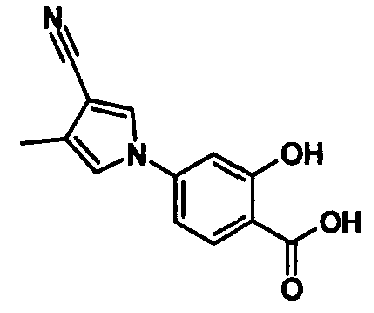
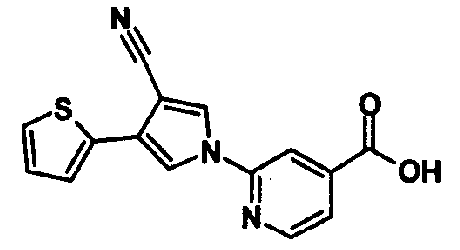
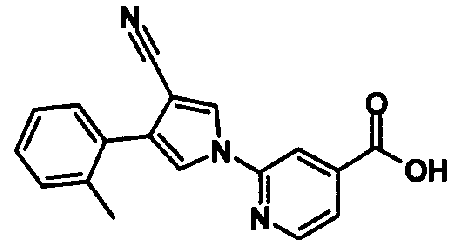
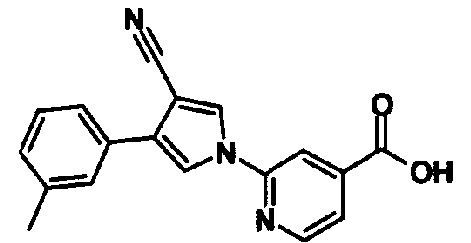
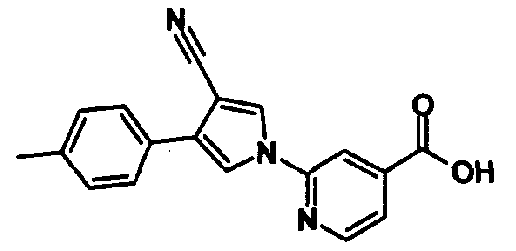
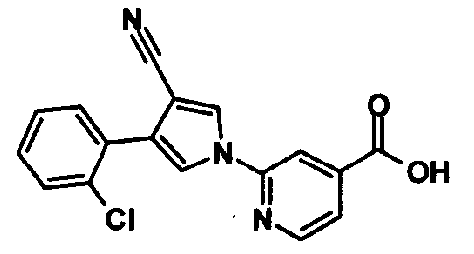
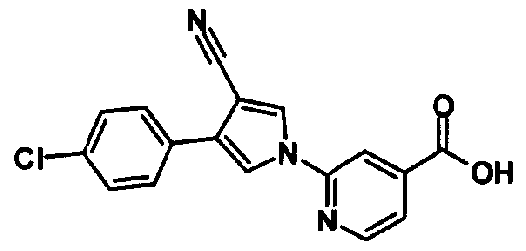
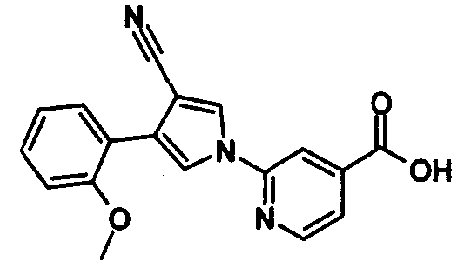
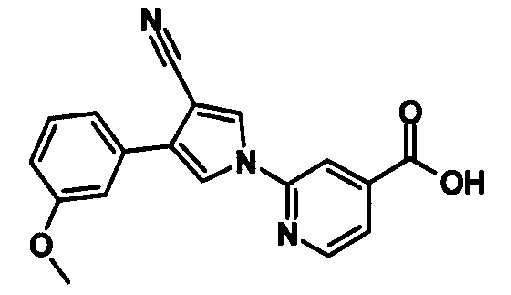
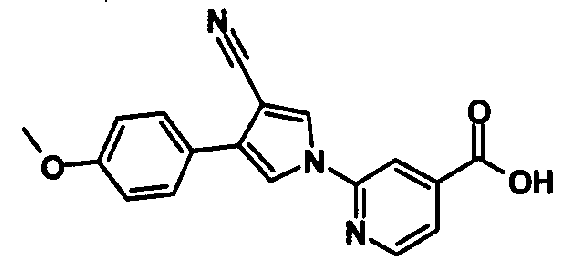
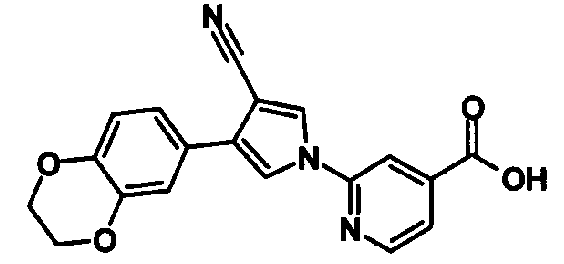
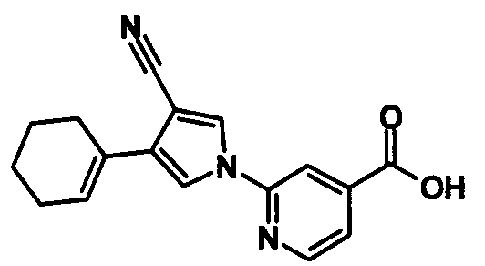
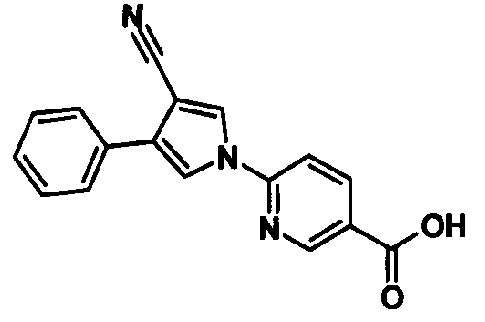
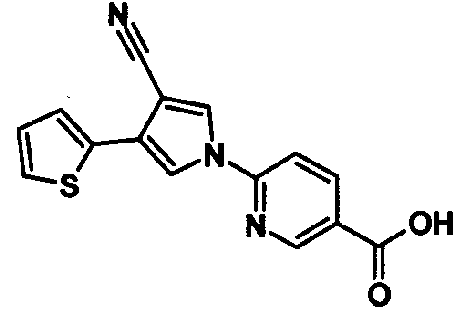
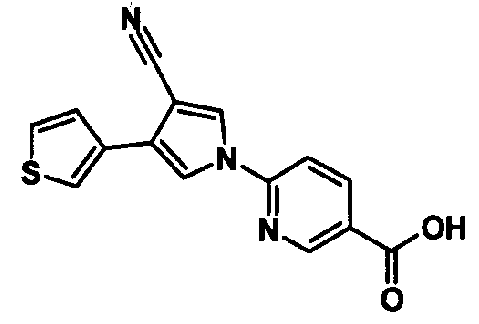
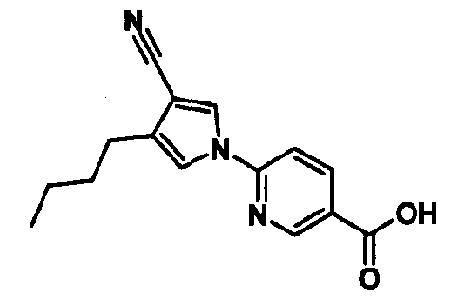
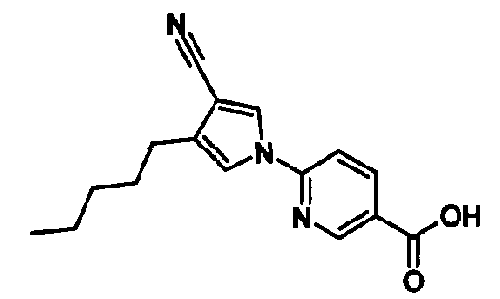
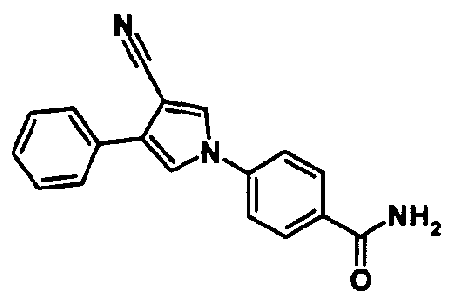
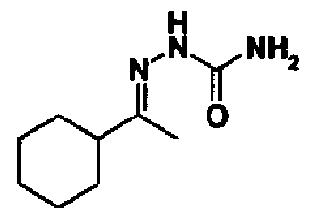
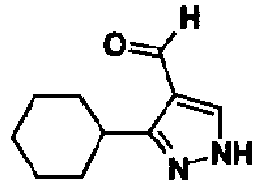
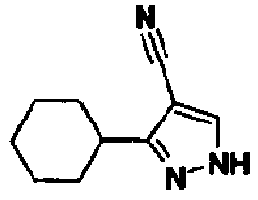
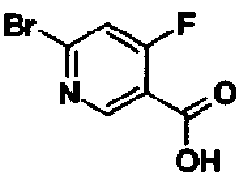
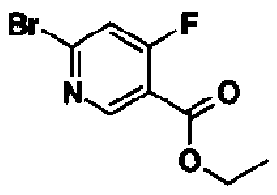
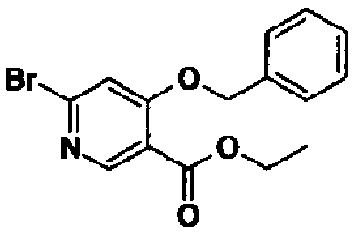
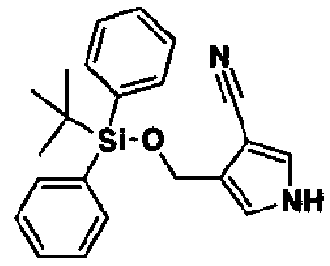
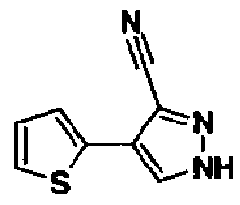
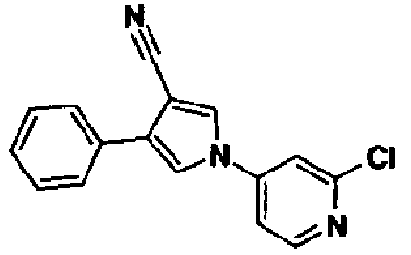
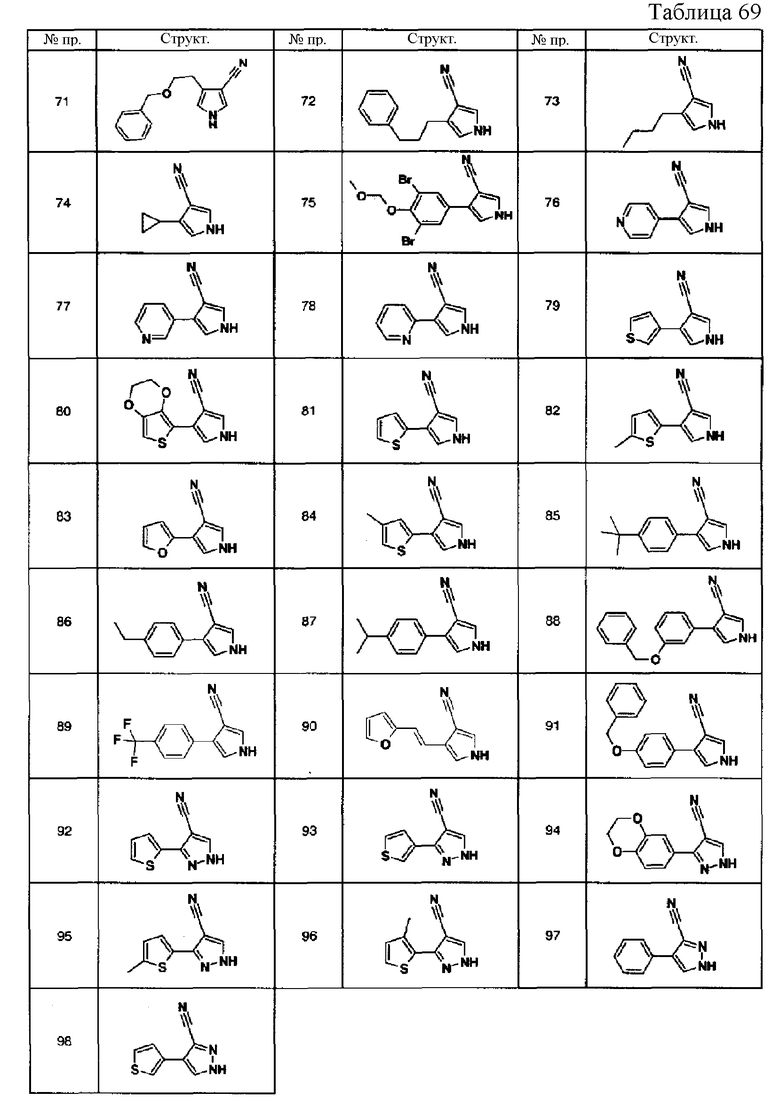
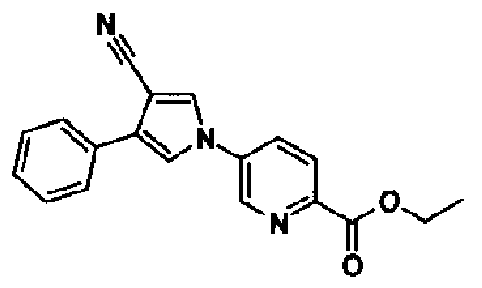
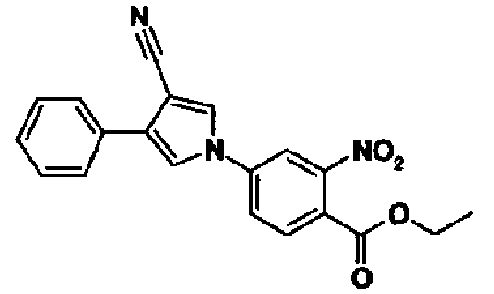
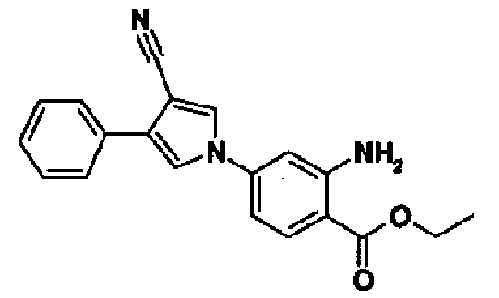
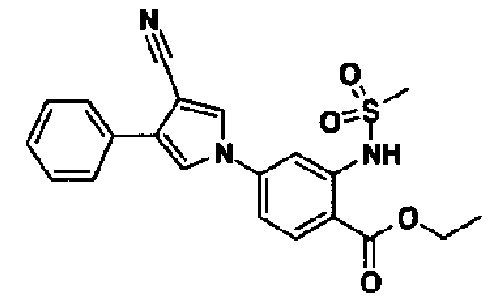
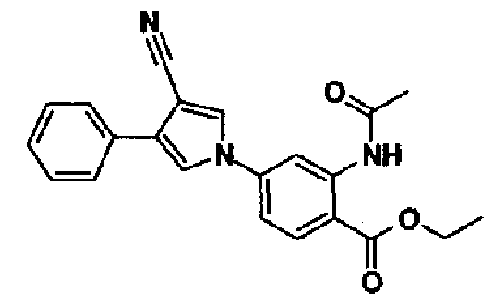

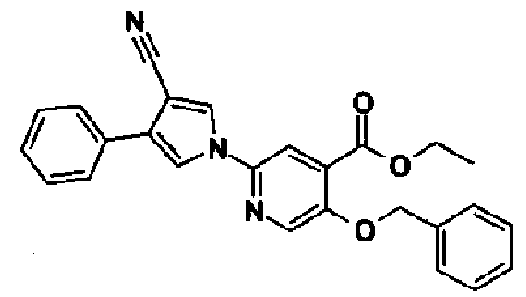
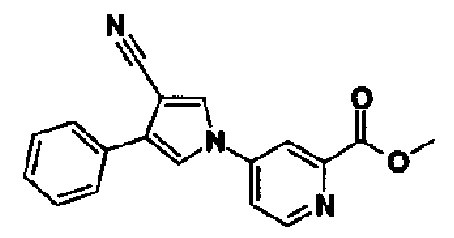
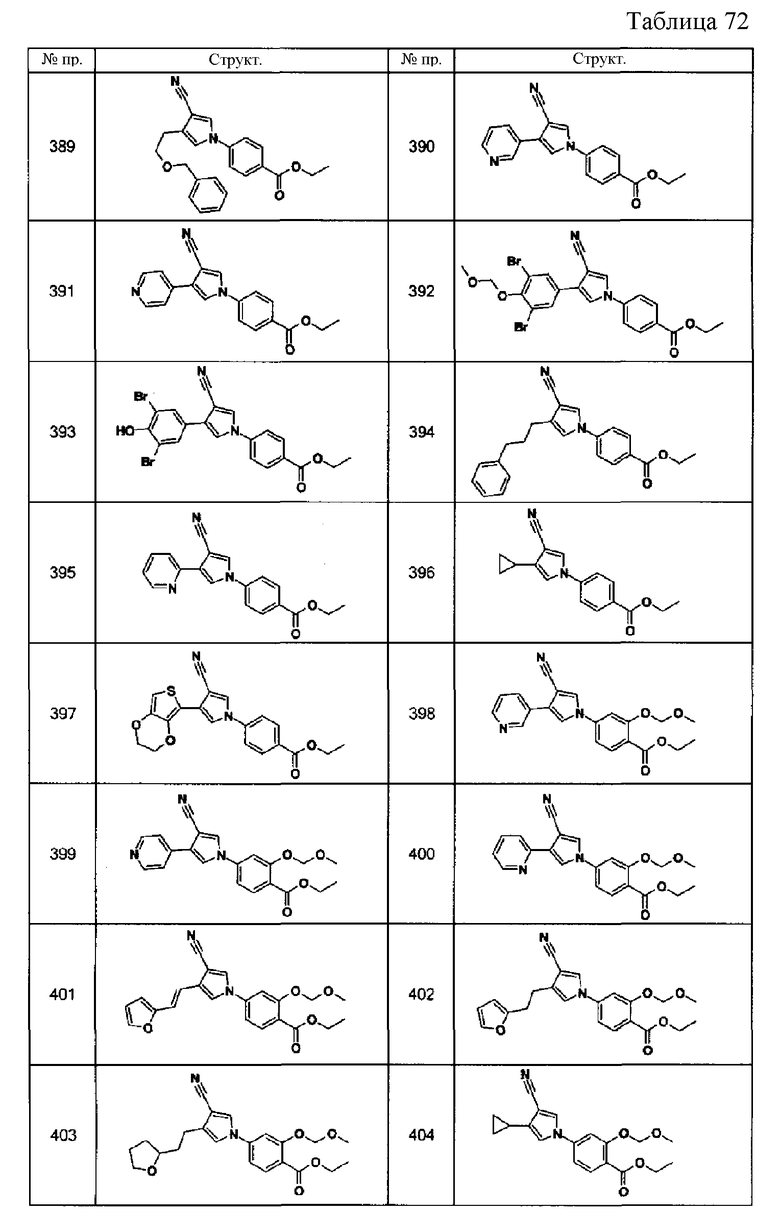
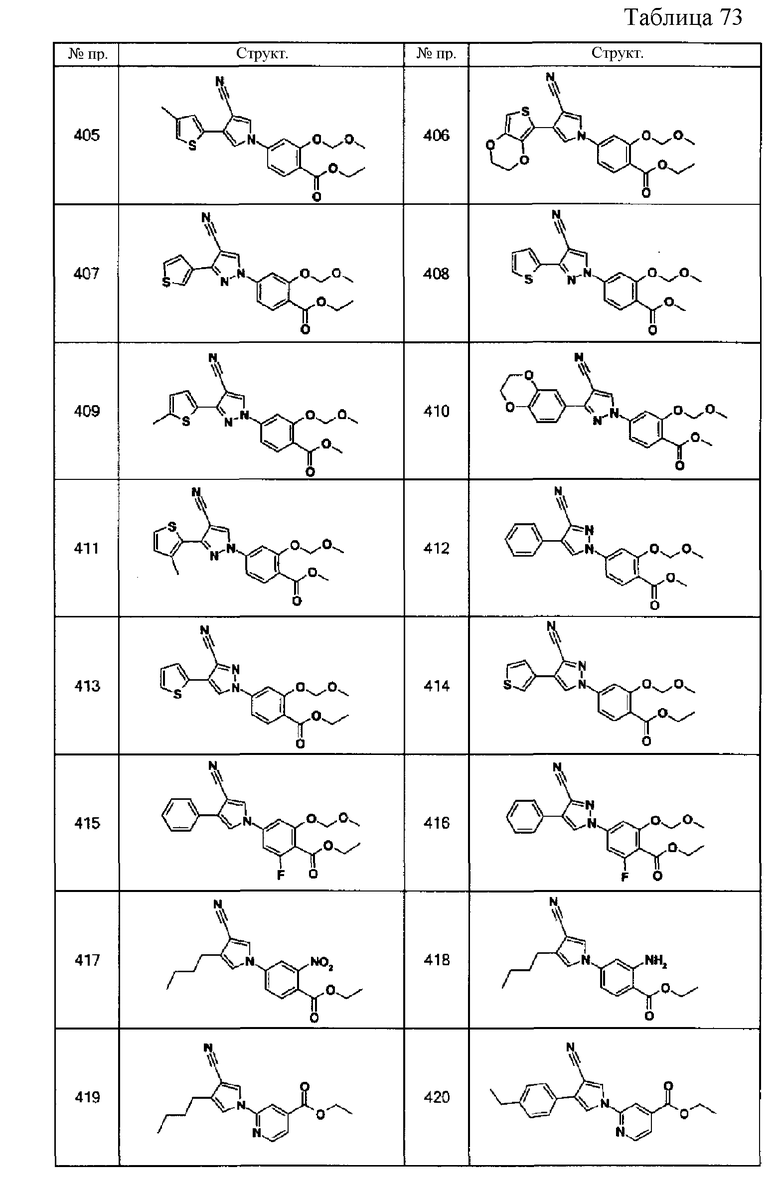
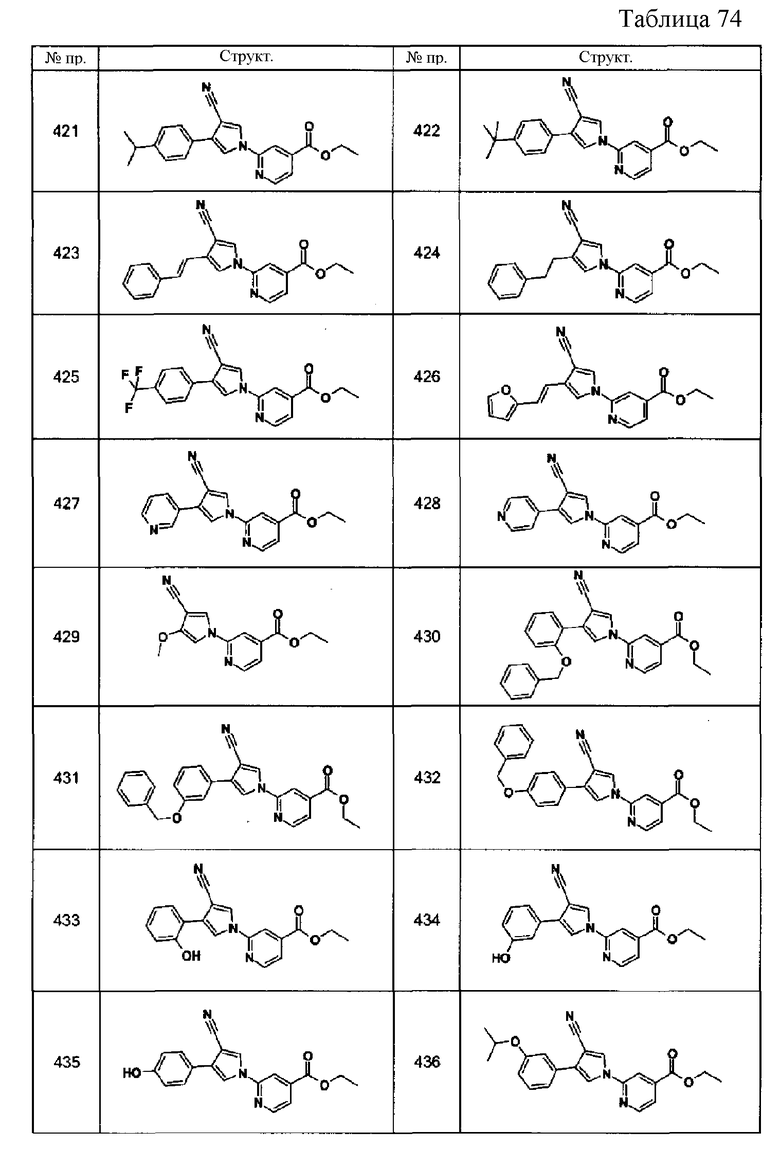
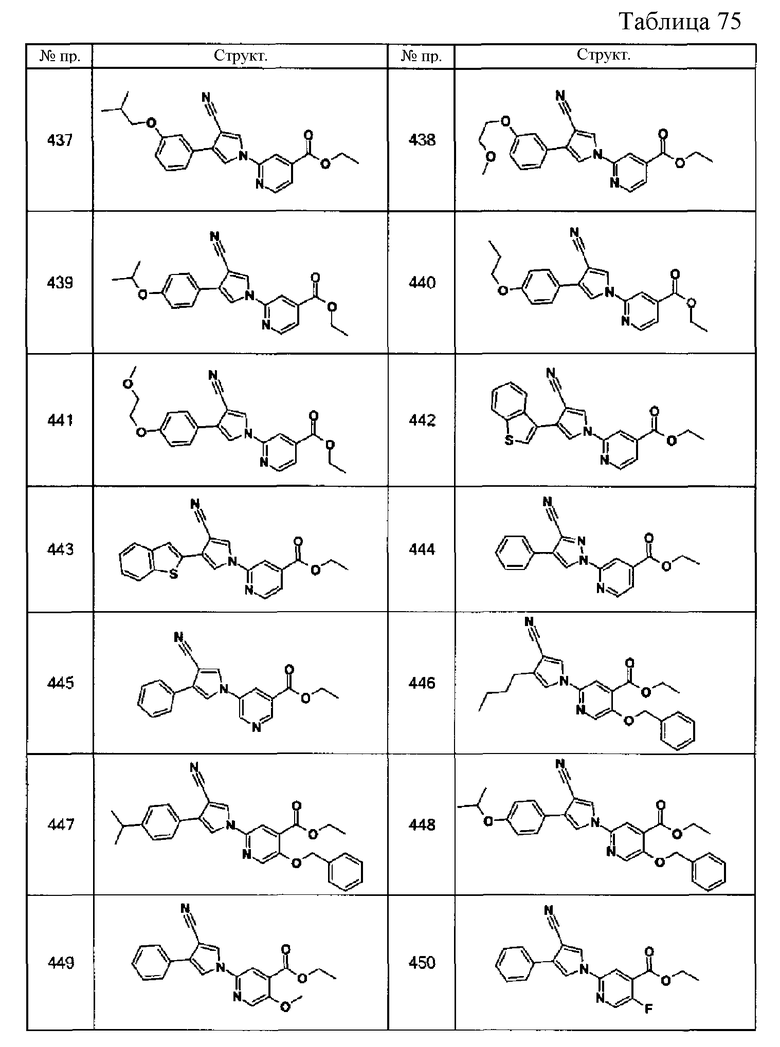
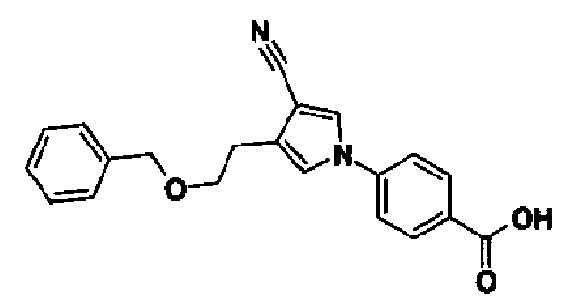
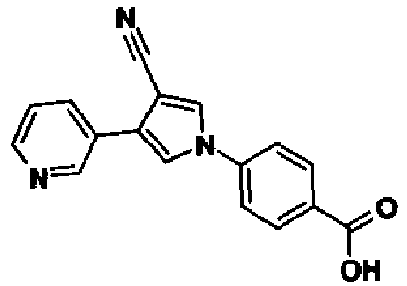
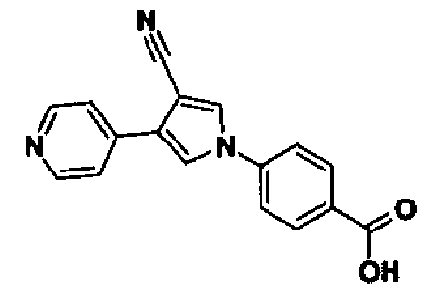
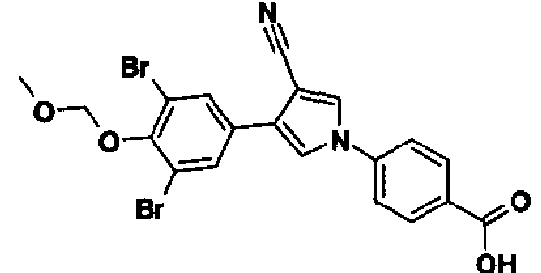
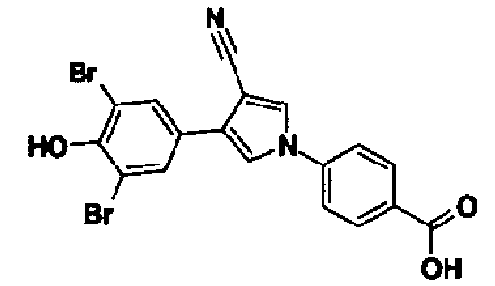
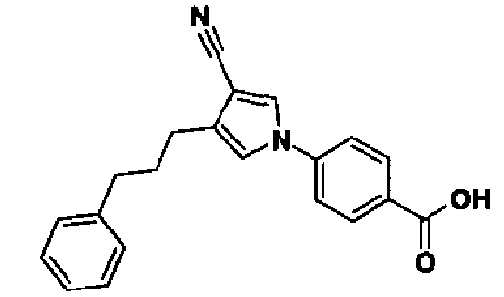
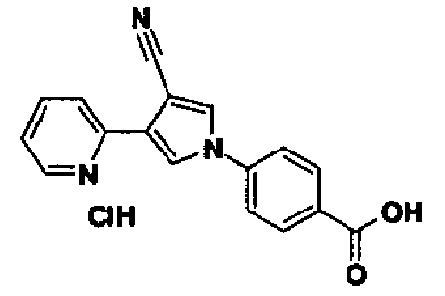
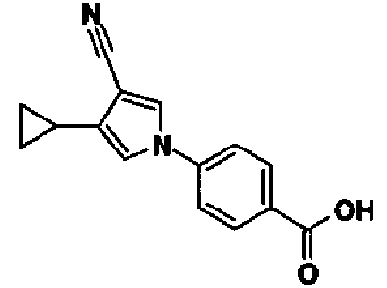
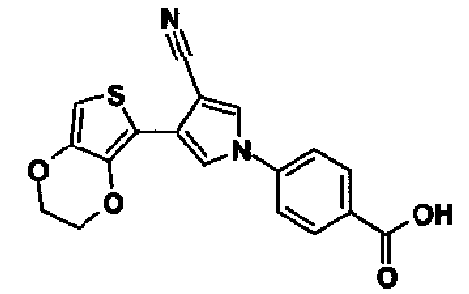
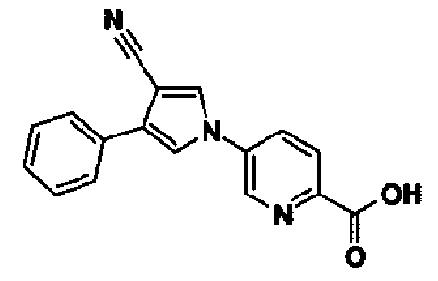
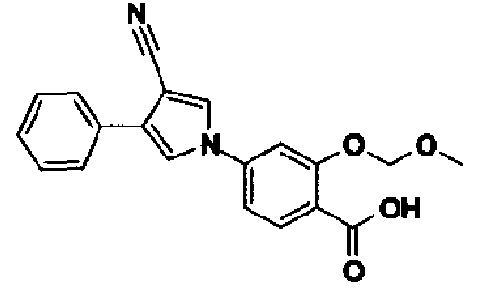
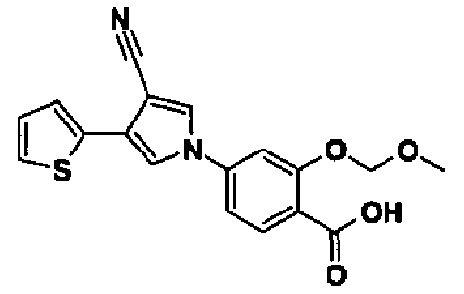
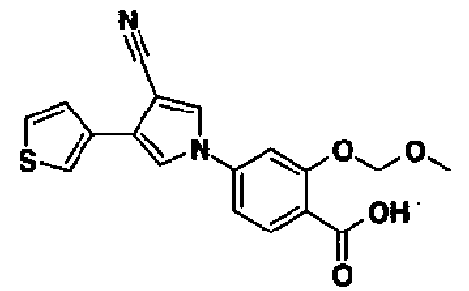
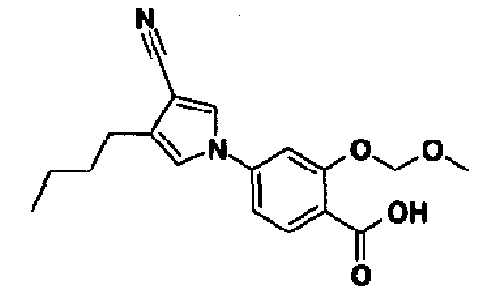
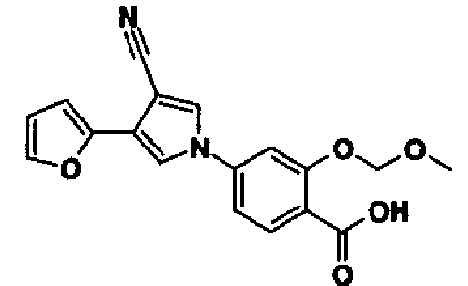
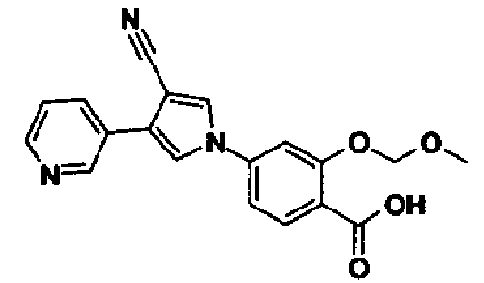
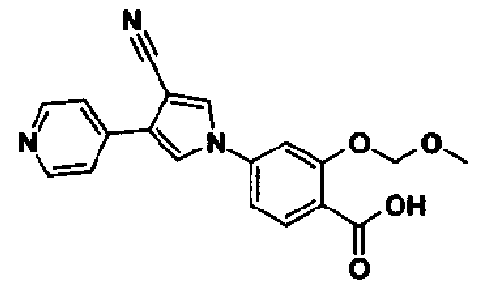
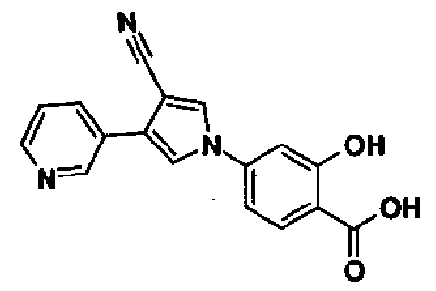
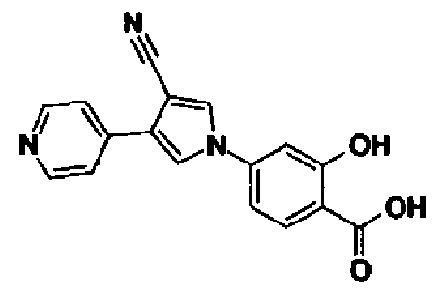
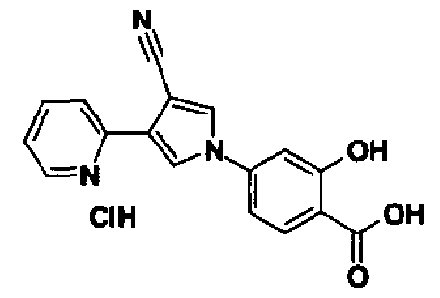
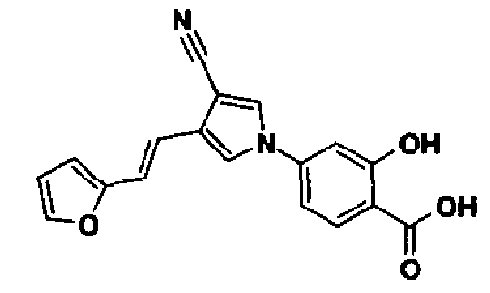
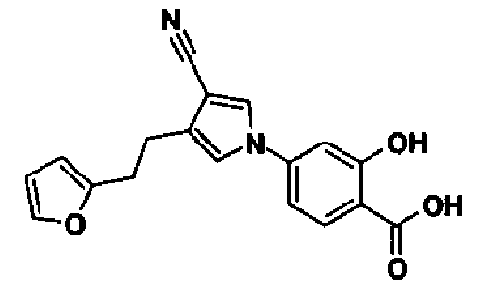
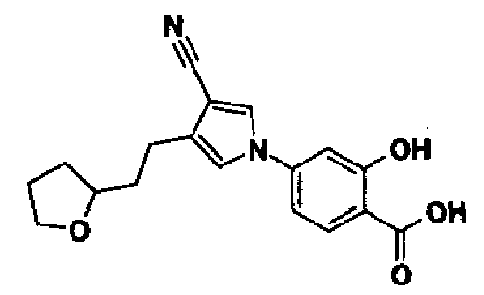
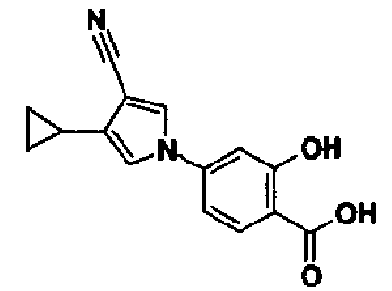
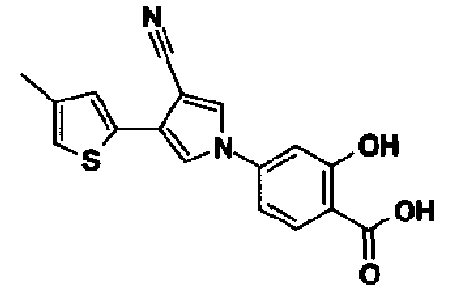
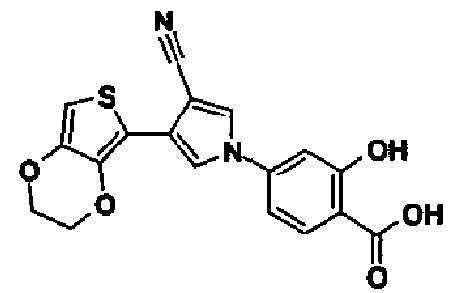
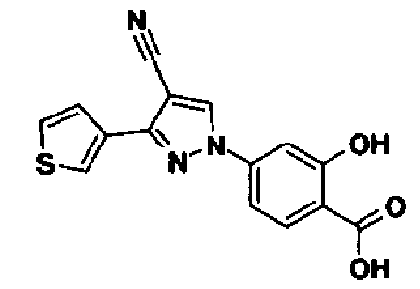
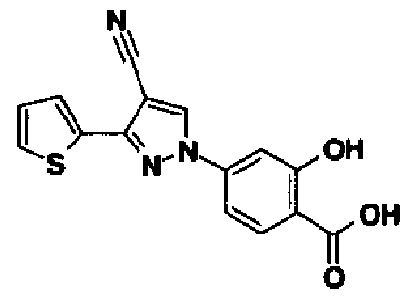
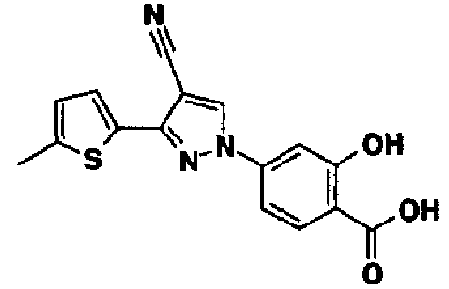
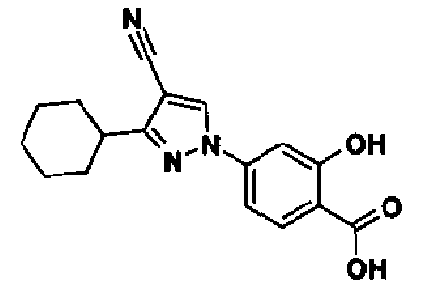
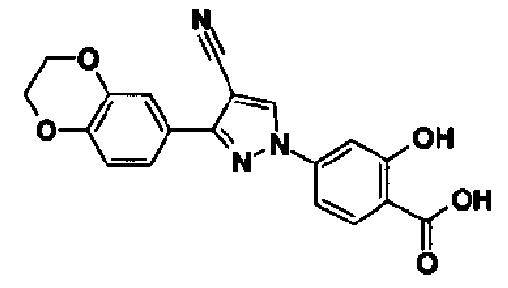
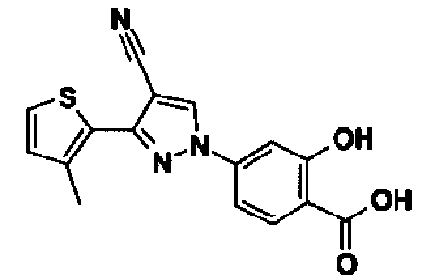
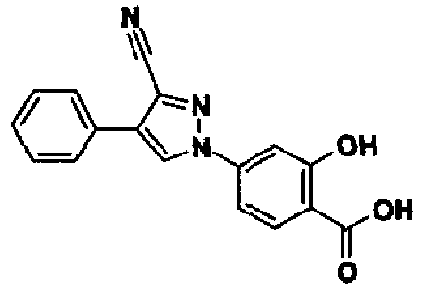

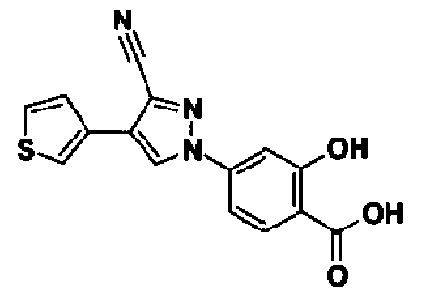
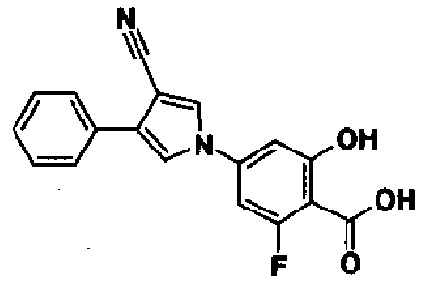
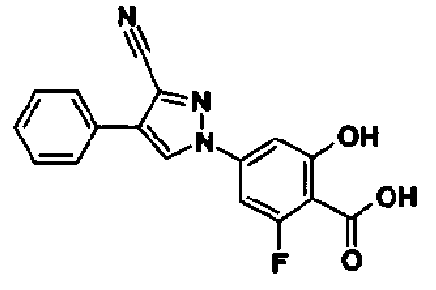
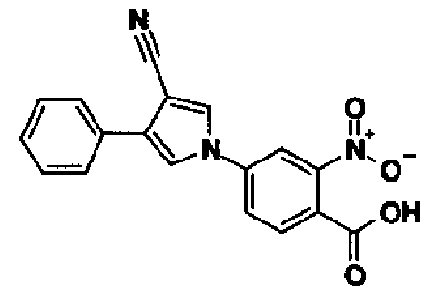
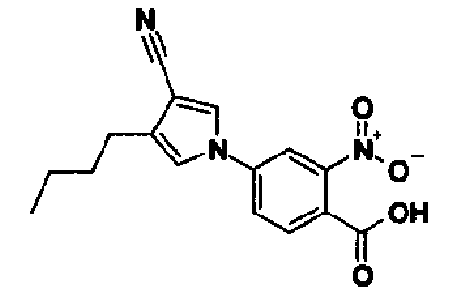
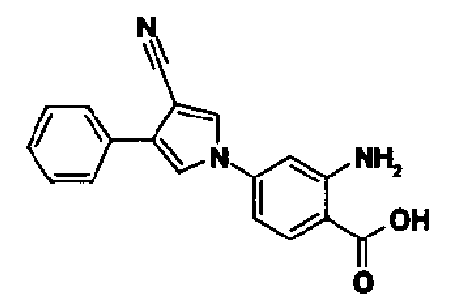
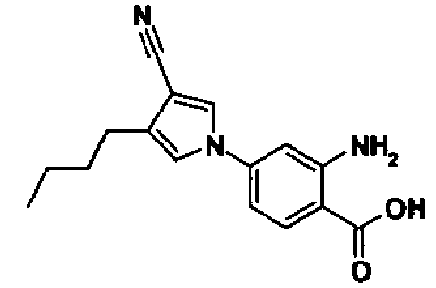
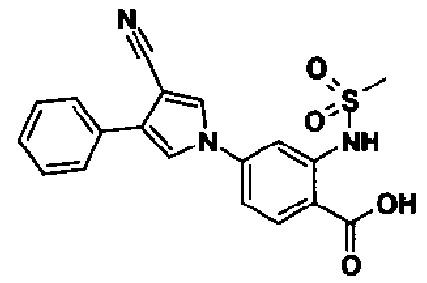
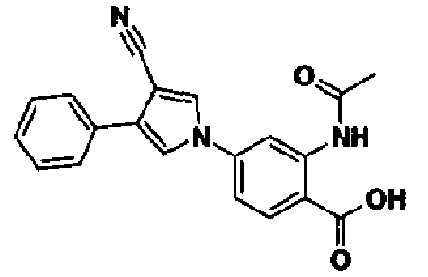
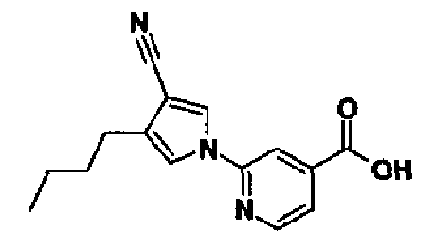
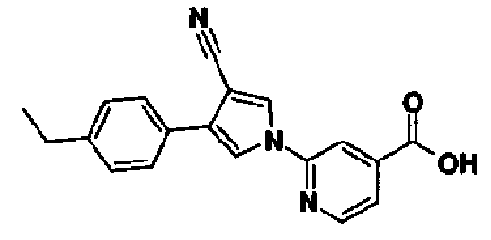
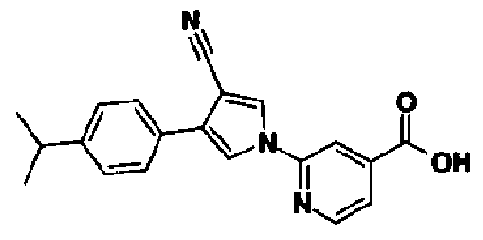
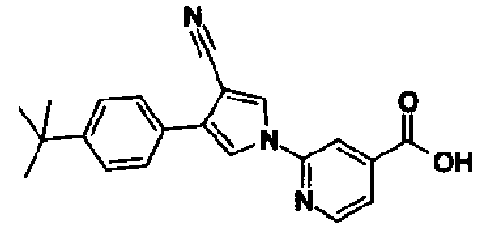
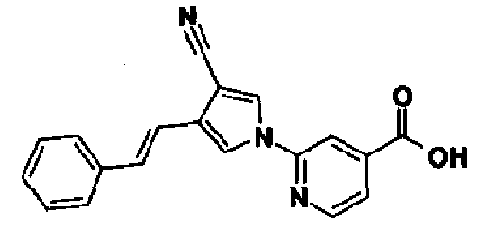
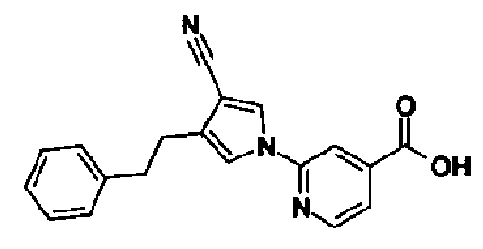
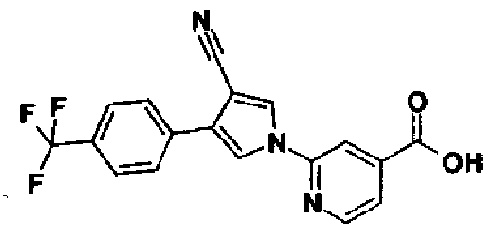
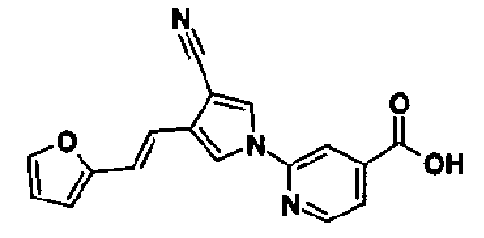
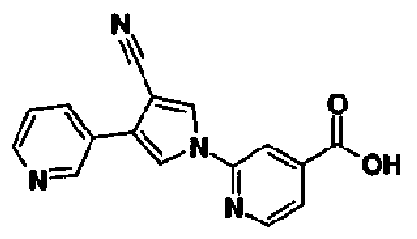
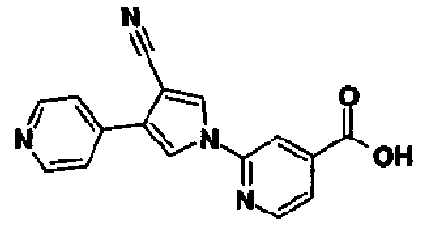
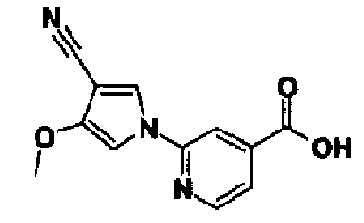
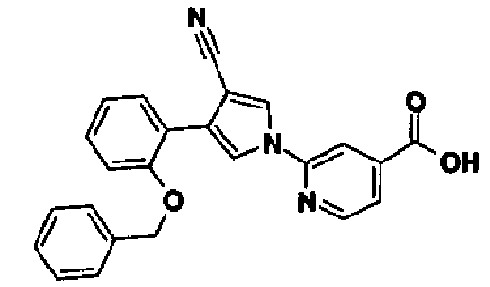
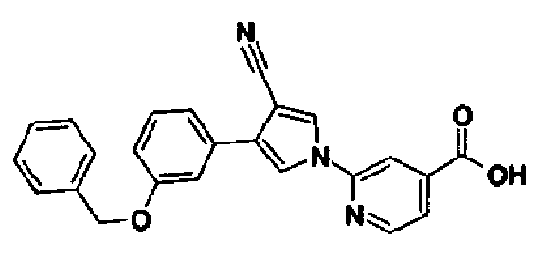
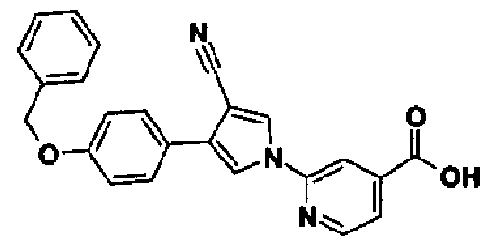
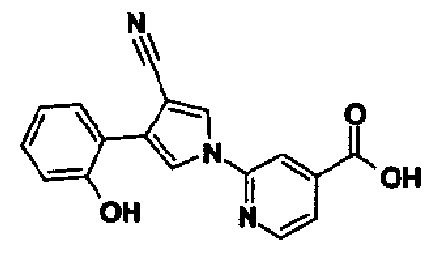
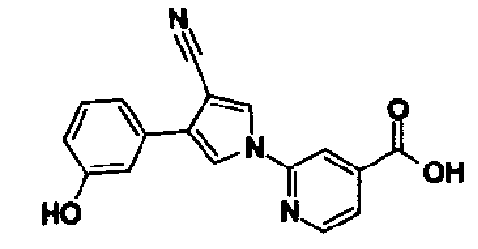
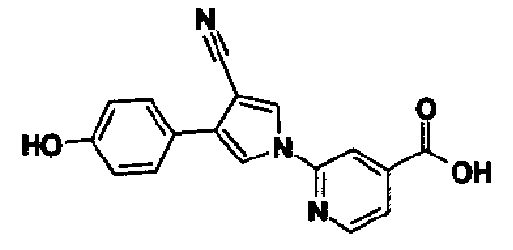
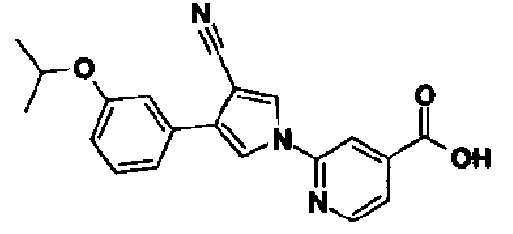
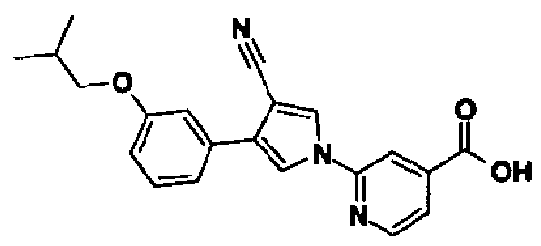
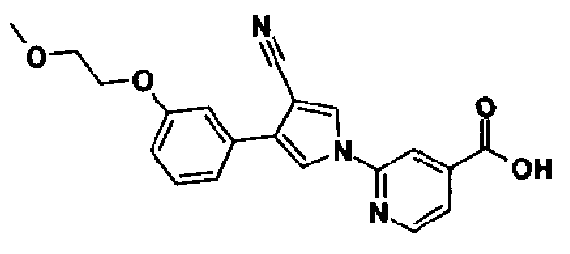
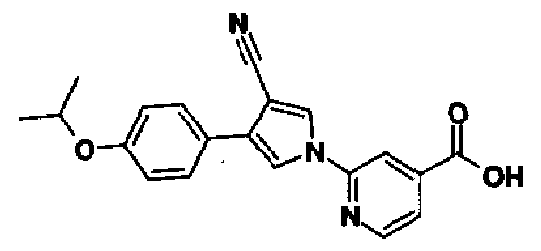
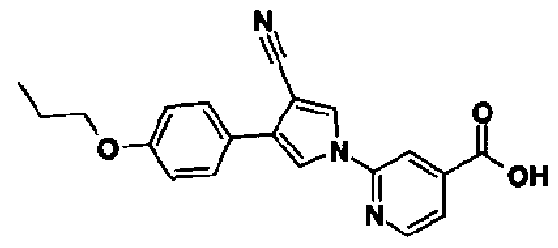
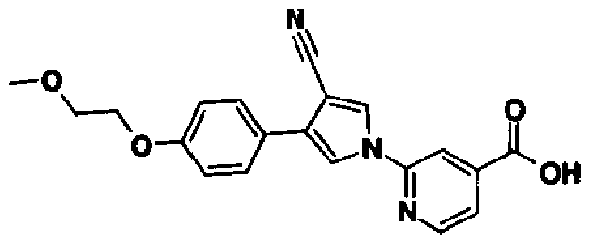
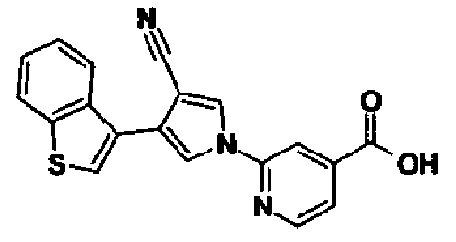
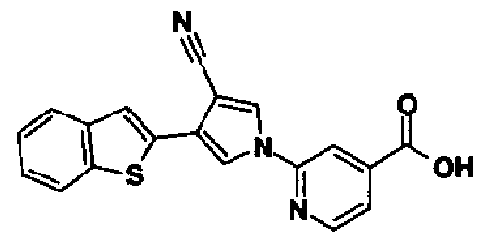
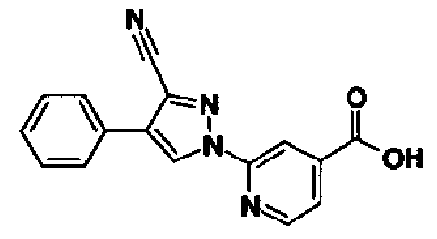
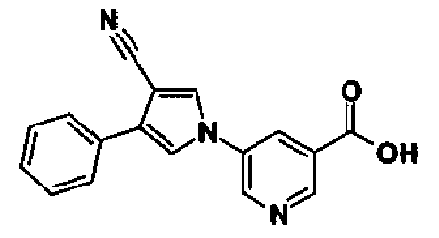
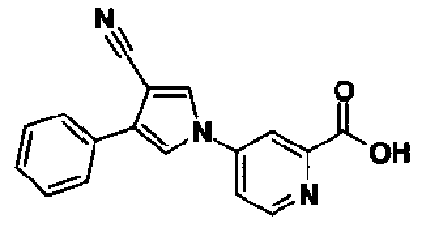
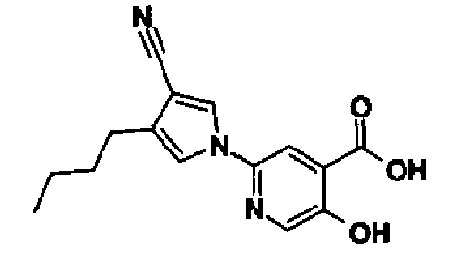
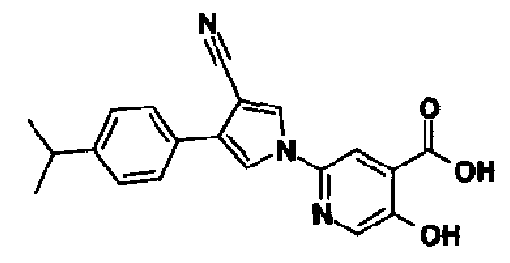
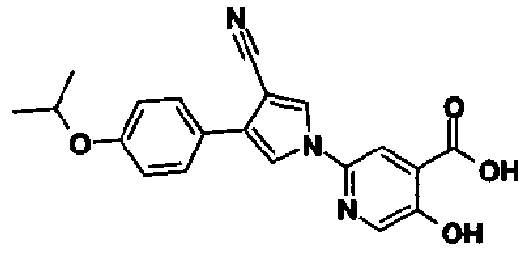
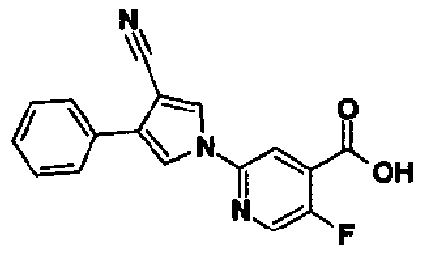
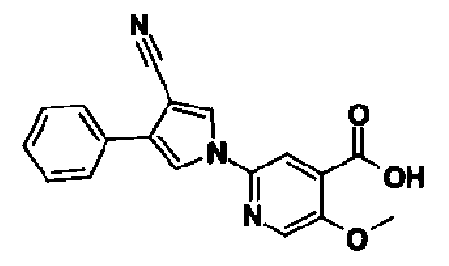
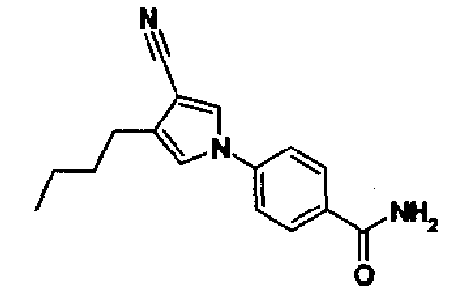
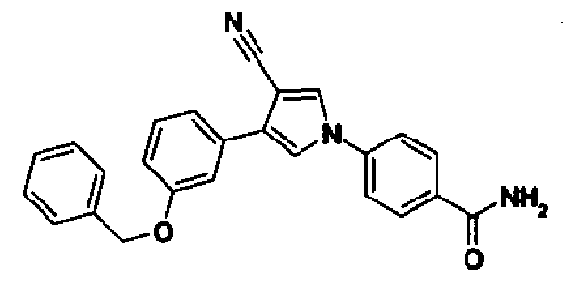
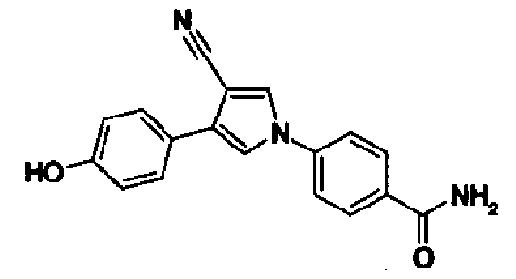
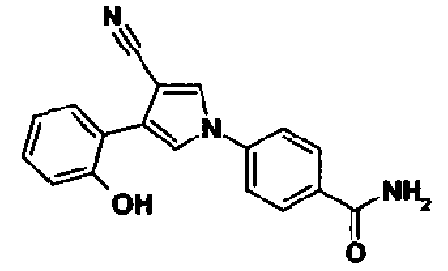
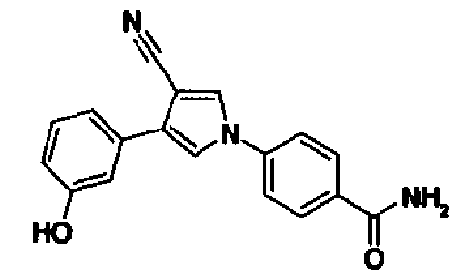
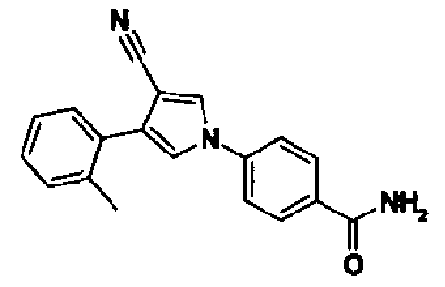
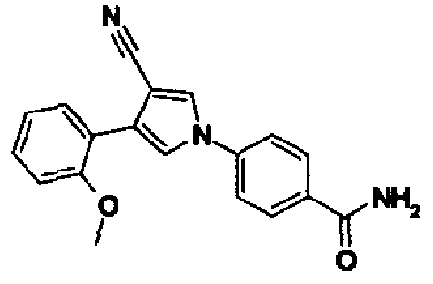
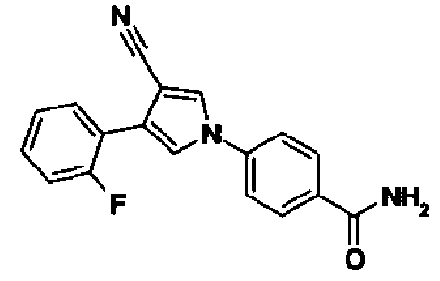
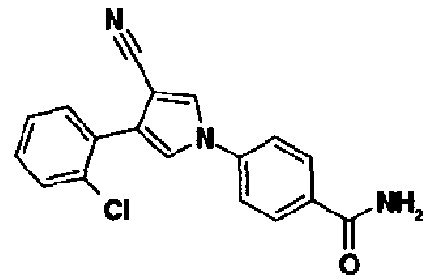
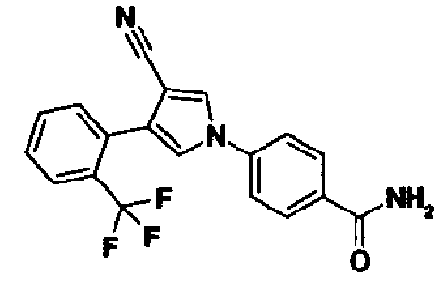
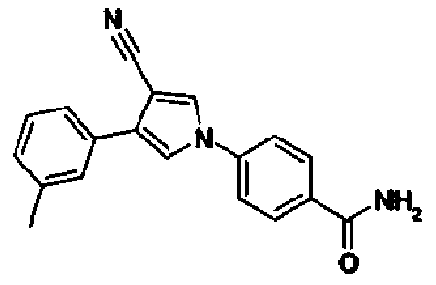
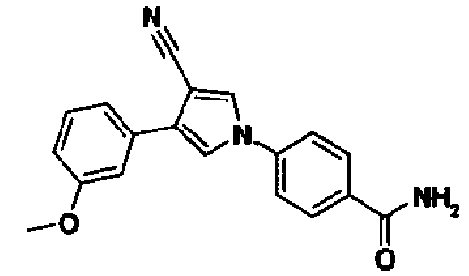
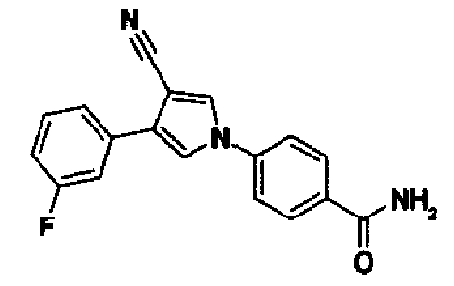
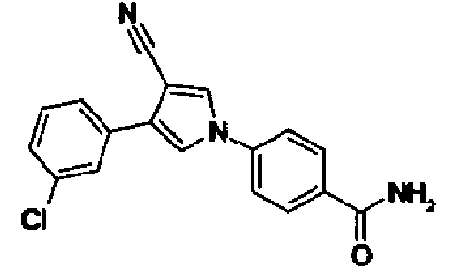
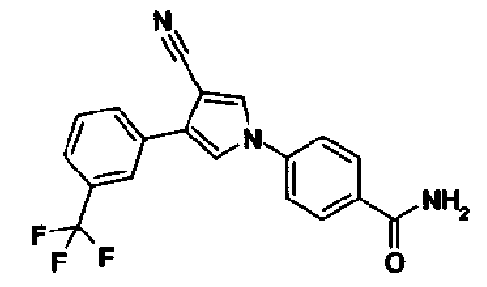
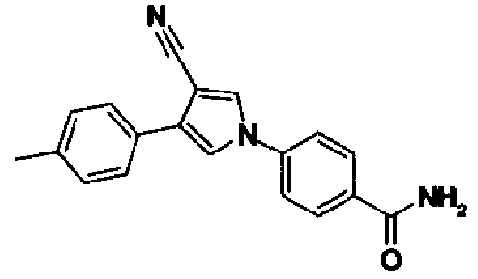
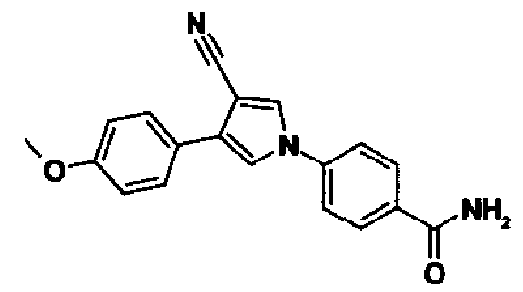
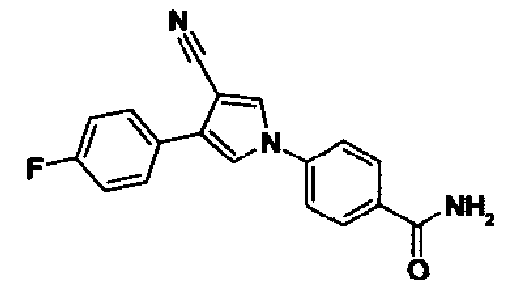
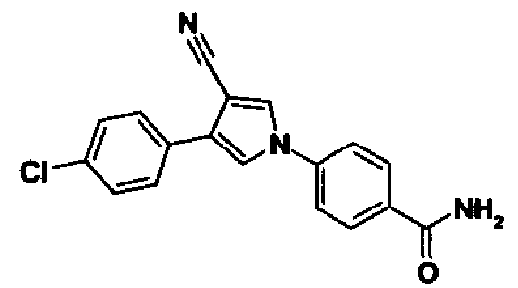
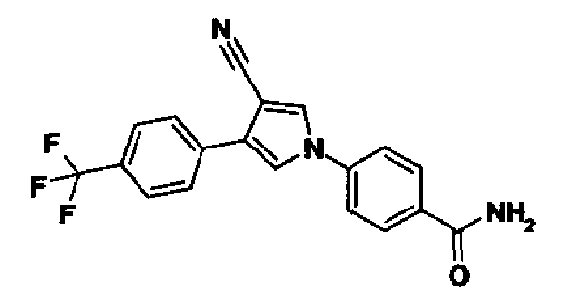
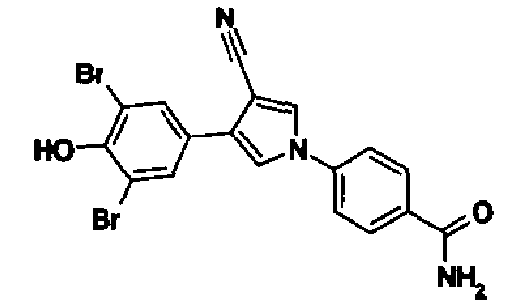
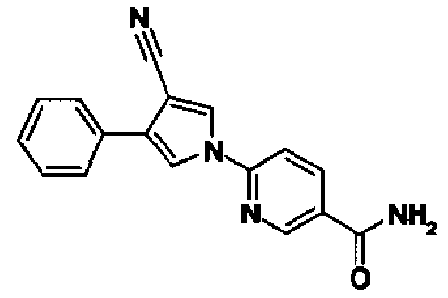
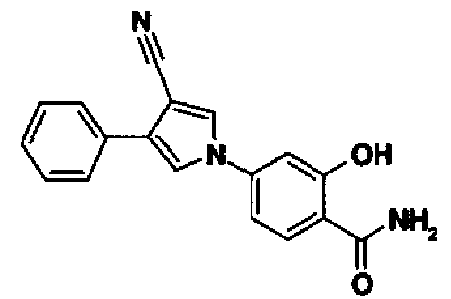
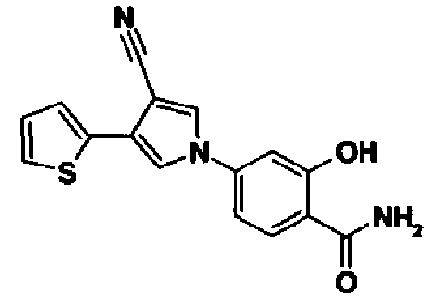
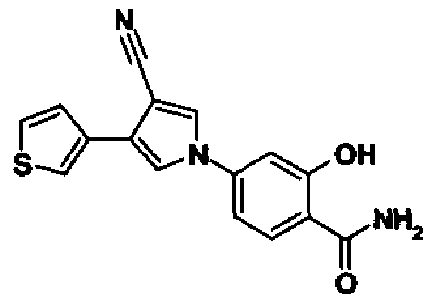
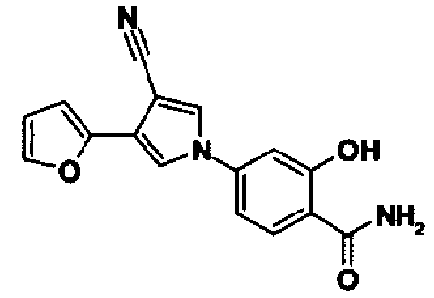
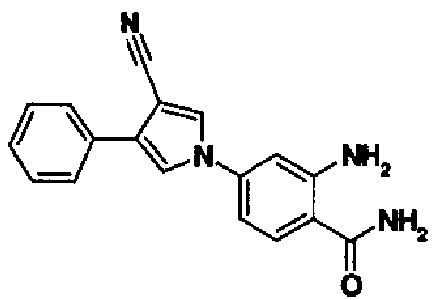
Пример испытания 1
Ингибирующая ксантиноксидазу активность
(1) Получение испытуемых соединений
Испытуемые соединения растворяли в ДМСО (Wako) при концентрации 40 мМ и затем разводили до заданных концентраций забуференным фосфатом физиологическим раствором (PBS).
(2) Способ измерения
Ксантиноксидазу (из коровьего молока, Sigma) получали растворением в забуференном фосфатом физиологическом растворе (PBS) при концентрации 0,02 единиц/мл и затем раствор добавляли в 96-луночные планшеты в количестве 50 мкл/лунку. Кроме того, добавляли испытуемые соединения, разведенные с PBS, в количестве 50 мкл/лунку. Раствор ксантина (Wako) при концентрации 200 мкМ, полученный с PBS, добавляли в количестве 100 мкл/лунку, и реакцию проводили в течение 10 минут при комнатной температуре. Поглощение при 290 нм измеряли с применением микропланшет-ридера SpectraMax Plus 384 (Molecular device). Поглощение в условиях без ксантина было 0% и в контроле без испытуемого соединения было 100%. Вычисляли ингибирующую 50% активности фермента концентрацию испытуемого соединения (IC50) (таблицы 91-92). № пр. в таблице означает номер примера.
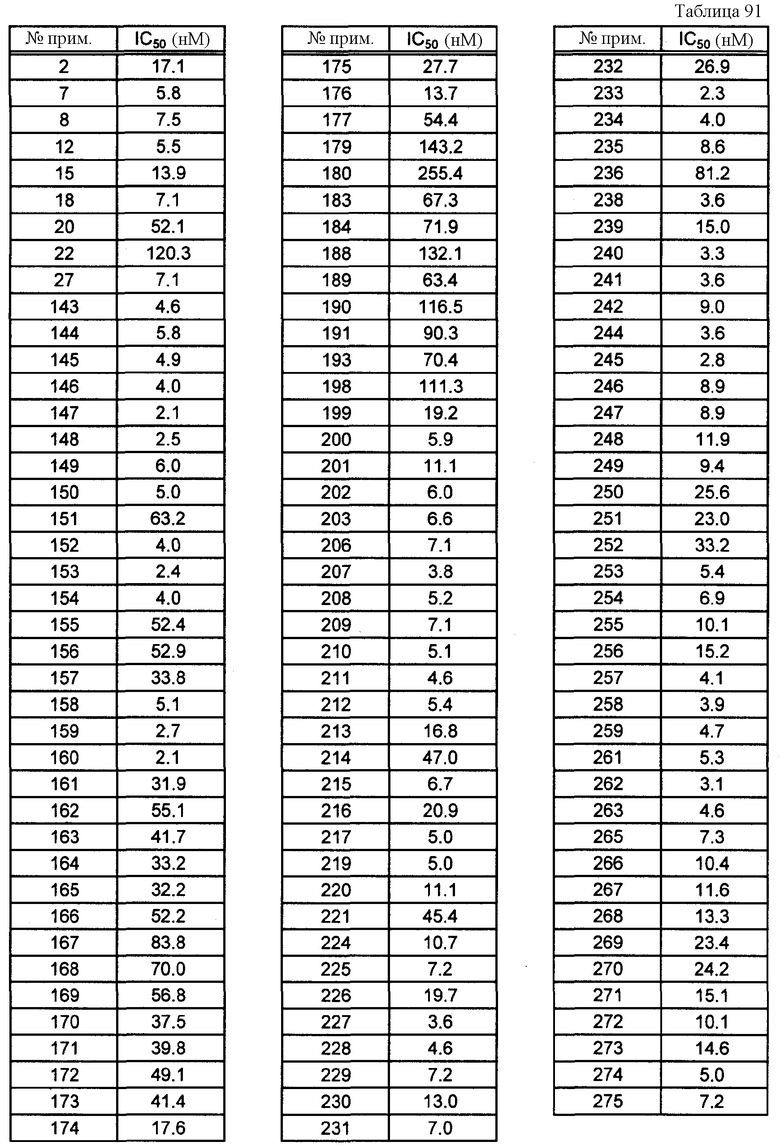
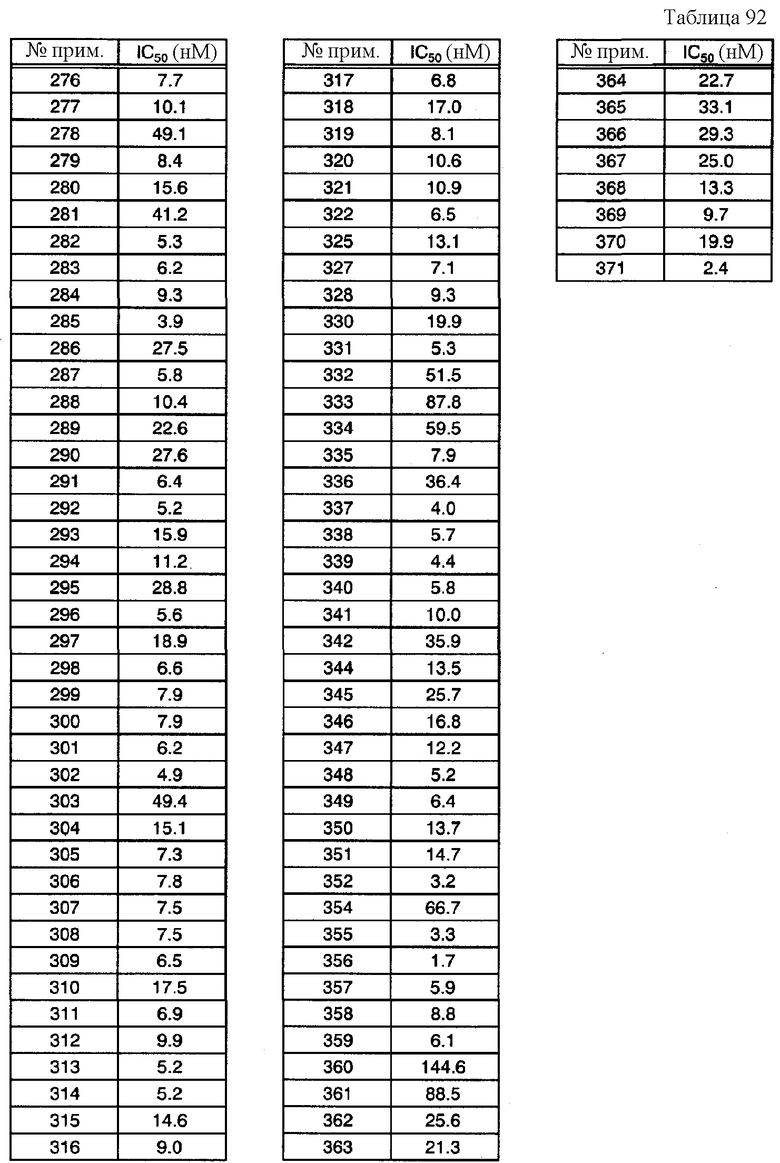
Пример испытания 2
Ингибирующая активность переноса мочевой кислоты везикулами мембран каемчатого эпителия (BBMV)
Определение ингибирующей активности переноса мочевой кислоты испытуемых соединений проводили на основе способов, описанных в ссылке (Am. J. Physiol. 266 (Renal Fluid Electrolyte Physiol. 35): F797-F805, 1994), с частичной модификацией.
(1) Получение BBMV из коркового вещества почки человека
BBMV из коркового вещества почки человека были куплены у КАС. Корковое вещество отсекали от почки человека и разрезали на маленькие кусочки. Затем корковое вещество гомогенизировали в 5 объемах охлажденного льдом изотонического буфера (300 мМ маннит, 5 мМ этиленгликоль-бис-(β-аминоэтиловый простой эфир)-N,N,N′,N′-тетрауксусная кислота (EGTA), 12 мМ соль (трис)•HCl трис(гидроксиметил)аминометана, рН 7,4). После добавления 1 М хлорида магния до конечной концентрации 12 мМ суспензию затем перемешивали и выдерживали на льду в течение 15 минут. Гомогенизированный раствор центрифугировали при 2500×g в течение 15 минут при 4°С, затем супернатант центрифугировали при 30000×g в течение 30 минут при 4°С. Гранулы снова суспендировали в охлажденном льдом буфере 1 (150 мМ маннит, 2,5 мМ EGTA, 6 мМ трис-HCl, рН 7,4). После добавления 1 М хлорида магния до конечной концентрации 12 мМ суспензию затем смешивали и выдерживали на льду в течение 15 минут. После центрифугирования снова при 2500×g в течение 15 минут при 4°С супернатант затем центрифугировали при 30000×g в течение 30 минут при 4°С. Гранулы снова суспендировали в охлажденном льдом буфере 2 (100 мМ маннит, 100 мМ глюконат калия, 20 мМ 2-[4-(2-гидроксиэтил)-1-пиперазинил]этансульфоновая кислота (Hepes)-Tris, рН 7,4). После центрифугирования при 30000×g в течение 30 минут при 4°С гранулы снова суспендировали в буфере 2 и затем определяли концентрацию белка.
(2) Получение испытуемых соединений
Испытуемые соединения растворяли в ДМСО (Wako) при концентрации 40 мМ и затем раствор разводили до концентрации, которая в 2 раза выше концентрации, чем предполагается, Cl--градиентным буфером (100 мМ маннит, 100 мМ глюконат калия, 20 мМ Hepes-Tris, рН 7,4). Cl--градиентный буфер без испытуемых соединений применяли для контроля. Кроме того, равный объем Cl--градиентного буфера, содержащего 14С-меченую мочевую кислоту (Moravek) и пробенецид (Wako), добавляли к испытуемым соединениям и контролю и, наконец, получали буфер для анализа, включающий в себя 40 мкМ мочевую кислоту и 5 мкМ пробенецид. Для измерения поглощения 14С-меченой мочевой кислоты при помощи Cl-градиент-независимого способа получали буфер для анализа с Cl--равновесным буфером (100 мМ маннит, 60 мМ глюконат калия, 40 мМ хлорид калия, 20 мМ Hepes-Tris, рН 7,4) вместо Cl--градиентного буфера.
(3) Способ измерения
BBMV оттаивали на льду. После добавления 8 мл внутрипузырного буфера (100 мМ маннит, 60 мМ глюконат калия, 40 мМ хлорид калия, 20 мМ Hepes-Tris, рН 7,4) к 200 мкл полученных BBMV (концентрация белка: 16 мг/мл) BBMV суспендировали при помощи иглы 24-размера и позволяли суспензии достичь равновесия при комнатной температуре в течение 60 минут. После центрифугирования при 30000×g в течение 30 минут при 4°С гранулы снова суспендировали в 1,2 мл внутрипузырного буфера. Суспензию выдерживали на льду до начала измерения. Поглощение мочевой кислоты в BBMV измеряли методикой быстрого фильтрования. По требованию способа измерения BBMV (20 мкл/1 реакцию) нагревали в течение 20 минут при комнатной температуре. Поглощение мочевой кислоты инициировали смешиванием с 100 мкл буфера для анализа. После инкубации в течение 20 секунд при комнатной температуре добавляли 3 мл охлажденного льдом раствора для остановки реакции (300 мМ маннит, 60 мМ сульфат натрия, 100 мкМ пробенецид (Wako), 5 мМ Трис-H2SO4, рН 7,4) и затем растворы быстро фильтровали через нитроцеллюлозные фильтры (размер пор 0,65 мкм, Sartorius) при отсасывании. Затем фильтры промывали дважды 3 мл раствора для остановки реакции и продукт растворяли в 10 мл Filter-Count (PerkinElmer) и радиоактивность определяли количественно в сцинтилляционном счетчике (PerkinElmer). Радиоактивность, связанную с фильтрами, в отсутствие BBMV применяли в качестве поправки. Кроме того, процентное ингибирование испытуемыми соединениями при 100 мкМ вычисляли согласно формуле, описанной ниже (таблица 93). № пр., Конц. и % ингибирования в таблице означают номер примера, концентрацию испытуемого соединения (мкМ) и процентное ингибирование (%), соответственно.
Процентное ингибирование (%) = [1-(B-C)/(A-C)] × 100.
А: радиоактивность контроля.
В: радиоактивность в случае добавления испытуемых соединений.
С: радиоактивность в Cl--равновесном буфере.
Пример испытания 3
Ингибирующая активность в отношении переноса мочевой кислоты клетками, экспрессирующими УРАТ1 человека
(1) Получение клеток, транзиторно экспрессирующих УРАТ1 человека
Полноразмерную кДНК УРАТ1 (NCBI Accession No. NM_144585) субклонировали в вектор экспрессии, pcDNA3.1 (Invitrogen). Вектор экспрессии УРАТ1 человека трансфицировали в клетки COS7 (RIKEN CELL BANK RCB0539) с применением липофектамина 2000 (Invitrogen). Клетки COS7 культивировали в покрытых коллагеном 24-луночных планшетах (Asahi Techno Glass) при 2×105/лунку в культуральной среде D-MEM (Introgen), содержащей 10% фетальной бычьей сыворотки (Sanko Junyaku), в течение 2 часов при 37°С в условиях 5% СО2. Для 1 лунки 2 мкл липофектамина 2000 разводили в 50 мкл OPTI-MEM (Invitrogen) и выдерживали при комнатной температуре в течение 7 минут (далее называли Lipo2000-OPTI). Для одной лунки 0,8 мкг вектора экспрессии УРАТ1 человека разводили в 50 мкл OPTI-MEM (Invitrogen) и осторожно смешивали с Lipo2000-OPTI. После выдерживания при комнатной температуре в течение 25 минут смесь добавляли к клеткам COS7 при 100 мкл/лунку. После этого клетки COS7 культивировали в течение 2 дней при 37°С в условиях 5% СО2 и применяли для измерения ингибирующей активности при поглощении.
(2) Получение испытуемых соединений
Испытуемые соединения растворяли в ДМСО (Wako) при концентрации 10 мМ и затем разводили до концентрации, которая в 2 раза выше концентрации, чем предполагается, буфером для предварительной обработки (125 мМ глюконат натрия, 4,8 мМ глюконат калия, 1,2 мМ дигидрофосфат калия, 1,2 мМ сульфат магния, 1,3 мМ глюконат кальция, 5,6 мМ глюкоза, 25 мМ Hepes, рН 7,4). Буфер для предварительной обработки без испытуемых соединений применяли для контроля. Кроме того, равный объем буфера для предварительной обработки, содержащего 14С-меченую мочевую кислоту (Moravek), добавляли к испытуемым соединениям и контролю и, наконец, получали буфер для анализа, включающий в себя 20 мкМ мочевую кислоту.
(3) Способ измерения
Все испытания проводили на нагретом планшете при 37°С. Буфер для предварительной обработки и буфер для анализа инкубировали при 37°С затем применяли для анализов. Из планшетов удаляли среду и добавляли 700 мкл буфера для предварительной обработки и клетки предварительно инкубировали в течение 10 минут. После повторения той же самой стадии буфер для предварительной обработки удаляли и добавляли буфер для анализа в количестве 400 мкл/лунку. Реакцию поглощения проводили в течение 5 минут. После окончания реакции буфер для анализа быстро удаляли и клетки промывали дважды с добавлением охлажденным льдом буфером для предварительной обработки в количестве 1,2 мл/лунку. Затем клетки лизировали добавлением 0,2 н гидроксида натрия в количестве 300 мкл/лунку. Лизированные растворы переносили в Picoplate (PerkinElmer) и добавляли Microscinti 40 (PerkinElmer) в количестве 600 мкл/лунку. После смешивания радиоактивность подсчитывали в сцинтилляционном счетчике (PerkinElmer). Радиоактивность в клетках COS7, нетрансфицированных вектором экспрессии УРАТ1, также определяли количественно в тех же условиях в качестве контроля. Кроме того, процентное ингибирование испытуемыми соединениями при 100 мкМ вычисляли согласно описанной ниже формуле (таблица 94). № пр., Конц. и % ингибирования в таблице означают номер примера, концентрацию испытуемого соединения (мкМ) и процентное ингибирование (%), соответственно.
Процентное ингибирование (%) = [1-(B-C)/(A-C)] × 100.
А: радиоактивность в контроле.
В: радиоактивность в случае добавления испытуемых соединений.
С: радиоактивность в клетках COS7, нетрансфицированных вектором экспрессии УРАТ1.
Пример испытания 4
Гипоуремическое действие на сыворотку
(1) Способ измерения
Испытуемые соединения в количестве 1 мг/кг, суспендированные в 0,5% растворе метилцеллюлозы вводили перорально голодавшим в течение ночи самцам крыс CD (SD) IGS (возраст 5 недель, Charls River Japan). Спустя 2 часа после введения кровь собирали при анестезии эфиром из абдоминальной аорты и сыворотку выделяли согласно общему способу. Величины содержания мочевой кислоту в сыворотке определяли применением набора для измерения мочевой кислоты (Uric acid C-Test Wako: Wako) и процентное уменьшение содержания мочевой кислоты вычисляли согласно описанной ниже формулы.
Процентное снижение содержания мочевой кислоты (%) = (величины содержания мочевой кислоты в сыворотке контрольных животных - величины мочевой кислоты в сыворотке у животных, которым вводили испытуемые соединения) × 100/величины мочевой кислоты в сыворотке у контрольных животных.
(2) Результаты
Соединения примеров 301 и 314 имеют более чем 50% гипоуремическое действие спустя 2 часа после перорального введения. В результате описанного выше подтверждается, что соединения настоящего изобретения обладают сильным действием по снижению содержания мочевой кислоты в сыворотке.
Промышленная применимость
5-членные гетероциклические соединения, представленные вышеуказанной общей формулой (I) настоящего изобретения, или их пролекарства или фармацевтически приемлемые соли проявляют превосходную ингибирующую ксантиноксидазу активностью и поэтому могут проявлять ингибирующую активность в отношении продуцирования мочевой кислоты и снижать уровень мочевой кислоты в крови. Поэтому в настоящем изобретении может быть предложен агент для профилактики или лечения гиперурикемии, подагрических узлов, подагрического артрита, почечного нарушения, связанного с гиперурикемией, мочевыми конкрементами или тому подобное.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВОЕ ПРОИЗВОДНОЕ КУМАРИНА, ОБЛАДАЮЩЕЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2007 |
|
RU2428420C2 |
| КОНДЕНСИРОВАННОЕ ГЕТЕРОЦИКЛИЧЕСКОЕ ПРОИЗВОДНОЕ, СОДЕРЖАЩАЯ ЕГО ЛЕЧЕБНАЯ КОМПОЗИЦИЯ И ЕЕ ПРИМЕНЕНИЕ В МЕДИЦИНЕ | 2006 |
|
RU2418803C2 |
| МОДУЛЯТОРЫ КАЛЬПАИНА И ИХ ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2017 |
|
RU2773288C2 |
| ГЕКСАЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ИХ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ПРОТИВООПУХОЛЕВЫХ СРЕДСТВ, СПОСОБ ПОЛУЧЕНИЯ ГЕКСАЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ | 2002 |
|
RU2299212C2 |
| ВОДОРАСТВОРИМЫЕ ПРОИЗВОДНЫЕ ФЕНИЛПИРИДАЗИНА И СОДЕРЖАЩИЕ ИХ ЛЕКАРСТВЕННЫЕ СРЕДСТВА | 2002 |
|
RU2302413C2 |
| ПРОИЗВОДНОЕ (АЗА)ИНДОЛА И ЕГО ПРИМЕНЕНИЕ В ЛЕЧЕБНЫХ ЦЕЛЯХ | 2008 |
|
RU2477274C2 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛА | 2004 |
|
RU2332412C2 |
| АКТИВАТОРЫ ГЛЮКОКИНАЗЫ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИХ В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА | 2008 |
|
RU2450001C2 |
| ПРОИЗВОДНЫЕ 3-ОКСО-1-ЦИКЛОБУТЕНА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2002 |
|
RU2296753C2 |
| ДИАМИНОТРИАЗОЛЫ, ПРИГОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗ | 2003 |
|
RU2350606C2 |
Изобретение относится к 5-членным гетероциклическим соединениям общей формулы (I), их пролекарствам или фармацевтически приемлемым солям, обладающим ингибирующей ксантиноксидазу активностью. В формуле (I) T представляет собой нитро, циано или трифторметил; J представляет собой кольцо фенила или гетероарила, где гетероарил представляет собой 6-членную ароматическую гетероциклическую группу, имеющую один гетероатом, выбранный из азота, или 5-членную ароматическую гетероциклическую группу, имеющую один гетероатом, выбранный из кислорода; Q представляет собой карбокси, низший алкоксикарбонил, карбамоил или 5-тетразолил; X1 и X2 независимо представляют собой CR2 или N, при условии, что оба из X1 и X2 одновременно не представляют собой N и, когда присутствуют два R2, эти R2 необязательно являются одинаковыми или отличными друг от друга; R2 представляет собой атом водорода или низший алкил; Y представляет собой атом водорода, гидрокси, амино, атом галогена, перфтор(низший алкил), низший алкил, низший алкокси, необязательно замещенный низшим алкокси; нитро, (низший алкил)карбониламино или (низший алкил)сульфониламино; R1 представляет собой перфтор(низший алкил), -AA, -A-D-L-M или -A-D-E-G-L-M (значения AA, A, D, E, G, L, M приведены в п.1 формулы изобретения). Изобретение относится также к ингибитору ксантиноксидазы и фармацевтической композиции, которые содержат соединение формулы (I). 3 н. и 24 з.п. ф-лы, 94 табл., 553 пр.

1. 5-членное гетероциклическое соединение, представленное общей формулой (I)
 ,
,
где
T представляет собой нитро, циано или трифторметил;
кольцо J представляет собой кольцо фенила или кольцо гетероарила, где указанный гетероарил представляет собой 6-членную ароматическую гетероциклическую группу, имеющую один гетероатом, выбранный из азота, или 5-членную ароматическую гетероциклическую группу, имеющую один гетероатом, выбранный из кислорода;
Q представляет собой карбокси, низший алкоксикарбонил, карбамоил или 5-тетразолил;
X1 и X2 независимо представляют собой CR2 или N, при условии, что оба из X1 и X2 одновременно не представляют собой N и, когда присутствуют два R2, эти R2 необязательно являются одинаковыми или отличными друг от друга;
R2 представляет собой атом водорода или низший алкил;
Y представляет собой атом водорода, гидрокси, амино, атом галогена, перфтор(низший алкил), низший алкил, низший алкокси, необязательно замещенный низшим алкокси; нитро, (низший алкил)карбониламино или (низший алкил)сульфониламино, при условии, что два или более Y необязательно присутствуют на кольце J, и эти Y необязательно являются одинаковыми или отличными друг от друга;
R1 представляет собой перфтор(низший алкил), -AA, -A-D-L-M или -A-D-E-G-L-M;
в формуле AA представляет собой карбокси или -CONHR3;
A представляет собой простую связь, -O-, -CO-, -COO-, -CON(R3)-, -N(R3)CO- или -N=CR3N(R4)-, где R3 и R4 независимо представляют собой атом водорода или низший алкил;
D представляет собой низший алкилен, низший алкенилен, C3-6циклоалкилен, гетероциклоалкилен, где указанный гетероциклоалкилен представляет собой двухвалентную группу, образованную из гетероциклоалкила, который представляет собой 6-членную алифатическую моноциклическую углеводородную группу, имеющую 1-2 гетероатома, выбранных из атомов кислорода и азота, арилен, где указанный арилен представляет собой двухвалентную группу, образованную из фенила или нафтила, необязательно замещенную атомом галогена, группой перфтор(низший алкил), циано или -OW8, где W8 представляет собой низший алкил или перфтор(низший алкил), при условии, что когда два -OW8 присутствуют у соседних атомов углерода в бензольном кольце, эти W8 могут связываться вместе с образованием метиленовой цепи, которая может быть замещена 1 или 2 атомами фтора, или этиленовой цепи, которая может быть замещена 1-4 атомами фтора, или гетероарилен, где указанный гетероарилен представляет собой двухвалентную группу, образованную из гетероарила, представляющего собой 5-членную ароматическую гетероциклическую группу, имеющую 1-2 гетероатома, которые выбраны из атомов кислорода, серы и азота, необязательно замещенную атомом галогена, и возможно конденсированную с 6-членным кольцом, или 6-членную ароматическую гетероциклическую группу, имеющую один гетероатом, выбранный из азота, при условии, что D необязательно дополнительно замещен -L-M;
E представляет собой простую связь, -O- или -COO-;
G представляет собой низший алкилен или фенилен;
L представляет собой простую связь, -O-, -S-, -COO- или -OCO-; и
M представляет собой атом водорода, низший алкил, гетероциклоалкил, где указанный гетероциклоалкил представляет собой 5-членную алифатическую моноциклическую углеводородную группу, имеющую один гетероатом, выбранный из кислорода, фенил, необязательно замещенный атомом галогена, низшим алкилом, группой перфтор(низший алкил) или низшим алкокси, или гетероарил, где указанный гетероарил представляет собой 5-членную ароматическую гетероциклическую группу, имеющую один гетероатом, выбранный из кислорода или серы, при условии, что, когда M представляет собой атом водорода, L представляет собой простую связь, -O-, -S-, -COO- или -OCO-, соответственно, за исключением 4-[4-циано-3-трифторметил-1H-пиразол-1-ил]бензойной кислоты;
или его пролекарство или его фармацевтически приемлемая соль,
где «низший» означает неразветвленную или разветвленную углеводородную группу, имеющую 6 или менее атомов углерода; и
«пролекарство» означает соединение, где одна или несколько групп, выбранных из гидроксигруппы и карбоксигруппы соединения, представленного вышеуказанной общей формулы (I), замещена группой, образующей пролекарство, где группой, образующей пролекарство, является (низший алкил)-CO- у гидроксигруппы, или низший алкил у карбоксигруппы.
2. 5-членное гетероциклическое соединение по п.1, где Y представляет собой атом водорода, гидрокси, амино, атом галогена, перфтор(низший алкил), низший алкил или низший алкокси, необязательно замещенный низшим алкокси, при условии, что на кольце J необязательно присутствуют два или более Y, и эти Y необязательно являются одинаковыми или отличными друг от друга, или его пролекарство или его фармацевтически приемлемая соль.
3. 5-членное гетероциклическое соединение по п.2, где
Q представляет собой карбокси, карбамоил или 5-тетразолил;
Y представляет собой атом водорода, гидрокси, амино, атом галогена или перфтор(низший алкил), при условии, что два или более Y необязательно присутствуют на кольце J, и эти Y необязательно являются одинаковыми или отличными друг от друга;
R1 представляет собой перфтор(низший алкил), -AA, -A-D-L-M или -A-D-E-G-L-M;
в формуле AA представляет собой -CONHR3;
A представляет собой простую связь, -O-, -CO-, -CON(R3)-, -N(R3)CO- или -N=CR3N(R4)-, где R3 и R4 независимо представляют собой атом водорода или низший алкил;
D представляет собой низший алкилен, низший алкенилен, C3-6циклоалкилен, гетероциклоалкилен, где указанный гетероциклоалкилен представляет собой двухвалентную группу, образованную из гетероциклоалкила, представляющего собой 6-членную алифатическую моноциклическую углеводородную группу, имеющую 1-2 гетероатома, выбранных из атомов кислорода и азота, арилен, где указанный арилен представляет собой двухвалентную группу, образованную из фенила или нафтила, необязательно замещенную атомом галогена, группой перфтор(низший алкил), циано или -OW8, где W8 представляет собой низший алкил или перфтор(низший алкил), при условии, что когда два -OW8 присутствуют у соседних атомов углерода в бензольном кольце, эти W8 могут связываться вместе с образованием метиленовой цепи, которая может быть замещена 1 или 2 атомами фтора, или этиленовой цепи, которая может быть замещена 1-4 атомами фтора, или гетероарилен, где указанный гетероарилен представляет собой двухвалентную группу, образованную из гетероарила, представляющего собой 5-членную ароматическую гетероциклическую группу, имеющую 1-2 гетероатома, которые выбраны из атомов кислорода, серы и азота, необязательно замещенную атомом галогена, и возможно конденсированную с 6-членным кольцом, или 6-членную ароматическую гетероциклическую группу, имеющую один гетероатом, выбранный из азота, при условии, что D необязательно дополнительно замещен -L-M;
E представляет собой простую связь, -O- или -COO-;
G представляет собой низший алкилен или фенилен;
L представляет собой простую связь, -O-, -S-, -COO- или -OCO-; и
M представляет собой атом водорода, низший алкил, гетероциклоалкил, где указанный гетероциклоалкил представляет собой 5-членную алифатическую моноциклическую углеводородную группу, имеющую один гетероатом, выбранный из кислорода, фенил, необязательно замещенный атомом галогена, низшим алкилом, группой перфтор(низший алкил) или низшим алкокси, или гетероарил, где указанный гетероарил представляет собой 5-членную ароматическую гетероциклическую группу, имеющую один гетероатом, выбранный из кислорода или серы, при условии, что когда M представляет собой атом водорода, L представляет собой простую связь, -O-, -S-, -COO- или -OCO-, соответственно, или его пролекарство или его фармацевтически приемлемая соль.
4. 5-членное гетероциклическое соединение по п.2 или 3, где X1 представляет собой N и X2 представляет собой CR11, где R11 представляет собой атом водорода или низший алкил, или его пролекарство или его фармацевтически приемлемая соль.
5. 5-членное гетероциклическое соединение по п.2 или 3, где X1 представляет собой CH и X2 представляет собой N, или его пролекарство или его фармацевтически приемлемая соль.
6. 5-членное гетероциклическое соединение по п.2 или 3, где X1 и X2 независимо представляют собой CR11, где эти R11 являются необязательно отличными друг от друга и представляют собой атом водорода или низший алкил, или его пролекарство или его фармацевтически приемлемая соль.
7. 5-членное гетероциклическое соединение по п.6, где X1 и X2 представляют собой CH, или его пролекарство или его фармацевтически приемлемая соль.
8. 5-членное гетероциклическое соединение по п.1, где Т представляют собой циано, или его пролекарство или его фармацевтически приемлемая соль.
9. 5-членное гетероциклическое соединение по п.1, где Q представляет собой карбокси, или его пролекарство или его фармацевтически приемлемая соль.
10. 5-членное гетероциклическое соединение по п.9, где группа, представленная общей формулой
 ,
,
является группой, представленной следующей общей формулой (IIa) или (IIb)
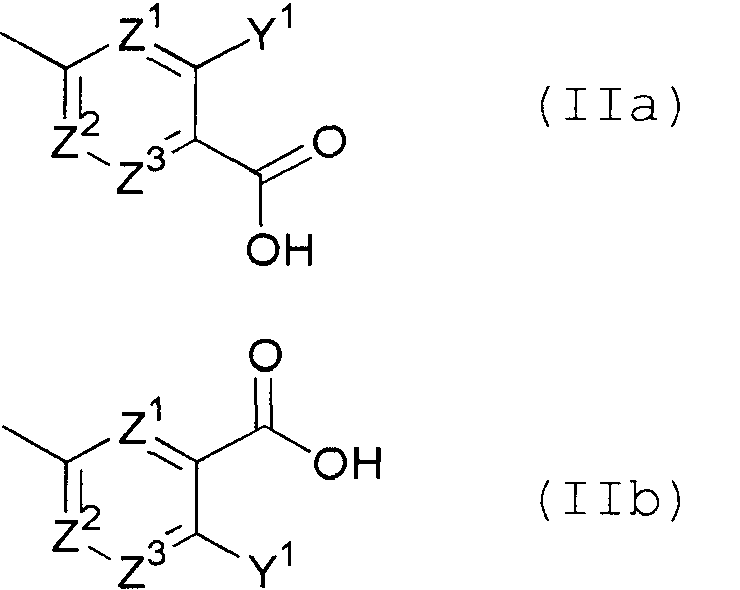 ,
,
в формулах
Z1, Z2 и Z3 независимо представляют собой CR12 или N; при условии, что два или более из Z1, Z2 и Z3 одновременно не представляют собой N; и
Y1 и R12 независимо представляют собой атом водорода, гидрокси, амино или атом галогена, при условии, что когда присутствуют два или более R12, эти R12 необязательно являются одинаковыми или отличными друг от друга, или его пролекарство или его фармацевтически приемлемая соль.
11. 5-членное гетероциклическое соединение по п.10, где группа, представленная общей формулой (II), является группой, представленной общей формулой (IIa), где Z1, Z2 и Z3 независимо представляют собой CR13, где R13 представляет собой атом водорода или атом галогена, и Y1 представляет собой атом водорода, гидрокси или амино, или его пролекарство или его фармацевтически приемлемая соль.
12. 5-членное гетероциклическое соединение по п.10, где группа, представленная общей формулой (II), является группой, представленной общей формулой (IIb), где Z1, Z2 и Z3 независимо представляют собой CR13, где R13 представляет собой атом водорода или атом галогена, и Y1 представляет собой атом водорода, гидрокси или амино, или его пролекарство или его фармацевтически приемлемая соль.
13. 5-членное гетероциклическое соединение по п.10, где группа, представленная общей формулой (II), является группой, представленной общей формулой (IIa), где один из Z1 и Z2 представляет собой N, другой представляет собой CH; Z3 представляет собой CH и Y1 представляет собой атом водорода, гидрокси или амино, или его пролекарство или его фармацевтически приемлемая соль.
14. 5-членное гетероциклическое соединение по п.10, где группа, представленная общей формулой (II), является группой, представленной общей формулой (IIb), где Z1 и Z3 независимо представляют собой CR13, где R13 представляет собой атом водорода или атом галогена; Z2 представляет собой N и Y1 представляет собой атом водорода, гидрокси или амино, или его пролекарство или его фармацевтически приемлемая соль.
15. 5-членное гетероциклическое соединение по п.9, где кольцо J представляет собой 5-членное гетероарильное кольцо, имеющее один гетероатом, выбранный из кислорода, в кольце, или его пролекарство или его фармацевтически приемлемая соль.
16. 5-членное гетероциклическое соединение по п.15, где группа, представленная общей формулой
 ,
,
является группой, представленной следующей общей формулой (IIc)
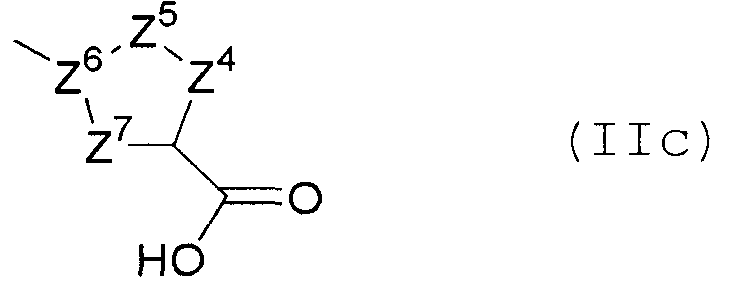 ,
,
в формуле
Z4, Z5 и Z7 независимо представляют собой атом кислорода или CR14, при условии, что два или более из Z4, Z5 и Z7 не являются одновременно атомом кислорода, где R14 представляет собой атом водорода, гидрокси, амино или атом галогена, при условии, что когда присутствуют два или более R14, эти R14 являются необязательно одинаковыми или отличными друг от друга; Z6 представляет собой атом углерода и Z4, Z5, Z6 и Z7 связаны вместе с атомом углерода, связанным с карбоксигруппой, с образованием 5-членного гетероарильного кольца, или его пролекарство или его фармацевтически приемлемая соль.
17. 5-членное гетероциклическое соединение по п.1, где R1 представляет собой -A1-D-L-M или -A1-D-E-G-L-M, в формуле A1 представляет собой простую связь и D, E, G, L и M имеют такие же значения, как указаны в п.1, или его пролекарство или его фармацевтически приемлемая соль.
18. 5-членное гетероциклическое соединение по п.1, где R1 представляет собой -A2-D-L-M или -A2-D-E-G-L-M, в формуле A2 представляет собой -O- и D, E, G, L и M имеют такие же значения, как указаны в п.1, или его пролекарство или его фармацевтически приемлемая соль.
19. 5-членное гетероциклическое соединение по п.1, где R1 представляет собой -A3-D-L-M или -A3-D-E-G-L-M, в формуле A3 представляет собой -CO- или -CON(R3)-, и D, E, G, L, M и R3 имеют такие же значения, как указаны в п.1, или его пролекарство или его фармацевтически приемлемая соль.
20. 5-членное гетероциклическое соединение по п.1, где R1 представляет собой -A4-D-L-M или -A4-D-E-G-L-M, в формуле A4 представляет собой -N(R3)CO или -N=CR3N(R4)-, и D, E, G, L, M, R3 и R4 имеют такие же значения, как указаны в п.1, или его пролекарство или его фармацевтически приемлемая соль.
21. 5-членное гетероциклическое соединение по п.1, которое выбрано из группы, включающей:
2-(3-циано-4-фенилпиррол-1-ил)изоникотиновую кислоту,
4-(3-циано-4-фенилпиррол-1-ил)-2-гидроксибензойную кислоту,
4-(4-циано-3-фенилпиразол-1-ил)-2-гидроксибензойную кислоту,
4-(3-циано-4-тиофен-2-илпиррол-1-ил)-2-гидроксибензойную кислоту,
4-(3-циано-4-тиофен-3-илпиррол-1-ил)-2-гидроксибензойную кислоту,
4-(3-бутил-4-цианопиррол-1-ил)-2-гидроксибензойную кислоту,
4-(3-циано-4-циклопропилпиррол-1-ил)-2-гидроксибензойную кислоту,
4-(4-циано-3-тиофен-3-илпиразол-1-ил)-2-гидроксибензойную кислоту,
4-(4-циано-3-тиофен-2-илпиразол-1-ил)-2-гидроксибензойную кислоту,
4-(3-циано-4-фенилпиразол-1-ил)-2-гидроксибензойную кислоту,
4-(3-циано-4-тиофен-2-илпиразол-1-ил)-2-гидроксибензойную кислоту, и
4-(3-циано-4-тиофен-3-илпиразол-1-ил)-2-гидроксибензойную кислоту, или
его фармацевтически приемлемая соль.
22. Ингибитор ксантиноксидазы, содержащий в качестве активного ингредиента 5-членное гетероциклическое соединение по любому из пп.1-21, его пролекарство или фармацевтически приемлемую соль.
23. Фармацевтическая композиция, обладающая ингибируюшей ксантиноксидазу активностью, содержащая в качестве активного ингредиента 5-членное гетероциклическое соединение по любому из пп.1-21, или его пролекарство или фармацевтически приемлемую соль.
24. Фармацевтическая композиция по п.23, которая является агентом для профилактики или лечения заболевания, выбранного из группы, состоящей из гиперурикемии, подагрических узлов, подагрического артрита, почечного нарушения, связанного с гиперурикемией и мочевыми конкрементами.
25. Фармацевтическая композиция по п.24, которая является агентом для профилактики или лечения гиперурикемии.
26. Фармацевтическая композиция по п.23, которая является агентом для снижения уровня мочевой кислоты в сыворотке.
27. Фармацевтическая композиция по п.23, которая является ингибитором продуцирования мочевой кислоты.
| US 5824691 A, 20.10.1998 | |||
| US 6511974 B1, 28.01.2003 | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
| J | |||
| COBB et al, Synthesis and Reactions of 1-Aryl-2-nitropyrroles | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Устройство для устранения мешающего действия зажигательной электрической системы двигателей внутреннего сгорания на радиоприем | 1922 |
|
SU52A1 |
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| A | |||
| BALSAMO | |||
Авторы
Даты
2014-05-20—Публикация
2008-04-10—Подача