Область техники, к которой относится изобретение
Настоящее изобретение относится к новым композициям на основе смешанных оксидов оксида церия и оксида циркония, имеющих высокую кислородную емкость. Настоящее изобретение относится также к приготовлению композиций смешанных оксидов и к способу применения композиций смешанных оксидов в качестве катализаторов и/или носителей катализаторов, в частности, для очистки и/или конверсии выхлопных газов двигателей внутреннего сгорания.
Предпосылки к созданию изобретения
Оксид церия широко применяется в качестве промотора катализатора для очистки выхлопных газов, выбрасываемых двигателем внутреннего сгорания, благодаря его высокой кислородной емкости. Обычно с целью повышения кислородной емкости (КЕ) оксид церия применяется в виде маленьких частиц, имеющих относительно высокую удельную поверхность. К сожалению, однако, оксид церия имеет тенденцию спекаться с уменьшением поверхности в условиях высоких температур, теряя в результате этого свою эффективность как кислородоемкого компонента.
Позднее потребность термически стабилизировать катализаторы на основе оксида церия в отношении высоких температур сконцентрировала внимание на легировании оксида церия широким рядом оксидов металлов. С этой целью, многочисленные, относящиеся к старой технике литературные источники предлагали вводить в оксид церия оксид циркония или другие оксиды редкоземельных элементов с целью ослабления процесса спекания и создания материалов с большой величиной поверхности. Например, в японской патентной заявке 55,15/1992 раскрывается способ приготовления смешанного оксида церия и оксида циркония, в котором раствор, содержащий соль трехвалентного церия и соль циркония, подвергают соосаждению с помощью какого-либо основания в присутствии перекиси водорода. Способ дает смешанные оксиды церия и циркония, имеющие высокую удельную поверхность и прекрасную термостойкость.
Было также предложено, чтобы чистые твердые растворы оксида церия и оксида циркония, имеющие большую величину поверхности, нашли применение в качестве эффективных кислородоемких компонентов в автомобильных каталитических конвертерах. Были опубликованы сообщения о различных композициях оксида церия с оксидом циркония.
Например, в патенте США 5693299 раскрывается смешанный оксид оксида церия и оксида циркония, обладающий термостабильностью и очень высокой удельной поверхностью, равной, по меньшей мере, 80 м2/г. Смешанные оксиды получаются с помощью высокотемпературного гидролиза и обладают чистой монофазной кубической формой кристаллизации СеО2, где цирконий встроен в кристаллическую форму оксида кремния.
В патенте США 5607892 раскрываются также частицы смешанного цериево-циркониевого смешанного оксида, имеющего устойчивую удельную поверхность. Смешанные оксиды получают тщательным перемешиванием золя циркония с золем церия, осаждением смеси с помощью основания с целью получения осадка и последующего прокаливания полученного осадка. Сообщалось, что кислородная емкость, измеренная у продукта, прокаленного при 1000°С, составляет только 2,8 мл СО/г CeO2 (62,5 μмоль О2 на 1 г CeO2).
С целью соответствия будущим жестким нормам по выхлопу необходимо, чтобы катализаторы на основе оксида церия обладали высокой кислородной емкостью даже после воздействия температуры, превышающей 1000°С. Поскольку у катализаторов на основе оксида церия, подвергнутых действию столь высоких температур, обычно происходит уменьшение поверхности, имеется потребность в разработке материалов на основе церия с кислородной емкостью, не зависящей от величины поверхности.
Далее, благодаря последним достижениям в области технологии контроля за двигателями новейшие двигатели обладают еще более жестким контролем состава топливно-воздушной смеси, обусловленным быстрыми изменениями парциального давления кислорода в месте размещения катализатора. Катализаторы, используемые в таких двигателях, должны не только обладать более высокой кислородной емкостью по сравнению с ранее известными катализаторами, но и высокой скоростью отдачи кислорода для того, чтобы реагировать на названные флуктуации парциального давления кислорода. Вследствие этого в автомобильной промышленности имеется потребность в материалах катализаторов и носителей катализаторов, которые обладали бы как высокой кислородной емкостью, так и повышенной скоростью отдачи кислорода в условиях высоких температур.
Краткое содержание изобретения
Разработаны новые композиции на основе смешанных оксидов церия и циркония, имеющие чрезвычайно высокие кислородную емкость и способность отдачи кислорода. Смешанные оксиды церия и циркония по изобретению обладают номинально кубической, многофазной формой кристаллизации, основанной на единообразно регулируемой доменной кристаллической подструктуре. Неожиданным образом оказалось, что соответствующие настоящему изобретению композиции смешанных оксидов обладают высокой кислородной емкостью, не зависящей от величины поверхности.
Композиции смешанных оксидов по изобретению содержат поликристаллические частицы на основе оксида церия и оксида циркония. Кристаллиты, включающие поликристаллические частицы, состоят из областей, или «доменов», на субкристаллическом уровне с различными соотношениями церия и циркония. В соответствии с настоящим изобретением было установлено, что когда прилегающие один к другому домены в пределах одного кристаллита значительно различаются атомными соотношениями церия и циркония, возникает уникальная кристаллическая подструктура, которая способствует повышению кислородной емкости и кислородной отдачи.
Не имея намерения вдаваться в какую-либо специальную теорию, можно предсказать, что причиной того, что прилегающие один к другому домены обладают разными параметрами решетки, является разница в составах между соседними доменами. Предполагается, что разница в параметрах решетки приводит к локальному напряжению на границах между доменами. Выдвигается гипотеза о том, что такое локальное напряжение вдоль границ между соседними доменами создает сеть внутренних путей через кристаллиты. Предполагается, что наличие таких путей позволяет кислороду быстро проникать внутрь кристаллической решетки и быстро из нее выходить, обеспечивая тем самым повышенные кислородную емкость и кислородную отдачу, не зависящие от площади внешней поверхности частиц.
В связи со сказанным основным преимуществом настоящего изобретения является то, что оно предлагает новые композиции оксида церия и оксида циркония, имеющие определенную доменную кристаллическую структуру, которая способствует повышенной кислородной емкости и скорости отдачи кислорода по сравнению с существующими композициями оксида церия и оксида циркония.
Другим преимуществом настоящего изобретения является то, что оно предлагает новые композиции оксида церия и оксида циркония, которые обладают высокой кислородной емкостью, не зависящей от величины поверхности.
Преимуществом настоящего изобретения является также то, что оно предлагает композиции оксида церия и оксида циркония, имеющие высокую кислородную емкость, причем в этих композициях не требуется, что до сих пор считалось необходимым, чистого однофазного кубического твердого раствора либо оксида церия, растворенного в оксиде циркония, либо оксида циркония, растворенного в оксиде церия.
Еще одним преимуществом настоящего изобретения является то, что оно предлагает новые смешанные оксиды церия и циркония, которые являются высокоэффективными в качестве катализатора/носителя для очистки выхлопных газов.
Наконец, еще одним преимуществом настоящего изобретения является то, что оно предлагает способ приготовления и применения новых композиций оксида церия и оксида циркония.
Другие преимущества и объекты настоящего изобретения будут продемонстрированы в описании, примерах и пунктах формулы изобретения.
Краткое описание чертежей
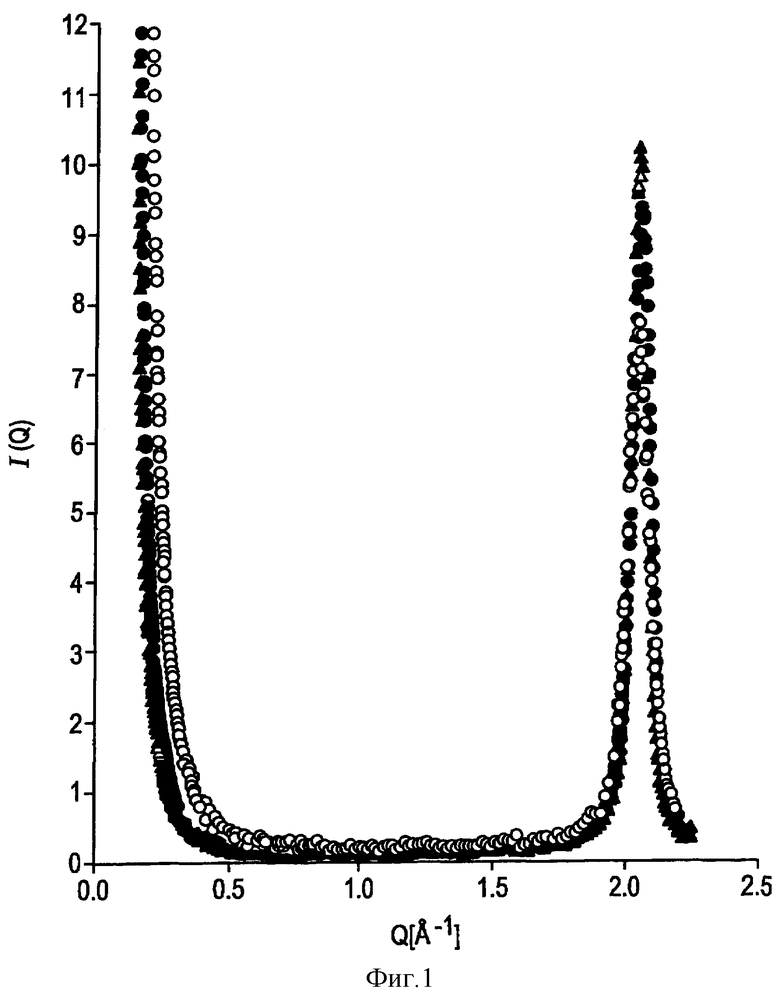
Фиг.1 представляет график зависимости нормализованной интенсивности рассеяния I(Q) в пределах от 0 до 12 от Q в пределах от 0,0 до 2,5 Å-1, определенной с помощью метода рассеяния рентгеновских лучей под малыми углами (SAXS) для композиций оксида церия и оксида циркония, приготовленных в соответствии с примером 1(•), сравнительным примером 1(▴) и сравнительньм примером 2(Ф), который (график) показывает положение первого дифракционного пика при Q, равном 2,06 Å-1, по которому нормализуется интенсивность рассеяния.
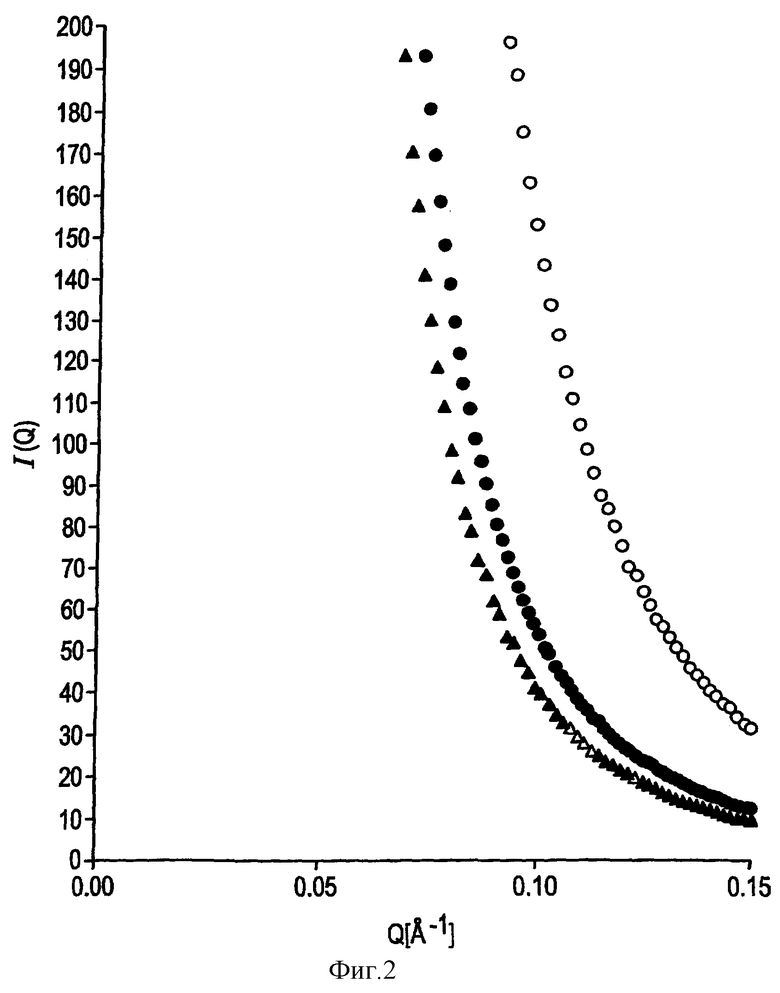
Фиг.2 представляет график зависимости нормализованной интенсивности рассеяния I(Q) в пределах от 0 до 200 от Q в пределах от 0,0 до 0,15 Å-1, определенной с помощью метода рентгеновского рассеяния под малыми углами (SAXS) для композиций оксида церия и оксида циркония, приготовленных в соответствии с примером 1(•), сравнительным примером 1(▴) и сравнительным примером 3(Ф).
Подробное описание изобретения
Далее настоящее изобретение будет объяснено подробным образом.
Используемый здесь термин «кислородная емкость» (КЕ) обозначает количество содержащегося в образце кислорода, определенного измерением потери массы с помощью традиционного термогравиметрического анализа (ТГА). Образец выдерживают в течение 60 мин при 500°С в токе воздуха, движущегося с объемной скоростью 120 мл/мин, до полного окисления образца. После этого поток воздуха сразу же заменяют смесью 10% Н2 в азоте при тех же температуре и объемной скорости и выдерживают при постоянной температуре в течение дополнительных 60 мин. Кислородную емкость определяют измерением потери массы при переходе от окислительных условий к восстановительным. Единицей, используемой для характеристики КЕ, является μмоль О2 в 1 г образца.
Используемый здесь термин «скорость отдачи кислорода» обозначает скорость, с которой кислород выходит из частиц Ce/Zr, измеренную с помощью ТГА. Образец выдерживают в течение 60 мин при 500°С в потоке воздуха, движущегося с объемной скоростью 120 мл/мин, до полного окисления образца. После этого поток воздуха сразу же заменяют смесью 10% H2 в азоте при тех же температуре и объемной скорости и выдерживают при постоянной температуре в течение дополнительных 60 мин. Скорость отдачи кислорода рассчитывают по кривой зависимости первой производной потери веса от времени и затем нормализуют по величине поверхности частиц. Единицей, используемой для характеристики скорости отдачи кислорода, является мг-О2/м2-мин.
Используемый здесь термин «поликристаллическая частица» обозначает частицу, состоящую из более чем двух кристаллитов на основании измерения с помощью традиционного метода дифракции рентгеновских лучей.
Используемый здесь термин «кристаллит» обозначает области внутри частицы, имеющие одну и ту же кристаллографическую ориентацию и структуру, определенные по уширению линий с помощью традиционного метода дифракции рентгеновских лучей.
Используемый здесь термин «домен» обозначает область или объем внутри монокристалла, имеющие однородный или существенно однородный состав, определенный с помощью метода рентгеновского рассеяния под малыми углами (SAXS). Согласно настоящему изобретению отношение Ce:Zr в домене регулируется таким образом, чтобы оно отличалось от этого отношения в соседних доменах, содержащих кристаллит.
Используемый здесь термин «субкристаллическая структура» обозначает область внутри монокристалла, которая состоит из двух или более доменов.
Используемый здесь термин «многофазный» обозначает материал, содержащий более чем одну кристаллическую фазу. Такая фаза может состоять из более чем одной кристаллической структуры, например, кубической или тетрагональной, или из одной и той же структуры, но с различными параметрами решетки.
Используемый здесь термин «неоднородность» обозначает прилегающие один к другому домены внутри монокристалла, имеющие различные атомные отношения Ce:Zr.
Используемый здесь термин «величина поверхности» обозначает площадь поверхности частицы, измеренную с помощью стандартного анализа по БЭТ.
Используемый здесь термин «старение» обозначает нагревание образца с целью ускорения изменения его свойств.
Используемый здесь термин «нормализованная интенсивность рассеяния I(Q)» обозначает интенсивность рассеяния, определенную с помощью метода рентгеновского рассеяния под малыми углами (SAXS) и поделенную на постоянную величину, такую как интенсивность, интегрированную под первым дифракционным пиком с центром при Q, приблизительно равным 2,06 Å-1, принятую за единицу.
Композиции смешанных оксидов в соответствии с настоящим изобретением имеют многофазную кристаллическую структуру и образованы поликристаллическими частицами. Каждая частица имеет компонент оксида церия и компонент оксида циркония и состоит из множества кристаллитов. Каждый кристаллит в частице состоит из субкристаллической структуры, которая содержит множество доменов с различным атомным отношением Ce:Zr в соседних доменах, характеризующихся заданной степенью неоднородности по отношению один к другому, определяемой с помощью метода рентгеновского рассеяния под малыми углами (SAXS). Нетрудно понять, что измерение с помощью SAXS проводится на многочастичном образце, и полученные данные представляют собой усредненное распределение степени неоднородности между доменами на субкристаллическом уровне частиц в образце. Таким образом, данные SAXS указывают на то, что индивидуальные частицы должны содержать описанную выше структуру в среднем.
Согласно изобретению средний размер доменов в свежеприготовленном материале составляет от примерно 10 до примерно 50 Å. После старения в течение 5 час при 1000°С средний размер доменов принимает значение от примерно 10 до 50 Å.
Домены распределены внутри кристаллитов оксида церия и оксида циркония, имеющих средний размер от примерно 40 до примерно 200 Å, преимущественно от примерно 50 до 120 Å, что легко определяется с помощью дифракции рентгеновских лучей с использованием пика при 28-30° 2Θ после прокаливания в течение 4 час при 900°С. Кристаллиты, в свою очередь, образуют поликристаллические частицы со средним размером частиц в пределах от примерно 0,1 до примерно 50 μм, преимущественно от примерно 0,5 до 20 μм.
Как правило, частицы смешанных оксидов настоящего изобретения содержат приблизительно от 80 до 20% мас. CeO2 и приблизительно от 20 до 80% мас. ZrO2, преимущественно приблизительно от 40 до 60% мас. СеО2 и приблизительно от 60 до 40% мас. ZrO2. В предпочтительном варианте композиция смешанных оксидов включает 50% мас. CeO2 и 50% мас. ZrO2. В оптимальном случае частицы смешанных оксидов изобретения могут включать до приблизительно 10% мас., преимущественно до 8% мас. и, наиболее предпочтительно, от примерно 2 до примерно 7% мас. дополнительного оксида металла, отличного от церия. Подходящие оксиды металлов включают, но не ограничены ими, оксиды редкоземельных металлов, отличных от церия, оксид кальция и их смеси. Подходящие оксиды редкоземельных металлов включают, но не ограничены ими, оксиды лантана, празеодима, неодима, самария, гадолиния и иттрия.
Обычно композиции смешанных оксидов изобретения имеют удельную поверхность после прокаливания в течение 2 час при 500°С, равную, по меньшей мере, 30 м2/г, предпочтительнее, по меньшей мере, 40 м2/г и, еще более предпочтительно, по меньшей мере, 60 м2/г, которая обычно лежит в пределах от примерно 30 до примерно 120, преимущественно от примерно 40 до примерно 100 и, наиболее предпочтительно, от примерно 50 до 90 м2/г. После старения в течение 4 час при 1000°С величина удельной поверхности не превышает 10 м2/г, преимущественно не превышает 5 м2/г и, наиболее предпочтительно, не превышает 3 м2/г, будучи обычно в пределах от примерно 10 до примерно 1, преимущественно от примерно 5 до примерно 1 и, наиболее предпочтительно, от примерно 3 до примерно 1 м2/г.
Смешанные оксиды настоящего изобретения обладают тем преимуществом, что они одновременно имеют высокую скорость отдачи кислорода и высокую кислородную емкость. Смешанные оксиды настоящего изобретения обычно имеют кислородную емкость, измеренную изотермически при 500°С, равную, по меньшей мере, 260 μмоль O2/г образца, преимущественно более 300 μмоль O2/г образца, предпочтительнее более 315 μмоль О2/г образца и, наиболее предпочтительно, более 330 μмоль О2/г образца после старения в течение 4 час при 1000°С. Обычно смешанные оксиды изобретения обладают КЕ в пределах от примерно 260 до примерно 800, преимущественно от примерно 300 до примерно 600 и, наиболее предпочтительно, от примерно 350 до примерно 450 μмоль O2/г образца после старения в течение 4 час при 1000°С.
Смешанные оксиды настоящего изобретения имеют высокую скорость отдачи кислорода, которая после старения в течение 4 час при 1000°С обычно выше 1,0 мг-O2/м2-мин, преимущественно выше 2,0 мг-О2/м2-мин и, наиболее предпочтительно, выше 5,0 мг-O2/м2-мин. Обычно смешанные оксиды после старения в течение 4 час при 1000°С обладают скоростью отдачи кислорода в пределах от примерно 1 до примерно 100, преимущественно от примерно 2 до примерно 50 и, наиболее предпочтительно, от примерно 5 до примерно 10 мг-O2/м2-мин.
Повышенные кислородная емкость и кислородная отдача, которыми обладают композиции оксида церия и оксида циркония изобретения, достигаются путем регулирования разницы в составе атомных отношений Ce:Zr прилегающих один к другому доменов в монокристаллите таким образом, чтобы в этих доменах создавались различные параметры решетки. Как несложно понять специалистам, некоторые домены окажутся при этом обогащенными оксидом церия, т.е. будут состоять преимущественно из оксида церия с оксидом циркония, растворенным в оксиде кремния, в то время как другие домены окажутся обогащенными оксидом циркония, т.е. будут состоять преимущественно из оксида циркония с оксидом церия, растворенным в оксиде циркония. Однако, если составы соседних доменов слишком однородны или слишком разнородны, в смешанных композициях не будет образовываться доменная структура, требуемая для обеспечения желаемых кислородной емкости и отдачи кислорода. Таким образом, степень различия в составе или однородности между соседними доменами является важной для получения композиций с повышенной кислородной емкостью и одновременно с повышенными скоростями отдачи кислорода, не зависящими от величины поверхности.
Степень различия в составе соседних доменов может быть, как это описано ниже, определена с использованием метода SAXS.
В то время как задачей традиционного метода рассеяния рентгеновских лучей является определение структуры кристалла и положений атомов, целью измерения методом SAXS является исследование особенностей локальной структуры в масштабе, превышающем атомное расстояние, обычно в масштабе десятков и сотен ангстремов. Угол рассеяния 2Θ между падающим лучом и детектором соотносится с вектором рассеяния Q как Q=(4π/λ)sinΘ, где λ есть длина волны рентгеновского излучения. Значение вектора рассеяния Q определяет характеристическую длину, которую исследуют с помощью рентгеновских лучей как π/Q. При измерении интенсивности дифракции рентгеновских лучей под меньшими углами, т.е. при меньших векторах рассеяния Q, можно исследовать пространственные структурные особенности в материалах. Для того, чтобы избежать интерференции между падающим лучом и интенсивностью рассеяния рентгеновских лучей, которую измеряют под очень малым углом, метод SAXS требует очень жестких условий коллимации на падающем луче. Таким образом, измерение с помощью SAXS не может быть произведено на стандартном рентгеновском дифрактометре. Однако для измерения, описанного в настоящем патенте, необходимо одновременно измерять интенсивность рассеяния под относительно большими углами с целью нормализации интенсивности, что будет подробно объяснено ниже. Идеальным средством для достижения названной цели является синхротронное рентгеновское излучение, поскольку его высокоинтенсивный падающий луч с малой расходимостью пучка облегчает коллимацию, позволяя тем самым измерять интенсивность рассеяния рентгеновских лучей при широком диапазоне углов и сводя к минимуму время измерения.
Описанные здесь измерения по методу SAXS были выполнены на лучевой линии Х-7А Национального синхротронного источника света в Брукхавенской национальной лаборатории, Уптон, Нью Йорк. Падающими рентгеновскими лучами с длиной волны λ=0,912 Å облучались материалы образца, обернутого тонкими слоями кантона - очень прозрачного по отношению к рентгеновским лучам полимерного материала. Типичная толщина образцов была в пределах от 10 до 100 μм. Интенсивность рассеяния измеряли с помощью стандартного детектора для углов 0,66°<2Θ<25,15°, что соответствует Q в пределах от примерно 0,08 Å-1 до примерно 3,0 Å-1. Падающий рентгеновский луч коллимировали таким образом, чтобы вклад падающего луча в интенсивность рассеяния, даже измеренную при самом малом угле 2Θ=0,66°С, был пренебрежимо малым. Рассеянная интенсивность рентгеновских лучей собиралась в каждой измеряемой точке в течение нескольких секунд.
Интенсивность в методе SAXS от систем с разделением фаз подчиняется закону Porod:

где I(Q) есть нормализованная интенсивность рассеяния. На фиг.1 график зависимости нормализованной интенсивности рассеяния I(Q) от вектора рассеяния Q обнаруживает первый дифракционный пик, центрированный около Q, приблизительно равного 2,06 Å-1, по которому была нормализована интенсивность рассеяния.
В уравнении (1) К определяется уравнением (2):

где Δρ есть разница в электронной плотности между двумя фазами и S - площадь граничной поверхности между фазами, измеряемая в единицах Å2. При данном значении S величина I возрастает с увеличением Δρ, которая в случае смешанных оксидов (Ce, Zr)O2 обусловлена, прежде всего, разницей между доменами внутри кристалла. Если рассматривать двухфазный образец с составами (Ce1-X2ZrX1)O2 в одной фазе и (Ce1-X2ZrX2)O2 в другой, а Δρ равна 0,49(Х1-Х2), то значение интенсивности при определенном Q является мерой разнородности составов.
Логарифмический график уравнения (1) является прямой линией, описываемой уравнением (3):
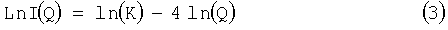
Таким образом, для интенсивностей рассеяния, собранного с разных образцов и нормализованного одинаковым способом, угол наклона результирующих прямых линий равен -4, в то время как отсекаемый на координате отрезок зависит от параметров Δρ и S.
Для определения степени разнородности внутри субкристаллической доменной структуры смешанных оксидов, соответствующих настоящему изобретению, проводится измерение методом SAXS для векторов рассеяния Q в пределах от примерно 0,08 Å-1 до примерно 3,0 Å-1. После этого строят график зависимости нормализованной интенсивности рассеяния 7(Q) от вектора рассеяния Q, как это указано выше (в единицах Å-1), а не от 2Θ, как это обычно делается.
Соответствующие настоящему изобретению смешанные оксиды обладают критической степенью неоднородности, когда они характеризуются нормализованной интенсивностью рассеяния I(Q) в пределах от примерно 49 до примерно 119, преимущественно от примерно 50 до примерно 100 и, наиболее предпочтительно, от примерно 54 до примерно 85 при рассеянии Q, равном 10 Å-1. Обычно угол наклона прямолинейного участка графика зависимости логарифма нормализованной интенсивности рассеяния LnI(Q) от логарифма вектора рассеяния ln(Q) при -2,5<ln(Q)<-1 равен приблизительно -4,0 и, таким образом, подчиняется закону Porod. Специалистам хорошо известно, что данные SAXS, которые соответствуют закону Porod, в наибольшей степени свидетельствуют о желаемой доменной структуре.
Согласно настоящему изобретению смешанные оксиды обычно приготовляют путем совместного осаждения раствора смешанных солей, содержащего соль церия и соль циркония, растворенные в подходящем растворителе, например, в воде или органическом растворителе. В одном из предпочтительных вариантов растворителем является вода.
Концентрация твердых материалов в растворах смешанных солей, используемых для приготовления смешанного оксида настоящего изобретения, является значительной. Если концентрация твердых материалов слишком низка, субкристаллическая структура, имеющая желаемую степень неоднородности, образовываться не будет. В связи с этим содержание твердых материалов в растворе регулируют с целью обеспечения желаемой неоднородности. Обычно раствор смешанных солей обладает концентрацией твердых материалов, которая достаточна для облегчения образования желаемой доменной структуры. Предпочтительно, чтобы раствор смешанных солей имел концентрацию твердых материалов выше примерно 23% мас., более предпочтительно выше примерно 25% мас. и, наиболее предпочтительно, выше примерно 27% мас. в расчете на оксидную основу. Обычно концентрация твердых материалов в растворе смешанных солей находится в пределах от примерно 24 до примерно 39% мас. и преимущественно от примерно 25 до примерно 29% мас. в расчете на оксидную основу.
Растворы смешанных солей, используемые для приготовления смешанных оксидов в соответствии с настоящим изобретением, могут быть приготовлены смешением цериевой соли с циркониевой солью таким образом и в таких условиях, которые обеспечили бы растворение всего или практически всего содержания твердых материалов в подходящем растворителе. В одном из вариантов раствор смешанных солей приготовляют смешением цериевой соли с водным раствором циркониевой соли, в котором мольное отношение катиона к аниону обычно составляет от 1:1 до 1:2. Например, когда циркониевой солью является оксинитрат циркония, мольное отношение катиона к аниону в растворе циркониевой соли обычно равно 1:2. С другой стороны, когда циркониевой солью является гидроксинитрат циркония, мольное отношение катиона к аниону в растворе циркониевой соли обычно равно 1:1.
В другом варианте изобретения раствор смешанных солей приготовляют растворением карбоната церия в растворе циркониевой соли с целью получения раствора, в котором мольное отношение катиона к аниону равно 1:2, с последующим добавлением к раствору минимального количества кислоты, достаточного для растворения всего или практически всего карбоната, о чем свидетельствует светлый или прозрачный раствор.
Подходящие цериевые и циркониевые соли, которые могут быть использованы для приготовления растворов смешанных солей, применимых для способа настоящего изобретения, включают (но не ограничиваются ими) нитраты, хлориды, сульфаты, карбонаты и т.п. К раствору смешанных солей могут быть добавлены дополнительные оксидные компоненты, т.е. легирующие компоненты, в любой растворимой форме.
Осаждение из раствора смешанных солей может быть осуществлено обработкой раствора каким-либо основанием, преимущественно аммиаком, при перемешивании, в результате чего в осадок выпадает соответствующий гидроксид. рН раствора во время осаждения является щелочным, например, обычно в пределах приблизительно от 8 до 11.
Вслед за осаждением образовавшийся осадок обрабатывают окислительным агентом в количестве, достаточном для того, чтобы полностью или в значительной степени окислить присутствующий Се+3 до Ce+4. Подходящие окислительные агенты включают (но не ограничиваются ими) водный раствор брома, перекиси водорода, бромата натрия, гипохлорита натрия, озона, диоксида хлора и т.п. Предпочтительным окислительным агентом является перекись водорода. Обычно осадок обрабатывают водным раствором перекиси водорода в количестве, достаточном для того, чтобы обеспечить мольное отношение перекиси водорода к Се обычно от примерно 0,25 до примерно 1. Предпочтительно, чтобы водный раствор перекиси водорода был разбавленной перекисью водорода, содержащей менее чем приблизительно 35% мас. перекиси водорода. Обычно разбавленную перекись водорода добавляют в количестве, достаточном для того, чтобы обеспечить мольное отношение перекиси водорода к Се от примерно 0,5 до примерно 1.
Желательно, чтобы температура при проведении стадий осаждения и окисления не превышала 80°С, преимущественно 70°С и, наиболее предпочтительно, 60°С. В предпочтительном варианте изобретения температура при проведении стадий осаждения и окисления обычно будет лежать в пределах от примерно 20 до примерно 70°С и преимущественно от примерно 30 до примерно 60°С. Вслед за осаждением осадок может быть подвергнут старению при температуре обычно от примерно 70 до 100°С в течение от примерно 30 мин до примерно 5 час.
Образовавшийся осадок отфильтровывают и затем промывают водой, получая фильтровальную лепешку. Лепешку сушат традиционным образом, получая сыпучий порошок. В предпочтительном варианте промытый осадок повторно суспендируют в воде, и полученную суспензию подвергают распылительной сушке. После этого высушенный осадок прокаливают при температуре от примерно 500 до примерно 600°С в течение времени от примерно 30 мин до примерно 3 час, преимущественно от примерно 1 до примерно 4 час и, наиболее предпочтительно, от примерно 2 до примерно 3 час с образованием смешанного оксида в соответствии с настоящим изобретением.
К смешанному оксиду может быть добавлен легирующий компонент. В случае его добавления легирующий компонент может быть добавлен в любой момент приготовления смешанных оксидов. Предпочтительно добавление легирующего компонента вслед за осаждением, до или после прокаливания смешанного оксида. Подходящие легирующие компоненты включают переходные металлы группы VIII в виде оксидов, солей и т.п. В качестве легирующих компонентов предпочтительны никель, палладий и платина, из которых наиболее предпочтительны палладий и платина. Обычно легирующие компоненты добавляют в количествах, достаточных для создания их концентрации в конечном продукте из смешанных оксидов от примерно 15 до примерно 1000 ч/млн от массы смешанного оксида. Легирующий компонент желательно добавлять в целях облегчения тестирования.
Для получения желаемого размера частиц прокаленный смешанный оксид может быть затем размолот с использованием способов помола ударного типа. Подходящие способы помола включают (но не ограничиваются ими) помол на высокомощной шаровой мельнице, помол на мельнице типа Spex, помол с помощью энергии жидкости и т.п.
Повышенная кислородная емкость и скорость отдачи кислорода композиций смешанных оксидов настоящего изобретения позволяют использовать их в многочисленных областях. В частности, смешанные оксиды изобретения хорошо подходят для использования в области катализа в качестве катализаторов и/или носителей катализаторов. В одном из предпочтительных вариантов композиции смешанных оксидов по изобретению используют как составляющие катализатора для очистки или конверсии выхлопных газов, выбрасываемых двигателями внутреннего сгорания. В случае такого применения к композициям смешанных оксидов обычно примешивают окись алюминия до или после пропитки каталитически активными элементами, такими как благородные металлы. Таким смесям после этого либо придают форму с образованием катализатора, например, форму бусин, либо эти смеси используют для образования покрытия для огнеупоров, таких как монолитная керамика или металл, причем такого рода покрытие само по себе известно в технике в качестве «промывочной облицовки», описанной, например, в патентах США 5491120, 5015617, 5039647, 5045521, 5063193, 5128306, 5139992 и 4965245 (названные ссылки включены в заявку в качестве ссылочного материала).
Для дальнейшего иллюстрирования настоящего изобретения и его преимуществ приведены следующие конкретные примеры. Следует, однако, иметь в виду, что изобретение не ограничивается приведенными в примерах частными деталями.
Все части и процентные доли в примерах, а также в остальной части описания, если не оговорено особо, выражены в массе.
Далее, любые пределы чисел, упомянутые в описании или пунктах формулы изобретения, такие как пределы, представляющие конкретный ряд свойств, единиц измерения, условий, физических состояний или процентных содержаний, предназначены для точной и определенной подачи, со ссылками или каким-либо иным образом, любого числа, входящего в названные пределы, включая сюда подмножества чисел, входящих в эти пределы.
ПРИМЕРЫ
Упоминаемую в примерах кислородную емкость (КЕ) определяли путем измерения потери массы с использованием традиционного термогравиметрического анализа. Образцы выдерживали в течение 60 мин в токе воздуха при 500°С с целью их полного окисления с последующим переключением на смесь с 10% H2 в азоте и изотермической выдержкой в течение дополнительных 60 мин. Кислородную емкость определяли по потере массы при переходе от окислительных условий к восстановительным.
Все упомянутые в примерах скорости отдачи кислорода были определены путем расчета первой производной зависимости изменения массы от временного графика измерения КЕ и нормализации ее по величине поверхности образца.
Пример 1
586 г карбоната церия (III) (49,5% оксида) растворяют в 1105 г 20%-ного водного раствора цирконил-нитрата и 310 г концентрированной азотной кислоты. Образовавшийся раствор содержит 26,7% мас. твердых материалов в виде оксидов. Раствор перемешивают в течение ночи до полного растворения карбоната. 93 г этого раствора вливают в 400 мл 5 н. раствора аммиака при температуре 40°С и перемешивании. Величина рН после добавления всего количества равна приблизительно 9. Взвесь перемешивают 30 мин при 40°С, после чего добавляют 52 г 3%-ного водного раствора перекиси водорода. Мольное отношение перекиси водорода к оксиду церия равно 0,25.
Осадок промывают 5 объемами горячей деионизованной воды. От осадка отмывают нитрат аммония до проводимости ниже 5 м. См/см.
Фильтровальную лепешку разбавляют водой в отношении 1:1 с образованием водной суспензии, которую подвергают распылительной сушке, получая порошок. Высушенный порошок прокаливают в течение 1 часа при 500°С, получая конечную композицию смешанных оксидов, содержащую 42% мас. оксида циркония и 58% мас. оксида церия. Порошок анализируют с помощью метода рассеяния рентгеновских лучей под малыми углами (SAXS). Порошок характеризуется нормализованной интенсивностью рассеяния I(Q), равной 0,57 при Q=0,1 Å-1, как показано на фиг.2. График зависимости нормализованной интенсивности рассеяния I(Q) от Q представлен на фиг.1.
Для измерения КЕ прокаленный порошок смешанных оксидов пропитывают 15 ч/млн палладия в виде водного раствора нитрата и прокаливают при 500°С. Порошок подвергают старению в течение 4 час при 1000°С и измеряют КЕ с использованием описанного выше ТГА. Величина поверхности после старения равна 1,0 м2/г, кислородная емкость (КЕ) 363 μмоль О2/г образца и скорость отдачи кислорода - 1,8 мг-О2/м2-мин.
Пример 2
Получают фильтровальную лепешку с использованием описанной в примере 1 процедуры за исключением того, что, когда лепешку разбавляют водой в отношении 1:1 с образованием взвеси, перед распылительной сушкой к взвеси добавляют 15 ч/млн палладия в виде водного раствора нитрата. Высушенный порошок прокаливают 1 час при 500°С. Порошок подвергают старению в течение 4 час при 1000°С и измеряют КЕ с использованием описанного выше ТГА. Величина поверхности после старения равна 1,0 м2/г, кислородная емкость (КЕ) - 376 μмоль О2/г образца и скорость отдачи кислорода - 7,5 мг-О2/м2-мин. Интенсивность нормализованного рассеяния I(Q) при Q=0,1 Å-1 равна 57.
Пример 3
586 г карбоната церия(III) (49,5% твердого материала) растворяют в 1105 г 20%-ного водного раствора цирконил-нитрата (20% мас. твердого материала) и 310 г концентрированной азотной кислоты. Раствор смешанных оксидов содержит 26,7% твердых материалов. 93 г этого раствора подвергают осаждению в 400 мл 5 н. раствора аммиака при 60°С. После 30 мин перемешивания к суспензии добавляют 1000 мл 3%-ного водного раствора перекиси водорода. Мольное отношение перекиси водорода к оксиду церия равно 0,25.
Суспензию фильтруют и промывают осадок 3 л деионизованной воды при 70°С. Фильтровальную лепешку повторно суспендируют в воде и добавляют 15 ч/млн Pd в виде нитрата с образованием конечного смешанного оксида с 15 ч/млн Pd. Полученную смесь подвергают распылительной сушке и прокаливают в течение 1 часа при 500°С. Конечная композиция содержит 42% мас. оксида циркония и 58% мас. оксида церия.
Порошок подвергают старению в течение 4 час при 1000°С. Восстановление при 500°С при использовании ТГА дает КЕ, равное 342 μмоль О2/г образца, и скорость отдачи кислорода - 1,9 мг-О2/м2-мин. Нормализованная интенсивность рассеяния I(Q) при Q=0,1 Å-1 равна 70.
Пример 4
Получают фильтровальную лепешку с использованием описанной в примере 3 процедуры за исключением того, что водную фильтрованную лепешку перед распылительной сушкой легируют 100 г/млн Pd в виде нитратов. Высушенный распылением порошок прокаливают и старят как в примере 3. Интенсивность рассеяния была равна 69 при Q=0,1 Å-1, КЕ равна 350 ммоль O2/г образца и скорость отдачи кислорода - 50,5 мг-O2/м2-мин.
Пример 5
Получают фильтровальную лепешку с использованием описанной в примере 3 процедуры за исключением того, что водную фильтровальную лепешку перед распылительной сушкой легируют 1000 ч/млн нитрата. Высушенный распылением порошок прокаливают и старят, как в примере 3. Интенсивность нормализованного рассеяния I(Q) при Q=0,1 Å-1 равна 69, КЕ равна 308 μмоль О2/г образца, и скорость отдачи кислорода - 1,2 мг-O2/м2-мин.
Пример 6
Раствор смешанных нитратов получают, соединяя 930 г водного раствора нитрата церия (III) (28,3% оксида) и 900 г водного раствора гидроксинитрата циркония с отношением Zr:NO3, равным приблизительно 1:1 (25,3% мас. оксида). Смешанный раствор содержит 26,8% мас. твердых материалов в расчете на оксид. Конечная оксидная композиция содержит 52,5% мас. CeO2 и 47,5% мас. ZrO2.
Раствор добавляют к 8 л 5 н. раствора аммиака при 40°С. Выпавший в осадок гидроксид обрабатывают 1000 мл 3%-ного водного раствора перекиси водорода.
Мольное отношение перекиси водорода к оксиду церия равно 0,25. Фильтровальную лепешку повторно суспендируют в воде и добавляют 15 ч/млн Pd в виде нитрата. Полученную смесь подвергают распылительной сушке и прокаливают в течение 1 часа при 500°С. Прокаленный порошок подвергают старению в течение 4 час при 1000°С, после чего измеряют присутствующий в образце кислород при 500°С с использованием гравиметрического прибора. КЕ равна 379 μмоль О2/г образца, и скорость отдачи кислорода - 14,23 мг-O2/м2-мин. Нормализованная интенсивность рассеяния I(Q) при Q=0,1 Å-1 равна 55.
Пример 7
Раствор смешанных нитратов получают смешением 633 г карбоната церия (III) (55% оксида), растворенного в 570 г 70%-ной азотной кислоты со 142 г деионизованной воды с образованием раствора нитрата церия (III) с 29% мас. твердых материалов. Раствор смешивают с 965 г водного раствора гидроксинитрата циркония (26,1% мас. оксида) с отношением Zr:NO3, равным приблизительно 1:1. Концентрация раствора смешанных нитратов составляет 27,7% мас. оксидных твердых материалов. Конечная оксидная композиция содержит 58,9% мас. CeO2 и 41,2% мас. ZrO2. Раствор добавляют к 8 л 5 н. раствора аммиака при 40°С и перемешивании. Выпавший в осадок гидроксид обрабатывают 1000 мл 3%-ного водного раствора перекиси водорода (Н2O2/CeO2=0,25 М), после чего отфильтровывают и отмывают от нитрата аммония. Фильтровальную лепешку повторно суспендируют в воде и легируют 15 ч/млн Pd в виде нитрата. Суспензию высушивают распылением и прокаливают 1 час при 500°С. После старения порошка в течение 4 час при 1000°С измеренная КЕ образца при 500°С с использованием гравиметрического прибора равна 377 μмоль О2/г образца, и скорость отдачи кислорода - 7,5 мг-O2/м2-мин. Нормализованная интенсивность рассеяния I(Q) при Q=0,1 Å-1 равна 77.
Пример 8
Раствор смешанных нитратов получают смешением 67,1 г водного раствора нитрата церия (III) (28% оксида) с 22,6 г водного раствора гидроксинитрата циркония с отношением Zr:NO3, равным приблизительно 1:1 (26,1% мас. оксида) с образованием конечного раствора смешанных нитратов с концентрацией 27,5% мас. твердых материалов в расчете на оксиды. Конечная оксидная композиция содержит 70% мас. CeO2 и 30% мас. ZrO2. Раствор добавляют к 400 мл 5 н. раствора аммиака при 40°С и перемешивают в течение 30 мин. Выпавший в осадок гидроксид обрабатывают 6,25 г перекиси водорода в 45 г деионизованной воды (Н2O2/CeO2=0,25 М), после чего отфильтровывают и отмывают от нитрата аммония. Фильтровальную лепешку повторно суспендируют в воде и легируют 15 ч/млн Pd в виде нитрата. Суспензию высушивают распылением, прокаливают 1 час при 500°С и подвергают старению в течение 4 час при 1000°С. КЕ образца при 500°С с использованием гравиметрического прибора равна 310 μмоль О2/г образца. Скорость отдачи кислорода равна 5,2 мг-О2/м2-мин. Нормализованная интенсивность рассеяния I(Q) при Q=0,1 Å-1 равна 70.
Пример 9
Нитратный раствор приготовляют и осаждают так же как в примере 6. К нитратам церия и циркония добавлен нитрат лантана, в результате чего содержание твердых материалов в растворе смешанных нитратов равно 27,3% мас. в расчете на оксид. Осаждение, сушку и прокаливание выполняют, как в примере 6, получая конечную оксидную композицию с 51% мас. CeO2, 44% мас. ZrO2 и 5% мас. La2О3. После старения порошка в течение 4 час при 1000°С кислородная емкость, основанная на измерениях с помощью ТГА, равна 391 μмоль О2/г образца. Скорость отдачи кислорода равна 3,4 мг-О2/м2-мин. Нормализованная интенсивность рассеяния I(Q) при Q=0,1 Å-1 равна 92.
Пример 10
46,5 г водного раствора нитрата церия (III) (28,5% твердого материала) смешивают с 61,8 г водного раствора нитрата циркония (20% мас. твердого материала) до концентрации смешанного раствора 23,6% мас. твердых материалов в расчете на оксиды. Раствор вливают в 400 мл 5 н. раствора аммиака при температуре 60°С и непрерывном перемешивании. Суспензию перемешивают 30 мин при 60°С, после чего добавляют 25 г 30%-ного раствора перекиси водорода.
Осадок промывают 3 л горячей деионизованной воды. Фильтровальную лепешку разводят водой в отношении 1:1 с образованием суспензии и перед распылительной сушкой добавляют 15 ч/млн палладия в виде раствора нитрата. Высушенный порошок прокаливают в течение 1 часа при 500°С с образованием конечной композиции смеси оксидов с 48,4% мас. оксида циркония и 51,6% мас. оксида церия.
Порошок подвергают старению в течение 4 час при 1000°С, получая продукт с величиной поверхности <1 м2/г. Кислородная емкость (КЕ) равна 339 μмоль О2/г образца, и скорость отдачи кислорода - 15,0 мг-O2/м2-мин. Образец был проанализирован с помощью метода рентгеновского рассеяния под малыми углами (SAXS), как описано выше, и обнаружил интенсивность нормализованного рассеяния I(Q) при Q=0,1 Å-1, равную 54.
Пример 11
Раствор смешанных нитратов получают, соединяя 17,2 г водного раствора нитрата церия (III) (29% оксида) и 67 г водного раствора гидроксинитрата циркония с отношением Zr:NO3, равным приблизительно 1:1 (26,1% мас. оксида). К этому раствору добавляют 3,5 г 28,5%-ного нитрата лантана и 4,85 г 31%-ного нитрата иттрия. Содержание твердых материалов в смешанном растворе составляет 27% мас. в расчете на оксиды. Конечная оксидная композиция содержит 20% мас. CeO2, 70% мас. ZrO2, 4% мас. La2О3 и 6% мас. Y2О3. Раствор добавляют к 300 мл 5 н. раствора аммиака при 40°С. Выпавший в осадок гидроксид обрабатывают 51 мл 3%-ного водного раствора перекиси водорода.
Мольное отношение перекиси водорода к оксиду церия равно 0,25. Фильтровальную лепешку повторно суспендируют в воде и добавляют 15 ч/млн Pd в виде нитрата. Полученную смесь подвергают распылительной сушке и прокаливают в течение 1 часа при 500°С. Прокаленный порошок подвергают старению в течение 4 час при 1000°С, после чего измеряют присутствующий в образце кислород при 500°С с использованием гравиметрического прибора. КЕ равна 260 μмоль О2/г образца, и нормализованная интенсивность рассеяния I(Q) при Q=0,1 Å-1 равна 85. Скорость отдачи кислорода - 5,8 мг-O2/м2-мин.
Пример 12
Раствор смешанных нитратов получают, соединяя 88,9 г водного раствора нитрата церия (III) (28,3% оксида) и 84,9 г водного раствора гидроксинитрата циркония с отношением Zr:NO3, равным приблизительно 1:1 (26,1% мас. оксида). К этому раствору добавляют 6,25 г карбоната празеодима и 1,5 г азотной кислоты. Содержание твердых материалов в смешанном растворе составляет 26,5% мас. в расчете на оксиды. Конечная оксидная композиция содержит 50% мас. CeO2, 44% мас. ZrO2 и 6% мас. Pr6О11. Раствор добавляют к 700 мл 5 н. раствора аммиака при 40°С. Выпавший в осадок гидроксид обрабатывают 103 мл 3%-ного водного раствора перекиси водорода.
Мольное отношение перекиси водорода к оксиду церия равно 0,25. Фильтровальную лепешку повторно суспендируют в воде и добавляют 15 ч/млн Pd в виде нитрата. Полученную смесь подвергают распылительной сушке и прокаливают в течение 1 час при 500°С. Прокаленный порошок подвергают старению в течение 4 час при 1000°С, после чего измеряют присутствующий в образце кислород при 500°С с использованием гравиметрического прибора. КЕ равна 396 μмоль О2/г образца, и нормализованная интенсивность рассеяния I(Q) при Q=0,1 Å-1 равна 79. Скорость отдачи кислорода - 7,6 мг-О2/м2-мин.
Пример 13
Раствор смешанных нитратов получают, соединяя 88,9 г водного раствора нитрата церия (III) (28,3% оксида) и 84,9 г водного раствора гидроксинитрата циркония с отношением Zr:NO3, равным приблизительно 1:1 (26,1% мас. оксида). К этому раствору добавляют 5,64 г карбоната иттрия и 3 г азотной кислоты. Содержание твердых материалов в смешанном растворе составляет 26% мас. в расчете на оксиды. Конечная оксидная композиция содержит 50,6% мас. СеО2, 44,4% мас. ZrO2 и 5% мас. Y2О3. Раствор добавляют к 700 мл 5 н. раствора аммиака при 40°С. Выпавший в осадок гидроксид обрабатывают 103 мл 3%-ного водного раствора перекиси водорода.
Мольное отношение перекиси водорода к оксиду церия равно 0,25. Фильтровальную лепешку повторно суспендируют в воде и добавляют 15 ч/млн Pd в виде нитрата. Полученную смесь подвергают распылительной сушке и прокаливают в течение 1 часа при 500°С. Прокаленный порошок подвергают старению в течение 4 час при 1000°С, после чего измеряют присутствующий в образце кислород при 500°С с использованием гравиметрического прибора. КЕ равна 344 μмоль О2/г образца и нормализованная интенсивность рассеяния I(Q) при Q=0,1 Å-1 равна 81. Скорость отдачи кислорода - 4,2 мг-О2/м2-мин.
Пример 14
Раствор смешанных нитратов получают, соединяя 87,4 г водного раствора нитрата церия (III) (29% оксида) и 84,1 г водного раствора гидроксинитрата циркония с отношением Zr:NO3, равным приблизительно 1:1 (26,4% мас. оксида). К этому раствору добавляют 2,5 г оксида гадолиния и 3 г азотной кислоты. Содержание твердых материалов в смешанном растворе составляет 27% мас. в расчете на оксиды. Конечная оксидная композиция содержит 50,6% мас. CeO2, 44,4% мас. ZrO2 и 5% мас. Gd2O3. Раствор добавляют к 700 мл 5 н. раствора аммиака при 40°С. Выпавший в осадок гидроксид обрабатывают 103 мл 3%-ного водного раствора перекиси водорода.
Мольное отношение перекиси водорода к оксиду церия равно 0,25. Фильтровальную лепешку повторно суспендируют в воде и добавляют 15 ч/млн Pd в виде нитрата. Полученную смесь подвергают распылительной сушке и прокаливают в течение 1 часа при 500°С. Прокаленный порошок подвергают старению в течение 4 час при 1000°С, после чего измеряют присутствующий в образце кислород при 500°С с использованием гравиметрического прибора. КЕ равна 384 μмоль О2/г образца, и нормализованная интенсивность рассеяния I(Q) при Q=0,1 Å-1 равна 65. Скорость отдачи кислорода - 4,0 мг-О2/м2-мин.
Пример 15
Раствор смешанных нитратов получают, соединяя 87,4 г водного раствора нитрата церия (III) (29% оксида) и 84,9 г водного раствора гидроксинитрата циркония с отношением Zr:NO3, равным приблизительно 1:1 (26,1% мас. оксида). К этому раствору добавляют 4 г карбоната самария и 4 г азотной кислоты. Содержание твердых материалов в смешанном растворе составляет 27% мас. в расчете на оксиды. Конечная оксидная композиция содержит 50,6% мас. СеО2, 44,4% мас. ZrO2 и 5% мас. Sm2О3. Раствор добавляют к 700 мл 5 н. раствора аммиака при 40°С. Выпавший в осадок гидроксид обрабатывают 103 мл 3%-ного водного раствора перекиси водорода.
Мольное отношение перекиси водорода к оксиду церия равно 0,25. Фильтровальную лепешку повторно суспендируют в воде и добавляют 15 ч/млн Pd в виде нитрата. Полученную смесь подвергают распылительной сушке и прокаливают в течение 1 часа при 500°С. Прокаленный порошок подвергают старению в течение 4 час при 1000°С, после чего измеряют присутствующий в образце кислород при 500°С с использованием гравиметрического прибора. КЕ равна 385 μмоль О2/г образца, и нормализованная интенсивность рассеяния I(Q) при Q=0,1 Å-1 равна 70. Скорость отдачи кислорода равна 3,8 мг-О2/м2-мин.
Пример 16
Раствор смешанных нитратов получают, соединяя 87,4 г водного раствора нитрата церия (III) (29% оксида) и 84,1 г водного раствора гидроксинитрата циркония с отношением Zr:NO3, равным приблизительно 1:1 (26,4% мас. оксида). К этому раствору добавляют 10,5 г карбоната кальция и 3 г азотной кислоты. Содержание твердых материалов в смешанном растворе составляет 27% мас. в расчете на оксиды. Конечная оксидная композиция содержит 50,6% мас. CeO2, 44,4% мас. ZrO2. и 5% мас. СаО. Раствор добавляют к 700 мл 5 н. раствора аммиака при 40°С. Выпавший в осадок гидроксид обрабатывают 103 мл 3%-ного водного раствора перекиси водорода.
Мольное отношение перекиси водорода к оксиду церия равно 0,25. Фильтровальную лепешку повторно суспендируют в воде и добавляют 15 ч/млн Pd в виде нитрата. Полученную смесь подвергают распылительной сушке и прокаливают в течение 1 часа при 500°С. Прокаленный порошок подвергают старению в течение 4 час при 1000°С, после чего измеряют присутствующий в образце кислород при 500°С с использованием гравиметрического прибора. КЕ равна 359 μмоль О2/г образца, и нормализованная интенсивность рассеяния I(Q) при Q=0,1 Å-1 равна 65. Скорость отдачи кислорода - 8,5 мг-O2/м2-мин.
Пример 17
Повторяют пример 3 за исключением того, что после осаждения суспензии при 60°С поднимают температуру и нагревают суспензию в маточной жидкости в течение 2 час при 90°С. Осадок после этого отфильтровывают, промывают и обрабатывают так, как описано в примере 3. При нагревании суспензии была в значительной степени изменена структура, и желаемая доменная структура была разрушена высокой температурой. Это привело к падению КЕ при 500°С до значения, равного лишь 290 μмоль О2/г образца. Материал показал нормализованную интенсивность рассеяния I(Q) при Q=0,1 Å-1, равную 107. Скорость отдачи кислорода была равной 4,3 мг-О2/м2-мин.
Сравнительный пример 1
Смешивают 1147 г воды и 136 г уксусной кислоты и добавляют 236 г карбоната церия с образованием светлого раствора ацетата церия. Смесь перемешивают 48 час до полного растворения карбоната. К ацетату церия добавляют 512 г ацетата циркония (20% мас. ZrO2) и перемешивают до образования гомогенного раствора. Раствор подвергают распылительной сушке при 110°С с образованием белого порошка смешанных ацетатов. Порошок прокаливают в течение 1 часа в муфельной печи при температуре 500°С с образованием конечного смешанного оксида.
Свежепрокаленный оксид пропитывают 15 ч/млн Pd из водного раствора нитрата и прокаливают 1 час при 500°С. Образец подвергают старению в течение 4 час при 1000°С. Измеренная с помощью ТГА при 500°С КЕ равна 290 μмоль O2/г образца. Образец был проанализирован методом SAXS. Нормализованная интенсивность рассеяния I(Q) при Q=0,1 Å-1 равна лишь 40, как это показано на фиг.2. Зависимость нормализованной интенсивности рассеяния I(Q) от Q представлена на фиг.1. Величина поверхности равна 1 м2/г. Скорость отдачи кислорода равна 0,5 мг-О2/м2-мин. Конечная оксидная композиция содержит 60% мас. СеО2, 38% мас. ZrO2 и 2% мас. La2O3.
Сравнительный пример 2
Порошок смешанных оксидов приготовляют с использованием процедуры сравнительного примера 1 за исключением того, что свежепрокаленный образец пропитывают 1000 ч/млн Ni из раствора нитрата. Порошок после этого прокаливают в течение 1 часа при 500°С. Образец подвергают старению в течение 4 час при 1000°С. Измеренная с помощью ТГА при 500°С КЕ равна 218 μмоль О2/г образца, а нормализованная интенсивность рассеяния I(Q) при Q=0,1 Å-1 равна 46. Скорость отдачи кислорода равна 0,2 мг-O2/м2-мин.
Сравнительный пример 3
Водный раствор нитрата церия (III) приготовляют растворением 58,6 г карбоната церия (III) (49,5% оксида) в 135 г воды и 50,4 г концентрированной азотной кислоты. К раствору добавляют 110,5 г цирконил-нитрата (20% мас. оксида). Концентрация твердых материалов в конечном растворе смешанных нитратов равна 15,7% мас. К нитратному раствору добавляют 50 г 30%-ной водной перекиси водорода. В 350 г деионизированной воде при 70°С обработанный перекисью нитратный раствор подвергают совместному осаждению в емкости с 300 мл 5 н. аммиака, сохраняя температуру 70°С и рН 8,6. После добавления всего количества раствора осадок подвергают старению в течение 0,5 час при 70°С.
Осадок отфильтровывают, промывают 3 л воды при 70°С. Промытую фильтровальную лепешку повторно суспендируют в воде и сушат распылением. Высушенный порошок пропитывают 15 ч/млн Pd в виде раствора нитрата и прокаливают в течение 1 часа при 500°С с образованием продукта с величиной поверхности >100 м2/г. После старения в течение 4 час при 1000°С величина поверхности равна 17 м2/г. КЕ, измеренная с помощью ТГА в изотермических условиях при 500°С, составляет лишь 274 μмоль О2/г образца. Образец был проанализирован с использованием метода SAXS. Нормализованная интенсивность рассеяния I(Q) при Q=0,1 Å-1, измеренная методом SAXS, как показано на фиг.2, равна 152. Скорость отдачи кислорода равна 2,4 мг-О2/м2-мин.
Сравнительный пример 4
Фильтровальную лепешку из сравнительного примера 4 пропитывают перед прокаливанием 100 ч/млн Pd. КЕ, измеренная с помощью ТГА в изотермических условиях при 500°С, составляет лишь 275 μмоль О2/г образца. Нормализованная интенсивность рассеяния I(Q) при Q=0,1 Å-1, измеренная методом SAXS, равна 120. Скорость отдачи кислорода равна 4,0 мг-О2/м2-мин.
Хотя настоящее изобретение описано в различных предпочтительных вариантах, опытному специалисту понятно, что, не выходя за рамки сути изобретения, можно производить различные модификации, замещения, пропуски и изменения.
| название | год | авторы | номер документа |
|---|---|---|---|
| КАТАЛИЗАТОР ОЧИСТКИ ВОДОРОДСОДЕРЖАЩЕЙ ГАЗОВОЙ СМЕСИ ОТ СО И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ | 2007 |
|
RU2336947C1 |
| ОДНОСЛОЙНЫЙ ВЫСОКОЭФФЕКТИВНЫЙ КАТАЛИЗАТОР ДЛЯ ОЧИСТКИ ОТРАБОТАВШИХ ГАЗОВ ДВИГАТЕЛЕЙ ВНУТРЕННЕГО СГОРАНИЯ И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ (ВАРИАНТЫ) | 2001 |
|
RU2279311C2 |
| КОМПОЗИЦИИ НА ОСНОВЕ ОКСИДА ЦИРКОНИЯ, ИСПОЛЬЗУЕМЫЕ В КАЧЕСТВЕ ТРОЙНЫХ КАТАЛИЗАТОРОВ | 2016 |
|
RU2727187C2 |
| ИМЕЮЩИЙ ПОКРЫТИЕ КОМПОЗИЦИОННЫЙ МАТЕРИАЛ, СОДЕРЖАЩИЙ AlO-CeO/ZrO, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2015 |
|
RU2699652C2 |
| СМЕШАННЫЕ ОКСИДЫ НА ОСНОВЕ ЦЕРИЯ И ЦИРКОНИЯ | 2016 |
|
RU2707888C1 |
| КОМПОЗИЦИЯ НА ОСНОВЕ ЦЕРИЯ, ЦИРКОНИЯ И ВОЛЬФРАМА, СПОСОБ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ В КАТАЛИЗЕ | 2011 |
|
RU2549573C2 |
| ТРЕХФУНКЦИОНАЛЬНЫЙ КАТАЛИЗАТОР ДЛЯ ИСПОЛЬЗОВАНИЯ В ВЫХЛОПНЫХ ГАЗАХ ТРАНСПОРТНОГО СРЕДСТВА И СИСТЕМА ОЧИСТКИ ВЫХЛОПНЫХ ГАЗОВ | 2014 |
|
RU2632877C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИТОВ ИЗ ОКСИДА АЛЮМИНИЯ И СМЕШАННЫХ ОКСИДОВ ЦЕРИЯ И ЦИРКОНИЯ | 2012 |
|
RU2590162C2 |
| КАТАЛИЗАТОР, НОСИТЕЛЬ КАТАЛИЗАТОРА, СПОСОБ ИХ ПРИГОТОВЛЕНИЯ (ВАРИАНТЫ) И СПОСОБ ОЧИСТКИ ОТХОДЯЩИХ ГАЗОВ ОТ ОКСИДОВ АЗОТА | 2001 |
|
RU2199389C1 |
| КАТАЛИТИЧЕСКИЙ НЕЙТРАЛИЗАТОР И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ (ВАРИАНТЫ) | 2000 |
|
RU2262983C2 |
Настоящее изобретение относится к новым смешанным оксидам из оксида церия и оксида циркония, которые могут использоваться в качестве катализаторов или носителей катализаторов для очистки выхлопных газов двигателей внутреннего старения. Смешанный оксид обладает многофазной кубической формой кристаллизации и кислородной емкостью, по меньшей мере, 260 μмоль O2/г образца и скоростью отдачи кислорода больше 1,0 мг-О2/м2-мин, которые измеряются после сгорания в течение 4 час при 1000°С. Также заявлена подложка с покрытием, содержащая указанный смешанный оксид. Способ получения поликристаллических частиц указанного смешанного оксида церия и циркония, включает следующие стадии: i) получение раствора смешанной соли, включающего, по меньшей мере, одну соль церия и, по меньшей мере, одну соль циркония в концентрации, достаточной для образования поликристаллических частиц соответствующего сухого продукта на основе смешанного оксида, причем названные частицы имеют церий-оксидный компонент и цирконий-оксидный компонент, в которых эти компоненты распределены внутри субкристаллической структуры частиц таким образом, что каждый кристаллит в частице состоит из множества прилегающих один к другому доменов, в которых атомные отношения Ce:Zr, которыми обладают прилегающие один к другому домены, характеризуются степенью неоднородности по отношению один к другому, определяемой с помощью метода рентгеновского рассеяния под малыми углами, и выраженной нормализованной интенсивностью рассеяния I(Q) в пределах от приблизительно 47 до приблизительно 119 при векторе рассеяния Q, равном 0,10 Å-1; ii) обработку раствора смешанной соли, полученного в соответствии со стадией (i), основанием с образованием осадка; iii) обработку осадка, полученного в соответствии со стадией (ii), окислительным агентом в количестве, достаточном для окисления Се+3 до Се+4; iv) промывку и сушку остатка, полученного в соответствии со стадией (iii); и v) прокаливание высушенного осадка, полученного в соответствии со стадией (iv), в результате чего получают поликристаллические частицы оксида церия и циркония в виде смешанного оксида с указанными выше характеристиками. Технический результат - получаемый смешанный оксид обладает как высокой кислородной емкостью, так и повышенной скоростью отдачи кислорода в условиях высоких температур. 9 н. и 59 з.п.ф-лы, 2 ил.
i) получение раствора смешанной соли, включающего, по меньшей мере, одну соль церия и, по меньшей мере, одну соль циркония в концентрации, достаточной для образования поликристаллических частиц соответствующего сухого продукта на основе смешанного оксида, причем названные частицы имеют церий-оксидный компонент и цирконий-оксидный компонент, в которых эти компоненты распределены внутри субкристаллической структуры частиц таким образом, что каждый кристаллит в частице состоит из множества прилегающих один к другому доменов, в которых атомные отношения Ce:Zr, которыми обладают прилегающие один к другому домены, характеризуются степенью неоднородности по отношению один к другому, определяемой с помощью метода рентгеновского рассеяния под малыми углами и выраженной нормализованной интенсивностью рассеяния I(Q) в пределах от приблизительно 47 до приблизительно 119 при векторе рассеяния Q, равном 0,10 Å-1, причем названный смешанный оксид отличается тем, что получают частицы оксида церия и циркония с кислородной емкостью, равной, по меньшей мере, 260 мкмоль О2/г образца и скоростью отдачи кислорода больше 1 мг-O2/м2-мин, которые измеряются после старения в течение 4 ч при 1000°С;
ii) обработку раствора смешанной соли, полученного в соответствии со стадией (i), основанием с образованием осадка;
iii) обработку осадка, полученного в соответствии со стадией (ii), окислительным агентом в количестве, достаточном для окисления Се+3 до Се+4;
iv) промывку и сушку остатка, полученного в соответствии со стадией (iii); и
v) прокаливание высушенного осадка, полученного в соответствии со стадией (iv), в результате чего получают поликристаллические частицы оксида церия и циркония.
| US 5607892 А, 04.03.1997 | |||
| US 6051529 А, 18.04.2000 | |||
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| US 5693299 А, 02.12.1997 | |||
| RU 2004116469 А, 10.04.2005 | |||
| RU 96124023 А, 27.01.1999 | |||
| RU 98106633 А, 27.02.2000. | |||
Авторы
Даты
2006-10-27—Публикация
2002-02-20—Подача