Область техники, к которой относится изобретение
Настоящее изобретение относится к области медицины и, в частности, к твердым дозированным лекарственным формам для орального введения, предназначенным для лечения инсулиннезависимого диабета.
Уровень техники
Инсулиннезависимый диабет является метаболическим заболеванием, которое характеризуется гипергликемией, возникающей вследствие недостатка инсулина, невосприимчивости по отношению к инсулину и сниженной толерантностью к глюкозе.
Существуют две основные группы оральных антидиабетических лекарственных средств: сульфонилмочевины и бигуанидины. Сульфонилмочевины действуют путем стимулирования выделения инсулина, и, таким образом, они эффективны только в отношении некоторых остаточных бета-клеток поджелудочной железы. Примерами подходящих сульфонилмочевин являются глибенкламид, гликлазид, толбутамид, глипизид, толазамид, гликвидон и хлорпропамид. Бигуанидины, такие как метформин, действуют путем снижения глибенкламида и повышения периферической утилизации глюкозы, при этом, так как они требуют наличия эндогенного инсулина, они эффективны только в отношении некоторых остаточных островковых клеток поджелудочной железы.
Первоначальное лечение инсулиннезависимого диабета включает контроль за диетой и физические упражнения. Только после того как будет установлено, что они не помогают, используют оральные антидиабетические лекарственные средства, в качестве дополнения к диете, но не заменяя ее. Монотерапия с помощью орального антидиабетического лекарственного средства может быть эффективной в течение многих лет. Однако с годами ее эффективность может снижаться. Поскольку тип действия сульфонилмочевин и бигуанидинов - дополняющий, такая комбинированная терапия является сейчас общепринятой формой лечения инсулинонезависимого диабета.
Для пациента безусловно удобнее применять комбинированную таблетку (лекарственную форму). Настоящее изобретение относится к твердым дозированным лекарственным формам для орального введения, включающим комбинацию метформина и глибенкламида (называемого также глибуридом).
Комбинация метформина с глибенкламидом была описана в заявке WO 97/17975 для лечения диабета II типа при определенном соотношении двух активных ингредиентов, которое является необходимым для достижения оптимального терапевтического эффекта. В указанной ссылке определено оптимальное для лечения соотношение метформина гидрохлорида и глибенкламида 100:1, например, 500 мг глибенкламида метформина к 5 мг глибенкламида в одной дозе. Это соотношение позволяет варьировать дневные дозы путем увеличения количества таблеток, принимаемых в течение дня, что позволяет избежать неполного контроля заболевания вследствие недостаточной дозы каждого ингредиента, если необходимо их совместное введение, и исключает гипогликемию в результате передозировки каждого ингредиента при необходимости их совместного введения. Уверенность в результатах клинического использования, обусловленных свойствами продукта, обеспечивающего соответствующую биодоступность глибенкламидного компонента, - вот основное требование врачей, желающих лечить больных с помощью комбинированных препаратов. Соответствующая биодоступность означает, что 5 мг глибенкламида, включенного в состав таблетки вместе с метформином, адсорбируется примерно в такой же мере и в сопоставимой степени, что и глибенкламид, вводимый индивидуально при совместном дозировании с монокомпонентным составом, включающим метформин.
В предшествующем уровне, однако, не раскрыто, как составить композицию из метформина и глибенкламида, обеспечивающую необходимую биодоступность глибенкламидного компонента. В этом отношении применительно к гидрохлориду метформина не возникает проблем в связи с его высокой растворимостью в воде, и потому биодоступность метформина в различных композициях в дальнейшем не обсуждается. Однако в отношении глибенкламида возникают значительные трудности, поскольку он является плохо растворимым лекарственным средством (растворимость в воде - 0,1 мг/мл при 25°С, практически нерастворимо по определению USP).
Сама по себе скорость его растворения после введения твердой дозированной формы будет влиять на скорость и меру поступления лекарства в кровь (биодоступность). Контроль за скоростью и мерой поступления в кровеносное русло весьма важен для обеспечения соответствующего терапевтического эффекта.
Следовательно, в указанном источнике раскрыто подходящее соотношение между двумя активными ингредиентами в единичной дозированной форме для того, чтобы смоделировать, как два индивидуальных ингредиента могут быть совместно введены (основываясь на том, как их следует дозировать согласно обычно принятой практике применения пригодных в настоящее время единичных реально существующих составов), при этом не объясняется, как гарантировать, что такой состав будет обеспечивать биодоступность глибенкламида. Эта биодоступность должна быть, по возможности, аналогичной той, которая имеет место при совместном введении соответствующих доз двух отдельных моносоставов каждого вещества.
Кроме того, при сравнении комбинированного препарата с помощью стандартных галеновых методов со стандартным глибенкламидом пониженная биодоступность по сравнению с индивидуальным введением была очевидна.
В настоящее время на основе опытов in vitro и in vivo установлено, что пониженная биодоступность глибенкламида связана с размером его частиц и распределением размера частиц. Установлено, что частицы, которые слишком малы, обуславливают высокие уровни глибенкламида в крови с последующим риском возникновения гипогликемии, а частицы, которые слишком велики, не могут достаточно быстро раствориться, чтобы обеспечить необходимую биодоступность. Следовательно, необходимо иметь четко определенное распределение размера частиц глибенкламида в композиции.
Выбор фракции частиц глибенкламида с определенным размером обеспечивает возможность получения твердой дозированной лекарственной формы для орального введения, включающей комбинацию метформина и глибенкламида, в частности, таблетку, в которой биодоступность глибенкламида сопоставима с биодоступностью, обеспечиваемой при раздельном введении метформина и глибенкламида, судя по площади под кривой в анализе in vivo.
Сущность изобретения
Настоящее изобретение касается, в частности, таблетки, включающей комбинацию метформина и глибенкламида, в которой биодоступность глибенкламида сопоставима с биодоступностью совместно вводимых таблеток.
В первом воплощении настоящее изобретение включает твердую дозированную лекарственную форму для орального введения, такую как таблетка, содержащая композицию из глибенкламида и метформина, в которой размер частиц глибенкламида таков, что не более 10% частиц имеют размер менее 2 μм и не более 10% частиц имеют размер более 60 μм. Предпочтительно, размер частиц глибенкламида таков, что не более 10% частиц имеют размер менее 3 μм и не более 10% частиц имеют размер более 40 μм. Этот специфический диапазон размера частиц глибенкламида может быть получен просеиванием сквозь сито или воздухоструйным измельчением.
Во втором воплощении настоящее изобретение включает твердую дозированную лекарственную форму для орального введения, включающую композицию из метформина и глибенкламида, в которой размер частиц глибенкламида таков, что не более 25% частиц имеют размер менее 11 μм и не более 25% частиц имеют размер более 46 μм.
Предпочтительно, 50% частиц имеют размер менее 23 μм.
Метформин может быть использован в форме его соли, например, гидрохлорида, фумарата, гидробромида, п-хлорфеноксиацетата или эмбоната. Весовое соотношение соли метформина к глибенкламиду предпочтительно должно составлять от 50/1 до 250/1.
Предпочтительные композиции дозированной формы для орального введения приведены ниже в таблице 1 с указанием диапазона концентраций компонентов:
Состав предпочтительных композиций по изобретению
Состав наиболее предпочтительных композиций по изобретению
Таблетка, согласно изобретению, может быть получена способом, включающим:
a) образование гранул влажным гранулированием смеси метформина и глибенкламида,
b) смешивание гранул с таблетирующей добавкой и разбавителем,
c) таблетирование смеси с получением таблеток.
Предпочтительно, смесь, используемая для образования гранул, содержит гранулирующее связующее. Таким гранулирующим связующим является, в частности, поливинилпирролидон, например, поливинилпирролидон с молекулярной массой 45000. Поливинилпирролидон может использоваться в количестве от 2 до 4% по весу по отношению к конечному продукту - таблетка.
После стадии гранулирования гранулы могут быть просеяны через сито и высушены.
Гранулы затем смешивают с разбавителем (наполнителем) и таблетирующей добавкой. Разбавителем может служить любой материал, используемый обычно для изготовления таблеток, например, микрокристаллическая целлюлоза. Таблетирующей добавкой может служить любой материал, используемый обычно для изготовления таблеток, например, стеарат магния.
Полученные таким образом таблетки могут иметь покрытие из гидрофильного полимера на основе целлюлозы и талька. Гидрофильный полимер на основе целлюлозы может быть 2-гидроксипропилметилцеллюлозой.
Сведения, подтверждающие возможность осуществления изобретения
Следующие примеры и тесты иллюстрируют настоящее изобретение.
Пример 1
Таблетки из метформина/глибенкламида получали следующим образом:
66,6 г поливинилпиролидона смешивали с 246 г очищенной воды при перемешивании 1500 г гидрохлорида метформина, 7, 5 г глибенкламида (10-90% имели размер частиц от 2 до 60 μм), 42 г натрийкроскармелозы и 284,4 г микрокристаллической целлюлозы смешивали в грануляторе. Раствор поливинилпирролидона добавляли в гранулятор и сырую массу гранулировали. Гранулы подвергали экструзии через 1 мм меш. Гранулы загружали в предварительно нагретую сушилку с движущимся слоем и высушивали 97,5 г микрокристаллической целлюлозы смешивали с гранулами с помощью смесителя барабанного типа. 12 г стеарата магния добавляли в барабанный смеситель и смешивали. Смесь для гранул таблетировали подходящим таблетирующим прессом. На таблетки наносили покрытие из 2% гидроксипропилметилцеллюлозы с помощью специального устройства для нанесения покрытий.
Пример 2
Таблетки из метформина/глибенкламида получали следующим образом:
5,83 г глибенкламида (10-90% имеют размер частиц от 2 до 60 μм) предварительно смешивали с 32,67 г натрий-кроскармелозы. 46,67 г поливинилпирролидона смешивали с 93,33 г очищенной воды при перемешивании. Смесь глибенкламида и натрий-кроскармелозы смешивали с 1166,6 г гидрохлорида метформина в грануляторе. Раствор поливинилпирролидона добавляли в гранулятор и влажную массу гранулировали. Гранулы загружали в предварительно нагретую сушилку с движущимся слоем и высушивали их. Размер частиц гранул уменьшали, просеивая их через 1 мм меш, 131,83 г микрокристаллической целлюлозы смешивали с гранулами в грануляторе. 16,3 г стеарата магния добавляли в гранулятор и смешивали. Смесь гранул таблетировали с помощью подходящего таблетирующего пресса. На таблетки наносили покрытие из 2% гидроксипропилметилцеллюлозы с помощью специального устройства.
Тест 1
Тесты in vivo на биодоступность проводили с таблетками, приготовленными, как описано в Примере 2, используя две партии глибенкламида. Две партии (10-90%) имели следующие размеры частиц:
Распределение размера частиц партий А и В показано на фиг.1.
Две партии таблеток назначали здоровым пациентам при сравнении с совместным индивидуальным введением глибенкламида (торговая марка Daonil) и гидрохлорида метформина (16 пациентов в каждой группе).
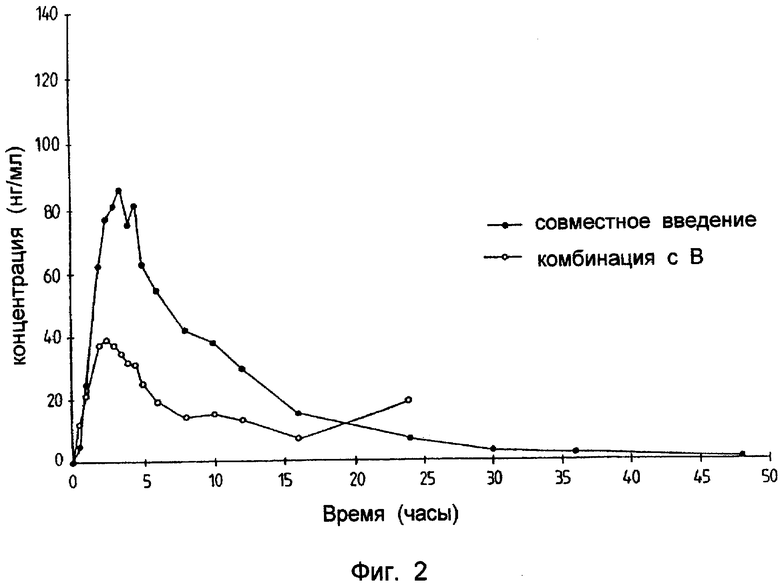
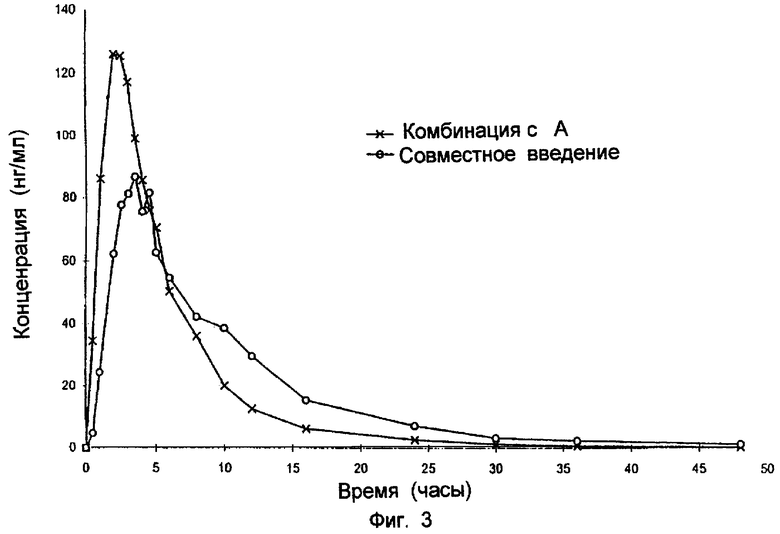
Концентрация глибенкламида при введении в таблетку, включающую комбинацию метформина и глибенкламида, из партии А и В, в сравнении с совместным назначением двух индивидуальных таблеток приведены на фиг.2 и 3 соответственно.
Как оказалось, значение AUC для комбинированных таблеток, полученных с партией А, примерно такая же, как и в случае совместного введения индивидуальных таблеток, в то время как AUC для комбинирования таблеток с партией В существенно отличается.
Тест 2
Тщательное изучение содержания глибенкламида в крови людей после назначения серий таблеток гидрохлорида метформина, скомбинированного с глибенкламидом (обозначенных как составы Combo 1, 2, 3 и 4), состав которых идентичен, кроме характеристик размеров частиц используемого глибенкламида, сопоставим с коммерчески доступными известными составами гидрохлорида метформина (Glucophage™, Bristol-Myers Squibb) и глибенкламида (Micronase Upjohn), дозируемыми совместно, позволили определить характеристики частиц глибенкламида, которые позволят гарантировать соответствующую биодоступность глибенкламидного компонента в составе композиции. Это означает, что контроль за заболеванием, когда больных впервые лечат такой композицией, будет предсказуемым, основанным на предварительном знании врача о лечебном эффекте применения любого отдельного лекарственного средства.
Или же, если у пациентов предварительно стабилизировано заболевание путем дополнительного лечения коммерческим продуктом типа Micronase™ до основного лечения Glucophage™ (или наоборот), то изменение направления в сторону более привычного лечения композицией в виде единичной таблетки (когда соответствующая биодоступность глибуридного компонента гарантирована) приведет к тому, что желаемый уровень контроля за заболеванием будет сохранен.
Данные, полученные в результате изучения таблеток гидрохлорида метформина и глибенкламида, полученных с использованием различных по размеру частиц глибенкламида, позволили выявить корреляцию между размерами частиц лекарственного средства и его действием in vivo.
Свойства различных глибенкламидов, использованных в различных комбинированных таблетках, приведены в таблице 3:
Распределение размера частиц глибенкламида в различных партиях таблеток
При приготовлении четырех композиционно-идентичных партий таблеток гидрохлорида метформина - глибенкламида 500/2,5 мг с использованием глибенкламида с указанным распределением размера частиц и введении их больным были получены следующие фармакокинетические характеристики путем исследования динамики изменения концентрации глибенкламида во времени (таблица 4).
Фармакокинетические характеристики глибенкламида
Была обнаружена приемлемая корреляция между размерами частиц и максимальной средней геометрической концентрацией глибенкламида в плазме (Смах), а также площадью среднего геометрического под кривой, показывающей изменение концентрации глибенкламида в плазме во времени AUC.
Исходя из этих корреляций, расчетные размеры частиц глибенкламида, которые обеспечивают предполагаемые величины Смах и AUC ±25% среднего значения для партий указанного состава глибенкламида, Micronase™, используемой в исследованиях in vivo, имеют значения, приведенные в табл.5.
Расчетные размеры частиц глибенкламида, полученные на основе Смах И AUC
С учетом двух величин Смах и AUC получают следующие возможности пределы (табл.6)
Расчетные размеры частиц
Глибенкламид с такими характеристиками размеров частиц имеет величину площади поверхности порошка 1,7-2,2 м2/г, что было определено с помощью метода азотной адсорбции. Поэтому использование в композиции глибенкламида с указанными свойствами по изобретению отличается от глибенкламида, описанного в патенте US 3979520, в котором используется глибенкламид с площадью поверхности порошка более 3 м2/г (предпочтительно 5-10 м2/г) для обеспечения соответствующей биодоступности глибенкламида. При введении в состав композиции описанным путем глибенкламида (со свойственным ему размером частиц), по изобретению, обеспечивается необходимая биодоступность глибенкламида для больных согласно описанному ниже.
Тест 3
Партию таблеток гидрохлорид метформина/глибенкламид 500/5 мг готовили следующим образом.
Глибенкламид (1,0 кг) с указанным выше размером частиц смешивали в смесителе барабанного типа с 2,8 кг натрийкроскармелозы, и эту смесь затем перемешивали в высокоскоростном смесителе с гидрохлоридом метформина (100 кг), к которому было добавлено 0, 5 вес.% стеарата магния.
Эту сухую смесь подвергали влажному гранулированию в высокоскоростном смесителе с 12,1 кг водного раствора повидона (содержащего 4 кг повидона). Влажные гранулы высушивали в сушилке с движущимся слоем при 60°С до необходимой влажности. Высушенные гранулы (потери веса при высушивании 2-3%) были отсеяны с помощью вибратора (проем сита 1,0 мм), затем перемешаны в смесителе барабанного типа с 18,0 кг микрокристаллической целлюлозы и затем с 0,9 кг любриканта - стеарата магния. Обработанные любрикантом гранулы прессовали с помощью устройства, прессующего капсулы размером 16×8 мм, на сердцевинки таблеток наносили пленочное покрытие (увеличение веса составляло примерно 2 вес.%/вес) из материала Opadry 32920 с получением в конце концов желтых капсулообразных таблеток. При фармакокинетическом исследовании, проводимом на людях, каждому добровольцу назначали либо одну из этих таблеток, либо две таблетки, содержащие 500 мг Glucophage™ и 5 мг Micronase™ соответственно. После введения лекарств определяли содержание глибенкламида в плазме. Полученные результаты приведены в табл.7.
Фармакокинетические параметры при введении глибенкламида в виде комбинированной и индивидуальной таблеток
Биодоступность глибенкламида при введении в виде комбинированной таблетки сравнима с биодоступностью при введении в виде индивидуальной таблетки (таблетки сравнения) Micronase™. Полученные данные подтверждают, что больные смогут принимать одну таблетку комбинированного состава вместо двух индивидуальных таблеток, принимаемых в настоящее время совместно, без опасения, что концентрация глибенкламида в крови будет низкая, что возможно при применении уже известных составов и может приводить к утрате контроля за заболеванием.
Пример 3
Вместо прессования таблеток согласно тесту 3 гранулами заполняли капсулы размером 00, дозируя в каждую гидрохлорид метформина/глибенкламид в соотношении 500/5 мг или 500/2,5 мг. Аналогично заполняли капсулы размера 1, чтобы обеспечить соотношение 250 мг/2,5 мг.
Также капсулы обеспечивали приемлемый лечебный эффект и могут представлять собой альтернативу таблеткам. Следует отметить, что составы, описанные в WO 97/17975, нельзя поместить в капсулы приемлемого для пациентов размера вследствие большой массы носителей, применяемых для этих составов.
| название | год | авторы | номер документа |
|---|---|---|---|
| ТВЕРДАЯ ДОЗИРОВАННАЯ ЛЕКАРСТВЕННАЯ ФОРМА ДЛЯ ОРАЛЬНОГО ПРИМЕНЕНИЯ, СОДЕРЖАЩАЯ КОМБИНАЦИЮ МЕТФОРМИНА И ГЛИБЕНКЛАМИДА | 1999 |
|
RU2226396C2 |
| ТВЕРДАЯ ДОЗИРОВАННАЯ ЛЕКАРСТВЕННАЯ ФОРМА ДЛЯ ЛЕЧЕНИЯ САХАРНОГО ДИАБЕТА | 2006 |
|
RU2333760C2 |
| КОМБИНАЦИЯ ДЛЯ ЛЕЧЕНИЯ САХАРНОГО ДИАБЕТА И ЕГО ОСЛОЖНЕНИЙ | 2011 |
|
RU2451506C1 |
| ПЕРОРАЛЬНАЯ ДОЗИРОВАННАЯ ФОРМА ГАБАПЕНТИНА ЗАМЕДЛЕННОГО ВЫСВОБОЖДЕНИЯ | 2005 |
|
RU2440112C2 |
| СПОСОБ ЛЕЧЕНИЯ ДИАБЕТА | 2000 |
|
RU2275915C2 |
| КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ГЛИБУРИД | 2001 |
|
RU2244707C2 |
| ПРЕПАРАТ ЛАМОТРИДЖИН С КОНТРОЛИРУЕМЫМ ВЫСВОБОЖДЕНИЕМ | 2003 |
|
RU2328274C2 |
| АНТИДИАБЕТИЧЕСКИЙ ПРЕПАРАТ И СПОСОБ ЛЕЧЕНИЯ ДИАБЕТА | 2000 |
|
RU2276604C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ АНТАГОНИСТ МИНЕРАЛОКОРТИКОИДНЫХ РЕЦЕПТОРОВ, И ЕЕ ПРИМЕНЕНИЕ | 2017 |
|
RU2725153C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ МЕТФОРМИНА С ДЛИТЕЛЬНЫМ ВЫСВОБОЖДЕНИЕМ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2006 |
|
RU2433821C2 |
Изобретение относится к медицине и лекарственным средствам, а именно к композициям для лечения инсулиннезависимого сахарного диабета типа 2, представляющим собой однократную твердую дозированную лекарственную форму для орального введения и содержащим эффективную дозу метформина и эффективную дозу глибенкламида, а также к способу лечения инсулиннезависимого диабета или гипергликемии, к способу обеспечения биодоступности глибенкламида в организме человека (варианты), а также к способу повышения биодоступности глибенкламида в организме человека (варианты), причем входящий в состав указанных однократных твердых дозированных лекарственных форм для орального введения глибенкламид имеет площадь поверхности порошка частиц от 1,7 до 2,2 м2/г. Настоящее изобретение обеспечивает биодоступность глибенкламида в составе комбинированных с метформином лекарственных форм, сопоставимую с биодоступностью моносоставов глибенкламида. 6 н. и 62 з.п. ф-лы, 7 табл., 3 ил.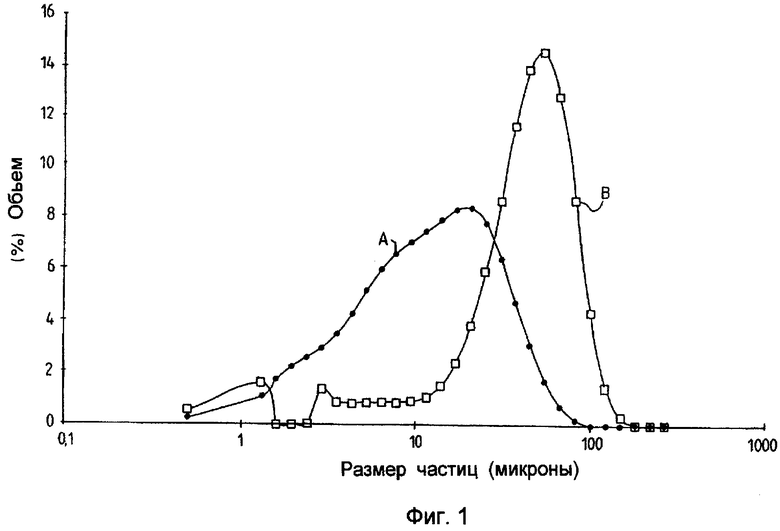
a) образование гранул влажным гранулированием смеси метформина и глибенкламида,
b) смешивание гранул с таблетирующей добавкой или разбавителем, и
c) таблетирование смеси с получением таблеток.
a) образование гранул влажным гранулированием смеси метформина и глибенкламида,
b) смешивание гранул с таблетирующей добавкой и разбавителем, и
c) таблетирование смеси с получением таблеток.
a) образование гранул влажным гранулированием смеси метформина и глибенкламида,
b) смешивание гранул с таблетирующей добавкой и разбавителем, и
c) таблетирование смеси с получением таблеток.
a) образование гранул влажным гранулированием смеси метформина и глибенкламида,
b) смешивание гранул с таблетирующей добавкой и разбавителем, и
c) таблетирование смеси с получением таблеток.
| WO 9717975 A1 (GENTILI 1ST SPA; BARELLI GIULIO; REGIS MASSIMO DE), 22.05.1997 | |||
| US 3979520 A (BOEHRINGER MANNHEIM GMBH), 07.09.1976 | |||
| VIGNERI R | |||
| et al | |||
| Treatment of NIDDM patients with secondary failure to glyburide: comparison of the addition of either metformin or bed-time NPH insulin to glyburide | |||
| - Diabete Metab | |||
| Циркуль-угломер | 1920 |
|
SU1991A1 |
| GR | |||
Авторы
Даты
2006-11-10—Публикация
1999-07-12—Подача