Настоящее изобретение относится к соединениям общей формулы
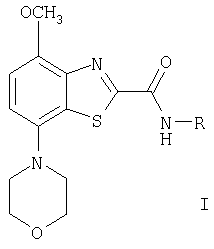
где
R означает водород,
-(СН2)n-фенил, необязательно замещенный заместителем ряда галоген, (низш.)алкил, (низш.)алкокси, трифторметил или -N(R')-С(O)-(низш.)алкил,
-(СН2)n-пиридинил, необязательно замещенный (низш.)алкилом,
-(СН2)n-С3-С6циклоалкил, необязательно замещенный гидроксигруппой,
-(СН2)n-N(R')-С3-С6циклоалкил, необязательно замещенный гидроксигруппой,
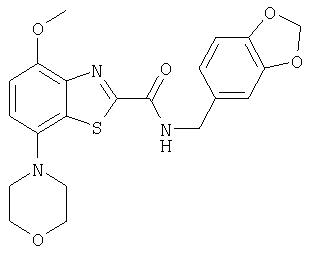
-(СН2)n-бензо[1,3]диоксолил,
-(CR'2)n-тиофенил, необязательно замещенный (низш.)алкилом,
-(CR'2)n-тиазолил, необязательно замещенный (низш.)алкилом,
-(СН2)n-С(O)-тиофенил, необязательно замещенный галогеном,
-(CH2)n-фуранил, необязательно замещенный (низш.)алкилом,
-(СН2)n-С(O)-(СН2)n-тиофенил,
-(CHR')n-бензофуран-2-ил,
-(СН2)n-бензо[b]тиофенил, необязательно замещенный (низш.)алкилом,
-(СН2)n-N(R')-С(O)-фенил, необязательно замещенный галогеном или (низш.)алкокси,
-(СН2)n-С(O)-фенил, необязательно замещенный (низш.)алкокси,
-(СН2)n-С(O)-2,3-дигидробензо[1,4]диоксин-6-ил,
-(CH2)n-N(R')-С(O)-пиридинил,
-(CH2)n-тетрагидрофуранил,
-СН-бифенил,
-СН-(фенил)пиридинил,
-(СН2)n-1-оксо-1,3-дигидроизоиндол-2-ил,
-(СН2)n-1,3-диоксо-1,3-дигидроизоиндол-2-ил,
-(СН2)n-СН-(фенил)тетрагидропиранил,
-(СН2)n-1-оксо-1,2,3,4-тетрагидроизохинолин-3-ил или
-(СН2)n-S-[1,3,4]тиазол-2-ил, необязательно замещенный аминогруппой,
R' означает водород или (низш.)алкил, независимо друг от друга в случае R'2, a n равно 0, 1, 2, 3 или 4, или к их фармацевтически приемлемым кислотно-аддитивным солям.
Неожиданно было установлено, что соединения общей формулы I являются лигандами рецептора аденозина. Более подробно соединения по настоящему изобретению обладают высоким сродством к рецептору А2А и высокой селективностью к рецепторам A1 и А3.
Аденозин модулирует широкий спектр физиологических функций благодаря взаимодействию с поверхностными рецепторами специфических клеток. Возможность использования рецепторов аденозина в качестве мишеней лекарственных средств впервые была описана в 1982 г. В структурном и метаболическом отношении аденозин близок биоактивным нуклеотидам: аденозинтрифосфату (АТФ), аденозиндифосфату (АДФ), аденозинмонофосфату (АМФ) и циклическому аденозинмонофосфату (цАМФ), биохимическому метилирующему агенту S-аденозил-L-метионину (SAM), а в структурном отношении близок коферментам НАД, ФАД и коферменту А, а также РНК. Аденозин и указанные родственные соединения выполняют важные функции в регуляции многих аспектов клеточного метаболизма и в модуляции различных типов активности ЦНС.
Рецепторы аденозина подразделяются на рецепторы A1, А2A, А2B и А3, принадлежащие к семейству рецепторов, сопряженных с G-белками. Активация рецепторов аденозина инициирует механизм передачи сигнала. Эти механизмы зависят от G-белка, ассоциированного с рецептором. Каждый из подвидов аденозиновых рецепторов, как правило, характеризуется аденилатциклазной эффекторной системой, использующей в качестве вторичного мессенджера цАМФ. Рецепторы A1 и А3, сопряженные с Gi-белками, ингибируют аденилатциклазу, что приводит к снижению внутриклеточного уровня цАМФ, в то время как рецепторы A2A и А2B сопряжены с GS-белками и активируют аденилатциклазу, что приводит к повышению внутриклеточного уровня цАМФ. Установлено, что система рецептора A1 включает активацию фосфолипазы С и модуляцию ионных калиевых и кальциевых каналов. Подвид рецептора А3 кроме связывания с аденилатциклазой стимулирует также фосфолипазу С и таким образом активирует ионные кальциевые каналы.
В настоящее время клонирован рецептор A1 (326-328 аминокислотных остатков) многих видов (псовых, человека, крысы, собаки, цыпленка, крупного рогатого скота, морских свинок), причем 90-95% аминокислотной последовательности оказалась идентичной у многих видов млекопитающих. Кроме того, клонирован рецептор A2A (409-412 аминокислотных остатков) псовых, крысы, человека, морских свинок и мыши. Клонирован также рецептор A2B (332 аминокислотных остатка) человека и мыши, причем рецептор A2B человека на 45% гомологичен рецепторам A1 и А2A человека. Клонирован также рецептор А3 (317-320 аминокислотных остатков) человека, крысы, собаки, кролика и овцы.
Предполагается, что подвиды рецептора А1 и А2А играют комплементарные роли в регуляции аденозином процесса выработки энергии. Аденозин, который является продуктом метаболической трансформации АТФ, диффундирует из клетки и действует на местном уровне, активируя аденозиновые рецепторы, которые стимулируют снижение потребности в кислороде (A1) или увеличение обеспечения кислородом (А2A) и, таким образом, регулируя равновесие между выработкой энергии и ее потребностью в тканях. Результатом действия обоих подвидов рецепторов является увеличение количества кислорода, доступного тканям, и защита клеток от повреждения, вызванного кратковременным дисбалансом в поступлении кислорода. Одной из важных функций эндогенного аденозина является предупреждение повреждения во время травм, таких как гипоксия, ишемия, гипотензия и эпилептический припадок.
Кроме того, установлено, что связывание агониста аденозинового рецептора с тучными клетками, экспрессирующими рецептор А3 крысы, приводит к увеличению концентраций инозиттрифосфата и внутриклеточного кальция, что вызывает антиген-индуцированную секрецию медиаторов воспалительного процесса. Следовательно, рецептор А3 принимает участие в опосредовании приступов астмы и других аллергических ответных реакций.
Аденозин является нейромодулятором, способным модулировать многие аспекты физиологической функции мозга. Эндогенный аденозин, центральное связующее звено между метаболизмом энергии и нейронной активностью, изменяется в зависимости от поведенческого статуса и (пато)физиологических состояний. В условиях повышенной потребности и ограниченного поступления энергии (таких, как гипоксия, гипогликемия и/или избыточная нейронная активность) аденозин обеспечивает эффективный защитный механизм обратной связи. Взаимодействие с аденозиновыми рецепторами представляет собой перспективную мишень для терапевтического вмешательства при ряде неврологических и психиатрических заболеваний, таких как эпилепсия, нарушения сна, нарушение опорно-двигательного аппарата (болезнь Паркинсона или Гентингтона), болезнь Альцгеймера, депрессия, шизофрения или наркомания. Увеличение высвобождения нейромедиаторов происходит при травмах, таких как гипоксия, ишемия и эпилептические припадки. Наконец, эти нейромедиаторы отвечают за дегенерацию нервной ткани и гибель нейронов, что приводит к повреждению мозга или летальному исходу. Следовательно, агонисты рецептора A1, которые имитируют ингибирующее действия аденозина на клетки центральной нервной системы, могут применяться в качестве нейропротективных агентов. Предполагается, что аденозин является эндогенным противосудорожным агентом, ингибирующим высвобождение глутамата из возбужденных нейронов и ингибирующим воспаление нейронов. Следовательно, агонисты аденозина можно использовать в качестве противоэпилептических агентов. Антагонисты аденозина стимулируют активность ЦНС и являются эффективными в качестве усилителей познавательной способности. Селективные антагонисты А2a обладают терапевтическим действием при лечении различных форм слабоумия, например, болезни Альцгеймера, и нейродегенеративных состояний, например, инсульта. Антагонисты аденозинового рецептора А2a модулируют активность стриарных ГАБАэргических нейронов и управляют спокойными и координированными движениями, открывая таким образом возможность лечения симптомов болезни Паркинсона. Кроме того, аденозин принимает участие в ряде физиологических процессов, включающих воздействие седативного средства, гипноз, шизофрению, тревогу, боль, дыхание, депрессию и привыкание к наркотическим средствам (амфетамину, кокаину, опиоидам, этанолу, никотину, каннабиноидам). Следовательно, лекарственные средства, действующие на аденозиновые рецепторы, также обладают лечебным действием в качестве седативных средств, мышечных релаксантов, антипсихотических средств, транквилизаторов, анальгетиков, стимуляторов дыхания, антидепрессантов и средств для лечения токсикомании. Кроме того, они могут использоваться при лечении ADHD (гиперактивное состояние в связи с недостаточностью внимания).
Важной функцией аденозина в сердечно-сосудистой системе является его кардиопротективное действие. Уровень эндогенного аденозина увеличивается в ответ на ишемию и гипоксию, а также обеспечивает защиту сердечной ткани во время и после травмы (предварительная обработка). При воздействии на рецептор А1 агонисты рецептора A1 могут защитить от повреждения, вызванного ишемией миокарда и реперфузией. Модулирующее влияние рецепторов А2a на адренергическую функцию может иметь значение для множества нарушений, таких как ишемическая болезнь сердца и сердечная недостаточность. Антагонисты рецептора А2a могут оказывать лечебное действие в случаях, при которых требуется усиленный антиадренергический ответ, таких как острый приступ ишемии миокарда. Селективные антагонисты рецептора A2a могут также повысить эффективность аденозина при подавлении суправентрикулярной экстрасистолии.
Аденозин модулирует многие аспекты функции почек, включая высвобождение ренина, скорость гломерулярной фильтрации и почечный кровоток. Соединения, которые являются антагонистами действия аденозина на почки, можно использовать в качестве почечных защитных агентов. Кроме того, антагонисты А3 и/или А2B могут применяться при лечении астмы и других аллергических ответных реакций или при лечении сахарного диабета и ожирения.
Современная информация об аденозиновых рецепторах приводится, например, в следующих публикациях:
Bioorganic & Medicinal Chemistry, 6, 619-641 (1998),
Bioorganic & Medicinal Chemistry, 6, 707-719 (1998),
J. Med. Chem., 41, 2835-2845 (1998),
J. Med. Chem., 41, 3186-3201 (1998),
J. Med. Chem., 41, 2126-2133 (1998),
J. Med. Chem., 42, 706-721 (1999),
J. Med. Chem., 39, 1164-1171 (1996),
Arch. Pharm. Med. Chem., 332, 39-41 (1999),
Am. J. Physiol, 276, H1113-1116 (1999) или
Naunyn Schmied, Arch. Pharmacol, 362, 375-381 (2000).
Объектами настоящего изобретения являются соединения формулы I, применение соединений формулы I и их фармацевтически приемлемых солей для получения лекарственных средств, предназначенных для лечения заболеваний, опосредованных рецептором аденозина А2, способы получения указанных соединений, лекарственные средства на основе соединений по изобретению и их получение, а также применение соединений формулы I для лечения или профилактики заболеваний, связанных с модуляцией аденозиновой системы, таких как болезнь Альцгеймера, болезнь Паркинсона, болезнь Гентингтона, нейрозащитное действие, шизофрения, тревога, боль, нарушения дыхания, депрессия, привыкание к наркотическим средствам (таким, как амфетамин, кокаин, опиоиды, этанол, никотин, каннабиноиды), астма, аллергические ответные реакции, гипоксия, ишемия, эпилептический припадок и токсикомания. Кроме того, соединения по настоящему изобретению могут применяться в качестве седативных средств, мышечных релаксантов, антипсихотических средств, противоэпилептических средств, противосудорожных средств и кардиопротективных агентов при таких заболеваниях, как ишемическая болезнь сердца и сердечная недостаточность. Наиболее предпочтительными показаниями по настоящему изобретению являются показания, основанные на антагонистическом действии на рецептор аденозина А2A и включающие нарушения центральной нервной системы, например, лечение или профилактика болезни Альцгеймера, некоторых депрессивных состояний, токсикомании, нейрозащитное действие, болезнь Паркинсона и ADHD.
Термин "(низш.)алкил", используемый в тексте заявки, означает насыщенную алкильную группу с прямой или разветвленной цепью, содержащую от 1 до 6 атомов углерода, например, метил, этил, пропил, изопропил, н-бутил, изобутил, 2-бутил, трет-бутил и т.п. Предпочтительными (низш.)алкильными группами являются группы, содержащие 1 -4 атома углерода.
Термин "галоген" означает хлор, иод, фтор и бром.
Термин "(низш.)алкокси" означает группу, в которой алкильный остаток имеет значения, указанные выше, и которая присоединена через атом кислорода.
Термин "фармацевтически приемлемые кислотно-аддитивные соли" означает соли неорганических и органических кислот, таких как хлористоводородная кислота, азотная кислота, серная кислота, фосфорная кислота, лимонная кислота, муравьиная кислота, фумаровая кислота, малеиновая кислота, уксусная кислота, янтарная кислота, винная кислота, метансульфоновая кислота, пара-толуолсульфоновая кислота и т.п.
Предпочтительными соединениями по настоящему изобретению являются соединения формулы I, в которых R означает водород, например следующее соединение:
амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты.
Кроме того, предпочтительными соединениями формулы I, являются соединения, в которых R означает -(СН2)n-фенил, необязательно замещенный галогеном, (низш.)алкокси или (низш.)алкилом, например, следующие соединения:
фенетиламид4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
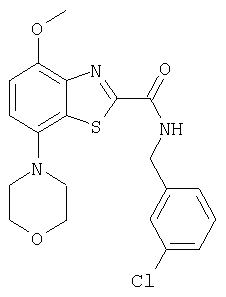
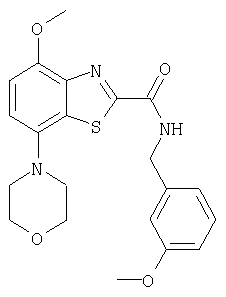
3-хлорбензиламид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
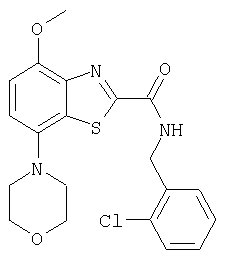
2-хлорбензиламид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
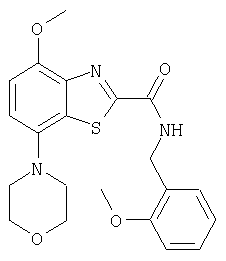
2-метоксибензиламид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
[2-(2-метоксифенил)этил]амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
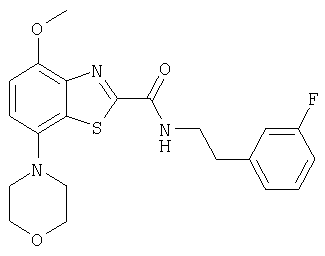
[2-(3-фторфенил)этил]амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
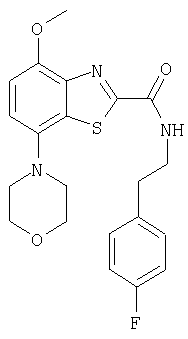
[2-(4-фторфенил)этил]амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
[2-(4-хлорфенил)этил]амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
[2-(2-хлорфенил)этил]амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
[2-(3-метоксифенил)этил]амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
[2-(3-хлорфенил)этил]амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты или
(2-мета-толилэтил)амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты.
Кроме того, предпочтительными являются такие соединения, в которых R означает -(СН2)n-пиридинил, например, следующие соединения:
пиридин-3-иламид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
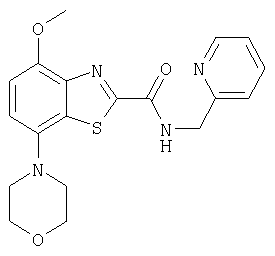
(пиридин-2-илметил)амид4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты или
(2-пиридин-3-илэтил)амид4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты.
Кроме того, предпочтительными являются соединения, в которых R означает -(CHR')n-тиофенил или -(СН2)n-С(O)-тиофенил, необязательно замещенный галогеном, например, следующие соединения:
(2-тиофен-2-илэтил)амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
(2-тиофен-3-илэтил)амид4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
[2-(3-хлортиофен-2-ил)-2-оксоэтил] амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты или
(1-метил-2-тиофен-2-илэтил)амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты.
Кроме того, предпочтительной группой соединений являются такие соединения, в которых R означает -(CHR')n-тиазолил, необязательно замещенный (низш.)алкилом, например, следующее соединение: [1-(4-метилтиазол-2-ил)этил]амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты.
Указанные соединения формулы I и их фармацевтически приемлемые соли получают известными методами, например, описанным ниже способом, который включает
а) взаимодействие соединения формулы
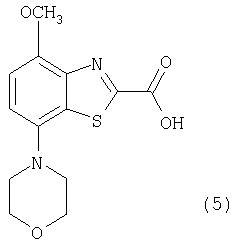
с соединением формулы

с образованием соединения формулы
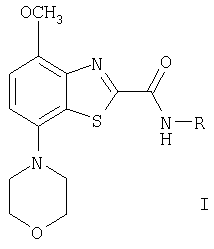
где R имеет значения, указанные выше, или
б) циклизацию соединения формулы
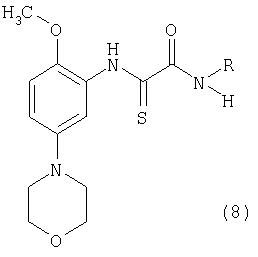
с образованием соединения формулы
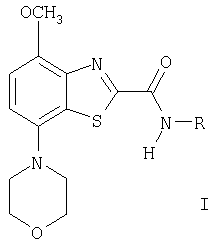
где R имеет значения, указанные выше, и
при необходимости превращение полученных соединений в фармацевтически приемлемые кислотно-аддитивные соли.
Соединения формулы I получают по вариантам способа а) и б), как показано на схемах 1 и 2. Кроме того, получение 84 соединения по изобретению более подробно описано в примерах.
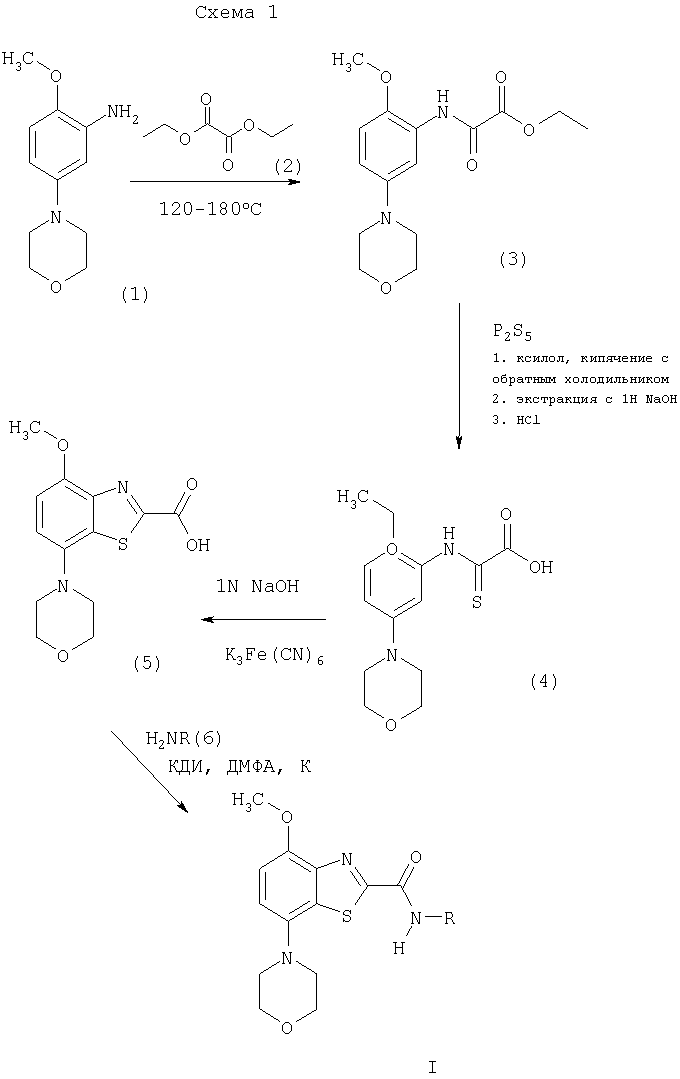
На схеме 1 R имеет значения, указанные выше, a CDI означает 1,1'-карбонилдиимидазол.
Получение исходного соединения формулы (1) описано в WO 01/97786.
По схеме 1 соединения формулы I получают, как описано ниже.
Диэтиловый эфир щавелевой кислоты (2) нагревают до приблизительно 120°С, очень осторожно небольшими порциями добавляют 2-метокси-5-морфолин-4-илфениламин (1) и нагревают при приблизительно 180°С в течение 90 мин. Затем смесь охлаждают до комнатной температуры, фильтруют и добавляют н-гексан. Полученный осадок отделяют фильтрованием, промывают гексаном и высушивают, при этом получают этиловый эфир N-(2-метокси-5-морфолин-4-илфенил)оксаминовой кислоты (3). Затем к полученному соединению формулы (3) в кипящем ксилоле в течение приблизительно 30 мин небольшими порциями добавляют пентасульфид фосфора, кипятят с обратным холодильником в течение 5 мин, охлаждают до комнатной температуры и фильтруют. Раствор экстрагируют 1н. NaOH, водную фазу промывают толуолом, фильтруют и при 0-5°С добавляют конц. соляную кислоту до рН 1. Осадок отделяют фильтрованием, при этом получают (2-метокси-5-морфолин-4-илфениламино)тиоксоуксусную кислоту (4).
К раствору феррицианида калия в воде добавляют раствор (2-метокси-5-морфолин-4-илфениламино)тиоксоуксусной кислоты (4) в 1н. NaOH, поддерживая температуру не выше 10°С. Смесь перемешивают при 10°С в течение 3 ч и добавляют конц. соляную кислоту до рН 1. Осадок отделяют фильтрованием и высушивают, при этом получают 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновую кислоту (5). Суспензию соединения формулы (5) и 1,1'-карбонилдиимидазола в диметилформамиде перемешивают при комнатной температуре в течение 1 ч, добавляют при перемешивании соединение формулы (6), например, бензиламин, и перемешивают в течение еще 20 ч. Затем добавляют воду и экстрагируют этилацетатом. Продукт очищают хроматографией на силикагеле (элюент: дихлометан/этилацетат), при этом получают соединение формулы I.
По схеме 1 получают соединения, описанные в примерах 3-84.
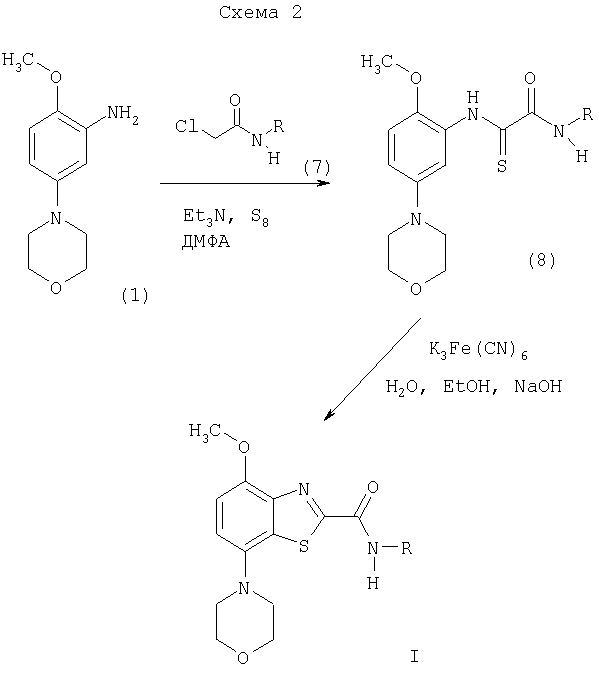
На схеме 2 R имеет значения, указанные выше.
По схеме 2 соответствующий хлорацетамид формулы (7) и серу в диметилформамиде обрабатывают триэтиламином и смесь перемешивают при комнатной температуре в течение приблизительно 15 ч. Затем добавляют 2-метокси-5-морфолин-4-илфениламин (1) и н-пропанол, и перемешивают при комнатной температуре в течение еще 6 ч. Затем смесь кипятят с обратным холодильником в течение двух суток. Кристаллический осадок отделяют фильтрованием и промывают н-пропанолом, при этом получают соединение формулы (8).
К раствору феррицианида калия в воде добавляют суспензию соединения формулы (8) в 1н. гидроксиде натрия, смесь перемешивают при 50°С в течение 30 мин, а затем при комнатной температуре в течение ночи. Осадок отделяют фильтрованием, растворяют в дихлорметане и очищают хроматографией на колонке с силикагелем (элюент: этилацетат/гексан), при этом получают соединение формулы I.
По схеме 2 получают соединения, описанные в примерах 1 и 2.
Выделение и очистка соединений
Выделение и очистку описанных выше соединений и промежуточных продуктов проводят при необходимости по любым пригодным методикам выделения или очистки, таким, например, как фильтрация, экстракция, кристаллизация, хроматография на колонке, хроматография в тонком и толстом слое сорбента, препаративная жидкостная хроматография при низком или высоком давлении или комбинация указанных методик. Конкретные иллюстрации пригодных методик разделения и выделения приводятся ниже в разделе Примеры. Однако можно также использовать и другие равноценные методики разделения или выделения веществ.
Соли соединений формулы I
Соединения формулы I являются основаниями, например, если остаток R содержит основную группу, такую как алифатический или ароматический амин. В таких случаях соединения формулы I можно превратить в соответствующую кислотно-аддитивную соль.
Получение солей проводят обработкой по меньшей мере стехиометрическим количеством соответствующей кислоты, такой как хлористоводородная кислота, бромистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота и т.п., или органическая кислота, такая как уксусная кислота, пропионовая кислота, гликолевая кислота, пировиноградная кислота, щавелевая кислота, яблочная кислота, малоновая кислота, янтарная кислота, малеиновая кислота, фумаровая кислота, винная кислота, лимонная кислота, бензойная кислота, коричная кислота, миндальная кислота, метансульфоновая кислота, этансульфоновая кислота, пара-толуолсульфоновая кислота, салициловая кислота и т.п. Обычно свободное основание растворяют в инертном растворителе, таком как диэтиловый эфир, этилацетат, хлороформ, этанол или метанол и т.п., и добавляют кислоту в том же растворителе. Температуру поддерживают от 0°С до 50°С. Полученная соль выпадает в осадок или ее можно высадить из раствора добавлением менее полярного растворителя.
Кислотно-аддитивные соли оснований соединений формулы I можно превратить в соответствующие свободные основания обработкой по меньшей мере стехиометрическим количеством соответствующего основания, такого как гидроксид натрия или калия, карбонат калия, бикарбонат натрия, аммиак и т.п.
Соединения формулы I и их фармацевтически приемлемые аддитивные соли обладают ценными фармакологическими свойствами. Конкретно было установлено, что соединения по настоящему изобретению являются лигандами аденозинового рецептора, обладают высоким сродством к аденозиновому рецептору А2A и высокой селективностью в отношении рецепторов A1 и А3.
Биологическую активность соединений определяли по следующей методике.
Связывание с аденозиновым рецептором A1 человека
Аденозиновый рецептор A1 человека рекомбинантно экспрессировали в яйцеклетках китайского хомячка (СНО) при использовании системы экспрессии вируса леса Семлики. Клетки собирали, дважды промывали центрифугированием, гомогенизировали и вторично промывали центрифугированием. Промытый осадок, содержащий мембранную фракцию, суспендировали в буферном растворе трис (50 мМ, рН 7,4), содержащем 120 мМ NaCl, 5 мМ KCl, 2 мМ CaCl2 и 10 мМ MgCl2 (буферный раствор А). Анализ связывания [3H]-DPCPX (0,6 нМ) ([пропил-3Н]-8-циклопентил-1,3-дипропилксантин) проводили в 96-луночных планшетах в присутствии 2,5 мкг мембранного белка, 0,5 мг гранул SPA, покрытых Ysi-поли-L-лизином, и 0,1 ед. аденозиндеаминазы в конечном объеме 200 мкл буфера А. Неспецифическое связывание определяли в присутствии родственного соединения ксантинамина (ХАС, 2 мкМ). Связывание анализируемых соединений определяли при 10 концентрациях от 10 мкМ до 0,3 нМ. Все анализы выполняли в повторных экспериментах, которые повторяли по меньшей мере дважды. Аналитические планшеты инкубировали при комнатной температуре в течение 1 ч, центрифугировали и определяли количество связанного лиганда, содержащего радиоактивную метку, на сцинтилляционном счетчике (Packard Topcount). Величины IC50 рассчитывали с использованием нелинейного регрессионного анализа и программного обеспечения, а значения Ki рассчитывали по уравнению Cheng-Prussoff.
Связывание с аденозиновым рецептором А2Aчеловека
Аденозиновый рецептор А2A человека рекомбинантно экспрессировали в яйцеклетках китайского хомячка (СНО) при использовании системы экспрессии вируса леса Семлики. Клетки собирали, дважды промывали центрифугированием, гомогенизировали и вторично промывали центрифугированием. Промытый осадок, содержащий мембранную фракцию, суспендировали в буферном растворе трис (50 мМ, рН 7,4), содержащем 120 мМ NaCl, 5 мМ KCl, 2 мМ CaCl2 и 10 мМ MgCl2 (буферный раствор А). Анализ связывания с [3H]-SCH-58261 (1нМ) (Dionisotti и др., Br. J. Pharmacol., 121, 353 (1997)) проводили в 96-луночных планшетах в присутствии 2,5 мкг мембранного белка, 0,5 мг гранул SPA, покрытых Ysi-поли-L-лизином, и 0,1 ед. аденозиндеаминазы в конечном объеме 200 мкл буфера А. Неспецифическое связывание определяли в присутствии родственного соединения ксантинамина (ХАС, 2 мкМ). Связывание анализируемых соединений определяли при 10 концентрациях от 10 мкМ до 0,3 нМ. Все анализы выполняли в повторных экспериментах, которые повторяли по меньшей мере дважды. Аналитичекие планшеты инкубировали при комнатной температуре в течение 1 ч, центрифугировали и определяли количество связанного лиганда, содержащего радиоактивную метку, на сцинтилляционном счетчике (Packard Topcount). Величины IC50 рассчитывали с использованием нелинейного регрессионного анализа и программного обеспечения, а значения Кi рассчитывали по уравнению Cheng-Prussoff.
Установлено, что соединения формулы I обладают высоким сродством к рецептору A2A и высокой селективностью в отношении рецептора A1.
Как показано в таблице, у предпочтительных соединений величины рКi составляют>7,5.
Соединения формулы I и фармацевтически приемлемые соли соединений формулы I можно использовать в качестве лекарственных средств, например, в форме фармацевтических препаратов. Фармацевтические препараты можно вводить пероральным способом, например, в форме таблеток, таблеток в оболочке, драже, твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий. Однако эффективным является также введение ректальным способом, например, в форме суппозиториев, или парентеральным способом, например, в форме инъекционных растворов.
Для получения фармацевтических препаратов соединения формулы IA и IB можно перерабатывать в смеси с фармацевтически инертными неорганическими или органическими носителями. В качестве таких носителей при получении таблеток, таблеток в оболочке, драже и твердых желатиновых капсул используются, например, лактоза, кукурузный крахмал или его производные, тальк, стеариновая кислота или ее соли и т.п. Пригодными носителями для мягких желатиновых капсул являются, например, растительные масла, воски, жиры, полутвердые и жидкие полиолы и т.п. Однако в случае мягких желатиновых капсул в зависимости от природы активного соединения обычно не требуется никакого носителя. Пригодными носителями при получении растворов и сиропов являются, например, вода, полиолы, глицерин, растительные масла и т.п. Пригодными носителями для суппозиториев являются, например, природные или отвержденные масла, воски, жиры, полутвердые или жидкие полиолы и т.п.
Кроме того, фармацевтические препараты могут содержать консерванты, солюбилизаторы, стабилизаторы, смачивающие агенты, эмульгаторы, подсластители, красители, ароматизаторы, соли для изменения осмотического давления, буферные вещества, маскирующие агенты или антиоксиданты. Кроме того, они могут содержать другие терапевтически ценные вещества.
Лекарственные средства, содержащие соединения формулы I или их фармацевтически приемлемую соль и терапевтически инертный носитель, также являются объектом настоящего изобретения. Объектом изобретения является также способ получения указанных лекарственных средств, включающий переработку одного или более соединений формулы I и/или их фармацевтически приемлемых кислотно-аддитивных солей и при необходимости одного или более других терапевтически ценных веществ в смеси в одним или более терапевтически инертным носителем в готовую галеновую форму.
Соединения формулы I по настоящему изобретению, а также их фармацевтически приемлемые соли, благодаря антагонистическому действию на аденозиновый рецептор применяются для лечения или профилактики заболеваний, таких как болезнь Альцгеймера, болезнь Паркинсона, нейрозащитное действие, шизофрения, тревога, боль, нарушения дыхания, депрессия, астма, аллергические ответные реакции, гипоксия, ишемия, эпилептический припадок и токсикомания. Кроме того, соединения по настоящему изобретению могут применяться в качестве седативных средств, мышечных релаксантов, антипсихотических средств, противоэпилептических средств, противосудорожных средств и кардиопротективных агентов и для получения соответствующих лекарственных средств.
Наиболее предпочтительными показаниями по настоящему изобретению являются показания, которые включают нарушение ЦНС, например, лечение или профилактику некоторых депрессивных состояний, нейрозащитное действие и болезнь Паркинсона.
Дозы могут изменяться в широких пределах и должны соответствовать индивидуальным требованиям в каждом конкретном случае. В общем случае при пероральном введении взрослым пациентам суточная доза может изменяться от приблизительно 0,01 мг до приблизительно 1000 мг соединения общей формулы I или соответствующего количества его фармацетически приемлемой соли. Суточная доза вводится в виде однократной дозы и разделенными дозами и, кроме того, в случае соответствующих показаний верхний предел можно превысить.
Методика получения
1. Компоненты 1, 2, 3 и 4 смешивают и гранулируют при добавлении очищенной воды.
2. Гранулы высушивают при температуре 50°С.
3. Гранулы измельчают на соответствующей мельнице.
4. Добавляют компонент и перемешивают в течение 3 мин; затем прессуют таблетки на соответствующем таблетирующем оборудовании.
Методика получения
1. Компоненты 1, 2, 3 смешивают в соответствующем смесителе в течение 30 мин.
2. Добавляют компоненты 4 и 5 и перемешивают в течение 3 мин.
3. Смесью заполняют соответствующие капсулы. Изобретение иллюстрируется следующими примерами, не ограничивающими его объем.
Пример 1
Амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты
а) 2-(2-Метокси-5-морфолин-4-илфениламино)-2-тиоксоацетамид
173 мг (1,85 ммоль) Хлорацетамида и 119 мг (3,70 ммоль) серы в 2 мл диметилформамида обрабатывали 772 мкл (5,55 ммоль) триэтиламина и смесь перемешивали при комнатной температуре в течение 15 ч. Затем добавляли 385 мг (1,85 ммоль) 2-метокси-5-морфолин-4-илфениламина и 10 мл н-пропанола, перемешивали при комнатной температуре в течение 6 ч, а затем смесь кипятили с обратным холодильником в течение двух суток. Кристаллический осадок отделяли фильтрованием и промывали н-пропанолом, при этом получали 320 мг (59%) 2-(2-метокси-5-морфолин-4-илфениламино)-2-тиоксоацетамида в виде кристаллов красно-коричневого цвета. МС: m/e (%) 296 (М+Н+, 100).
Элементный анализ:
рассч. для C13H17N3O3S (295,357): С 52,87, Н 5,80, N 14,23, S 10.86;
найд.: С 52,38, Н 5,82, N 13,85, S 10,86.
б) Амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты
Суспензию 220 мг (0,75 ммоль) 2-(2-метокси-5-морфолин-4-илфениламино)-2-тиоксоацетамида в 2,88 мл 1н. гидроксида натрия добавляли к раствору 813 мг (2,47 ммоль) феррицианида калия в 2 мл воды и смесь перемешивали при 50°С в течение 30 мин, а затем при комнатной температуре в течение ночи. Осадок отделяли фильтрованием, растворяли в дихлорметане и очищали хроматографией на колонке с силикагелем (элюент: этилацетат/гексан, 1:1), при этом получали амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты (32 мг, 15%) в виде кристаллов желтого цвета, tпл.228-230°С. МС: m/е (%) 294 (М+Н+, 100).
Пример 2
(4-Фторфенил)амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты
а)N-(4-Фторфенил)-2-(2-метокси-5-морфолин-4-илфениламино)-2-тиоксоацетамид
919 мг (4,80 ммоль) α-хлор-4-фторацетанилида и 308 мг (9,60 ммоль) серы в 10 мл диметилформамида обрабатывали 2,01 мл (14,4 ммоль) триэтиламина и смесь перемешивали при комнатной температуре в течение 2 сут. Затем добавляли 1,00 г (4,80 ммоль) 2-метокси-5-морфолин-4-илфениламина в 5 мл диметилформамида и 25 мл н-пропанола, перемешивали при комнатной температуре в течение 6 ч, а затем смесь кипятили с обратным холодильником в течение 6,5 ч. Кристаллический осадок отделяли фильтрованием, промывали водой и высушивали, при этом получали 434 мг (24%) N-(4-фторфенил)-2-(2-метокси-5-морфолин-4-илфениламино)-2-тиоксоацетамида в виде порошка красного цвета. tпл.206-208°C. MC: m/e (%) 390 (М+Н+, 100).
б) (4-Фторфенил)амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты
Суспензию 100 мг (0,26 ммоль) N-(4-фторфенил)-2-(2-метокси-5-морфолин-4-илфениламино)-2-тиоксоацетамида в 3,60 мл 1н. гидроксида натрия добавляли к раствору 285 мг (0,87 ммоль) феррицианида калия в 1 мл воды и смесь перемешивали при 50°С в течение 2 сут, а затем экстрагировали дихлорметаном. Продукт очищали хроматографией на колонке с силикагелем (элюент: этилацетат/гексан, 3:7), при этом получали 3,5 мг (4-фторфенил)амида 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты в виде кристаллов грязно-белого цвета. MC: m/e (%) 388 (М+Н+, 100).
Пример 3
Бензиламид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты
а) Этиловый эфир N-(2-метокси-5-морфолин-4-илфенил)оксаламовой кислоты
139 мл (1015 ммоль) диэтилового эфира щавелевой кислоты нагревали до 120°С, осторожно небольшими порциями добавляли 30,3 г (145 ммоль) 2-метокси-5-морфолин-4-илфениламина и смесь нагревали при 180°С в течение 90 мин. Затем смесь охлаждали до комнатной температуры, фильтровали и добавляли 1,5 л н-гексана. Полученный осадок отделяли фильтрованием, промывали гексаном и высушивали, при этом получали 34,4 г (77%) этилового эфира N-(2-метокси-5-морфолин-4-илфенил)оксаламовой кислоты в виде кристаллов зеленоватого цвета. tпл.95-97°С. MC: m/e (%) 309 (М+Н+, 100).
б) (2-Метокси-5-морфолин-4-илфениламино)тиоксоуксусная кислота
К 33,9 г (110 ммоль) этилового эфира N-(2-метокси-5-морфолин-4-илфенил)оксаминовой кислоты в 652 мл кипящего ксилола небольшими порциями в течение 30 мин добавляли 8,80 г (40 ммоль) пентасульфида фосфора, смесь кипятили с обратным холодильником в течение 5 ч, охлаждали до комнатной температуры и фильтровали. Раствор семикратно экстрагировали 100 мл 1н. NaOH. Водную фазу дважды промывали 100 мл толуола, фильтровали и при 0-5°С добавляли конц. соляную кислоту до рН 1. Осадок отделяли фильтрованием, при этом получали 20,2 г (62%) (2-метокси-5-морфолин-4-илфениламино)тиоксоуксусной кислоты в виде кристаллов желтого цвета. tпл.156-158°С. МС: m/е (%) 297 (М+Н+, 100).
в) 4-Метокси-7-морфолин-4-илбензотиазол-2-карбоновая кислота
Раствор 10,5 г (35,4 ммоль) (2-метокси-5-морфолин-4-илфениламино)тиоксоуксусной кислоты в 248 мл (248 ммоль) 1н. NaOH добавляли по каплям к раствору 40,1 г (119 ммоль) феррицианида калия в 119 мл воды, поддерживая температуру не выше 10°С. Смесь перемешивали при 10°С в течение 3 ч, а затем добавляли конц. соляную кислоту до рН 1. Осадок отделяли фильтрованием и высушивали, при этом получали 8,80 г (84%) 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты в виде кристаллов желтого цвета. tпл.99-100°С. МС: m/е (%) 295 (M+H+, 100).
г) Бензиламид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты
Суспензию 29,4 мг (0,10 ммоль) 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты и 18,4 мг (0,11 ммоль) 1,1'-карбонилдимидазола в 3 мл диметилформамида перемешивали при комнатной температуре в течение 1 ч. Затем добавляли 12,1 мкл (0,11 ммоль) бензиламина и перемешивали в течение 20 ч. К смеси добавляли 15 мл воды, экстрагировали этилацетатом и продукт очищали хроматографией на колонке с силикагелем (элюент: дихлорметан/этилацетат, 95:5), при этом получали 31,2 мг (41%) бензиламида 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты. tпл.156-158°С. МС: m/е (%) 384 (М+Н+, 100).
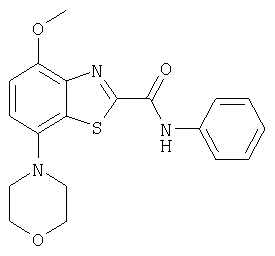
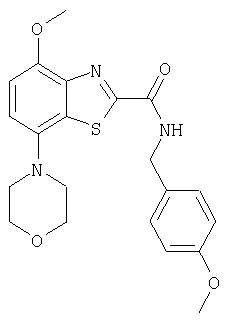
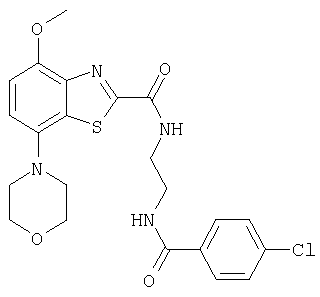
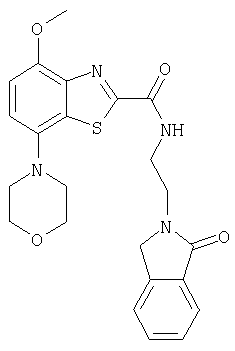
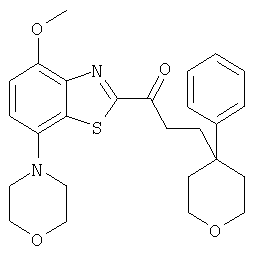
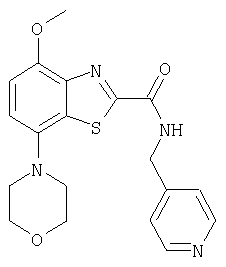
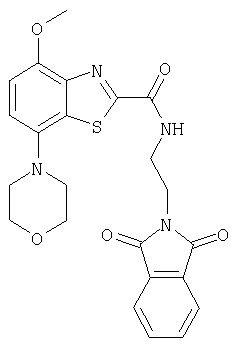
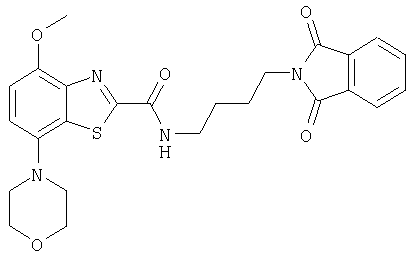
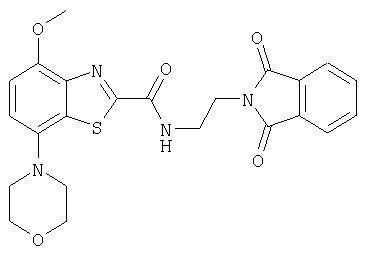
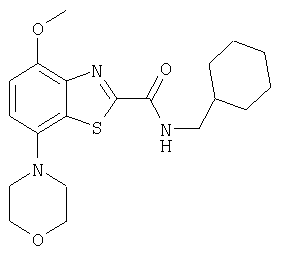
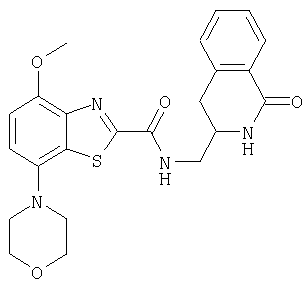
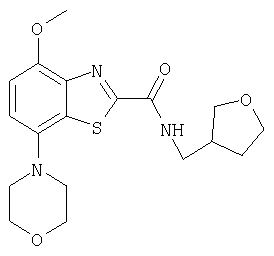
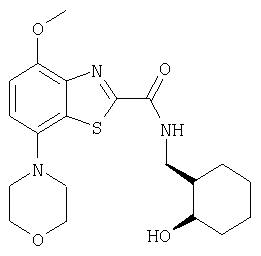
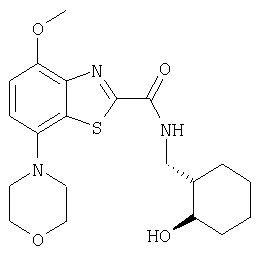
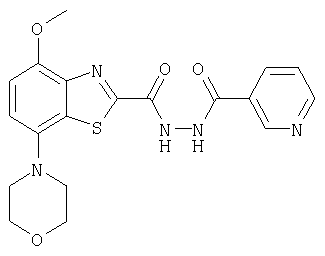
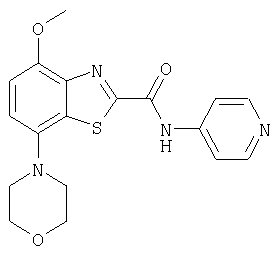
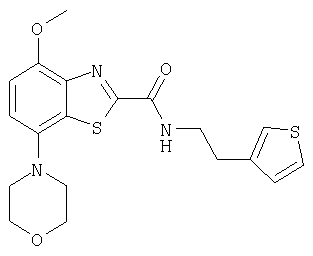
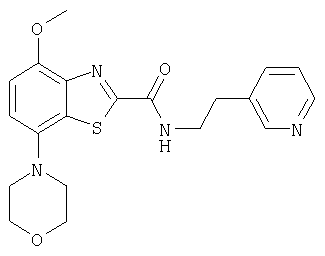
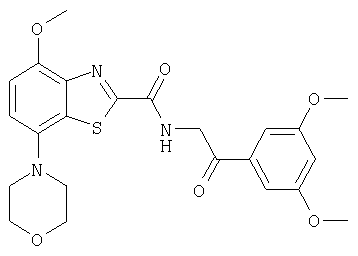
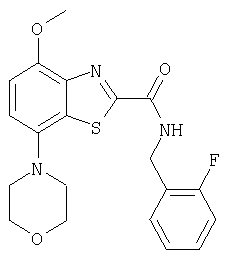
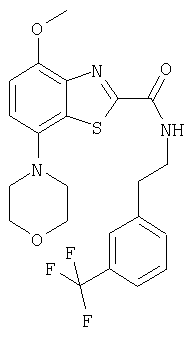
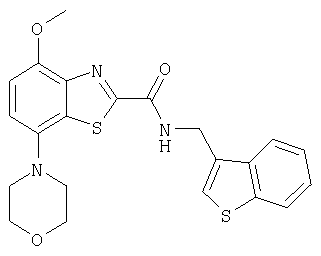
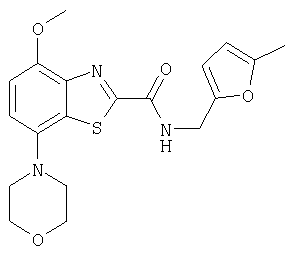
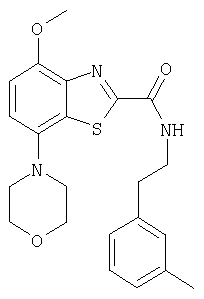
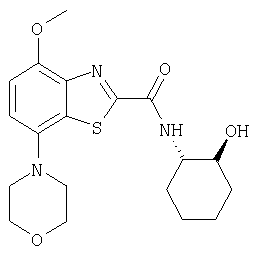
Ниже в таблице приведены характеристики соединений (примеры 4-81), синтезированных, как описано в примере 3 г.
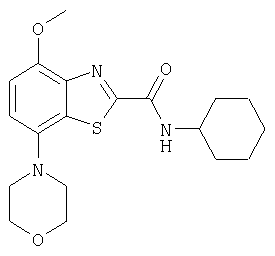
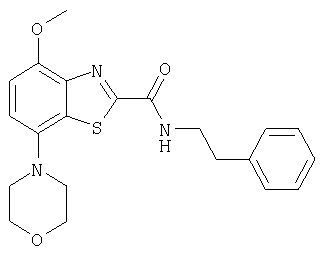
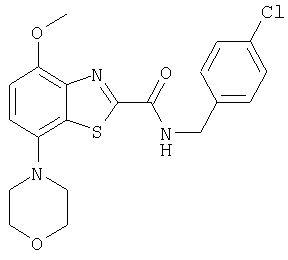
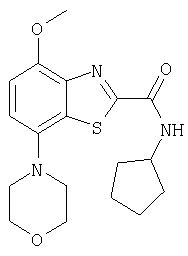
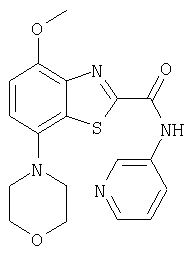
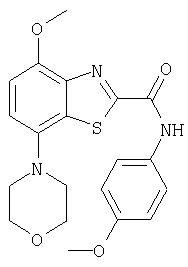
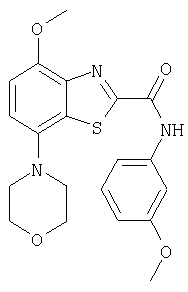
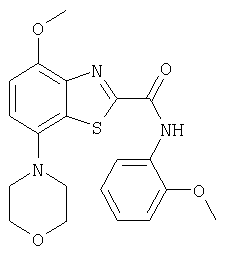
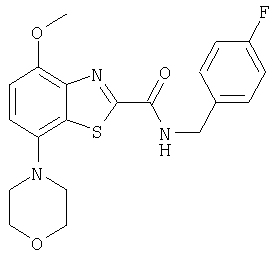
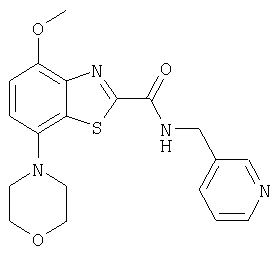
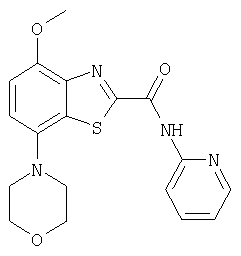
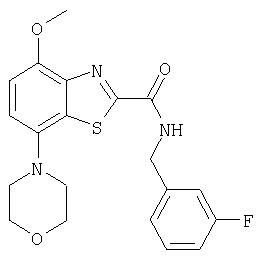
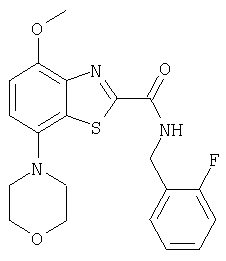
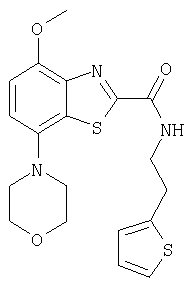
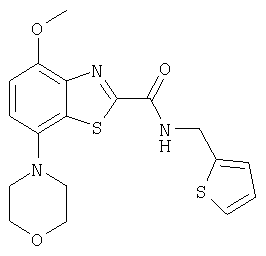
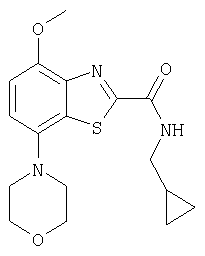
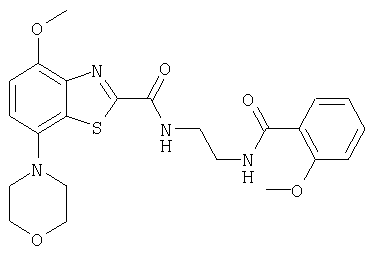
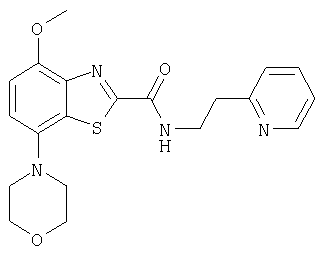
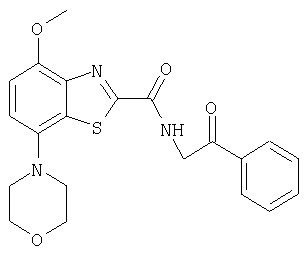
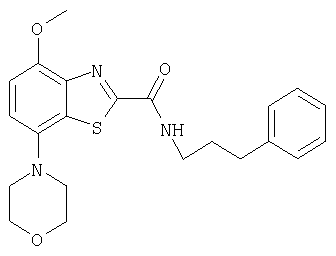
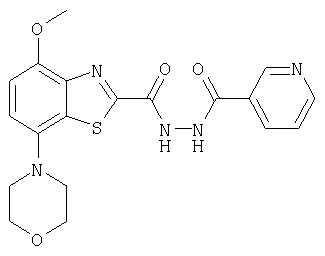
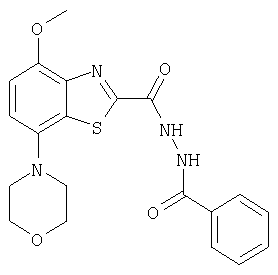
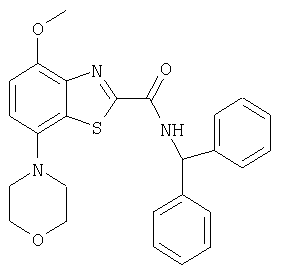
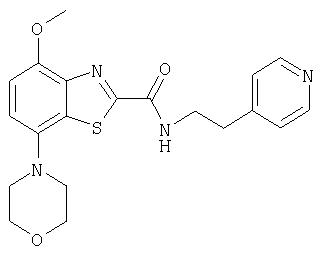
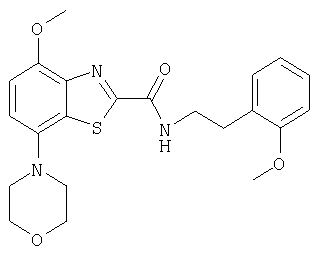
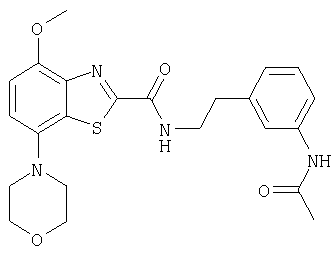
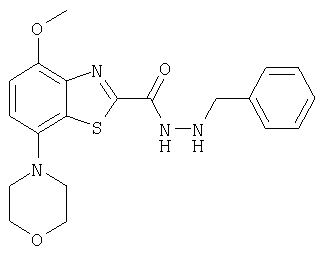
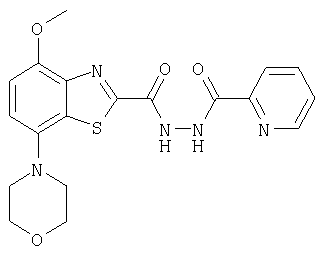
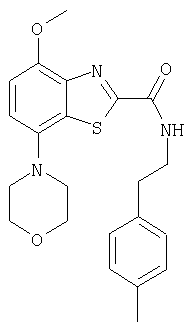
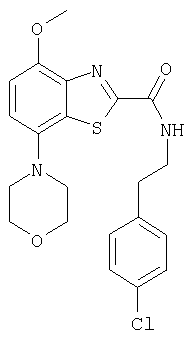
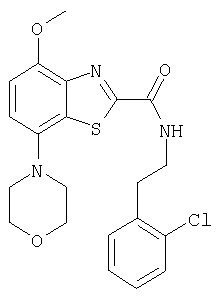
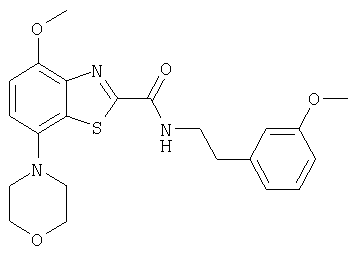
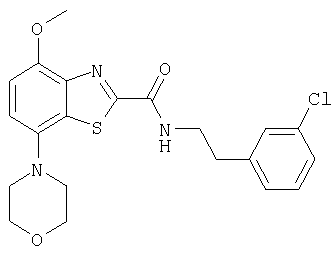
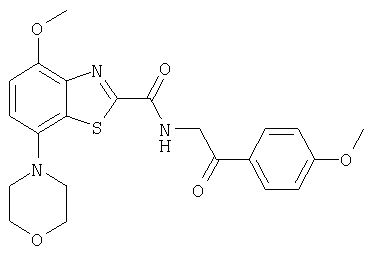
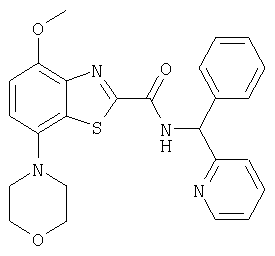
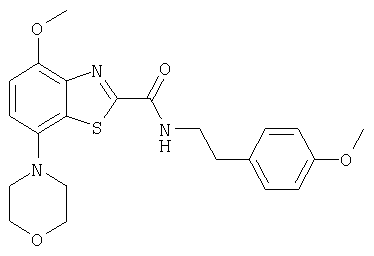
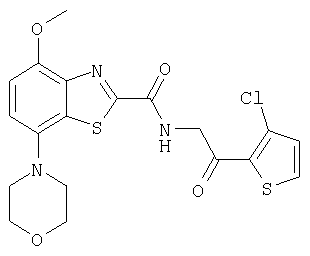
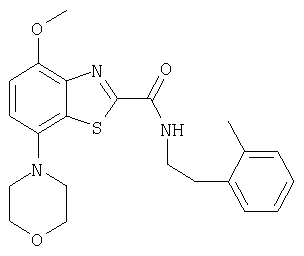
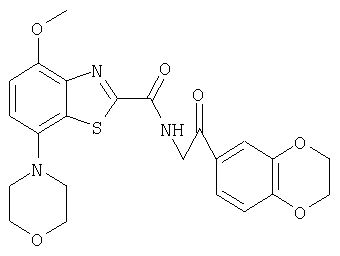
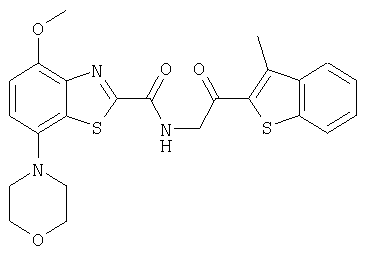
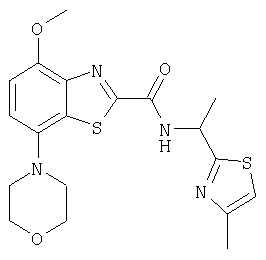
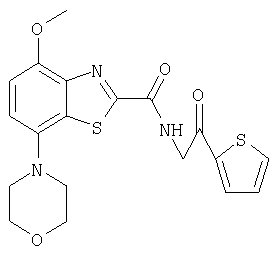
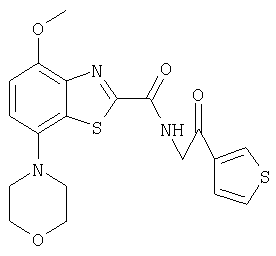
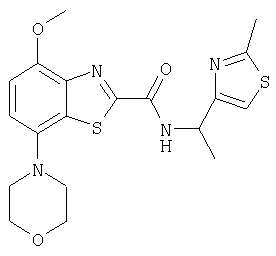
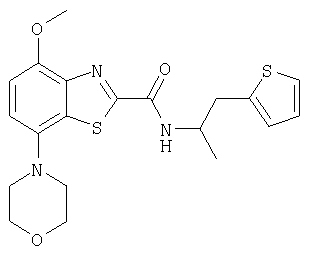
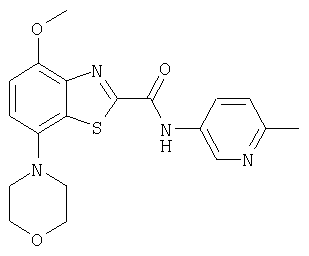
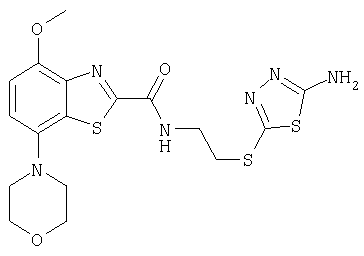
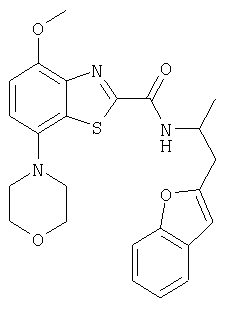
| название | год | авторы | номер документа |
|---|---|---|---|
| 2-ИМИДАЗОБЕНЗОТИАЗОЛЫ КАК ЛИГАНДЫ АДЕНОЗИНОВОГО РЕЦЕПТОРА | 2004 |
|
RU2340612C2 |
| ПРОИЗВОДНЫЕ БЕНЗОТИАЗОЛА | 2001 |
|
RU2251419C2 |
| ПРОИЗВОДНЫЕ БЕНЗОТИАЗОЛА В КАЧЕСТВЕ ЛИГАНДОВ РЕЦЕПТОРА АДЕНОЗИНА И ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2002 |
|
RU2295523C2 |
| БЕНЗОТИОФЕНЫ В КАЧЕСТВЕ МОДУЛЯТОРОВ АДЕНОЗИНОВОГО РЕЦЕПТОРА | 2002 |
|
RU2299882C2 |
| ПРОИЗВОДНЫЕ НИКОТИН- ИЛИ ИЗОНИКОТИНБЕНЗОТИАЗОЛА И ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2002 |
|
RU2294933C2 |
| ПРОИЗВОДНЫЕ БЕНЗОТИАЗОЛА | 2005 |
|
RU2382782C2 |
| 2-АМИНОБЕНЗОТИАЗОЛИЛМОЧЕВИНЫ В КАЧЕСТВЕ МОДУЛЯТОРОВ АДЕНОЗИНА | 2002 |
|
RU2311905C2 |
| ПРОИЗВОДНЫЕ 8-МЕТОКСИ[1,2,4]ТРИАЗОЛО[1,5-a]ПИРИДИНА И ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ НА ИХ ОСНОВЕ | 2002 |
|
RU2297416C2 |
| БЕНЗОТИАЗОЛЫ | 2002 |
|
RU2293736C2 |
| ПРОИЗВОДНЫЕ БЕНЗОТИАЗОЛА В КАЧЕСТВЕ ЛИГАНДОВ АДЕНОЗИНОВЫХ РЕЦЕПТОРОВ | 2004 |
|
RU2351597C2 |
Изобретение относится к производным бензотиазола общей формулы
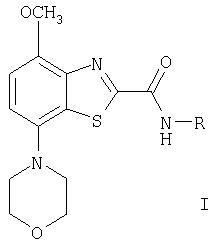
где R означает водород; -(СН2)n-фенил, необязательно замещенный заместителем ряда галоген, (низш.)алкил, (низш.)алкокси, трифторметил или -N(R')-С(O)-(низш.)алкил; -(СН2)n-пиридинил, необязательно замещенный (низш.)алкилом; -(СН2)N-С3-С6циклоалкил, необязательно замещенный гидроксигруппой; -(СН2)n-бензо[1,3]диоксолил; -(CR'2)n-тиофенил; -(CR'2)n-тиазолил, необязательно замещенный (низш.)алкилом; -(СН2)n-С(O)-тиофенил, необязательно замещенный галогеном; -(СН2)n-фуранил, необязательно замещенный (низш.)алкилом; -(CHR')n-бензофуран-2-ил; -(СН2)n-бензо[b]тиофенил; -(СН2)n-N(R')-С(O)-фенил, необязательно замещенный галогеном или (низш.)алкокси; -(СН2)n-С(O)-фенил, необязательно замещенный (низш.)алкокси; -(СН2)n-С(O)-2,3-дигидробензо[1,4]диоксин-6-ил; -(СН2)n-N(R')-С(O)-пиридинил; -(СН2)n-тетрагидрофуранил; -СН-бифенил; -СН-(фенил)пиридинил; -(СН2)n-1-оксо-1,3-дигидроизоиндол-2-ил; -(СН2)n-1,3-диоксо-1,3-дигидроизоиндол-2-ил; -(СН2)n-СН-(фенил)тетрагидропиранил; -(СН2)n-1-оксо-1,2,3,4-тетрагидроизохинолин-3-ил или -(СН2)n-S-[1,3,4]тиадиазол-2-ил, необязательно замещенный аминогруппой, R' означает водород или (низш.)алкил, независимо друг от друга в случае R'2, a n равно 0, 1, 2, 3 или 4. Изобретение также относится к лекарственному средству, обладающему высоким сродством к аденозиновому рецептору а2а и высокой селективностью в отношении рецептора а1, содержащее одно или более производное бензотиазола формулы I и фармацевтически приемлемые эксципиенты. Технический результат - производные бензотиазола, в качестве лигандов рецепторов аденозина. 2 н. и 11 з.п. ф-лы, 2 табл.
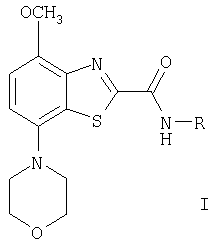
где R означает водород,
-(CH2)n-фенил, необязательно замещенный заместителем ряда галоген, (низш.)алкил, (низш.)алкокси, трифторметил или -N(R')-С(O)-(низш.)алкил,
-(CH2)n-пиридинил, необязательно замещенный (низш.)алкилом,
-(СН2)n-С3-С6циклоалкил, необязательно замещенный гидроксигруппой,
-(СН2)n-бензо[1,3]диоксолил,
-(CR'2)n-тиофенил,
-(CR'2)n-тиазолил, необязательно замещенный (низш.)алкилом,
-(СН2)n-С(O)-тиофенил, необязательно замещенный галогеном,
-(СН2)n-фуранил, необязательно замещенный (низш.)алкилом,
-(CHR')n-бензофуран-2-ил,
-(СН2)n-бензо[b]тиофенил,
-(СН2)n-N(R')-С(O)-фенил, необязательно замещенный галогеном или (низш.)алкокси,
-(СН2)n-С(O)-фенил, необязательно замещенный (низш.)алкокси,
-(СН2)n-С(O)-2,3-дигидробензо[1,4]диоксин-6-ил,
-(СН2)n-N(R')-С(O)-пиридинил,
-(СН2)n-тетрагидрофуранил,
-СН-бифенил,
-СН-(фенил)пиридинил,
-(СН2)n-1-оксо-1,3-дигидроизоиндол-2-ил,
-(СН2)n-1,3-диоксо-1,3-дигидроизоиндол-2-ил,
-(СН2)n-СН-(фенил)тетрагидропиранил,
-(СН2)n-1-оксо-1,2,3,4-тетрагидроизохинолин-3-ил или
-(СН2)n-S-[1,3,4]тиадиазол-2-ил, необязательно замещенный аминогруппой;
R' означает водород или (низш.)алкил, независимо друг от друга в случае R'2, а n равно 0, 1, 2, 3 или 4.
фенетиламид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
3-хлорбензиламид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
2-хлорбензиламид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
2-метоксибензиламид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
[2-(2-метоксифенил)этил]амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
[2-(3-фторфенил)этил]амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
[2-(4-фторфенил)этил]амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
[2-(4-хлорфенил)этил]амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
[2-(2-хлорфенил)этил]амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
[2-(3-метоксифенил)этил]амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
[2-(3-хлорфенил)этил]амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты или
(2-мета-толилэтил)амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты.
пиридин-3-иламид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
(пиридин-2-илметил)амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты или
(2-пиридин-3-илэтил)амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты.
(2-тиофен-2-илэтил)амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
(2-тиофен-3-илэтил)амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты,
[2-(3-хлортиофен-2-ил)-2-оксоэтил]амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты или
(1-метил-2-тиофен-2-илэтил)амид 4-метокси-7-морфолин-4-илбензотиазол-2-карбоновой кислоты.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| BARALDI P.G | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ получения тиазолилкарбамоилзамещенных эфирных производных азотной кислоты или их аддитивных солей с галоидводородными кислотами | 1989 |
|
SU1760984A3 |
Авторы
Даты
2007-02-10—Публикация
2002-11-18—Подача