Настоящее изобретение относится к соединениям общей формулы
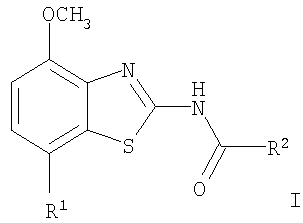
где R1 представляет собой 1,4-диоксепанил или тетрагидропиран-4-ил;
R2 представляет собой -N(R)-(СН2)n-5-или 6-членный неароматический гетероцикл, необязательно замещенный одним или более заместителями, выбранными из группы, состоящей из низшего алкила или -NR2, или
представляет собой -(СН2)n-5- или 6-членный неароматический гетероцикл, необязательно замещенный группой -(СН2)n-ОН, низший алкил, низший алкокси, или
представляет собой -(СН2)n-5-или 6-членный ароматический гетероцикл, необязательно замещенный группой низший алкил, низший алкокси, галоген, галоген-низший алкил), -CH2N(R)(CH2)2OCH3, -N(R)(СН2)2OCH3, -СН2-морфолинил или -СН2-пирролидинил или
представляет собой (СН2)n-циклоалкил, необязательно замещенный группой гидрокси, или
представляет собой -N(R)-циклоалкил, необязательно замещенный группой гидрокси или группой низший алкил, или
представляет собой фенил, необязательно замещенный группой низший алкокси, галоген, галоген-(низший алкил), низший алкил, -СН2-пирролидин-1-ил, -СН2-морфолинил, -СН2N(R)(СН2)2OCH3 или -СН2-N(R)С(O)-(низший алкил), или
означает 1,4-диокса-8-азаспиро[4,5]декан, или
означает 2-окса-5-азабицикло[2,2,1]гептан, или
означает 1-окса-8-азаспиро[4,5]декан, или
означает -N(R)-7-оксабицикло[2,2,1]гепт-2-ил, или
означает 2-азабицикло[2,2,2]октан;
R представляет собой водород или низший алкил;
n означает 0 или 1; и
и к их фармацевтически приемлемым кислотно-аддитивным солям (солям - продуктам присоединения кислоты).
Неожиданно было обнаружено, что соединения общей формулы I представляют собой лиганды аденозинового рецептора. А именно, соединения согласно настоящему изобретению обладают значительным сродством к А2А-рецептору и высокой селективностью по отношению к Ai- и А3-рецепторам.
Аденозин является модулятором большого числа физиологических функций, что осуществляется посредством взаимодействия со специфическими рецепторами поверхности клетки. Обзор, посвященный возможному использованию аденозиновых рецепторов в качестве мишеней для лекарственных средств, был впервые выполнен в 1982 году.
Аденозин связан как структурно, так и метаболически с биологически активными нуклеотидами аденозинтрифосфатом (АТФ), аденозиндифосфатом (АДФ), аденозинмонофосфатом (АМФ) и циклическим аденозинмонофосфатом (цАМФ); с биохимическим метилирующим агентом S-аденозил-L-метионом (SAM); и структурно - с коферментами NAD, FAD и коферментом А; и с РНК. Аденозин и родственные ему соединения играют важную роль в регулировании многих аспектов клеточного метаболизма и в модулировании различных видов активности центральной нервной системы.
Аденозиновые рецепторы классифицируют как A1, A2A, А2В и А3 рецепторы, принадлежащие к семейству рецепторов, сопряженных с G-белками. Активация аденозиновых рецепторов аденозином инициирует систему передачи сигнала. Эти механизмы опосредованы G-белком, ассоциированным с рецептором. Каждый подтип аденозинового рецептора обычно характеризуется аденилатциклазной эффекторной системой, в которой в качестве вторичного мессенджера используется цАМФ. A1 и А3 рецепторы, связанные с Gi белками, ингибируют аденилатциклазу, что приводит к снижению содержания цАМФ в клетках, в то время как A2A и А2В рецепторы сопряжены с Gs белками и активируют аденилатциклазу, что приводит к повышению содержания цАМФ в клетках. Известно, что система A1 рецептора включает активацию фосфолипазы С и модулирование как калиевых, так и кальциевых ионных каналов. Подтип А3, в дополнение к ассоциации с аденилатциклазой, также стимулирует фосфолипазы С и таким образом активирует кальциевые ионные каналы.
Клонирован A1 рецептор (326-328 аминокислот) различных видов (семейства псовых, человека, крысы, собаки, цыпленка, крупного рогатого скота, морской свинки), при этом у млекопитающих наблюдается 90-95%-ная идентичность последовательности. Клонирован A2A рецептор (409-412 аминокислот) семейства псовых, крысы, человека, морских свинок и мышей. Клонирован A2B рецептор (332 аминокислоты) человека и мыши, при этом наблюдается 45%-ная гомологичность последовательности рецептора А2B человека по отношению к A1 и А2Ф рецепторам человека. Клонирован А3 рецептор (317-320 аминокислоты) человека, крысы, собаки, кролика и овцы.
Предполагается, что подтипы рецептора A1 и A2A дополняют друг друга при регуляции аденозином процесса обеспечения энергией. Аденозин, который является продуктом метаболической трансформации АТФ, диффундирует из клетки и локально воздействует на активацию аденозиновых рецепторов, снижая потребность в кислороде (A1) или увеличивая снабжение кислородом (А2A) и таким образом поддерживая равновесие между обеспечением энергией и ее потреблением в тканях. Действие обоих подтипов заключается в увеличении количества доступного для тканей кислорода и в защите клеток от повреждения, вызванного кратковременным дисбалансом в поступлении кислорода. Одной из важных функций эндогенного аденозина является предупреждение повреждения при травмах, таких как гипоксия, ишемия, гипотензия и эпилептические припадки.
Кроме того, известно, что связывание агониста аденозинового рецептора с тучными клетками, экспрессирующими рецептор А3 крысы, приводит к увеличению уровня инозиттрифосфата и концентрации кальция внутри клетки, что усиливает антигениндуцируемую секрецию медиаторов воспалительной реакции. Следовательно, рецептор A3 играет важную роль в качестве медиатора в случае приступов астмы и других аллергических реакций.
Аденозин является также нейромодулятором, способным модулировать различные аспекты физиологической деятельности мозга. Эндогенный аденозин, центральное связующее звено между энергетическим обменом и нейрональной активностью, изменяется в соответствии с поведенческим состоянием и (пато)физиологическими состояниями. В условиях повышения потребности и снижения доступности энергии (таких как гипоксия, гипогликемия, и/или чрезмерная активность нейронов) аденозин обеспечивает эффективный защитный механизм обратной связи. Взаимодействие с аденозиновыми рецепторами является многообещающим направлением терапевтического воздействия в случае разнообразных неврологических и психиатрических заболеваний, таких как эпилепсия, расстройства и нарушения сна и двигательной активности (болезнь Паркинсона или болезнь Хантингтона (Huntington), болезнь Альцгеймера, депрессия, шизофрения или привыкание.
Увеличение скорости высвобождения нейромедиатора происходит при травме, такой как гипоксия, ишемия и эпилептические припадки. Эти нейромедиаторы в конечном счете отвечают за дегенерацию и гибель нейронов, что влечет за собой повреждение мозга или смерть организма. Таким образом, агонисты аденозинового рецептора A1, имитирующие ингибиторные процессы в центральной нервной системе (ЦНС), вызываемые аденозином, могут найти применение в качестве нейропротекторных агентов. Аденозин предполагается использовать в качестве эндогенного противосудорожного агента, ингибирующего высвобождение глутамата из возбужденных нейронов и ингибирующего возбуждение нейронов. Таким образом, агонисты аденозина могут быть использованы в качестве противоэпилептических агентов. Антагонисты аденозина стимулируют активность ЦНС и, как установлено, являются эффективными усиливающими агентами в отношении познавательных (когнитивных) способностей. Селективные A2a антагонисты обладают терапевтическим потенциалом в отношении лечения различных форм деменции, например в случае болезни Альцгеймера, и при нейродегенеративных заболеваниях, например при нарушении мозгового кровообращения. Антагонисты аденозинового А2a рецептора модулируют активность стриатальных GABA-эргических нейронов и регулируют плавные движения и координацию, таким образом предоставляя возможность для лечения симптомов, наблюдающихся при паркинсонизме. Аденозин также принимает участие в ряде физиологических процессов, лежащих в основе седативного эффекта, гипноза, шизофрении, беспокойства и тревоги, боли, дыхания, депрессии, наркомании и лекарственного привыкания (амфетамин, кокаин, опиоиды, этанол, никотин, каннабиноиды). Следовательно, лекарственные средства, воздействующие на аденозиновые рецепторы, обладают терапевтическим потенциалом в качестве седативных агентов, мышечных релаксантов, антипсихотических средств, транквилизаторов, анальгетиков, стимуляторов дыхания и антидепрессантов и при лечении наркомании и лекарственного привыкания. Они также могут быть использованы для лечения нарушений и расстройств, связанных с дефицитом внимания и гиперактивностью (ADHD).
В сердечно-сосудистой системе аденозин выполняет важную функцию в качестве кардиопротектора (кардиозащитного средства). Уровень эндогенного аденозина повышается как реакция на ишемию и гипоксию, что защищает ткани сердца при травме и после травмы (стабилизация). Посредством воздействия на A1 рецептор, агонисты аденозинового A1 могут осуществлять защиту от повреждений, вызываемых ишемией миокарда и реперфузией. Модулирование воздействия А2a рецепторов на адренергическую функцию может иметь большое значение в случае различных заболеваний, например, таких как заболевания коронарной артерии и сердечная недостаточность. А2a антагонисты могут представлять интерес для терапии при таких ситуациях, когда необходима повышенная адренергическая реакция, например, при остром инфаркте миокарда. Селективные антагонисты по отношению к А2a рецепторам также могут повышать эффективность аденозина при непериодической наджелудочковой (суправентрикулярной) аритмии.
Аденозин является модулятором множества аспектов функционирования почек, включая высвобождение ренина, скорость гломерулярной (клубочковой) фильтрации и почечный кровоток. Соединения, которые противодействуют воздействию аденозина на почки, являются защитными агентами для почек. Кроме того, антагонисты аденозиновых рецепторов А3 и/или А2B могут быть полезны при лечении астмы и других аллергических реакций или при лечении сахарного диабета и ожирения.
Современное состояние исследований в области аденозиновых рецепторов отражает множество опубликованных документов, например следующие публикации:
Bioorganic & Medicinal Chemistry, 6, (1998), 619-641,
Bioorganic & Medicinal Chemistry, 6, (1998), 707-719,
J. Med. Chem., (1998), 41, 2835-2845
J. Med. Chem., (1998), 41, 3186-3201,
J. Med. Chem., (1998), 41, 2126-2133.
J. Med. Chem., (1999), 42, 706-721,
J. Med. Chem., (1996), 39, 1164-1171,
Arch. Pharm. Med. Chem., 332, 39-41, (1999),
Am. J. Physiol, 276, H1113-1116, (1999) или
Naunyn Schmied, Arch. Pharmacol. 362, 375-381, (2000).
Целью настоящего изобретения являются соединения формулы I сами по себе, применение соединений формулы I и их фармацевтически приемлемых солей для получения лекарственных средств, предназначенных для лечения заболеваний, связанных с аденозиновым А2 рецептором, их получение, лекарственные средства на основе соединения согласно настоящему изобретению и их получение, а также применение соединений формулы I для контроля или профилактики заболеваний, связанных с модулированием аденозиновой системы, например таких, как болезнь Альцгеймера, болезнь Паркинсона, болезнь Хантингтона, нейропротективное действие, шизофрения, беспокойство, боль, дефицит дыхания, депрессия, привыкание к наркотическим и лекарственным средствам, таким как амфетамин, кокаин, опиоиды, этанол, никотин, каннабиноиды или применение при астме, аллергических реакциях, гипоксии, ишемии, припадках и злоупотреблении алкоголем или наркотиками. Кроме того, соединения согласно настоящему изобретению могут быть полезны в качестве седативных средств, мышечных релаксантов, антипсихотических средств, противоэпилептических средств, противосудорожных средств и кардиопротекторных средств при таких заболеваниях, как например заболевания коронарной артерии и сердечная недостаточность. Наиболее предпочтительными показаниями в соответствии с настоящим изобретением являются такие, которые основаны на антагонистической активности в отношении A2A рецептора и которые включают расстройства центральной нервной системы, например лечение или профилактику болезни Альцгеймера, некоторые депрессивные нарушения или расстройства, наркоманию, лекарственное привыкание, нейропротективное действие и болезнь Паркинсона, а также нарушения и расстройства, связанные с дефицитом внимания и гиперактивностью (ADHD).
При использовании в тексте настоящей заявки термин "низший алкил" означает насыщенную алкильную группу с линейной или разветвленной цепью, содержащую от 1 до 6 атомов углерода, например, такую как метил, этил, пропил, изопропил, н-бутил, изобутил, 2-бутил, трет-бутил и подобные группы. Предпочтительные группы низший алкил представляют собой группы, содержащие 1-4 атома углерода.
Термин "галоген" означает хлор, йод, фтор и бром.
Термин "низший алкокси" означает группу, в которой алкильные остатки являются такими, как указано выше, и которая присоединена через атом кислорода.
Термин "циклоалкил" означает насыщенную карбоциклическую группу, содержащую 3-7 атомов углерода.
Термин "5-или 6-членный неароматический гетероцикл" означает кольцевую систему, такую как морфолин, пиперазин, пиперидин, тетрагидропиран или тетрагидрофуран.
Термин "5-или 6-членный ароматический гетероцикл" означает кольцевую систему, например, такую как тиофен, имидазол, пиразол или пиридин.
Термин "фармацевтически приемлемые аддитивные соли с кислотами" (соли - продукты присоединения кислоты) включает соли с неорганическими и органическими кислотами, такими как хлороводородная кислота, азотная кислота, серная кислота, фосфорная кислота, лимонная кислота, муравьиная кислота, фумаровая кислота, малеиновая кислота, уксусная кислота, янтарная кислота, винная кислота, метансульфоновая кислота, n-толуолсульфоновая кислота, и подобными им кислотами.
Предпочтительными соединениями согласно настоящему изобретению являются такие соединения формулы I, где R1 представляет собой 1,4-диоксепан-6-ил, и R2 является таким, как описано выше, например следующие соединения:
(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид морфолин-4-карбоновой кислоты,
(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид пиперидин-1-карбоновой кислоты,
1-циклогексил-3-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-1-метилмочевина,
(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид 4-гидроксиметил-пиперидин-1-карбоновой кислоты,
3-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-1-метил-1-(1-метил-пиперидин-4-ил)мочевина,
(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид 1,4-диокса-8-аза-спиро[4,5]декан-8-карбоновой кислоты,
(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид 4-гидроксипиперидин-1-карбоновой кислоты,
(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид 5-метилтиофен-2-карбоновой кислоты,
N-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-4-метоксибензамид,
N-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-4-фторбензамид,
(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид циклогексанкарбоновой кислоты,
N-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-2-(тетрагидропиран-4-ил)ацетамид,
(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид(R)-тетрагидрофуран-2-карбоновой кислоты,
(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид 3-метил-3Н-имидазол-4-карбоновой кислоты,
N-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)изоникотинамид,
N-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-2-метокси-изоникотинамид,
транс-1-(4-гидроксициклогексил)-3-(4-метокси-7-[1,4]диоксепан-6-ил-бензотиазол-2-ил)-1-метилмочевина,
(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид(1S,4S)-2окса-5-азабицикло[2,2,1]гептан-5-карбоновой кислоты,
(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид 4-метоксипиперидин-1-карбоновой кислоты,
4-хлорметил-N-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-бензамид,
(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид 1-метил-1Н-пиразол-4-карбоновой кислоты,
N-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-4-[(метил-пропионил-амино)метил]бензамид или
N-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-2-пирролидин-1-ил-изоникотинамид.
Кроме того, предпочтительными соединениями согласно настоящему изобретению являются такие соединения формулы I, где R1 представляет собой тетрагидропиран-4-ил, и R2 является таким, как описано выше, например следующие соединения:
3-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метил-1-(1-метилпиперидин-4-ил)мочевина,
транс-1-(4-гидроксициклогексил)-3-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метилмочевина,
цис-1-(4-гидроксициклогексил)-3-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метилмочевина,
1-(4-цис-гидрокси-4-метилциклогексил)-3-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метилмочевина,
3-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метил-1-(тетрагидропиран-4-ил)мочевина,
3-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метил-1-(тетрагидрофуран-3-илметил)мочевина,
(рац)-(экзо)-3-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метил-1-(7-оксабицикло[2,2,1]гепт-2-ил)мочевина,
(рац)(эндо)-3-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метил-1-(7-окса-бицикло[2,2,1]гепт-2-ил)мочевина,
[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]амид 4-изопропил-пиперазин-1-карбоновой кислоты,
[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]амид 1,4-диокса-8-аза-спиро[4,5]декан-8-карбоновой кислоты,
[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]амид 4-гидрокси-4-метил-пиперидин-1-карбоновой кислоты,
[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]амид (1S,4S)-2-окса-5-аза-бицикло[2,2,1]гептан-5-карбоновой кислоты,
[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]амид 2-аза-бицикло[2,2,2]октан-2-карбоновой кислоты,
N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-2-(тетрагидропиран-4-ил)ацетамид,
N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-2-морфолин-4-илметилизоникотинамид,
2-[(2-метоксиэтиламино)метил]-N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]изоникотинамид,
(транс)-2-(4-гидроксициклогексил)-N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]ацетамид,
[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]амид 4-гидроксиметилпиперидин-1-карбоновой кислоты,
(экзо)-(+)-3-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метил-1-(7-окса-бицикло[2,2,1]гепт-2-ил)мочевина или
(экзо)-(-)-3-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метил-1-(7-окса-бицикло[2,2,1]гепт-2-ил)мочевина.
Соединения формулы I согласно настоящему изобретению и их фармацевтически приемлемые соли могут быть получены с использованием методов, известных из предшествующего уровня техники, например, способом, который описан ниже, где указанный способ включает:
а) взаимодействие соединения формулы
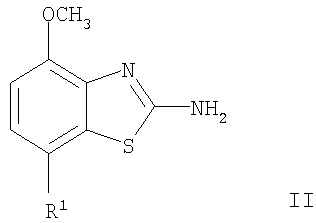
с соединением формулы
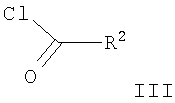
с получением при этом соединения формулы
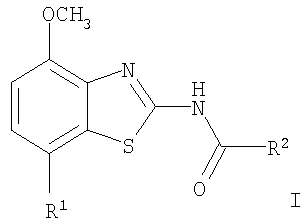
где R1 и R2 имеют значения, приведенные выше, или
б) взаимодействие соединения формулы
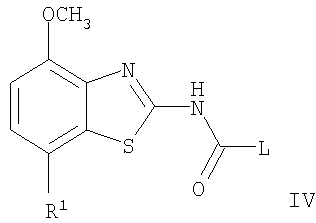
с соединением формулы
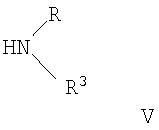
с получением при этом соединения формулы
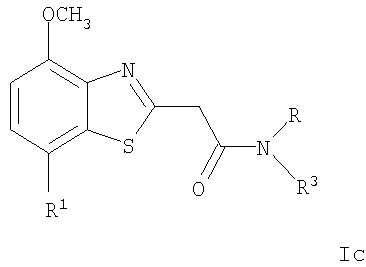
где R1 и R являются такими, как определено выше, L означает отщепляемую группу, такую как галоген, -O-фенил или O-низший алкил, и R3 представляет собой -(CH2)n-5- или 6-членный неароматический гетероцикл, необязательно замещенный одним или более заместителями, выбранными из группы, состоящей из низшего алкила или -NR2, или представляет собой циклоалкил, необязательно замещенный радикалом гидрокси или низший алкил, или представляет собой 7-окса-бицикло[2,2,1]гепт-2-ил; и если необходимо, превращение полученного соединения в фармацевтически приемлемые кислотно-аддитивные соли.
В примерах 1-56 и на приведенных ниже схемах 1-3 получение соединений формулы I описано более подробно.
Исходные вещества представляют собой известные соединения или могут быть получены согласно методикам, известным из предшествующего уровня техники.
Получение соединений формулы I
Получение соединения формулы Ia может быть описано следующим образом:
Схема 1
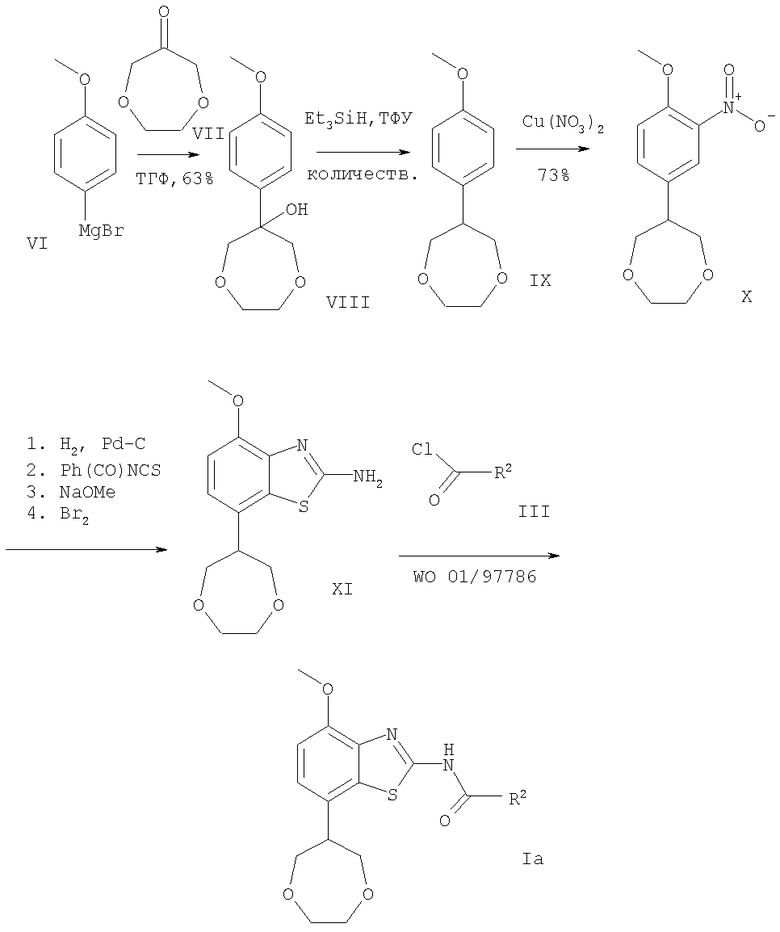
Получение соединений формулы (XI)
Промежуточное соединение 7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-иламин формулы (XI) может быть получено исходя из 6-(4-метокси-3-нитрофенил)-[1,4]диоксепана (X) в соответствии с методами, раскрытыми в опубликованной международной заявке WO 01/97786. Получение соединений формулы 1а также описано в опубликованной международной заявке WO 01/97786 и в конкретных примерах синтеза. Получение соединений формул (VIII), (IX) и (X) описано более подробно в примерах 36, 37 и 38.
Получение промежуточного соединения формулы XVII может быть представлено следующим образом:
Схема 2

Получение соединений формулы (XIV)
Производные арилбромида формулы (XIII) подвергают взаимодействию с небольшим избытком бис(пинаколято)диборона в органическом растворителе, предпочтительно диметилсульфоксиде, содержащем палладиевый катализатор, предпочтительно аддукт дихлор(1,1'-бис(дифенилфосфино)ферроцен)-палладий(II) дихлорметан, и избыток ацетата калия. Взаимодействие проводят при повышенной температуре, предпочтительно приблизительно при 80°С, в течение приблизительно 2-24 часов, предпочтительно в течение приблизительно 2 часов. Полученный продукт формулы (XIV) выделяют по общепринятым методикам и предпочтительно очищают посредством хроматографии или перекристаллизации.
Получение соединений формулы (XV)
Один из способов получения соединений формулы (XV) заключается в обработке соединения формулы (XIV) производным винилбромида, винилиодида или винилтрифлата в присутствии палладиевого катализатора, предпочтительно, такого как аддукт дихлор(1,1'-бис(дифенилфосфино)ферроцен)палладий(II) дихлорметан, и неорганического основания, предпочтительно, такого как карбонат натрия. Взаимодействие проводят в смеси растворителей, предпочтительно в смеси этанола, толуола и вода. Взаимодействие проводят при повышенной температуре, предпочтительно при приблизительно 80°С, в течение приблизительно 0,1-2 часов, предпочтительно в течение приблизительно 20 минут. Полученный продукт формулы (XV) выделяют по общепринятым методикам и предпочтительно очищают посредством хроматографии или перекристаллизации. Исходные соединения - производные винилбромида, винилиодида или винилтрифлата могут быть коммерчески доступными, например, от фирмы «Fluka», или могут быть получены согласно методикам, известным из предшествующего уровня техники.
Получение соединений формулы (XVI)
Соединения формулы (XVI) могут быть получены посредством гидрирования соединений формулы (XV) в присутствии катализатора гидрирования, предпочтительно такого, как 10%-ный палладий на углероде. Эти взаимодействия можно проводить в различных органических растворителях, например, таких как метанол, этанол или тетрагидрофуран, предпочтительно в метаноле, при комнатной температуре и давлении, составляющем одну атмосферу или более, в течение 16-72 часов, предпочтительно в течение приблизительно 72 часов. Полученный продукт формулы (XVI) выделяют по общепринятым методикам и предпочтительно очищают посредством хроматографии или перекристаллизации.
Получение соединений формулы (XVII)
Промежуточное соединение 4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-иламин формулы (XVII) может быть получено исходя из 2-метокси-5-(тетрагидропиран-4-ил)фениламина (XVI) в соответствии с методиками, раскрытыми в опубликованной международной заявке WO 01/97786. Получение соединений формулы Ib с использованием промежуточного соединения формулы (XVII) также описано в опубликованной международной заявке WO 01/97786.
Схема 3
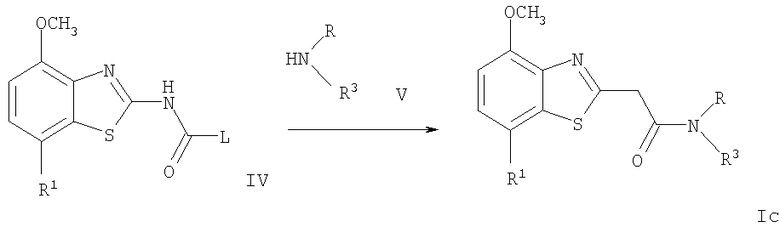
где R1 и R являются такими, как определено выше, L означает отщепляемую группу, такую как галоген, -O-фенил или O-низший алкил, и R3 представляет собой -(CH2)n-5- или 6-членный неароматический гетероцикл, необязательно замещенный одним или более заместителями, выбранными из группы, состоящей из низшего алкила или -NR2, или представляет собой циклоалкил, необязательно замещенный радикалом гидрокси или низший алкил, или представляет собой 7-окса-бицикло[2,2,1]гепт-2-ил;
В соответствии со схемой 3 соединения формулы Ic могут быть получены обычным образом из промежуточного соединения формулы IV (известные соединения, описанные в опубликованной международной заявке WO 01/97786), как описано более подробно в примерах.
Выделение и очистка соединений
Выделение и очистка соединений и промежуточных соединений, описанных в тексте настоящей заявки, могут быть выполнены, если необходимо, с использованием любой подходящей методики разделения или очистки, например такой, как фильтрация, экстракция, кристаллизация, колоночная хроматография, тонкослойная хроматография, хроматография в толстом слое, препаративная хроматография низкого или высокого разрешения или жидкостная хроматография при высоком давлении, или с использованием комбинации этих методик. Конкретные иллюстрации использования подходящих методик разделения и выделения можно найти в разделе, посвященном синтезу и примерам конкретного выполнения ниже в тексте настоящей заявки. Однако, безусловно, могут быть использованы и другие эквивалентные методики разделения и выделения.
Соли соединений формулы I
Соединения формулы I могут быть основного характера, например, в тех случаях, когда остаток R содержит группу основного характера, например такую, как фрагмент алифатического или ароматического амина. В таких случаях соединения формулы I могут быть превращены в соответствующую кислотно-аддитивную соль (продукт присоединения кислоты).
Превращение осуществляют посредством обработки по меньшей мере стехиометрическим количеством соответствующей кислоты, например, такой как хлороводородная кислота, бромоводородная кислота, серная кислота, азотная кислота, фосфорная кислота и подобные кислоты, и такой как органическая кислота, например уксусная кислота, пропионовая кислота, гликолевая кислота, пировиноградная кислота, щавелевая кислота, яблочная кислота, малоновая кислота, янтарная кислота, малеиновая кислота, фумаровая кислота, винная кислота, лимонная кислота, бензойная кислота, коричная (β-фенилакриловая) кислота, миндальная кислота, метансульфоновая кислота, этансульфоновая кислота, n-толуолсульфоновая кислота, салициловая кислота и подобные кислоты. Обычно свободное основание растворяют в инертном органическом растворителе, например, таком как диэтиловый эфир, этилацетат, хлороформ, этанол или метанол и подобном им, и добавляют кислоту в подобном растворителе. Температуру поддерживают в интервале от 0°С до 50°С. Полученная соль выпадает в осадок спонтанно или может быть выделена из раствора с использованием менее полярного растворителя.
Аддитивные соли с кислотами соединений основного характера формулы I могут быть превращены в соответствующие свободные основания посредством обработки по меньшей мере стехиометрическим эквивалентом подходящего основания, например, такого как гидроксид натрия или калия, карбонат калия, бикарбонат натрия, аммиак, и тому подобного основания.
Соединения формулы I и их фармацевтически приемлемые аддитивные соли с кислотами обладают ценными фармакологическими свойствами. А именно, было показано, что соединения согласно настоящему изобретению являются лигандами аденозинового рецептора и обладают высоким сродством по отношению к аденозиновому A2A рецептору.
Соединения были исследованы в соответствии с приведенными ниже методиками тестирования.
Аденозиновый A2A рецептор человека
Аденозиновый A2A рецептор человека рекомбинантно экспрессируют в клетках яичника китайского хомячка (СНО) с использованием системы экспрессии вируса semliki forest. Клетки собирают, дважды промывают посредством центрифугирования, гомогенизируют и снова промывают посредством центрифугирования. Промытый осадок мембранной фракции суспендируют в Трис-буферном растворе (50 мМ), содержащем 120 мМ NaCl, 5 мМ KCl, 2 мМ CaCl2 и 10 мМ MgCl2 (pH 7,4) (буфер А). Исследование связывания [3H]-SCH-58261 (Dionisotti et al., 1997, Br J Pharmacol 121, 353; 1 нМ) проводят в 96-луночных планшетах в присутствии 2,5 мкг мембранного белка, 0,5 мг Ysi-поли-1-лизин-SPA гранул и 0,1 Ед. аденозиндеаминазы в конечном объеме буфера А, составляющем 200 мкл. Неспецифическое связывание определяют с использованием соединения того же класса - ксантинамина (ХАС; 2 мкМ). Соединения анализируют при 10 концентрациях от 10 мкМ до 0,3 нМ. Все исследования проводят в двух параллельных сериях и анализ повторяют по меньшей мере два раза. Планшеты, в которых проводят исследование, инкубируют в течение 1 часа при комнатной температуре перед центрифугированием и затем связанный лиганд определяют с использованием сцинтилляционного счетчика «Packard Topcount». Значения IC50 рассчитывают с использованием программы нелинейной аппроксимации, а значения Ki рассчитывают по уравнению Ченга-Прусоффа.
Значения pKi для соединений согласно настоящему изобретению находятся в интервале 7,5-9,0. Для предпочтительных соединений значения pKi>8,5.
Соединения формулы I и фармацевтические соли соединений формулы I могут быть использованы в качестве лекарственных средств, например в виде фармацевтических препаратов. Фармацевтические препараты могут быть введены перорально, например в виде таблеток, таблеток с покрытием, драже, твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий. Кроме того, введение эффективно может быть осуществлено ректально, например в виде суппозиториев, парентерально, например в виде растворов для инъекций.
Соединения формулы I могут быть использованы вместе с фармацевтически инертными, неорганическими или органическими носителями для получения фармацевтических композиций. В качестве носителей для таблеток, таблеток с покрытием, драже и твердых желатиновых капсул могут быть использованы, например, лактоза, кукурузный крахмал или его производные, тальк, стеариновые кислоты или их соли и тому подобные соединения. Подходящие носители для мягких желатиновых капсул представляют собой, например, растительные масла, воски, жиры, полутвердые и жидкие полиолы и тому подобные соединения. Однако в зависимости от природы активного соединения в случае мягких желатиновых капсул носитель может и не использоваться. Подходящие носители для получения растворов и сиропов представляют собой, например, воду, полиолы, глицерин, растительное масло и тому подобные соединения. Подходящие носители для суппозиториев представляют собой, например, природные или отвержденные масла, воски, жиры, полужидкие или жидкие полиолы и тому подобные соединения.
Фармацевтические композиции, кроме того, могут содержать консерванты, солюбилизаторы, стабилизаторы, агенты, улучшающие смачиваемость, эмульгаторы, подсластители, подкрашивающие вещества, агенты, улучшающие вкус и запах, соли для регулирования осмотического давления, буферы, маскирующие агенты или антиоксид анты. Также они могут содержать и другие терапевтически значимые соединения.
Лекарственные средства, содержащие соединение формулы I или его фармацевтически приемлемую соль и терапевтически инертный носитель, также являются объектом настоящего изобретения, так же как и способ их получения, который включает введение одного или более соединения формулы I и/или фармацевтически приемлемой аддитивной соли с кислотой и, если необходимо, одного или более терапевтически значимого вещества в состав лекарственного препарата вместе с одним или более терапевтически инертным носителем.
В соответствии с настоящим изобретением соединения формулы I, а также их фармацевтически приемлемые соли можно использовать для контроля или профилактики заболеваний, связанных с агонистической активностью в отношении аденозинового рецептора, например таких, как болезнь Альцгеймера, болезнь Паркинсона, болезнь Хантингтона, нейропротективное действие, шизофрения, беспокойство, боль, дефицит дыхания, депрессия, астма, аллергические реакции, гипоксия, ишемия, припадки и злоупотребление алкоголем или наркотиками. Кроме того, соединения согласно настоящему изобретению могут быть полезны в качестве седативных средств, мышечных релаксантов, антипсихотических средств, противоэпилептических средств, противосудорожных средств и кардиопротекторных средств и для получения соответствующих лекарственных средств.
Наиболее подходящие показания согласно настоящему изобретению - это показания, которые включают нарушения или расстройства центральной нервной системы, например такие показания, как лечение или профилактика некоторых депрессивных нарушений или расстройств, нейропротективное действие и болезнь Паркинсона.
Дозировка может варьироваться в широких пределах и будет, безусловно, регулироваться в зависимости от индивидуальных требований в каждом конкретном случае. В случае перорального введения дозировка для взрослых может варьироваться от приблизительно 0,01 мг до приблизительно 1000 мг в день соединения общей формулы I или соответствующего количества его фармацевтически приемлемой соли. Дневная дозировка может быть введена в виде одной дозы или разделенной на несколько доз и, в дополнение к этому, может быть превышен верхний предел, если обнаружится, что это необходимо по показаниям.
Изготовление таблеток (влажное гранулирование)
Методика получения
1. Смешивают соединения по позициям 1, 2, 3 и 4 и проводят гранулирование, используя очищенную воду.
2. Высушивают гранулы при 50°С.
3. Пропускают гранулы через подходящее устройство для размола.
4. Добавляют вещество согласно позиции 5 и перемешивают в течение трех минут, затем прессуют, используя подходящий пресс.
Получение капсул
Методика приготовления
1. Смешивают соединения по позициям 1, 2 и 3 в подходящем смесителе в течение 30 минут.
2. Добавляют соединения согласно позициям 4 и 5 и смешивают в течение 3 минут.
3. Помещают в подходящие капсулы.
Приведенные ниже подготовительные примеры и примеры служат только для иллюстрации изобретения и, как предполагается, не ограничивают объем настоящего изобретения.
Пример 1
(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид морфолин-4-карбоновой кислоты
7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-иламин сначала подвергают взаимодействию с фенилхлороформиатом, как описано в отношении бензилового эфира (4-метокси-7-фенил-бензотиазол-2-ил)карбаминовой кислоты в опубликованной международной заявке WO 01/97786, и затем с морфолином. После обычного выделения, препаративной обращенно-фазовой ЖХВР и заключительной сублимационной сушки получают указанное в заголовке соединение в виде светло-коричневого порошка. Масс-спектр: m/е=394(М+Н+).
В соответствии с общей методикой, описанной в примере 1, получают соединения согласно примерам 2-7.
Пример 2
(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид пиперидин-1-карбоновой кислоты
Используя 7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-иламин, фенилхлороформиат и пиперидин, указанное в заголовке соединение получают в виде светло-желтого порошка. Масс-спектр: m/е=392(М+Н+).
Пример 3
1-Циклогексил-3-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-1-метилмочевина
Используя 7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-иламин, фенилхлороформиат и циклогексилметиламин, указанное в заголовке соединение получают в виде легкого не совсем белого порошка. Масс-спектр: m/е=420(M+H+).
Пример 4
(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид 4-гидроксиметилпиперидин-1-карбоновой кислоты
Используя 7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-иламин, фенилхлороформиат и 4-гидроксиметилпиперидин, указанное в заголовке соединение получают в виде не совсем белого порошка. Масс-спектр: m/е=422(M+H+).
Пример 5
3-(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)-1-метил-1-(1-метил-пиперидин-4-ил)мочевина
Используя 7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-иламин, фенилхлороформиат и 1-метил-4-(метиламино)пиперидин, указанное в заголовке соединение получают в виде светло-коричневого порошка. Масс-спектр: m/е=435(M+H+).
Пример 6
(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид 1,4-диокса-8-аза-спиро[4,5]декан-8-карбоновой кислоты
Используя 7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-иламин, фенилхлороформиат и 1,4-диокса-8-аза-спиро[4,5]декан, указанное в заголовке соединение получают в виде не совсем белого порошка. Масс-спектр: m/е=450(M+H+).
Пример 7
(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид 4-гидроксипиперидин-1-карбоновой кислоты
Используя 7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-иламин, фенилхлороформиат и 4-гидроксипиперидин, указанное в заголовке соединение получают в виде не совсем белого порошка. Масс-спектр: m/e=408(М+Н+).
Пример 8
(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид 5-метилтиофен-2-карбоновой кислоты
7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-иламин и 5-метилтиофен-2-карбоновой кислоты подвергают взаимодействию, как описано в отношении N-(4-метокси-7-фенил-бензотиазол-2-ил)бензамида в опубликованной международной заявке WO 01/9786. После обычного выделения, препаративной обращенно-фазовой ЖХВР и заключительной сублимационной сушки получают указанное в заголовке соединение в виде белого порошка. Масс-спектр: m/e=405 (М+Н+).
Соединения согласно примерам 9-16 получают в соответствии с общей методикой, описанной в примере 1.
Пример 9
N-(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)-4-метоксибензамид
Используя 7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-иламин и 4-метоксибензойную кислоту, указанное в заголовке соединение получают в виде белого порошка. Масс-спектр: m/e=415(М+Н+).
Пример 10
N-(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)-4-фторбензамид
Используя 7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-иламин и 4-фторбензойную кислоту, указанное в заголовке соединение получают в виде белого порошка. Масс-спектр: m/e=403(М+Н+).
Пример 11
(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид циклогексанкарбоновой кислоты
Используя 7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-иламин и циклогексанкарбоновую кислоту, указанное в заголовке соединение получают в виде белого порошка. Масс-спектр: m/e=391(М+Н+).
Пример 12
N-(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)-2-(тетрагидропиран-4-ил)ацетамид
Используя 7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-иламин и тетрагидропиран-4-ил уксусную кислоту, указанное в заголовке соединение получают в виде белого порошка. Масс-спектр: m/e=407(М+Н+).
Пример 13
(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид(R)-тетрагидрофуран-2-карбоновой кислоты
Используя 7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-иламин и (R)-тетрагидрофуран-2-карбоновую кислоту, указанное в заголовке соединение получают в виде белого порошка. Масс-спектр: m/e=379(М+Н+).
Пример 14
(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид 3-метил-3Н-имидазол-4-карбоновой кислоты
Используя 7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-иламин и 3-метил-3Н-имидазол-4-карбоновую кислоту, получают указанное в заголовке соединение. Масс-спектр: m/e=389(M+H+).
Пример 15
N-(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)-изоникотинамид
Используя 7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-иламин и изоникотиновую кислоту, получают указанное в заголовке соединение. Масс-спектр: m/e=386(M+H+).
Пример 16
N-(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)-2-метокси-изоникотинамид
Используя 7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-иламин и 2-метоксиизоникотиновую кислоту, получают указанное в заголовке соединение. Масс-спектр: m/e=416(M+H+).
Соединения согласно примерам 17-34 получают в соответствии с общей методикой, описанной в примере 1.
Пример 17
транс1-(4-Гидроксициклогексил)-3-(4-метокси-7-[1,4]диоксепан-6-ил-бензотиазол-2-ил)-1-метилмочевина
Используя 7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-иламин, фенилхлороформиат и транс-4-метиламиноциклогексанол, указанное в заголовке соединение получают в виде не совсем белого твердого вещества. Масс-спектр: m/e=452(M+H+).
Пример 18
(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид (1S,4S)-2-окса-5-аза-бицикло[2,2,1]гептан-5-карбоновой кислоты
Используя 7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-иламин, фенилхлороформиат и (1S,4S)-2окса-5-аза-бицикло[2,2,1]гептан, указанное в заголовке соединение получают в виде не совсем белого твердого вещества. Масс-спектр: m/e=422(M+H+).
Пример 19
(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид 4-метоксипиперидин-1-карбоновой кислоты
Используя 7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-иламин, фенилхлороформиат и 4-метоксипиперидин, указанное в заголовке соединение получают в виде не совсем белого твердого вещества. Масс-спектр: m/e=438(M+H+).
Пример 20
3-[4-Метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метил-1-(1-метилпиперидин-4-ил)мочевина
Используя 4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-иламин, фенилхлороформиат и 1-метил-4-(метиламино)пиперидин, указанное в заголовке соединение получают в виде белых кристаллов (выход 56%). Масс-спектр: m/e=419(M+H+), т. пл. 152-155°С.
Пример 21
транс-1-(4-Гидроксициклогексил)-3-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метилмочевина
Используя 4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-иламин, фенилхлороформиат и (транс)-4-метиламиноциклогексанол, указанное в заголовке соединение получают в виде белых кристаллов, т. пл. 160°С (выход 76%). Масс-спектр: m/e=420(M+H+), т. пл. 160°С.
Пример 22
цис-1-(4-Гидроксициклогексил)-3-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метилмочевина
Используя 4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-иламин, фенилхлороформиат и (цис)-4-метиламиноциклогексанол, указанное в заголовке соединение получают в виде белого твердого вещества (выход 70%). Масс-спектр: m/e=420(M+H+), т. пл. 191-193°С.
Пример 23
1-(4-цис-Гидрокси-4-метилциклогексил)-3-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метилмочевина
Используя 4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-иламин, фенилхлороформиат и (цис)-1-метил-4-метиламиноциклогексанол, указанное в заголовке соединение получают в виде белого порошка (выход 64%). Масс-спектр: m/e=434(M+H+), т. пл. 211-213°С.
Пример 24
3-[4-Метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метил-1-(тетрагидропиран-4-ил)мочевина
Используя 4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-иламин, фенилхлороформиат и метил-(тетрагидропиран-4-ил)амин, указанное в заголовке соединение получают в виде белого твердого вещества (выход 16%). Масс-спектр: m/e=406(M+H+), т. пл. 237-238°С.
Пример 25
3-[4-Метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метил-1-(тетрагидрофуран-3-илметил)мочевина
Используя 4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-иламин, фенилхлороформиат и метил-(тетрагидрофуран-3-илметил)амин, указанное в заголовке соединение получают в виде белых кристаллов (выход 80%). Масс-спектр: m/e=406(M+H+), т. пл. 185-186°С.
Пример 26
(рац)-(экзо)-3-[4-Метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метил-1-(7-окса-бицикло[2,2,1]гепт-2-ил)мочевина
Используя 4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-иламин, фенилхлороформиат и (экзо)метил-(7-оксабицикло[2,2,1]гепт-2-ил)амин, указанное в заголовке соединение получают в виде белых кристаллов (выход 93%). Масс-спектр: m/e=418(M+H+), т. пл. 197-200°С.
Пример 27
(рац)(эндо)-3-[4-Метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метил-1-(7-окса-бицикло[2,2,1]гепт-2-ил)мочевина
Используя 4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-иламин, фенилхлороформиат и (эндо)-метил-(7-окса-бицикло[2,2,1]гепт-2-ил)амин, указанное в заголовке соединение получают в виде белых кристаллов (выход 45%). Масс-спектр: m/e=418(M+H+), т. пл. 214-216°С.
Пример 28
[4-Метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]амид 4-изопропилпиперазин-1-карбоновой кислоты
Используя 4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-иламин, фенилхлороформиат и 1-изопропилпиперазин, указанное в заголовке соединение получают в виде светло-желтых кристаллов (выход 36%). Масс-спектр: m/e=419(M+H+), т. пл. 200-204°С.
Пример 29
[4-Метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]амид 1,4-диокса-8-азаспиро[4,5]декан-8-карбоновой кислоты
Используя 4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-иламин, фенилхлороформиат и 1,4-диокса-8-аза-спиро[4,5]декан, указанное в заголовке соединение получают в виде белых кристаллов (выход 53%). Масс-спектр: m/e=434(M+H+), т. пл. 208-209°С.
Пример 30
[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]амид 4-гидрокси-4-метил-пиперидин-1-карбоновой кислоты
Используя 4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-иламин, фенилхлороформиат и 4-гидрокси-4-метилпиперидин, указанное в заголовке соединение получают в виде не совсем белого твердого вещества (выход 56%). Масс-спектр: m/e=406(M+H+), т. пл. 90-95°С.
Пример 31
[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]амид (1S,4S)-2-окса-5-аза-бицикло[2,2,1]гептан-5-карбоновой кислоты
Используя 4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-иламин, фенилхлороформиат и (1S,4S)-2-аза-5-оксабицикло-[2,2,1]гептан, указанное в заголовке соединение получают в виде белых кристаллов (выход 52%). Масс-спектр: m/e=390(M+H+), т. пл. 193-197°С.
Пример 32
[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]амид 2-аза-бицикло[2,2,2]октан-2-карбоновой кислоты
Используя 4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-иламин, фенилхлороформиат и 2-аза-бицикло[2,2,2]октан, указанное в заголовке соединение получают в виде не совсем белых кристаллов (выход 53%). Масс-спектр: m/e=402(M+H+), т. пл. 237-239°С.
Пример 33
N-[4-Метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-2-(тетрагидропиран-4-ил)ацетамид
Используя 4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-иламин и (тетрагидропиран-4-ил)уксусную кислоту, указанное в заголовке соединение получают в виде светло-желтых кристаллов (выход 17%). Масс-спектр: m/e=391(M+H+), т. пл. 218-220°С.
Пример 34
N-[4-Метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-2-морфолин-4-илметилизоникотинамид
2-Хлорметил-N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-изоникотинамид (300 мг, 0,7 ммоль) и морфолин (2,1 мл, 25 ммоль) нагревают до 30°С в течение 30 мин. Затем полученную смесь охлаждают до комнатной температуры, обрабатывают дихлорметаном (15 мл) и насыщенным водным раствором карбонат натрия (15 мл), фазы разделяют и полученный водный слой экстрагируют два раза дихлорметаном. Объединенные органические фазы высушивают над сульфатом натрия и концентрируют в вакууме. После экспресс-хроматографии (силикагель, элюент - смесь хлороформ/этилацетат, затем смесь хлороформ/метанол) получают указанное в заголовке соединение в виде белого твердого вещества (выход 60%). Масс-спектр: m/e=469(M+H+), т. пл. 199-201°С.
Пример 35
2-[(2-Метоксиэтиламино)метил]-N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]изоникотинамид
Указанное в заголовке соединение получают из 2-хлорметил-N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]изоникотинамида и 2-метокси-этиламина точно таким же образом, как описано в отношении N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-2-морфолин-4-илметил-изоникотинамида, соединение получают в виде желтого твердого вещества (выход 60%). Масс-спектр: m/e=457(M+H+), т. пл. 93-95°С.
2-Хлорметил-N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-изоникотинамид получают из 4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-иламина и 2-хлорметилизоникотиновой кислоты точно таким же образом, как описано в отношении (7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амида 5-метилтиофен-2-карбоновой кислоты, получая при этом светло-желтое твердое вещество (выход 60%). Масс-спектр: m/e=419(M+H+).
Пример 36
(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид 1-окса-8-азаспиро[4,5]декан-8-карбоновой кислоты
Используя 7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-иламин, фенилхлороформиат и 1-окса-8-азаспиро[4,5]декан, указанное в заголовке соединение получают в виде светло-коричневого порошка. Масс-спектр: m/e=448(M+H+).
Пример 37
(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид 4-гидроксиметил-4-метил-пиперидин-1-карбоновой кислоты
Используя 7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-иламин, фенилхлороформиат и 4-гидроксиметил-4-метил-пиперидин, указанное в заголовке соединение получают в виде светло-коричневого порошка. Масс-спектр: m/e=436(M+H+).
Пример 38
N-(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)-4-фтор-3-метил-бензамид
Используя 7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-иламин и 4-фтор-3-метилбензойную кислоту, указанное в заголовке соединение получают точно таким же образом, как описано для (7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амида 5-метилтиофен-2-карбоновой кислоты, соединение получают в виде светло-коричневого порошка. Масс-спектр: m/e=417(M+H+).
Пример 39
4-Хлорметил-N-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-бензамид
Используя 7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-иламин и 4-хлорметилбензойную кислоту, указанное в заголовке соединение получают точно таким же образом, как описано в отношении (7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амида 5-метилтиофен-2-карбоновой кислоты, соединение получают в виде светло-коричневого порошка. Масс-спектр: m/e=434(M+H+).
Пример 40
N-(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)-4-пирролидин-1-илметилбензамид
4-Хлорметил-N-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-бензамид и пирролидин подвергают взаимодействию таким образом, как описано в отношении N-(4-метокси-7-фенил-бензотиазол-2-ил)-4-пирролидин-1-илметил-бензамида в опубликованной международной заявке WO 01/9786. После обычного выделения, препаративной обращенно-фазовой ЖХВР и заключительной сублимационной сушки получают указанное в заголовке соединение в виде светло-коричневого порошка. Масс-спектр: m/e=468(M+H+).
Пример 41
2-Хлорметил-N-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-изоникотинамид
Используя 7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-иламин и 2-хлорметилизоникотиновую кислоту, указанное в заголовке соединение получают точно таким же образом, как описано в отношении (7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амида 5-метилтиофен-2-карбоновой кислоты, соединение получают в виде коричневого твердого вещества. Масс-спектр: m/e=435(M+H+).
Пример 42
N-(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)-4-{[(2-метокси-этил)метил-амино]метил}бензамид
4-Хлорметил-N-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-бензамид и N-(2-метоксиэтил)метиламин подвергают взаимодействию таким же образом, как описано в отношении N-(4-метокси-7-фенил-бензотиазол-2-ил)-4-пирролидин-1-илметилбензамида в опубликованной международной заявке WO 01/97786. После обычного выделения, препаративной обращенно-фазовой ЖХВР и заключительной сублимационной сушки получают указанное в заголовке соединение в виде светло-коричневого порошка. Масс-спектр: m/e=486(M+H+).
Пример 43
(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид 1-метил-1Н-пиразол-4-карбоновой кислоты
Используя 7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-иламин и 1-метил-1H-пиразол-4-карбоновую кислоту, указанное в заголовке соединение получают точно таким же образом, как описано в отношении (7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амида 5-метилтиофен-2-карбоновой кислоты, соединение получают в виде белого твердого вещества. Масс-спектр: m/e=389(M+H+).
Пример 44
N-(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)-4-[(метил-пропиониламино)метил]бензамид
Гидрид натрия (4,8 мг, 60%-ная дисперсия в минеральном масле, 0,2 ммоль) добавляют к N-метилпропионамиду (1 мл, 11 ммоль), а затем добавляют 4-хлорметил-N-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)бензамид (50 мг, 1, ммоль), после чего полученную реакционную смесь нагревают до 55°С в течение 3 часов. После охлаждения полученную смесь разбавляют водой (5 мл) и экстрагируют два раза этилацетатом (5 мл). Объединенные органические фазы высушивают сульфатом магния, фильтруют и упаривают. После окончательной очистки с использованием препаративной ЖХВР и заключительной сублимационной сушки получают указанное в заголовке соединение в виде белого твердого вещества (23 мг, выход 42%). Масс-спектр: m/e=484(M+H+).
Пример 45
N-(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)-2-[(2-метокси-этил)метиламино]изоникотинамид
N-(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)бром-изоникотинамид и N-(2-метоксиэтил)метиламин подвергают взаимодействию таким образом, как описано в отношении 2-(2-метоксиэтиламино)-N-(4-метокси-7-морфолин-4-ил-бензотиазол-2-ил)изоникотинамида в опубликованной международной заявке WO 03/043636. После обычного выделения, препаративной обращенно-фазовой ЖХВР и заключительной сублимационной сушки получают указанное в заголовке соединение в виде светло-коричневого твердого вещества. Масс-спектр: m/e=473(M+H+).
Пример 46
N-(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)-2-пирролидин-1-ил-изоникотинамид
N-(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)бром-изоникотинамид и пирролидин подвергают взаимодействию таким образом, как описано в отношении 2-(2-метокси-этиламино)-N-(4-метокси-7-морфолин-4-ил-бензотиазол-2-ил)изоникотинамида в опубликованной международной заявке WO 03/043636. После обычного выделения, препаративной обращенно-фазовой ЖХВР и заключительной сублимационной сушки получают указанное в заголовке соединение в виде светло-коричневого твердого вещества. Масс-спектр: m/e=455(M+H+).
Пример 47
NM-(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)-2-пирролидин-1-илметилизоникотинамид
2-Хлорметил-N-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-изоникотинамид и N-(2-метоксиэтил)метиламин подвергают взаимодействию таким же образом, как описано в отношении 2-{[(2-метоксиэтил)метиламино]-метил}-N-(4-метокси-7-морфолин-4-ил-бензотиазол-2-ил)-изоникотинамида в опубликованной международной заявке WO 03/043636. После обычного выделения, препаративной обращенно-фазовой ЖХВР и заключительной сублимационной сушки получают указанное в заголовке соединение в виде светло-желтого твердого вещества (выход 48%). Т. пл. 108-111°С, масс-спектр: m/e=469(M+H+).
Пример 48
N-(7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-ил)-2-{[(2-метоксиэтил)метиламино]метил}изоникотинамид
2-Хлорметил-N-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-изоникотинамид и пирролидин подвергают взаимодействию таким же образом, как описано в отношении 2-{[(2-метоксиэтил)метиламино]метил}-N-(4-метокси-7-морфолин-4-ил-бензотиазол-2-ил)изоникотинамида в опубликованной международной заявке WO 03/043636. После обычного выделения, препаративной обращенно-фазовой ЖХВР и заключительной сублимационной сушки получают указанное в заголовке соединение в виде светло-коричневого твердого вещества (выход 56%). Т. пл. 100-107°С, масс-спектр: m/e=487(M+H+).
Пример 49
2-Бром-N-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-изоникотинамид
Используя 7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-иламин и 2-бром-изоникотиновую кислоту, указанное в заголовке соединение получают таким же образом, как описано в отношении (7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амида 5-метилтиофен-2-карбоновой кислоты, соединение получают в виде не совсем белого порошка. Масс-спектр: m/e=452(M+H+).
Пример 50
(транс)-2-(4-Гидроксициклогексил)-N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]ацетамид
Используя 4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-иламин и (4-гидроксициклогексил)уксусную кислоту, указанное в заголовке соединение получают таким же образом, как описано в отношении N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-2-(тетрагидропиран-4-ил)ацетамида, соединение получают в виде белых кристаллов (выход 25%). Т. пл. 120-145°С, масс-спектр: m/e=405 (M+H+).
Пример 51
[4-Метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]амид (R)-тетрагидрофуран-2-карбоновой кислоты
Используя 4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-иламин и (R)-тетрагидрофуран-2-карбоновую кислоту, указанное в заголовке соединение получают таким же образом, как описано в отношении N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-2-(тетрагидропиран-4-ил)ацетамида, соединение получают в виде не совсем белого твердого вещества (выход 62%). Т. пл.158-161°С, масс-спектр: m/e=363(M+H+).
Пример 52
[4-Метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]амид 4-гидроксиметилпиперидин-1-карбоновой кислоты
Используя 4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-иламин, фенилхлороформиат и 4-гидроксиметил-пиперидин, указанное в заголовке соединение получают в виде белых кристаллов (выход 87%). Т. пл. 202-203,5°С, масс-спектр: m/e=406(M+H+).
Пример 53
1-(1-Диметиламинопиперидин-4-ил)-3-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метилмочевина
Используя 4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-иламин, фенилхлороформиат и N,N,N'-триметил-пиперидин-1,4-диамин, указанное в заголовке соединение получают в виде белых кристаллов (выход 77%). Т. пл. 167-170°С, масс-спектр: m/e=448(M+H+).
Пример 54
N-[4-Метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-2-(тетрагидрофуран-2-ил)ацетамид
Используя 4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-иламин и (тетрагидрофуран-2-ил)уксусную кислоту, указанное в заголовке соединение получают таким же образом, как описано в отношении N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-2-(тетрагидропиран-4-ил)ацетамида, соединение получают в виде белого твердого вещества (выход 50%). Т. пл. 170-174°С, масс-спектр: m/e=377(М+Н+).
Пример 55
(экзо)-(+)-3-[4-Метокси-7-(тетрагидропиран-4-ил)бензотаазол-2-ил]-1-метил-1-(7-оксабицикло[2,2,1]гепт-2-ил)мочевина
Используя 4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-иламин, фенилхлороформиат и (экзо)метил-(7-оксабицикло[2,2,1]гепт-2-ил)амин, указанное в заголовке соединение получают в виде рацемата. После хирального разделения с использованием «Chiralpak AD» (элюент 20% EtOH в гептане) получают первый элюируемый изомер в виде белых кристаллов (выход 39%). Т. пл. 185-188°С, масс-спектр: m/e=418(M+H+).
Пример 56
(экзо)-(-)-3-[4-Метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метил-1-(7-оксабицикло[2,2,1]гепт-2-ил)мочевина
Используя 4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-иламин, фенилхлороформиат и (экзо)метил-(7-окса-бицикло[2,2,1]гепт-2-ил)амин, указанное в заголовке соединение получают в виде рацемата. После хирального разделения с использованием «Chiralpak AD» (элюент 20% EtOH в гептане) получают второй элюируемый изомер в виде белого твердого вещества (выход 29%). Т. пл. 155-190°С, масс-спектр: m/e=418(M+H+).
Промежуточные соединения
Пример 57
6-(4-метоксифенил)-[1,4]-диоксепан-6-ол (VIII)
Магний (1,27 г, 0,053 моль) высушивают термостате в течение 1 часа при 75°С, перемешивают с ТГФ (125 мл) в трехгорлой колбе емкостью 500 мл при нагревании с обратным холодильником. Добавляют кристаллический иод, а затем добавляют по каплям раствор 4-метоксибромбензола в ТГФ (50 мл) в течение 15 мин. После добавления 10 мл раствора начинается взаимодействие. После добавление всего раствора реакционную смесь кипятят с обратным холодильником в течение 2 часов. Полученный серый раствор охлаждают до 0°С и затем добавляют по каплям раствор 1,4-диоксепан-6-она (получен таким образом, как описано в патенте США 4410354) (5,08 г, 0,044 моль) в ТГФ (25 мл). Реакционную смесь перемешивают при комнатной температуре в течение ночи, затем упаривают. Полученный остаток подкисляют до рН 1, используя 1 Н раствор HCl, и затем экстрагируют эфиром (2×250 мл). Эфирные экстракты промывают водой, высушивают (MgSO4), фильтруют и концентрируют, получая при этом липкое коричневое твердое вещество (9,45 г). Это соединение очищают колоночной хроматографией на силикагеле, элюируя смесью этилацетат-гексан. Соответствующие фракции концентрируют, получая при этом целевой продукт (6,21 г, выход 63%).
Пример 58
6-(4-метоксифенил)-[1,4]диоксепан (IX)
К раствору 6-(4-метоксифенил)-[1,4]-диоксепан-6-ол (6,20 г, 0,028 моль) в CH2Cl2 добавляют триэтилсилан (3,53 г, 0,031 моль) и трифторуксусную кислоту (35,1 г, 0,31 моль). Реакционную смесь перемешивают в течение ночи. Затем реакционную смесь подщелачивают, используя раствор К2СО3, до рН 10. Органический слой высушивают (MgSO4), фильтруют и упаривают досуха, получая при этом целевой продукт в виде красного маслянистого вещества (5,84 г, выход 100%).
Пример 59
6-(4-Метокси-3-нитрофенил)-1,4-диоксепан (X)
Раствор 6-(4-метоксифенил)-1,4-диоксепана (5,84 г, 0,028 моль) и уксусного ангидрида (40 мл) в трехгорлой колбе емкостью 100 мл нагревают до 65°С. Нагревание прекращают и добавляют порциями нитрат меди(II) (7,7 г, 0,033 моль) в течение 2 часов, пока температура не достигнет 60-70°С (внимание: реакция экзотермична). После окончания добавления синюю суспензию перемешивают при 65°С дополнительно в течение 1,5 ч. Добавляют воду (400 мл) и перемешивают реакционную смесь в течение 1 часа, затем добавляют твердый К2СО3 до рН 10. Полученную смесь экстрагируют этилацетатом (3×150 мл). Объединенные органические слои высушивают (MgSO4), фильтруют и упаривают, получая при этом красное маслянистое вещество (7,37 г). Неочищенный продукт очищают колоночной хроматографией, элюируя смесью 20%-30% EtOAc-гексан. Соответствующие фракции объединяют и концентрируют, получая при этом целевой продукт в виде оранжевого маслянистого вещества (5,80 г, выход 83%). Масс-спектр: m/e=254(M+H+).
Пример 60
7-[1,4]Диоксепан-6-ил-4-метоксибензотиазол-2-иламин (XI)
Указанное в заголовке соединение получают из 6-(4-метокси-3-нитрофенил)-1,4-диоксепана по точно такой же методике, как описано в опубликованной международной заявке WO 01/97786 в отношении 4-метокси-7-феноксибензотиазол-2-ил-амина, выход 57% (3,7 г). Масс-спектр: m/e=281(M+H+).
Пример 61
4-Метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-иламин (XVII)
а) 2-(4-Метокси-3-нитрофенил)-4,4,5,5-тетраметил-[1,3,2]диоксаборолан
К перемешиваемому раствору 1,30 г (5,60 ммоль) 4-бром-2-нитроанизола в 25 мл ДМСО добавляют 1,57 г (6,16 ммоль) бис(пинаколято)диборона, 123 мг (0,17 ммоль) аддукта-дихлор(1,1'-бис(дифенилфосфино)ферроцен)палладий(II) - дихлорметан и 1,65 г (16,8 ммоль) ацетата калия. Полученную смесь нагревают при 80°С в течение 2 ч и затем охлаждают до комнатной температуры, выливают в воду и экстрагируют три раза этилацетатом. Объединенные органические фазы высушивают над сульфатом натрия и концентрируют в вакууме. После экспресс-хроматографии (этилацетат/гексан в соотношении Ѕ, затем этилацетат) получают 1,39 г 2-(4-метокси-3-нитрофенил)-4,4,5,5-тетраметил-[1,3,2]диоксаборолана в виде не совсем белого твердого вещества. Масс-спектр (ES-MS): m/e (%): 280 (М+Н+, 100).
б) 4-(4-Метокси-3-нитрофенил)-3,6-дигидро-2H-пиран
К перемешиваемому раствору 4,36 г (15,6 ммоль) 2-(4-метокси-3-нитро-фенил)-4,4,5,5-тетраметил-[1,3,2]диоксаборолана и 3,30 г (14, ммоль) 3,6-дигидро-2H-пиран-4-илового эфира трифторметансульфоновой кислоты в 33 мл этанола и 82 мл толуола добавляют 580 мг (0,71 ммоль) аддукта-дихлор(1,1'-бис(дифенилфосфино)ферроцен)палладий(II) дихлорметан. Полученную смесь нагревают при 80°С и добавляют по каплям 16,5 мл (33,0 ммоль) 2 М водного раствора карбоната натрия. Реакционную смесь перемешивают в течение 20 минут при 80°С и затем охлаждают до комнатной температуры, выливают в воду и экстрагируют три раза этилацетатом. Объединенные органические фазы высушивают над сульфатом натрия и концентрируют в вакууме. После экспресс-хроматографии (этилацетат/гексан в соотношении 1/4) получают 2,00 г (выход 60%) 4-(4-метокси-3-нитрофенил)-3,6-дигидро-2H-пирана в виде светло-желтого твердого вещества. Масс-спектр (ES-MS): m/e (%): 253 (M+NH4 +, 100), 236 (М+Н+, 24).
в) 2-Метокси-5-(тетрагидропиран-4-ил)фениламин
К перемешиваемому раствору 3,30 г (14,0 ммоль) 4-(4-метокси-3-нитрофенил)-3,6-дигидро-2H-пирана в 70 мл метанола и 70 мл дихлорметана добавляют на кончике шпателя 10%-ный палладий на углероде и затем полученную смесь перемешивают в течение 20 минут при комнатной температуре в атмосфере водорода. После этого полученную смесь фильтруют, промывают дихлорметаном и полученный фильтрат концентрируют в вакууме, получая при этом 2,75 г (выход 95%) 2-метокси-5-(тетрагидропиран-4-ил)фениламина в виде не совсем белого твердого кристаллического вещества. Масс-спектр (ES-MS): m/e (%): 208 (М+Н+), 100).
г) 1-Бензоил-3-[2-метокси-5-(тетрагидропиран-4-ил)фенил]тиомочевина
К перемешиваемому раствору 1,11 г (14,6 ммоль) роданида аммония в 60 мл ацетона добавляют по каплям 1,54 мл (13,3 ммоль) бензоилхлорида и полученную смесь кипятят с обратным холодильником в течение 10 минут. Затем добавляют по каплям раствор 2,75 г (13,3 ммоль) 2-метокси-5-(тетрагидропиран-4-ил)фениламина в 30 мл ацетона и реакционную смесь кипятят с обратным холодильником дополнительно в течение 10 минут. Затем полученную смесь охлаждают до комнатной температуры, выливают в раствор бикарбоната натрия и экстрагируют три раза дихлорметаном. Объединенные органические фазы высушивают над сульфатом натрия и концентрируют в вакууме. После экспресс-хроматографии (этилацетат/гексан в соотношении 1/1) с последующим растиранием в эфире получают 3,25 г (выход 66%) 1-бензоил-3-[2-метокси-5-(тетрагидропиран-4-ил)фенил]тиомочевины в виде белого твердого вещества. Масс-спектр (ES-MS): m/e (%): 371 (М+Н, 100).
д) [2-Метокси-5-(тетрагидропиран-4-ил)фенил]тиомочевина
К перемешиваемому раствору 3,25 г (8,77 ммоль) 1-бензоил-3-[2-метокси-5-(тетрагидропиран-4-ил)фенил]тиомочевины в 45 мл метанола добавляют по каплям 0,25 мл (1,3 ммоль) 5,3 М раствора метилата натрия и продолжают перемешивание в течение 1 ч при комнатной температуре. Полученную смесь затем выливают в воду и экстрагируют три раза этилацетатом. Объединенные органические фазы высушивают над сульфатом натрия и концентрируют в вакууме. После экспресс-хроматографии (этилацетат) получают 1,90 г (выход 81%) [2-метокси-5-(тетрагидропиран-4-ил)фенил]тиомочевины в виде белого вспененного вещества. Масс-спектр (ES-MS): m/e (%): 267 (М+Н+, 100).
е) 4-Метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил-амин
К перемешиваемому раствору 1,90 г (7,13 ммоль) [2-метокси-5-(тетрагидропиран-4-ил)фенил]тиомочевины в 20 мл уксусной кислоты, нагретому до 80°С, добавляют по каплям 1,45 мл (8,27 ммоль) бромоводородной кислоты (5,7 М раствор в уксусной кислоте) и продолжают перемешивание в течение 30 мин при 80°С. Затем добавляют по каплям 0,56 мл (7,85 ммоль) ДМСО и реакционную смесь перемешивают дополнительно в течение 30 мин при 80°С. Полученную смесь затем охлаждают до комнатной температуры, медленно выливают в раствор бикарбоната натрия и добавляют этилацетат. Полученную смесь перемешивают в течение 10 минут при комнатной температуре и полученные кристаллы собирают фильтрацией, промывая этилацетатом. Маточную жидкость разделяют и полученную органическую фазу концентрируют в вакууме до объема 5 мл. Полученную вторую партию кристаллов собирают фильтрацией и объединяют с первой партией, получая при этом 920 мг (выход 49%) 4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-иламина в виде белого твердого вещества. ES-MS m/e (%): 265 (M+H+, 100).
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ БЕНЗОТИАЗОЛА И ИХ ПРИМЕНЕНИЕ ПРИ ЛЕЧЕНИИ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С АДЕНОЗИНОВЫМИ А-РЕЦЕПТОРАМИ | 2004 |
|
RU2348622C2 |
| БЕНЗОТИАЗОЛЫ | 2002 |
|
RU2293736C2 |
| ПРОИЗВОДНЫЕ БЕНЗОТИАЗОЛА И ИХ ПРИМЕНЕНИЕ ПРИ ЛЕЧЕНИИ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С АДЕНОЗИНОВЫМИ A-РЕЦЕПТОРАМИ | 2004 |
|
RU2348629C2 |
| 7-АМИНОБЕНЗОТИАЗОЛЬНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ЛИГАНДОВ АДЕНОЗИНОВОГО РЕЦЕПТОРА | 2002 |
|
RU2299203C2 |
| ПРОИЗВОДНЫЕ БЕНЗОТИАЗОЛА | 2001 |
|
RU2251419C2 |
| 2-АМИНОБЕНЗОТИАЗОЛИЛМОЧЕВИНЫ В КАЧЕСТВЕ МОДУЛЯТОРОВ АДЕНОЗИНА | 2002 |
|
RU2311905C2 |
| ПРОИЗВОДНЫЕ БЕНЗОТИАЗОЛА | 2005 |
|
RU2382782C2 |
| АМИДНЫЕ ПРОИЗВОДНЫЕ 2,3,4,5-ТЕТРАГИДРОБЕНЗО [f]-[1,4] ОКСАЗЕПИН-5-КАРБОНОВОЙ КИСЛОТЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ГАММА-СЕКРЕТАЗЫ, ПРЕДНАЗНАЧЕННЫХ ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ АЛЬЦГЕЙМЕРА | 2004 |
|
RU2332408C2 |
| ПРОИЗВОДНЫЕ НИКОТИН- ИЛИ ИЗОНИКОТИНБЕНЗОТИАЗОЛА И ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2002 |
|
RU2294933C2 |
| N-ПИРИДИН-3-ИЛ ИЛИ N-ПИРАЗИН-2-ИЛ КАРБОКСАМИДЫ В КАЧЕСТВЕ АГЕНТОВ, ПОВЫШАЮЩИХ УРОВЕНЬ ХОЛЕСТЕРИНА ЛПВП | 2011 |
|
RU2540069C2 |
Изобретение относится к производным бензотиазола общей формулы (I) и их фармацевтически приемлемым кислотно-аддитивным солям в качестве лигандов рецептора аденозина и к лекарственному средству на их основе. Соединения могут найти применение для лечения и профилактики заболеваний, опосредованных рецепторами аденозина А2А и A1, например болезни Альцгеймера, некоторых депрессивных состояний, токсикомании, болезни Паркинсона. В общей формуле (I)
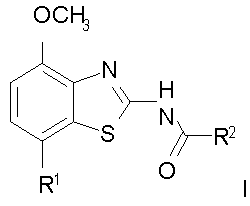
R1 представляет собой 1,4-диоксепанил или тетрагидропиран-4-ил; R2 представляет собой -N(R)-(CH2)n-5- или 6-членный неароматический гетероцикл, содержащий 1-2 гетероатома азота, необязательно замещенный одним-двумя заместителями, выбранными из группы, состоящей из C1-С6алкила или -NR2, или представляет собой -(СН2)n-5- или 6-членный неароматический гетероцикл, содержащий 1-2 гетероатома, выбранных из N, S или О, необязательно замещенный группой -(CH2)n-OH, C1-C6алкил, C1-С6алкокси, или представляет собой -(СН2)n-5- или 6-членный ароматический гетероцикл, содержащий 1-2 гетероатома азота, необязательно замещенный следующей группой: C1-С6алкил, C1-C6алкокси, галоген, галоген-(С1-С6алкил), -СН2N(R)(СН2)2OCH3, -N(R)(СН2)2OCH3, -СН2-морфолинил или -СН2-пирролидинил или представляет собой (СН2)n-С3-С6циклоалкил, необязательно замещенный группой гидрокси, или представляет собой -Н(R)-С3-С6циклоалкил, необязательно замещенный группой гидрокси или C1-С6алкил, или представляет собой фенил, необязательно замещенный группой C1-С6алкокси, галоген, галоген-(С1-С6алкил), C1-С6алкил, -СН2-пирролидин-1-ил, СН2N(R)(СН2)2OCH3 или -CH2-N(R)C(O)-(C1-C6алкил), или представляет собой 1,4-диокса-8-азаспиро[4,5]декан, или 2-окса-5-азабицикло[2,2,1]гептан, или 1-окса-8-азаспиро[4,5]декан, или -N(R)-7-оксабицикло[2,2,1]гепт-2-ил, или 2-азабицикло[2,2,2]октан; R представляет собой водород или C1-С6алкил; n означает 0 или 1. 2 н. и 6 з.п. ф-лы.
1. Соединения общей формулы:
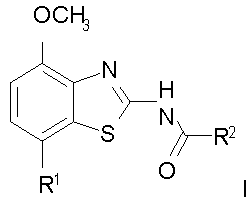
где R1 представляет собой 1,4-диоксепанил или тетрагидропиран-4-ил;
R2 представляет собой -N(R)-(CH2)n-5- или 6-членный неароматический гетероцикл, содержащий 1-2 гетероатома азота, необязательно замещенный одним-двумя заместителями, выбранными из группы, состоящей из C1-С6алкила или -NR2, или
представляет собой -(СН2)n-5- или 6-членный неароматический гетероцикл, содержащий 1-2 гетероатома, выбранных из N, S или О, необязательно замещенный группой -(СН2)nОН, C1-С6алкил, C1-С6алкокси, или
представляет собой -(СН2)n-5- или 6-членный ароматический гетероцикл, содержащий 1-2 гетероатома азота, необязательно замещенный следующей группой: C1-С6алкил, C1-С6алкокси, галоген, галоген-(С1-С6алкил), -СН2N(R)(СН2)2OCH3, -N(R)(CH2)2OCH3, -СН2-морфолинил или -СН2-пирролидинил, или представляет собой (СН2)n-С3-С6циклоалкил, необязательно замещенный группой гидрокси, или
представляет собой -N(R)-С3-С6циклоалкил, необязательно замещенный группой гидрокси или C1-С6алкил, или
представляет собой фенил, необязательно замещенный группой C1-C6алкокси, галоген, галоген-(С1-С6алкил), C1-С6алкил, -СН2-пирролидин-1-ил, -CH2N(R)(CH2)2OCH3 или -СН2-N(R)C(O)-(C1-C6алкил), или
представляет собой 1,4-диокса-8-азаспиро[4,5]декан, или
представляет собой 2-окса-5-азабицикло[2,2,1]гептан, или
представляет собой 1-окса-8-азаспиро[4,5]декан, или
представляет собой -N(R)-7-оксабицикло[2,2,1]гепт-2-ил, или
представляет собой 2-азабицикло[2,2,2]октан;
R представляет собой водород или C1-С6алкил;
n означает 0 или 1;
и фармацевтически приемлемые кислотно-аддитивные соли этих соединений.
2. Соединения по п.1 общей формулы

где R1 представляет собой 1,4-диоксепанил и
R2 представляет собой -N(R)-(СН2)n-5- или 6-членный неароматический гетероцикл, содержащий 1-2 гетероатома азота, необязательно замещенный одним-двумя заместителями, выбранными из группы, состоящей из C1-C6алкила, или
представляет собой -(СН2)n-5- или 6-членный неароматический гетероцикл, содержащий 1-2 гетероатома, выбранных из N, S или О, необязательно замещенный группой -(СН2)n-ОН, или
представляет собой -(СН2)n-5- или 6-членный ароматический гетероцикл, содержащий 1-2 гетероатома азота, необязательно замещенный C1-С6алкилом, C1-С6алкокси или группой -СН2-пирролидинил, или
представляет собой С3-С6циклоалкил, или
представляет собой -N(R)-С3-С6циклоалкил, необязательно замещенный группой гидрокси, или
представляет собой фенил, необязательно замещенный группой C1-С6алкокси, галоген, -(СН2)nпирролидинил или -СН2-N(СН3)С(O)-(С1-С6алкил), или
представляет собой 1,4-диокса-8-аза-спиро[4,5]декан, или
представляет собой 2-окса-5-аза-бицикло[2,2,1]гептан, или
представляет собой 1-окса-8-аза-спиро[4,5]декан;
или
R1 представляет собой тетрагидропиран-4-ил и
R2 представляет собой -N(R)-(СН2)n-5- или 6-членный неароматический гетероцикл, содержащий 1-2 гетероатома азота, необязательно замещенный группой C1-С6алкил, или
представляет собой -(СН2)n-5- или 6-членный неароматический гетероцикл, содержащий 1-2 гетероатома, выбранных из N, S или О, или
представляет собой -N(R)-С3-С6циклоалкил, необязательно замещенный группой гидрокси или C1-С6алкил, или
представляет собой пиперидин-1-ил, замещенный группой гидрокси и C1-С6алкилом в 4-положении, или
представляет собой пиперазин-1-ил, замещенный изопропилом в 4-положении, или представляет собой пиридин-4-ил, замещенный группой -СН2-морфолинил, или
представляет собой пиридин-4-ил, замещенный группой -СН2NH(CH2)2ОСН3, или
представляет собой -N(R)-7-оксабицикло[2,2,1]гепт-2-ил, или
представляет собой 2-окса-5-азабицикло[2,2,1]гептан, или
представляет собой 2-азабицикло[2,2,2]октан, или
представляет собой 1,4-диокса-8-азаспиро[4,5]декан;
R представляет собой водород или C1-С6алкил;
n означает 0 или 1; и
и фармацевтически приемлемые кислотно-аддитивные соли этих соединений.
3. Соединения формулы I по п.1, где R1 представляет собой 1,4-диоксепан-6-ил, и R2 является таким, как указано в п.1.
4. Соединения формулы I по п.2, которые представляют собой следующие соединения:
(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид морфолин-4-карбоновой кислоты,
(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид пиперидин-1-карбоновой кислоты,
1-циклогексил-3-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-1-метилмочевина,
(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид 4-гидроксиметил-пиперидин-1-карбоновой кислоты,
3-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-1-метил-1-(1-метил-пиперидин-4-ил)мочевина,
(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид 1,4-диокса-8-аза-спиро[4,5]декан-8-карбоновой кислоты,
(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид 4-гидроксипиперидин-1-карбоновой кислоты,
(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид 5-метилтиофен-2-карбоновой кислоты,
N-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-4-метоксибензамид,
N-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-4-фторбензамид,
(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид циклогексанкарбоновой кислоты,
N-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-2-(тетрагидропиран-4-ил)ацетамид,
(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид (R)-тетрагидрофуран-2-карбоновой кислоты,
(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид 3-метил-3Н-имидазол-4-карбоновой кислоты,
N-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)изоникотинамид,
N-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-2-метокси-изоникотинамид,
транс-1-(4-гидроксициклогексил)-3-(4-метокси-7-[1,4]диоксепан-6-ил-бензотиазол-2-ил)-1-метилмочевина,
(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид(1S,4S)-2окса-5-азабицикло[2,2,1]гептан-5-карбоновой кислоты,
(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид 4-метоксипиперидин-1-карбоновой кислоты,
4-хлорметил-N-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-бензамид,
(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)амид 1-метил-1Н-пиразол-4-карбоновой кислоты,
N-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-4-[(метил-пропионил-амино)метил]бензамид или
N-(7-[1,4]диоксепан-6-ил-4-метоксибензотиазол-2-ил)-2-пирролидин-1-ил-изоникотинамид.
5. Соединения формулы I по п.1, где R1 представляет собой тетрагидропиран-4-ил, и R2 является таким, как указано в п.1.
6. Соединения формулы I по п.5, которые представляют собой следующие соединения:
3-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метил-1-(1-метилпиперидин-4-ил)мочевина,
транс-1-(4-гидроксициклогексил)-3-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метилмочевина,
цис-1-(4-гидроксициклогексил)-3-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метилмочевина,
1-(4-цис-гидрокси-4-метилциклогексил)-3-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метилмочевина,
3-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метил-1-(тетрагидропиран-4-ил)мочевина,
3-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метил-1-(тетрагидрофуран-3-илметил)мочевина,
(рац)-(экзо)-3-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метил-1-(7-оксабицикло[2,2,1]гепт-2-ил)мочевина,
(рац)(эндо)-3-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метил-1-(7-окса-бицикло[2,2,1]гепт-2-ил)мочевина,
[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]амид 4-изопропил-пиперазин-1-карбоновой кислоты,
[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]амид 1,4-диокса-8-аза-спиро[4,5]декан-8-карбоновой кислоты,
[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]амид 4-гидрокси-4-метил-пиперидин-1-карбоновой кислоты,
[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]амид (1S,4S)-2-окса-5-аза-бицикло[2,2,1]гептан-5-карбоновой кислоты,
[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]амид 2-аза-бицикло [2,2,2] октан-2-карбоновой кислоты,
N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-2-(тетрагидропиран-4-ил)ацетамид,
N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-2-морфолин-4-илметилизоникотинамид,
2-[(2-метоксиэтиламино)метил]-N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]изоникотинамид,
(транс)-2-(4-гидроксициклогексил)-N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]ацетамид,
[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]амид 4-гидроксиметилпиперидин-1-карбоновой кислоты,
(экзо)-(+)-3-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метил-1-(7-окса-бицикло[2,2,1]гепт-2-ил)мочевина или
(экзо)-(-)-3-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-1-метил-1-(7-окса-бицикло[2,2,1]гепт-2-ил)мочевина.
7. Лекарственное средство, обладающее свойствами лиганда аденозинового рецептора A2A, содержащее одно или более соединение по любому из пп.1-6 и фармацевтически приемлемые наполнители.
8. Лекарственное средство по п.7 для лечения заболеваний, связанных с аденозиновым рецептором А2A.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Способ получения производных N-(бензтиазолил-2)амидов бензойной или тиазол-4-карбоновой кислоты | 1989 |
|
SU1681728A3 |
| 0 |
|
SU295656A1 |
Авторы
Даты
2009-04-10—Публикация
2004-05-14—Подача