Изобретение относится к области медицины, а именно хирургии, и может быть использовано при хирургическом лечении диффузного токсического зоба (ДТЗ) с целью профилактики послеоперационных осложнений в виде гипотиреоза, гипопаратиреоза и повреждений возвратного гортанного нерва.
Диффузный токсический зоб является аутоиммунным заболеванием, которое сопровождается повышенной продукцией гормонов щитовидной железы (ЩЖ). В результате резекции щитовидной железы усиливаются аутоиммунные процессы, что приводит к деструкции оставшейся ткани за счет воздействия цитотоксических лимфоцитов. В результате развивается гипотиреоз (нехватка гормонов щитовидной железы). Частота развития послеоперационного гипотиреоза достигает 73%.
Одним из способов профилактики послеоперационного гипотиреоза при операциях на щитовидной железе по поводу ДТЗ является оставление от каждой или одной доли щитовидной железы "достаточного" количества тиреоидной ткани от 2 до 12 г в каждом индивидуальном случае.
Известен способ хирургического лечения ДТЗ (Николаев О.В. Хирургия эндокринной системы. М., 1952), который заключается в субтотальной субфасциальной резекции ЩЖ с внутрикапсулярной перевязкой сосудов и оставлением 1,5-3 г ткани ЩЖ в виде кусочка ладьевидной формы по бокам от трахеи.
Недостатком известного способа является слишком малое количество оставляемой после резекции ткани. Вследствие этого проводимая в предоперационном периоде тиреостатическая терапия, направленная на подавление секреции гормонов ЩЖ, одновременно угнетает ее регенераторные возможности, а оставленной в результате резекции ткани недостаточно для восполнения гормонопродуцирующей функции железы.
Наиболее близким к предложенному является способ хирургического лечения диффузного токсического зоба, заключающийся в субтотальной субфасциальной резекции обеих долей щитовидной железы с оставлением ее ткани по заднемедиальной поверхности в количестве 4-6 г от каждой (И.С.Брейдо. Хирургическое лечение заболеваний щитовидной железы. - 2-е изд., перераб. и доп. - СПб.: Гиппократ, 1998 г., с.173-183).
Недостатком данного способа является высокая частота развития послеопрационнного гипотиреоза в связи с аутоиммунной агрессией.
Предложенное изобретение направлено на повышение эффективности лечения за счет стимуляции репаративной регенерации ткани щитовидной железы и подавления аутоиммунных процессов.
Поставленная задача решается способом хирургического лечения диффузного токсического зоба, заключающимся в субтотальной субфасциаольной резекции обеих долей щитовидной железы с оставлением слоя ее ткани по заднемедиальной поверхности в количестве 4-6 г в каждой доле, в котором в отличие от прототипа после резекции перед зашиванием раны осуществляют интраоперационную стимуляцию регенерации остаточной ткани железы путем введения в толщу паренхимы каждой доли 1-2 мл комплексного аллогенного биоматериала, разведенного в физиологическом растворе в соотношении: 40-50 мг биоматериала на 1 мл физраствора, причем комплексный биоматериал представляет собой многокомпонентный состав, включающий, мас.%:
Новый неочевидный результат предложенного изобретения заключается в следующем.
Применение комплексного аллогенного биоматериала вызывает полную репаративную регенерацию остаточной ткани щитовидной железы, обеспечивающую формирование органоспецифических структур без нарушения эпителиально-стромального соотношения. При этом каждый из компонентов биоматериала оказывает свое направленное воздействие.
Стимулятор васкулогенеза стимулирует рост и новообразование сосудов микроциркуляторного русла. Он используется в связи с тем, что при перевязке сосудов в процессе операции уменьшается кровоснабжение ткани щитовидной железы, что приводит к гипоксии ткани в послеоперационном периоде.
Стимулятор регенерации вызывает активацию клеток макрофагально-фибропластического ряда, что приводит к формированию полноценной соединительной ткани без образования рубцов.
Специфический тиреотропный стимулятор содержит характерные для щитовидной железы структурные элементы, которые способствуют активации гистиоцитов и в конечном итоге - запуску механизмов специфической регенерации щитовидной железы с формированием функционально-адекватной структуры, способной вырабатывать гормоны щитовидной железы.
Таким образом, предложенная интраоперационная стимуляция остаточной ткани щитовидной железы путем воздействия комплексным аллогенным биоматериалом обеспечивает:
- быстро наступающую реваскуляризацию культи щитовидной железы;
- формирование полноценной соединительной ткани;
- подавление аутоиммунной активности на остаточную ткань щитовидной железы в послеоперационном периоде за счет формирования макрофагально-гистиоцитарной инфильтрации в месте введения, которая в свою очередь посредством действия короткодистантных цитокинов блокирует активность цитотоксичных лимфоцитов и подавляет аутоиммунные процессы. Это является новым неочевидным результатом и позволяет существенно повысить эффективность хирургического лечения диффузного токсического зоба.
Компоненты аллогенного биоматериала стимулятор васкулогенеза и стимулятор регенерации являются серийно выпускаемыми препаратами (ТУ 42-2-537-2002).
Специфический тиреотропный стимулятор приготавливают следующим образом. Аллогенную донорскую щитовидную железу очищают от остатков прилегающих тканей, нарезают на мелкие (не более 5 мм) кусочки и промывают под проточной водой в течение 5-10 минут. Затем помещают в 3% раствор перекиси водорода на 5-19 минут, после чего трижды отполаскивают 0,9% раствором натрия хлорида. Далее ткани замораживают и лиофильно высушивают под вакуумом. Высушенные ткани измельчают, расфасовывают в стеклянные флаконы, стерилизуют γ-облучением в дозе 2,5 Мрад.
Существо изобретения иллюстрируется изображениями, где на фиг.1 показано интраоперационное введение биоматериала в остаточную ткань (культю) правой доли щитовидной железы;
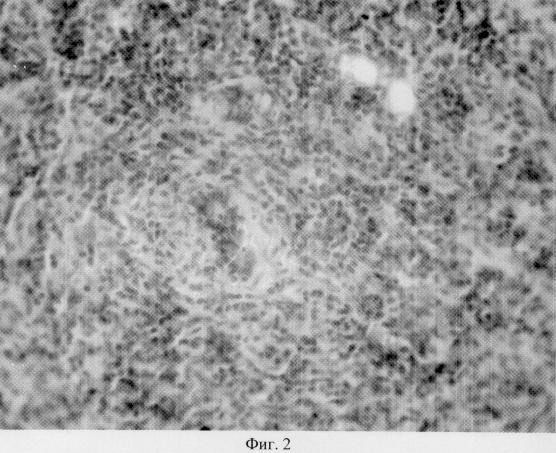
на фиг.2 показано гистологическое строение ткани щитовидной железы на 30 сутки после ее субтотальной резекции в группе без стимуляции регенерации;
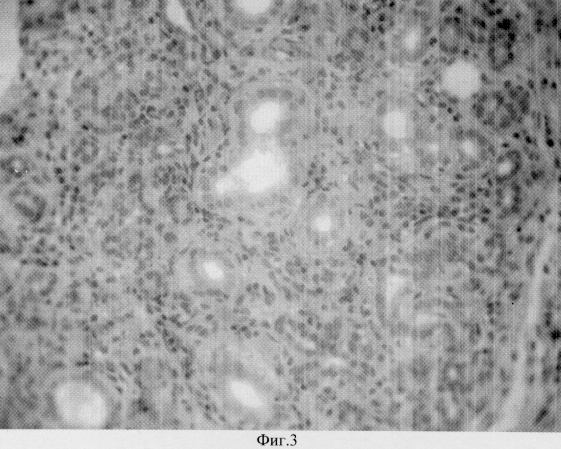
на фиг.3 - то же со стимуляцией комплексным аллогенным биоматериалом;
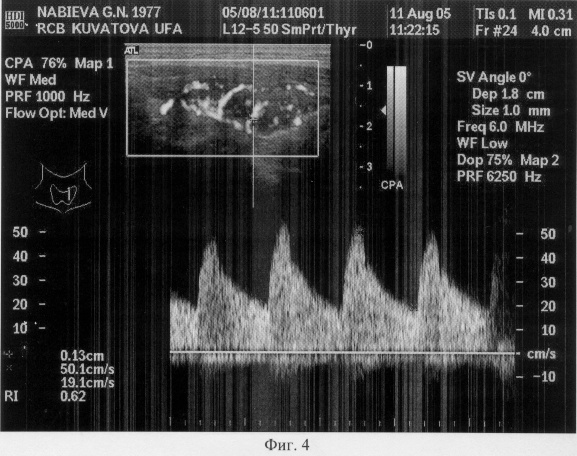
на фиг.4 - ультразвуковое исследование щитовидной железы в режиме цветного энергетического доплеровского картирования (ЦЭДК) до операции;
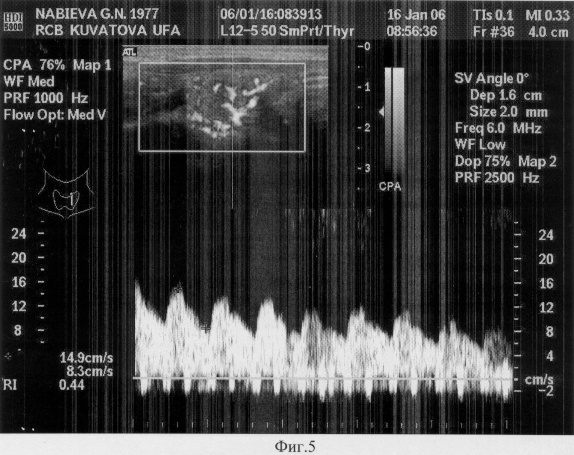
на фиг.5 - ультразвуковое исследование щитовидной железы в режиме цветного энергетического доплеровского картирования через 5 месяцев после операции с применением комплексного аллогенного биоматериала.
Способ осуществляют следующим образом.
Применяют эндотрахеальный метод обезболивания. После обработки операционного поля растворами антисептиков и обкладывания его стерильным бельем производится воротникообразный разрез на шее по Кохеру на 2-3 см выше яремной вырезки или по нижней шейной складке. Послойно рассекаются кожа, подкожная клетчатка, поверхностная фасция шеи и подкожная мышца. Гемостаз выполняется с использованием электрокоагуляции. Перевязываются и пересекаются передние яремные вены. Кожные лоскуты (верхний и нижний) вместе с подкожной мышцей отсепаровываются в стороны от раны. Шейная фасция рассекается по средней ("белой") линии. Грудино-щитовидная и грудино-подъязычная мышцы тупо раздвигаются латерально в стороны, если железа большая, то рассекаются. Доля железы ретируется медиально, средние щитовидные вены перевязываются и пересекаются. Наружная ветвь верхнего гортанного нерва, нижний глоточный констриктор и перстневидно-щитовидные мышцы идентифицируются и сохраняются.
Резекция обычно начинается с большей по размерам, как правило, левой доли. Мобилизация долей проводится без пересечения перешейка. Магистральные щитовидные артерии перевязываются около капсулы. Зажимы накладывают на сосуды вдоль и параллельно заднебоковой поверхности в нижней части доли и сверху по мере доступности, последовательно переходя с одной стороны доли на другую с оставлением тиреоидной ткани по заднебоковой поверхности. Аналогично зажимы накладываются и на перешеек. После мобилизации доли с полюсами производится клиновидная резекция последней. Затем накладываются несколько капроновых П-образных швов, соединяющие латеральный и медиальный края капсулы доли. Манипуляции по мобилизации, резекции и формированию культи второй доли осуществляют по той же методике. После резекции железы в толщу сформированной культи каждой доли щитовидной железы инъекционно вводят 1-2 мл комплексного аллогенного биоматериала (фиг.1), разведенного в физиологическом растворе в соотношении: 40-50 мг биоматериала на 1 мл физраствора. Затем рану послойно зашивают с оставлением дренажа.
Предложенный способ был апробирован в серии экспериментов на белых крысах. Были проведены гистологические исследования щитовидных желез, на 30 сутки после резекции в группе без стимуляции (фиг.2 ) и со стимуляцией (фиг.3). В первом случае наблюдается выраженная лимфо-плазмоцитарная инфильтрация, разрушающая ткань щитовидной железы. Во втором случае (фиг.3) наблюдается снижение лимфо-плазмоцитарной инфильтрации в результате подавления аутоиммунной агрессии, видны типичные фолликулы щитовидной железы, новообразованные сосуды.
Клинический пример
Больная Б., 1958 г.р., поступила в РКБ им. Г.Г.Куватова 09.08.2005 с диагнозом диффузный токсический зоб III степени, тиреотоксикоз средней тяжести, стадия декомпенсации.
Гормональное исследование: тиреотропный гормон (ТТГ) - 0,02 мМЕ/мл (норма 0,23-3,4 мМЕ/мл), свободный тироксин (Т4) - 42,2 пмоль/л (норма 10,9-23,2 пмоль/л), общий тироксин (Т4) - 253,5 нмоль/л (норма 54-156 нмоль/л), общий трийодтиронин (Т3) - 18,9 нмоль/л (норма 1,0-2,8 нмоль/л).
Иммунологическое исследование - антитела к тиреоглобулину 70,8 ЕД/мл (норма до 65 ЕД/мл), антитела к тиреопероксидазе 364,2 ЕД/мл (норма до 30 ЕД/мл).
УЗИ - правая доля 26×18×58 мм, объем - 13 см3, левая доля 26×23×68 мм, объем - 19,4 см3. Расположение на обычном уровне, контуры четкие, ровные.
Имеется выраженная васкуляризация, повышенная скорость кровотока на артериях в толще железы, высокий индекс резистивности (Ri=0,62), отражающий высокое периферическое сопротивление кровотоку в сосудах ткани железы. Индекс резистивности отражает степень выраженности лимфоидной инфильтрации и склероза ткани железы (фиг.4).
Выполнена тонкоигольная аспирационная биопсия. Цитологическое исследование: диффузный токсический зоб, "пламенеющие клетки", выраженная лимфоидная инфильтрация (до 10 лимфоцитов в 5 полях зрения).
После достижения медикаментозного эутиреоза 05.09.2005 произведена субтотальная резекция ЩЖ. При этом в остаточную ткань каждой доли щитовидной железы в толщу паренхимы инъекционно ввели по 1 мл разведенного в физиологическом растворе комплексного аллогенного биоматериала, содержащего, мас.%: стимулятор васкулогенеза - 48, стимулятор регенерации - 45, специфический тиреотропный стимулятор - 7.
Послеоперационное гистологическое исследование: диффузный токсический зоб, выраженная лимфоидная инфильтрация с образованием лимфоидных фолликулов.
Послеоперационное течение без осложнений. Больная выписана на 8 сутки после операции. Больная находилась на диспансерном наблюдении. Наблюдение через 5 месяцев после операции.
Гормональное исследование: ТТГ - 1,8 мМЕ/мл (норма 0,23-3,4 мМЕ/мл), свободный Т4 - 13,4 пмоль/л (норма 10,9-23,2 пмоль/л), общий Т4 - 110,6 нмоль/л (норма 54-156 нмоль/л), общий Т3 - 2,5 нмоль/л (норма 1,0-2,8 нмоль/л). Заключение: эутиреоидное состояние.
Иммунологическое исследование - антитела к тиреоглобулину 68 ЕД/мл (норма до 65 ЕД/мл), антитела к тиреопероксидазе 102 ЕД/мл (норма до 30 ЕД/мл).
УЗИ - правая доля 16×17×37 мм, объем 4,8 см3, левая доля 16×14×32 мм, объем 3,4 см3, расположение на обычном уровне, контуры четкие, неровные, эхогенность ткани умеренно снижена, структура диффузно-неоднородная. Степень васкуляризации ткани железы выше среднего (фиг.5).
Отмечается снижение скорости кровотока в толще железы, снижение индекса резистивности (Ri=0,44), что свидетельствует о снижении выраженности аутоиммунных (лимфоидная инфильтрация) и склеротических процессов в ткани железы.
Анализ приведенного клинического примера показывает, что у пациентки до операции отмечалась выраженная степень аутоиммунной агрессии в отношении тканей щитовидной железы и склеротические процессы. Проведенное хирургическое лечение ДТЗ с применением комплексного аллогенного биоматериала согласно предложенному способу позволило избежать развития послеоперационного гипотиреоза.
Таким образом, изобретение позволяет повысить эффективность лечения диффузного токсического зоба за счет стимуляции репаративной регенерации ткани щитовидной железы и подавления аутоиммунных процессов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ДИФФУЗНОГО ТОКСИЧЕСКОГО ЗОБА | 2005 |
|
RU2281040C1 |
| Способ хирургического лечения рака щитовидной железы при тиреотоксикозе | 2020 |
|
RU2751971C1 |
| СПОСОБ ПРОФИЛАКТИКИ РАЗВИТИЯ АУТОИММУННОГО ПРОЦЕССА ПРИ ОПЕРАТИВНОМ ЛЕЧЕНИИ УЗЛОВОГО ЗОБА | 2009 |
|
RU2410037C1 |
| Способ дифференциальной диагностики йоддефицитного и йодиндуцированного нарушения функции щитовидной железы у лиц, проживающих в регионах с йодным дефицитом | 2019 |
|
RU2728261C2 |
| СПОСОБ ДООПЕРАЦИОННОГО ОПРЕДЕЛЕНИЯ ОБЪЕМА ОПЕРАЦИИ У БОЛЬНЫХ ДИФФУЗНЫМ ТОКСИЧЕСКИМ ЗОБОМ | 2014 |
|
RU2557946C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ РАЗЛИЧНЫХ АУТОИММУННЫХ ПОРАЖЕНИЙ ЩИТОВИДНОЙ ЖЕЛЕЗЫ | 2006 |
|
RU2315322C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ ДИФФУЗНОГО ТОКСИЧЕСКОГО ЗОБА | 2005 |
|
RU2291434C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ГИПЕРТРОФИЧЕСКОГО АУТОИММУННОГО ТИРЕОИДИТА И ДИФФУЗНОГО ТОКСИЧЕСКОГО ЗОБА | 2004 |
|
RU2251975C1 |
| СПОСОБ АУТОТРАНСПЛАНТАЦИИ ТКАНИ ЩИТОВИДНОЙ ЖЕЛЕЗЫ ПРИ ВЫПОЛНЕНИИ СУБТОТАЛЬНОЙ РЕЗЕКЦИИ ЩИТОВИДНОЙ ЖЕЛЕЗЫ ПО ПОВОДУ ДВУСТОРОННЕГО МНОГОУЗЛОВОГО ЗОБА | 2006 |
|
RU2319458C1 |
| Способ лечения диффузного токсического зоба | 2024 |
|
RU2828535C1 |
Изобретение относится к медицине, а именно к хирургии. Выполняют субтотальную субфасциальную резекцию обеих долей щитовидной железы с оставлением слоя ее ткани по заднемедиальной поверхности в количестве 4-6 г в каждой доле. При этом после резекции перед зашиванием раны осуществляют интраоперационную стимуляцию регенерации остаточной ткани железы путем введения в толщу паренхимы 1-2 мл комплексного аллогенного биоматериала, разведенного в физиологическом растворе в соотношении: 40-50 мг биоматериала на 1 мл физраствора, причем комплексный биоматериал представляет собой многокомпонентный состав, включающий, мас.%: стимулятор васкулогенеза 40-50, стимулятор регенерации 40-50, специфический тиреотропный стимулятор 5-10, который готовят следующим образом: очищают аллогенную донорскую щитовидную железу от остатков прилегающих тканей, нарезают на мелкие кусочки и промывают под проточной водой в течение 5-19 минут, после чего трижды отполаскивают 0,9% раствором натрия хлорида, далее ткани замораживают и лиофильно высушивают под вакуумом, измельчают высушенные ткани, расфасовывают в стеклянные флаконы, стерилизуют γ-облучением в дозе 2,5 Мрад. Способ обеспечивает быструю реваскуляризацию культи щитовидной железы, формирование полноценной соединительной ткани, позволяет подавить аутоиммунную активность на остаточную ткань щитовидной железы в послеоперационном периоде. 5 ил.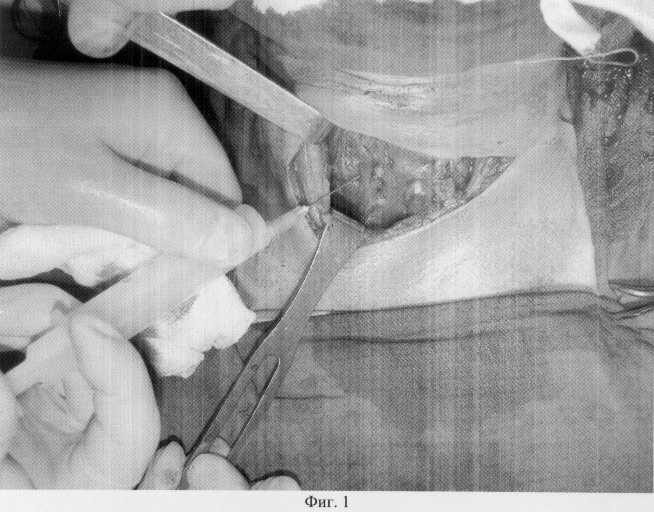
Способ хирургического лечения диффузного токсического зоба, заключающийся в субтотальной субфасциальной резекции обеих долей щитовидной железы с оставлением слоя ее ткани по заднемедиальной поверхности в количестве 4-6 г в каждой доле, отличающийся тем, что после резекции перед зашиванием раны осуществляют интраоперационную стимуляцию регенерации остаточной ткани железы путем введения в толщу паренхимы 1-2 мл комплексного аллогенного биоматериала, разведенного в физиологическом растворе в соотношении 40-50 мг биоматериала на 1 мл физраствора, причем комплексный биоматериал представляет собой многокомпонентный состав, включающий, мас.%:
который готовят следующим образом: очищают аллогенную донорскую щитовидную железу от остатков прилегающих тканей, нарезают на мелкие кусочки и промывают под проточной водой в течение 5-19 мин, после чего трижды отполаскивают 0,9%-ным раствором натрия хлорида, далее ткани замораживают и лиофильно высушивают под вакуумом, измельчают высушенные ткани, расфасовывают в стеклянные флаконы, стерилизуют γ-облучением в дозе 2,5 Мрад.
| БРЕЙДО И.С | |||
| Хирургическое лечение заболеваний щитовидной железы | |||
| - СПб.: Гиппократ, 1998, с.173-183 | |||
| АЛЛОГЕННЫЙ ПРЕПАРАТ ПЛАЦЕНТЫ ЧЕЛОВЕКА, ОБЛАДАЮЩИЙ ПРОТИВОВОСПАЛИТЕЛЬНЫМ, РЕПАРАТИВНЫМ, АНТИМИКРОБНЫМ, РАНОЗАЖИВЛЯЮЩИМ ДЕЙСТВИЕМ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1998 |
|
RU2137486C1 |
| БИОМАТЕРИАЛ АЛЛОПЛАНТ ДЛЯ РЕГЕНЕРАТИВНОЙ ХИРУРГИИ | 2001 |
|
RU2189257C1 |
| ВОСКОБОЙНИКОВ В.В | |||
| и др | |||
| Диагностика, тактика и хирургическое лечение больных с многоузловым эутиреоидным зобом | |||
| Проблемы эндокринологии, 2001, № 2, с.5-12 | |||
| ПАВЛОВ А.В | |||
| и др | |||
| Регенерация | |||
Авторы
Даты
2007-03-10—Публикация
2006-02-26—Подача