Изобретение относится к области медицины, а именно хирургии, и может быть использовано при хирургическом лечении диффузного токсического зоба (ДТЗ) с целью профилактики послеоперационных осложнений в виде гипотиреоза, гипопаратиреоза и повреждений возвратного гортанного нерва.
Одним из способов профилактики послеоперационного гипотиреоза при операциях на щитовидной железе (ЩЖ) по поводу ДТЗ, является оставление от каждой или одной доли щитовидной железы "достаточного" количества тиреоидной ткани от 2 до 12 г в каждом индивидуальном случае.
Наиболее широкое распространение и признание на территории России и стран СНГ, почти полностью вытеснив все другие способы резекции щитовидной железы при ДТЗ, получили способы О.В.Николаева и Е.С.Драчинской. Как сами авторы, так и приверженцы этих методик, отмечая преимущества избранного способа, указывают на недостатки другого.
Методика операции по О.В.Николаеву (Николаев О.В. Хирургия эндокринной системы. М., 1952) заключается в субтотальной субфасциальной резекции ЩЖ с внутрикапсулярной перевязкой сосудов и оставлением 1,5-3 г ткани ЩЖ в виде кусочка ладьевидной формы по бокам от трахеи. Перешеек удаляют целиком. Однако даже опытному хирургу нелегко определить, каких размеров участки железы следует оставить по бокам от трахеи, и как следствие развивается послеоперационный гипотиреоз или рецидив зоба. Указанные недостатки реже встречаются при способе резекции ЩЖ, предложенной в 40-х гг. Е.С.Драчинской (Драчинская Е.С., Брейдо И.С. Хирургия щитовидной железы. Л., 1963), заключающемся в тотальном субфасциальном удалении правой доли щитовидной железы с перешейком и субтотальной резекции левой доли щитовидной железы, с оставлением кусочка ткани верхнего полюса весом около 3-6 г и питающей его верхней щитовидной артерией (ВЩА). При этом способе легче и точнее определяется объем оставляемой культи, имеющей довольно стандартную форму - от усеченного конуса до шаровидной, в зависимости от степени гипертрофии железы. Т.к. во время оперативного вмешательства можно не только видеть весь оставляемый участок, но и измерить его, то, зная плотность ткани щитовидной железы, которая равна 1,04 г/см3, с учетом соотношения размеров основания и высоты тиреоидного остатка, легко сформировать культю желаемой массы. Оставление магистральной артерии позволяет избежать патологических процессов, связанных с ишемизацией оставленной паренхимы щитовидной железы. Однако, как отмечает О.В.Николаев (Николаев О.В. Хирургия эндокринной системы. М., 1952), субтотальная резекция по Е.С.Драчинской справедливо считается анатомически необоснованной, так как при ней создаются больше условий для двухстороннего повреждения околощитовидных желез и возвратных нервов не только во время операции, но и в процессе заживления раны вследствие вовлечения их в рубцовый процесс. Кроме того, перевязка нижней щитовидной артерии (НЩА) ведет к неоправданной и обширной травме и вскрытию глубоких клетчаточных пространств шеи, связанных со средостением.
Размеры тиреоидного остатка являются важным, но не единственным фактором, определяющим результаты хирургического лечения ДТЗ. Очень важную прогностическую роль в развитии послеоперационного гипотиреоза кроме сохранения адекватного кровоснабжения тиреоидного остатка имеет выраженность лимфоидной инфильтрации в культе щитовидной железы. Общепризнано, что отсутствие достаточного кровоснабжения в культе щитовидной железы приводит к избыточному разрастанию соединительной ткани и усугубляет аутоиммунные процессы.
Прототипом является способ хирургического лечения ДТЗ по Микуличу-Мартынову-Мелихову (Мелихов П.Г. Базедова болезнь и ее хирургическое лечение. М., 1941), заключающийся в двухсторонней клиновидной резекции ЩЖ без мобилизации ИЩА с оставлением участков ткани ЩЖ размером не менее 3×2×1 см с каждой стороны, что соответствует 12-20 г. Преимуществом данной методики является низкий риск повреждения паращитовидных желез и возвратных нервов вследствие сохранения задней пластинки и боковых поверхностей обеих долей ЩЖ, а также места вхождения НЩА в железу, что является актуальным при интимном взаиморасположении НЩА и возвратного нерва.
Однако, как отмечают Драчинская Е.С. и Брейдо И.С. (Драчинская B.C., Брейдо И.С. Хирургия щитовидной железы. Л., 1963, С.114), в настоящее время эта методика представляет лишь исторический интерес, поскольку оставление большой массы ткани ШЖ очень часто ведет к рецидиву.
Задачей настоящего изобретения является снижение частоты развития послеоперационных осложнений в виде:
1. послеоперационного гипотиреоза;
2. повреждения паращитовидных желез с развитием гипопаратиреоза;
3. повреждения возвратного нерва.
Технический результат - улучшение функциональных результатов лечения за счет сохранения магистрального кровоснабжения и адекватного количества ткани щитовидной железы, предотвращение послеоперационных осложнений.
Указанный технический результат достигается тем, что сначала проводят резекцию меньшей доли спереди назад в каудально-краниальном направлении ладьевидно, огибая верхний полюс щитовидной железы с латеральной и медиальной стороны, формируют культю доли из нижнего полюса и субкортикальной заднебоковой пластинки без перевязки питающей нижней щитовидной артерии, после чего производят субтотальную резекцию другой доли щитовидной железы с сохранением по ее заднемедиальной поверхности ткани массой 2-4 г.
Для предлагаемой методики отбирались пациенты с высоким риском развития послеоперационного гипотиреоза вследствие аутоиммунных процессов, у которых имелись выраженная лимфоидная инфильтрация щитовидной железы по данным предоперационного цитологического исследования и высокий титр антитиреоидных антител.
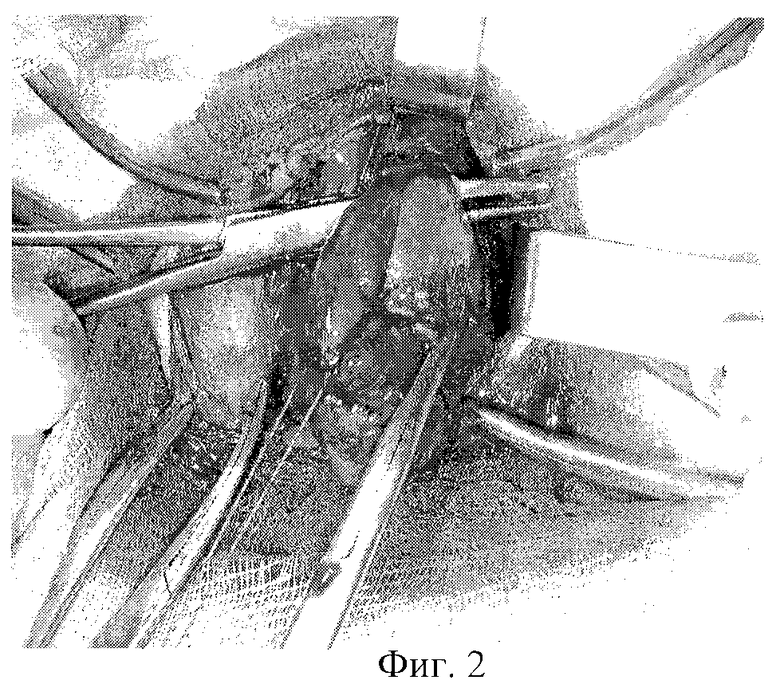
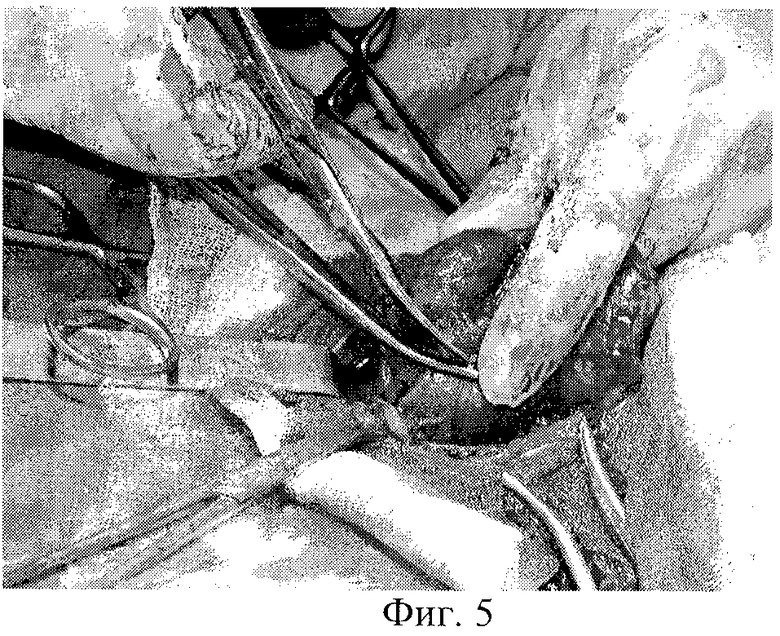
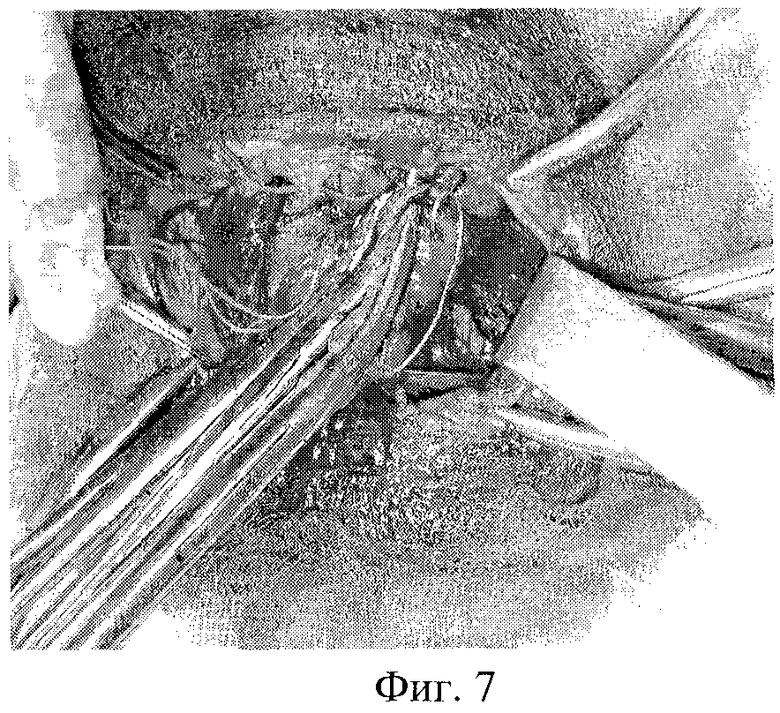
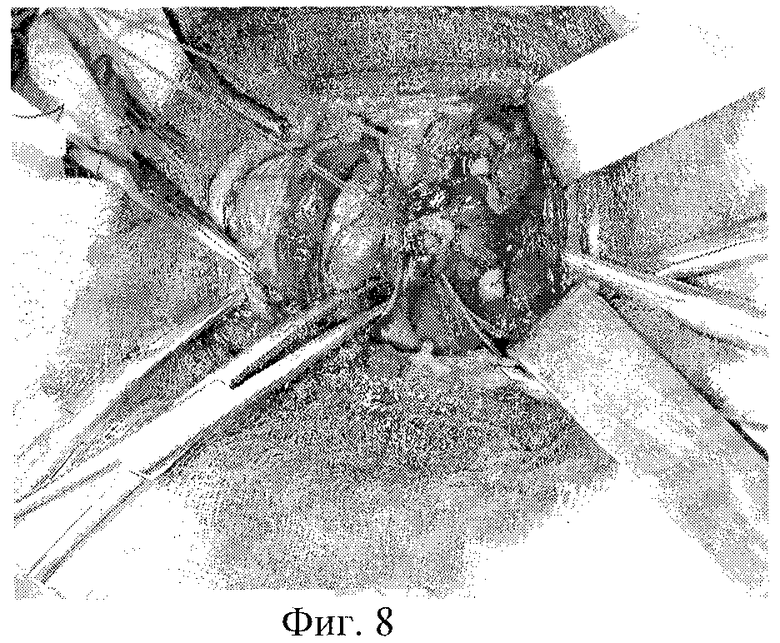
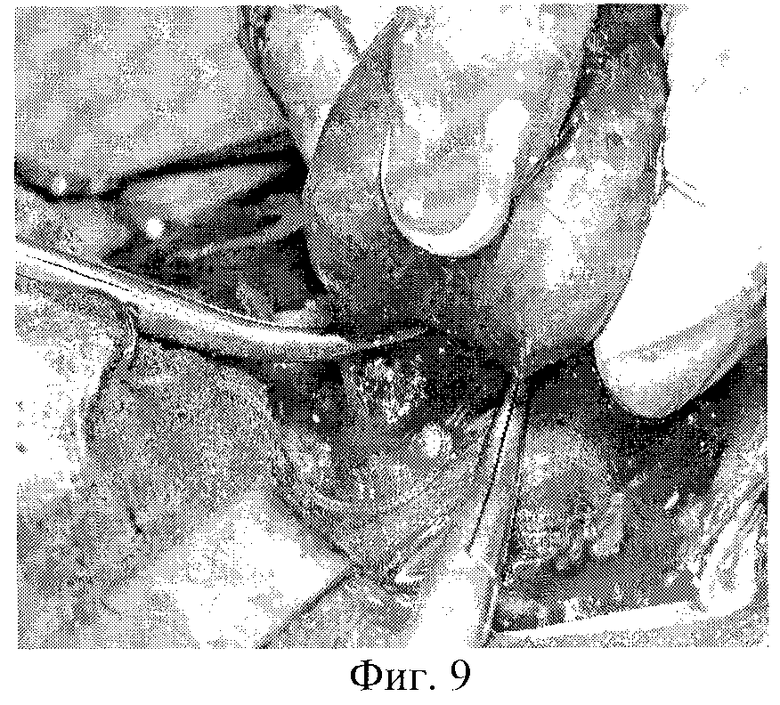
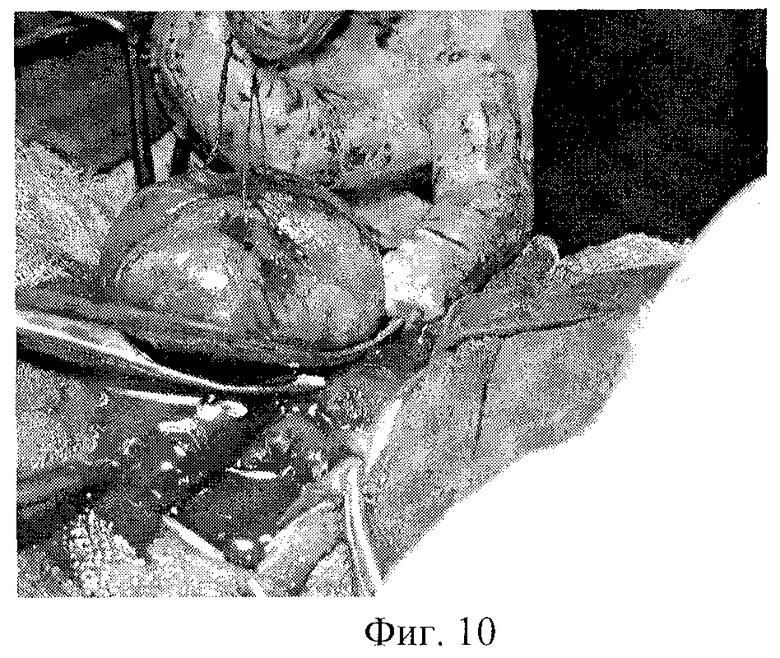
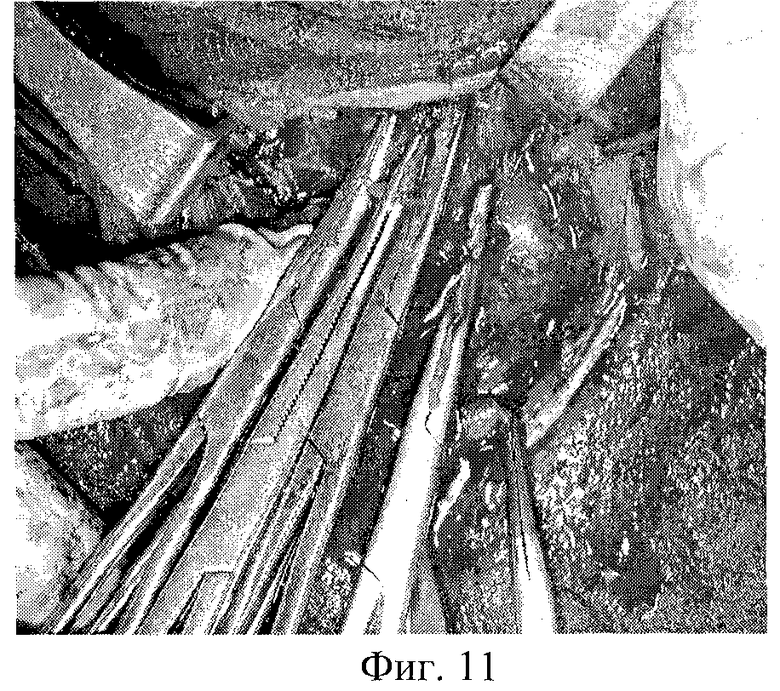
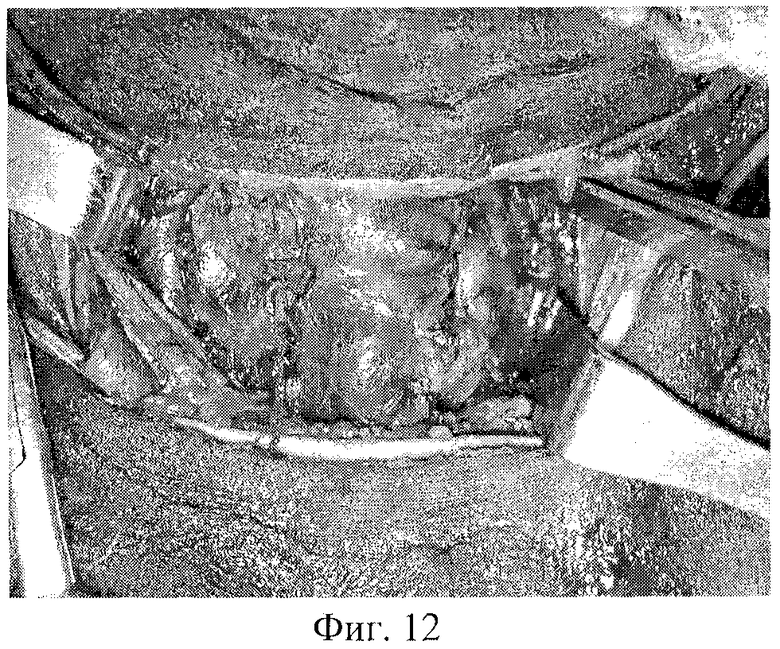
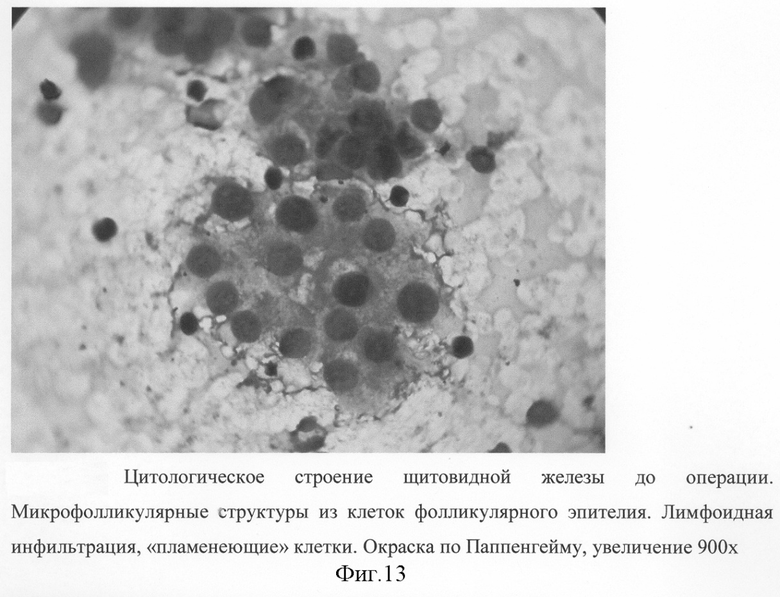
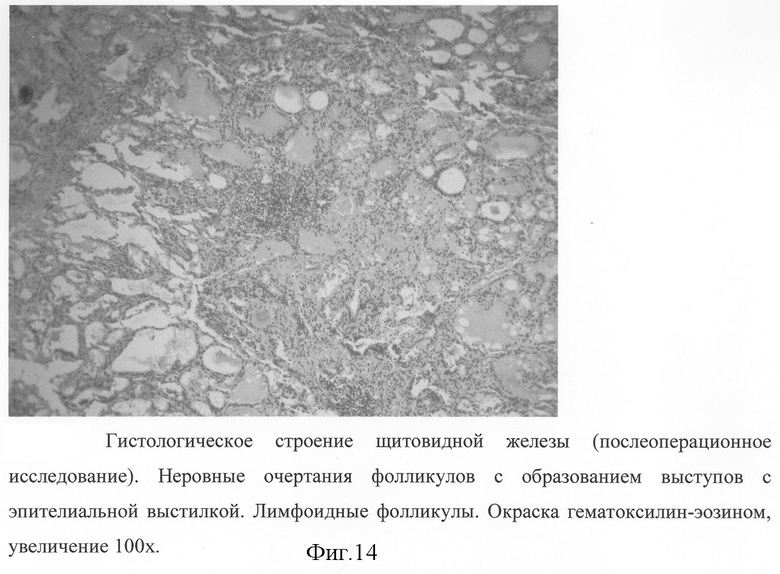
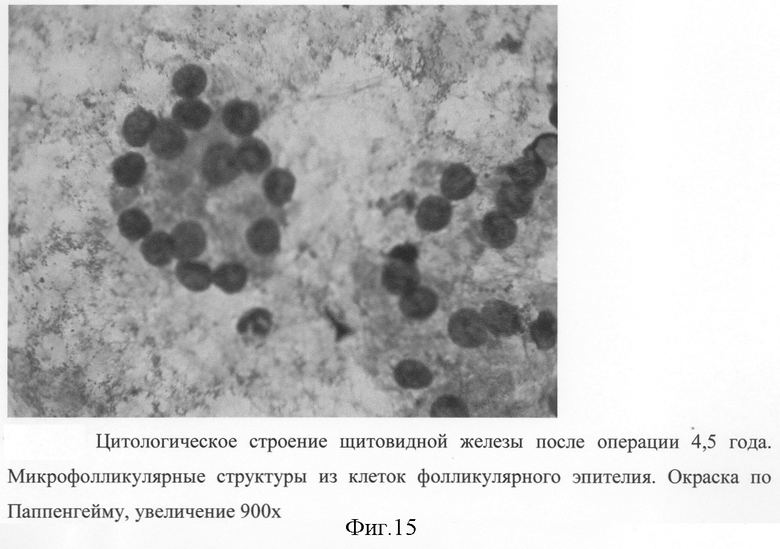
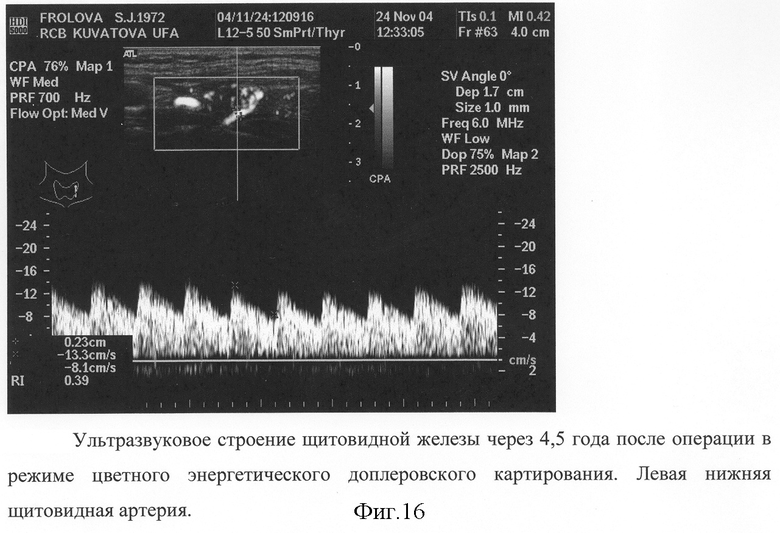
На фиг.1 изображена мобилизация боковых вен левой доли; на фиг.2-3 - мобилизация ВЩА левой доли; на фиг.4 - выделение нижнего полюса левой доли и питающей НЩА; на фиг.5-6 - наложение зажимов по латеральной поверхности левой доли ЩЖ и резекция паренхимы над зажимами; на фиг 7-8 формирование культи левой доли после резекции; на фиг.9-10 - наложение зажимов по латеральному и медиальному краю правой доли ЩЖ; на фиг.11-12 - формирование культи правой доли и общий вид после операции; на фиг.13 - цитологическое строение щитовидной железы до операции. Микрофолликулярные структуры из клеток фолликулярного эпителия. Лимфоидная инфильтрация, "пламенеющие" клетки. Окраска по Паппенгейму, увеличение 900х; на фиг.14 - гистологическое строение щитовидной железы (послеоперационное исследование). Неровные очертания фолликулов с образованием выступов с эпителиальной выстилкой. Лимфоидные фолликулы. Окраска гематоксилин-эозином, увеличение 100×; на фиг.15 - цитологическое строение щитовидной железы после операции. Микрофолликулярные структуры из клеток фолликулярного эпителия. Окраска по Паппенгейму, увеличение 900×; на фиг.16 - Ультразвуковое строение щитовидной железы через 4,5 года после операции в режиме цветного энергетического доплеровского картирования. Левая нижняя щитовидная артерия.
Техника операции. Эндотрахеальный метод обезболивания. Больного укладывают на операционном столе на спину, под лопатки подкладывается валик, голову запрокидывают назад. После обработки операционного поля растворами антисептиков и обкладывания его стерильным бельем производят воротникообразный разрез на шее по Кохеру на 2-3 см выше яремной вырезки или по нижней шейной складке. Длина разреза должна быть достаточной для лучшей мобилизации щитовидной железы. Послойно рассекают кожу, подкожную клетчатку, поверхностную фасцию шеи и m.platysma. Гемостаз выполняется с использованием электрокоагуляции. Кожные лоскуты (верхний и нижний) вместе с подкожной мышцей отсепаровывают в стороны от раны. Шейную фасцию рассекают по средней ("белой") линии. Передние яремные вены, как правило, не пересекаются. Грудино-щитовидная и грудино-подъязычные мышцы тупо раздвигают латерально в стороны, если железа большая, то рассекают. Обнажив железу, надсекают и сдвигают в стороны висцеральный листок четвертой фасции шеи. Для сохранения нижнего полюса доли щитовидной железы с питающей артерией выбирают предпочтительно долю с меньшим объемом.
Операцию начинают с меньшей по объему доли. Мобилизацию долей проводят без пересечения перешейка. Однако при чрезмерной толщине перешейка, представляющего собой конгломерат с одной из долей, чаще правой, производят резекцию перешейка вместе с долей.
Боковые щитовидные вены перевязывают и пересекают (фиг.1). Под верхним полюсом левой доли, со стороны гортани, скользя по собственной фасции, проводят изогнутый зажим Бильрота, протягивают лигатуру и перевязывают ВЩА на протяжении. При этом во избежание соскальзывания лигатуры небольшой участок ткани верхнего полюса железы (0,3×0,3 см) дополнительно прошивают, после чего артерию пересекают по ткани железы (фиг.2-3). Как только верхний полюс освобожден, доля легко "вывихивается" в рану. Далее выделяют нижний полюс левой доли и питающую его НЩА (фиг.4). В области нижнего полюса по передней его поверхности, краниальнее впадения НЩА на 0,5-1 см производят надсечение собственной капсулы железы для пережатия сосудов. Резекцию доли начинают по латеральной поверхности ЩЖ. В паренхиму железы вводят браншу кровоостанавливающего зажима, близко к собственной капсуле с учетом ее расположения под сосудами второго и третьего порядка. Другую браншу располагают снаружи железы. Для субфасциальной мобилизации сосудов достаточно 2-3 зажимов с каждой стороны. При большом объеме железы возникает необходимость наложения зажимов на паренхиму ЩЖ параллельно и глубже зажимов, расположенных на капсуле. Зажимы располагают спереди назад, в каудально-краниальном направлении, огибая верхний полюс ЩЖ, резецируют паренхиму железы над зажимами (фиг.5-6). По медиальному краю доли ЩЖ зажимы накладывают, таким же образом огибая верхний полюс по задней поверхности. После чего изогнутыми ножницами над зажимами производят ладьевидную резекцию 3/4 объема железы согласно описанной проекционной линии. Основным условием является сохранение субкортикального слоя по задней поверхности до средней трети доли, толщиной 0,5-0,7 см. Таким образом, формируется культя доли, состоящая из нижнего полюса и задней пластинки. Затем накладывают несколько П-образных швов, соединяющих латеральный и медиальный края капсулы доли. Иногда приходится накладывать 3-4 дополнительных гемостатических Z-образных шва в дополнение к основным (фиг.7-8).
Далее операцию продолжают на контралатеральной доле. Долю железы ротируют медиально. ВЩА мобилизуют аналогично приведенной выше методике. Верхний полюс выводят в рану. Затем освобождают нижний полюс щитовидной железы. НЩА пересекают и перевязывают около капсулы. Для мобилизации собственных сосудов доли щитовидной железы зажимы накладывают на сосуды вдоль и параллельно заднебоковой поверхности, начиная с нижней части доли и краниально по мере доступности, последовательно переходя с одной стороны доли на другую сторону с оставлением тиреоидной ткани по заднебоковой поверхности. При этом одна бранша зажима остается снаружи собственной фасции железы, а другая проходит в тиреоидной ткани близко к поверхности железы (под сосудами). Аналогично зажимы накладывают и на перешеек (фиг.9-10). После мобилизации доли с полюсами производят предельно субтотальную резекцию последней с оставлением ткани по заднемедиальной ее поверхности (паратрахеально) массой 2-4 г. При рассечении ткани ЩЖ зажимы практически не накладывают, так как крупные сосуды проходят по поверхности железы и значительного кровотечения не бывает. Затем для формирования культи и гемостаза накладывают несколько П-образных швов, соединяющих латеральный и медиальный края капсулы доли. Иногда приходится накладывать 3-4 дополнительных гемостатических Z-образных шва в дополнение к основным (фиг.11-12).
К ложу железы подводят две резиновые полоски, рану ушивают послойно до дренажа. Сшивают пересеченные претрахеальные мышцы, m.platysma с клетчаткой, на кожу накладываются металлические скобки или внутрикожный косметический шов. Дренаж удаляют через 24-48 часов.
Преимуществом данного метода является:
1. сохраняется ткань в области нижнего полюса и субкортикальный слой задней поверхности доли щитовидной железы с адекватным зональным кровоснабжением, что уменьшает прогрессирование аутоиммунных процессов вследствие ишемии культи в послеоперационном периоде и снижается вероятность развития послеоперационного склероза остаточной ткани;
2. учитывая интимный вариант взаиморасположения возвратного нерва и нижней щитовидной артерии, сохранение последней исключает риск двухстороннего повреждения возвратных нервов;
3. не повреждаются паращитовидные железы, прилегающие к задней поверхности нижнего полюса;
4. во время операции несложно рассчитать и варьировать объем оставляемой ткани железы.
Предлагаемым способом было прооперировано 78 больных.
Способ иллюстрируется следующим примером.
Больная Ф., 1972 г.р., поступила в РКБ им. Г.Г.Куватова с диагнозом диффузный токсический зоб III степени, тиреотоксикоз средней тяжести, стадия декомпенсации.
Гормональное исследование - ТТГ - 0,07 мМЕ/мл (норма 0,23-3,4 мМЕ/мл), Св. Т4 - 38,4 пмоль/л (норма 10,9-23,2 пмоль/л). Общ. Т4 - 208,1 нмоль/л (норма 54-156 нмоль/л), Общ. Т3 - 16,7 нмоль/л (норма 1,0-2,8 нмоль/л).
Иммунологическое исследование - антитела к тиреоглобулину 92 ЕД/мл (норма до 65 ЕД/мл), антитела к тиреопероксидазе 516 ЕД/мл (норма до 30 ЕД/мл)
УЗИ - правая доля 26×18×58 мм, объем - 13 см3, левая доля 26×23×68 мм, объем 19,4 см3. Расположение на обычном уровне, контуры четкие, ровные. Эхогенность ткани средняя, структура однородная. Степень васкуляризации ткани повышенная. Регионарные лимфоузлы не изменены, структура сохранена.
Цитологическое исследование - диффузный токсический зоб. Фолликулярные клетки увеличены в размерах, в мазках расположены однослойными пластами, россыпью и образуют микрофолликулярные структуры. Выраженный анизонуклеоз тироцитов, цитоплазма обильная. По краю цитоплазмы определяются краевые вакуоли с паравакуолярными красными гранулами - "пламенеющие" клетки. Лимфоидная инфильтрация средней выраженности, скопление лимфоидных клеток в количестве 8-10 лимфоцитов в поле зрения (фиг.13).
По поводу диффузного токсического зоба III степени 11.07.2000 произведена предельно субтотальная резекция правой доли ЩЖ с перевязкой верхней и нижней щитовидной артерий, субтотальная резекция левой доли с перевязкой верхней щитовидной артерии и оставлением нижнего полюса, задней субкортикальной пластинки щитовидной железы и питающей нижней щитовидной артерии.
Гистологическое исследование - диффузный токсический зоб, ткань железы с неровными очертаниями фолликулов с образованием выступов с эпителиальной выстилкой. В межуточной ткани скопления лимфоцитов с образованием лимфоидных фолликулов (фиг.14).
Послеоперационное течение без осложнений.
Наблюдение через 4,5 года после операции.
Гормональное исследование - ТТГ - 0,34 мМЕ/мл (норма 0,23-3,4 мМЕ/мл), Св. Т4 - 13,7 пмоль/л (норма 10,9-23,2 пмоль/л), Общ. Т4 - 110,6 нмоль/л (норма 54-156 нмоль/л), Общ. Т3 - 1,8 нмоль/л (норма 1,0-2,8 нмоль/л).
Иммунологическое исследование - антитела к тиреоглобулину 76 ЕД/мл (норма до 65 ЕД/мл), антитела к тиреопероксидазе 83 ЕД/мл (норма до 30 ЕД/мл)
Цитологическое исследование - микрофолликулярные структуры из клеток фолликулярного эпителия без признаков гиперфункции. Лимфоидная инфильтрация отсутствует (фиг.15).
УЗИ - правая доля - культя 12×14×33 мм, объем 2,7 см3, левая доля - культя 17×17×42 мм, объем доли 5,8 см3, расположение на обычном уровне, контуры четкие, неровные, эхогенность ткани умеренно снижена, структура диффузно-неоднородная. Сохранена нижняя щитовидная артерия слева - диаметр 2,3 мм, максимальная систолическая скорость - 13,3 см/сек, минимальная диастолическая скорость - 8,1 см/сек (фиг.16). Степень васкуляризации ткани железы средняя. Регионарные лимфоузлы не изменены, структура сохранена.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ДИФФУЗНОГО ТОКСИЧЕСКОГО ЗОБА | 2006 |
|
RU2294704C1 |
| СПОСОБ ФОРМИРОВАНИЯ КУЛЬТИ ЩИТОВИДНОЙ ЖЕЛЕЗЫ ПРИ ХИРУРГИЧЕСКОМ ЛЕЧЕНИИ ДИФФУЗНОГО ТОКСИЧЕСКОГО ЗОБА | 1994 |
|
RU2113176C1 |
| СПОСОБ ГЕМОСТАЗА ПРИ ОПЕРАЦИЯХ НА ЩИТОВИДНОЙ ЖЕЛЕЗЕ | 2011 |
|
RU2469653C1 |
| Способ хирургического лечения рака щитовидной железы при тиреотоксикозе | 2020 |
|
RU2751971C1 |
| СПОСОБ РЕЗЕКЦИИ ЩИТОВИДНОЙ ЖЕЛЕЗЫ ПРИ ДИФФУЗНОМ ТОКСИЧЕСКОМ ЗОБЕ | 2007 |
|
RU2339315C1 |
| СПОСОБ ЭКСТРАФАСЦИАЛЬНОГО УДАЛЕНИЯ ДОЛИ ЩИТОВИДНОЙ ЖЕЛЕЗЫ | 2007 |
|
RU2357684C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЛЕЧЕБНОЙ ТАКТИКИ ПРИ ДИФФЕРЕНЦИРОВАННОМ РЩЖ В СОЧЕТАНИИ С АУТОИММУННЫМ ТИРЕОИДИТОМ С УЗЛООБРАЗОВАНИЕМ | 2013 |
|
RU2522388C1 |
| Способ резекции щитовидной железы | 1984 |
|
SU1242129A1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ БОЛЬНЫХ РАКОМ ЩИТОВИДНОЙ ЖЕЛЕЗЫ С МЕТАСТАЗАМИ В ЛИМФАТИЧЕСКИХ УЗЛАХ ШЕИ | 2015 |
|
RU2616763C1 |
| Способ хирургического лечения рака щитовидной железы с метастазами в лимфатические узлы центральной клетчатки шеи | 2022 |
|
RU2800313C1 |



Изобретение относится к медицине, а именно к хирургической эндокринологии, и может быть использовано для лечения диффузного токсического зоба. Для сначала проводят резекцию 3/4 объема меньшей доли спереди назад в каудально-краниальном направлении ладьевидно, огибая верхний полюс щитовидной железы с латеральной и медиальной стороны. Далее формируют культю доли из нижнего полюса и субкортикального слоя по задней поверхности железы без перевязки питающей нижней щитовидной артерии. Далее производят субтотальную резекцию другой доли щитовидной железы с сохранением по заднемедиальной поверхности ткани массой 2-4 г. Способ позволяет улучшить функциональные результаты лечения за счет сохранения магистрального кровообращения и адекватного количества ткани щитовидной железы, предотвратить послеоперационные осложнения. 16 ил.
Способ хирургического лечения диффузного токсического зоба путем двухсторонней резекции щитовидной железы, отличающийся тем, что сначала проводят резекцию 3/4 объема меньшей доли спереди назад в каудально-краниальном направлении ладьевидно, огибая верхний полюс щитовидной железы с латеральной и медиальной стороны, формируют культю доли из нижнего полюса и субкортикального слоя по задней поверхности железы без перевязки питающей нижней щитовидной артерии, после чего производят субтотальную резекцию другой доли щитовидной железы с сохранением по ее заднемедиальной поверхности ткани массой 2-4 г.
| МЕЛИХОВ П.Г | |||
| Базедова болезнь и ее хирургическое лечение | |||
| М., 1941 | |||
| СПОСОБ СУБТОТАЛЬНОЙ РЕЗЕКЦИИ ЩИТОВИДНОЙ ЖЕЛЕЗЫ ПРИ ЗЛОКАЧЕСТВЕННЫХ И ДОБРОКАЧЕСТВЕННЫХ ОПУХОЛЯХ | 1999 |
|
RU2147839C1 |
| ЛАВИН Н., КЛАРК О | |||
| Эндокринология, хирургическое лечение эндокринных болезней | |||
| Металлический водоудерживающий щит висячей системы | 1922 |
|
SU1999A1 |
| МАТЯШИН Н.М., ГЛУЗМАН А.М | |||
| Справочник хирургических операций | |||
| Киев: Здоров'я, 1979, с.7. | |||
Авторы
Даты
2006-08-10—Публикация
2005-07-07—Подача