Предпосылки создания изобретения
1. Область техники изобретения
Настоящее изобретение относится к пероральной доставке паратиреоидного гормона (РТН). Более конкретно изобретение направлено на применение кальцитонина в комбинации с РТН с целью перорального введения РТН.
2. Описание родственной области техники
Исследования РТН, проведенные на животных и на людях с РТН, родственными РТН пептидами и аналогами РТН, продемонстрировали его полезность при усилении остеогенеза и костной резорбции и вызвали интерес к его применению при лечении остеопороза и родственных костных нарушений. Однако клиническое использование РТН ограничивается появлением повышенного содержания кальция в крови, повышенного содержания кальция в моче и мочекаменной болезни. Появление этих потенциально токсичных побочных эффектов и изменения в метаболизме кальция остаются препятствием для использования преимуществ более высоких доз РНТ и по соображениям безопасности необходимо, чтобы концентрации РТН в плазме оставались в узком диапазоне. Если бы эффекты гиперкальциемии, в значительной степени опосредуемые остеокластами, можно было отделить от эффектов остеогеназа, в значительной мере опосредуемых остеобластами, то терапевтическое «окно» для пероральной терапии с РТН могло быть увеличено. В противоположность РТН кальцитонины снижают концентрации кальция в сыворотке путем взаимодействия непосредственно с остеокластами, приводя к уменьшению площади поверхности кости, подвергающейся резорбции с помощью остеокластов, и к уменьшению общей костной резорбции. Благодаря снижению концентрации кальция в плазме наблюдается соответствующее снижение концентраций кальция в моче, известного фактора риска для мочекаменной болезни. Настоящее изобретение описывает способ перорального введения РТН, который расширяет терапевтическое «окно» для введения РТН и допускает пероральное введение более высоких доз РТН без токсических побочных эффектов гиперкальциемии.
Краткое содержание изобретения
Соответственно настоящее изобретение направлено на создание способа перорального введения эффективной дозы РТН, включающего пероральное совместное введение эффективного количества РТН и эффективного количества кальцитонина пациенту, нуждающемуся в РТН.
Введение РТН приматам приводит к повышенным концентрациям в плазме сывороточного паратиреоидного гормона и сывороточного кальция. Наоборот, введение приматам кальцитонина лосося (sCT) приводит к повышению в сыворотке концентраций sCT и уменьшению в сыворотке кальция. В настоящее время найдено, что пероральное введение комбинации РТН и кальцитонина, хотя и приводит к уровням концентраций в плазме РТН и кальцитонина, подобным тем, которые достигаются при введении каждого компонента в отдельности, но довольно неожиданно имеет своим результатом снижение концентраций кальция в сыворотке до уровня, наблюдаемого при введении одного кальцитонина. Фактически кальцитонин сводит на нет гиперкальциемическое действие РТН, в то же время достигая вышеупомянутого снижения содержания кальция в сыворотке, получаемого, когда вводится один кальцитонин в отсутствие РТН. Введение кальцитонина вместе с терапией с РТН дает дополнительные терапевтические эффекты без побочной гиперкальциемии при недопустимых к применению в настоящее время дозах РТН. Кроме того, кальцитонин обеспечивает некоторое обезболивающее действие, которое полезно при устранении костной боли, обычно ассоциируемой с введением РТН.
Изобретение направлено также на создание способа стимуляции остеогенеза, включающего пероральное введение пациенту, нуждающемуся в остеогенезе, терапевтически эффективного количества РТН и терапевтически эффективного количества кальцитонина.
В дополнительном варианте воплощения изобретение направлено на создание способа лечения или предупреждения остеопороза, включающего пероральное введение пациенту, нуждающемуся в упомянутом лечении, терапевтически эффективного количества РТН и терапевтически эффективного количества кальцитонина.
Изобретение направлено также на создание композиции, применимой для пероральной доставки РТН и кальцитонина, например, для одновременного, раздельного или последовательного введения РТН и кальцитонина.
Далее изобретение направлено на применение РТН и кальцитонина при получении вводимого перорально лекарственного средства для стимуляции остеогенеза, например, для одновременного, раздельного или последовательного введения РТН и кальцитонина.
Изобретение, кроме того, направлено далее на создание набора для стимуляции остеогенеза, включающего РТН и кальцитонин, применимого для перорального введения, наряду с инструкциями для его перорального введения, например, для одновременного, раздельного или последовательного перорального введения РТН и кальцитонина.
Дополнительные признаки и преимущества по изобретению станут очевидными из следующего далее подробного описания изобретения.
Подробное описание изобретения
Паратиреоидный гормон или РТН может быть полной длины, разновидностью паратиреоидного гормона из 84 аминокислот, например, человеческой разновидностью, hPTH (1-84), или каким-либо полипептидом, белком, белковым фрагментом или модифицированным фрагментом, т.е. родственными РТН пептидами и аналогами РТН, способными имитировать активность hPTH(1-84) в регуляции метаболизма кальция и фосфата при создании костной ткани в организме человека. Фрагменты РТН, как правило, будут включать, по меньшей мере, первый 28 N-концевой остаток и охватывают РТН (1-28), РТН (1-31), РТН (1-34), РТН (1-37), РТН (1-38) и РТН (1-41) или их аналоги, например, PTS893. РТН может быть единственным или любой комбинацией двух или нескольких PTHs. Эти паратиреоидные гормоны имеются в продаже или могут быть получены рекомбинантным способом, пептидным синтезом или путем экстракции из человеческой жидкости способами, хорошо известными в этой области.
Кальцитонин для применения по настоящему изобретению может быть любого происхождения, включая его природные, синтетические или рекомбинантные источники, а также производные кальцитонина, такие как 1,7-аспарагиновое производное кальцитонина из угря. Различные кальцитонины, включая кальцитонин из лосося, свиньи и угря, имеются в продаже и обычно применяются для лечения болезни Пэджета, гиперкальциемии беременных и остеопороза. Кальцитонин может включать одну разновидность кальцитонина или любую комбинацию из двух или нескольких кальцитонинов. Предпочтительным кальцитонином является синтетический кальцитонин лосося.
Кальцитонины имеются в продаже или могут быть получены известными способами.
Количество РТН, которое должно быть введено, как правило, является эффективным при остеогенезе, т.е. терапевтически эффективным количеством. Данное количество будет неизбежно меняться в зависимости от возраста, размера, пола и состояния субъекта, подвергаемого лечению, от природы и тяжести нарушения, подлежащего лечению, и тому подобного. Однако количество может быть меньше по сравнению с тем случаем, когда должно быть введено несколько композиций, т.е. общее эффективное количество может быть введено в стандартных кумулятивных дозах. Количество РТН может быть больше, чем эффективное количество, когда композиция обеспечивает замедленное высвобождение фармакологически активного агента. Общее количество РТН, которое должно быть применено, может определяться способами, известными специалистам в данной области. Однако в большинстве случаев удовлетворительные результаты будут систематически получаться при ежедневных дозах примерно от 0,001 мкг/кг до примерно 10 мг/кг массы тела животного, предпочтительно 1 мкг/кг до примерно 6 мкг/кг массы тела.
Соответствующая доза кальцитонина, которая должна быть введена, будет, безусловно, меняться в зависимости, например, от количества РТН, необходимого для введения, и тяжести состояния, подвергающегося лечению. Однако, как правило, удовлетворительные результаты будут систематически получаться при ежедневных дозах от примерно 0,5 мкг/кг до примерно 10 мкг/кг массы тела животного, предпочтительно 1 мкг/кг до примерно 6 мкг/кг массы тела.
Пероральное введение может проводиться регулярно, например, один или несколько раз в день или в неделю; скачкообразно, т.е. нерегулярно в течение дня или недели; или циклически, например, регулярно в течение периода нескольких дней или недель после периода без введения.
Совместное введение РТН и кальцитонина включает одновременное, раздельное или последовательное введение двух соединений. Одновременное введение означает введение двух соединений в одной лекарственной форме; раздельное введение означает введение двух соединений примерно в одно и то же время, но в отдельных лекарственных формах; и последовательное введение означает введение одного соединения, после которого вводится другое. Последовательное введение может также принимать форму одновременного или раздельного введения, сопровождаемого прекращением одновременного или раздельного введения, и затем непрерывное введение только одного из двух соединений.
Пероральное введение РТН и кальцитонина по данному изобретению может быть выполнено любым известным способом, например, в виде жидких или твердых лекарственных форм.
Жидкие лекарственные формы включают растворы, эмульсии, суспензии, сиропы и эликсиры. Помимо РТН и/или кальцитонина, жидкие композиции могут также включать инертные наполнители, обычно применяемые в этой области, такие как способствующие растворению агенты, такие как этанол; масла, такие как хлопковое, касторовое и кунжутное масла; смачивающие агенты; эмульгаторы, суспендирующие агенты; подсластители; ароматизаторы; и растворитель, такой как вода.
Твердые лекарственные формы включают капсулы, мягкие гелевые капсулы, таблетки, каплетки, порошки, гранулы или другие твердые пероральные лекарственные формы, все они могут быть получены способами, хорошо известными специалистам. Помимо РТН и/или кальцитонина, эти твердые лекарственные формы, как правило, включают фармацевтически приемлемый агент доставки для РТН и/или кальцитонина.
Соответствующие агенты доставки представляют собой любую из 123 модифицированных аминокислот, раскрытых в патенте US 5866536, или любую из 193 модифицированных аминокислот, описанных в патенте US 5773647, или любую их комбинацию. Содержание упомянутых выше патентов US 5773647 и 5866536 во всей их полноте тем самым включено путем цитирования. Кроме того, агент доставки может быть динатриевой солью любой из упомянутых выше аминокислот, а также ее сольватом с этанолом и гидратом. Соответствующие соединения включают соединения следующей формулы I.
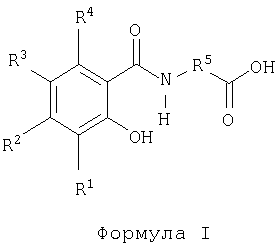
где R1, R2, R3 и R4 независимо означают водород, -ОН, -NR6R7, галоид, (С1-С4)алкил или (С1-С4)алкокси;
R5 означает замещенный или незамещенный (С2-С16)алкилен, замещенный или незамещенный (С2-С16)алкенилен, замещенный или незамещенный (С1-С12)алкил(арилен) или замещенный или незамещенный арил(С1-С12)алкилен;
R6 и R7 независимо означают водород, кислород или (С1-С4)алкил; и их гидраты и сольваты со спиртом. Соединения формулы I, а также их динатриевые соли и сольваты со спиртом и их гидраты описаны в WO 00/059863 наряду со способами их получения.
Предпочтительными агентами доставки являются N-(5-хлорсалицилоил)-8-аминокаприловая кислота (5-CNAC), N-(10-[2-гидроксибензоил]амино)декановая кислота (SNAD), N-(8-[2-гидроксибензоил]амино)каприловая кислота (SNAC) и их мононатриевые и динатриевые соли, сольваты с этанолом их натриевых солей и моногидраты их натриевых солей и любая их комбинация. Наиболее предпочтительным агентом доставки является динатриевая соль 5-CNAC и ее моногидрат.
Фармацевтические композиции по настоящему изобретению обычно содержат эффективное для доставки количество одного или нескольких агентов доставки, т.е. количество, достаточное для того, чтобы доставить РТН и/или кальцитонин для требуемого воздействия. Как правило, агент доставки присутствует в количестве 2,5-99,4 мас.%, более предпочтительно 25-50 мас.% от всей композиции.
Композиции могут дополнительно содержать добавки в количествах, обычно используемых, включая, но без ограничения, регулятор рН, консервант, ароматизатор, маскирующий вкус агент, аромат, гигроскопичное вещество, тонизирующий агент, краситель, поверхностно-активное вещество, пластификатор, смазывающий агент, такой как стеарат магния, средство для текучести, средство для сжатия, растворитель, наполнитель, разбавитель, такой как микрокристаллическая целлюлоза, например, авицел РН 102, поставляемый корпорацией FMC, или любую их комбинацию. Другие добавки могут включать соли фосфатного буфера, лимонную кислоту, гликоли и другие диспергирующие агенты.
Композиция может также включать один или несколько ингибиторов, таких как актинонин или эпиактинонин и их производные; апротинин, трасулол и ингибитор Баумана-Бирка.
Кроме того, ингибитор транспорта, т.е. ρ-гликопротеин, такой как кетопрофин, может присутствовать в композиции по настоящему изобретению.
Твердые фармацевтические композиции по данному изобретению могут быть получены обычными способами, например, путем смешения активного агента или активных агентов, агента доставки и любых других ингредиентов, перемешивания и заполнения капсул или, вместо заполнения капсул, формованием, сопровождающимся таблетированием или компрессионным формованием для получения таблеток. Кроме того, твердая дисперсия может быть образована известными способами, сопровождающимися дальнейшей обработкой для формирования таблетки или капсулы.
Предпочтительно ингредиенты в фармацевтических композициях по данному изобретению являются гомогенными или однородно смешанными по всей лекарственной форме.
Пероральное введение по настоящему изобретению может предназначаться любому нуждающемуся в этом животному, включая, но без ограничений, млекопитающих, таких как грызуны, коровы, свиньи, собаки, кошки и приматы, особенно люди.
Следующие примеры служат для дальнейшей иллюстрации изобретения.
Пример 1
Нижеперечисленные капсулы готовили следующим образом.
Капсулы приготавливали из 400 мг динатриевой соли 5-CNAC/800 мкг sCT/800 мкг РТН (капсула 1А).
Капсулы приготавливали из 400 мг динатриевой соли 5-CNAC/800 мкг РТН (капсула 1Б).
Капсулы приготавливали из 400 мг динатриевой соли 5-CNAC/800 мкг sCT (капсула 1В).
Капсулы приготавливали из 800 мкг РТН (капсула 1Г).
РТН означает фрагмент 1-34 РТН, имеющийся в продаже. sCT означает кальцитонин из лосося. Все капсулы приготавливали в виде сухих смесей путем взвешивания индивидуальных компонентов, смешивания их вместе до гомогенного состояния и затем вручную помещали 400 мг смеси в каждую капсулу. Для капсул, содержащих только РТН, взвешивали РТН и 400 мг помещали непосредственно внутрь каждой капсулы.
Пример 2
Введение приматам
Капсулы, приготовленные в примере 1, вводили макакам резус следующим образом: каждой из четырех обезьян в группе давали 1 капсулу, приготовленную в примере 1, следующим образом.
Макаки резус голодали в течение ночи перед получением дозы и в полном сознании удерживались в креслах для продолжения периода исследования. Капсулы и последующие 10 мл воды вводили через желудочный зонд.
Образцы крови собирали после введения через 0, 0,25, 0,5, 0,75, 1, 1,5, 2, 3, 4, 5 и 6 ч. Кальцитонин лосося в плазме и РТН в плазме определяли радиоиммунологическим анализом. Данные по содержанию кальцитонина лосося (sCT) и РТН в плазме приматов, полученные от каждой группы обезьян, усредняли и максимальное среднее содержание кальцитонина рассчитывали и представляли в таблицах 1-5.
2*SD означает среднеквадратичное отклонение,
3*SEM означает среднее значение среднеквадратичной ошибки,
4*LLOQ означает нижний предел определения количества.
2*SD означает среднеквадратичное отклонение,
3*SEM означает среднее значение среднеквадратичной ошибки,
4*LLOQ означает нижний предел определения количества.
2* SD означает среднеквадратичное отклонение,
3* SEM означает среднее значение среднеквадратичной ошибки.
2* SD означает среднеквадратичное отклонение,
3* SEM означает среднее значение среднеквадратичной ошибки.
2* SD означает среднеквадратичное отклонение,
3* SEM означает среднее значение среднеквадратичной ошибки,
4* LLOQ означает нижний предел определения количества.
Как можно видеть из данных таблиц 1-5, уровни sCT и РТН в плазме фактически одни и те же, вводились ли соединения раздельно или вместе. Однако пероральное введение комбинации РТН и кальцитонина, хотя и приводит к концентрационным уровням РТН и кальцитонина в плазме, соответствующим тем, которые достигаются при введении каждого агента в отдельности, но довольно неожиданно имеет своим результатом снижение концентраций кальция в сыворотке до уровня, наблюдаемого при введении одного кальцитонина.
Упомянутые выше варианты воплощения и примеры приведены только для иллюстрации изобретения и не предназначены для того, чтобы быть ограничением. Многочисленные и разнообразные другие варианты воплощения, входящие в объем изобретения, легко доступны специалистам в данной области.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ КАЛЬЦИТОНИНА ПРИ ОСТЕОАРТРИТЕ | 2004 |
|
RU2368390C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2006 |
|
RU2469709C2 |
| 5-CNAC В КАЧЕСТВЕ АГЕНТА ДЛЯ ПЕРОРАЛЬНОЙ ДОСТАВКИ ФРАГМЕНТОВ ПАРАТИРОИДНОГО ГОРМОНА | 2002 |
|
RU2322256C2 |
| КРИСТАЛЛИЧЕСКИЕ ФОРМЫ ДИНАТРИЕВОЙ СОЛИ N-(5-ХЛОРСАЛИЦИЛОИЛ)-8-АМИНОКАПРИЛОВОЙ КИСЛОТЫ | 2006 |
|
RU2507196C2 |
| ПРИМЕНЕНИЕ КАЛЬЦИТОНИНА ДЛЯ ЛЕЧЕНИЯ РЕВМАТОИДНОГО АРТРИТА | 2006 |
|
RU2453330C2 |
| ПЕРОРАЛЬНОЕ ВВЕДЕНИЕ КАЛЬЦИТОНИНА | 2003 |
|
RU2355417C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ ДЛЯ ПЕРОРАЛЬНОГО ВВЕДЕНИЯ ФАРМАКОЛОГИЧЕСКИ ДЕЙСТВУЮЩИХ ВЕЩЕСТВ | 2001 |
|
RU2287999C2 |
| ЛЕЧЕНИЕ ДИАБЕТА И МЕТАБОЛИЧЕСКОГО СИНДРОМА | 2010 |
|
RU2537181C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ чГР, ДЛЯ ПЕРОРАЛЬНОГО ВВЕДЕНИЯ | 2007 |
|
RU2493868C2 |
| ПЕПТИДНЫЕ АНАЛОГИ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ И РАССТРОЙСТВ | 2012 |
|
RU2616511C2 |
Настоящая группа изобретений относится к пероральной доставке паратиреоидного гормона РТН. Более конкретно изобретение направлено на применение кальцитонина в комбинации с РТН с целью перорального введения РТН. Способ перорального введения эффективной дозы паратиреоидного гормона РТН включает совместное пероральное введение пациенту, нуждающемуся в РТН, эффективного количества РТН и эффективного количества кальцитонина. Способ по изобретению делает возможным пероральное введение РТН без побочных эффектов повышенного содержания кальция в крови, повышенного содержания кальция в моче и почечнокаменной болезни. 6 н. и 7 з.п. ф-лы, 5 табл.
| WO 9830590 A1, 16.07.1998 | |||
| WO 8700750 A1, 12.02.1987 | |||
| US 5364840 А, 15.11.1994 | |||
| RU 99124209 А, 20.09.2001. |
Авторы
Даты
2007-06-10—Публикация
2002-05-31—Подача