Область изобретения
Настоящее изобретение относится к препарату, содержащему формотерол и будесонид, для применения в лечении воспалительных состояний/расстройств, особенно респираторных заболеваний, таких как астма, хроническая обструктивная болезнь легких (ХОБЛ) и ринит.
Предшествующий уровень техники
Стабильность представляет собой один из наиболее важных факторов, определяющих, могут ли соединение или смесь соединений быть представлены в виде терапевтически пригодного фармацевтического продукта.
Комбинации формотерола и будесонида известны из области техники, например из WO 93/11773, где описана такая комбинация, которая в настоящее время имеется в продаже как Symbicort® в сухом порошковом ингаляторе. Существует множество других ингаляторов, при помощи которых может быть введен вдыхаемый продукт, такие как дозирующие ингаляторы под давлением (ДИпД). Препаратам для ДИпД могут требоваться определенные эксципиенты, как описано в WO 93/05765.
В настоящее время было обнаружено, что некоторые HFA (гидрофторалкан) препараты, содержащие формотерол и будесонид вместе с поливинилпирролидоном (ПВП) и полиэтиленгликолем (ПЭГ), демонстрируют превосходную физическую стабильность суспензии.
Описание изобретения
В соответствии с настоящим изобретением предложена фармацевтическая композиция, содержащая формотерол, будесонид, HFA 227, ПВП и ПЭГ, отличающаяся тем, что ПВП присутствует в количестве от приблизительно 0,0005 до приблизительно 0,03 мас.%, а ПЭГ присутствует в количестве от приблизительно 0,05 до приблизительно 0,35 мас.%
Предпочтительно ПВП присутствует в количестве 0,001 мас.% Предпочтительно ПВП представляет собой ПВП К25.
Предпочтительно ПЭГ присутствует в количестве 0,3 мас.% Предпочтительно ПЭГ представляет собой ПЭГ 1000.
Предпочтительно концентрации формотерола/будесонида являются такими, что препарат доставляет формотерол/будесонид в количестве 4,5/40 мкг, 4,5/80 мкг, 4,5/160 мкг или 4,5/320 мкг на выброс.
Формотерол может находиться в форме смеси энантиомеров. Предпочтительно формотерол находится в форме единственного энантиомера, предпочтительно R,R-энантиомера. Формотерол может находиться в форме свободного основания, соли, или сольвата, или сольвата соли, предпочтительно формотерол находится в форме его соли, представляющей собой фумарата дигидрат. Другие физиологически приемлемые соли, которые могут быть использованы, включают в себя хлорид, бромид, сульфат, фосфат, малеат, тартрат, цитрат, бензоат, 4-метоксибензоат, 2- или 4-гидроксибензоат, 4-хлорбензоат, пара-толуолсульфонат, бензолсульфонат, аскорбат, ацетат, сукцинат, лактат, глутарат, глюконат, трикабаллат, гидроксинафталинкарбоксилат или олеат.
Предпочтительно второй активный ингредиент представляет собой будесонид, включая его эпимеры, сложные эфиры, соли и сольваты. Более предпочтительно второй активный ингредиент представляет собой будесонид или его эпимер, такой как 22R-эпимер будесонида.
Фармацевтические композиции по данному изобретению могут применяться для лечения или профилактики респираторного заболевания, в частности для лечения или профилактики астмы, ринита или ХОБЛ.
В дополнительном аспекте данного изобретения предлагается способ лечения респираторного заболевания, в частности астмы, ринита или ХОБЛ, у млекопитающего, при котором пациенту вводят фармацевтическую композицию, определенную в данном изобретении.
Композиции по данному изобретению могут быть ингалированы из любого пригодного устройства, представляющего собой ДИ (дозирующий ингалятор). Дозы зависят от тяжести заболевания и типа пациента, но предпочтительно составляют 4,5/80 мкг или 4,5/160 мкг на выброс, как было определено выше.
Было обнаружено, что концентрация ПВП (0,001 мас.%), используемая в этом препарате, дает равным образом стабильные препараты во всем требуемом диапазоне доз, включающем в себя широкий диапазон концентраций активных компонентов, и при гораздо более низкой концентрации, чем указано в предшествующем уровне техники.
Данное изобретение иллюстрируется следующими примерами.
Экспериментальный раздел
Для оценки физической стабильности суспензии могут быть использованы два метода: определение оптических характеристик суспензии (OSCAR) и TURBISCAN. Оба метода применяются для полуколичественного определения скоростей седиментации/разрушения суспензии. OSCAR измерения проводят с использованием непосредственно РЕТ-бутылей (бутылей из полиэтилентерефталата). Для анализа TURBISCAN суспензии переносят в специально изготовленные ячейки под давлениме для измерения пропускания света и обратного рассеяния.
МЕТОДИКА
OSCAR
Прибор для определения оптических характеристик суспензии (OSCAR) изготовлен специальным образом для быстрого и воспроизводимого полуколичественного определения характеристик суспензии дозирующего ингалятора.
В приборе OSCAR для определения характеристик препарата предварительно перемешанной суспензии используют изменения пропускания света в зависимости от времени (схематическое изображение прибора приведено на Фиг.1). Прибор состоит из тестового узла с двумя головками. Головка с левой стороны прибора используется для разбавленных суспензий, а правая - для концентрированных суспензий. Селекторный переключатель, вмонтированный между двумя тестовыми головками, используется для изменения выбора концентрации. Выходной сигнал с выбранной тестовой головки направляется во вмонтированный в прибор индикатор напряжения и на компьютер для регистрации показаний. Аналоговые сигналы, поступающие с фотодетекторов, оцифровываются и значения сохраняются в файлах с данными, а затем обрабатываются с использованием соответствующего пакета программного обеспечения. В приборе имеются два вмонтированных индикатора напряжения, один - для верхнего, а другой - для нижнего фотодетектора. Верхний и нижний фотодетекторы регулируются по высоте, и имеется индикатор считывания положения для показа установленной высоты для каждого теста.
Для калибровки чувствительности прибора OSCAR используют стандарты мутности Reagecon (2500-4000 нефелометрических единиц мутности (NTU, nephelometric turbidity unit)). В этом случае в качестве стандартного калибровочного контроля используется калибровочный стандарт мутности 3000 NTU. Однако для установления чувствительности зондов в отношении специфического напряжения, соответствующего данному препарату, может применяться любой из стандартов мутности.
Образцы для теста на приборе OSCAR представляют в PET бутылях, закрытых недозирующими клапанами.
Информация по предшествующему уровню техники и аналогам для данного способа описана в статьях из Drug Delivery to the Lungs IX, 1997, Method Development of the OSCAR technique for the characterization of metered dose inhaler formulations, авторы N.Govind, P.Lambert, и Drug delivery to the Lungs VI, 1995, A Rapid Technique for Characterisation of the Suspension Dynamics of metered Dose Inhaler Formulations, автор Р.A.Jinks (3M Healthcare Ltd).
TURBISCAN
Tubiscan MA 2000 представляет собой анализатор стабильности и нестабильности концентрированной дисперсии и эмульсии или вертикальный сканирующий макроскопический анализатор. Он состоит из считывающей магнитной головки, перемещающейся вдоль плоскодонной цилиндрической стеклянной ячейки на 5 мл и снимающей показания пропущенного и рассеянного в обратном направлении света каждые 40 мкм на максимальной высоте образца 80 мм. Сканирование может быть повторено с программируемой частотой для получения макроскопического отпечатка образца.
В считывающей магнитной головке используются источник пульсирующего излучения в ближней инфракрасной области (длина волны = 850 нм) и два синхронных детектора:
Детектор пропускания: улавливает свет, прошедший через раствор в пробирке при 0°С.
Детектор обратного рассеяния: улавливает свет, рассеянный в обратном направлении продуктом при 135°С.
Полученный профиль характеризует гомогенность образцов, концентрацию и средний диаметр частиц. Он дает возможность количественной оценки физических процессов, происходящих в образце. Выявляя также дестабилизацию, Turbiscan обеспечивает возможность сравнения, например, скорости осаждения в различных суспензиях.
Turbiscan может использоваться в различных режимах, например в режимах пропускания или обратного рассеяния. Turbiscan был использован в приведенных примерах для измерения пропускания света в зависимости от времени.
Нестабильность дисперсии представляет собой результат двух физических процессов: а) увеличения размера частиц в результате образования агрегатов вследствие флокуляции, б) перемещения частиц, имеющего результатом разрушение или седиментацию. Когда продукт стабилен (то есть отсутствует флокуляция, разрушение или седиментация), проходящий и отраженный в обратном направлении свет остается постоянным, то есть его развертки демонстрируют постоянный уровневый профиль. Если продукт претерпевает изменения размера частиц, вариации проходящего/отраженного в обратном направлении света отражаются как изменение в направлении развертки от горизонтального профиля или профиля в устойчивом состоянии.
Для систем под давлением требуется ячейка, пригодная для таких образцов под давлением. Такая ячейка была использована для оценки данных HFA препаратов. Развертки снимались в AUTO режиме.
Средние величины % пропускания были получены в зоне вокруг середины образца суспензии.
ИСХОДНАЯ ОЦЕНКА
Для исходной оценки использовали только OSCAR.
Препараты, содержавшие дигидрат фумарата формотерола, будесонид, 0,001 мас.% ПВП К25 и либо 0,1 мас.%, либо 0,3% ПЭГ 1000 в HFA-227, готовили в бутылях из полиэтилентерефлата (PET, polyethylene terephlate), закрытых клапаном непрерывного действия. Для всех препаратов концентрация дигидрата фумарата формотерола оставалась постоянной и равной 0,09 мг/мл (эквивалентно 4,5 мкг дигидрата фумарата формотерола на выброс), а концентрация будесонида варьировала между приблизительно 1 мг/мл и 8 мг/мл (эквивалентно от 40 мкг до 320 мкг на выброс).
Анализ OSCAR этих препаратов дал относительно низкие значения пропускания света на нижнем датчике, что является показателем стабильных суспензий с низкими показателями флокуляции. Начальные показания были таковы, что 0,001 мас.% ПВП с 0,3 мас.% ПЭГ 1000 дают наилучшую суспензию.
ДАЛЬНЕЙШАЯ ОЦЕНКА: различные концентрации ПВП К25 с постоянной концентрацией ПЭГ 1000, составлявшей 0,3 мас.%.
Для оценки препаратов использовали OSCAR, Turbiscan и фотографические методы. Методики OSCAR и Turbiscan были описаны ранее. Анализировали образцы с различными концентрациями ПВП для определения стабильности суспензии с течением времени.
ФОТОГРАФИЧЕСКИЙ АНАЛИЗ
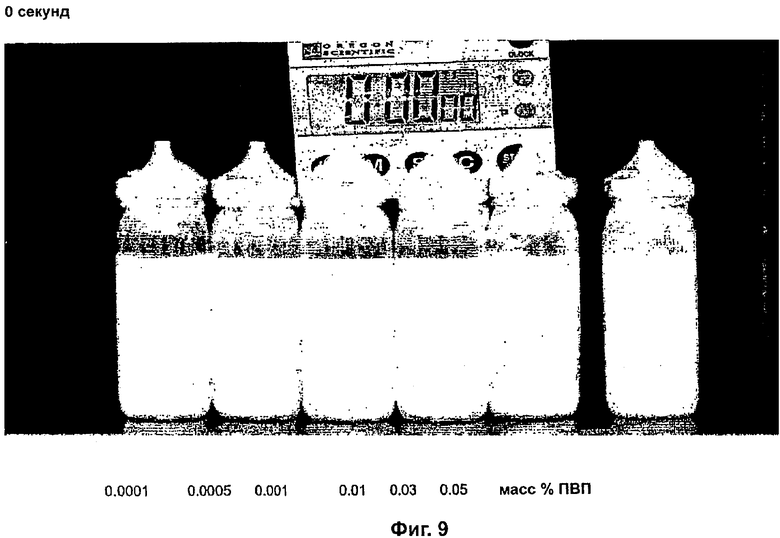
Для фотографического анализа готовили образцы в PET-бутылях и осуществляли цифровое фотографирование во времени, используя черный фон. Эти фотографии (некоторые из которых представлены здесь) демонстрируют поведение суспензии во времени и обеспечивают возможность легкого сравнения эффективности различных концентраций ПВП. Концентрация ПВП варьировала от 0,0001 до 0,05 мас.% На фотографиях концентрация ПВП составляет, слева направо:
ЦИФРОВОЕ ФОТОГРАФИРОВАНИЕ ПРЕПАРАТОВ, ДЕМОНСТРИРУЮЩЕЕ СТЕПЕНЬ ДИСПЕРСНОСТИ ВО ВРЕМЕНИ
Фиг.9, 10 и 11 демонстрируют будесонид 160 мкг/выброс, формотерол 4,5 мкг/выброс с различными концентрациями ПВП К25 и 0,3% ПЭГ 1000 при времени стояния, составлявшем 0, 15, 30 и 60 секунд.
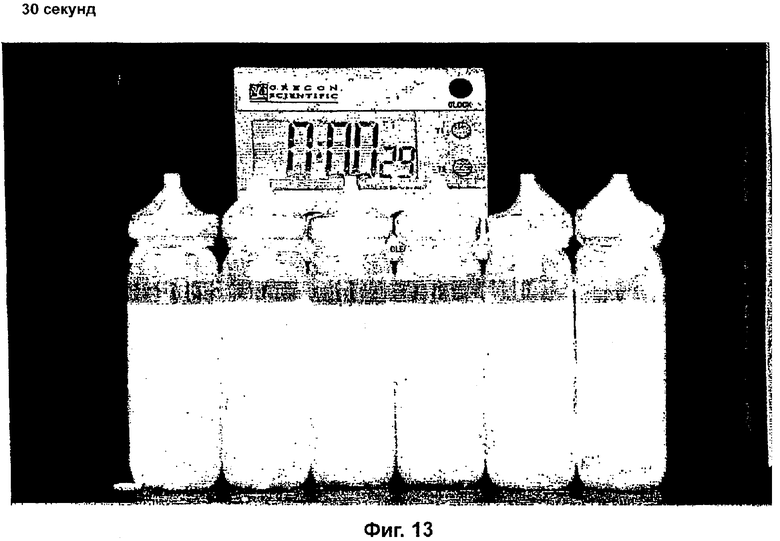
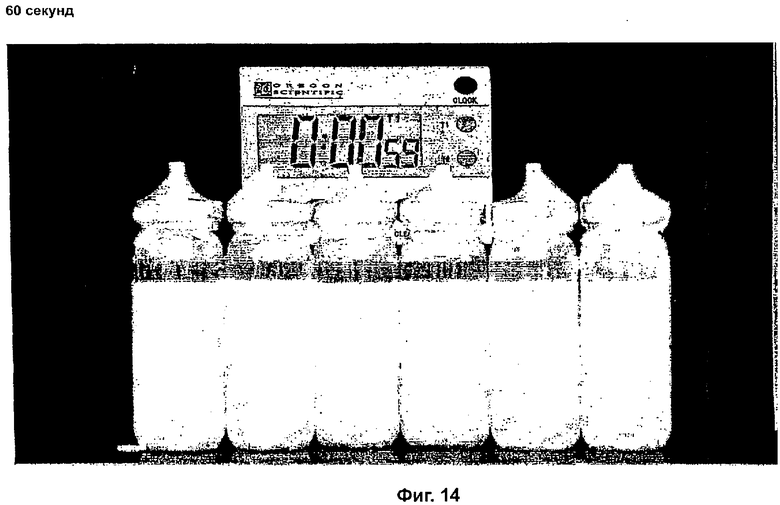
Фиг.12, 13 и 14 демонстрируют будесонид 80 мкг/выброс, формотерол 4,5 мкг/выброс с различными концентрациями ПВП К25 и 0,3% ПЭГ 1000 при времени стояния, составлявшем 0, 30 и 60 секунд.
ТАБЛИЦА СТЕПЕНИ ДИСПЕРСНОСТИ СУСПЕНЗИЙ В ЗАВИСИМОСТИ ОТ ВРЕМЕНИ (ВСЕ ОБРАЗЦЫ)
Фотографии были получены при всех дозах (от 320 мкг/4,5 мкг до 40 мкг/4,5 мкг) в моменты времени 0, 15, 30, 60, 90 секунд и 2, 5 и 10 минут. Поскольку при этом было получено слишком много фотографий для того, чтобы их можно было представить здесь, была построена диаграмма, представляющая степень дисперсности в зависимости от времени.
Если образец был полностью суспендирован, его оценивали как 0, например, в момент времени 0 минут он был полностью диспергирован. Исходя из этого образцы оценивали по возрастающей от 1 до 5 с 20%-ными интервалами так, чтобы выразить степень дисперсности, то есть О соответствовал полностью суспендированной суспензии, а 5 - полностью разрушенной суспензии. Это дает возможность для определенного сравнения на всем диапазоне доз и в использовавшемся диапазоне концентраций ПВП.
(Примечание: концентрация формотерола во всех образцах составляет 4,5 мкг/выброс).
(Образцы были полностью диспергированы в момент времени 0 секунд и поэтому все имели оценку 0).
Полностью диспергированный - 0.
Более чем 80% диспергировано, то есть присутствует менее 20% прозрачной жидкости - 1.
Более чем 60% диспергировано, то есть присутствует менее 40% прозрачной жидкости - 2.
Менее чем 40% диспергировано, то есть присутствует более 60% прозрачной жидкости - 3.
Менее чем 20% диспергировано, то есть присутствует более 80% прозрачной жидкости - 4.
Полностью разрушена - 5.
Суспензии, признанные превосходными, выделены жирным шрифтом.
Можно видеть, что препараты с 0,001 мас.% ПВП давали наилучшую стабильность суспензии.
ДАННЫЕ OSCAR (Графики зависимости пропускания света от времени)
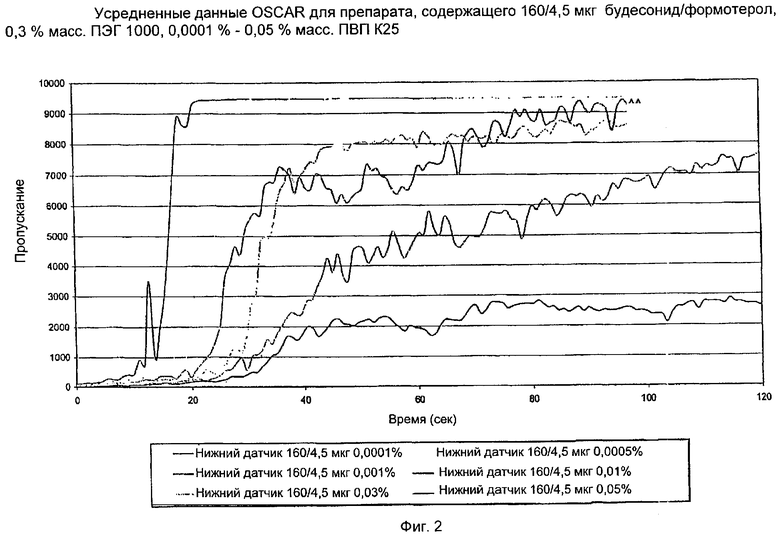
На Фиг.2 показаны усредненные OSCAR показатели пропускания (только нижний датчик) для различных концентраций ПВП К25. Низкий показатель пропускания свидетельствует о том, что суспензия дисперсная и не пропускает свет. Отсюда видно, что самая низкая линия представляет собой наиболее стабильный препарат. Он представляет собой образец 0,001% ПВП.
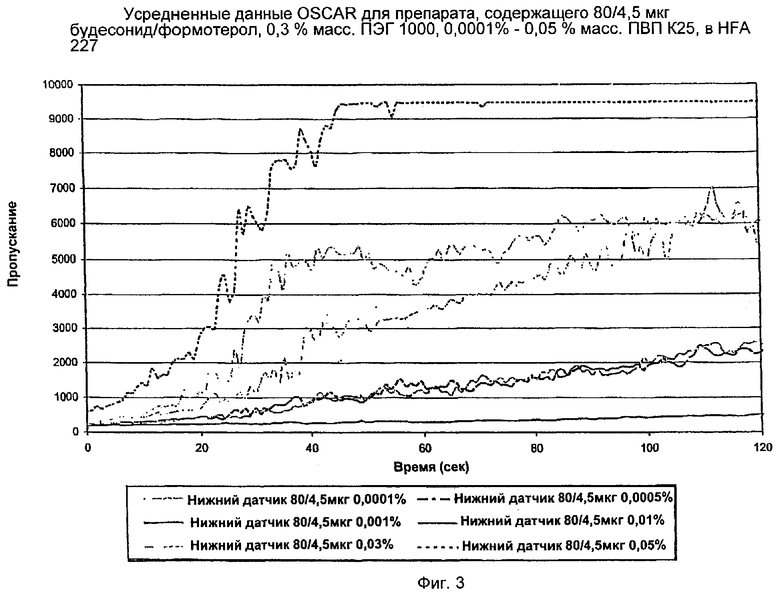
На Фиг.3 линия внизу, опять же с низкими показателями пропускания, очевидно демонстрирует, что препарат, содержащий 0,001% ПВП, является наиболее стабильным.
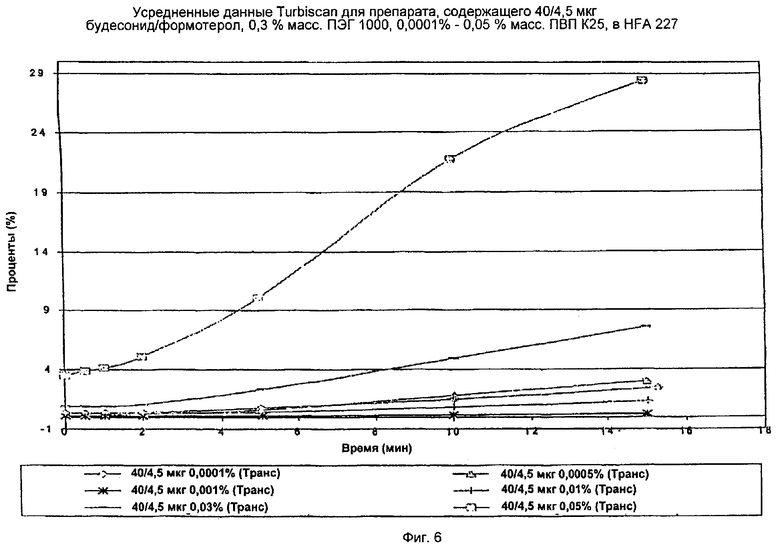
ДАННЫЕ TURBISCAN (Графики зависимости процента (%) пропускания света от времени)
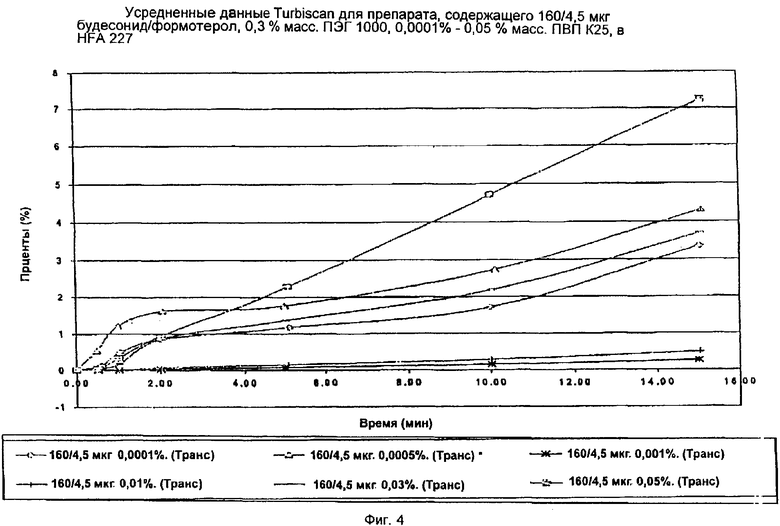
Данные согласно Turbiscan могут быть интерпретированы подобно данным OSCAR в том, что низкий процент (%) пропускания указывает на то, что суспензия дисперсная. Усредненные показатели % пропускания, приведенные здесь, были получены в зоне вокруг средней части образца суспензии. На фиг.4 наиболее стабильный препарат представляет собой самую низкую линию с самым низким % пропускания, а именно черную жирную линию с 0,001 мас.% ПВП.
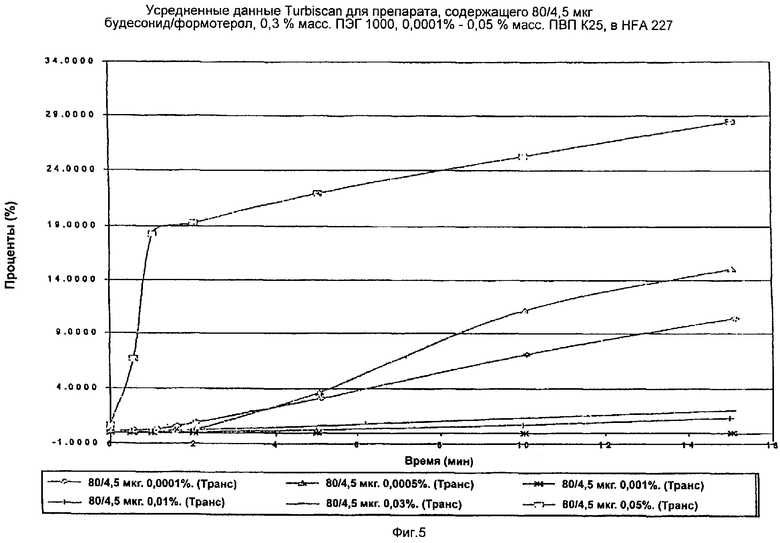
На фиг.5 и 6 показано, что суспензия с 0,001 мас.% ПВП наиболее стабильна (жирная линия внизу) с наименьшим % пропускания.
ДОПОЛНИТЕЛЬНАЯ ОЦЕНКА: Определение оптимальной концентрации ПЭГ1000
Для этой оценки использовали данные фотографирования, turbiscan и данные по силе выброса (работа клапана) для определения оптимальной концентрации ПЭГ.
МЕТОДОЛОГИЯ - Сила выброса (усилие отвода при возврате штока 0,5 мм)
Тестирование силы выброса осуществляли, используя аппарат для тестирования Lloyd LRX. Тестируемый узел ДИпД помещают клапаном вниз в держателе баллона на нижней платформе блока. Верхний ползун затем перемещают до положения прямо над основанием баллона. Приведение баллона в действие осуществляют в соответствии со стандартным протоколом. В процессе измерения данные по силе собирают при помощи динамометрического элемента, расположенного в верхней части верхнего ползуна. Эта программа была разработана для получения усилия отвода при возврате штока 0,5 мм, поскольку считается, что это именно та точка, в которой дозировочная камера снова заполняется.
Низкое усилие отвода является показателем высокого трения и потенциальных проблем залипания. Она также свидетельствует о том, что может возникнуть проблема низких выбрасываемых масс, поскольку пропеллент поступает в дозирующую камеру медленнее и имеется время для его испарения. Тестирование силы выброса осуществляли при данных выбросах.
ДАННЫЕ
ДАННЫЕ ПО СИЛЕ ВЫБРОСА
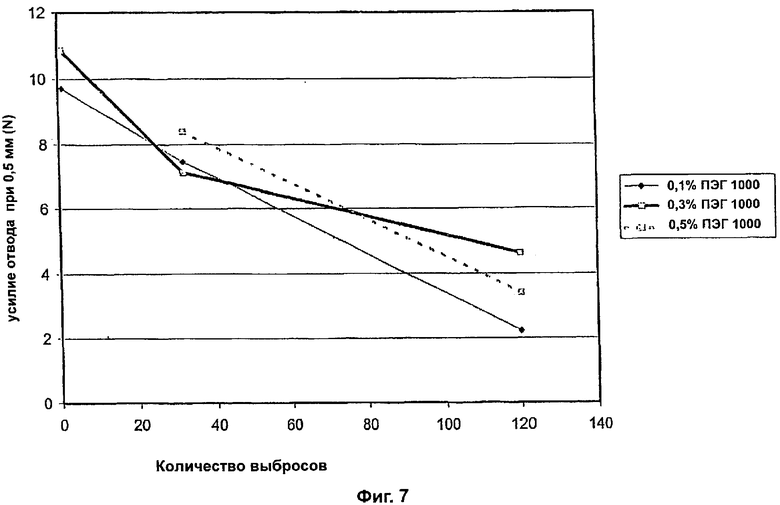
На Фиг.7 показано влияние концентрации ПЭГ 1000 на усилие отвода штока для препарата 4,5/160 мкг формотерол/будесонид.
Видно, что при 120 выбросах усилие отвода для концентрации ПЭГ 1000, составляющей 0,3 мас.%, больше, чем для других концентраций, составляющих 0,5% и 0,1%. В общем, чем больше усилие отвода, тем меньше вероятность залипания штока клапана. Вышеприведенные данные свидетельствуют о том, что в данном случае предпочтительной является концентрация 0,3%.
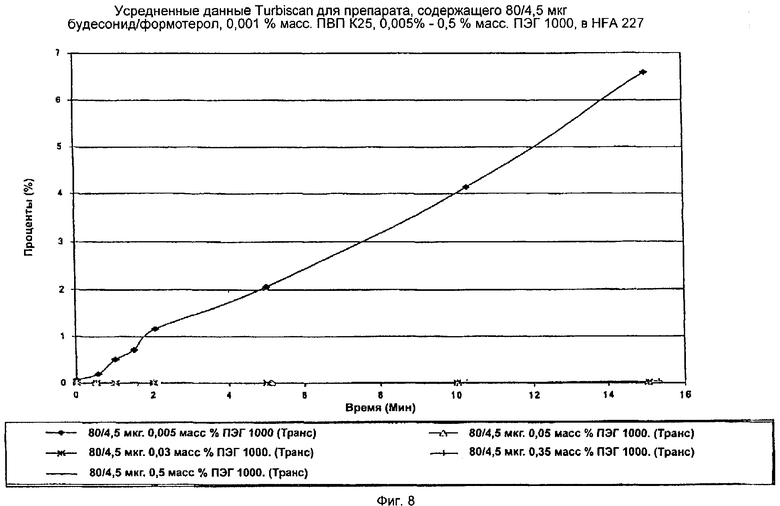
ДАННЫЕ TURBISCAN
Данные Turbiscan (Фиг.8) показывают, что существует небольшое различие между стабильностью суспензий, приготовленных с различными уровнями ПЭГ 1000, за исключением уровня 0,005 мас.%, который оказался неудовлетворительным.
ФОТОГРАФИЧЕСКИЙ АНАЛИЗ
Цифровые фотографии суспензий, содержащих будесонид, формотерол, HFA 227, 0,001 мас.% ПВП и различные уровни ПЭГ 1000, продемонстрировали небольшое изменение стабильности суспензий с течением времени (от 0 секунд до 10 минут) за исключением уровня ПЭГ, составляющего 0,005 мас.%(соответствует данным Turbiscan).
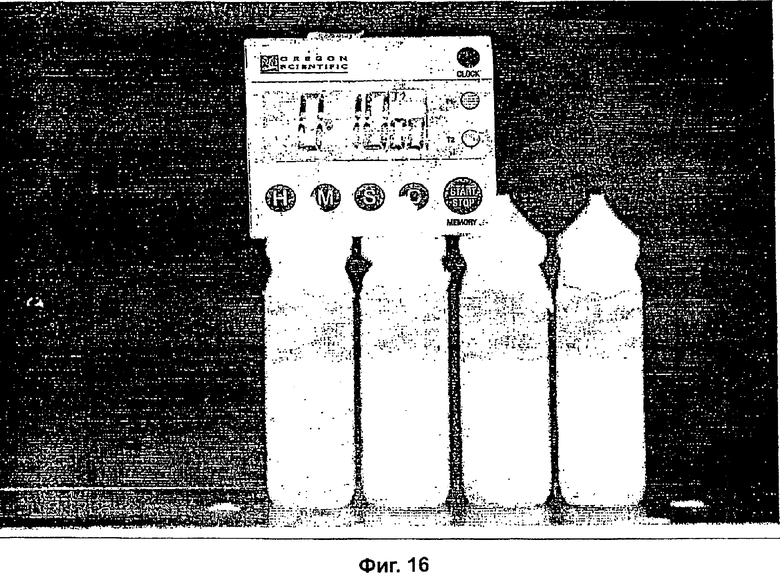
На Фиг.15 и 16 показан будесонид 80 мкг/выброс, формотерол 4,5 мкг/выброс с 0,001% ПВП К25 и различными концентрациями ПЭГ 1000 в моменты времени простоя 0 (1) и 10 (2) минут.
ДАННЫЕ ПО РАБОТЕ ПРОДУКТА
В дополнение к вышеизложенному, данные по характеристикам продукта для препаратов, содержащих дигидрат фумарата формотерола/будесонид, при производительности, составляющей 4,5/80 мкг на выброс и 4,5/160 мкг на выброс с 0,001% ПВП К25 и либо 0,1%, либо 0,3% ПЭГ 1000, были стабильны в течение времени вплоть до 12 месяцев включительно при 25°С/60% О В (относительная влажность).




Изобретение относится к химико-фармацевтической промышленности и касается композиции, содержащей в своем составе формотерол и будесонид, HFA 227, ПВП (поливинилпирролидон) в концентрации 0,001 мас.%, и ПЭГ (полиэтиленгликоль) в концентрации 0,3 мас.%, при этом ПВП представляет собой ПВП К25 и ПЭГ представляет собой ПЭГ 1000. Композиция применяется для лечения респираторных заболеваний. Композиция обладает значительно сниженными побочными эффектами за счет малых концентраций вспомогательных веществ и высокой стабильностью при хранении. 7 з.п. ф-лы, 5 табл., 16 ил.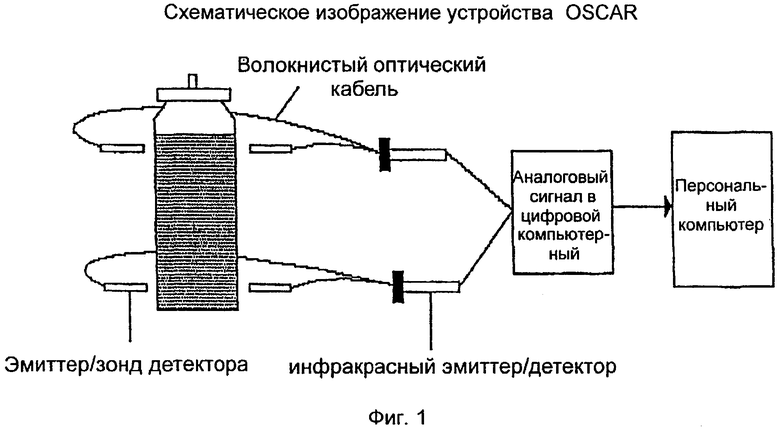
| Домовый номерной фонарь, служащий одновременно для указания названия улицы и номера дома и для освещения прилежащего участка улицы | 1917 |
|
SU93A1 |
| Способ записи изображения на полупроводниковом слое | 1973 |
|
SU534731A1 |
| US 6004537 A, 21.12.1999 | |||
| RU 2000131218 A, 10.11.2002 | |||
| реф | |||
| Bames PJ., «Scientific rationale for inhaled combination therapy with long-acting beta2-agonists and corticosteroids.», Eur Respir J | |||
| Топчак-трактор для канатной вспашки | 1923 |
|
SU2002A1 |
| реф | |||
| Chuchalin AG et al., «A health-related quality-of-life comparison of | |||
Авторы
Даты
2007-06-27—Публикация
2003-01-29—Подача