Изобретение относится к ингибиторам полициклического нуклеотида ксантин фосфодистеразы V.
Соединения ингибиторов фосфодистеразы (ФДЭ) V описаны Kenneth J Murray в Phosphodiesterase VA Inhibitors, DN&P 6 (3), pp.150-156 (April, 1993), (которая включена здесь в качестве ссылки во всей своей полноте), имеющие потенциальное терапевтическое значение для ряда физиологических расстройств. Одним соединением, раскрытым в статье Муррея, является MIMAX, полициклический ингибитор ксантин ФДЭ V, замещенный в положении 8 группой -NHCH3.
Патент США US 5409934 (включен здесь в качестве ссылки во всей своей полноте) раскрывает ряд ингибиторов ксантин ФДЭ V, которые замещены в положении 8, наряду с другими группами, одной из следующих групп: -NO2, -NRsRt или -NR6SO2R5, где Rs и Rt, независимо друг от друга, являются каждая атомом водорода или алкильной группой, либо Rs и Rt вместе с атомом азота, к которому они оба присоединены, образуют фталимидную группу, R5 представляет собой алкильную или арильную группу, a R6 представляет собой атом водорода или -SO2R7, где R7 - алкильная или арильная группа.
Патент США US 5470579 (включен здесь в качестве ссылки во всей своей полноте) раскрывают ингибитор ксантин ФДЭ V, имеющий замещенную или незамещенную группу -NH2 в положении 8, например -NHR, где R представляет собой алкильную группу с 1-6 атомами углерода.
Международная заявка WO 93/23401 (включена здесь в качестве ссылки во всей своей полноте) раскрывает ингибиторы ксантин ФДЭ V, которые замещены в положение 8 группой -NH(CH2)2CH(CH2OR4)2.
Международная заявка WO 92/05176 (включена здесь в качестве ссылки во всей своей полноте) раскрывает ингибиторы 8-ациламиноксантин ФДЭ V, которые замещены в положение 8 группой -NHCOC6H5COOH.
Международная заявка WO 92/05175 (включена здесь в качестве ссылки во всей своей полноте) раскрывает ингибиторы 8-аминоксантин ФДЭ V, которые замещены в положение 8 группами -NH2 или -NHR, где R представляет собой алкильную, аралкильную или ненасыщеннную гетероциклическую (например, гетероарильную) группу.
Было обнаружено, что специфические ингибиторы ФДЭ V полезны при специфических показаниях. Например, использование ингибиторов ФДЭ V для лечения импотенции нашло коммерческий успех с введением сильденафилцитрата, более известного как Viagra® (Pfizer, New-York, New-York). Химизм и использование Виагры®, включающее механизм ее действия при лечении нарушения эрекции, указаны в европейской заявке на патент ЕР 0702555 В1 (включена здесь в качестве ссылки во всей своей полноте). Дополнительные ингибиторы ФДЭ V, полезные для лечения нарушения эрекции, раскрыты в международной заявке WO 99/24433 (включена здесь в качестве ссылки во всей своей полноте).
Нарушение эрекции излечимо и в существенной степени касается здоровья, затрагивая более 30 миллионов человек в Соединенных Штатах, включая каждого четвертого в возрасте более 65 лет. Нарушение эрекции имеет место, когда мужчина не способен надежно поддерживать эрекцию, достаточную для проведения совокупления. В прошлом психологические причины были наиболее распространенным объяснением нарушения эрекции либо его рассматривали как естественную составную часть старения. Однако сегодня исследователи утверждают, что более 70 процентов примеров нарушения эрекции обусловлены физическими или медицинскими проблемами. Имеется несколько факторов, которые могут вносить вклад в нарушение эрекции, включая
- недостаточную циркуляция крови - атеросклероз или затвердение артерий, высокое артериальное давление и высокое содержание холестерина,
- неврологические нарушения - рассеянный склероз, болезнь Альцгеймера и болезнь Паркинсона,
- гормональные дисбалансы - диабеты, нарушения работы щитовидной железы и низкие уровни тестостерона,
- травма - повреждение спинного мозга, хирургические операции простаты или другие травмы тазовой области,
- выписываемые и продаваемые без рецепта лекарства - лекарства, влияющие на артериальное давление, антидепрессанты и определенные сочетания препаратов,
- особенности образа жизни - курение, злоупотребление алкоголем и использование запрещенных наркотиков.
Патенты США US 5939419 и 5393755 (включены здесь в качестве ссылки во всей их полноте) раскрывают полициклические производные гуанин ФДЭ V, которые полезны для лечения сердечно-сосудистых и легочных расстройств.
Как было показано специалистами, цитированными выше, определенные ингибиторы ксантин/гуанин ФДЭ V, как было установлено, являются полезными для лечения сердечно-сосудистых и легочных расстройств, в то время как некоторые другие, как было установлено, полезны для лечения импотенции. Также было показано, что определенные ингибиторы ксантин ФДЭ V могут быть замещены в положение 8 разнообразными группами, включая нитрогруппы и незамещенные или замещенные аминогруппы. Замещенные аминогруппы включают насыщенные гетероциклы, где атом азота и его заместители вместе образуют ненасыщенную гетероциклическую группу (например, -NRxRy может образовывать гетероцикл).
Задача этого изобретения состоит в том, чтобы создать полициклический ингибитор ксантин ФДЭ V, который обладает полезными терапевтическими свойствами.
Другая задача изобретения состоит в том, чтобы создать полициклический ингибитор ксантин ФДЭ V, который имеет особенно полезные фармакологические свойства.
Следующая задача изобретения состоит в том, чтобы создать полициклический ингибитор ксантин ФДЭ V, который имеет хорошую метаболическую стабильность.
Еще одна задача изобретения состоит в том, чтобы создать полициклический ингибитор ксантин ФДЭ V, который является эффективным для лечения множества физиологических симптомов и заболеваний, в которых играет роль ФДЭ V.
Задача изобретения состоит также в том, чтобы создать полициклический ингибитор ксантин ФДЭ V, который является особенно эффективным для лечения нарушения эрекции с минимальными побочными эффектами.
Эти и другие задачи изобретения станут очевидными по мере последующего описания.
Определения и использование терминов
Следующие определения и термины используют здесь или они иным образом известны специалистам. За исключением того, где указано иное, следующие определения используются во всем описании и пунктах формулы изобретения. Эти определения используют независимо от того, используется ли термин сам по себе или в сочетании с другими терминами, если не указано иное. Следовательно, определение «алкил» применяют к «алкилу», а также к «алкильной» части «гидроксиалкила», «галогеналкила», «алкоксида» и т.д.
Термин «химически совместимый», как он используется здесь, означает, что заместитель или различие в структуре, процессе или тому подобном выбраны так, чтобы быть способными приводить к стабильному соединению.
Термин «замещенный» или фраза «с... одним или несколькими заместителями», как они используются здесь, означают замещение одного или нескольких атомов или радикалов, обычно атомов водорода, в данной структуре химически совместимым(и) атомом(ами) или радикалом(ами), выбранными из специфической группы. В ситуациях, где более одного атома или радикала могут быть замещены заместителями, выбранными из той же самой специфической группы, заместители могут быть, если не указано иное, либо теми же самыми, либо различными в каждом положении. Радикалы специфических групп, такие как алкильные, циклоалкильные, алкенильные, циклоалкенильные, алкинильные, аралкильные, алкиларильные, гетероциклоалкильные, арильные и гетероарильные группы, независимо или вместе друг с другом, могут быть заместителями для любой замещенной группы, если не известно, не установлено или не показано противоположное.
Представленные заместители для алкильных, циклоалкильных, алкенильных, циклоалкенильных, алкинильных, аралкильных, алкиларильных, арильных, гетероарильных и гетероциклоалкильных групп включают, но не ограничиваются ими, следующие структуры: алкил, циклоалкил, алкенил, циклоалкенил, алкинил, аралкил, алкиларил, арил, гетероарил, гетероциклоалкил, гидроксиалкил, аминоалкил, галогеналкил, тиоалкил, алкилтиоалкил, карбоксиалкил, имидазолилалкил, индолилалкил, моно-, ди- и тригалогеналкил, моно-, ди- и тригалогеналкоксид, амин, алкиламин, диалкиламин, алкоксид, гидроксил, галоген (например, -Cl и -Br), нитрогруппу, оксиминогруппу, группы -COOR50, -COR50, -SO0-2R50, -SO2NR50R51, -NR52SO2R50, =C(R50R51), =N-OR50, =N-CN, =С(галоген)2, =S, =O, -CON(R50R51), -OCOR50, -OCON(R50R51), -N(R52)CO(R50), -N(R52)COOR50 и -N(R52)CON(R50R51), где
R50, R51 и R52 могут быть независимо друг от друга выбраны из следующего: атом водорода и разветвленные или с нормальной цепью алкильная группа с 1-6 атомами углерода, циклоалкильная группа с 3-6 атомами углерода, гетероциклоалкильная группа с 4-6 атомами углерода, гетероарильная и арильная группы с заместителями или без них.
Когда допустимо, R50 и R51 могут быть соединены вместе с образованием карбоциклической или гетероциклической системы. R50, R51 и R52 могут также включать
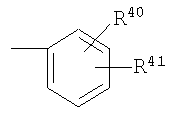 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
, 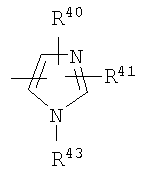 ,
,  ,
,
 ,
, 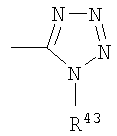 ,
, 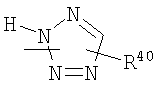 ,
,
где R40 и R41 представляют собой, независимо от друг друга, каждый атом водорода или разветвленные или с нормальной цепью, необязательно, замещенные алкил, циклоалкил, гетероциклоалкил, галоген, арил, имидазолилалкил, индолилалкил, гетероарил, аралкил, арилалкокси, гетероаралкил, гетероарилалкокси, аминоалкил, галогеналкил, моно-, ди- или тригалогеналкил, моно-, ди- или тригалогеналкокси, нитрогруппу, цианогруппу, алкокси, гидрокси, аминогруппу, фосфин, фосфат, алкиламиногруппу, диалкиламиногруппу, формил, алкилтиогруппу, триалкилсилил, алкилсульфонил, арилсульфонил, алкилсульфинил, аминоалкил, алкиламиноалкил, диалкиламиноалкил, гидроксиалкил, морфолил, тиоалкил, алкилтиоалкил, карбоксиалкил, оксиминогруппу, группы -COOR50, -COR50, -SO0-2R50, -SO2NR50R51, -NR52SO2R50, -CON(R50R51), -OCON(R50R51), -N(R52)CO(R50), -N(R52)COOR50, -N(R52)CON(R50R51) или -OCONR50, где R50, R51 и R52 являются такими, как они определены выше;
R42 представляет собой атом водорода или разветвленную или с нормальной цепью, необязательно, замещенную алкильную, алкенильную, аралкильную или ацильную группу,
R43 представляет собой атом водорода или разветвленную или с нормальной цепью, необязательно, замещенную алкильную или арильную группу,
где возможные заместители определены такими же, как они определены выше для одного или нескольких заместителей.
Предпочтительные заместители в арильной и гетероарильной группах включают, но не ограничиваются ими, любую из структур, указанных выше в определении для R40 и R41.
Термин «гетероатом», как он используется здесь, означает атом азота, серы или кислорода. Несколько гетероатомов в той же самой группе могут быть одинаковыми или различными.
Термин «углеводород», как он используется здесь, означает соединение или радикал, состоящий только из атомов углерода и водорода, включая алифатические, ароматические, с нормальной цепью, замещенные или незамещенные углеводороды.
Термин «алкил», как он используется здесь, означает незамещенную или замещенную, нормальную или разветвленную углеводородную цепь (то есть включает атомы углерода и водорода, соединенные вместе), имеющую предпочтительно от одного до двадцати четырех атомов углерода, более предпочтительно от одного до двенадцати атомов углерода и наиболее предпочтительно от одного до восьми атомов углерода.
Термин «циклоалкил» или «циклоалкан», как он используется здесь, означает незамещенный или замещенный, насыщенный, стабильный неароматический углеродный цикл, имеющий, предпочтительно, от трех до пятнадцати атомов углерода, более предпочтительно от трех до восьми атомов углерода. Углеродный циклический радикал является насыщенным и может быть конденсирован, например, через бензольный цикл, с от одного до трех циклоалкильными, ароматическими, гетероциклическими или гетероароматическими кольцами. Циклоалкил может быть присоединен через любой из атомов углерода в цикле, что приводит к стабильной структуре. Предпочтительные карбоциклы имеют от пяти до шести атомов углерода. Примеры карбоциклических радикалов включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и тому подобные.
Термин «алкенил», как он используется здесь, означает незамещенную или замещенную, ненасыщенную, нормальную или разветвленную углеводородную цепь, имеющую, по меньшей мере, наличие одной двойной связи и, предпочтительно, от двух до пятнадцати атомов углерода, более предпочтительно от двух до двенадцати атомов углерода.
Термин «циклоалкенил», как он используется здесь, означает незамещенный или замещенный, ненасыщенный углеродный цикл, имеющий, по меньшей мере, наличие одной двойной связи и, предпочтительно, от трех до пятнадцати атомов углерода, более предпочтительно от пяти до восьми атомов углерода. Циклоалкенильная группа является ненасыщенной карбоциклической группой. Примеры циклоалкенильных групп включают циклопентенил и циклогексенил.
Термин «алкинил», как он используется здесь, означает незамещенную или замещенную, ненасыщенную, нормальную или разветвленную углеводородную цепь, имеющую, по меньшей мере, наличие одной тройной связи и, предпочтительно, от двух до двенадцати атомов углерода, более предпочтительно от двух до десяти атомов углерода.
Термин «бициклоалкил», как он используется здесь, представляет насыщенный, конденсированный линейно или мостичной связью углеродный цикл, имеющий, предпочтительно, от 5 до 12 атомов углерода.
Термин «арил», как он используется здесь, означает замещенную или незамещенную ароматическую, моно- или бициклическую углеродную систему, имеющую от одного до двух ароматических циклов. Арильная структура обычно будет иметь от 6 до 14 атомов углерода со всеми доступными для замещения атомами углерода в арильной структуре, являющимися возможными местами присоединения. Представленные примеры включают фенил, толил, ксилил, куменил, нафтил, тетрагидронафтил, инданил, инденил и тому подобные. Если желательно, карбоциклическая структура может быть замещена от одной до пяти, предпочтительно, от одной до трех структурами, такими как от одного до пяти галогенами, алкилом, трифторметилом, фенилом, гидроксилом, алкоксидом, феноксидом, аминогруппой, моноалкиламиногруппой, диалкиламиногруппой и тому подобными.
Термин «гетероарил», как он используется здесь, означает моно- или бициклическую систему, содержащую одно или два ароматических кольца и, по меньшей мере, один атом азота, кислорода или серы в ароматическом кольце. Гетероарильные группы (включая бициклические гетероарильные группы) могут быть незамещенными или замещенными несколькими заместителями, предпочтительно, от одного до пяти заместителями, более предпочтительно, одним, двумя или тремя заместителями (например, от одного до пяти галогенами, алкилом, трифторметилом, фенилом, гидроксилом, алкоксидом, феноксидом, аминогруппой, моноалкиламиногруппой, диалкиламиногруппой и тому подобным). Как правило, гетероарильная группа представляет собой циклическую группу из пяти или шести атомов или бициклическую группу из девяти или десяти атомов, по меньшей мере, один из которых является углеродом, и имеющую, по меньшей мере, один атом кислорода, серы или азота, прерывающий углеродный цикл, имеющую достаточное число пи (π) электронов, чтобы обеспечивать ароматический характер. Представленные гетероарильные (гетероароматические) группы включают пиридинильную, пиримидинильную, пиразинильную, пиридазинильную, фуранильную, бензофуранильную, тиенильную, бензотиенильную, тиазолильную, тиадиазолильную, имидазолильную, пиразолильную, триазолильную, изотиазолильную, бензотиазолильную, бензоксазолильную, оксазолильную, пирролильную, изоксазолильную, 1,3,5-триазинильную и индолильную группы.
Термин «аралкил», как он используется здесь, означает алкильную структуру, замещенную возможным заместителем - арильной или гетероарильной группой. Представленные аралкильные группы включают бензильную группу и конденсированные бициклические системы, которые содержат одну арильную группу.
Термин «алкиларил», как он используется здесь, означает арильную или гетероарильную структуру, замещенную возможным заместителем - алкильной группой. Представленные алкиларильные группы включают присоединенные в о-, м- и п-положение толильную и ксилильную группы.
Если не известно, не установлено или не показано противоположное, местом присоединения заместителя с многозначным термином (многозначными терминами являются те, которые образуют сочетание для идентификации одной структуры), как полагают для данной структуры, является названный последним термин из многозначного термина. Например, «аралкильный» заместитель присоединяется к основной структуре через «алкильную» часть заместителя. Наоборот, когда заместитель является «алкиларильным», он присоединяется к основной структуре через «арильную» часть заместителя. Точно так же циклоалкилалкильный заместитель присоединяется к объекту через последнюю «алкильную» часть заместителя (например, структура алкил-циклоалкил).
Термин «гетероцикпоалкил», как он используется здесь, означает незамещенную или замещенную насыщенную циклическую систему, имеющую от трех до пятнадцати членов, предпочтительно от трех до восьми членов, и включающую атомы углерода и, по меньшей мере, один гетероатом в качестве части цикла.
Термин «гетероциклическое кольцо» или «гетероцикл», как он используется здесь, означает незамещенный или замещенный, насыщенный, ненасыщенный или ароматический цикл, включающий атомы углерода и один или несколько гетероатомов в кольце. Гетероциклические кольца могут быть моноциклическими или полициклическими. Моноциклические кольца, предпочтительно, содержат от трех до восьми атомов, наиболее предпочтительно от пяти до семи атомов. Системы полициклических колец, состоящие из двух колец, предпочтительно, содержат от шести до шестнадцати атомов, наиболее предпочтительно, от десяти до двенадцати атомов. Системы полициклических колец, состоящие из трех колец, содержат, предпочтительно, от тринадцати до семнадцати атомов, наиболее предпочтительно, от четырнадцати до пятнадцати атомов. Каждое гетероциклическое кольцо имеет, по меньшей мере, один гетероатом. Если не установлено иное, гетероатомы могут быть независимо выбраны из следующих: атомы азота, серы и кислорода.
Термин «карбоциклическое кольцо» или «карбоцикл», как он используется здесь, означает незамещенное или замещенное, насыщенное, ненасыщенное или ароматическое (например, арильное), углеводородное кольцо, если специально не обозначено иное. Карбоциклы могут быть моноциклическими или полициклическими. Моноциклические кольца, предпочтительно, содержат от трех до восьми атомов, наиболее предпочтительно от пяти до семи атомов. Полициклические кольца, имеющие два кольца, предпочтительно, содержат от шести до шестнадцати атомов, наиболее предпочтительно от десяти до двенадцати атомов, а таковые, имеющие три кольца, предпочтительно, содержат от тринадцати до семнадцати атомов, наиболее предпочтительно от четырнадцати до пятнадцати атомов.
Термин «алкокси», как он используется здесь, означает атом кислорода, присоединенный к углеводородной цепи, такой как алкильная или алкенильная группа (например, -O-алкил или -O-алкенил). Представленные алкоксигруппы включают метокси-, этокси- и изо-пропоксигруппы.
Термин «гидроксиалкил», как он используется здесь, означает замещенную углеводородную цепь, предпочтительно алкильную группу, имеющую, по меньшей мере, один гидроксильный заместитель (то есть -ОН). Дополнительные заместители в алкильной группе также могут присутствовать. Представленные гидроксиалкильные группы включают гидроксиметильную, гидроксиэтильную и гидроксипропильную группы.
Термин «карбоксиалкил», как он используется здесь, означает замещенную углеводородную цепь, предпочтительно замещенную алкильную группу, которая имеет карбоксильный заместитель (например, -СООН) и может также иметь дополнительные заместители (такие как один из представленных заместителей, идентифицированных выше для термина «замещенный»). Представленные карбоксиалкильные группы включают карбоксиметильную (-СН2СО2Н) и карбоксиэтильную (-СН2СН2CO2Н) группы и их производные, такие как соответствующие сложные эфиры.
Термин «аминоалкил», как он используется здесь, означает алкильную группу, замещенную аминной структурой (например, -алкил-NH2), такую как аминометил.
Термин «алкиламиногруппа», как он используется здесь, означает структуру амина, имеющую один или два алкильных заместителя (например, -NH-алкил), такую как диметиламиногруппа.
Термин «алкениламиногруппа», как он используется здесь, означает структуру амина, имеющую один или два алкенильных заместителя, где атом азота аминогруппы не присоединен к образующему алкен атому углерода (например, -NH-СН2-алкенил), такую как дибутениламиногруппа.
Термин «ариламиногруппа», как он используется здесь, означает структуру амина, замещенную арильной группой (то есть -NH-арил).
Термин «алкилиминогруппа», как он используется здесь, означает структуру имина, имеющую один алкенильный или два алкильных заместителя (например, -С=N-алкил).
Термин «оксиминогруппа», как он используется здесь, означает соединения, содержащие радикал -C=N-OR69, где R69 представляет собой атом водорода или алкильную или арильную группу.
Термин «ароил», как он используется здесь, означает радикал R-CO-, где R представляет собой ароматическую группу. Представленными ароилами являются бензоил и нафтоил.
Термин «арилокси», как он используется здесь, означает атом кислорода, имеющий арильный заместитель (например, -O-арил).
Термин «сложный эфир», как он используется здесь, означает соединения, содержащие замещенную карбоновую кислоту (например, -СОО-арил).
Термины «ацил» или «карбонил», как они используются здесь, означают углерод с двойной связью с кислородом, (например, R-C(=O)-), который может быть радикалом карбоновой кислоты, имеющим формулу алкил-СО-, арил-СО-, аралкил-СО-, циклоалкил-СО-, алкилциклоалкил-СО- или гетероарил-СО-. Представленные ацильные группы включают ацетильную, пропионильную, бутаноильную и бензоильную группы.
Термин «ацилокси», как он используется здесь, означает атом кислорода, имеющий ацильный заместитель (например, -O-ацил), например -O-С(=O)-алкил.
Термин «ациламиногруппа», как он используется здесь, означает структуру амина, имеющую ацильный заместитель (например, -NH-ацил), например амид с формулой -NH-(С=O)-алкил, мочевина с формулой -NH-(С=O)-NH-алкил или карбамат с формулой -NH-(C=O)-OR, где R представляет собой алкильную, циклоалкильную, алкенильную, циклоалкенильную, алкинильную, аралкильную или гетероциклоалкильную группу.
Термин «гало-», «галоген» или «галогенид», как они используются здесь, означают радикал атома хлора, брома, фтора или йода. Хлориды, бромиды и фториды являются предпочтительными галогенидами.
Термин «низший углеводород» (например, «низший алкил»), как он используется здесь, означает углеводородную цепь, включающую от, если не установлено иное, одного до восьми атомов углерода, предпочтительно от одного до шести атомов углерода и наиболее предпочтительно от одного до четырех атомов углерода.
Термин «полигало-», как он используется здесь, представляет замещение, по меньшей мере, двумя атомами галогена в группе, модифицированной термином «полигало-».
Термин «аминосульфонил», как он используется здесь, представляет группу, имеющую формулу: -SO2NR79R89, где R79 и R89 представляют собой, независимо друг от друга, каждый атом водорода или низшую алкильную (например, от 1 до 6 атомов углерода) или арильную группу.
Термин «сульфонил», как он используется здесь, представляет группу, имеющую формулу -S(O2)-.
Когда переменная появляется более одного раза в структурной формуле, например, R59 для случая, где Х представляет собой -C(OR59)2-, идентификация каждой переменной, появляющейся более одного раза, может быть независимо выбрана из определения для этой переменной.
Термин «пролекарство», как он используется, здесь, представляет соединение, которое является предшественником лекарства, которое при последующем назначении пациенту освобождает лекарство in vivo путем некоторого химического и/или физиологического процесса (например, при доведении пролекарства до физиологического рН и/или через действие фермента оно превращается в желаемую лекарственную форму).
Термин «соединение формулы (I) или (II)», как он используется здесь, представляет соединение, имеющее химическую структуру, охватываемую формулами (I) или (II), и включает любые и все энантиомеры, стереоизомеры, ротомеры, таутомеры и пролекарства соединения. Соединения формулы (I) или (II) также включают их соответствующие фармацевтически приемлемые соли, сольваты, сложные эфиры и производные.
Термин «фармацевтически приемлемые инертные наполнители», как он используется здесь, включает любой физиологически инертный, фармакологически неактивный материал, известный специалистам, который является совместимым с физическими и химическими характеристиками специфического активного ингредиента, выбираемого для использования. Фармацевтически приемлемые инертные наполнители включают полимеры, смолы, пластификаторы, наполнители, связующие вещества, смазочные материалы, агенты, придающие скользкость, агенты, вызывающие дезинтеграцию, растворители, сорастворители, буферные системы, поверхностно-активные вещества, консервирующие агенты, подсластители, ароматизирующие агенты, фармацевтические красители или пигменты и агенты, влияющие на вязкость.
Термин «фармацевтическая композиция», как он используется здесь, означает сочетание, по меньшей мере, одного соединения в соответствии с изобретением (например, ингибитор ФДЭ V) и, по меньшей мере, одного фармацевтически приемлемого инертного наполнителя.
Термины «соединение [имеющее формулу (I)] или его фармацевтическая композиция» включают нейтральные, кислотные и щелочные формы соединения или композиции, а также его сольваты, сложные эфиры и соли (как определено ниже), а также включают производные соединений в соответствии с изобретением.
Термин «фармацевтически приемлемая соль», как он используется здесь, означает катионную соль, сформированную при кислотной (например, карбоксильной) группе, или анионную соль, сформированную при основной (например, аминной) группе соединения. Много таких солей известно специалистам, например те, которые описаны в международной заявке WO 87/05297 (1987), которая тем самым включена здесь при ссылке во всей своей полноте. Предпочтительные катионные соли включают соли щелочных металлов (например, натрия и калия) и соли щелочноземельных металлов (например, магния и кальция). Предпочтительные анионные соли включают галогениды (например, хлориды), ацетаты и соли фосфорных кислот.
Фраза «эффективное количество», как она используется здесь, означает количество соединения или композиции, которое является достаточным, чтобы существенно и положительно изменять симптомы и/или состояния при лечении (например, обеспечивает положительную клиническую реакцию). Фраза «безопасное и эффективное количество», как она используется здесь, означает, что «эффективное количество» должно также быть безопасным, то есть количество, которое является достаточным, чтобы вызвать положительную реакцию, при этом оно достаточно мало, чтобы избежать серьезных побочных эффектов (при приемлемом отношении благоприятное действие/риск), в пределах области обоснованной медицинской оценки. Эффективное количество активного ингредиента для использования в фармацевтической композиции будет меняться в зависимости от специфического состояния, подлежащего лечения, серьезности состояния, продолжительности лечения, природы сопутствующей терапии, причем применяют специфический активный ингредиент, используют специфические фармацевтически приемлемые инертные наполнители и тому подобные факторы в пределах знания и экспертизы лечащего врача.
Фраза «назначение [пациенту безопасного и эффективного количества соединения в соответствии с изобретением]», как она используется здесь, относится к любому способу введения любой формы (например, твердого тела, жидкости или газа) соединений в соответствии с изобретением in vivo пациенту (например, человеку или млекопитающему). Например, введение соединения в соответствии с изобретением пациенту может быть выполнено путем перорального приема (например, таблетки, капсулы, гели, растворы и т.д.), путем адсорбции, всасывания (например, назначение через слизистую оболочку под языком или во рту), применениями через кожу (например, местные применения через пластырь, лосьоны и т.д.), суппозитории и т.д.
Термин «пероральная форма дозирования», как он используется здесь, означает любую фармацевтическую композицию, предназначенную для систематического назначения индивиду доставкой композиции в желудочно-кишечный тракт индивида через рот индивида. Для целей изобретения доставляемая форма может быть таблеткой (покрытой или не покрытой), раствором, суспензией или капсулой (покрытой или не покрытой).
Термин «инъекция», как он используется здесь, означает любую фармацевтическую композицию, предназначенную для систематического назначения человеку или другому млекопитающему через введение раствора или эмульсии, содержащих активный ингредиент, прокалыванием кожи указанного индивида, чтобы ввести раствор или эмульсию в систему кровообращения индивида инъекцией либо внутривенно, либо внутримышечно, либо в брюшную полость, либо подкожно.
В отличие от того, что показано в примерах или указано где-либо иначе, все числа, использованные в указаниях и пунктах формулы изобретения, выражающие количества ингредиентов, условия реакции и так далее, понимают как модифицированные во всех примерах термином «около».
Изобретение включает соединение, имеющее формулу (I)
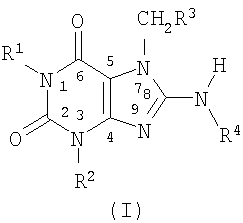
где (a) R1 и R2, независимо от друг друга, каждый представляет собой алкильную группу с 1-15 атомами углерода, разветвленную или с нормальной цепью, с одним или несколькими заместителями, либо без них, такими как гидроксильная или алкоксильная замещающие группы, алкенильную группу с 2-15 атомами углерода, разветвленную или с нормальной цепью, с одним или несколькими заместителями, либо без них, алкинильную группу с 2-15 атомами углерода, разветвленную или с нормальной цепью, с одним или несколькими заместителями, либо без них, циклоалкильную группу с 3-15 атомами углерода с одним или несколькими заместителями, либо без них, аралкильную группу с одним или несколькими заместителями, либо без них, арильную группу с одним или несколькими заместителями, либо без них, гетероарильную группу с одним или несколькими заместителями, либо без них, группу -OR5, -COOR5, -C(O)R5 или -С(О)N(R5)2, где R5 представляет собой атом водорода или углеводородный радикал с одним или несколькими заместителями, либо без них, предпочтительно, R5 представляет собой атом водорода или алкильную группу, разветвленную или с нормальной цепью, с одним или несколькими заместителями, либо без них, или
один из R1 и R2 представляет собой атом водорода, а другой из R1 и R2 определяют, как указано выше;
(б) R3 представляет собой арильную группу с одним или несколькими заместителями, либо без них, такими как гидроксильная или алкоксильная замещающие группы, гетероарильную группу с одним или несколькими заместителями, либо без них, или гетероциклическую группу, имеющую от 1 до 3 гетероатомов, конденсированную с 5- или 6-членным арильным циклом с одним или несколькими заместителями, либо без них, при условии, что R3 не является арильной группой, замещенной в пара-положение группой -Y-арил, где Y представляет собой одинарную углерод-углеродную связь, -СО-, -O-, -S-, -N(R21)-, -CON(R22)-, -N(R22)CO-, -ОСН2-, -CH2O-, -SCH2-, -CH2S-, -NHC(R23)(R24)-, -NR23SO2-, -SO2NR23-, -C(R23)(R24)NH-, -CH=CH-, -CF=CF-, -CH=CF-, -CF=CH-, -CH2CH2-, -CF2CF2-,
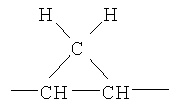 ,
,  ,
,  ,
,
 ,
, 
где R21 представляет собой атом водорода или -CO(алкил C1-4), алкильную группу с 1-6 атомами углерода, аллильную группу, циклоалкильную группу с 3-6 атиомами углерода, фенильную или бензильную группу;
R22 представляет собой атом водорода или алкильную группу с 1-6 атомами углерода;
R23 представляет собой атом водорода или алкильную группу с 1-5 атомами углерода, арильную группу или -СН2-арильную группу;
R24 представляет собой атом водорода или алкильную группу с 1-4 атомами углерода;
R25 представляет собой атом водорода или алкильную группу с 1-8 атомами углерода, перфторалкильную группу с 1-8 атомами углерода, циклоалкильную группу с 3-6 атомами углерода, фенильную или бензильную группу;
R26 представляет собой атом водорода или алкильную группу с 1-6 атомами углерода, циклоалкильную группу с 3-6 атомами углерода, фенильную или бензильную группу;
R27 представляет собой -NR23R24, -OR24, -NHCONH2, -NHCSNH2,
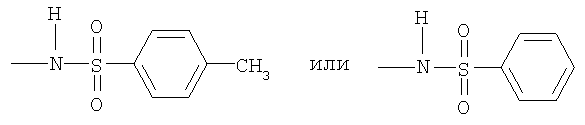
R28 и R29, независимо друг от друга, каждая представляет собой алкильную группу с 1-4 атомами углерода или вместе группу -(CH2)q-, где q составляет 2 или 3;
где группы с R21 по R29 имеют один или несколько заместителей, либо не имеют их, и
(в) R4 представляет собой циклоалкильную группу с 3-15 атомами углерода с заместителями или без них, такими как гидроксильная замещающая группа, циклоалкенильную группу с 3-15 атомами углерода с одним или несколькими заместителями, либо без них, или гетероциклоалкильную группу с от 3 до 15 членами с одним или несколькими заместителями, либо без них;
где, необязательно, один или несколько заместителей для всех групп являются химически совместимыми и, независимо друг от друга, каждый определяется так же, как перечислено выше в разделе определений.
Изобретение включает, по меньшей мере, одно соединение формулы (I), которое включает любые и все энантиомеры, стереоизомеры, ротомеры, таутомеры и пролекарства, по меньшей мере, одного соединения в соответствии с изобретением. Соединения формулы (I) также включают их соответствующие соли, сольваты (например, гидраты), сложные эфиры и тому подобное. Изобретение также включает фармацевтически приемлемые композиции, полученные из соединения в соответствии с изобретением или смеси соединений в соответствии с изобретением, или его соли, сольвата или сложного эфира. Соединения формулы (I) могут быть полезны для лечения разнообразных заболеваний, симптомов и физиологических расстройств, таких как сексуальные нарушения, особенно импотенция (например, нарушение эрекции).
Дальнейшее понимание изобретения будет происходить из следующего описания предпочтительных вариантов его осуществления.
Соединения в соответствии с изобретением, имеющие формулу (I), замещены в положение 8 их химической структурой аминогруппой, которая сама замещена одной из следующих групп: ненасыщенная или насыщенная карбоциклическая группа и насыщенная гетероциклическая группа. Замещенные ксантины в соответствии с изобретением показали неожиданно улучшенные свойства в отношении активности фермента и избирательности фермента. Полагают, что замещение в положение 8 данных соединений ингибитора ФДЭ V этими специфическими группами помогает получать ксантины с неожиданно высоким потенциалом и избирательностью, которые показывают повышенную избирательность в отношении изоэнзима по сравнению с обычными ксантинами. Фармацевтические композиции, включающие соединения в соответствии с изобретением, обладают неожиданно высокими терапевтическими свойствами.
В отношении вышеуказанных соединений ингибитора ксантин ФДЭ V в соответствии с изобретением, имеющих формулу (I), положение 8 в химической структуре замещено группой -NHR4, где R4 представляет собой карбоциклическую или гетероциклическую систему, определяемую следующим образом: циклоалкильная группа с 3-15 атомами углерода, циклоалкенильная группа с 3-15 атомами углерода или гетероциклоалкильная группа с от 3 до 15 членами. Все циклические системы, необязательно, являются замещенными. Предпочтительные заместители в циклических системах включают циклоалкильную группу с 3-6 атомами углерода, алкокси-С1-6-алкильную C1-6 группу, алкильную группу с 1-6 атомами углерода, аминоалкильную C1-6 группу, диалкил-С1-6-аминоалкильную C1-6 группу, дициклоалкил-С3-6-аминоалкильную C1-6 группу, гидроксильную группу, алкоксильную группу, оксиминогруппу, группу -COR6, -SO2R6, -COOR6, -CONR6R7, -SO2NR6R7, -N(R8)SO2R6 и -NR6R7, где
R6 представляет собой атом водорода или, необязательно, замещенные алкильную группу с 1-6 атомами углерода, циклоалкильную группу с 3-6 атомами углерода, гетероциклоалкильную С3-6, арильную или гетероарильную группы;
R7 представляет собой атом водорода или, необязательно, замещенные алкильную группу с 1-6 атомами углерода, циклоалкильную группу с 3-6 атомами углерода, гетероциклоалкильную группу с 3-6 атомами углерода, арильную или гетероарильную группы, или
R6 и R7, когда допустимо, могут быть соединены вместе, образуя систему гетероциклического кольца, и
R8 представляет собой атом водорода или, необязательно, замещенные алкильную группу с 1-6 атомами углерода, циклоалкильную группу с 3-8 атомами углерода, гетероциклоалкильную группу с 3-8 атомами углерода, арильную или гетероарильную группы.
Кроме того, R4 может также быть замещенной -ZR70Z'-, где R70 вместе с Z и Z' образуют спироконденсированный от 5- до 7-членный цикл или линейно конденсированную от 4- до 7-членную циклическую систему, а Z и Z', независимо друг от друга, каждый представляет собой атом кислорода, серы или азота. Например, когда Z=Z'=О, R4 может быть замещена следующей структурой, имеющей формулу (VIII)
 .
.
Предпочтительными заместителями являются определенные выше группы. Другие заместители также могут быть использованы, такие как кетонные, оксимные, циклические системы, включающие линейно конденсированные и мостичные, моно-, би- и трициклические кольца, спироциклические системы, включая кетали и тиокетали, непосредственно присоединенные к R4, галогены и сульфонамиды. Квалифицированный специалист может определять другие возможные заместители в зависимости от используемых условий и желательных свойств.
Предпочтительная структура в соответствии с изобретением представлена формулой (II)

где R1, R2 и R3 определены такими же, как выше для соединения формулы (I);
R9 представляет собой один из следующих атомов или групп:
(а) атом водорода;
(б) оксиминогруппа;
(в) карбоксиалкильная группа;
(г) алкокси-С1-6-алкильная С1-6 группа;
(д) арилоксиалкильная C1-6 группа;
(е) циклоалкокси-С3-6-алкильная C1-6 группа;
(ж) гетероарилоксиалкильная С1-6 группа;
(з) группа -СООН;
(и) сложноэфирная группа;
(к) алкильная группа с 1-6 атомами углерода;
(л) циклоалкильная группа с 3-6 атомами углерода;
(м) гетероциклическая группа с 3-6 атомами углерода;
(н) гидроксиалкильная C1-6 группа с 1-6 атомами углерода;
(о) арильная группа или
(п) гетероарильная группа,
где все из вышеуказанных групп, необязательно, замещены;
R10 и R11 представляют собой заместители у того же или других атомов углерода цикла и, независимо друг от друга, каждый определен так же, как указано выше для R9, и, кроме того, каждый может быть одним из следующих групп:
(а) гидроксильная группа;
(б) сложноэфирная группа, полученная из гидроксильной группы с
(1) карбоновой C1-6 кислотой;
(2) циклоалкил-С3-6-карбоновой C1-6 кислотой;
(3) арилкарбоновой C1-6 кислотой или
(4) гетероарилкарбоновой C1-6 кислотой;
(в) алкоксигруппа с 1-6 атомами углерода;
(г) аминогруппа;
(д) моно- или диалкил-С1-6-аминогруппа;
(е) алкил-С1-6-ациламиногруппа;
(ж) алкил-С1-6-сульфониламиногруппа или
(з) группа -NHCON(R14)2, где R14 представляет собой атом водорода или, необязательно, замещенную алкильную или арильную группу, или
R10 и R11, вместе друг с другом, и, необязательно, с одним или несколькими атомами углерода и/или гетероатомами кольца образуют, необязательно, замещенную, спироконденсированную, линейно конденсированную, би- или трициклическую систему кольца с от 8 до 12 членами, включая от 0 до 4 гетероатомов, где все выше указанные группы R10, R11 и R14, необязательно, замещены;
m и n, независимо от друг друга, каждая составляет от 1 до 3 и
Х представляет собой химически совместимую группу, которая является группой -C(R10R11)-, -S(O)y, -O-, -N(R60)-, где
R10 и R11 определены, независимо друг от друга, так же, как ранее;
у составляет от 0 до 2;
R60 представляет собой атом водорода или алкильную группу с 1-8 атомами углерода, алкинильную группу с 2-8 атомами углерода, алкенильную группу с 2-8 атомами углерода, циклоалкильную группу с 3-8 атомами углерода, арильную группу, гетероарильную группу, гетероциклоалкильную группу с 4-8 атомами углерода, группу -COR61, -SO2R61, -COOR61, -CONR61R62 или -SO2NR61R62 с заместителями или без них, где
R61 представляет собой атом водорода или алкильную группу с 1-8 атомами углерода, алкинильную группу с 2-8 атомами углерода, алкенильную группу с 2-8 атомами углерода, циклоалкильную группу с 3-8 атомами углерода, арильную группу, гетероарильную группу или гетероциклоалкильную группу с 4-8 атомами углерода с заместителями или без них;
R62 представляет собой атом водорода или алкильную группу с 1-8 атомами углерода, алкинильную группу с 2-8 атомами углерода, алкенильную группу с 2-8 атомами углерода, циклоалкильную группу с 3-8 атомами углерода, арильную группу, гетероарильную группу или гетероциклоалкильную группу с 4-8 атомами углерода с заместителями или без них, и
когда R61 и R62 представляют собой (одинаковые или различные) алкильные группы, они могут, если желательно, быть соединены вместе с образованием системы карбоциклического или гетероциклического кольца,
где эти возможные заместители и один или несколько заместителей определяются так же, как для одного или нескольких заместителей формулы I выше.
В соединении формулы (II) различные атомы углерода, к которым могут быть присоединены R10 и R11, могут быть смежными или не смежными. Предпочтительно, R9, R10 и R11 все представляют собой атомы водорода. В другом варианте осуществления изобретения одна из R10 или R11, преимущественно, представляет собой гидроксигруппу.
В соединениях формул (I) и (II) R1, предпочтительно, представляет собой алкильную группу или аралкильную группу, особенно бензильную группу. Более предпочтительно, R1 является низшей алкильной группой с от 1 до 4 атомами углерода и наиболее предпочтительно метильной или этильной группой.
R2 представляет собой в соединениях формул (I) и (II), предпочтительно, алкильную группу, особенно алкильную группу, замещенную гидроксильной группой. Более предпочтительно, R2 является низшей алкильной группой с от 1 до 3 атомами углерода или гидроксиалкильной группой и наиболее предпочтительно R2 является метильной, этильной, изобутильной или гидроксиэтильной группой.
В соединениях формул (I) и (II) R3, предпочтительно, представляет собой арильную группу, особенно арильную группу, замещенную гидроксильной, алкоксильной или аминосульфонильной группой, которая может быть, преимущественно, замещена 1 или 2 атомами галогена. Когда R3 представляет собой гетероарильную группу в соединениях формул (I) и (II), обычно предпочтительно использовать гетероарильные группы, отличные от фурановой.
Наиболее предпочтительно, R3 является метоксиарильной группой, замещенной в ее арильном цикле, по меньшей мере, одним атомом галогена, например замещенной 1 или 2 атомами галогена, такими как хлор или бром. Например, R3 может быть 4-гидроксифенильной, 3-хлор-4-гидроксифенильной, 3-бром-4-гидроксифенильной, 4-метоксифенильной, 3-хлор-4-метоксифенильной, 3-бром-4-метоксифенильной, 4-аминосульфонилфенильной, 3-хлор-4-аминосульфонилфенильной или 3-бром-4-аминосульфонилфенильной группой.
R4 представляет собой в соединении формулы (I), предпочтительно, циклоалкильную или гетероциклоалкильную группу, особенно циклоалкильную группу, замещенную гидроксильной группой. Более предпочтительно, R4 является циклогексильной, гидроксициклопентильной или тетрагидропиранильной группой. Наиболее предпочтительно, R4 является гидроксициклопентильной группой. Например, R4 может быть 2(R)-гидрокси-1(R)-циклопентильной группой. Все из предпочтительных вариантов осуществления могут быть незамещенными или замещенными.
Соединения формул (I) и (II) полезны для лечения мочеполовых заболеваний, таких как мужские (например, импотенция/нарушение эрекции) и женские сексуальные нарушения. Следующие соединения, перечисленные в Таблицах 1 и 2, иллюстрируют изобретение.
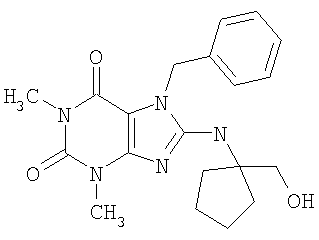
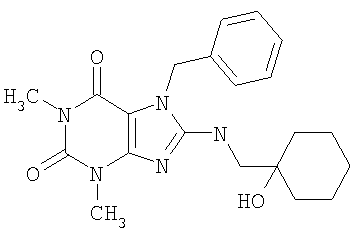
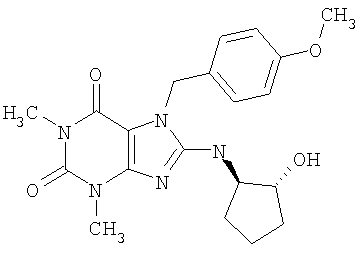



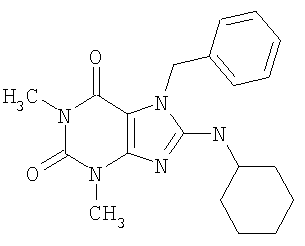



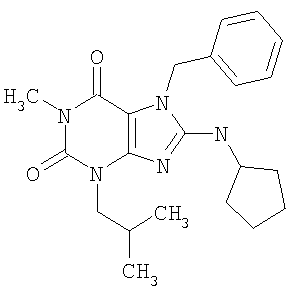

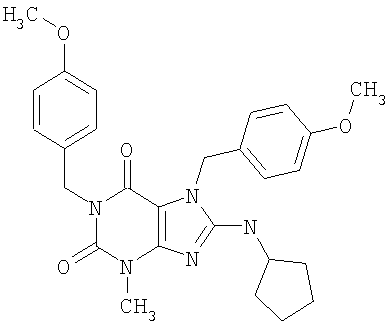

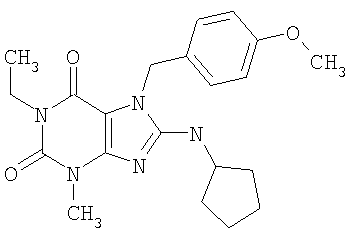
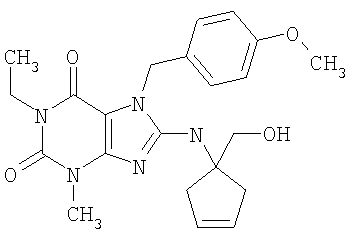



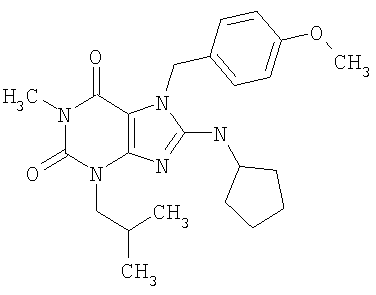

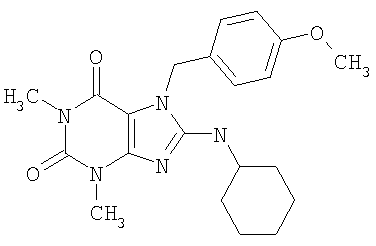

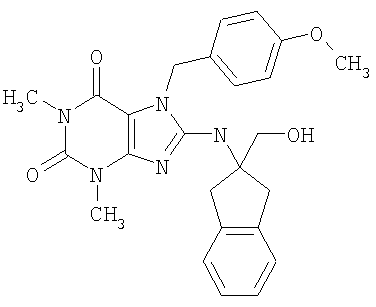


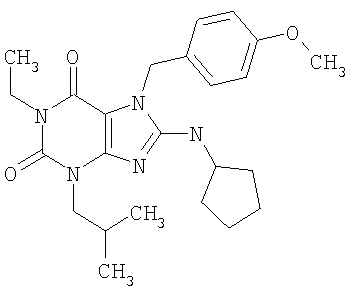


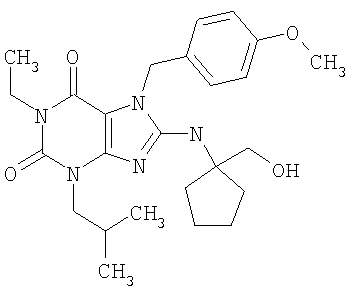

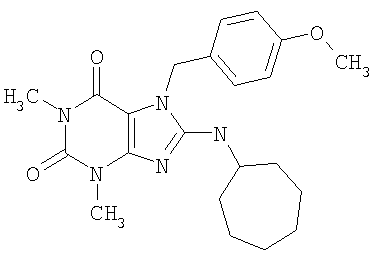


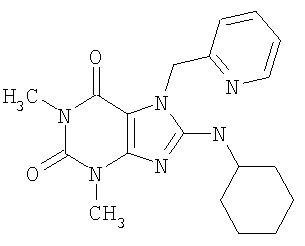

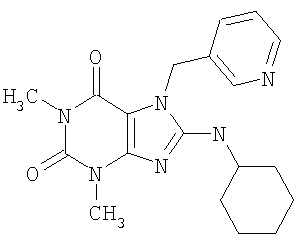
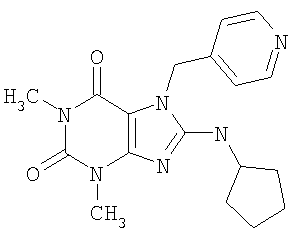

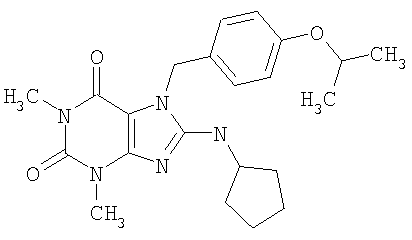





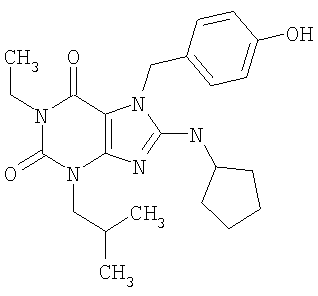
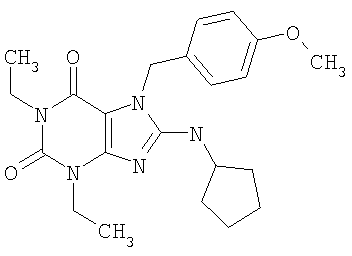




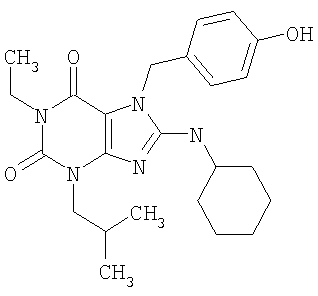

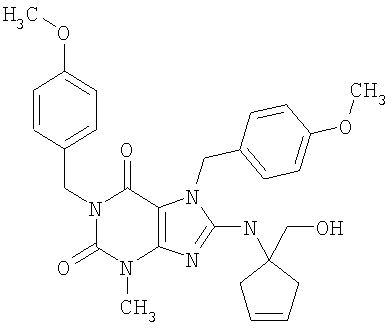
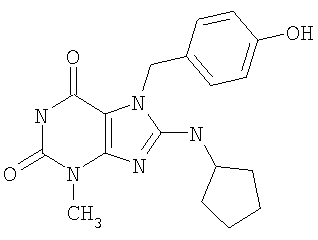
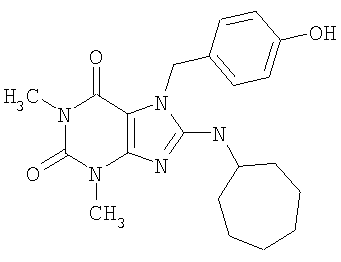
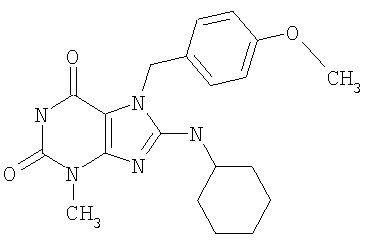
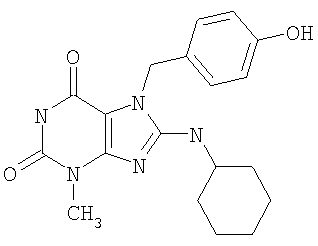
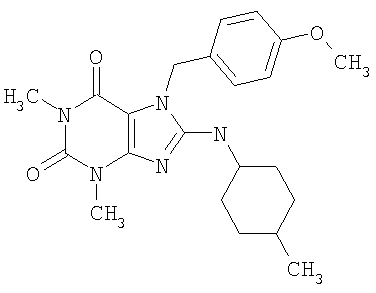




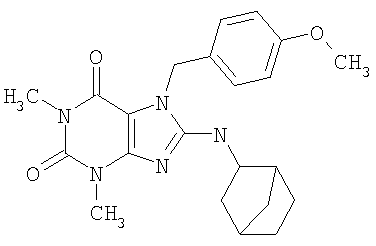

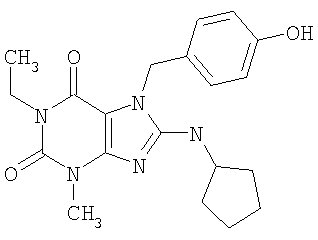
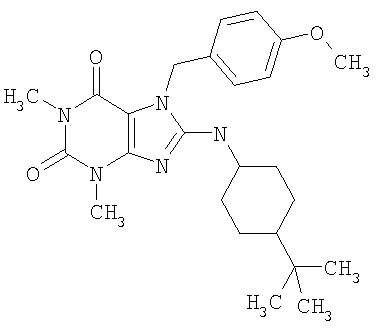

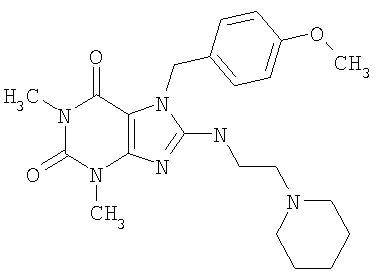
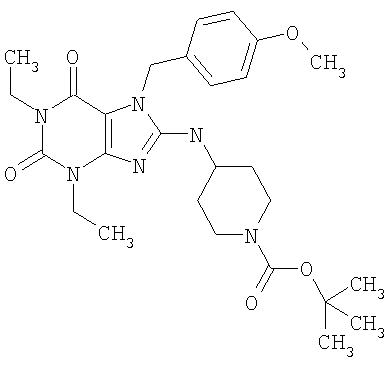
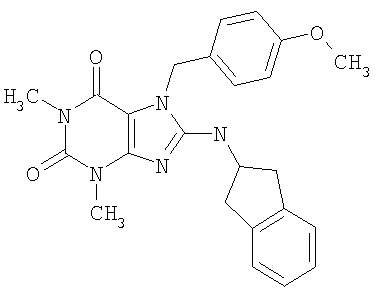
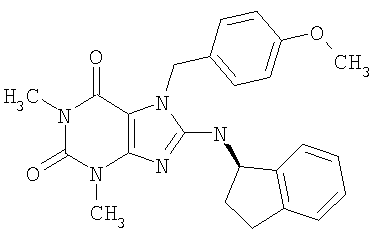


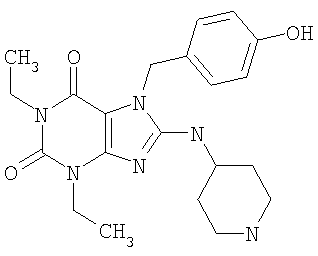




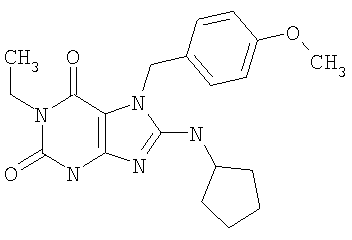
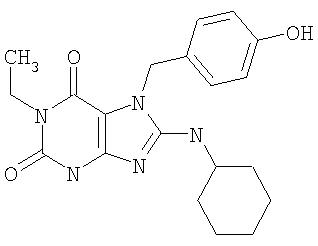



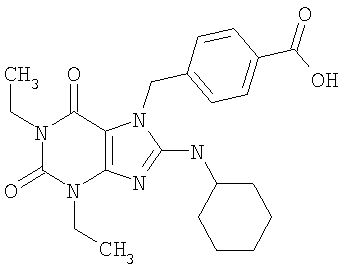

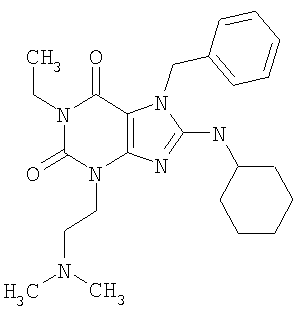

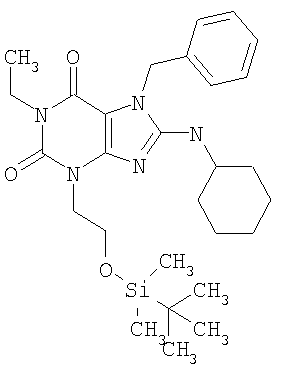
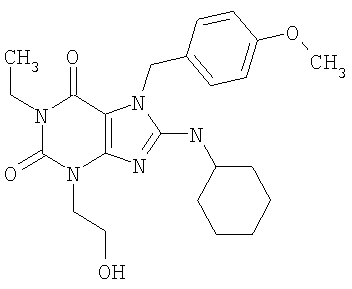

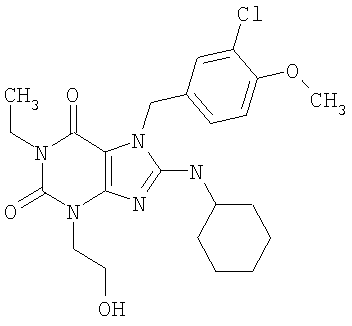
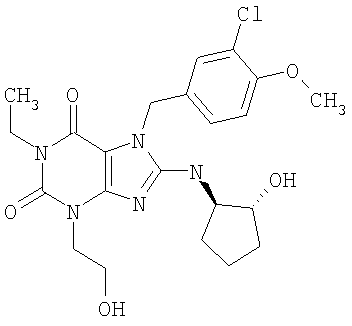
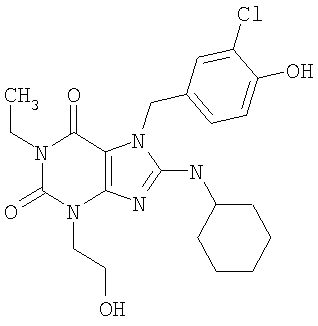



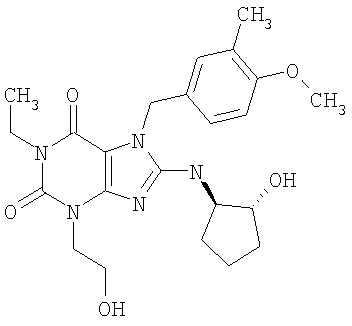
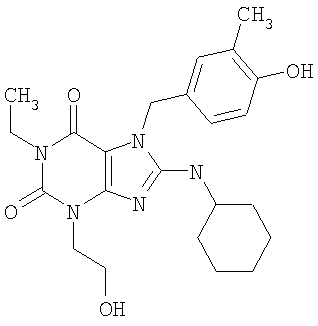


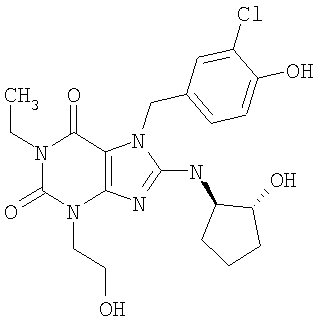
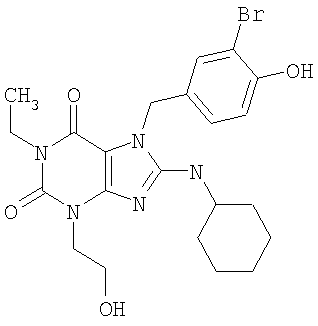


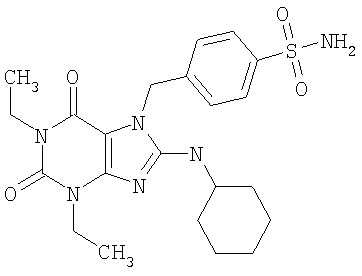

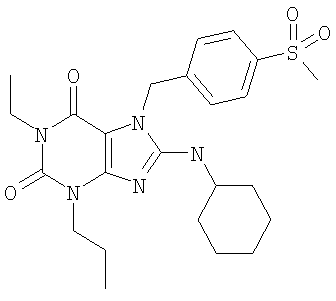


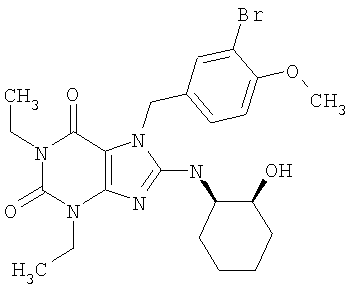
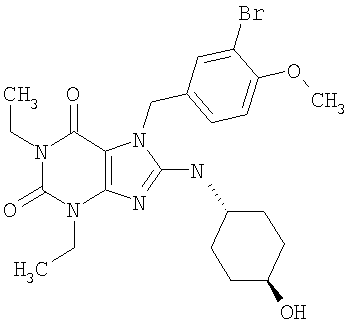


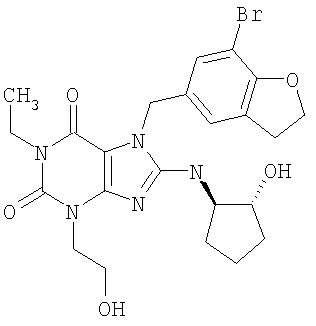
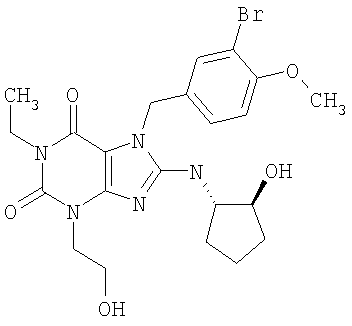
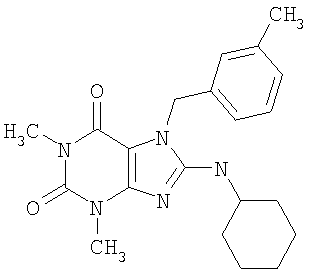
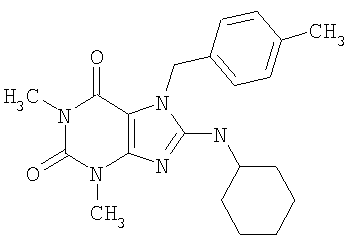

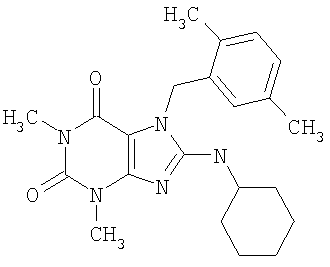
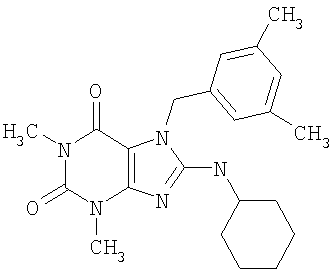

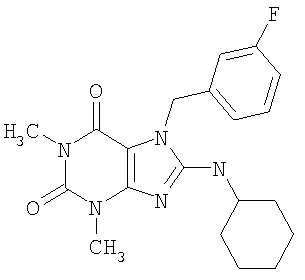
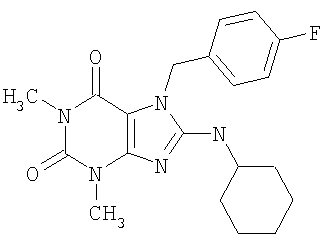
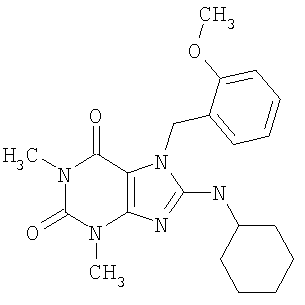

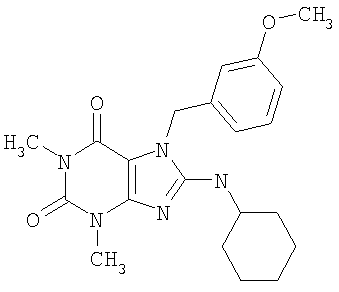

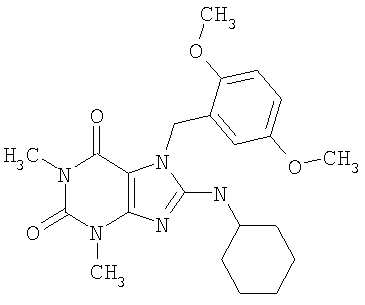


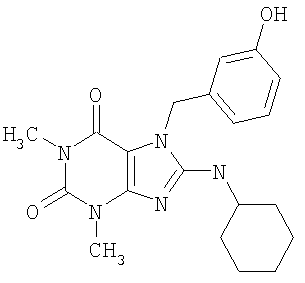




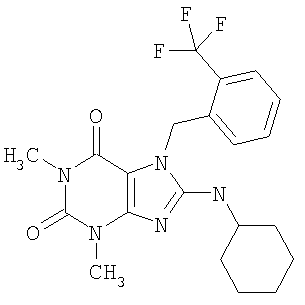

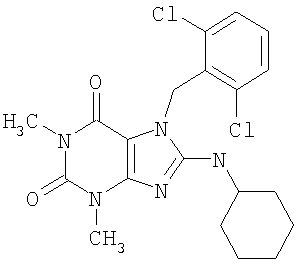
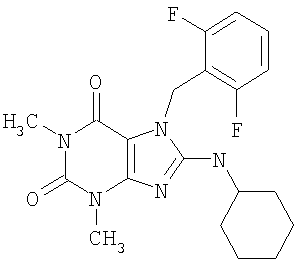

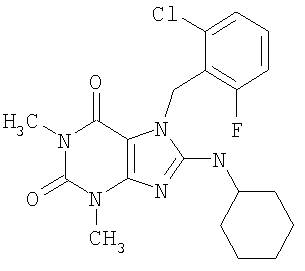


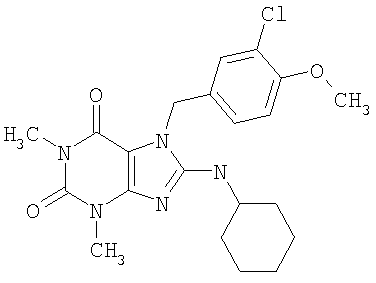



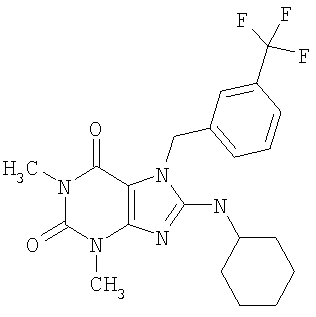
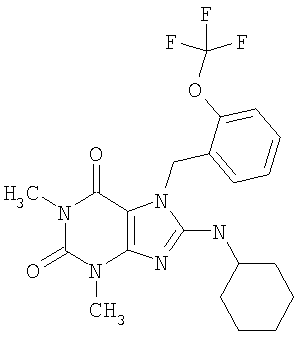

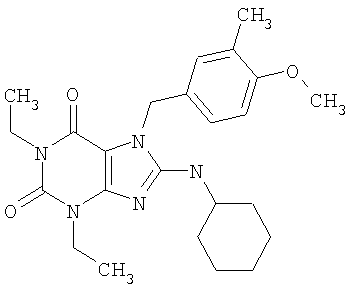




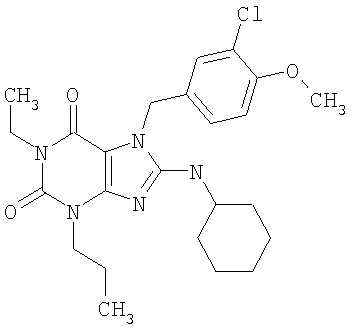


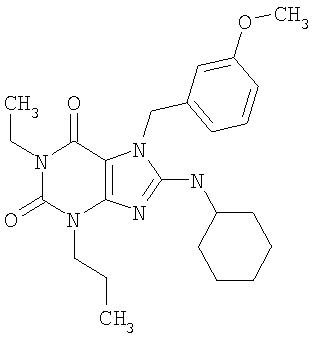
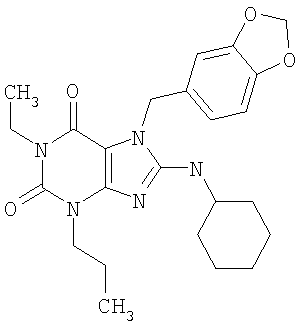

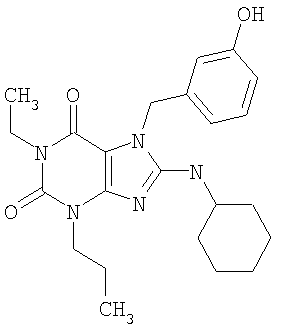



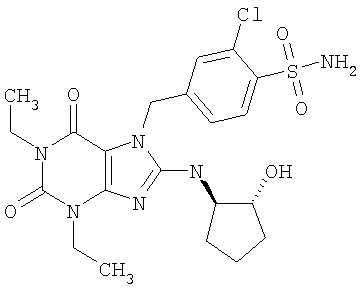
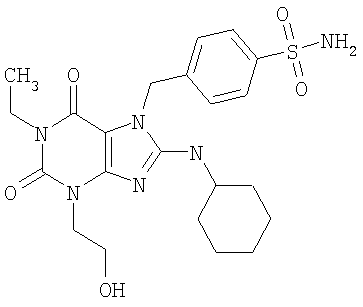



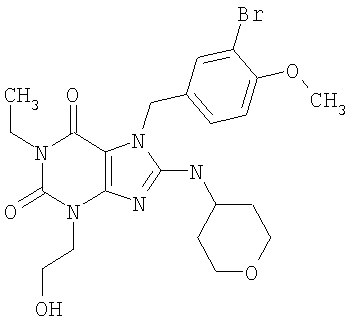





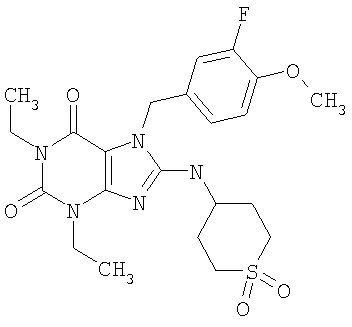
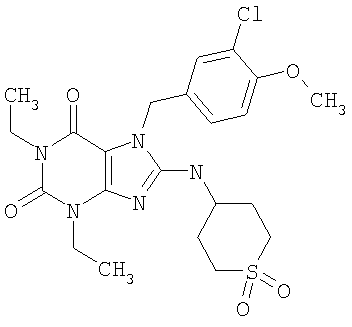
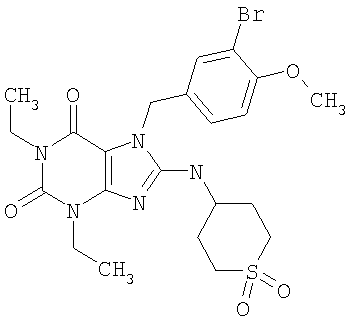
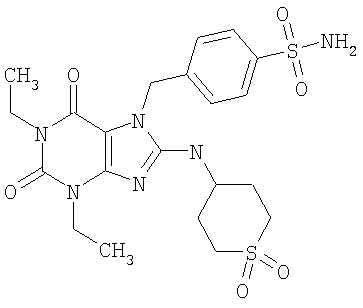

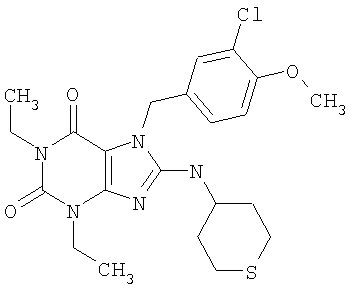
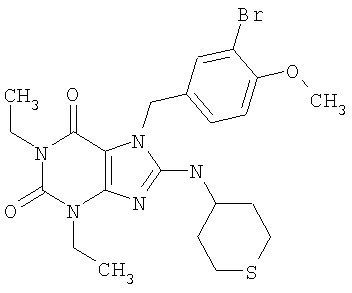

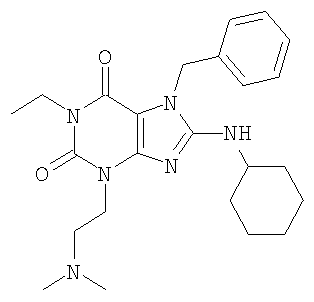
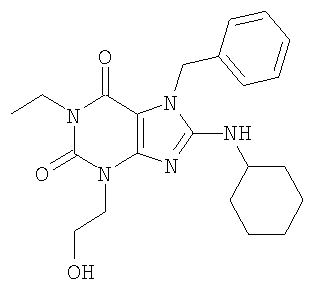
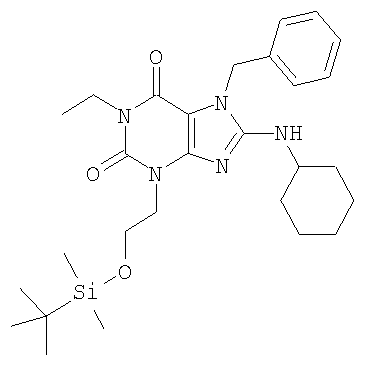

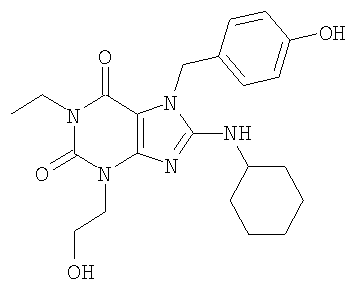
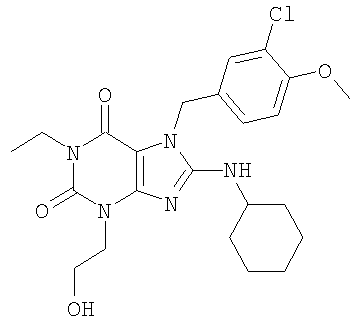
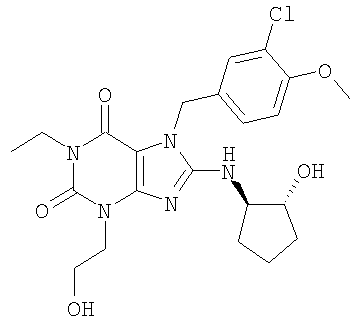
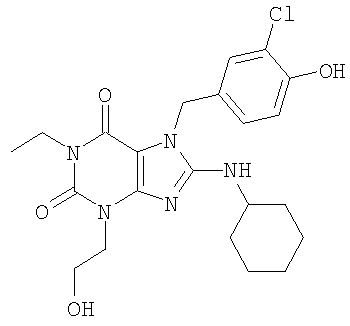
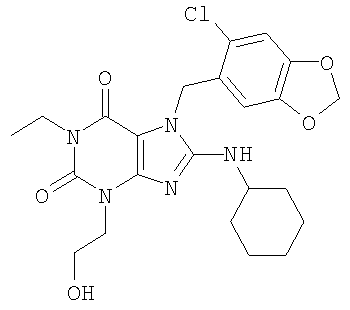
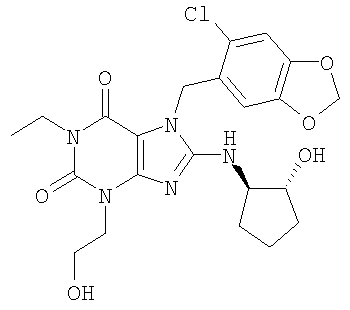



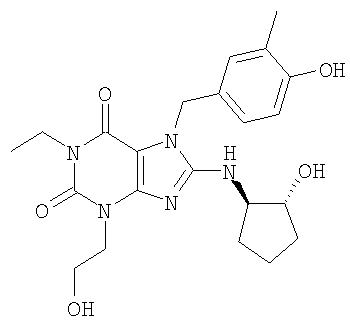




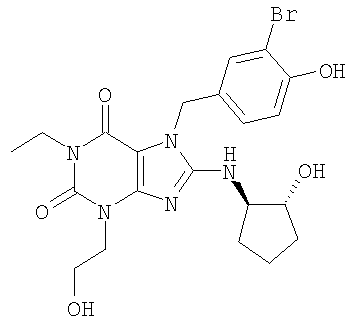
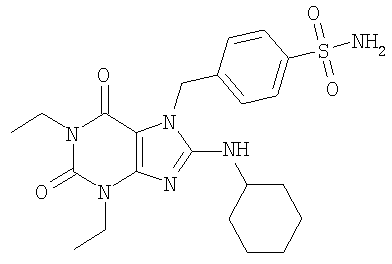
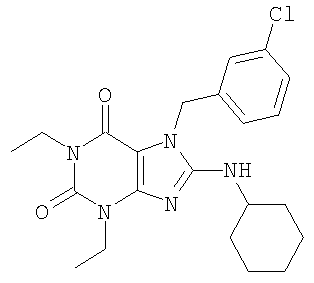


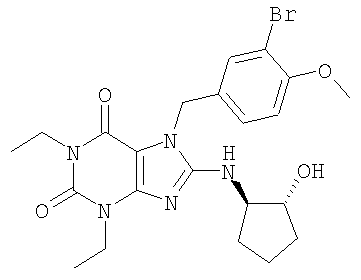
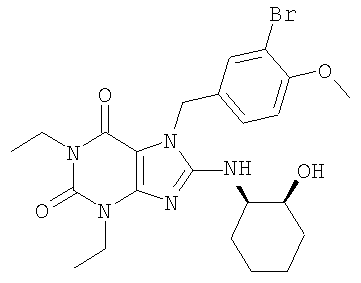
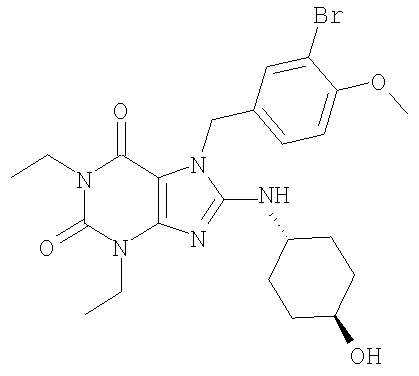

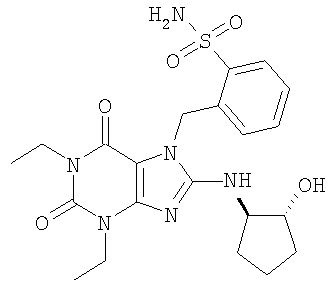
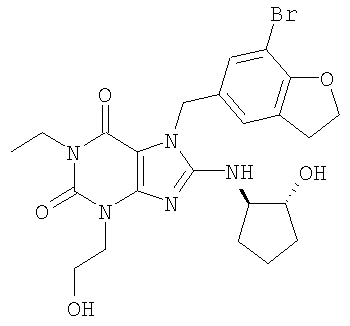
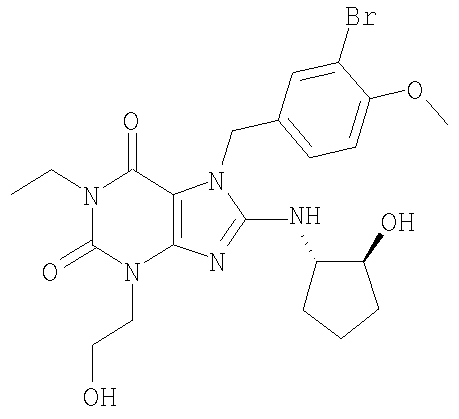
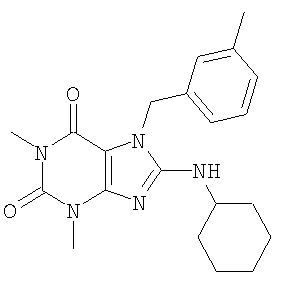

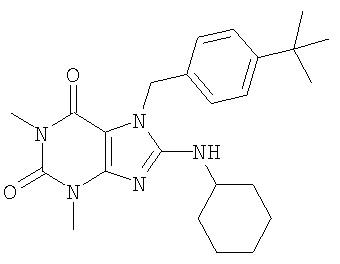

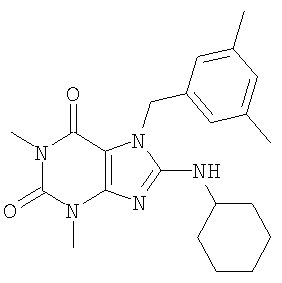
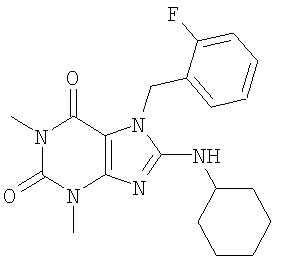

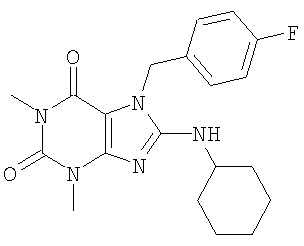

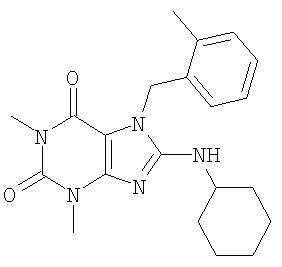
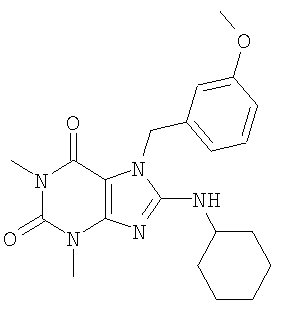

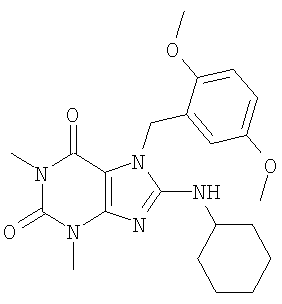



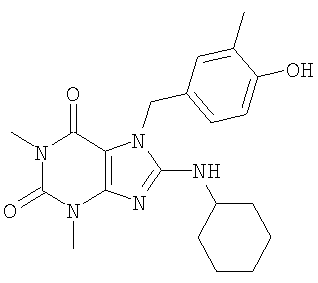
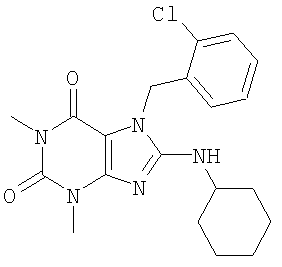


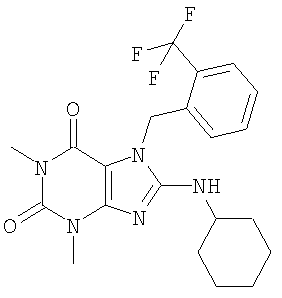
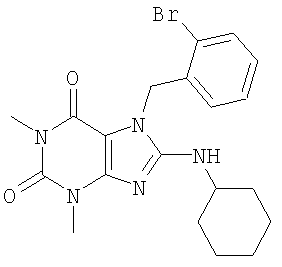

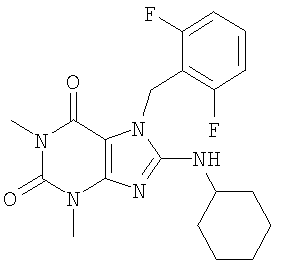


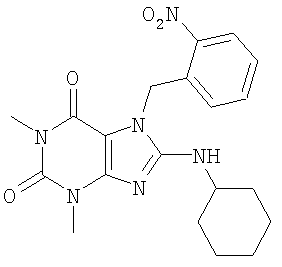

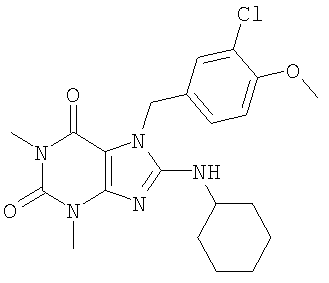





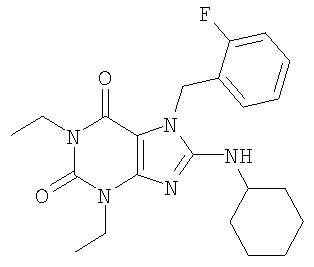
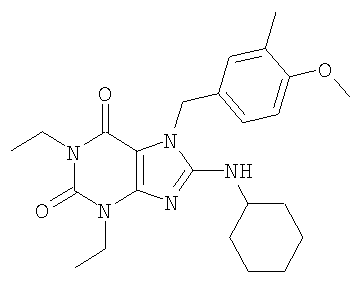

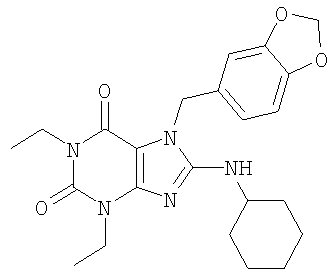
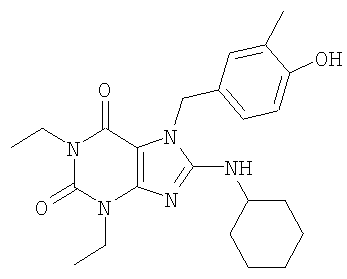



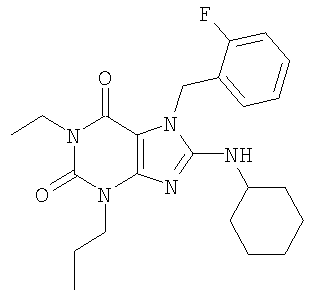

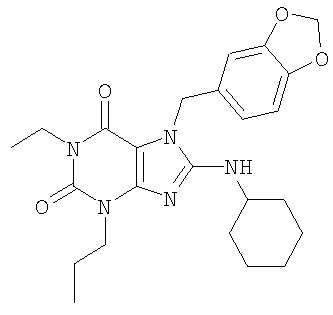
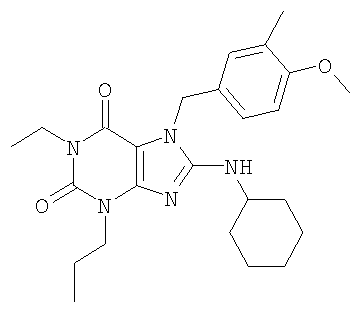






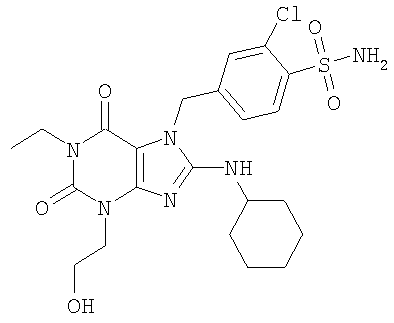
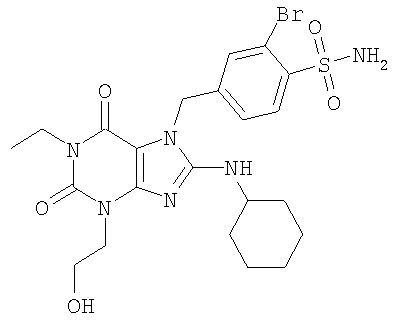














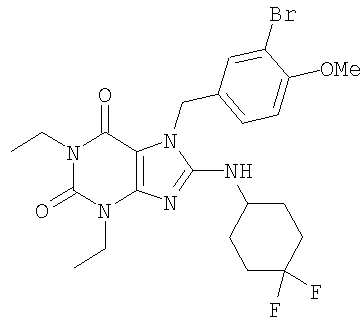
Соединения в соответствии с изобретением полезны для ингибирования ферментов ФДЭ V. Активности ферментов и избирательности ферментов могут быть оценены рядом способов. В частности, активность фермента может быть измерена величиной IC50 ФДЭ V, которая представляет собой концентрацию (в нМ) соединения, требуемую для обеспечения ингибирования ФДЭ V на 50%. Чем ниже величина IC50, тем более активно соединение. Измерения на соединениях в таблицах 1 и 2 дали следующие данные (все числа модифицированы словом «около»):
А. все соединения имели IC50 ФДЭ V в интервале от <1 нМ до >100 нМ;
Б. соединения номера 13-18, 25, 30-32, 38, 41-43, 55-58, 69-71, 77, 85, 92, 96, 98, 101, 113, 120, 121, 126, 128, 131, 137, 138, 141, 146-148, 165, 166, 173, 176, 181, 182, 184, 185, 193 и 194 имели IC50 ФДЭ V в интервале от больше 15 до 100 нМ;
В. соединения номера 23, 24, 29, 33, 34, 39, 40, 93, 94, 108, 111, 112, 125, 136, 144, 160 и 161 имели IC50 ФДЭ V в интервале от больше 10 до 15 нМ.
Г. соединения номера 21, 22, 28, 36, 37, 59, 66, 68, 78, 79, 89, 95, 99, 110, 115, 132, 159, 171, 172, 175, 180, 183, 190 и 199 имели IC50 ФДЭ V в интервале от больше 5 до 10 нМ и
Д. соединения номера 60-65, 67, 103-107, 114, 116-119, 122-124, 142, 168-170, 177, 178, 179, 186-188, 191, 197 и 198 имели IC50 ФДЭ V в интервале до 5 нМ.
Кроме того, другой тип измерения, которое может быть сделано, представляет собой отношение IC50 ФДЭ VI/IC50 ФДЭ V (обозначаемое как ФДЭ VI/ФДЭ V), которое является показателем избирательности фермента. Чем выше это отношение, тем более избирательным является соединение в отношении ингибирования фермента ФДЭ V относительно фермента ФДЭ VI. Измерения на соединениях (за исключением соединений номера 189, 192, 195 и 196) в таблице 2 дали следующие данные (все числа модифицированы словом «около»):
Е. соединения номера 1-188, 190, 191, 193, 194 и 197-199 имели отношение ФДЭ VI/ФДЭ V больше 0;
Ж. соединения номера 165 и 193 имели отношение ФДЭ VI/ФДЭ V в интервале от больше 0 до 10;
3. соединения номера 101, 108, 136, 141, 146, 148, 168, 173 и 194 имели отношение ФДЭ VI/ФДЭ V в интервале от больше 10 до 25;
И. соединения номера 104, 125, 131-132, 137-138, 142, 144, 170, 175, 177, 185 и 199 имели отношение ФДЭ VI/ФДЭ V в интервале от больше 25 до 50;
К. соединения номера 103, 110, 111, 117, 159, 166, 182 и 187 имели отношение ФДЭ VI/ФДЭ V в интервале от больше 50 до 75;
Л. соединения номера 105, 106, 147 и 171 имели отношение ФДЭ VI/ФДЭ V в интервале от больше 75 до 100;
М. соединения номера 112, 113, 123, 124, 126, 169, 172 и 184 имели отношение ФДЭ VI/ФДЭ V в интервале от больше 100 до 140; и
Н. соединения номера 107, 114-116, 118-122, 128, 160-161, 176, 178-181, 183, 186, 188, 190, 191, 197 и 198 имели отношение ФДЭ VI/ФДЭ V от больше 140.
Предпочтительные соединения в соответствии с изобретением включают те, которые находятся в классах Д и/или Н: соединения номера 60-65, 67, 103-107, 114-124, 128, 142, 160-161, 168-170 и 176-178, 179, 186, 188,191, 197 и 198. Более предпочтительными соединениями в соответствии с изобретением являются соединения номера 107, 114, 116, 118, 119, 122, 160 и 178 из таблицы 2.
Другое предпочтительное соединение в соответствии с изобретением могло бы иметь следующую химическую структуру

Специфические и общие процедуры для получения трех предпочтительных соединений указаны ниже (соединения номера 107, 114 и 160). Очевидные модификации этих процедур могут быть предприняты обычным специалистом. Другие соединения в соответствии с изобретением могут быть получены теми же самыми путями.
Синтез соединения номер 107 в таблице 2
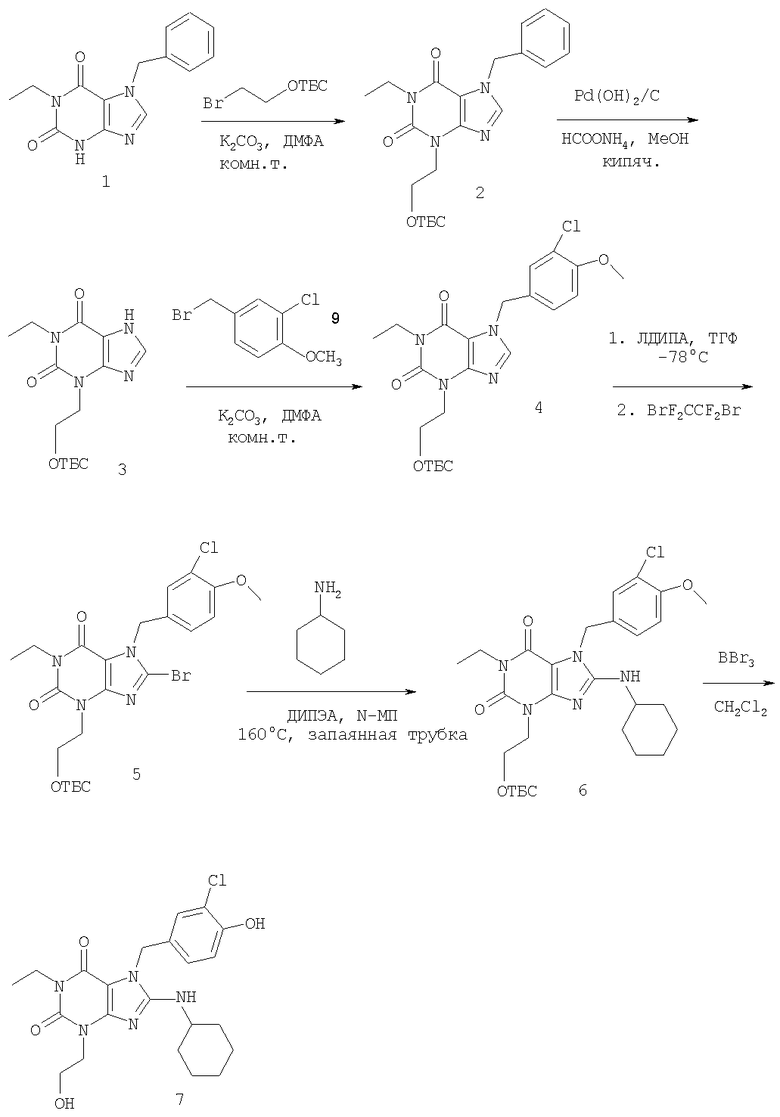
Получение 9

Процедура эксперимента: соединение номер 107 в таблице 2 (7)
1 (20,0 г, 74,0 ммоля) растворяли в диметилформамиде (370 мл) в атмосфере азота и добавляли по каплям (2-бромэтокси)-трет-бутилдиметилсилан (31,8 мл, 148 ммоля). Реакционную смесь перемешивали при комнатной температуре 115 часов, затем разбавляли этилацетатом и промывали водой несколько раз. Органическую смесь высушивали над карбонатом калия, фильтровали и концентрировали в вакууме. Очисткой методом флеш-хроматографии (этилацетат/гексаны 30/70) получено 2 (28,1 г, 88%).
1H ЯМР (400 МГц, CDCl3): δ 7,52 (s, 1H), 7,29-7,39 (m, 5H), 5,49 (s, 2H), 4,25 (t, 2H, J=6,0 Гц), 4,07 (q, 2H, J=7,2 Гц), 3,93 (t, 2H, J=6,0 Гц), 1,24 (t, 3H, J=7,2 Гц), 0,75 (s, 9H), 0,08 (s, 6H). Масс-спектрометрия высокого разрешения (МСВР): расч. для С22Н32N4O3Si (М+Н) 429,2322; найдено 429,2329.
К раствору 2 (2,10 г, 4,89 ммоля) в метаноле (375 мл) добавляли муравьинокислый аммоний (4,64 г, 73,6 ммоля) и 20% гидроокиси палладия на угле (980 мг). Реакционную смесь нагревали до кипения с обратным холодильником 1,5 часа, затем охлаждали до комнатной температуры, фильтровали и концентрировали в вакууме. Очисткой методом флеш-хроматографии (этилацетат/гексаны 50/50) получено 3 (1,26 г, 94%).
1H ЯМР (400 МГц, CDCl3): δ 7,82 (s, 1H), 4,33 (t, 2H, J=6,0 Гц), 4,16 (q, 2H, J=7,2 Гц), 3,99 (t, 2H, J=6,0 Гц), 1,29 (t, 3H, J=7,2 Гц), 0,78 (s, 9H), 0,06 (s, 6H). МСВР: расч. для С15Н26N4O3Si (М+Н) 339,1852; найдено: 339,1864.
К 3 (970 мг, 2,86 ммоля) добавляли диметилформамид (14 мл), 3-хлор-4-метоксибензилбромид 9 (1,72 г, 5,70 ммоля) и карбонат калия (785 мг, 5,70 ммоля) в атмосфере азота. Реакционную смесь перемешивали при комнатной температуре 24 часа, затем разбавляли этилацетатом и промывали водой несколько раз. Органическую смесь сушили над карбонатом калия, фильтровали и концентрировали в вакууме. Очисткой методом флеш-хроматографии (этилацетат/гексаны 30/70) получено 4 (1,14 г, 81%).
1H ЯМР (400 МГц, CDCl3): δ 7,52 (s, 1H), 7,33 (d, 1H, J=2,4 Гц), 7,25 (dd 1H, J=2,0 Гц, J=8,4 Гц), 6,90 (d, 1H, J=8,8 Гц), 5,40 (s, 2H), 4,25 (t, 2H, J=6,0 Гц), 4,07 (q, 2H, J=7,2 Гц), 3,93 (t, 2H, J=6,0 Гц), 3,89 (s, 3Н), 1,25 (t, 3H, J=7,2 Гц), 0,75 (s, 9H), 0,08 (s, 6H). MCBP: расч. для С23Н33ClN4O4Si (М+Н) 493,2038; найдено: 493,2032.
К раствору 4 (1,14 г, 2,32 ммоля) в тетрагидрофуране (20 мл) в атмосфере азота при -78°С (баня сухой лед/ацетон) добавляли диизопропиламид лития (2 М в смеси ТГФ/гептан, 1,7 мл, 3,48 ммоля). После перемешивания в течение тридцати минут добавляли по каплям 1,2-дибромтетрафторэтан (0,55 мл, 4,63 ммоля) за время более пяти минут. Реакционную смесь перемешивали 1,5 часа при -78°С, затем гасили насыщенным водным раствором бикарбоната натрия и нагревали до комнатной температуры. Смесь экстрагировали хлористым метиленом, сушили над карбонатом калия, фильтровали и концентрировали в вакууме. Очисткой методом флеш-хроматографии (этилацетат/гексаны 30/70) получено 5 (640 мг, 48%).
1H ЯМР (400 МГц, CDCl3): δ 7,42 (d, 1H, J=2,4 Гц), 7,31 (dd, 1H, J=2,0 Гц, J=8,4 Гц), 6,88 (d, 1H, J=8,8 Гц), 5,45 (s, 2H), 4,22 (t, 2H, J=5,6 Гц), 4,07 (q, 2H, J=7,2 Гц), 3,92 (t, 2H, J=5,6 Гц), 3,88 (s, ЗН), 1,25 (t, 3H, J=7,2 Гц), 0,74 (s, 9H), 0,08 (s, 6H). MCBP: расч. для С23Н32BrClN4O4Si (М+Н) 571,1143; найдено: 571,1149.
К 5 (320 мг, 0,56 ммоля) добавляли циклогексиламин (0,25 мл, 2,24 ммоля), диизопропилэтиламин (2,8 мл) и 1-метил-2-пирролидинон (2,8 мл). Реакционную смесь нагревали до 160°С в запаянной трубке 18 часов, затем охлаждали до комнатной температуры. Добавляли воду, затем смесь экстрагировали этилацетатом и промывали водой несколько раз. Органическую смесь сушили над карбонатом калия, фильтровали и концентрировали в вакууме. Очисткой методом флеш-хроматографии (этилацетат/гексаны 30/70) получено 6 (210 мг, 64%).
1H ЯМР (400 МГц, CDCl3): δ 7,27 (d, 1H, J=2,0 Гц), 7,13 (dd, 1H, J=2,0 Гц, J=8,4 Гц), 6,89 (d, 1H, J=8,8 Гц), 5,23 (s, 2H), 4,19 (t, 2H, J=6,2 Гц), 4,05 (q, 2H, J=7,2 Гц), 3,93 (t, 2H, J=6,2 Гц), 3,89 (s, 3Н), 3,86-3,91 (m, 1H), 3,69-3,80 (m, 1H), 1,88-1,96 (m, 2H), 1,52-1,64 (m, 3Н), 1,28-1,42 (m, 2H), 1,23 (t, 3Н, J=7,2 Гц), 1,04-1,22 (m, 3Н), 0,81 (s, 9H), 0,01 (s, 6H). MCBP: расч. для C29H44ClN5O4Si (М+Н) 590,2937; найдено 590,2929.
6 (191 мг, 0,324 ммоля) растворяли в хлористом метилене (4,0 мл) в атмосфере азота и охлаждали до 0°С в бане со льдом. Трибромид бора (0,14 мл, 1,42 ммоля) добавляли к реакционной смеси и нагревали до комнатной температуры. Через 1,25 ч реакционную смесь разбавляли хлористым метиленом и промывали водой несколько раз. Органическую фазу сушили над карбонатом калия, фильтровали и концентрировали в вакууме. Очисткой методом жидкостной хроматографии с программированием температуры (этилацетат/гексаны 70/30) получено 7 (соединение номер 107 в таблице 2) (122 мг, 74%).
1H ЯМР (400 МГц, CDCl3): δ 7,25-7,28 (m, 1H), 7,09 (dd, 1H, J=2,0 Гц, J=8,0 Гц), 7,01 (d, 1H, J=8,0 Гц), 5,69 (s, 1H), 5,23 (s, 2H), 4,32-4,36 (m, 2H), 4,16 (t, 1H, J=6,0 Гц), 4,06 (q, 2H, J=7,2 Гц), 3,90-3,98 (m, 3H), 3,62-3,72 (m, 1H), 1,87-1,96 (m, 2H), 1,54-1,66 (m, 3H), 1,31-1,43 (m, 2H), 1,25 (t, 3H, J=7,2 Гц), 1,06-1,22 (m, 3H). МСВР: расч. для C22H28ClN5O4 (M+H) 462,1908; найдено 462,1901.
3-Хлор-4-метокситолуол 8 (2,6 мл, 19,2 ммоля) растворяли в хлористом метилене (30 мл) и добавляли N-бромсукцинимид (3,75 г, 21,1 ммоля), после чего добавляли азо-бис-(изобутиронитрил) (36,0 мг). Реакционную смесь нагревали до кипения с обратным холодильником 19 часов, затем охлаждали до комнатной температуры и осадок отфильтровывали. Фильтрат разбавляли хлористым метиленом и промывали 0,5 М водным раствором бикарбоната натрия, затем водой. Органическую смесь сушили над сульфатом натрия, фильтровали и концентрировали в вакууме, получая 9 (4,73 г, 82%). Бензилбромид использовали как сырой материал без дальнейшей очистки.
1H ЯМР (400 МГц, CDCl3): δ 7,42 (d, 1H, J=2,4 Гц), 7,26 (dd, 1H, J=2,4 Гц, J=8,4 Гц), 6,88 (d, 1H, J=8,4 Гц), 4,44 (s, 2H), 3,90 (s, 3H).
Общая схема синтеза соединения номер 107 в таблице 2 (7):
а) реакция 1 с алкилгалогенидом и основанием с образованием 2;
б) дебензилирование 2 с образованием 3;
в) алкилирование 3 бензилгалогенидом с образованием 4;
г) депротонирование 4 с последующим добавлением бромирующего агента с образованием 5;
д) замещение брома в 5 амином с образованием 6 и
е) Обработка 6 трибромидом бора с образованием соединения номер 107 в таблице 2 (7) путем расщепления как силильного так и метильного простых эфиров.
Синтез соединения 114 в таблице 2 (13)

Получение 15
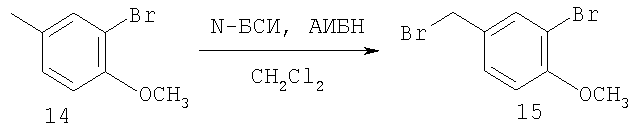
Процедура эксперимента: соединение 114 в таблице 2 (13)
1 (20,0 г, 74,0 ммоля) растворяли в диметилформамиде (370 мл) в атмосфере азота и добавляли по каплям (2-бромэтокси)-трет-бутилдиметилсилан (31,8 мл, 148 ммоля). Реакционную смесь перемешивали при комнатной температуре 115 часов, затем разбавляли этилацетатом и промывали водой несколько раз. Органическую смесь сушили над карбонатом калия, фильтровали и концентрировали в вакууме. Очисткой методом флеш-хроматографии (этилацетат/гексаны 30/70) получено 2 (28,1 г, 88%).
1H ЯМР (400 МГц, CDCl3): δ 7,52 (s, 1Н), 7,29-7,39 (m, 5H), 5,49 (s, 2H), 4,25 (t, 2H, J=6,0 Гц), 4,07 (q, 2H, J=7,2 Гц), 3,93 (t, 2H, J=6,0 Гц), 1,24 (t, 3H, J=7,2 Гц), 0,75 (s, 9H), 0,08 (s, 6H). МСВР: расч. для С22Н32N4O3Si (М+Н) 429,2322; найдено 429,2329.
К раствору 2 (2,10 г, 4,89 ммоля) в метаноле (375 мл) добавляли муравьинокислый аммоний (4,64 г, 73,6 ммоля) и 20% гидроокиси палладия на угле (980 мг). Реакционную смесь нагревали до кипения с обратным холодильником 1,5 часа, затем охлаждали до комнатной температуры, отфильтровывали и концентрировали в вакууме. Очисткой методом флеш-хроматографии (этилацетат/гексаны 50/50) получено 3 (1,26 г, 94%).
1H ЯМР (400 МГц, CDCl3): δ 7,82 (s, 1Н), 4,33 (t, 2H, J=6,0 Гц), 4,16 (q, 2H, J=7,2 Гц), 3,99 (t, 2H, J=6,0 Гц), 1,29 (t, 3H, J=7,2 Гц), 0,78 (s, 9H), 0,06 (s, 6H). МСВР: расч. для C15H26N4O3Si (M+H): 339,1852; найдено 339,1864.
К 3 (970 мг, 2,86 ммоля) добавляли диметилформамид (25 мл), 3-бром-4-метоксибензилбромид 15 (1,62 г, 5,79 ммоля) и карбонат калия (800 мг, 5,79 ммоля) в атмосфере азота. Реакционную смесь перемешивали при комнатной температуре 21 час, затем разбавляли этилацетатом и промывали водой несколько раз. Органическую смесь сушили над карбонатом калия, фильтровали и концентрировали в вакууме. Очисткой методом флеш-хроматографии (этилацетат/гексаны 30/70) получено 10 (1,55 г, 100%).
1H ЯМР (400 МГц, CDCl3): δ 7,52 (s, 1H), 7,51 (d, 1H, J=2,4 Гц), 7,30 (dd 1H, J=2,0 Гц, J=8,4 Гц), 6,87 (d, 1H, J=8,8 Гц), 5,40 (s, 2H), 4,25 (t, 2H, J=6,0 Гц), 4,07 (q, 2H, J=7,0 Гц), 3,93 (t, 2H, J=6,0 Гц), 3,88 (s, 3Н), 1,25 (t, 3H, J=7,0 Гц), 0,75 (s, 9H), 0,08 (s, 6H). MCBP: расч. для С23Н33BrN4O4Si (М+Н) 537,1533; найдено 537,1540.
К раствору 10 (1,50 г, 2,80 ммоля) в тетрагидрофуране (24 мл) в атмосфере азота при -78°С (баня сухой лед/ацетон) добавляли диизопропиламид лития (2 М в смеси ТГФ/гептан, 2,2 мл, 4,33 ммоля). После перемешивания в течение тридцати минут добавляли по каплям 1,2-дибромтетрафторэтан (0,69 мл, 5,77 ммоля) в течение более пяти минут. Реакционную смесь перемешивали 1,25 часа при -78°С, затем гасили насыщенным водным раствором бикарбоната натрия и нагревали до комнатной температуры. Смесь экстрагировали хлористым метиленом, сушили над карбонатом калия, фильтровали и концентрировали в вакууме. Очисткой методом флеш-хроматографии (30/70 этилацетат/гексаны) получено 11 (600 мг, 34%).
1H ЯМР (400 МГц, CDCl3): δ 7,60 (d, 1H, J=2,4 Гц), 7,35 (dd, 1H, J=2,0 Гц, J=8,4 Гц), 6,84 (d, 1H, J=8,4 Гц), 5,45 (s, 2H), 4,21 (t, 2H, J=5,6 Гц), 4,07 (q, 2H, J=6,8 Гц), 3,90 (t, 2H, J=5,6 Гц), 3,87 (s, 3Н), 1,24 (t, 3H, J=6,8 Гц), 0,73 (s, 9H), 0,08 (s, 6H). МСВР: расч. для С23Н32Br2N4O4Si (М+Н) 615,0638; найдено 615,0633.
К 11 (1,89 г, 3,07 ммоля) добавляли солянокислую соль аминоспирта (1,31 г, 12,27 ммоля), диизопропилэтиламин (15,4 мл) и 1-метил-2-пирролидинон (15,4 мл). Реакционную смесь нагревали до 160°С в запаянной трубке 13 часов, затем охлаждали до комнатной температуры. Добавляли воду, затем экстрагировали смесь этилацетатом и промывали водой несколько раз. Органическую смесь сушили над карбонатом калия, фильтровали и концентрировали в вакууме. Очисткой методом флеш-хроматографии (метанол/хлористый метилен 3/97) получено 12 (1,77 г, 90%).
1H ЯМР (400 МГц, CDCl3): δ 7,45 (d, 1H, J=2,0 Гц), 7,17 (dd, 1H, J=2,4 Гц, J=8,6 Гц), 6,86 (d, 1H, J=8,4 Гц), 5,18-4,34 (m, 3Н), 4,00-4,23 (m, 5H), 3,86-3,98 (m, 6H), 3,69-3,79 (m, 1H), 2,10-2,21 (m, 1H), 1,99-2,10 (m, 1H), 1,60-1,84 (m, 3Н), 1,32-1,43 (m, 1H), 1,24 (t, ЗН, J=7,2 Гц), 0,75 (s, 9H), 0,07 (d, 6H, J=4,0 Гц). МСВР: расч. для C28H43BrN5O5Si (М+Н) 636,2217; найдено 636,2207.
12 (1,77 г, 2,78 ммоля) растворяли в тетрагидрофуране (28 мл) в атмосфере азота и добавляли по каплям тетрабутиламмонийфторид (1 М в ТГФ, 28 мл). Реакционную смесь перемешивали при комнатной температуре 15 часов, затем разбавляли хлористым метиленом и промывали водой несколько раз. Органическую смесь сушили над карбонатом калия, фильтровали и концентрировали в вакууме. Очисткой методом флеш-хроматографии (метанол/хлористый метилен 3/97) получено 13 (соединение номер 114 в таблице 2) (760 мг, 52%).
1H ЯМР (400 МГц, CDCl3): δ 7,47 (d, 1H, J=2,0 Гц), 7,19 (dd, 1H, J=2,0 Гц, J=8,4 Гц), 6,88 (d, 1H, J=8,4 Гц), 5,25 (s, 2H), 5,09 (s, 1H), 4,21-4,27 (m, 3H), 4,06 (q, 2H, J=7,0 Гц), 3,90-3,97 (m, 3H), 3,89 (s, 1H), 3,74-3,82 (m, 1H), 3,08 (s, 1H), 2,12-2,22 (m, 1H), 1,98-2,08 (m, 1H), 1,60-1,86 (m, 3H), 1,33-1,43 (m, 1H), 1,25 (t, 3H, J=7,0 Гц), 1,06-1,22 (m, 3H). MCBP: расч. для C22H28BrN5O5 (M+H) 522,1352; найдено 522,1346.
2-Бром-4-метиланизол 14 (2,2 мл, 14,9 ммоля) растворяли в хлористом метилене (30 мл) и добавляли N-бромсукцинимид (3,75 г, 16,4 ммоля), а затем азо-бис-(изобутиронитрил)(26,0 мг). Реакционную смесь нагревали до кипения с обратным холодильником 19 часов, затем охлаждали до комнатной температуры и осадок отфильтровывали. Фильтрат разбавляли хлористым метиленом и промывали 0,5 М водным раствором бикарбоната натрия, затем водой. Органическую смесь сушили над сульфатом натрия, фильтровали и концентрировали в вакууме, получая 15 (4,16 г, 100%). Бромистый бензил использовался как сырой материал без дополнительной очистки.
1H ЯМР (400 МГц, CDCl3): δ 7,59 (d, 1H, J=2,0 Гц), 7,30 (dd, 1H, J=2,4 Гц, J=8,4 Гц), 6,85 (d, 1H, J=8,4 Гц), 4,37 (s, 2H), 3,90 (s, 3H).
Общая схема синтеза соединения номер 114 в таблице 2 (13):
а) реакция 1 с алкилгалогенидом и основанием с образованием 2;
б) дебензилирование 2 с образованием 3;
в) алкилирование 3 бензилгалогенидом с образованием 10;
г) депротонирование 10 с последующим добавлением бромирующего агента с образованием 11;
д) замещение брома в 11 амином с образованием 12 и
е) Расщепления силильного простого эфира 12 с образованием соединения номер 114 в таблице 2 (13).
Синтез соединения номер 160 в таблице 2 (18)

Процедура эксперимента: соединение номер 160 в таблице 2 (18)
К 16 (150 мг, 0,579 ммоля) добавляли диметилформамид (3 мл), 6-хлорпиперонилхлорид (142 мг, 0,694 ммоля) и карбонат калия (120 мг, 0,868 ммоля) в атмосфере азота. Реакционную смесь перемешивали при комнатной температуре 137 часов, затем разбавляли этилацетатом и промывали водой несколько раз. Органическую смесь сушили над сульфатом магния, фильтровали и концентрировали в вакууме. Очисткой методом жидкостной хроматографии с программированием температуры (этилацетат/гексаны 1/1) получено 17 (84,1 мг, 34%).
1H ЯМР (400 МГц, CDCl3): δ 6,89 (s, 1H), 6,09 (s, 1H), 5,95 (s, 2H), 5,59 (s, 2H), 3,60 (s, 3H), 3,38 (s, 3H). МСВР: расч. для C15H12BrClN4O4 (M+H) 426,9809; найдено 426,9802.
К 17 (72,0 мг, 0,169 ммоля) добавляли циклогексиламин (86,7 мг, 0,883 ммоля), диизопропилэтиламин (0,8 мл) и 1-метил-2-пирролидинон (0,8 мл). Реакционную смесь нагревали при 160°С в запаянной трубке 17 часов, затем охлаждали до комнатной температуры. Добавляли воду, затем смесь экстрагировали этилацетатом и промывали водой несколько раз. Органическую смесь сушили над сульфатом магния, фильтровали и концентрировали в вакууме. Очисткой методом жидкостной хроматографии с программированием температуры (этилацетат/гексаны 1/1) получено соединение номер 160 в таблице 2 (18) (50,9 мг, 68%).
1H ЯМР (400 МГц, CDCl3): δ 6,84 (s, 1H), 6,815 (s, 1H), 5,96 (s, 2H), 5,33 (s, 2H), 4,42 (d, 1H, J=7,2 Гц), 3,68-3,79 (m, 1H), 3,53 (s, 3H), 3,40 (s, 3H), 1,94-2,05 (m, 2H), 1,55-1,74 (m, 3H), 1,25-1,42 (m, 2H), 1,10-1,22 (m, 3H). МСВР: расч. для C21H24ClN5O4 (M+H) 444,2400; найдено 444,2394.
Общая схема синтеза соединения номер 160 в таблице 2 (18):
а) алкилирование 16 бензилгалогенидом с образованием 17 и
б) замещение брома в 17 амином с образованием соединения номер 160 в таблице 2 (18).
Соответственно, изобретение включает способ получения соединения, имеющего формулу (I), включающий
(1) реакцию соединения, имеющего формулу (III), с алкилгалогенидом в присутствии основания с образованием соединения, имеющего формулу (IV)

где (а) R1 представляет собой атом водорода или алкильную группу с 1-15 атомами углерода, разветвленную или с нормальной цепью, с одним или несколькими заместителями, либо без них, алкенильную группу с 2-15 атомами углерода, разветвленную или с нормальной цепью, с одним или несколькими заместителями, либо без них, алкинильную группу с 2-15 атомами углерода, разветвленную или с нормальной цепью, с одним или несколькими заместителями, либо без них, циклоалкильную группу с 3-15 атомами углерода с одним или несколькими заместителями, либо без них, аралкильную группу с одним или несколькими заместителями, либо без них, арильную группу с одним или несколькими заместителями, либо без них, гетероарильную группу с одним или несколькими заместителями, либо без них, группу -OR5, -COOR5, -C(O)R5 или -C(O)N(R5)2, где R5 представляет собой атом водорода или углеводородный радикал, разветвленный или с нормальной цепью, с одним или несколькими заместителями, либо без них,
(б) L представляет собой R2 или защищенную форму R2;
(в) Ph представляет собой фенильную группу;
(2) дебензилирование и затем алкилирование соединения, имеющего формулу (IV) алкилгалогенидом, XCH2R3 с образованием соединения, имеющего формулу (V)

где X представляет собой атом галогена (например, атом хлора или брома) и
R3 представляет собой арильную группу с одним или несколькими заместителями, либо без них, гетероарильную группу с одним или несколькими заместителями, либо без них, или гетероциклическую группу, имеющую от 1 до 3 гетероатомов, конденсированную с 5- или 6-членным арильным циклом, с одним или несколькими заместителями, либо без них, при условии, что R3 не является арильной группой, замещенной в пара-положение -Y-арильной группой, где Y представляет собой углерод-углеродную одинарную связь, -СО-, -O-, -S-, -N(R21)-, -CON(R22)-, -N(R22)CO-, -ОСН2-, -СН2O-, -SCH2-, -CH2S-, -NHC(R23)(R24)-, -NR23SO2-, -SO2NR23-, -C(R23)(R24)NH-, -CH=CH-, -CF=CF-, -CH=CF-, -CF=CH-, -CH2CH2-, -CF2CF2-,
 ,
,  ,
,  ,
,
 ,
, 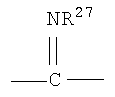 или
или 
где R21 представляет собой атом водорода или -CO(алкил C1-4), алкильную группу с 1-6 атомами углерода, аллильную группу, циклоалкильную группу с 3-6 атомами углерода, фенильную или бензильную группу;
R22 представляет собой атом водорода или алкильную группу с 1-6 атомами углерода;
R23 представляет собой атом водорода или алкильную группу с 1-5 атомами углерода, арильную или -СН2-арильную группу;
R24 представляет собой атом водорода или алкильную группу с 1-4 атомами углерода;
циклоалкильную группу с 3-6 атомами углерода, фенильную или бензильную группу;
R25 представляет собой атом водорода или алкильную группу с 1-8 атомами углерода; перфторалкильную группу с 1-8 атомами углерода, циклоалкильную группу с 3-6 атомами углерода, фенильную или бензильную группу;
R26 представляет собой атом водорода или алкильную группу с 1-8 атомами углерода, циклоалкильную группу с 3-6 атомами углерода, фенильную или бензильную группу;
R27 представляет собой группу -NR23R24, -OR24, -NHCONH2, -NHCSNH2,
 или
или 
и
R28 и R29, независимо друг от друга, каждый представляет собой алкильную группу с 1-4 атомами углерода или R28 и R29 вместе друг с другом представляют собой группу -(CH2)q, где q составляет 2 или 3, и
(3) депротонирование и затем галогенирование соединения, имеющего формулу (V), с образованием соединения, имеющего формулу (VI)

где Hal представляет собой атом галогена;
(4) реакцию соединения, имеющего формулу (VI), с амином, имеющим формулу R4NH2, с образованием соединения, имеющего формулу (VII)
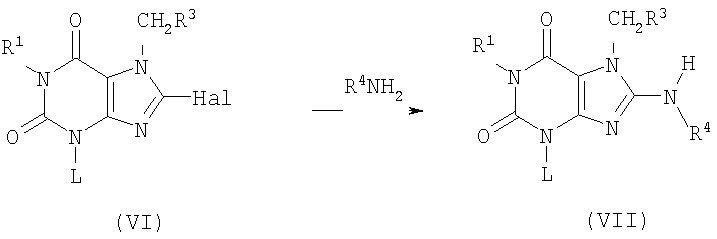
где R4 представляет собой циклоалкильную группу с 3-15 атомами углерода с одним или несколькими заместителями, либо без них, циклоалкенильную группу с 3-15 атомами углерода с одним или несколькими заместителями, либо без них, или гетероциклоалкильную группу с от 3 до 15 членами с одним или несколькими заместителями, либо без них, и
(5) удаление защитной части L, где L представляет собой защищенную форму R2, в соединении, имеющем формулу (VII), с образованием соединения, имеющего формулу (I)

где R2 определена так же, как выше R1, при условии что, по меньшей мере, одна из R1 и R2 не является атомом водорода;
где один или несколько заместителей определены выше так же, как для одного или нескольких заместителей в формуле (I).
Фармацевтически приемлемые формы дозирования
Соединения в соответствии с настоящим изобретением могут быть назначены людям или другим млекопитающим различными путями, включая формы для перорального применения и инъекции (внутривенные, внутримышечные, внутрибрюшинные, подкожные и тому подобные). Многочисленные другие формы дозирования, содержащие соединения в соответствии с настоящим изобретением, могут быть легко скомпонованы специалистами с использованием подходящих фармацевтических инертных наполнителей, которые определены ниже. Из соображений одобрения пациентами обычно наиболее предпочтительны формы для перорального применения.
Скорость физиологической доставки может быть удовлетворительно проконтролирована специалистами манипулированием одним или несколькими из следующих факторов:
(а) точное дозирование активного ингредиента;
(б) фармацевтически приемлемый(е) инертный(е) наполнитель(и), до тех пор пока варианты не мешают действенности выбранного специфического активного ингредиента;
(в) тип инертного(ых) наполнителя(ей) и соответствующие желательные толщина и проницаемость (свойства набухания) инертного(ых) наполнителя(ей);
(г) зависящие от времени условия инертного(ых) наполнителя(ей);
(д) размер частиц гранулированного активного ингредиента и
(е) зависящие от рН условия инертного(ых) наполнителя(ей).
Фармацевтически приемлемые инертные наполнители включают ароматизирующие агенты, красители или пигменты фармацевтического класса, растворители, сорастворители, буферные системы, поверхностно-активные вещества, консервирующие средства, подсластители, агенты, регулирующие вязкость, наполнители, смазочные вещества, агенты, регулирующие скользкость, дезинтегрирующие агенты, связующие и смолы.
Могут быть использованы обычные ароматизирующие агенты, такие как те, что описаны в Remington's Pharmaceutical Science, 18-oe изд., Mack Publishing Co., стр.1288-1300 (1990)(включена здесь в качестве ссылки во всей своей полноте). Фармацевтические композиции в соответствии с изобретением обычно содержат приблизительно от 0 до 2% ароматизирующих агентов.
Также могут быть использованы обычные красители и/или пигменты, такие как те, что описаны в Handbook of Pharmaceutical Excipients, by the American Pharmaceutical Association & the Pharmaceutical Society of Great Britain, pp.81-90 (1986) (включена здесь в качестве ссылки во всей своей полноте). Фармацевтические композиции в соответствии с изобретением обычно содержат приблизительно от 0 до 2% красителей и/или пигментов.
Фармацевтические композиции в соответствии с изобретением обычно содержат приблизительно от 0,1 до 99,9% растворителя(ей). Предпочтительным растворителем является вода. Предпочтительные сорастворители включают этиловый спирт, глицерин, пропиленгликоль, полиэтиленгликоль и тому подобные. Фармацевтические композиции в соответствии с изобретением могут включать приблизительно от 0 до 50% сорастворителей.
Предпочтительные буферные системы включают уксусную, борную, угольную, фосфорную, янтарную, яблочную, винную, лимонную, бензойную, молочную, глицериновую, глюконовую, глутаровую и глутаминовую кислоты и их соли с натрием, калием и аммонием. Особенно предпочтительными буферами являются фосфорные, винная, лимонная и уксусная кислоты и их соли. Фармацевтические композиции в соответствии с изобретением обычно содержат приблизительно от 0 до 5% буфера.
Предпочтительные поверхностно-активные вещества включают сложные эфиры полиэтиленоксида, сорбита и жирных кислот, простые моноалкильные эфиры полиэтиленоксида, сложные моноэфиры сахарозы и сложные и простые эфиры ланолина, соли алкилсульфокислот и натриевые, калийные и аммонийные соли жирных кислот. Фармацевтические композиции в соответствии с изобретением обычно содержат приблизительно от 0 до 2% поверхностно-активных веществ.
Предпочтительные консервирующие средства включают фенол, сложные алкиловые эфиры пара-гидроксибензойной кислоты, о-фенилфенолбензойной кислоты и их соли, борную кислоту и ее соли, сорбиновую кислоту и ее соли, хлорбутанол, бензиловый спирт, тимерозол, фенилмеркурацетат и фенилмеркурнитрат, нитромерзол, бензалконийхлорид, цетилпиридийхлорид, метиловый и пропиловый эфиры пара-аминобензойной кислоты. Особенно предпочтительными консервирующими средствами являются соли бензойной кислоты, цетилпиридийхлорид, метиловый и пропиловый эфиры пара-аминобензойной кислоты. Фармацевтические композиции в соответствии с изобретением обычно включают приблизительно от 0 до 2% консервирующих средств.
Предпочтительные подсластители включают сахарозу, глюкозу, сахарин, сорбит, маннит и аспартам. Особенно предпочтительными подсластителями являются сахароза и сахарин. Фармацевтические композиции в соответствии с изобретением обычно включают приблизительно от 0 до 5% подсластителей.
Предпочтительные агенты, регулирующие вязкость, включают метилцеллюлозу, натрий карбоксиметилцеллюлозу, гидроксипропилметилцеллюлозу, гидроксипропилцеллюлозу, альгинат натрия, карбомер, повидон, гуммиарабик, гуаровую смолу, ксантановую смолу и трагакант. Особенно предпочтительными агентами, регулирующими вязкость, являются метилеллюлоза, карбомер, ксантановая смола, гуаровая смола, повидон, натрийкарбоксиметилцеллюлоза и алюмосиликат магния. Фармацевтические композиции в соответствии с изобретением обычно включают приблизительно от 0 до 5% агентов, регулирующих вязкость.
Предпочтительные наполнители включают лактозу, маннит, сорбит, трехосновный фосфорнокислый кальций, двухосновный фосфорнокислый кальций, прессованный сахар, крахмал, сульфат кальция, декстрины и микрокристаллическую целлюлозу. Фармацевтические композиции в соответствии с изобретением обычно содержат приблизительно от 0 до 75% наполнителей.
Предпочтительные смазывающие вещества/агенты, регулирующие скользкость, включают стеарат магния, стеариновую кислоту и тальк. Фармацевтические композиции в соответствии с изобретением обычно включают приблизительно от 0 до 7%, предпочтительно приблизительно от 1 до 5% смазывающих веществ/агентов, регулирующих скользкость.
Предпочтительные дезинтегрирующие агенты включают крахмал, крахмалгликолят натрия, сшитые повидон и кармелозу натрия и микрокристаллическую целлюлозу. Фармацевтические композиции в соответствии с изобретением обычно включают приблизительно от 0 до 20%, предпочтительно приблизительно от 4 до 15% дезинтегрирующих агентов.
Предпочтительные связующие компоненты включают гуммиарабик, трагакант, гидроксипропилцеллюлозу, преджелатинированный крахмал, желатин, повидон, гидроксипропилметилцеллюлозу, метилцеллюлозу, растворы сахаров, таких как сахароза и сорбит, и этилцеллюлозу. Фармацевтические композиции в соответствии с изобретением обычно включают приблизительно от 0 до 12%, предпочтительно приблизительно от 1 до 10% связующих компонентов.
Дополнительные агенты, известные специалистам по композициям, могут быть использованы в сочетании с соединениями в соответствии с изобретением, чтобы создать единую форму дозировки. В ином случае дополнительные агенты могут быть отдельно прописаны млекопитающему как часть множественной формы дозировки.
Для получения фармацевтических композиций, содержащих соединения в соответствии с изобретением, инертные фармацевтически приемлемые носители могут быть либо в виде твердого тела, либо жидкости. Твердые формы препаратов включают порошки, таблетки, диспергируемые гранулы, капсулы, облатки и суппозитории. В порошки и таблетки может быть включено приблизительно от 5 до 95 процентов по весу активного ингредиента. Подходящие твердые носители известны специалистам, например углекислый магний, стеарат магния, тальк, сахар и лактоза. Таблетки, порошки, облатки и капсулы могут быть использованы как твердые формы дозировки, подходящие для назначения перорально. Примеры фармацевтически приемлемых носителей и способов производства различных композиций могут быть найдены в Remington's Pharmaceutical Science, 18-oe изд., Mack Publishing Co. (1990) (включена здесь в качестве ссылки во всей своей полноте).
Жидкие формы препаратов включают растворы, суспензии и эмульсии. Обычные жидкие формы препаратов включают водные растворы и растворы в смеси воды с пропиленгликолем для парентеральных инъекции или добавления подсластителей и агентов, заглушающих вкус, для растворов, суспензий и эмульсий для перорального применения. Жидкие формы препаратов могут также включать растворы для интраназального назначения.
Аэрозольные препараты, пригодные для ингаляции, включают растворы и твердые частицы в форме порошка, которые могут быть объединены с фармацевтически приемлемым носителем, таким как сжатый инертный газ (например, азот).
Также включают твердые формы препаратов, которые могут быть превращены за короткое время перед использованием в жидкие формы препаратов для приема либо перорально, либо парентерально. Такие жидкие формы включают растворы, суспензии и эмульсии.
Соединения в соответствии с изобретением также могут быть доставлены через кожу. Трансдермальные композиции могут иметь форму кремов, лосьонов, аэрозолей и эмульсий и могут быть включены в трансдермальный пластырь типа матрицы или резервуара, который является обычным в работе для этой цели.
Предпочтительным способом назначения соединений в соответствии с изобретением является пероральный. Предпочтительно фармацевтический препарат находится в единичной форме дозировки. В такой форме препарат подразделяется на подходящие по размерам единицы дозировки, содержащие подходящие количества активного компонента, например, эффективное количество для достижения желаемой цели.
Количество активного ингредиента (соединения) в единичной дозе препарата может быть изменено или отрегулировано приблизительно от 0,01 до 4,000 мг, предпочтительно приблизительно от 0,02 до 1,000 мг, более предпочтительно приблизительно от 0,3 до 500 мг и наиболее предпочтительно приблизительно от 0,04 до 250 мг, в соответствии со специфическим применением. Типичные рекомендуемые ежедневные режимы дозировки для перорального назначения могут находиться в интервале приблизительно от 0,02 до 2,000 мг/день, поделенные на от двух до четырех доз. Для удобства полная ежедневная доза может быть разделена и назначена частями в течение дня, как требуется. Как правило, фармацевтические композиции в соответствии с изобретением будут назначаться приблизительно от 1 до 5 раз в день или, в ином случае, как непрерывное вливание. Такое назначение может быть использовано в терапии как хронических, так и острых заболеваний. Количество активного ингредиента, которое может быть объединено с материалами носителя, чтобы получить единичную форму дозировки, будет варьироваться в зависимости от подвергаемого лечению пациента и специфического способа назначения. Типичный препарат будет содержать приблизительно от 5 до 95% (по массе) активного соединения. Предпочтительно такие препараты будут содержать приблизительно от 20 до 80% по массе активного соединения.
Фармацевтически приемлемые носители, используемые в сочетании с соединениями настоящего изобретения, используют в концентрации, достаточной, чтобы обеспечить практически приемлемый размер в отношении дозировки. Фармацевтически приемлемые носители в сумме могут составлять приблизительно от 0,1 до 99,9% по массе от фармацевтических композиций в соответствии с изобретением, предпочтительно приблизительно от 20 до 80% по массе.
Для улучшения состояния пациента может быть назначена, если необходимо, поддерживающая доза соединения, композиции или сочетания в соответствии с изобретением. Впоследствии дозировка или частота назначения, или обе, могут быть снижены, в зависимости от симптоматики, до уровня, при котором улучшенное состояние сохраняется. Когда симптоматика снижается до желательного уровня, лечение должно прекращаться. Пациентам может, однако, требоваться лечение с перерывами на долговременной основе на случай повторения симптомов болезни.
Специфическая дозировка и режимы лечения для любого специфического пациента могут варьироваться и будут зависеть от множества факторов, включая активность используемого специфического соединения, возраст, вес тела, общее состояние здоровья, пол и диету пациента, время приема, скорость выделения, специфическое сочетание лекарств, тяжесть случая и течение симптомов, требующих лечения, поведение пациента относительно состояния при лечении и мнение лечащего врача. Определение правильного режима дозировки для специфической ситуации находится в пределах квалификации специалиста. Количество и частота приема соединений в соответствии с изобретением или их фармацевтически приемлемых солей могут быть отрегулированы в соответствии с мнением ведущего клинициста, основанного на факторах, указанных выше. Как оценит квалифицированный специалист, могут требоваться более низкие или более высокие дозы, чем те, которые указаны выше.
Например, часто имеет место, что правильный уровень дозировки основан на весе пациента. Например, уровни дозировки между приблизительно 0,01 и 100 мг/кг веса тела в день, предпочтительно между приблизительно 0,5 и 75 мг/кг веса тела в день и более предпочтительно между приблизительно 1 и 50 мг/кг веса тела в день соединений, их солей и композиций в соответствии с изобретением, описанных здесь, являются терапевтически используемыми для лечения множества биологических расстройств, особенно мужских и женских сексуальных нарушений. Между двумя пациентами различного веса более высокая дозировка будет использована для более тяжелого пациента, при прочих равных условиях.
Соединения в соответствии с изобретением, как понимают, обеспечивают эффективное лечение нарушения эрекции (у мужчин), включая приемлемое время начала приема лекарства и приемлемую продолжительность после приема. Например, в лечении нарушения эрекции дозировка соединения в соответствии с изобретением может быть принята около часа перед тем, как будет предпринят половой акт. Специфические дозировки будут работать в пределах приблизительно тридцати минут после приема. Идеальные дозировки будут воздействовать на пациента в пределах приблизительно пятнадцати минут после приема. Хотя питание, диета, предшествующие состояния, алкоголь и других физиологические условия могут удлинять задержку действия препарата в соответствии с изобретением после его приема, понятно, что оптимальные дозировки в сочетании с сексуальным возбуждением будут приводить к эффективному лекарственному лечению в его ходе и на приемлемое количество времени.
Соединения в соответствии с изобретением могут существовать как в несольватированных, так и в сольватированных формах, включая гидратированные формы. Обычно сольватированные формы с фармацевтически приемлемыми растворителями, такими как вода, этиловый спирт и тому подобными, являются эквивалентными несольватированным формам для целей этого изобретения.
Соединения в соответствии с изобретением могут образовывать фармацевтически приемлемые соли с органическим и неорганическими кислотами.
Примерами подходящих кислот для образования солей являются соляная, серная, фосфорная, уксусная, лимонная, малоновая, салициловая, яблочная, фумаровая, янтарная, аскорбиновая, малеиновая, метансульфокислота и другие минеральные и карбоновые кислоты, хорошо известные специалистам. Соли получают взаимодействием форм свободного основания с достаточным количеством желаемой кислоты, чтобы получить соль обычным способом. Формы свободного основания могут быть регенерированы обработкой соли подходящим разбавленным водным раствором основания, таким как разбавленные водные растворы гидроокиси натрия, карбоната калия, аммиака или бикарбоната натрия. Формы свободных оснований могут несколько отличаться от соответствующих форм солей по некоторым физическим свойствам, таким как растворимость в полярных растворителях, но эти соли представляют собой иной эквивалент соответствующим формам их свободных оснований для целей этого изобретения.
Изобретение включает соединение, имеющее формулу (I) или (II), способ получения соединения в соответствии с изобретением, способ получения фармацевтической композиции из, по меньшей мере, одного соединения в соответствии с изобретением и, по меньшей мере, одного фармацевтически приемлемого носителя и способ использования одного или нескольких соединений в соответствии с изобретением для лечения различных расстройств, симптомов и заболеваний.
Соединения в соответствии с изобретением и их фармацевтически приемлемая соль и нейтральные композиции могут быть скомпонованы вместе с фармацевтически приемлемым носителем. Полученная композиция может быть назначена in vivo млекопитающим, таким мужчины или женщины, для лечения различных расстройств, симптомов и заболеваний. Например, соединения и композиции в соответствии с изобретением могут быть использованы для лечения заболеваний мочеполовой системы, особенно нарушения эрекции у мужчин (например, импотенции) и сексуальных расстройств у женщин. Нарушение эрекции у мужчины может быть определено как неспособность мужчины получить и/или поддерживать эрекцию, достаточную для полового сношения с партнершей. В лечении нарушения эрекции, как полагают, ингибиторы ФДЭ V формул (I) и (II) в соответствии с изобретением являются превосходными терапевтическими агентами, потому что они повышают уровни циклического гуанозинмонофосфата (цГМФ) в теле человека. Это воздействие облегчает релаксацию гладкой мускулатуры пещеристого тела, которая обеспечивает повышенный приток крови туда и приводит к эрекции. Это делает соединения в соответствии с изобретением особенно полезными для лечения импотенции и других типов заболеваний, на которые воздействуют уровни цГМФ.
Соответственно, другой аспект изобретения состоит в способе лечения нарушения эрекции у млекопитающих при необходимости такого лечения, включающем назначение млекопитающему, по меньшей мере, одного соединения, имеющего формулу (I) или (II), или его фармацевтической композиции в количестве, эффективном для улучшения и/или уменьшения одного или нескольких симптомов, связанных с нарушением эрекции, в достаточном количестве для того, чтобы млекопитающее могло совокупляться с другим млекопитающим.
Введенная в 1998 г. как первая пилюля для лечения импотенции Виагра® сегодня представляет собой наиболее часто предписываемый лекарственный препарат для лечения физиологически вызванного нарушения эрекции (НЭ). Некоторые пациенты, однако, могут испытывать нежелательные побочные эффекты при приеме Виагры®. Например, использование Виагры® противопоказано пациентам, которые используют органические нитраты либо регулярно, либо периодически, Physicians' Desk Reference®, 55th Ed, pp.2534-37 (2001). Сочетание Виагры® с нитратами может вызывать гипотензивное действие или внезапно понижать артериальное давление до опасных уровней, которые могут вызывать сердечный приступ. Там же. Соответственно, мужчины, кто имеет состояние сердца, которое требует использования нитратных лекарств, не должны использовать Виагру®. Там же. Также сообщалось, что Виагра® может оказывать побочный эффект на зрение, состоящий в ослабленном различении пациентом цветов (синего/зеленого), что вызывает световое зрительное отклонение «синее гало». Там же. Этот побочный эффект, по-видимому, обусловлен ингибированием изоэнзима ФДЭ VI (находящегося в сетчатке). Там же.
Преимущество соединений в соответствии с изобретением состоит в том, что они могут быть особенно избирательны в отношении изоэнзима ФДЭ V по сравнению с другими типами изоэнзимов ФДЭ, таких как изоэнзим ФДЭ VI. Полагают, что эта повышенная избирательность будет уменьшать побочные эффекты, связанные с использованием Виагры®. В частности, высокая избирательность соединений в соответствии с изобретением должна минимизировать и, может быть, даже предотвращать появление светового зрительного отклонения «синего гало». Полагают, что повышенная избирательность в отношении изоэнзима при ингибировании изоэнзима ФДЭ V (находящегося в пенисе) относительно изоэнзима ФДЭ VI (находящегося в сетчатке) объясняет устранение зрительного побочного эффекта «синее гало».
Кроме того, предложенное соединение в соответствии с изобретением не взаимодействуют неблагоприятным образом с нитратными лекарственными препаратами в организме крысы. Полагают, что такое же отсутствие неблагоприятного взаимодействия будет относиться ко всем соединениям в соответствии с изобретением у всех млекопитающих, включая людей. Неблагоприятная реакция с лекарственными нитратами может быть опасной и губительной. Неблагоприятные реакции включают любую реакцию, которая могла бы подвергать опасности или иным образом ограничивать физиологические функции организма. Более точно, в случае комбинированной терапии для пациента, включающей назначение пациенту нитратного донорного агента в сочетании с агентом ингибирования ФДЭ V, неблагоприятная нитратная реакция будет такой, при которой артериальное давление у пациента падает значительно больше, чем при любом средстве, назначаемом отдельно.
Эта особенность открывает способ лечения нарушения эрекции у многих пациентов, которые страдают как от нарушения эрекции, так и от сердечно-сосудистого или другого заболевания(ий), которые лечат нитратными донорными медикаментами. Пациенты, страдающие от двух или нескольких различных заболеваний, которые требуют двойного (или множественного) лечения, возможно, родились с одной или обеими болезнями или позже приобрели одну или обе болезни вследствие генетики или какого-то другого типа повреждения или заболевания, такого как нервное расстройство, повреждения спинного мозга, диабеты и тому подобное. Соответственно, другой вариант осуществления этого изобретения состоит в лечении пациента, страдающего от как (1) нарушения эрекции, так и (2), по меньшей мере, одного состояния, которое может быть излечено нитратным донорным лекарственным препаратом, причем лечение в соответствии с изобретением включает комбинированную терапию, включающую назначение млекопитающему, по меньшей мере, одного соединения в соответствии с изобретением или его фармацевтической композиции и, по меньшей мере, одного нитратного донорного соединение или его фармацевтической композиции. Пациент как страдающий от нарушения эрекции, так и испытывающий необходимость в нитратном донорном медикаменте, может быть излечен от обоих состояний последовательно, совместно и/или одновременно. Комбинированная терапия может быть предпринята отдельно в любой форме, предпочтительно путем перорального дозирования или через пластырь, или может быть скомпонована вместе в единую объединенную дозировку.
Соединения настоящего изобретения могут быть использованы по отдельности или в сочетании с другими агентами, в особенности с другими типами ингибиторов ФДЭ (особенно ингибиторов цГМФ ФДЭ V), простаноидами, α-адренегическими рецепторами, агонистами рецепторов допамина, агонистами рецепторов меланокортина, антагонистами рецепторов эндотелина, ингибиторами ферментов преобразования эндотелина, антагонистами рецепторов ангиотензина II, ингибиторами фермента преобразования ангиотензина, ингибиторами нейтральной металлоэндопептидазы, ингибиторами ренина, агонистами рецепторов серотонина 5-НТ2с, агонистами рецепторов ноцицептина, ингибиторами киназы ро, модуляторами каналов калия и ингибиторами протеина 5 мультилекарственной устойчивости.
Примеры терапевтических агентов, которые могут быть использованы в сочетании с соединениями в соответствии с изобретением, представляют собой следующие: ингибиторы ФДЭ V, такие как силденафилцитрат (Виагра®, Pfizer, Коннектикут, Соединенные Штаты), Vardenafil™ (Bayer, Германия) и IC-351 (Cialis™, Lilly-ICOS, Вашингтон и Индиана, Соединенные Штаты); простаноиды, такие как простагландин E1; α-адренегические агонисты, такие как мезилат фентоламина; агонисты рецепторов допамина, такие как апоморфин; антагонисты ангиотензина II, такие как лосартан, ирбесартан, валсартан и кандесартан, и антагонисты ЕТА, такие как босентан и АВТ-627.
Понятно, что можно взять другие сочетания, оставаясь при этом в пределах сферы изобретения. Хотя одно или несколько соединений в соответствии с изобретением может быть использовано в применении монотерапии для лечения нарушения эрекции, они также могут быть использованы в комбинированной терапии, в которой соединения в соответствии с изобретением сочетают с одним или несколькими другими фармацевтическими соединениями, которые являются полезными для лечения нарушения эрекции и/или других типов расстройств, симптомов и заболеваний.
Как обсуждалось выше, вследствие их активности в ингибировании цГМФ-ФДЭ V соединения в соответствии с изобретением полезны для лечения урологических расстройств, в особенности женских и мужских сексуальных нарушений. Течение других физиологических расстройств, симптомов и заболеваний также может улучшаться от ингибирования цГМФ-ФДЭ V. Более точно, соединения в соответствии с изобретением, их соли и производные могут быть использованы для лечения сердечно-сосудистых и церебрально-васкулярных заболеваний, стенокардии, гипертонии, рестеноза после ангио-пластики, эндартерэктомии, введения стента, заболеваний периферийных сосудов, мозгового инсульта, расстройств дыхательных путей, таких как обратимая заложенность дыхательных путей, хронические астма и бронхиты, аллергических нарушений, связанных с атопией, таких как крапивница, экзема и риниты, легочной гипертонии, ишемических болезней сердца, ухудшенной переносимости глюкозы, диабета и связанных с ним осложнений, синдрома резистентности к инсулину, гипергликемии, синдрома поликистоза яичника, заболеваний почечных клубочков, почечной недостаточности, нефритов, трубчатого коллагеноза, автоиммунных заболеваний, глаукомы, нарушений моторики кишечника, кахексии и рака.
Другой аспект этого изобретения состоит в том, чтобы обеспечить набор, включающий отдельные составные части в едином пакете, где фармацевтические соединения в соответствии с изобретением, их композиции и/или соли используют в сочетании с фармацевтически приемлемыми носителями для лечения расстройств, симптомов и заболеваний, где играет роль ингибирование цГМФ-ФДЭ V.
Вышеприведенное описание не предназначено, чтобы детализировать все модификации и варианты изобретения. Квалифицированными специалистами будет оценено, что могут быть сделаны изменения к вариантам осуществления изобретения, описанным выше, без отхода от концепции изобретения. Следовательно, понятно, что изобретение не ограничивается специфическими вариантами осуществления, описанными выше, но предназначено, чтобы охватить модификации, которые находятся в пределах духа и сферы изобретения, как определено на языке следующих пунктов формулы изобретения.
Данные, показывающие лечение дисфункции эрекции
Наркотизированных мужских дворняжек подвергали электрической стимуляции тазового нерва с получением частотно-зависимого (1-16 Гц) быстрого усиления тока крови внутри срамной артерии (в 10-15 раз) и, после короткого латентного периода, усиления давления в пещеристом теле (ДПТ). Усиление ДПТ при 16 Гц составляло около 90% среднего давления крови (СДК) и было квалифицировано как полная эрекция. В течение 2 мин до стимуляции внутривенной инъекцией вводили соединение №114 в количестве 10, 30 и 100 мкг/кг. Введение указанного соединения не имело никакого влияния на базальное давление в пещеристом теле, а потенцировало усиление ДПТ, достигаемое при электрической стимуляции. Полученные данные по усилению ДПТ (в % в расчете на СДК) отражены на графике.
Из вышеприведенных данных однозначно вытекает действие предлагаемых соединений формулы (I) против дисфункции эрекции in vivo.
Кроме того, заявитель представляет следующие примеры возможных препаратов предлагаемой фармацевтической композиции.
Данные препараты получают обычным в конфеционировании фармацевтических препаратов методом.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВОЕ БИЦИКЛИЧЕСКОЕ ГЕТЕРОЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ | 2009 |
|
RU2518073C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ БЕНЗИМИДАЗОЛА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2004 |
|
RU2369601C2 |
| ПРОИЗВОДНЫЕ ЭФИРА ГЕТЕРОАРИЛКАРБОНОВОЙ КИСЛОТЫ | 2013 |
|
RU2664544C2 |
| ПРОИЗВОДНЫЕ 1-ТИО-D-ГЛЮЦИТОЛА | 2006 |
|
RU2387649C2 |
| АЦИЛИРОВАННЫЕ ГЕТЕРОАЛИЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ, ЛЕКАРСТВЕННОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ СЕЛЕКТИВНОЙ АНТАГОНИСТИЧЕСКОЙ АКТИВНОСТЬЮ ПРОТИВ NK-РЕЦЕПТОРОВ, СПОСОБ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЯ | 1998 |
|
RU2174122C1 |
| НОВЫЕ ЗАМЕЩЕННЫЕ СУЛЬФАМАТНЫЕ ПРОТИВОСУДОРОЖНЫЕ ПРОИЗВОДНЫЕ | 2003 |
|
RU2328502C2 |
| ПРОИЗВОДНЫЕ 3-ГИДРОКСИ-2-ПИРИДОНА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2003 |
|
RU2311410C2 |
| НИЗКОМОЛЕКУЛЯРНЫЕ МОДУЛЯТОРЫ ПАНТОТЕНАТКИНАЗ | 2018 |
|
RU2797123C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ЭТИЛЕНДИАМИНА, ИМЕЮЩИХ ГАЛОГЕНИРОВАННУЮ КАРБАМАТНУЮ ГРУППУ И АЦИЛЬНУЮ ГРУППУ, И ПРОМЕЖУТОЧНЫХ ВЕЩЕСТВ ДЛЯ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ | 2007 |
|
RU2404963C2 |
| ПРОИЗВОДНЫЕ 4-АМИНОМЕТИЛБЕНЗОЙНОЙ КИСЛОТЫ | 2014 |
|
RU2673245C2 |

Изобретение относится к новым соединениям формулы (I), обладающим свойствами полициклического ингибитора ксантин фосфодиэстеразы (ФДЭ) V, способу их получения, а также к фармацевтической композиции на основе новых соединений и применению соединений для лечения различных расстройств, симптомов или заболеваний, опосредствованных действием ФДЭ V, в частности для лечения дисфункции эрекции. В соединениях формулы (I)
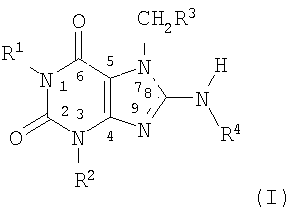
R1 и R2, независимо от друг друга, каждый представляет собой алкильную группу с 1-15 атомами углерода, разветвленную или с нормальной цепью, с одним или несколькими заместителями, выбранными из гидрокси, амино, алкиламино или диалкиламино с 1-4 атомами или O-Si(алкил)3 с 1-4 атомами углерода в алкильной части, либо без них, бензильную группу, с одним или несколькими заместителями в фенильном кольце, выбранным из O-алкила с 1-4 атомами углерода, либо без них, R3 представляет собой фенильную группу с одним или несколькими заместителями, либо без них, 6-членную азотсодержащую гетероарильную группу с одним или несколькими заместителями, либо без них, или 5-членную гетероциклическую группу, имеющую от 1 до 2 гетероатомов, выбранных из кислорода, конденсированную с фенильным кольцом, с одним или несколькими заместителями, либо без них, R4 представляет собой циклоалкильную группу с 3-15 атомами углерода с одним или несколькими заместителями, либо без них, циклоалкенильную группу с 3-15 атомами углерода с одним или несколькими заместителями, либо без них, или гетероциклоалкильную группу с от 3 до 8 членов, или ее S-оксиды, с одним или несколькими заместителями, либо без них, или инданильную группу, где один или несколько заместителей для всех групп R3 и R4 представляют собой, независимо друг от друга, каждый группу: алкил с 1-4 атомами углерода, фенил, 6-членный азотсодержащий гетероарил, гидроксиалкил с 1-4 атомами углерода, алкилтиоалкил с 1-4 атомами углерода в каждой алкильной группе, карбоксиалкил с 1-4 атомами углерода, моно-, ди- и тригалогеналкил с 1-4 атомами углерода, моно-, ди- и тригалогеналкокси с 1-4 атомами углерода, алкокси с 1-4 атомами углерода, гидрокси, галоген, нитрогруппу, -COOR50, -SO0-2R50, -SO2NR50R51, -OCOR50, где R50 и R51 представляют собой, независимо друг от друга, каждый атом водорода и разветвленный или с нормальной цепью, необязательно, замещенный алкил с 1-6 атомами углерода. 7 н. и 28 з.п. ф-лы, 2 табл., 1 ил.
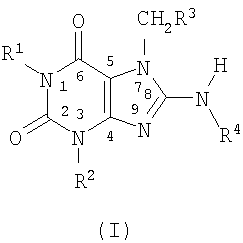
где (a) R1 и R2, независимо от друг друга, каждый представляет собой алкильную группу с 1-15 атомами углерода, разветвленную или с нормальной цепью, с одним или несколькими заместителями, выбранными из гидрокси, амино, алкиламино или диалкиламино с 1-4 атомами углерода или O-Si(алкил)3 с 1-4 атомами углерода в алкильной части, либо без них, бензильную группу, с одним или несколькими заместителями в фенильном кольце, выбранным из O-алкила с 1-4 атомами углерода, либо без них,
(б) R3 представляет собой фенильную группу с одним или несколькими заместителями, либо без них, 6-членную азотсодержащую гетероарильную группу с одним или несколькими заместителями, либо без них или 5-членную гетероциклическую группу, имеющую от 1 до 2 гетероатомов, выбранных из кислорода, конденсированную с фенильным кольцом, с одним или несколькими заместителями, либо без них,
при условии, что R3 не является арильной группой, замещенной в пара-положении группой -Y-арил, где Y представляет собой одинарную углерод-углеродную связь,
(в) R представляет собой циклоалкильную группу с 3-15 атомами углерода с одним или несколькими заместителями, либо без них, циклоалкснильную группу с 3-15 атомами углерода с одним или несколькими заместителями, либо без них или гетероциклоалкильную группу с от 3 до 8 членами, или ее S-оксиды, с одним или несколькими заместителями, либо без них, или инданильную группу;
где один или несколько заместителей для всех групп R3 и R4 представляют собой, независимо друг от друга, каждый группу: алкил с 1-4 атомами углерода, фенил, 6-членный азотсодержащий гетероарил, гидроксиалкил с 1-4 атомами углерода, алкилтиоалкил, с 1-4 атомами углерода в каждой алкильной группе, карбоксиалкил с 1-4 атомами углерода, моно-, ди- и тригалогеналкил с 1-4 атомами углерода, моно-, ди- и тригалогеналкокси с 1-4 атомами углерода, алкокси с 1-4 атомами углерода, гидрокси, галоген, нитрогруппу, -COOR50, -SO0-2R50, -SO2NR50R51, -OCOR50,
где R50 и R51 представляют собой независимо друг от друга каждый атом водорода и разветвленный или с нормальной цепью, необязательно, замещенный алкил с 1-6 атомами углерода.
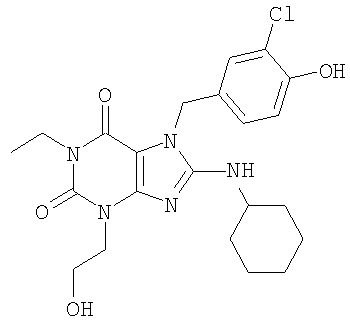

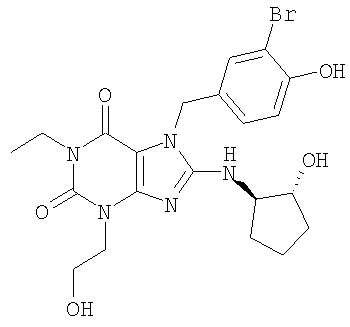
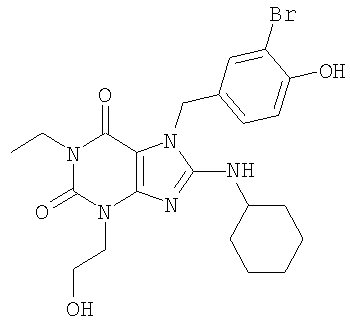

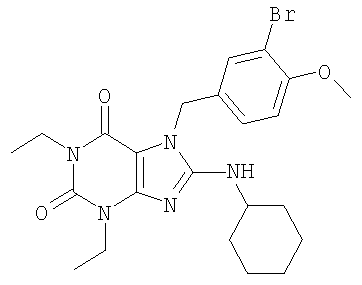
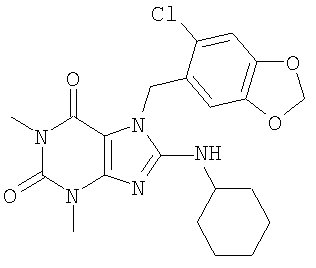

 или
или 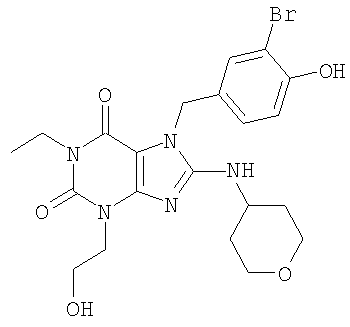

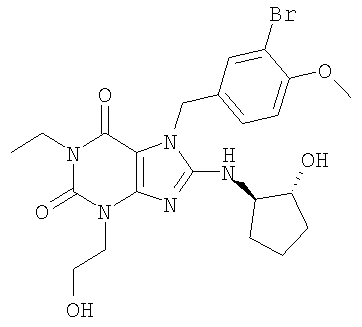




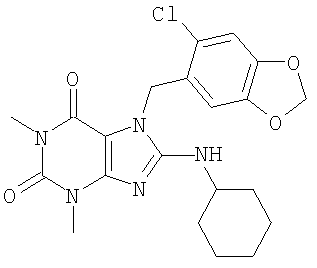

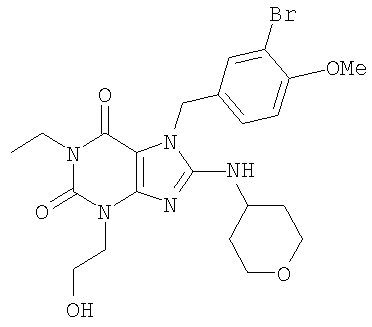

R4 представляет собой
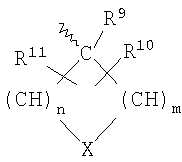
где R9 представляет собой атом водорода или, необязательно, замещенную карбоксиалкильную группу с 1-4 атомами углерода, -СООН, сложноэфирную группу с
С1-С6-алкильной группой, алкильную группу с 1-4 атомами углерода,
гидроксиалкильную группу с 1-4 атомами углерода, фенильную или 6-членную азотсодержащую гетероарильную группу;
R10 и R11 представляют собой заместители на одном и том же или различных атомах углерода кольца и, независимо друг от друга, каждый представляет собой:
(а) значения, определенные выше, как для R9;
(б) гидроксильную группу или сложноэфирную группу, полученную из гидроксильной группы с карбоновой кислотой С1-6; или
(в) алкоксигруппу с 1-4 атомами углерода, алкил- С1-6-ациламино-, или алкил-C1-6-сульфониламиногруппу, с одним или несколькими заместителями, либо без них, m и n, независимо друг от друга, каждая составляет от 1 до 3;
Х представляет собой -C(R10R11)-, -S(O)Y-, -O-, где R10 и R11 определены выше;
у представляет от 0 до 2;
где возможные заместители имеют значения, указанные в п.1.
(1) реакцию соединения, имеющего формулу (III)

где R1 имеет значения, указанные в п.1, и
Ph представляет собой фенильную группу;
с алкилгалогенидом в присутствии основания с получением соединения, имеющего формулу (IV)

где R1 и Ph имеют вышеуказанные значения, а
L представляет собой R2 или защищенную форму R2, причем R2 имеет значения, указанные в п.1;
(2) дебензилирование и затем алкилирование соединения, имеющего формулу (IV), алкилгалогенидом, имеющим формулу XCH2R3, где Х представляет собой атом галогена и R3 имеет значения, указанные в п.1;
с образованием соединения, имеющего формулу (V)

где R1, R3 и L имеют вышеуказанные значения, и
(3) депротонирование и затем галогенирование соединения, имеющего формулу (V), с образованием соединения, имеющего формулу (VI)
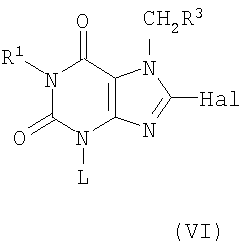
где Hal представляет собой атом галогена, a R1, R3 и L имеют вышеуказанные значения;
(4) реакцию соединения, имеющего формулу (VI) с амином, имеющим формулу R4NH2, где R4 имеет значения, указанные в п.1;
с образованием соединения, имеющего формулу (VII)

где R1,R3,R4 и L имеют вышеуказанные значения,
(5) удаление защитной части группы L, когда L представляет собой защищенную форму R2 в соединении, имеющем формулу (VII), с образованием соединения, имеющего формулу (I)
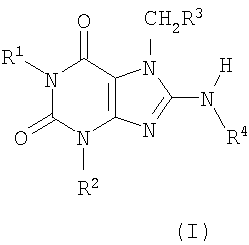
где R2 имеет те же значения, что и R1, a R1, R3 и R4 имеют вышеуказанные значения.
34 Способ повышения уровня цГМФ, включающий введение пациенту эффективного количества соединения по п.1 или фармацевтической композиции по п.30.
| ПРОИЗВОДНЫЕ КСАНТИНА И ИХ ФАРМАКОЛОГИЧЕСКИ ПЕРЕНОСИМЫЕ СОЛИ | 1993 |
|
RU2138500C1 |
| Автоматический огнетушитель | 0 |
|
SU92A1 |
| Автоматический огнетушитель | 0 |
|
SU92A1 |
| US 5409934 A, 25.04.1995 | |||
| 0 |
|
SU389282A1 | |
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| Экономайзер | 0 |
|
SU94A1 |
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ТАКСАНА И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ПРИ ИХ ПОЛУЧЕНИИ | 1993 |
|
RU2116302C1 |
| РОМАНЕНКО Н.И | |||
| и др | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
Авторы
Даты
2007-07-10—Публикация
2001-09-17—Подача