Содержащие никотин трансдермальные терапевтические системы (ТТС) известны как на рынке сбыта, так и из многочисленных описаний изобретений к патентам. Например, можно назвать европейские заявки на патент ЕР-А 708 627, ЕР-А 366 240 и ЕР-А 720 474, патент США US-A 5 364 630, международные патенты WO 95/24172, WO 94/04109, WO 00/33812 и WO 88/01516. Кроме того, в этой связи следует упомянуть ТТС-продукцию, занимающую в настоящее время ведущее место на рынке сбыта, в частности Nicotinell® (выпускается в США под торговой маркой Habitrol®), Nicorette® (выпускается в США под торговой маркой Nicotrol®), а также Nicoderm®.
Разработка содержащих никотин ТТС определяется, главным образом, двумя следующими проблемами:
1. Никотин является легколетучим соединением, что осложняет осуществление способов получения ТТС, включающих технологическую стадию сушки, которая может оказаться вообще невозможной.
2. Никотин является активным пластификатором и растворителем наиболее типичных полимеров и полимерных пленочных материалов, используемых для получения ТТС.
Решение первой проблемы привело к разработке способов, не требующих сушки содержащих никотин материалов, благодаря чему удается избежать испарения или улетучивания этого соединения.
Результатом решения второй проблемы явилось использование для получения ТТС многократно описанных полимеров и полимерных пленочных материалов, обладающих особенно высокой устойчивостью по отношению к никотину. Это относится не только к рецептурам контактных клеев, защитных слоев и обратных слоев, но и к материалам, используемым для первичной упаковки этих систем.
Однако любое из найденных до сих пор технических решений указанных выше проблем связано с необходимостью идти на уступки, касающиеся как комплексной структуры ТТС, так и, в особенности, чрезмерно большой толщины некоторой части ТТС.
Чтобы избежать нанесения покрытий и сушки, были описаны способы, предусматривающие частичное или полное запечатывание поверхности ТТС или отдельных ее слоев, однако использование таких способов требует введения в состав ТТС впитывающего слоя, состоящего из нетканых материалов или бумаги. Наряду с этими способами возможно дозирование никотина, находящегося в системе соответствующих резервуаров в жидком или концентрированном состоянии. Однако изготовление таких систем сопряжено со значительными расходами, зачастую они обладают значительной толщиной и выглядят мало привлекательными. Кроме того, могут быть реализованы способы горячего плавления, благодаря чему использование растворителей и сушка становятся излишними. Однако иногда при этом возникают серьезные проблемы, связанные с выбором подходящих полимеров и вспомогательных веществ. Пластифицирующие свойства никотина являются причиной затруднений, возникающих, в частности, при использовании контактных клеев из акрилатов, поскольку такие клеи даже в чистом состоянии (без добавок) обладают пониженной температурой стеклования, что является причиной их способности к самопроизвольному приклеиванию к коже человека. В связи с этим такие клеи даже при пониженной концентрации никотина обладают мягкой, приближающейся к критическому уровню консистенцией, что является причиной их размазывания, вытягивания полимерных нитей и, вообще, неудовлетворительной способности нанесения слоя контактного клея, осуществляемого машинным или ручным способом.
В связи с вышеизложенным использование в составе терапевтических систем контактных клеев из акрилатов до последнего времени почти всегда вынуждало создавать многослойные, обладающие значительной толщиной системы, способные поглощать никотин лишь в относительно низких концентрациях. Несмотря на то, что из группы акрилатов могут быть выбраны и высокомолекулярные полимеры, которые благодаря высокой молекулярной массе обладают повышенной устойчивостью по отношению к пластифицирующим веществам, в частности никотину, такие акрилаты могут быть переработаны только способом горячего плавления. Однако выбор акрилатов указанного типа, пригодных для использования в фармацевтических целях, в отличие от контактных клеев на основе растворителей чрезвычайно ограничен. В связи с этим до последнего времени предлагались многочисленные системы на основе других полимерных материалов, менее чувствительных по отношению к никотину, например углеводородных полимеров, в частности полиизобутиленов или полибутиленов, а также блок-сополимеров стирола с изопреном или бутадиеном.
Кроме того, в состав ТТС предлагалось вводить силиконовые полимеры, которые, вне всякого сомнения, являются наиболее дорогими из доступных полимерных материалов. Наконец, поставляемые на рынок сбыта ТТС при одинаковом показателе выделения активного вещества обладают сильно различающимися размерами, что, наряду с прочими факторами, обусловлено различной устойчивостью таких систем по отношению к содержащемуся в них никотину.
В общем случае справедливо условие, согласно которому устойчивые по отношению к никотину полимеры должны обладать относительно высокой молекулярной массой и/или относительно высокой температурой стеклования, если речь идет об их использовании для получения контактных клеев. Среди высокомолекулярных полимеров, наиболее часто используемых для получения контактных клеев ТТС, данному условию в наименьшей степени удовлетворяют акрилаты, предназначенные для переработки с использованием растворителей.
Обобщая вышеизложенное, можно утверждать, что по указанным выше причинам поставляемая в настоящее время на рынок сбыта, содержащая никотин ТТС-продукция по сравнению с обычными матричными системами, в состав которых входят иные активные вещества, например эстроген, обладает весьма значительной толщиной и высокой жесткостью, что существенно снижает удобство ее использования потребителями, если площадь поверхности изделий составляет от 20 до 30 см2.
Задача настоящего изобретения состояла в том, чтобы создать тонкую, содержащую никотин и обладающую высокой гибкостью ТТС, которая по сравнению с обычными содержащими никотин системами обладает гораздо лучшей носкостью. Наряду с этим конструкция создаваемой системы должна быть как можно более простой, и ее можно получать путем нанесения содержащего растворитель покрытия.
Согласно настоящему изобретению указанную задачу решают благодаря трансдермальной терапевтической системе, содержащей никотин и, при необходимости, оказывающие воздействие на центральную нервную систему дополнительные активные и/или вспомогательные вещества, состоящей из обратного слоя (1), непроницаемого для никотина, прочих активных и вспомогательных веществ и предпочтительно водяного пара; содержащего никотин промежуточного слоя матрицы (2), непосредственно примыкающего к обратному слою; содержащего никотин дополнительного слоя матрицы (3) и способной к повторяемому отслаиванию защитной пленки (4), отличающейся тем, что все слои матрицы образованы сополимерами (мет)акрилата, способными к переработке с использованием растворителя, причем общая толщина указанных слоев (то есть только слоев матрицы в совокупности с обратным слоем (1) без защитной пленки (4)) не превышает 250 мкм. Таким образом, трансдермальные терапевтические системы согласно изобретению состоят только из сополимеров (мет)акрилата, способных к переработке с использованием растворителя, без необходимости добавления состоящих из чужеродных полимеров усиливающих слоев или опорных элементов, образованных, в частности, бумагой и нетканым материалом.
При этом под сополимерами (мет)акрилата подразумевают сополимеры акрилатов и/или метакрилатов, то есть сложные алкиловые эфиры, у которых алкильные остатки содержат предпочтительно 1-8, наиболее предпочтительно 1-6, в частности 1-4 атомов углерода. Такие сополимеры могут быть получены также при дополнительном использовании винилацетата, акриловой и/или метакриловой кислоты. Под "способностью к переработке с использованием растворителя" подразумевается, что сополимеры (мет)акрилата могут до такой степени растворяться или набухать в органических растворителях, что их можно без каких-либо проблем наносить на поверхность путем выливания. Молекулярная масса обладающих этим свойством сополимеров (мет)акрилата предпочтительно не превышает 400 кДа, однако однозначная констатация предельной величины молекулярной массы в данном случае не представляется возможной, поскольку на растворимость сополимеров (мет)акрилата может оказывать влияние, например, добавление некоторых вспомогательных веществ.
В состав трансдермальной терапевтической системы согласно изобретению предпочтительно вводят такое количество никотина, чтобы на см2 используемой поверхности ТТС приходилось, по меньшей мере, 1,5 мг никотина. В соответствии с предпочтительным вариантом осуществления настоящего изобретения систему конструируют таким образом, чтобы в течение 24 часов, предпочтительно в течение 16 часов, она выделяла от 0,7 до 1,4 мг, предпочтительно от 1,0 до 1,4 мг, никотина на см2 кожи.
Основой содержащего никотин промежуточного слоя матрицы (2) является полимер из группы сополимеров (мет)акрилата, предпочтительно сополимер бутилметакрилата, 2-диметиламиноэтилметакрилата и метилметакрилата, в частности, содержащий эти мономерные звенья в мольном соотношении 1:2:1, или сополимер бутилметакрилата и метилметакрилата.
Под содержащим никотин слоем матрицы (3) подразумевают клеящий слой, то есть самоприклеивающийся к коже слой. Основой клеящего слоя предпочтительно являются сополимеры акрилатов, которые содержат неэтерифицированные карбоксильные группы, представляющие собой остатки акриловой или метакриловой кислоты. Такие сополимеры характеризуются кислотным числом от 20 до 100 мг КОН на 1 г полимера и могут быть полностью или частично нейтрализованы путем введения одного или нескольких дополнительных оснований. Сополимеры указанного типа обладают особенно высокой устойчивостью по отношению к пластификаторам и при предпочтительно осуществляемой частичной нейтрализации карбоксильных групп характеризуются чрезвычайно высокой способностью выделять свободный никотин. Трансдермальные терапевтические системы согласно изобретению могут обладать поразительно малой толщиной и высокой гибкостью даже по сравнению с конкурентоспособной продукцией аналогичной толщины. Неожиданно оказалось, что благодаря настоящему изобретению впервые представилась возможность получать содержащие никотин терапевтические системы, обладающие небольшой толщиной в сочетании с высокой гибкостью: предел их прочности при изгибе не превышает 2 сН × см2.
В качестве дополнительных веществ к содержащим карбоксильные группы сополимерам акрилатов добавляют, например, гидроксиды щелочных металлов, предпочтительно гидроксид калия, или щелочные полимеры, предпочтительно упомянутый выше сополимер бутилметакрилата с 2-диметиламино-этилметакрилатом и метилметакрилатом. В соответствии с особенно предпочтительным вариантом исполнения настоящего изобретения содержащий карбоксильные группы сополимер акрилатов подвергают структурированию ионами алюминия или титана.
Предпочтительно, если ТТС согласно настоящему изобретению содержит также, по меньшей мере, одно связывающее влагу вспомогательное вещество. Таким вспомогательным веществом предпочтительно является содержащий карбоксильные группы полимер или его фармацевтически приемлемая соль. Речь при этом предпочтительно идет о вспомогательном веществе из группы структурированных поперечными связями натриевых или кальциевых солей карбоксиметилцеллюлозы или полиакриловой кислоты, причем предпочтительно, если находящееся в порошкообразном состоянии вспомогательное вещество диспергируют в одном или нескольких слоях матрицы. Содержание связывающего влагу компонента в матрице в общем случае составляет от 1 до 10% (мас./мас.), предпочтительно от 2 до 4% (мас./мас.).
В качестве дополнительных активных и/или вспомогательных веществ, оказывающих воздействие на центральную нервную систему, могут использоваться описанные ранее продукты согласно уровню техники, вводимые в состав трансдермальных терапевтических систем в сочетании с никотином, например средства, обеспечивающие стабилизацию систем, в частности обычные антиоксиданты, предпочтительно витамин Е и аскорбилпальмитат.
Под гибкостью следует понимать способность изделий плоской формы, изгибаясь, принимать характерную для неровной поверхности конфигурацию. Практически на всех участках тела кожа человека обладает неровной конфигурацией, тем более если учесть ее постоянное изменение при движении тела. Методы и результаты сравнительных испытаний, касающихся гибкости ТТС, описываются ниже. Из них следует однозначный вывод, что низкая жесткость, то есть предел прочности при изгибе, не превышающий 2 сН × см2, обусловлен не только малой толщиной ТТС, но также и особенно высокой гибкостью структуры слоев (композиции матрицы). Высокой гибкости ТТС согласно изобретению способствует то обстоятельство, что в ее составе отсутствуют специальные, содержащие активные вещества резервуары, опорные элементы или иные усиливающие элементы, а также распределительные мембраны.
Вместе с тем ТТС нового типа по сравнению с аналогичной поставляемой в настоящее время на рынок сбыта продукцией характеризуется, по меньшей мере, аналогичной или даже более высокой способностью выделять никотин на единицу площади в единицу времени, что подтверждают дополнительные, описанные ниже сравнительные исследования.
Использование никотина и, при необходимости, жидких вспомогательных веществ, как правило, означает повышенное содержание пластифицирующих компонентов в составе слоев соответствующей матрицы. В связи с этим для получения контактного(-ных) слоя(-ев) матрицы используют рецептуры, обладающие устойчивостью, в частности, по отношению к воздействию пластификаторов. Основой таких рецептур являются, например, структурированные катионами сополимеры акрилатов. Особенно пригодными являются частично нейтрализованные, содержащие карбоксильные группы сополимеры акрилатов, например, описанные в немецкой заявке на патент DE-A 199 18 106.
Конструкция типичной матричной системы согласно изобретению представлена на Фиг.1А. После предпочтительно пропускающего пары влаги обратного слоя (1) следует промежуточный слой матрицы (2), к которому примыкает слой контактного клея матрицы (3). Контактный клей (3) закрыт защитной пленкой (4), которую отслаивают перед использованием ТТС.
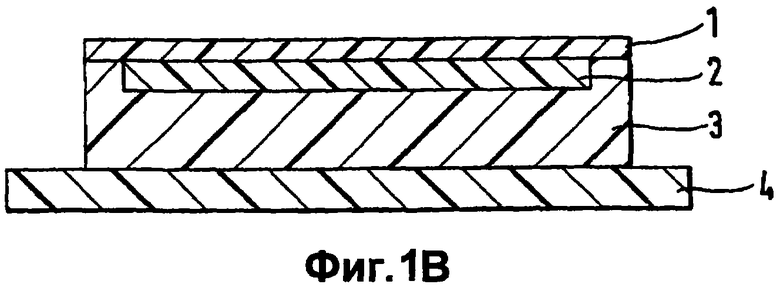
Кроме того, может оказаться целесообразной получаемая особым способом конструкция системы, изображенная на Фиг.1В. Обладающий неполной поверхностью промежуточный слой матрицы (2) получают, например, используя технику нанесения печатного оттиска. Непосредственно к краевым зонам обратного слоя (1) примыкает спой контактного клея матрицы (3), который выполняет функцию изолирующей внешней кромки расположенного внутри промежуточного слоя матрицы (2).
Полимеры, пригодные для загущения легколетучего компонента ТТС, описаны ранее в немецкой заявке на патент DE-A 43 32 094. Такие полимеры преимущественно не обладают клеящей способностью, поскольку в торговой сети могут быть приобретены лишь не полностью свободные от растворителя, обладающие клеящими свойствами полимеры, которые с большим трудом могут быть переведены в чистое состояние.
Согласно настоящему изобретению особенно пригодными для загущения оказались полимеры на основе метакриловой кислоты или их сложных эфиров. Типичные представители этой группы полимеров, например, продукты, выпускаемые под торговой маркой Eudragit®, в частности Eudragit® E, или полимер Plastoid® (оба продукта изготавливает фирма Rohm GmbH, Дармштадт, Германия), обладают лишь ограниченной способностью загущать раствор, что является желательным свойством, благодаря которому в начальный момент получения покрытия содержание полимера в растворе может быть относительно высоким, в общем случае составляя от 20 до 40% (мас./мас.). Благодаря этому в ходе установления равновесия при дальнейшем протекании процесса может быстро наступить затвердевание раствора, сопровождающееся образованием полимерной пленки, которая обладает достаточными толщиной и когезионной прочностью. Наряду с этим полиметакрилаты обладают хорошей способностью закрепляться на поверхности несущей подложки, состоящей из полиэтилентерефталата, который, с другой стороны, является предпочтительным материалом для использования в качестве обратного слоя.
При необходимости содержание активного вещества в используемом никотиновом растворе может быть уменьшено не только благодаря присутствию в нем полимера, но и путем добавления дополнительных вспомогательных веществ. Это может оказаться целесообразным для регулирования количества выделяемого никотина на единицу площади поверхности, а также надлежащей вязкости этого раствора, необходимой для нанесения покрытия. Кроме того, добавление вспомогательных веществ может способствовать повышению клеящей способности и адгезии между отдельными слоями композиции после установления в системе равновесия. Без каких-либо претензий на полноту информации примерами предпочтительно используемых дополнительных веществ могут служить триглицериды насыщенных жирных кислот (например, Miglyol® 812 фирмы Degussa, Германия, являющийся смешанным кислым триглицеридом фракционированных жирных кислот кокосового масла), моноглицериды жирных кислот (например, монолаурат или моноолеат глицерина), сложные эфиры, образованные метанолом, этанолом, изопропанолом или пропиленгликолем и жирными кислотами (например, изопропил-пальмитат), а также жесткие и эластичные смолы, являющиеся производными абиетиновой кислоты.
Предпочтительными пригодными для использования в качестве обратного слоя являются полимерные пленки, лишь в незначительной степени проницаемые для никотина. Такие пленки получают, в частности, из полиэтилентерефталата (например, полимера, выпускаемого фирмой Mitsubishi под торговой маркой Hostaphan®) или из термопластичных сополимеров акрилонитрила, полученных, например, путем привитой полимеризации 73-77 мас. частей акрилонитрила и 23-27 мас. частей метилакрилата в присутствии 8-18 мас. частей сополимера бутадиена с акрилонитрилом, содержащего 70% мас. бутадиеновых звеньев. Такие сополимеры поступают в продажу под названием Barex® (прежняя торговая марка фирмы Vistron Corp., Кливленд, Охио, США; нынешняя торговая марка - ВР) (смотри М. Th. Schuler, Kunstoffe-Plastics, 9/1974, Seiten 13-20). С учетом косметических требований эти пленки могут быть покрыты лаком. Для предохранения от воздействия света на содержащие никотин слои матрицы при необходимости может быть нанесено алюминиевое покрытие.
Сравнительные испытания гибкости
Чтобы объективно определить качество продукции, весьма легко оцениваемое потребителями, использовали видоизмененную методику измерения предела прочности полимерных пленок и текстильных изделий плоской формы при изгибе в соответствии со стандартом DIN 53-362 (способ с использованием кантилевера), осуществляя измерения посредством предусматриваемого указанным стандартом прибора фирмы Richard Hess MBV GmbH (47663 Sonsbeck, Германия). Для этого подвергаемый испытанию образец изделия в форме полоски свободно перемещали над кромкой камеры прибора. С увеличением длины свешивающейся под действием собственной массы части образца плоского изделия он изгибался и опускался вниз. Фиксировали длину свешивающейся части, при которой изгиб образца достигал заданного значения, составляющего 41°30', и в зависимости от собственной массы образца осуществляли расчет предела прочности при изгибе в [сН × см2].
В качестве образцов использовали вырезанные из готовой ТТС полоски, причем их длину в отличие от заданной в указанном выше стандарте (250 мм) были вынуждены уменьшить в связи с ограниченной длиной поступающей в торговлю ТТС-продукции (фактическая длина образцов составляла от 40 до 70 мм). Прежде чем приступить к измерениям, контактный слой освобождали от защитной пленки и в соответствии с предписаниями указанного выше стандарта припудривали тальком с целью устранения клеящей способности.
Результаты измерений (средние значения из двух определений), а также соответствующие длины образцов приведены в таблице 1. Предел прочности при изгибе каждого образца измеряли в двух направлениях: для первого измерения использовали образец, повернутый обратной стороной вверх, а для второго - образец, повернутый обратной стороной вниз, что было обусловлено тем обстоятельством, что прикрепленная к коже ТТС обычно должна обладать гибкостью в обоих из указанных направлений. Показатели содержащей никотин новой терапевтической системы согласно изобретению, полученной в соответствии с примером 1, сравнивали с тремя поставляемыми на рынок сбыта, содержащими никотин системами, а также с двумя поставляемыми на рынок сбыта изделиями, содержащими эстрадиол, высокая гибкость и удобство практического использования которых получили положительную оценку потребителей.
*) образец получали в соответствии с примером 1 (содержащая никотин система);
**) n.а. = измерение невозможно вследствие скручивания образца.
Содержащая никотин система ТТС А представляет собой изделие, выпускаемое фирмой Phannacia & Upjohn GmbH под торговой маркой Nicorette®. Содержащую никотин систему ТТС В поставляет на рынок сбыта под торговой маркой Nicoderm® CQ фирма SmithKline Beecham Consumer Healthcare L.P. (США), а содержащую никотин систему ТТС С под торговой маркой Nicotine Transdermal USP выпускает фирма Pharmaceutical Inc. (США). Содержащая эстрадиол система ТТС Е имеет торговое название Dermestril® и поставляется на рынок сбыта фирмой Rottaphamn s.r.l. (Монца, Италия), а поставщиком содержащей эстрадиол системы ТСС F, выпускаемой под торговым названием FemT®, является фирма Merck KGaA (Дармштадт, Германия).
Направление А означает, что измерение осуществляют, используя образец ТТС, повернутый обратной стороной вниз. Измерение в направлении В, напротив, осуществляют, используя повернутый обратной стороной вверх образец.
В связи с высокой жесткостью определенной части образцов в области доступных для измерения длин свешивающейся части не удалось достичь угла изгиба, равного 41°30'. В этих случаях исходили из того, что подлежащий измерению показатель превышает длину свешивающейся части образца, которая соответствовала бы критическому углу изгиба.
Для образца ТТС С обнаружена явная склонность к скручиванию или короблению, в связи с чем отсутствовала возможность измерения предела его прочности при изгибе в направлении А. Поэтому в таблице 1 приведены результаты измерения этого показателя образца ТТС С лишь в направлении В.
Анализ результатов измерений показывает, что содержащая никотин терапевтическая система согласно изобретению обладает значительно более низким пределом прочности при изгибе по сравнению с известными системами, также содержащими никотин. Неожиданным оказалось то обстоятельство, что показателям изгиба ТТС согласно изобретению соответствует диапазон, аналогичный характерному для обеих однослойных тонких матричных систем, содержащих в качестве активного вещества эстрадиол, которые в первом приближении можно считать наиболее гибкими терапевтическими системами, поставляемыми в настоящее время на рынок сбыта.
Неожиданным фактом явился также значительно более низкий предел прочности при изгибе содержащей никотин терапевтической системы согласно изобретению по сравнению с образцом ТТС А, также содержащим никотин, хотя данные системы лишь незначительно отличаются по толщине (толщина первой из указанных систем составляет около 218 мкм, второй около 238 мкм).
Пример 1
Из немецкой заявки на патент DE-A 43 32 094 известны продукты и способы, благодаря использованию которых возможно введение легколетучих, фармацевтических, активных или вспомогательных веществ в состав ТТС. С этой целью путем растворения полимера и, при необходимости, дополнительных твердых вспомогательных веществ в играющем роль растворителя легколетучем компоненте раствор загущают до такой степени, чтобы из него можно было получить покрытие на поверхности несущей подложки (технологическая стадия 1). На полученное таким способом покрытие могут быть нанесены дополнительные, отдельно изготовляемые слои ТТС, после чего благодаря диффузии может установиться равновесная концентрация легколетучего вещества в общей ТТС (технологическая стадия 2). Данный процесс сопровождается упрочнением слоя, до этого находящегося в жидком состоянии, реализуемого благодаря диффузии легколетучего компонента, используемого в остальных слоях системы в качестве единственного растворителя.
Полимерный раствор, предназначенный для осуществления технологической стадии 1, обладает приведенным в таблице 2 составом. Используя устройство для получения покрытий, этот раствор наносят на поверхность пленки полиэтилентерефталата, обладающей толщиной 19 мкм, получая покрытие массой 54 г/м2. Полученный продукт немедленно подвергают переработке, осуществляя технологическую стадию 2, состоящую в нанесении слоя контактного клея массой 144 г/м2, обладающего приведенным в таблице 3 составом. Полученный продукт в течение 10 минут нагревают при температуре 60°С, после чего наматывают в рулон. В заключение его сразу же или по истечении определенного периода промежуточного хранения подвергают обычной переработке, заключающейся в продольной резке или вырубке, получая конечную ТТС.
Клеевой слой, обладающий приведенным в таблице 3 составом, получали обычным используемым для нанесения покрытий способом, предусматривающим использование растворителя и последующую сушку полученного слоя. В качестве растворителя использовали смесь этилацетата, метанола и ацетилацетона. Клеевой слой наносили на силиконизированную защитную пленку из полиэтилентерефталата марки Hostaphan®, обладающую толщиной 100 мкм.
В качестве активного вещества полученная терапевтическая система содержит 1,75 г никотина на см2 используемой поверхности, что в точности соответствует содержанию никотина в известной системе ТТС D.
Толщина терапевтической системы согласно изобретению не превышает 218 мкм (без учета защитной пленки) и, следовательно, меньше, чем толщина упомянутых выше известных систем.
Сравнительные Фармакологические испытания
Сравнивали фармакологическую эффективность полученной в соответствии с примером 1, содержащей никотин ТТС согласно изобретению и содержащей никотин системы ТТС D (Nicotinell® фирмы Novartis Consumer Health Care S.A., Базель, Швейцария). Испытанию подвергали шесть обладающих нормальным здоровьем мужчин, которые поочередно применяли препарат согласно изобретению и сравнительный препарат (cross-over Design). Площадь под представленной на Фиг.2 кривой концентрации никотина в плазме при использовании содержащей никотин ТТС согласно изобретению по порядку величины составляет 140% от соответствующей площади используемого для сравнения образца ТТС. Этот результат согласуется со скоростью выделения свободного никотина, составляющей около 1 мг на см2 в течение 24 часов, по сравнению с соответствующим декларированным для системы ТТС D показателем, составляющим 0,7 мг на см2 в течение 24 часов.
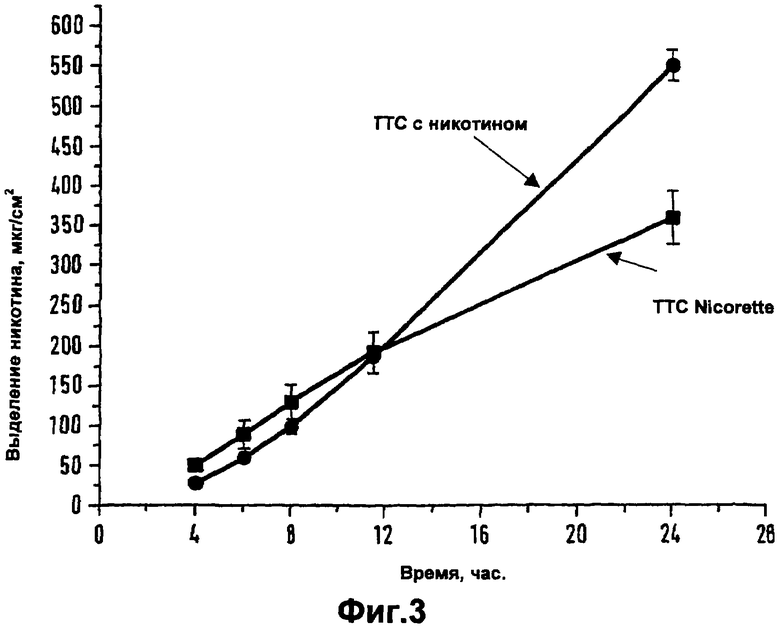
Кроме того, ТТС согласно изобретению сравнивали с содержащим никотин образцом ТТС A in vitro, измеряя проницаемость никотина через кожу человека в модифицированной диффузионной ячейке по Францу. Температура в сравнительном эксперименте составляла 32°С, в качестве акцепторной среды использовали водный буфер с рН 5,5. Полученные данные являются средними значениями из результатов исследования трех образцов кожи одного и того же донора, установленных с использованием образцов ТТС площадью 1,12 см2. Представленные на Фиг.3 результаты свидетельствуют о более высоком выделении никотина терапевтической системой согласно изобретению на см2 в течение 24 часов по сравнению с содержащими никотин образцами ТТС А.
Пример 2
В европейской заявке на патент ЕР-В 0 3030025 описан способ печати, посредством которого никотин может быть введен в состав отдельных терапевтических систем. Используя этот принцип, с помощью печатного устройства фирмы Tampoprint непосредственно на слой контактного клея, состав которого приведен в таблице 5, наносили обладающий круглой формой плоский печатный оттиск раствора активного вещества, состав которого приведен в таблице 4, при этом на слой контактного клея площадью около 6 см2 наносили около 25 мг содержащего никотин раствора. Масса слоя контактного клея, состав которого приведен в таблице 5, составляла 144 г/м2.
После нанесения печатного оттиска слой контактного клея сразу же накрывали пленкой из полиэтилентерефталата марки Hostaphan® толщиной 15 мкм, образующей обратную сторону получаемой терапевтической системы, и клеевой слой подвергали кашированию этой пленкой, осуществляемому механическим способом. Поверхность с нанесенным на нее печатным оттиском высекали из композиции, используя листовой штамп, диаметр которого примерно на 4 мм превышал диаметр запечатанной поверхности, что соответствовало разности соответствующих площадей, составляющей около 8 см2. В конечном итоге получали систему, аналогичную приведенной на Фиг.1В. В процессе хранения системы устанавливалось равновесное содержание никотина во всех входящих в ее состав слоях.
Клеевой слой, обладающий приведенным в таблице 5 составом, получали обычным способом из раствора и подвергали последующей сушке. В качестве растворителя использовали смесь этилацетата, метанола и ацетилацетона. Клеевой слой наносили на силиконизированную защитную пленку из полиэтилентерефталата марки Hostaphan®, обладающую толщиной 100 мкм.

Объектом настоящего изобретения является способ получения трансдермальной терапевтической системы, содержащей в качестве активного вещества никотин и обладающей особенно высокой гибкостью. Благодаря повышенной гибкости улучшается носкость системы, поскольку она обладает способностью легко изменять свою конфигурацию, которая всегда соответствует изменяющейся при движении тела конфигурации поверхности кожи. Оказалась гораздо более высокая гибкость содержащей никотин трансдермальной терапевтической системы по сравнению с аналогичными системами, занимающими сегодня ведущие позиции на рынке сбыта, хотя толщина, по меньшей мере, некоторых из этих систем сравнима с толщиной системы согласно изобретению. 6 з.п. ф-лы, 3 ил., 5 табл.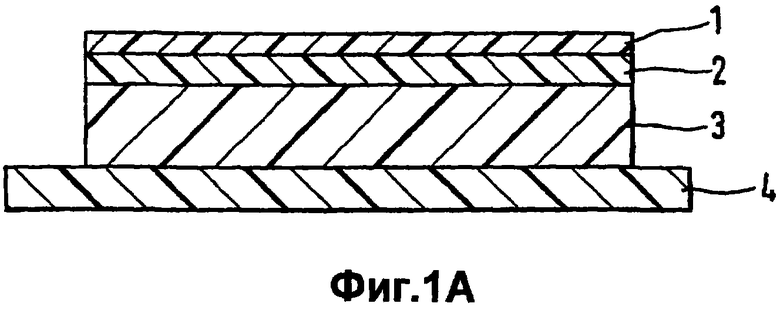
| US 5603947 А, 18.02.1997 | |||
| US 6139868 А, 31.10.2000 | |||
| RU 2052997 С1, 27.01.1996 | |||
| ПЛЕНКООБРАЗУЮЩАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ТРАНСДЕРМАЛЬНОГО ВВЕДЕНИЯ | 1996 |
|
RU2161957C2 |
Авторы
Даты
2007-07-20—Публикация
2002-02-19—Подача