Область техники, к которой относится изобретение
Настоящее изобретение относится к способам стимуляции и активации длительного естественного ответа иммунной системы, приводящего к повышению устойчивости организма и подавлению инфекционных агентов, включая вирусы, бактерии, грибы и паразиты, а также другие агенты, связанные с развитием иммунодефицита. Более конкретно, изобретение относится к схеме перемежающегося введения лекарственного средства для активации длительного повышенного уровня продукции Т-клеток (цитотоксичных Т-клеток).
Предпосылки создания изобретения
Иммунная система защищает организм от инфекционных агентов, включая бактерии, вирусы, грибы и паразиты. Кроме того, иммунная система выполняет функцию защиты от рака, а также от развития болезненных состояний, возникающих в результате нарушения баланса иммунной системы, условно-патогенных инфекций и аутоиммунных заболеваний (Penney, U.S. Patent 5980913). Стимуляция иммунной системы фармацевтическими средствами представляет собой важный подход в профилактике или лечении состояний, вызванных агентами, подавляющими иммунный ответ.
Реакция иммунной системы на иммуноген может быть подавлена вследствие развития ряда заболеваний или патологических состояний. Так, например, у пациентов, инфицированных вирусами иммунодефицита человека (ВИЧ-1), может развиться синдром приобретенного иммунодефицита (СПИД) или предСПИДа (состояния, предшествующего СПИДу), и в этой связи они могут иметь подавленную иммунную реакцию. Такой класс пациентов более чувствителен к патологическим инфекционным агентам или к развитию злокачественных новообразований, против которых нормальная иммунная система создает достаточную защиту. Другие индивидуумы с ослабленным иммунитетом включают раковых больных или пациентов, подвергавшихся лучевой терапии, хирургическому или химиотерапевтическому лечению.
Используемые в настоящее время способы профилактики развития иммунодефицита у индивидуумов с вирусными инфекциями, например с ВИЧ-инфекцией, обычно подразумевают введение соединений, которые ингибируют синтез вирусной ДНК, что таким образом замедляет наступление вирус-опосредованной иммуносупрессии. В случае лечения ВИЧ-инфицированных пациентов часто используют введение соединений, таких, например, как, 3′-азидо-3′-дезокситимидин (АЗТ), 2′-3′-дидезоксицитидин (ДДЦ) и 2′-3′-дидезоксиинозин (ДДИ), зидовудин, диданозин, залцитабин, ставудин и вирамун. Разработанные в последнее время способы лечения ВИЧ-инфекции подразумевают введение ингибиторов протеазы, таких, например, как саквиновир, нефинавир, ритонавир, индинавир и другие. Для лечения пациентов со СПИД также применяют лечение с использованием цитокинов, при этом в испытуемых группах показана эффективность интерлейкина-2 (ИЛ-2) с точки зрения повышения субпопуляции CD4 Т-клеток у ВИЧ-положительных пациентов (Kovacs, et al., N.Engl. J. Med., 1996; 335: 1350-1356). В отчетах, сделанных по результатам испытаний, дополнительно отмечается, что ИЛ-2 также может повышать количество CD8 Т-клеток (Schmitz, et. al., Science, 1999; 283: 857-860). К сожалению, использование ИЛ-2 обычно сопровождается значительной токсичностью (Davey, et al., JAMA, 2000; 284: 183-189). Тем не менее, несмотря на потенциальную значимость указанных видов лечения с точки зрения антиретровирусного эффекта, ни одно из них не доказало полную эффективность в плане лечения или профилактики СПИД. Кроме того, многие из указанных соединений вызывают неблагоприятные побочные реакции, включая низкий уровень тромбоцитов, диарею, тошноту, токсичность для почек и цитопению костного мозга (Kempf, et al., U.S. Patent 6017928; Lai, et al., U.S. Patent 6093743). Многочисленные клинические исследования с использованием метионин-энкефалинов (мет-энкефалина), проведенные на здоровых добровольцах, ВИЧ-положительных и раковых больных, показали отсутствие выраженной токсичности (Plotnikoff, et al., Clin. Immun. Immunopath., 1997). Однако измеряемый в плазме период полувыведения мет-энкефалина составляет примерно 2 минуты (Bihari, et al., Seventh. Int. Conf. On AIDS, 1991). Таким образом, необходима разработка улучшенных способов стимуляции длительного ответа иммунной системы пациентов, при необходимости указанного лечения, у таких пациентов как пациенты со сниженным ответом иммунной системы (например, со СПИДом) или пациенты, имеющие предрасположенность к снижению иммунитета (например, ВИЧ-инфицированные пациенты).
Краткое описание изобретения
Все цитированные патенты, заявки на патент и ссылки включены в настоящее описание в качестве ссылок.
Последние исследования мет-энкефалина показали, что мет-энкефалин активирует транскрипцию гена ИЛ-2 (Wybran, et al., из Some Immunological Effects of Methionine-Enkephalin In Man: Potential Therapeutical Use Leukocytes and Host Defence, 205-212, Alan R, Liss. Inc. 1986), гамма-интерферона (Brown, et al., Immunology, 1986; 103; 19-26) и ИЛ-12 (Zhong, et al., Augmentation of TNF-alpha Production, NK cell activity and IL-12p35 mRNA Expression by Metliaonine Enkephalin, 1996; 17 (2): 182-5), тогда как пациенты со СПИДом характеризуются дефицитом ИЛ-2 и гамма-интерферона (Fauci, et al., Science, 1993; 262: 1011-1018). В последнее время у ВИЧ-положительных пациентов показана недостаточность мет-энкефалина (Valentine, et al., FASEB J. 1988; 2 (5): 4518; Chao, Thesis, University of Illinois College of Pharmacy 1993). Все указанные выше цитокины происходят из прогормонов в Т-хелперных клетках (Plotnikoff, et al., Clin. Immun. Immunopath., 1997; 82 (2): 93-101). Иммуносупрессия представляет собой, в частности, последствие дефицита цитокинов (Fauci, et al., Science, 1993; 262: 1011-1018).
Приведенные выше данные, однако, не дают специалистам оснований ожидать, что активные агенты согласно изобретению могут использоваться в способах лечения с целью достижения у пациентов длительного иммунного ответа, включающих в себя введение пациентам, при необходимости такого лечения, активных средств по схеме перемежающейся дозировки.
Настоящее изобретение основано на неожиданном открытии того факта, что регулярное введение доз мет-энкефалина является эффективным в плане активации длительного иммунного ответа, включая повышение в течение длительного срока уровня иммунокомпетентных клеток у пациентов по меньшей мере в течение одного месяца после прекращения введения данного агента.
Настоящее изобретение относится, в том числе, к способам лечения, применяемым для индукции длительной иммунной реакции у пациентов со сниженным иммунитетом, при необходимости такого лечения, отличающимся тем, что указанный способ включает в себя введение пациенту эффективного количества энкефалиноваго пептида, индивидуально или в сочетании с другими соединениями, применяемыми для повышения реакции иммунной системы, включая вакцины. В данном контексте термин "сниженный иммунитет" относится к любому снижению числа Т-клеток или их функции.
Настоящее изобретение также относится, в том числе, к способам лечения, применяемым для индукции длительной иммунной реакции у ВИЧ-инфицированных больных, отличающимся тем, что указанный способ включает в себя введение ВИЧ-инфицированному пациенту эффективного количества энкефалинового пептида, индивидуально либо в сочетании с другими соединениями, применяемыми для замедления прогрессирования ВИЧ-пролиферации или ВИЧ-ассоциированных инфекций, включая ингибиторы обратной транскриптазы, такие, например, как 3′-азидо-3′-дезокситимидин (АЗТ), 2′-3′-дидезоксицитидин (ДДЦ) и 2′-3′-дидезоксиинозин (ДДИ), зидовудин, диданозин, залцитабин, ставудин и вирамун; ингибиторы протеазы, такие, например, как саквиновир, нефинавир, ритонавир и индинавир; цитокины, такие как Г-КСФ (гранулоцитарный колониестимулирующий фактор), ИЛ-11, ИЛ-12, ИЛ-2; а также гамма-интерферон и антибиотики или другие средства, используемые для лечения или профилактики инфекций у ВИЧ-инфицированных пациентов.
Подробное описание предпочтительных вариантов осуществления изобретения
Определения
Если особо не оговорено иное, термин "активные агенты" относится здесь к группе соединений, включающих в себя класс энкефалиновых пептидов.
Если особо не оговорено иное, термин "энкефалин" или "энкефалиновые пептиды" включает в себя любое соединение, которое попадает в общую категорию опиоидных пептидных молекул, включая соединения, имеющие следующую пептидную структуру на одном из концов:
Tyr-Gly-Gly-Phe-R,
где R означает метионин (Met) или лейцин (Leu). Примеры энкефалиновых пептидов показаны в Таблице 1.
Опиоидные пептиды и их предшественники и структуры
Аналоги энкефалина также охватываются рамками настоящего изобретения, и описание их содержится в приведенных ниже литературных ссылках: патент США №4468383 (Rodbard et al., опубликован в 28 августа 1984 г.); патент США №4371463 (Pert et al., опубликован 1 февраля 1983 г.); патент США №4261883 (Smolarsky, опубликован 14 апреля 1981 г.); патент США №4254106 (Wilkinson, опубликован 3 марта 1981 г.); патент США №4213968 (Kastin et al., опубликован 22 июля, 1980 г.); патент США. №4198398 (Hudson et al., опубликован 15 апреля 1980 г.); патент США №4127534 (Coy et al., опубликован 28 ноября 1978 г.); патент США №4092304 (Jones Jr. et al., опубликован 30 мая 1978 г.); патент США №4028319 (Jones Jr. et al., опубликован 7 июня 1977 г.); J.Chang et al., "Opiate Receptor Affinities and Behavioral Effects of Enkephalin: Structure Activity Relationship of Ten Synthetic Peptide Analogues", 18 Life Sci. 1473-1482 (1976); G.A.Gacel et al., "Synthesis, Biochemical and Pharmacological Properties of BUBUC, a Highly Selective and Systematically Active Agonist for in Vivo Studies of Delta-Opioid Receptors", 11 Peptides 983-988 (1990); and B.P.Roques, "Peptidomimetics as Receptor Agonists or Peptidase Inhibitors: A Structural Approach in the Field of Enkephalins, ANP and CCK", 32 Biopolymers 407-410 (1992).
Здесь термин "длительная реакция иммунной системы" означает поддержание у пациента повышенного уровня клеток и молекул, связанных с иммунной системой, относительно их базового уровня в сыворотке, включая Т-клетки, такие как CD3, CD4, CD8, CD56, CD25 и CD38, и молекулы, такие как интерлейкины и интерфероны.
Термин "базовый уровень" или "базовый уровень реакции" означает здесь уровень в сыворотке у пациентов перед введением активного агента клеток и молекул, связанных с иммунной системой, включая Т-клетки, такие как CD3, CD4, CD8, CD56, CD25 и CD38, и молекулы, такие как интерлейкины и интерфероны.
Фраза "схема перемежающегося введения дозы" энкефалиновых пептидов здесь относится к начальной стадии обычного повторного введения энкефалиновых пептидов, которое варьируется от ежедневного до еженедельного в течение некоторого определенного периода времени (или, альтернативно, соединения, которое активирует in vivo продукцию энкефалиновых пептидов в течение некоторого определенного периода времени) (в целом определяемое как "схема начального дозирования"), за которым следует период, когда такое введение прерывают. Дополнительные энкефалиновые пептиды (или соединения, которые активируют in vivo продукцию энкефалиновых пептидов) вводятся позже в режиме перемежающейся схемы.
Примеры схем перемежающегося введения дозы включают в себя, не ограничиваясь приведенным списком, введение энкефалиновых пептидов от одного до пяти раз в неделю в течение 12-недельного периода, затем следует перерыв на период времени от 4 до 24 недель. После этого, на основании ряда определенных критериев, дают усиленные дозы (бустер-дозы) до 5 раз в неделю в течение 1-4 недель. Другие примеры схем перемежающегося введения дозы, охватываемые рамками настоящего изобретения, включают в себя введение энкефалиновых пептидов от 1 до 5 раз в неделю в течение 4 недель с последующим перерывом на период от 4 до 16 недель. После этого дают усиленные дозы до 5 раз в неделю в течение 1-4 недель, в зависимости от уровня пролонгированной реакции, определяемой в ходе такого лечения. Другие схемы перемежающегося введения также могут быть использованы.
Здесь термин "ВИЧ" включает в себя все варианты и типы ВИЧ-1, ВИЧ-2 и другие синонимы ретровирусов, такие как Т-лимфотропный вирус человека типа III (HTLV-III) и вирус, ассоциированный с лимфоаденопатией (LAV-1 и LAV-2).
Термин "СПИД" здесь относится к синдрому приобретенного иммунодефицита, предСПИДу и к состоянию, характеризующемуся снижением числа лимфоцитов у ВИЧ-инфицированных индивидуумов.
Здесь термин "лечение или профилактика СПИДа" включает в себя предупреждение или снижение иммуносупрессии, вызванной СПИДом, например, за счет снижения уровня ВИЧ в лимфоцитах периферической крови пациента или за счет повышения числа лимфоцитов; пересадку костного мозга; повышение уровня выживаемости ВИЧ-инфицированных пациентов; а также профилактику или снижение симптомов, заболеваний и инфекций, ассоциированных с ВИЧ-инфекцией, которые включают в себя, не ограничиваясь приведенным списком, чувствительность к патогенным и условно-патогенным организмам и инфекциям, анемию, тромбоцитопению и лимфопению.
Здесь термин "условно-патогенная инфекция" включает в себя инфекции, вызванные организмом, который в норме не является патологическим для пациентов с нормально функционирующей иммунной системой.
Многие из пептидов, рассматриваемых в настоящем изобретении, являются коммерчески доступными, но в альтернативном варианте они могут быть синтезированы любым традиционным способом, который включает в себя, не ограничиваясь этим, приведенные в литературе способы, связанные с использованием твердофазного синтеза, (J.M.Stewart and J.D.Young, Solid Phase Peptide Synthesis, 2nd ed., Pierce Chemical Co., Rockford, III, (1984) и J.Meienhofer, Hormonal Proteins and Peptides, Vol.2, Academic Press, New York, (1973), и с использованием синтеза в растворе (E.Schroder and K.Lubke, The Peptides, Vol.1, Academic Press, New York, (1965)). Описание указанных выше способов лечения включено в настоящую заявку в качестве ссылки.
В целом указанные способы включают в себя последовательное добавление защищенных аминокислот к растущей пептидной цепи (Патент США №5693616, полностью включенный в настоящее описание в качестве ссылки). В норме защите подвергают аминогруппу или карбоксильную группу первой аминокислоты и любую реакционноспособную группу в боковой цепи. Затем защищенную аминокислоту присоединяют к инертной твердой подложке или используют в растворе, и следующую аминокислоту, также защищенную соответствующим образом, добавляют в условиях, пригодных для образования амидной связи. После связывания в соответствующей последовательности всех желаемых аминокислот удаляют защитные группы и твердую подложку с получением неочищенного полипептида. Далее полипептид обессоливают и очищают, предпочтительно хроматографически, с получением готового продукта.
Пептиды могут быть синтезированы с использованием стандартных методик твердофазного синтеза, таких, которые могут быть осуществлены на пептидном синтезаторе Applied Biosystems Model 430A (Applied Biosystems, Foster City, Calif.), в соответствии с инструкциями производителя. Специалистам известны также другие способы синтеза пептидов или пептидоподобных веществ либо с использованием методик твердофазного синтеза, либо с использованием методик синтеза в жидкой фазе.
Альтернативно, пептиды могут быть получены с помощью традиционных методов молекулярной биологии.
Описание
В одном варианте настоящего изобретения пациенту вводят эффективное количество активного агента один раз в неделю в течение 12-недельного курса, после чего введение прекращают. Иммунный ответ пациента (количество Т-клеток) измеряют в период от 4 до 16 недель после прекращения ввода начальной дозы и сравнивают полученные результаты с базовым уровнем ответа и с уровнями ответа измеренного в конце фазы введения указанной дозы. Затем, при необходимости, дают усиленные дозы до 5 раз в неделю в течение 1-4 недель.
В других вариантах осуществления настоящего изобретения пациенту вводят эффективное количество активного агента от 1 до 5 раз в неделю в течение всего периода 4-недельного курса, после чего введение прекращают. Измерение иммунного ответа пациента (количества Т-клеток) осуществляют в период от 4 до 16 недель после прекращения ввода начальной дозы. Затем, при необходимости, дают усиленные дозы до 5 раз в неделю в течение 1-4 недель, в зависимости от измеренного уровня длительного ответа. Могут использоваться также другие схемы перемежающегося введения дозы.
В одном аспекте согласно изобретению рассматриваются способы лечения или профилактики СПИДа у ВИЧ-инфицированного пациента, включающие в себя введение ВИЧ-инфицированному пациенту эффективного для лечения или профилактики СПИДа количества по меньшей мере одного соединения, выбранного из группы активных агентов, индивидуального или в сочетании друг с другом или в сочетании с другими соединениями, которые благоприятны для лечения или профилактики СПИДа у ВИЧ-инфицированных индивидуумов, включая, но не ограничиваясь приведенным списком, ингибиторы обратной транскриптазы, включая, но не ограничиваясь указанными соединениями, 3′-азидо-3′-дезокситимидин (АЗТ), 2′,3′-дидезоксицитидин (ДДЦ) и 2′,3′-дидезоксиинозин (ДДИ), зидовудин, диданозин, залцитабин, ставудин и вирамун; ингибиторы протеазы, такие как саквиновир, нефинавир, ритонавир и индинавир; цитокины, такие как Г-КСФ, ИЛ-11, ИЛ-12 и ИЛ-2, и эритропоэтин; антибиотики или другие средства, используемые для лечения или профилактики инфекций у ВИЧ-инфицированных пациентов, или вакцины.
Для использования с целью лечения или профилактики начала СПИДа у ВИЧ-инфицированного индивидуума указанные активные агенты могут вводиться любым подходящим способом, но предпочтительно вводятся перорально, парентерально, путем ингаляции, чрескожно, внутривенно, ректально, внутриартериально, назально, в виде глазных капель, в виде защечных пластырей или местно, в виде стандартных дозированных композиций, содержащих традиционные фармацевтически приемлемые носители, адъюванты и наполнители. Термин "парентеральное" здесь включает в себя подкожное, внутримышечное, внутривенное, внутриартериальное или внутрисухожильное введение.
Активный агент может также вводиться непосредственно индивидууму в фармацевтически приемлемом носителе, например, в растворе 5% ДМСО или 10% этанола в физиологическом солевом растворе. В предпочтительном варианте осуществления настоящего изобретения осуществляют множественное введение активных агентов в течение периода, необходимого для эффективного лечения.
Известно большое множество альтернативных вариантов, которые подходят для целей пролонгированного высвобождения, и все они включаются в область настоящего изобретения. Соответствующие носители включают в себя, не ограничиваясь приведенным списком, следующие агенты: микрокапсулы или микросферы, липосомы и другие липидные системы высвобождения; кристаллоидные и вязкие инстилляты; абсорбируемые и/или биодеградируемые механические барьеры; а также полимерные материалы, такие как блок-сополимеры полиэтиленоксида/полипропиленоксида (например, полоксамеры), полиортоэфиры, поперечно-сшитый поливиниловый спирт, полиангидриды, гидрогели полиметакрилата и полиметакриламида, анионные углеводные полимеры, полиэтиленгликоль и т.п. Подходящие системы доставки известны в технике и описаны, например, в патенте США №4937254, полное описание которого включено в настоящую работу в качестве ссылки.
Активные агенты могут быть также представлены в жидкой форме (например, в виде растворов, суспензий или эмульсий), и они могут подвергаться обычным фармацевтическим операциям, таким как стерилизация, и/или могут содержать традиционные фармацевтически приемлемые вспомогательные вещества, такие как стабилизаторы, смачивающие вещества, эмульгаторы, консерванты, дополнительные растворители, средства, способствующие суспендированию, усилители вязкости, средства, используемые для корректировки ионной силы и осмотических свойств, а также другие эксципиенты, в дополнение к забуферивающим средствам. Соответствующие водорастворимые консерванты, которые могут использоваться в композиции лекарственного средства, включают бисульфит натрия, тиосульфат натрия, аскорбат, хлорид бензалкония, хлорбутанол, тимерозал, борат фенилртути, парабены, бензиловый спирт, фенилэтанол или антиоксиданты, такие как витамин Е и токоферол, а также хелатирующие средства, такие как ЭДТА и ЭГТА. Указанные средства могут содержаться, например, в количествах примерно от 0,001 мас.% до 5 мас.% и предпочтительно в количестве от 0,01 мас.% примерно до 2 мас.%.
Для введения активный агент обычно объединяют с одним или более фармацевтически приемлемыми вспомогательными компонентами, подходящими для используемого способа введения. Указанные соединения могут смешиваться с лактозой, сахарозой, порошком крахмала, сложными эфирами целлюлозы и алканоевых кислот, стеариновой кислотой, тальком, стеаратом магния, оксидом магния, фосфорными и сернокислыми солями натрия и кальция, аравийской камедью, желатиной, альгинатом натрия, поливинилпирролидином и/или поливиниловым спиртом, и могут подвергаться таблетированию или инкапсулированию для целей традиционного введения. Альтернативно, соединения согласно изобретению могут быть растворены в физиологическом солевом растворе, в воде, полиэтиленгликоле, пропиленгликоле, в коллоидных растворах карбоксиметилцеллюлозы, в этаноле, кукурузном масле, арахисовом масле, хлопковом масле, кунжутном масле, трагаканте и/или в различных буферах, включая фосфатно-буферный физиологический солевой раствор. Другие вспомогательные компоненты и способы введения хорошо известны в фармацевтической области. Носитель или разбавитель может включать в себя материал, задерживающий внедрение, такой как глицеринмоностеарат или глицерилдистеарат, отдельно или с воском, или другие хорошо известные в данной области материалы.
Схема дозирования активных агентов для индукции длительного иммунного ответа у ВИЧ-инфицированных пациентов основана на множестве факторов, включая возраст, вес, пол, состояние здоровья индивидуума, тяжесть заболевания, способ введения и природу конкретного активного агента, подлежащего введению. Так, схема дозирования может варьироваться в широких пределах, но может быть определена простым способом лечащим врачом с использованием стандартных методик. Для всех раскрываемых в настоящем описании способов введения могут использоваться уровни дозирования от 10-14 мкг/кг до 30000 мкг/кг активных агентов на вес тела. Предпочтительны уровни дозирования от 1 мкг/кг до 250 мкг/кг в режиме перемежающегося введения дозы. В предпочтительном варианте осуществления настоящего изобретения дозирование в начальной стадии введения дозы составляет 20 мкг/кг веса тела субъекта, а перемежающееся дозирование после такой фазы начального лечения варьирует от 20 до 100 мкг/кг веса тела.
Эффективность схем дозирования определяется с использованием методов, которые позволяют измерить такие факторы как снижение уровня ВИЧ в лимфоцитах периферической крови пациента (вирусная нагрузка), анемия, тромбоцитопения и лимфопения, а также увеличение числа клеток CD4+, CD8+, CD3+ и CD56+, число лимфоцитов, титр антител, устойчивость к патогенным и условно-патогенным инфекциям и выживаемость ВИЧ-инфицированных пациентов.
Активные агенты согласно изобретению могут также вводиться в другой стабилизированной форме, такой, например, как в сочетании с полиэтиленгликолем, или в виде белка слияния, или в виде других хорошо известных форм.
Было показано, что пациенты со СПИДом, хирургические пациенты и раковые больные имеют повышенный уровень кортизола, приводящий к супрессии образования цитокинов, таких как ИЛ-2 и гамма-интерферон. Такая супрессия образования цитокинов определяет подавление иммунной системы. Считается, в частности, что кортизол обладает ингибирующим действием на транскрипцию гена ИЛ-2 и оказывает супрессирующий эффект на цитотоксические клетки и NK-лимфоциты. (См., например, K.Ogawa et. al., "Suppression of Cellular Immunity by Surgical Stress", Surgery, 127 (3): 329-36 (Март, 2000); "Suppressant Effects of Cortisol", Goodman and Gilmans, The Pharmacological Basis of Therapeutics, Pergamon Press, New York (8th Ed. 1990.) Кортизол также ответственен за слабость и утомляемость пациентов со СПИДом. Приведенные в примерах отчеты об исследованиях показывают, что применение схемы перемежающегося дозирования мет-энкефалина приводит к реверсии ВИЧ-индуцированного подавления иммунитета, что сказывается на повышении уровня ИЛ-2 и Т-клеток, и, как можно ожидать, приведет к реверсии такого подавления иммунитета, которое вызывает обычный путь через кортизол, наблюдаемого у пациентов со СПИДом, хирургических больных, раковых больных и других пациентов.
Настоящее изобретение для лучшего пояснения сопровождается приведенными ниже примерами, которые даны с целью иллюстрации и никоим образом не должны рассматриваться как ограничивающие область настоящего изобретения.
Пример 1. Введение in vivo мет-энкефалина в качестве "терапевтической вакцины"
Было осуществлено 12-недельное исследование по методу двойной слепой метки для измерения влияния регулярного введения дозы мет-энкефалина на уровень Т-клеток у ВИЧ-инфицированных пациентов. Дозировки для каждого пациента варьировались, в зависимости от группы: (1) 60 мкг/кг; (2) 125 мкг/кг и (3) плацебо. Пациентам вводят либо активный агент (мет-энкефалин), либо плацебо (нормальный физиологический солевой раствор; контрольная группа) один раз в неделю в течение двенадцати недель посредством внутривенной инфузии. В точках восемь и двенадцать недель у каждого пациента отбирают образцы для измерения уровня Т-клеток. На двенадцатой неделе инфузию останавливают. Новое измерение числа Т-клеток проводят через 4 недели после прекращения инфузии (точка 16 недель). Полученные результаты показывают длительную реакцию по уровню цитотоксических Т-клеток через месяц после введения последней дозы мет-энкефалина.
Иммунологические характеристики через месяц после последней инфузии N-физиологического солевого раствора
Иммунологические характеристики через месяц после последней инфузии N-метионин-энкефалина
Краткое описание результатов:
Было показано, что количество цитотоксических Т-клеток (включая CD3, CD4 и CD8 клетки) в сравнении с базовым значением оказывается повышенным через один месяц после введения последней дозы метионин-энкефалина (инфузия в течение 8-12 недель). Резко отличается контрольная группа, принимавшая плацебо, в которой отмечается прогрессирующее снижение числа тех же клеток в ходе 16-недельного исследования. Результаты показывают, что лечение мет-энкефалином увеличивает содержание цитотоксических Т-клеток (которые могут снизить уровень вируса) и может рассматриваться как стратегия применения «терапевтической вакцины» при лечении ВИЧ по схеме введения перемежающейся дозы. Указанные длительные результаты являются в особенности удивительными в связи с тем, что измеряемая длительность полупериода выведения мет-энкефалина в плазме составляет примерно две минуты.
CD3, CD4 и CD8 клетки
У пациентов, для лечения которых в течение месяца использовали метионин-энкефалин, было обнаружено длительное повышение уровня Т-клеток в сравнении с базовым уровнем (среднее значение CD3+180, CD4+37, CD8+128). Резко отличаются результаты, полученные в группе пациентов, которым в течение одного месяца вводили путем инфузии нормальный солевой раствор; у них отмечается резкое снижение числа Т-клеток в сравнении с базовым уровнем (CD3-284, CD4-79-246).
CD56 клетки
Число естественных клеток-киллеров было выше базового уровня как в группе, которой вводили путем инфузии мет-энкефалин, так и в группе, которой также путем инфузии вводили нормальный солевой раствор, в сравнении с базовым уровнем. Однако в группе, принимавшей мет-энкефалин, результаты были значительно выше, чем в группе, принимавшей нормальный солевой раствор (80+18 против 137+21, р=0,03).
CD25 клетки (рецептор ИЛ-2)
Экспрессия рецептора интерлейкина II повышается в обеих группах в сравнении с базовым уровнем, хотя повышение в группе мет-энкефалина было выше, чем в группе, принимавшей нормальный солевой раствор (45 против 87 клеток).
CD38 клетки
Было показано, что в обеих группах отмечается повышение числа CD38 клеток относительно базового уровня (285 в группе, принимавшей солевой раствор, против 316 в группе, принимавшей энкефалин).
Результаты исследования подтверждают гипотезу, предложенную Уолкером и сотрудниками, о том, что наиболее важными клетками в поддержании иммунной системы у пациентов со СПИДом являются цитотоксические Т-клетки (CD3, CD8) (Walker et al., Nature, 1987; 328: 345-348). Указанные цитотоксические Т-клетки являются теми же самыми клетками, которые активируются вакцинами (Belyakov, et al., J. Clin. Invest. 1998; 102 (112): 2072-2081). Подмножество CD4 также оказывает цитотоксическое действие в отношении ВИЧ (Hahn, et al., Int. Rev. Immunol., 1999; 18 (5-6): 449-464). NK-клетки также обладают цитотоксическим действием против ВИЧ (Melder et al., FASEB J., 1989; 3: 4).
В настоящем исследовании число CD56-клеток повышено в обеих группах, принимавших как энкефалин, так и солевой раствор (инфузия в течение 8-12 недель). Значительно большее повышение в группе энкефалина может быть связано с активирующим действием энкефалина, а итоговое повышение в энкефалиновой группе может быть связано с действием NK-клеток. Инфузия солевого раствора в течение 8-12 недель может также активировать до некоторой степени те же самые системы в связи со стрессовым действием процедуры, приводящей к некоторому повышению цитокинов и CD25.
Пример 2. Введение in vivo мет-энкефалина пациентам с развившимся СПИДом
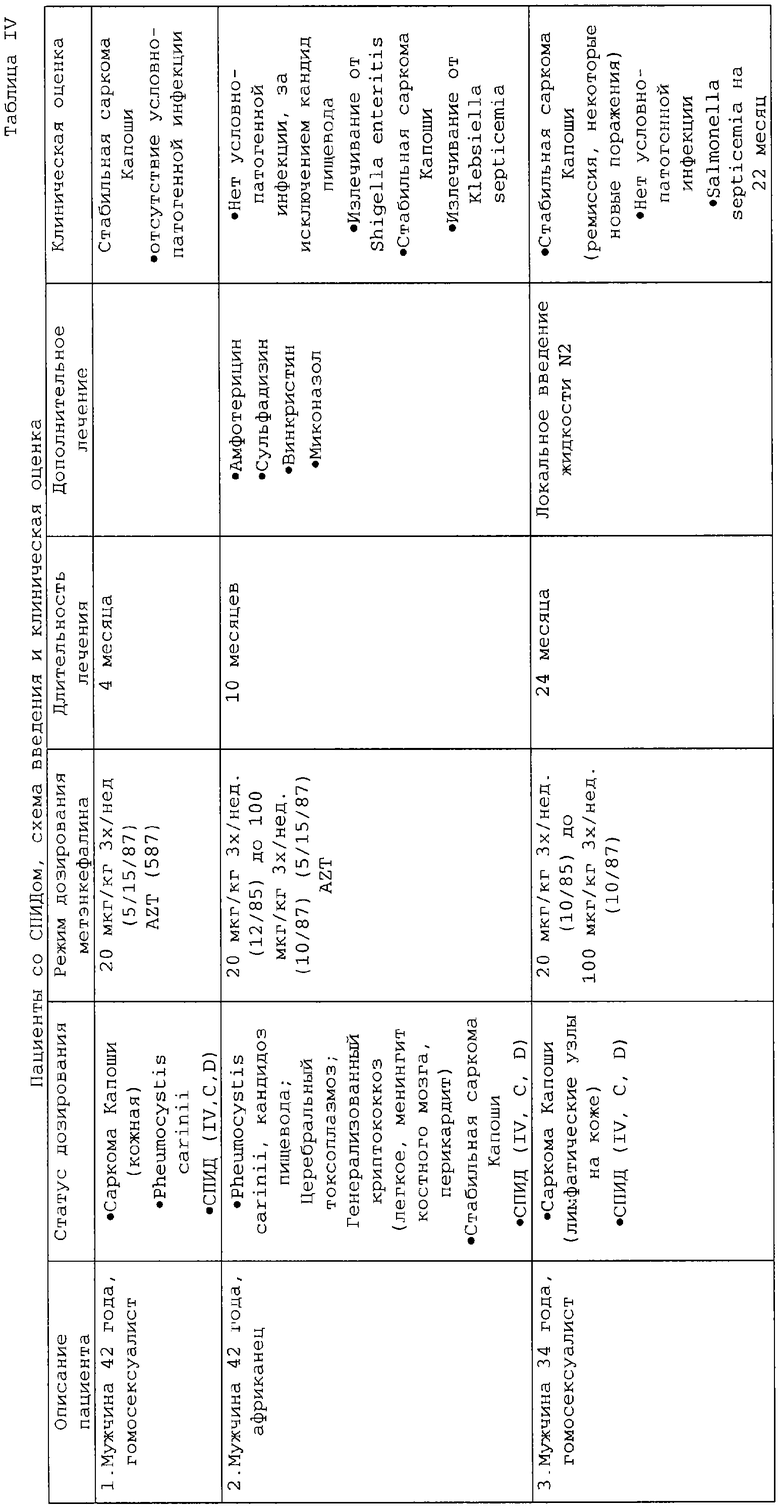
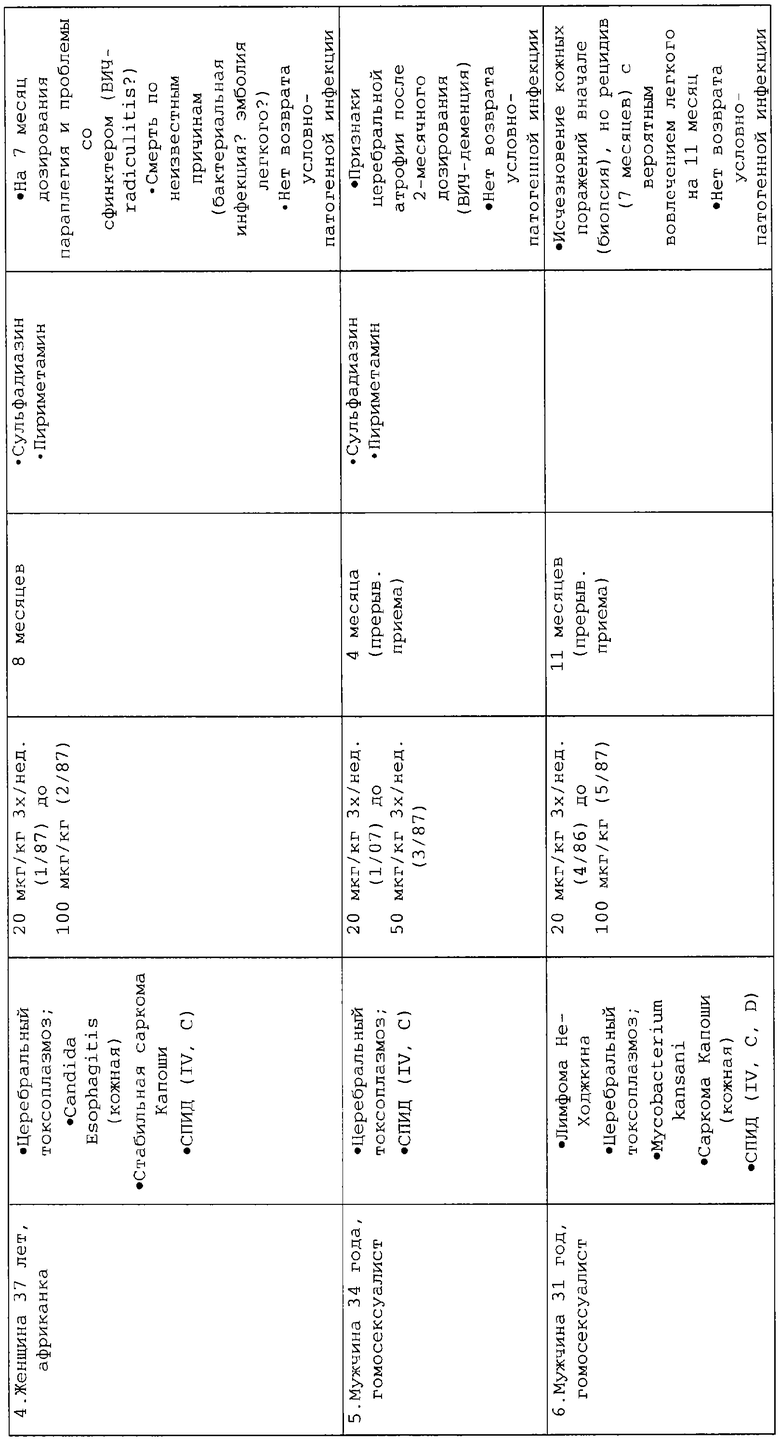
Шесть пациентов с прогрессирующим СПИДом, число CD4-клеток у которых составляло менее 200 клеток на мкл, подвергли лечению перемежающимися дозами мет-энкефалина. Во время начальной фазы дозирования дозы мет-энкефалина составляли 20 мкг/кг веса тела субъекта три раза в неделю в течение 4 недель.
Затем субъектам давали 20-100 мкг/кг веса тела, в зависимости от потребности. Пациенты 4 и 6 получали перемежающееся лечение после режима начального дозирования.
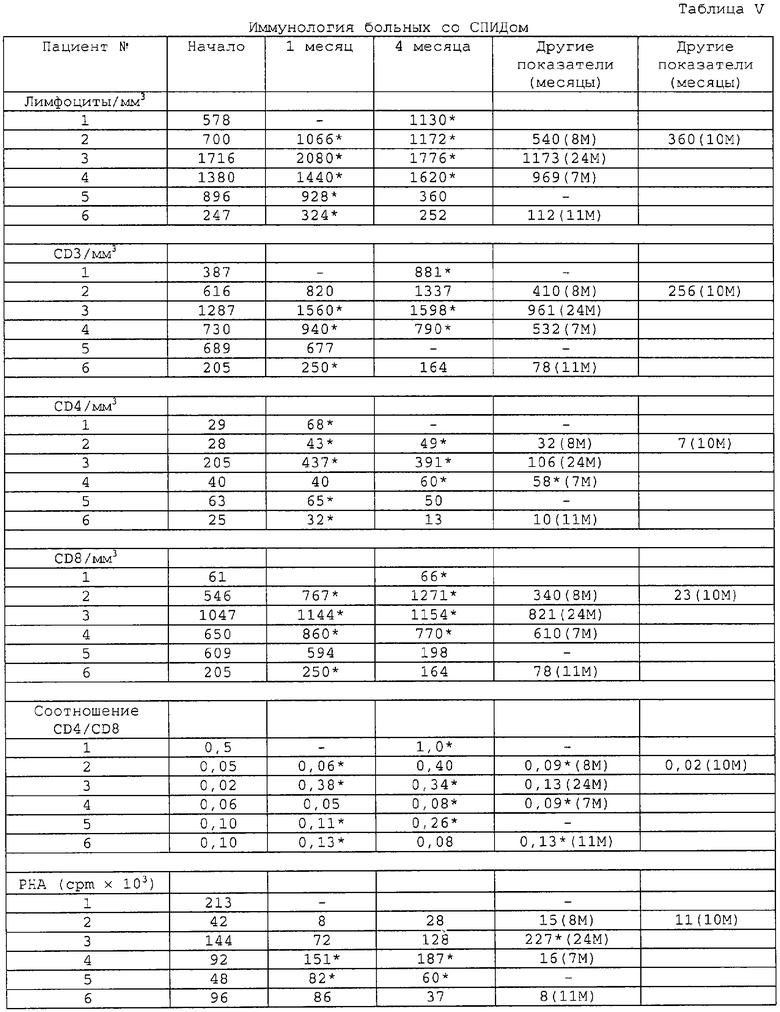
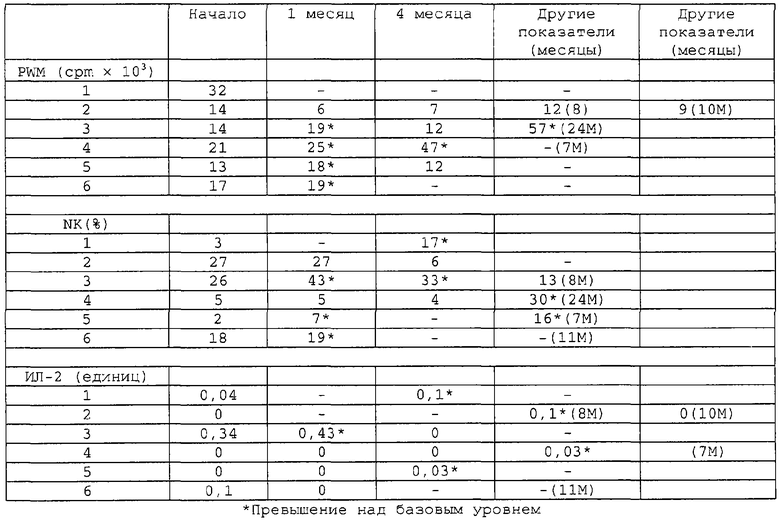
В Таблицах 4 и 5 приведены результаты исследования на момент начала схемы введения, через месяц после регулярного начального введения дозы, а для пациентов 4 и 6 - через три дополнительных месяца введения перемежающихся доз.
Сводка результатов
Исследование, описанное в примере 2, показывает, что схемы введения перемежающихся дозировок дают сравнимые или даже лучшие результаты у ряда пациентов в сравнении с пациентами, которым вводили постоянные дозы, сравнимые с дозировкой начального введения. В частности, у пациентов 4 и 6 отмечены в течение длительного периода времени положительные результаты без возврата условно-патогенной инфекции. У пациента 6 наблюдалось исчезновение кожных поражений в течение длительного периода времени. Изменения включали также видимое снижение размера некоторых опухолей, а также разрешение окраски опухоли на белый цвет.
У пациента 4 наблюдалось повышение уровня лимфоцитов, числа CD3, CD4 и CD8, а у пациента 6 - повышение уровня лимфоцитов в сравнении с базовым уровнем. Основные иммунологические эффекты включали в себя повышение субпопуляции Т-клеток (числа CD3, CD4 и CD8) и усиление бластогенеза с активацией транскрипции генов.
Таким образом, полученные клинические данные показывают, что лечение мет-энкефалином по схеме перемежающегося введения может повысить транскрипцию генов у пациентов с развившимся СПИДом и снизить или стабилизировать количество узлов при саркоме Капоши.
Для специалистов в данной области ясно, что активные агенты и способы согласно изобретению могут быть далее модифицированы без отхода от принципов и тематики настоящего изобретения, и они не ограничиваются приведенными выше примерами или вариантами осуществления. Данное описание должно рассматриваться как охватывающее все такие вариации, способы использования или варианты адаптации настоящего изобретения, которые в основном вытекают из принципиальных положений настоящего изобретения, в той области, к которой оно принадлежит.
Изобретение относится к медицине, в частности к иммунологии, и касается способов индукции длительного иммунного ответа у пациентов со сниженным иммунитетом. Для этого используют энкефалиновые пептиды, которые вводят по схеме начального дозирования с перерывом во ведении не менее 4-х недель и последующим переходом на поддерживающие дозы. Способ обеспечивает длительное и эффективное повышение уровня Т-клеток у больных со сниженным иммунитетом. 6 н. и 8 з.п. ф-лы, 5 табл.
| US 4537878, 27.08.1985 | |||
| US 4801614, 31.01.1989 | |||
| МАШКОВСКИЙ М.Д | |||
| Лекарственные средства | |||
| - М.: Медицина, 1986, т.2, с.171, 173 | |||
| YANG S | |||
| X | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Пуговица для прикрепления ее к материи без пришивки | 1921 |
|
SU1992A1 |
| GALIGIURI V.A | |||
| et al." Selective modulation of human natural | |||
Авторы
Даты
2007-12-27—Публикация
2002-05-16—Подача