Настоящее изобретение относится к пероральной композиции твердого раствора малорастворимого в воде активного вещества. Более конкретно, настоящее изобретение относится к композиции твердого раствора малорастворимого активного вещества, биодоступность которого сильно увеличивается.
Композиции твердых растворов, которые обычно имеют форму желатиновых капсул, известны специалистам. В ЕР 0001822 описаны фармацевтические композиции в форме твердых желатиновых капсул, заполненных жидким наполнителем, который содержит активное вещество и который отверждается в твердую композицию или в тиксотропный гель. В патенте США № 4795643 описана композиция твердого раствора с замедленным высвобождением активного вещества. Замедленное высвобождение обеспечивается использованием специальных полимеров, таких как акрилатные полимеры или этерифицированные целлюлозы.
Различные активные вещества очень плохо растворяются в воде. Когда указанные активные вещества вводят в организм, они часто обладают плохой биодоступностью вследствие плохой растворимости в пищеварительных соках. Для решения данной проблемы было разработано несколько способов, таких как микронизация, включение в циклодекстрины, использование инертных водорастворимых носителей, использование твердых дисперсий (WO 00/00179) или нанокристаллических или аморфных форм активного вещества.
Влияние описанных выше способов на биодоступность часто зависит от свойств активного вещества. Кроме того, лекарственные формы, разработанные к настоящему времени, часто имеют недостатки, такие как плохая термодинамическая стабильность, трудные процессы производства или плохая воспроизводимость между партиями продукта.
Целью настоящего изобретения является создание пероральной композиции для малорастворимого активного вещества со значительно улучшенной биодоступностью по сравнению с указанным активным веществом в традиционной лекарственной форме. Еще одной целью настоящего изобретения является создание композиции, которую можно изготовить с помощью обычных технологий и оборудования, что не требует больших капиталовложений.
Данной цели можно достичь, согласно настоящему изобретению, с помощью пероральной композиции с немедленным высвобождением и повышенной биодоступностью, включающей твердый гомогенный и термодинамически стабильный раствор малорастворимого в воде биологически активного вещества, отличающейся тем, что указанный твердый раствор включает:
а) активное вещество в количестве до 50% от общей массы композиции,
b) неионогенный гидрофильный поверхностно-активный агент, который находится в жидкой форме при температуре между 15°С и 30°С, в количестве от 20% до 70% от общей массы композиции,
с) фармацевтически приемлемый органический полимер или смесь полимеров, которые находятся в жидкой форме при температуре выше 60°С и в твердой форме при температуре ниже 30°С, в количестве от 5% до 70% от общей массы композиции и,
d) необязательно, включает разрыхляющий агент в количестве от 1% до 10% от общей массы композиции.
Следующие определения приводятся для облегчения понимания некоторых терминов, используемых в рамках настоящей заявки.
"Немедленное высвобождение" относится к высвобождению по меньшей мере 75% лекарственного средства в растворенной форме из лекарственной формы в течение 90 минут.
"Термодинамически стабильный" относится к отсутствию значительных физических или химических изменений продукта, которые могут повлиять на качество продукта во время хранения в течение периода времени до 5 лет при обычных условиях.
"Малорастворимый в воде" означает, что растворимость в воде активного вещества составляет менее 1 в 1000. Это означает, что в данное определение включены определения веществ в фармакопее, такие как "очень незначительно растворимые", "практически нерастворимые" и "нерастворимые" (USP 24/NF 19, стр.10; январь 2000 г.).
Термин "неионогенный гидрофильный поверхностно-активный агент" относится к таким амфифильным веществам, которые растворимы в воде (они имеют более высокие величины HLB (гидрофильно-липофильного баланса)), обладают поверхностной активностью и не ионизируются в водных растворах (H. Auterhoff, Worterbuch der Pharmazie, Wissenschafliche Verlagsgesellschaft GmbH, Stuttgart 1981, стр.192).
Под величиной HLB подразумевается величина по шкале от 0 до 20, которая присваивается каждому поверхностно-активному агенту на основании относительных пропорций гидрофильной и гидрофобной частей молекулы. Поверхностно-активные агенты, растворимые в маслах, имеют низкие величины HLB, в то время как поверхностно-активные агенты, растворимые в воде, имеют более высокие величины HLB.
Величину HLB рассчитывают следующим образом:
HLB=20(1-Мо/М),
где М представляет собой молекулярную массу молекулы, а Мо представляет собой молекулярную массу гидрофобной части молекулы.
Соотношение между активным веществом в композиции и неионогенным гидрофильным поверхностно-активным агентом составляет от 1:0,75 до 1:5, предпочтительно от 1:1,5 до 1:4, наиболее предпочтительно 1:3. Соотношение между неионогенным гидрофильным поверхностно-активным агентом и фармацевтически приемлемым полимером или смесью полимеров составляет от 1:4 до 1:0,05, предпочтительно от 1:1,5 до 1:0,1, наиболее предпочтительно приблизительно 1:0,75.
Неионогенный гидрофильный поверхностно-активный агент предпочтительно выбирают из группы, состоящей из сложных эфиров полиоксиэтиленгликольсорбита и жирных кислот (полисорбатов) и негидрогенизированных полиоксиэтиленовых производных касторового масла; указанные поверхностно-активные агенты имеют величину гидрофильно-липофильного баланса (HLB) от 14 до 16.
Полиоксиэтиленгликолевые полисорбаты можно приобрести у компании ICI Inc. с товарным знаком Tween®. Для настоящего изобретения предпочтительными являются Tween® 40, Tween® 60 или Tween® 80. Наиболее предпочтительным соединением является Tween® 80. Негидрированные полиоксиэтиленовые производные касторового масла можно приобрести у компании BASF Corporation с товарным знаком Cremophor®. Наиболее предпочтительным соединением для настоящего изобретения является Cremophor® EL.
В одном варианте осуществления настоящего изобретения фармацевтически приемлемый органический полимер или смесь полимеров состоит преимущественно из полиэтиленгликоля (ПЭГ) или смеси полиэтиленгликолей. PEG представляют собой конденсированные полимеры оксида этилена, которые можно приобрести у компании Union Carbide Corporation под торговым наименованием Carbowax®. Предпочтительными ПЭГ являются те из них, которые имеют молекулярную массу от 1000 до 50000 дальтон. Более предпочтительными являются ПЭГ с молекулярной массой от 4000 до 10000 дальтон. Наиболее предпочтительными являются ПЭГ с молекулярной массой приблизительно 6000 дальтон.
В еще одном варианте осуществления настоящего изобретения фармацевтически приемлемый органический полимер или смесь полимеров состоит преимущественно из поливинилпирролидона или смеси поливинилпирролидонов, которые можно приобрести у компании BASF под товарным знаком Kollidon®, имеющих молекулярные массы приблизительно от 2500 до 3000000 дальтон.
В еще одном варианте осуществления настоящего изобретения фармацевтически приемлемый органический полимер или смесь полимеров состоит преимущественно из поливинилового спирта или смеси поливиниловых спиртов, которые можно приобрести у компании Shin-Etsu Chemical Co. под товарным знаком Poval®, имеющих молекулярные массы приблизительно от 30000 до 200000 дальтон.
Композиция, необязательно, включает разрыхляющий агент в количестве от 1% до 10% от общей массы композиции. Обычно разрыхляющий агент не является необходимым, но в некоторых случаях может быть выгодным его добавление в малом количестве с целью повышения растворимости композиции вследствие набухания и увеличения транспорта воды в композицию при контакте с растворяющими средами. Примером разрыхляющего агента является Primojel®, который можно приобрести у компании Penwest Pharmaceuticals. Другими разрыхляющими агентами, которые можно использовать, являются Ac-di-Sol®, который можно приобрести у компании FMC, Kollidon CL®, который можно приобрести у компании BASF, или Polyplasdone XL®, который можно приобрести у компании ISP.
Особенно предпочтительной лекарственной формой для описанной выше композиции является твердая желатиновая капсула, которую заполняют гомогенной расплавленной смесью и позволяют ей отверждаться in situ.
Другую лекарственную форму изготавливают путем заполнения расплавленной смесью мягких эластичных желатиновых капсул или путем изготовления формованных таблеток, например, заполнением расплавленной смесью таблеточных пресс-форм, или путем придания формы таблеток частично отвержденным расплавленным смесям, как это осуществляют с помощью процесса экструзии расплава в Knoll AG, Ludwigshafen, BRD.
Активные вещества, которые можно включать в состав композиций по настоящему изобретению, практически не имеют ограничений. Как уже упоминалось выше, активные вещества, предназначенные для изготовления композиций, плохо растворяются в воде, и настоящее изобретение относится к усилению свойств растворения указанных активных веществ таким образом, что они становятся более растворимыми в главным образом водной системе пищеварительного тракта человека. Активное вещество обычно используют в количестве приблизительно от 0,1 до 50% мас., предпочтительно в количестве приблизительно от 1 до 50% мас., более предпочтительно в количестве приблизительно от 10 до 50% мас.
Класс активных веществ, которые плохо растворяются в воде и для которых настоящее изобретение является особенно подходящим, представляет собой вещества, описанные в ЕР 0733642, общей формулы
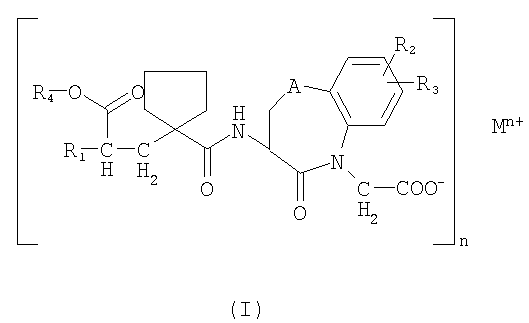
где
R1 выбран из группы, состоящей из (С1-С6)алкокси(С1-С6)алкила, который может быть замещен (С1-С6)алкокси, фенил(С1-С6)алкила и фенилокси(С1-С6)алкила, где фенильная группа может быть замещена (С1-С6)алкилом, (С1-С6)алкокси или галогеном, и нафтил(С1-С6)алкила,
R2 и R3 независимо представляют собой водород или галоген,
R4 представляет собой группу, образующую биолабильный сложный эфир,
М представляет собой ион металла, предпочтительно ион двухвалентного металла,
n равно 1, 2 или 3.
(С1-С4)Алкил определен как алкильная группа c прямой или разветвленной цепью, состоящая из 1-4 атомов углерода. (С1-С4)Алкокси определен как алкоксильная группа с прямой или разветвленной цепью, состоящая из 1-4 атомов углерода.
Таким образом, настоящее изобретение относится также к композиции твердого раствора, как описано выше, малорастворимого в воде соединения формулы I. М предпочтительно представляет собой ион Li+, Mg2+, Zn2+ или Са2+, наиболее предпочтительно ион Са2+, R1 предпочтительно представляет собой фенилэтил, R2 и R3 предпочтительно представляют собой водород, и R4 предпочтительно представляет собой этил. Предпочтительным соединением является кальциевая соль 1Н-1-бензазепин-1-уксусной кислоты, 3-[[[1-[2-(этоксикарбонил)-4-фенилбутил]циклопентил]карбонил]амин]-2,3,4,5-тетрагидро-2-оксо-. Наиболее предпочтительным соединением является указанное соединение в его 3S,2'R форме. Данное соединение упоминается как соединение S-Ca; соответствующая кислота (1Н-1-бензазепин-1-уксусная кислота, 3-[[[1-[2-(этоксикарбонил)-4-фенилбутил]циклопентил]карбонил]амин]-2,3,4,5-тетрагидро-2-оксо-) упоминается как соединение S-H, и соответствующая S-α-метилбензиламинная соль упоминается как соединение S-Mba.
Описанную выше композицию можно изготовить с помощью обычных технологий и оборудования. Таким образом, другим аспектом настоящего изобретения является обеспечение способа получения композиции, как описано выше, который характеризуется тем, что а) неионогенный гидрофильный поверхностно-активный агент смешивают с фармацевтически приемлемым органическим полимером или смесью полимеров при температуре от 50 до 100°С, предпочтительно от 60 до 70°С, b) активный ингредиент добавляют и растворяют при указанной температуре, с) полученной смесью, необязательно, наполняют капсулы и d) полученная смесь отверждается при комнатной температуре.
Альтернативно, неионогенный гидрофильный поверхностно-активный агент, фармацевтически приемлемый органический полимер или смесь полимеров и активные вещества смешивают и нагревают до температуры от 50 до 100°С, предпочтительно от 60 до 70°С, до получения прозрачного раствора, после чего, необязательно, наполняют раствором капсулы.
Следующие примеры предназначены только для дальнейшей иллюстрации настоящего изобретения, и, таким образом, данные примеры не предназначены для ограничения каким-либо образом объема настоящего изобретения.
ПРИМЕРЫ.
Пример 1. Влияние типа и количества поверхностно-активного агента на высвобождение.
ПОЛУЧЕНИЕ КОМПОЗИЦИЙ.
Неионогенный гидрофильный поверхностно-активный агент, Tween® 80 или Cremophor® EL, нагревают вместе с гидрофильным полимером, PEG 6000, до температуры выше 60°С. Добавляют активное вещество и растворяют его в расплаве при указанной температуре. Полученным раствором наполняют капсулы размера 0 (ноль). Раствор отверждается в капсуле при комнатной температуре.
Составляли композиции из возрастающих количеств поверхностно-активного агента с малорастворимым в воде активным веществом и гидрофильным полимером. Композиции представлены в таблице 1 для наполняемых жидкостью капсул, которые содержат 50 мг активного вещества. Определяли влияние количества и влияние типа поверхностно-активного агента на высвобождение активного вещества из наполняемых жидкостью капсул.
Влияние количества и типа поверхностно-активного агента на растворение активного вещества (количества выражены в %)
n.a.: не применимо
ИСПЫТАНИЯ НА РАСТВОРИМОСТЬ IN VITRO
Система для растворения
Испытания на растворимость наполненных жидкостью капсул осуществляют в искусственных желудочно-кишечных жидкостях при температуре 37°С с использованием аппарата USP II со скоростью лопасти 100 об/мин и грузила для каждой капсулы. Растворение изучается в последовательном ряде возрастающих значений pH среды, начиная с 400 мл pH 2, изготовленных из 400 мл 0,01н. хлористоводородной кислоты. Через один час после начала растворения отбирают 15 мл среды и изменяют pH буфера до 4,5 добавлением 88,5 мл 0,05н. ледяной уксусной кислоты и 211,5 мл 0,05н. раствора ацетата натрия. Через 30 минут отбирают 5 мл среды и изменяют pH буфера до 6,8 добавлением 180 мл 0,2н. гидрофосфата динатрия и 120 мл 0,2н. дигидрофосфата калия. Через 2,5 часа отбирают 5 мл среды и прекращают испытания на растворение.
Хроматографическая система
Используется высокоэффективная жидкостная хроматографическая система, снабженная колонкой с термостатируемой температурой, детектором УФ-поглощения с регулируемой длиной волны и интегрирующей системой. Аналитическая колонка (длина 3 см, внутренний диаметр 3 мм) представляет собой модифицированную колонку с диоксидом кремния С18, предпочтительно колонку Inertsil® ODS-3, с размером частиц 3 мкм. Подвижная фаза состоит из дегазированной смеси 350 мл воды, содержащей 800 мг ацетата аммония и 800 мкл трифторуксусной кислоты, и 650 мл ацетонитрила. Скорость потока составляет 0,5 мл/мин. Температура колонки составляет 40°С. Вводимый объем составляет 5 мкл, а длина волны детектора УФ-поглощения составляет 236 нм. Для внешней стандартизации растворяют 0,12 мг соединения S-Mba RS в 1 мл подвижной фазы. Количество растворенного соединения S-H, выраженное в процентах относительно заявленного на этикетке, рассчитывают по уравнению 1:
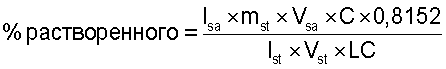
Уравнение 1. Расчет количества растворенного соединения S-H,
где
Ist=площадь пика соединения S-H на стандартной хроматограмме;
Isa=площадь пика соединения S-H на хроматограмме образца;
Vst=объем разведения стандартного раствора, в мл (=50 мл);
Vsa=объем разведения раствора образца, в мл (=400, 700 и 1000 мл);
mst=взвешенное количество соединения S-Mba RS, в мг;
С=чистота соединения S-Mba RS, в % м/м;
LC=заявленное на этикетке количество в анализируемой капсуле, выраженное как соединение S-H;
0,8152=соотношение между молекулярными массами соединения S-H и соединения S-Mba.
Результаты тестов на растворение композиций A, B, C и D (см. таблицу 1), содержащих в качестве поверхностно-активного агента Tween® 80, определенные описанным выше способом ВЭЖХ, представлены на фиг.1 (◆=0%;  =12%;
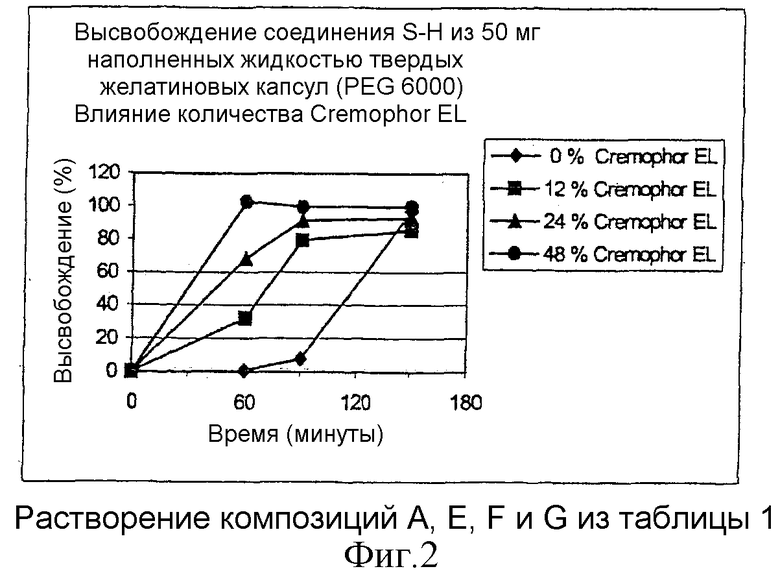
=12%;  =24% и •=48% Tween® 80). Результаты тестов на растворение композиций E, F и G (см. таблицу 1), содержащих Cremophor® EL в качестве поверхностно-активного агента, представлены на фиг.2 (◆=0%;
=24% и •=48% Tween® 80). Результаты тестов на растворение композиций E, F и G (см. таблицу 1), содержащих Cremophor® EL в качестве поверхностно-активного агента, представлены на фиг.2 (◆=0%;  =12%;
=12%;  =24% и •=48% Cremophor® EL).
=24% и •=48% Cremophor® EL).
Из результатов, представленных на фиг.1 и фиг.2, ясно, что высвобождение активного вещества из наполненных жидкостью капсул определяется количеством гидрофильного поверхностно-активного агента в композиции. Количество высвободившегося активного вещества возрастает с увеличением количеств поверхностно-активного агента.
Более конкретно, можно видеть, что высвобождение активного вещества при pH 2 (данные о высвобождении в течение первых 60 минут теста на растворение) определяется количеством поверхностно-активного агента в композиции. Изменение pH от 2 до 4,5 (данные о высвобождении в течение следующих 30 минут) улучшает высвобождение активного вещества из композиций, которые содержат малое количество гидрофильного поверхностно-активного агента. К концу периода pH 5 наблюдается полное растворение активного вещества, когда композиция содержит по меньшей мере 12% поверхностно-активного агента Cremophor® EL или 24% Tween® 80. Завершающее изменение pH с 4,5 до 6,8 более не влияет на высвобождение. Активное вещество остается полностью растворенным, когда используется по меньшей мере 12% Cremophor® EL или 24% Tween® 80.
Пример 2. Влияние типа гидрофильного полимера на высвобождение.
Гидрофильный полимер в наполняемых жидкостью капсулах может представлять собой полиэтиленгликоль. Влияние молекулярной массы данного полимера на растворение испытывали с использованием композиций, представленных в таблице 2. Композиции получали, как описано в примере 1.
Композиции с различными типами полиэтиленгликоля (n.a.: не применимо)
Испытания на растворимость выполняют, как описано в примере 1.
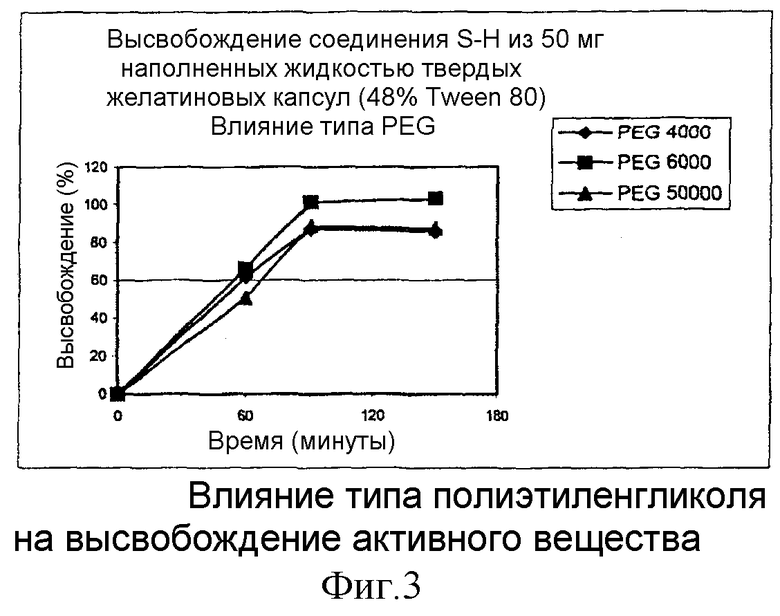
Результаты тестов на растворение композиций с Tween® 80 и с различными типами полиэтиленгликоля представлены на фиг. 3 (◆=PEG 4000;  =PEG 6000;
=PEG 6000;  =PEG 50000). Ясно показано, что высвобождение активного вещества из композиции, содержащей PEG 4000 и PEG 50000, сопоставимо, но задерживается по сравнению с PEG 6000, однако без образования композиций с замедленным высвобождением.
=PEG 50000). Ясно показано, что высвобождение активного вещества из композиции, содержащей PEG 4000 и PEG 50000, сопоставимо, но задерживается по сравнению с PEG 6000, однако без образования композиций с замедленным высвобождением.
Наиболее предпочтительным гидрофильным полимером является PEG 6000, поскольку PEG 4000 будет вызывать более раннюю утечку из капсул вследствие своей более низкой температуры плавления. С другой стороны, PEG 50000 труднее обрабатывать из-за относительно высокой вязкости данного материала в расплавленном виде.
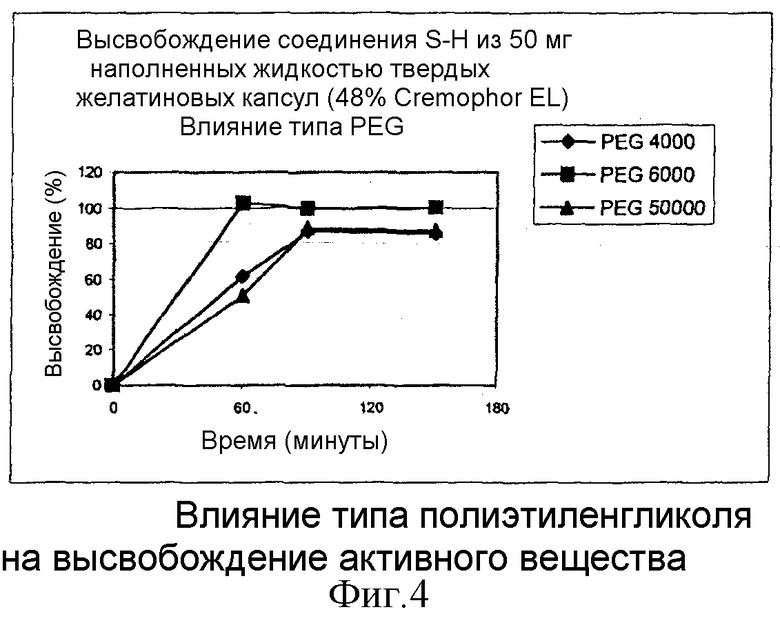
Влияние типа гидрофильного полимера также показано с использованием капсульных композиций, содержащих Cremophor® EL в качестве поверхностно-активного агента. Поверхностно-активный агент Tween® 80 в предыдущих примерах, композициях D, H и J, заменяют на такое же количество Cremophor® EL. Тест на растворение выполняют, как описано ранее. Результаты тестов на растворение наполненных жидкостью капсул, содержащих 48% Cremophor® EL, представлены на фиг. 4 (◆=PEG 4000;  =PEG 6000;
=PEG 6000;  =PEG 50000). Фиг.4 ясно показывает, что высвобождение активного вещества из наполненных жидкостью капсул, содержащих гидрофильные полимеры PEG 4000 и PEG 50000, сопоставимо, но по сравнению с PEG 6000 задерживается. Композиции, однако, нельзя считать композициями с замедленным высвобождением.
=PEG 50000). Фиг.4 ясно показывает, что высвобождение активного вещества из наполненных жидкостью капсул, содержащих гидрофильные полимеры PEG 4000 и PEG 50000, сопоставимо, но по сравнению с PEG 6000 задерживается. Композиции, однако, нельзя считать композициями с замедленным высвобождением.
Пример 3. Влияние различных катионов на высвобождение активного вещества.
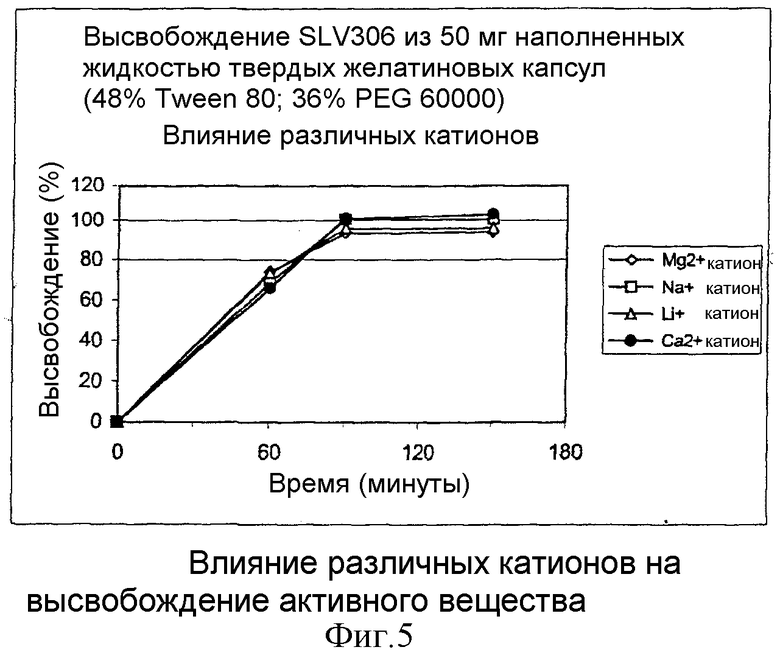
Наиболее предпочтительный ион Са2+ в формуле активного вещества заменяют на несколько ионов других металлов, таких как Mg2+, Na+ и Li+. Из данных активных веществ изготавливают композиции, подобные композиции D, описанной в таблице 1. Это означает, что композиции содержат 16% активного вещества, 48% Tween® 80 и 36% PEG 6000. Данные композиции изготавливают способом, описанным в примере 1. Результаты тестов на растворение активного вещества с ионом Са2+, Mg2+, Na+ или Li+ представлены на фиг.5 (•=Са2+, ⋄=Mg2+,  =Na+ или
=Na+ или  =Li+). Из результатов теста на растворение можно видеть, что указанные катионы не влияют на высвобождение активного вещества. Профили при pH 2, pH 4,5 и pH 6,8 сравнимы.
=Li+). Из результатов теста на растворение можно видеть, что указанные катионы не влияют на высвобождение активного вещества. Профили при pH 2, pH 4,5 и pH 6,8 сравнимы.
Пример 4. Изучение биодоступности.
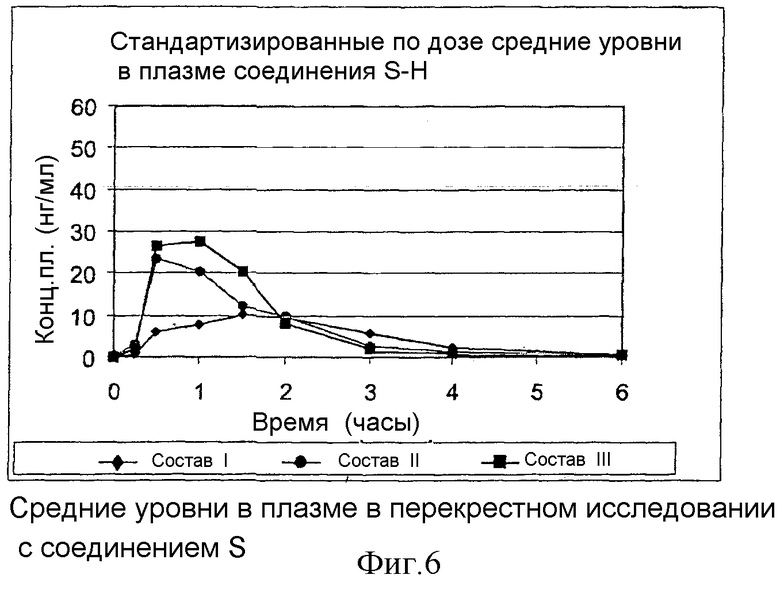
Перекрестное исследование выполняется для изучения биодоступности наполненной жидкостью твердой желатиновой капсулы. В качестве лекарственного вещества используются соединение S-Ca (композиция I и III) или соединение S-Н (композиция II).
Субъектам вводят следующие композиции: (I) 2×103,7 мг соединения S-Ca (соответствует 100 мг соединения S-Н), которым в жидком виде наполняют твердую желатиновую капсулу, изготовленную в соответствии с примером 1 с композицией D, (II) 2×100 мг соединения S-H в твердой желатиновой капсуле в виде 25% м/м порошкообразной смеси с фосфатом кальция, (III) 8×25 мг простая таблетка, состоящая из 25,94 мг соединения S-Ca (соответствует 25 мг соединения S-Н), 172 мг микрокристаллической целлюлозы РН101, 172 мг маннита-25, 8 мг гидроксипропилметилцеллюлозы Е5, 20 мг гликолята натрий-крахмала и 2 мг стеарилфумарата натрия. Исходя из средних уровней в плазме, показанных на фиг.6, были получены результаты, представленные в таблице 3.
Результаты перекрестного исследования с участием 15 субъектов мужского пола.
Результаты, представленные в таблице 3, указывают, что биодоступность лекарственного вещества из наполненной жидкостью твердой желатиновой капсулы, содержащей 103,7 мг соединения S-Ca, 311 мг Tween® 80 и 234 мг полиэтиленгликоля 6000, улучшается на 80% по сравнению с биодоступностью композиции III, в которой соединение S-H адсорбировано на фосфате кальция в виде 25% м/м порошкообразной смеси, и на 20% по сравнению с простой таблеткой соединения S-Ca.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ АДЕМЕТИОНИНА И ЕГО ЛЕКАРСТВЕННОЙ ФОРМЫ | 2015 |
|
RU2587331C1 |
| ПЕРОРАЛЬНЫЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ СЛОЖНЫЙ ЭФИР 17-ГИДРОКСИПРОГЕСТЕРОНА, И СООТВЕТСТВУЮЩИЕ СПОСОБЫ | 2012 |
|
RU2640912C2 |
| ФАРМАЦЕВТИЧЕСКАЯ ЛЕКАРСТВЕННАЯ ФОРМА ИНГИБИТОРА ТИРОЗИНКИНАЗЫ ДЛЯ ПЕРОРАЛЬНОГО ВВЕДЕНИЯ | 2007 |
|
RU2468788C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПРЕДНАЗНАЧЕННАЯ ДЛЯ ПЕРОРАЛЬНОГО ВВЕДЕНИЯ ПРОИЗВОДНОГО ПИРАЗОЛ-3-КАРБОКСАМИДА | 2004 |
|
RU2321404C1 |
| ПРОТИВОГРИБКОВАЯ КОМПОЗИЦИЯ ДЛЯ ПЕРОРАЛЬНОГО ВВЕДЕНИЯ, ВКЛЮЧАЮЩАЯ ИТРАКОНАЗОЛ, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2000 |
|
RU2216323C2 |
| ТВЕРДАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ПРОИЗВОДНЫЕ БЕНЗОФУРАНА | 1998 |
|
RU2191578C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ДИАЦЕРЕИН | 2009 |
|
RU2542461C2 |
| РЕЖИМЫ ДОЗИРОВАНИЯ ДЛЯ СОЕДИНЕНИЙ КЛАССА ЭХИНОКАНДИНОВ | 2013 |
|
RU2719579C2 |
| Режимы дозирования для соединений класса эхинокандинов | 2013 |
|
RU2639483C2 |
| ТВЁРДЫЕ ДИСПЕРСИИ | 2016 |
|
RU2694832C2 |
Пероральная композиция немедленного высвобождения включает твердый гомогенный и термодинамический стабильный раствор малорастворимого в воде биологически активного вещества, неионогенный гидрофильный поверхностно-активный агент, который находится в жидком виде при температуре от 15°С до 30°С, в количестве от 20% до 70% от общей массы композиции, фармацевтически приемлемый органический полимер или смесь полимеров, которые находятся в жидком виде при температуре выше 60°С и в твердом виде при температуре ниже 30°С, в количестве от 5% до 70% от общей массы композиции и, необязательно, включает разрыхляющий агент в количестве от 1% до 10% от общей массы композиции. Указанное малорастворимое в воде активное вещество предпочтительно представляет собой кальциевую соль 3-[[[1-[2-(этоксикарбонил)-4-фенилбутил]циклопентил]карбонил]амин]-2,3,4,5-тетрагидро-2-оксо-1Н-1-бензазепин-1-уксусной кислоты. Изобретение обеспечивает улучшенную биодоступность активного вещества по сравнению с традиционной лекарственной формой, также композицию можно получать с помощью обычных технологий и оборудования, что не требует больших капиталовложений. 3 н. и 9 з.п. ф-лы, 3 табл., 6 ил.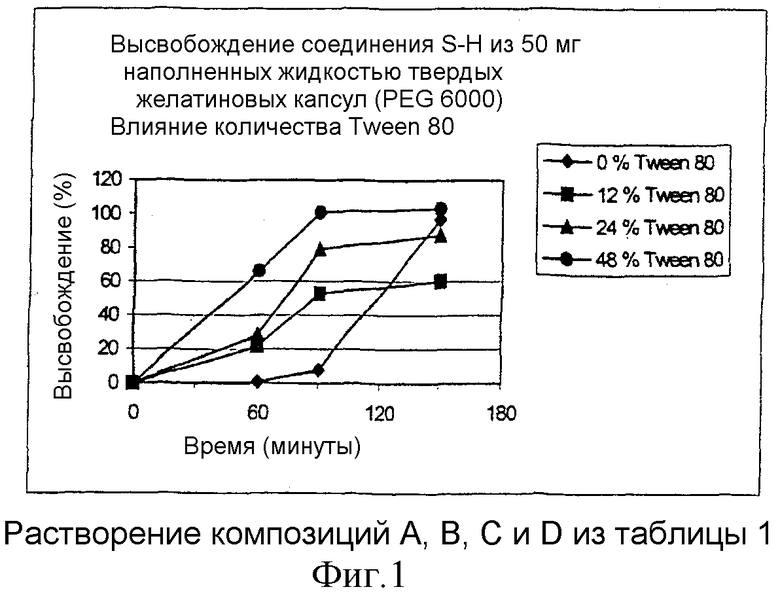
а) соединение общей формулы
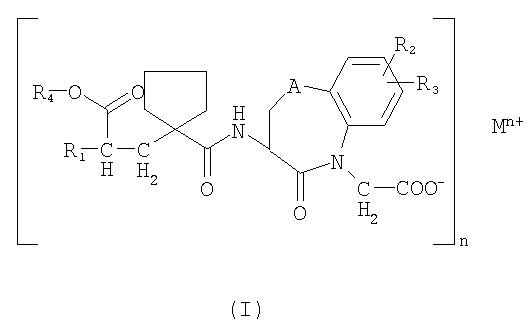
где R1 выбран из группы, состоящей из (C1-С6) алкокси (C1-С6) алкила, который может быть замещен (C1-С6) алкокси, фенил (C1-С6) алкила и фенилокси (C1-С6) алкила, где фенильная группа может быть замещена (C1-С6) алкилом, (C1-С6) алкокси или галогеном, и нафтил (C1-С6) алкила,
R2 и R3 независимо представляют собой водород или галоген,
R4 представляет собой группу, образующую биолабильный сложный эфир,
М представляет собой ион металла предпочтительно ион двухвалентного металла,
А представляет собой СН2;
n равно 1, 2 или 3;
в количестве до 50% от общей массы композиции,
b) неионогенный гидрофильный поверхностно-активный агент, который находится в жидком виде при температуре от 15 до 30°С, в количестве от 20 до 70% от общей массы композиции и
c) фармацевтически приемлемый органический полимер или смесь полимеров, которые находятся в жидком виде при температуре выше 60°С и в твердом виде при температуре ниже 30°С, в количестве от 5 до 70% от общей массы композиции и
d) необязательно включает разрыхляющий агент в количестве от 1 до 10% от общей массы композиции.
b) добавляют и растворяют при указанной температуре соединение общей формулы (I),
c) полученной смесью необязательно наполняют капсулу и
d) полученная смесь отверждается при комнатной температуре.
b) полученной смесью необязательно наполняют капсулу и
c) полученная смесь отверждается при комнатной температуре.
| WO 9833512 A1, 06.08.1998 | |||
| US 4325970 A, 20.04.1982 | |||
| US 5281420 A, 25.01.1994 | |||
| 0 |
|
SU292050A1 | |
| Вагонетка для движения по одной колее в обоих направлениях | 1920 |
|
SU179A1 |
| Машина для печатания ярлыков | 1956 |
|
SU103699A2 |
| Способ лечения ишемической болезни сердца | 1977 |
|
SU733642A1 |
| Радиоприемник | 1935 |
|
SU48601A1 |
| ЕР 0830863 А, 25.03.1998. | |||
Авторы
Даты
2008-01-20—Публикация
2003-02-11—Подача