Изобретение относится к биологии и медицине и может быть использовано для профилактики ВИЧ-инфекции и лечения СПИД(а), а также в исследовательской работе для изучения лиганд-рецепторных взаимодействий (типа поверхностные вирусные белки - клеточные рецепторы).
Известно комплексное антиВИЧ соединение, включающее в свой состав полимерную матрицу, выполненную в виде наночастиц, на поверхности которых нанесены путем пассивной адсорбции пептиды, представляющие собой моноклональные антиCD4-антитела (Международная заявка (WO) 94/24168, МПК С07К 17/08, опубл. 27.10.1994) [1]. Указанное комплексное соединение может быть использовано как лекарственное средство для профилактики или лечения патологических состояний, связанных с ВИЧ-инфекцией.
Однако данный антиВИЧ комплекс является высокомолекулярным соединением, которое плохо элиминируется из организма, что может вызвать тяжелые токсические последствия при его применении.
Известны комплексные антиВИЧ соединения, включающие в свой состав полианионную матрицу и синтетический фармакофор модификатор Норборнен [2, 3, 4].
Однако не известно и не описано их сочетанное использование с пептидсодержащими комплексными препаратами, связанными с полианионной полимерной матрицей, что ограничивает сферу применения данных препаратов и их эффективность.
Известно комбинированное применение синергично взаимодействующих антиВИЧ соединений, гуанозиннуклеозида с инозинмонофосфатдегидрогеназой (патент США №6514979, МПК А61К 31/52, опубл. 04.02.2003 г.) [5]. Указанные комбинации антиретровирусных препаратов используются для лечения ВИЧ-инфекции.
Однако эти комбинации включают в себя препараты, которые воздействуют на внутриклеточные этапы жизненного цикла вируса, кроме того, при применении этих комбинаций отмечаются токсические эффекты и возникновение устойчивых к данным препаратам генераций ВИЧ.
Наиболее близким техническим решением (прототипом) является другое комплексное антиВИЧ соединение, включающее полианионную матрицу и химически с ней связанный псевдолиганд для gp120 ВИЧ-1/2. Псевдолиганд для gp120 ВИЧ-1/2 представляет собой синтетический фармакофор модификатор, например Адамантан [6, прототип].
Недостатком вышеуказанных соединений-аналогов, в том числе и прототипа, является относительно узкий спектр потенциальных мишеней в многоэтапном процессе взаимодействия ВИЧ-1/2 - чувствительная клетка и относительно позднее (внутриклеточное) действие на вирус мишень, т.е. эти препараты эффективны, когда вирус уже проник в чувствительную клетку и они не блокируют начальные этапы инфицирования клеток вирусом иммунодефицита человека. Таким образом, данные химические соединения не могут полноценно блокировать начальные этапы инфицирования клеток вирусом иммунодефицита человека.
Техническим результатом изобретения является создание комплекса мембранотропных соединений, обеспечивающих адресную доставку противовирусного препарата к очагу поражения (ткани) ВИЧ-1/2 и подавление специфической вирусной инфекции на начальных и более поздних этапах ее развития (синергичное взаимодействие противовирусных соединений, связывающихся с различными сайгами белка оболочки ВИЧ gp120 на этапе проникновения вируса в клетку и блокирующих инфицирование чувствительных клеток и подавление специфической вирусной инфекции на начальных ее этапах).
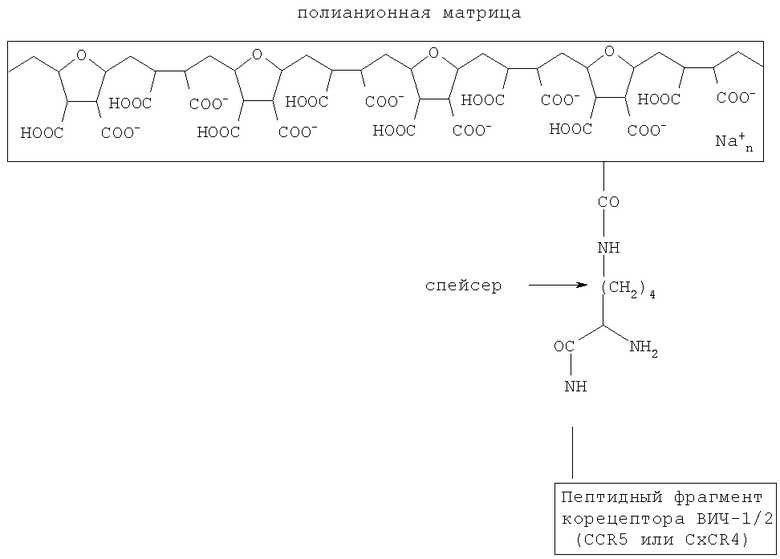
Указанный технический результат достигается тем, что в комплексе мембранотропных соединений для профилактики и лечения ВИЧ-инфекции, включающем первую полианионную матрицу и химически с ней связанный псевдолиганд для gp120 ВИЧ-1/2, согласно изобретению он дополнительно содержит вторую полианионную матрицу и химически с ней связанный псевдолиганд для gp120 ВИЧ-1/2, причем псевдолиганд для gp120 ВИЧ-1/2, связанный с первой полианионной матрицей, содержит пептидный фрагмент корецептора ВИЧ-1/2 CCR5 или CXCR4, а псевдолиганд для gp120 ВИЧ-1/2, связанный со второй полианионной матрицей, содержит фармакофор норборнен или фармакофор адамантан, причем первая полианионная матрица и связанный с ней пептидный фрагмент корецептора ВИЧ-1/2 CCR5 или CXCR4 имеет следующую общую формулу:
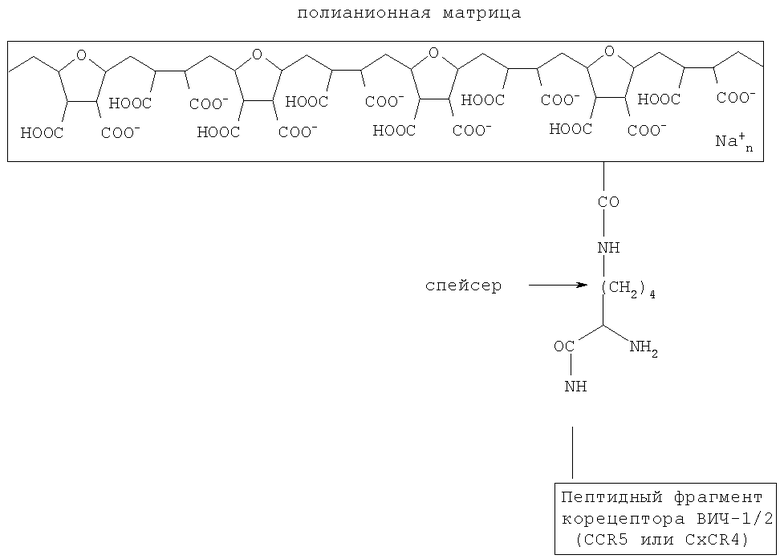
а вторая полианионная матрица и связанный с ней фармакофор норборнен или фармакофор адамантан имеют следующую общую формулу:
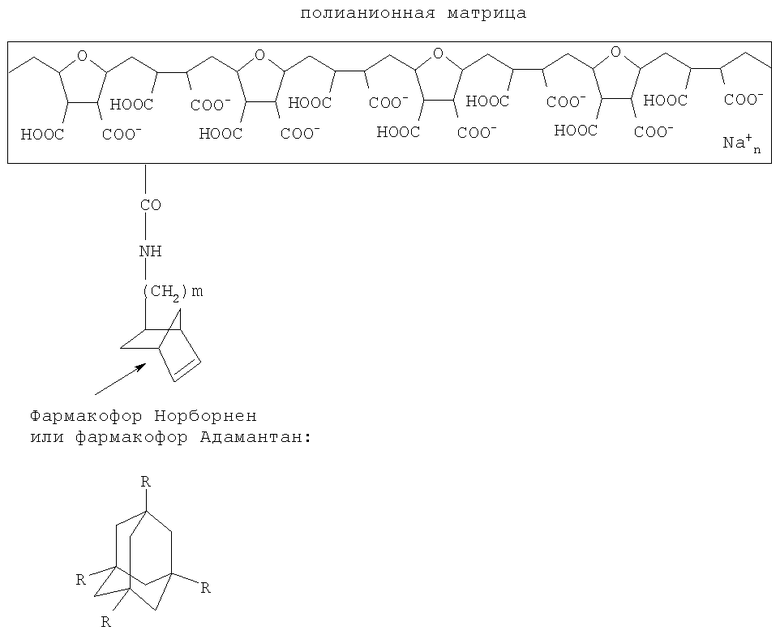
где R - замещенный или незамещенный NH2.
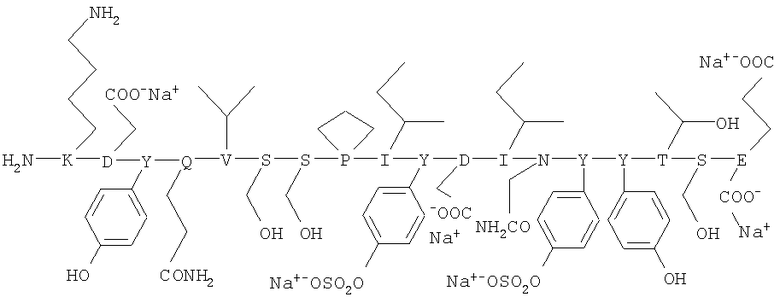
Пептидный фрагмент корецептора ВИЧ-1/2 CCR5 (структура пептидного фрагмента из N-конца (K-D2-E18) хемокинового рецептора CCR5) имеет следующую формулу:
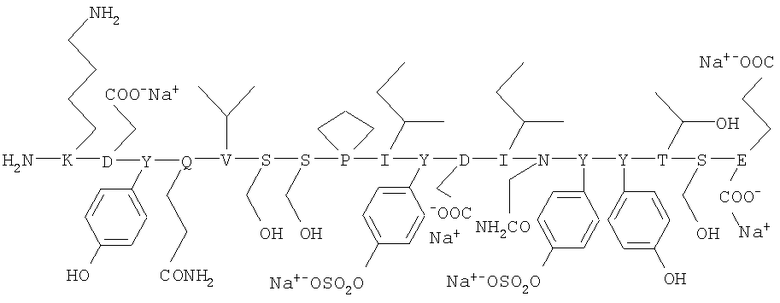
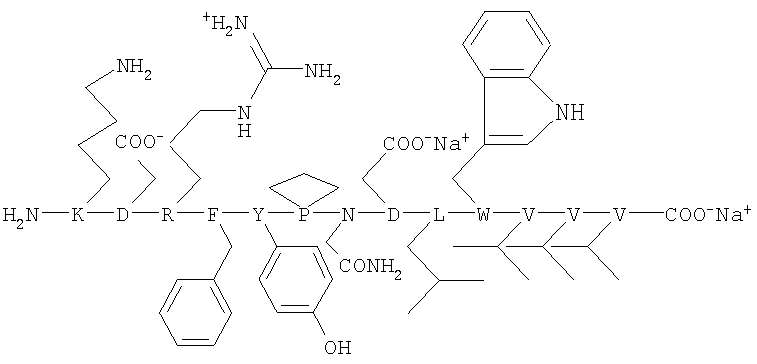
Пептидный фрагмент корецептора ВИЧ-1/2 CXCR4 имеет (структура пептидного фрагмента из области внеклеточной второй петли (EXL2) хемокинового рецептора CxCR4 (K-D187-V198) следующую формулу:
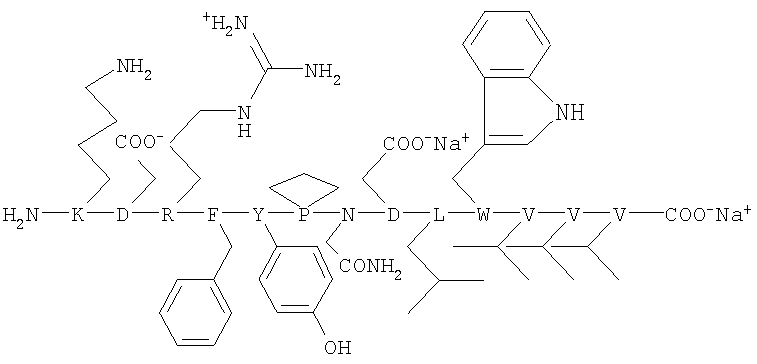
Причем соотношение первой полианионной матрицы с химически с ней связанным пептидным фрагментом корецептора ВИЧ-1/2 CCR5 или CXCR4 и второй полианионной матрицы с химически с ней связанным фармакофором норборненом или фармакофором адамантаном находится в пределах от 1:10 до 1:1. Соотношения заявляемых компонентов в комплексном соединении основаны на том, что оно проявляет примерно одинаковую активность при соотношении первого и второго компонентов от 1:10 до 1:1. Однако стоимость получения первой полианионной матрицы с химически с ней связанным пептидным фрагментом корецептора ВИЧ-1/2 CCR5 или CXCR4 значительно выше, чем стоимость получения второй полианионной матрицы с химически с ней связанным фармакофором норборненом или фармакофором адамантаном. В этой связи предпочтительнее использовать комплекс соединений, в котором содержание первого компонента в 5-10 раз меньше, чем второго компонента.
Норборнен - циклический алифатический углеводород с одной двойной связью семейства борненов, у которого отсутствуют метальные группы, в том числе и у мостикового углеродного атома.
Адамантан и его производные используют в качестве иммунорегуляторов, в частности для борьбы с вирусом СПИДа, следующей формулы:
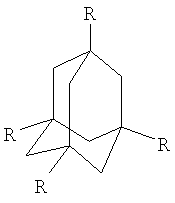
где R - замещенный или незамещенный NH2.
Таким образом, для получения заявляемого синергичного эффекта используют адресные антиВИЧ соединения на основе фармакофора норборнена или адамантана и пептидов-имитаторов корецепторов ВИЧ-1/2 CCR5 или CXCR4, которые химически связаны с полианионными матрицами в комплексный препарат, обеспечивающий высокий уровень защиты ВИЧ-инфицированных клеток как на начальной стадии инфицирования, так и в процессе лечения СПИДа.
Пептиды-имитаторы клеточных корецепторов ВИЧ-1/2 CCR5 и CxCR4 играют ключевую роль при взаимодействии лигандов gp120 ВИЧ с нативными хемокиновыми рецепторами.
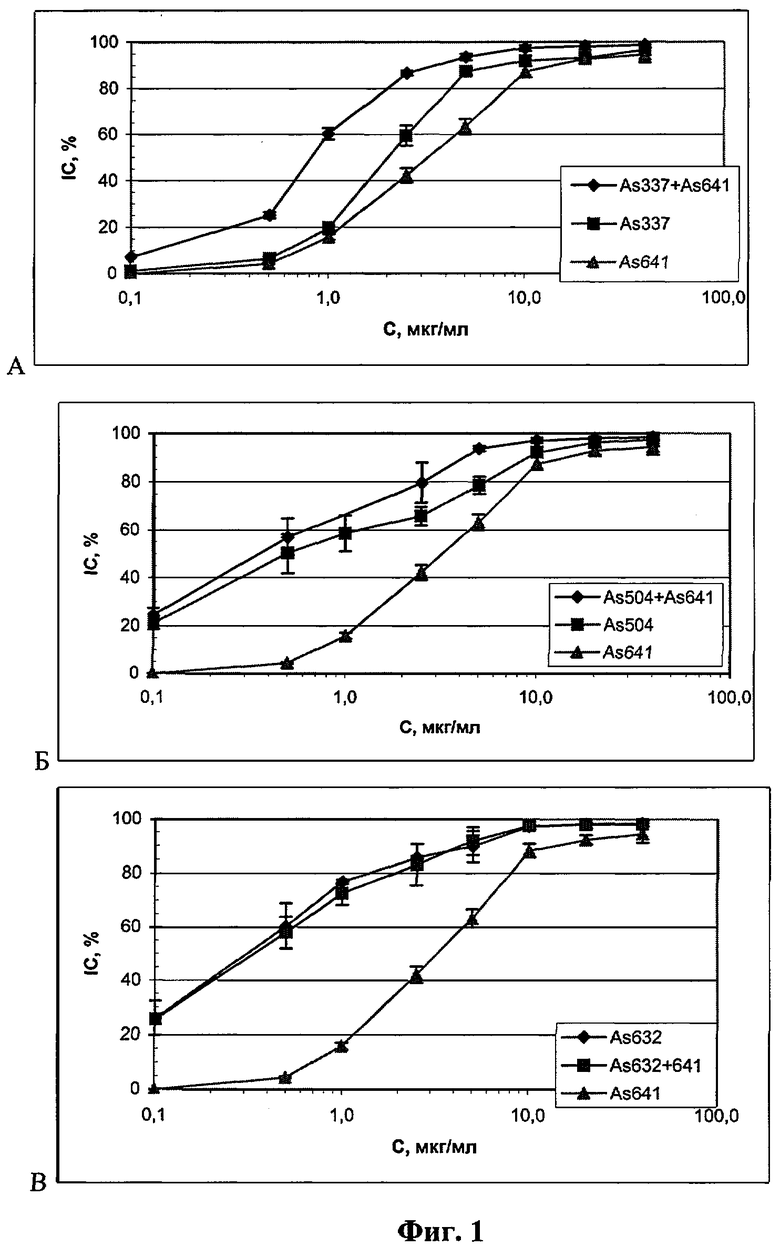
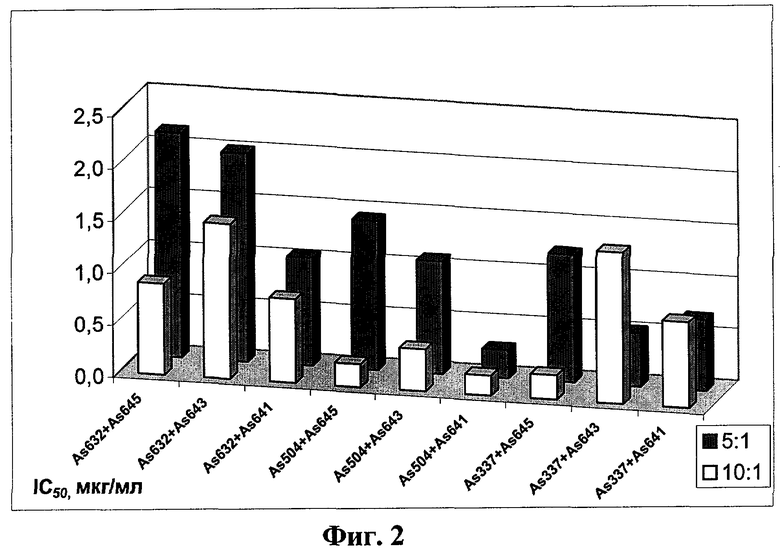
На Фиг.1 (а, б, в) приведены графики антиВИЧ-активности препаратов As337 (A), As504 (В), As632 (С), As641 и их комбинации (А, В, С) в соотношении 1:1. На фиг.2 приведена диаграмма антиВИЧ-активности (IC50) комбинаций препаратов M-Nb/Ad - М-Р в соотношениях (5:1; 10:1) в период адсорбции вируса (штамм ВИЧ-levk, линия клеток МТ-4).
Пример 1. Синтез пептидных фрагментов
Синтез пептидных фрагментов-имитаторов функционально значимых участков корецепторов CCR5 и CXCR4 осуществляют твердофазным методом на колонке с хлортритильным полимером с использованием щелочелабильной 2-(4-нитрофенилсульфонил) этоксикарбонильной (Nsc) группы для временной защиты N-конца [7]. Сущность твердофазного синтеза пептидов состоит в ступенчатом наращивании пептидной цепи посредством повторяющихся циклов химических реакций, начиная с С-концевой аминокислоты, закрепленной на нерастворимом носителе. При этом целевые продукты всех реакций в процессе синтеза остаются связанными с носителем, а избыточные реагенты и побочные продукты удаляются фильтрованием и промыванием носителя.
Для проведения твердофазного синтеза пептида С-концевую аминокислоту целевой аминокислотной последовательности, защищенную по α-аминогруппе, через α-карбоксильную группу ковалентно связывают с нерастворимым полимерным носителем путем образования амидной или эфирной связи. Затем с полученного Nα - защищенного аминоацил-полимера отщепляют Nα-защитную группу и получают аминоацил-полимер со свободной α-аминогруппой. Далее этот полимер ацилируют следующей аминокислотой, защищенной по α-аминогруппе, и получают Nα-защищенный дипептидил-полимер. Синтетические циклы, состоящие из стадий отщепления Nα-защитной группы и ацилирования свободной аминогруппы пептидил-полимера последующей аминокислотой, защищенной по α-аминогруппе, повторяют до тех пор, пока не будет собрана полная аминокислотная последовательность целевого пептида.
Так как в процессе твердофазного синтеза применяются большие молярные избытки ацилирующих реагентов (2-10-кратные по отношению к свободным аминогруппам), все реакционноспособные группы в боковых радикалах аминокислот, в частности амино-, карбокси-, гидрокси-, меркапто-, гуанидиногруппы, должны быть блокированы защитными группами. Защитные группы для этой цели подбирают таким образом, чтобы, с одной стороны, обеспечить полную и постоянную защиту боковых радикалов аминокислот в условиях реакций ацилирования пептидил-полимера и отщепления временной Nα-защитной группы и, с другой стороны, иметь возможность количественно и без повреждения структуры синтезированного пептида отщепить эти защитные группы в одну или две стадии.
Очистку синтезированных пептидов осуществляют препаративной ВЭЖХ. На выходе получают пептиды с 90-98% чистоты по данным аналитической ВЭЖХ. С N-концевого фрагмента пептида вводят аминокислоту лизин, имеющую стерически доступную для химической модификации аминогруппу с целью осуществления последующего химического связывания пептидов с поликарбоксилатной матрицей.
Пример 2. Получение полимерной матрицы и присоединение к ней псевдолиганда
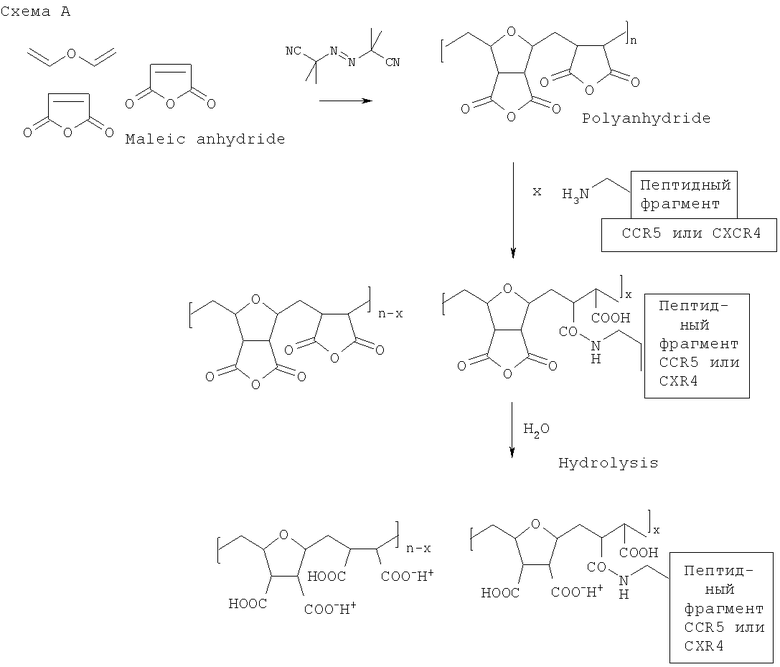
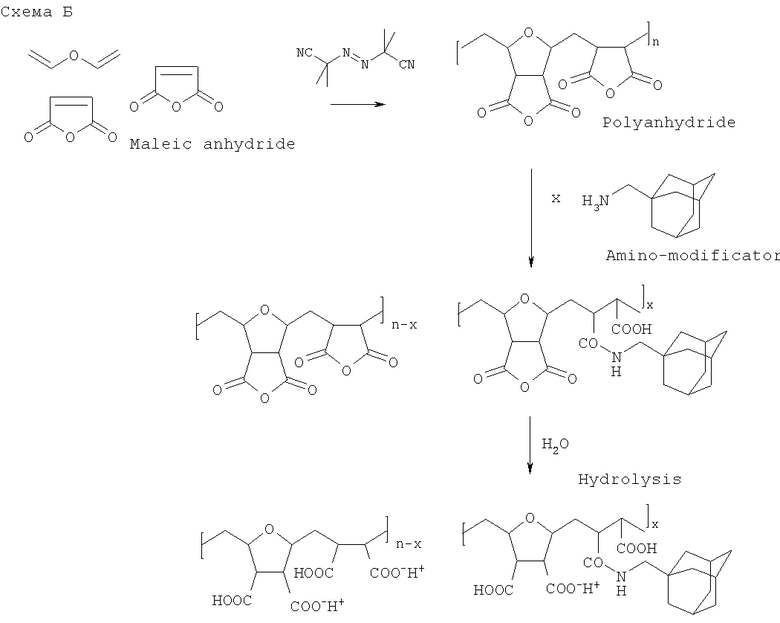
Выше приведена схема трехстадийного синтеза поликарбоксилатной матрицы из малеинового ангидрида, а также схема ковалентного присоединения псевдолиганда: пептидного фрагмента (схема А) или фармакофора адамантана (схема Б). Схема ковалентного присоединения псевдолиганда фармакофора норборнена аналогична схеме Б.
Ниже приведена процедура синтеза полианионной матрицы по 16-стадийной схеме:
Схема 1
Процедура синтеза полианионной матрицы
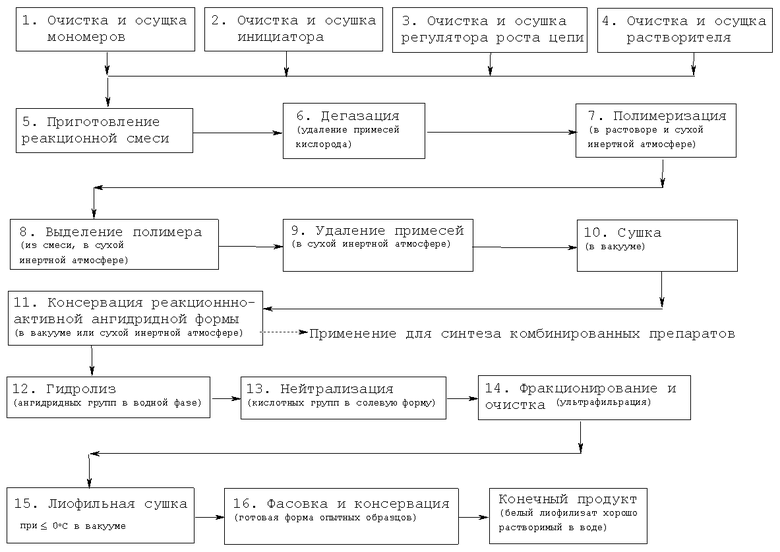
Далее приведена процедура (схема 2) синтеза комплекса мембранотропных антиВИЧ соединений (химических конъюгатов аминопроизводных норборнена или адамантана или пептидов с реакционно активной ангидридной формой полианионной матрицы (получена по схеме 1 до стадии 11 включительно).
Для модификации матрицы используют ее ангидридную форму, реакционно активную в отношении синтетических пептидов. Суммарную степень модификации матрицы ограничивали пределом не более 20% для сохранения необходимого количества немодифицированных карбоксильных групп матрицы, ответственных за обеспечение отрицательного заряда и ее специфических адъювантных свойств. Указанные карбоксильные группы получали после предварительных стадий модификации пептидными или химическими фармакофорами путем исчерпывающего гидролиза оставшихся немодифицированными ангидридных циклов матрицы. Продукты гидролиза очищали от остатков органических растворителей и непрореагировавших реагентов методом ультрафильтрации водных растворов с применением мембраны проницаемостью 3KD. Конечные продукты в форме натриевой полусоли выделяли лиофильной сушкой.
Схема 2.
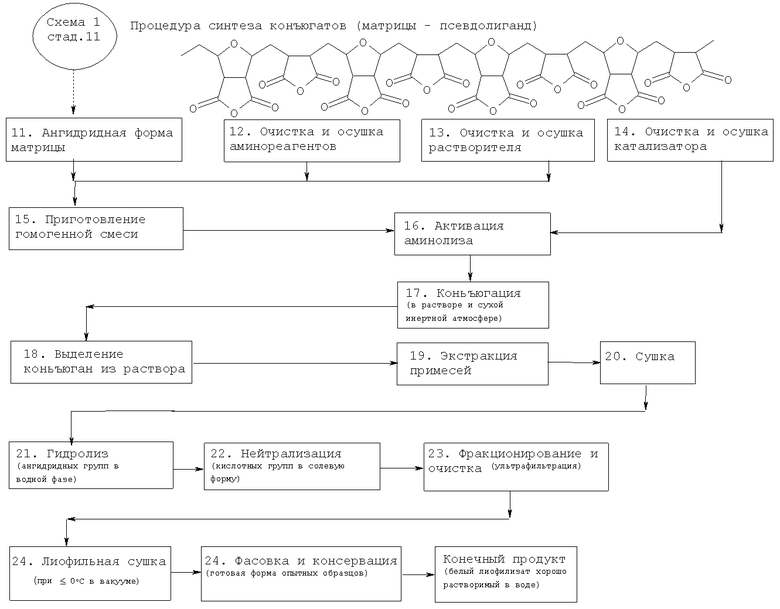
Пример 4. Исследование антиВИЧ активности заявляемого комплекса антиВИЧ мембранотропных соединений для профилактики и лечения ВИЧ-инфекции
Вирус. Для оценки эффективности антиВИЧ соединений в работе использовали макрофаготропный штамм ВИЧ-1EVK (ГКВ 4005).
Клеточные линии. Высокочувствительная к инфекции ВИЧ-1/2 перевиваемая культура лимфобластоидных клеток человека МТ-4. МТ-4 клетки культивировали в полной ростовой питательной среде RPMI-1640, содержащей 0,06% L-глутамина, 10% сыворотки эмбрионов коров, линкомицина (60 ед/мл) и гентамицина (100 мкг/мл) при температуре 37°С, 5% СО2 в течение 4 суток. Посевная концентрация клеток составляла 0,5×106 кл/мл. На 4 сутки культивирования учитывали количество клеток, разводили ростовой питательной средой до посевной концентрации и культивировали вновь.
Исследование антиВИЧ активности препаратов проводили по следующей схеме: раствор препарата в концентрациях от 0,1 до 500 мкг/мл (по три лунки на каждую концентрацию) вносили в клеточную культуру (МТ-4, МКПК), одновременно вносили вирус и инкубировали в течение 4-х суток. Множественность заражения составляла 0,2-1 инфекционных единицы на клетку. Культуры клеток инкубировали в течение 4 суток при температуре 37°С во влажной атмосфере 5% СО2. В качестве контролей служили ВИЧ-инфицированные клетки без добавления противовирусных препаратов и неинфицированные клетки.
АнтиВИЧ активность оценивали после окончании инкубации по снижению жизнеспособности культуры и по подавлению продукции вирусспецифического белка р24 ВИЧ-1. Долю жизнеспособных клеток учитывали методом исключения трипановым синим (Sigma, USA) или методом, основанном на редукции красителя МТТ (ICN, USA) с накоплением формазана в живых клетках. Количество вирусспецифического белка р24 в культуральной среде оценивали с помощью иммуноферментного анализа (тест-система "ВектоВИЧ-1 р24-антиген", чувствительность 20×10-12 г/мл производства ЗАО "Вектор-Бест", Россия). На основе экспериментальных данных строили дозозависимые кривые и вычисляли процент подавления репродукции ВИЧ-1 по сравнению с контролем, а также вычисляли концентрации препаратов, на 50% (EC50) защищающие инфицированные клетки от гибели, и определяли подавление продукции вирусспецифического белка р24 и концентрации препарата, на 50% (IC50), снижающие накопление этого белка в культуральной среде.
Для поиска ЕС50, IC50, строились графики зависимости доза-эффект, и по их линейным участкам вычислялись соответствующие концентрации и погрешности по формулам обратной регрессии [Н.Дрейпер, Г.Смит, Прикладной регрессионный анализ. - М.: Финансы и статистика, 1986]. Для каждого значения концентрации было проведено одновременно три различных измерения, нормальность распределения проверялась по критерию R/s, равенство дисперсий по критерию Кочрена.
Сравнение эффективности комплексных соединений проводили как по проценту подавления репродукции ВИЧ, определенному вирусологическими методами в культуре пермессивных клеток, так и по ингибиции продукции вирусспецифического р24 ВИЧ-1 инфицированными клетками. При этом учитывалась ошибка воспроизводимости, оцененная по трем независимым повторам измерений. На основании количественных характеристик ингибирования ВИЧ-инфекции и расчетных концентраций IC50 для каждого соединения и сочетания препаратов рассчитывали комбинационные индексы (FIC), определяемые согласно L.B.Allen et al., 1999 [Alien L.B., Teepe A.G; Kehoe M.J., Holland C.S., Mc Namara D.J. and Cook P.D. Antiviral and cytotoxicity evaluation of 3-nitro-3-deazaurICine// Antiviral Res. - 1989. - V.12. - P.259-268] по формуле
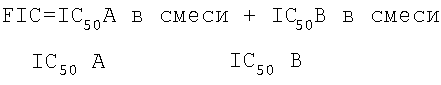
где А и В - индивидуальные препараты в тестируемой смеси.
Ниже в таблице 1 приведены примеры составов комплекса заявляемых мембранотропных соединений, которые получены в соответствии с примерами 1 и 2.
Примеры составов комплекса мембранотропных соединений
В таблице 2 приведены данные по влиянию мембранотропных препаратов и их комплексных соединений (в соотношении 1:1) на репродукцию штамма ВИЧ-1evk в культуре клеток МТ-4.
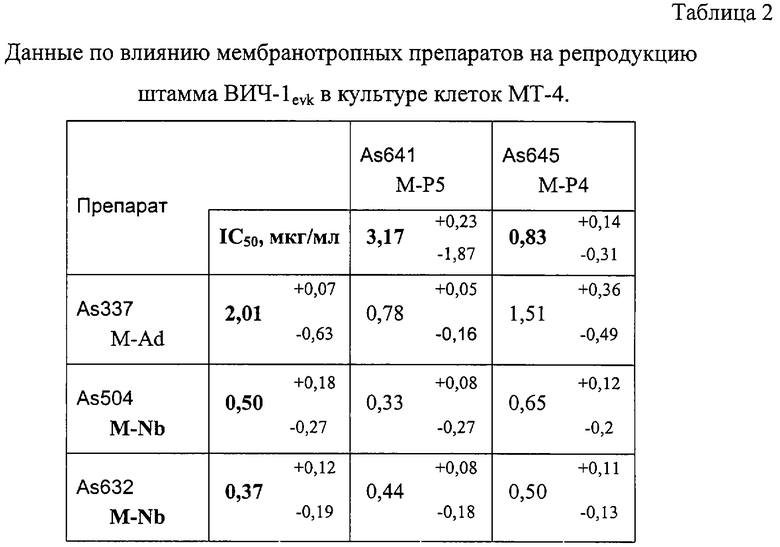
Как следует из полученных данных (таблица 2), лучшие показатели подавления продукции вирусного белка р24 (IC50) обнаруживают комбинации препаратов As337, As504 и As632 с соединением As641, содержащим пептид Р5 -имитатор N-концевого фрагмента корецептора ВИЧ-1/2 CCR5 (IC50=0,78; 0,33 и 0,44 (мкг/мл), соответственно). Комбинационные индексы (CI), рассчитанные по значениям IC50 и IC90 данных препаратов и их смесей, указывают на синергизм либо независимость действия этих соединений.
Данные о совместном антиВИЧ действии заявляемых препаратов
В таблице 3 представлено совместное антиВИЧ действие мембранотропных препаратов, модифицированных гидрофобными агентами и пептидсодержащего соединения As641. Как видно из таблицы 3, наиболее удачным для комбинаций с Ad-/Nb-/Nba-модифицированными соединениями оказался пептидсодержащий препарат As641 (М-Р5). Он в двух случаях проявил синергизм действия и в одном - независимый характер действия.
Дополнительно был проведен анализ антиВИЧ активности комбинаций данных препаратов, кроме As639, в других соотношениях (M-Nb/Ad-М-Р-5:1; 10:1) и только на стадии адсорбции ВИЧ на пермиссивные клетки (1 час). Проявляемый препаратами антиВИЧ эффект при использовании только на стадии адсорбции вируса подтвердил верность утверждения о действии соединений на первоначальных этапах проникновения ВИЧ в чувствительные клетки. Результаты этих экспериментов представлены в таблицах 4-5.
Данные о действии препарата при взаимодействии с вирусом на разных стадиях
Как видно из представленных данных в табл.4, мембранотропные бинарные препараты и их комбинации при внесении только на стадии адсорбции вируса эффективно ингибируют репродукцию ВИЧ и обеспечивают защиту клеток от инфекции. Наиболее эффективными являются сочетания препаратов As504+As641, As504+As643 и As337+As645, которые демонстрируют выраженный синергизм антиВИЧ действия. Препарат As643 (M-P3) эффективно ингибирует накопление р24 в комбинациях как с адамантановым (As337), так и норборнановыми (As504, As632) производными.
В табл.5 представлены результаты изучения антиВИЧ эффективности комбинаций бинарных препаратов в различных их соотношениях
АнтиВИЧ эффективность комбинаций бинарных препаратов в различных их соотношениях (клетки МТ-4, ВИЧ-1evk)
Как видно из представленных данных, комплекс мембранотропных соединений в различных сочетаниях при внесении только на стадии адсорбции вируса эффективно ингибирует репродукцию ВИЧ-1evk и обеспечивает защиту клеток от инфекции. Наиболее эффективными являются сочетания препаратов As504+As641, As337+As645, которые ингибируют наработку р24 ВИЧ-1 в концентрациях <1.0 mkg/ml. Таким образом, можно считать, что сочетание бинарных препаратов обеспечивает наиболее оптимальные условия для эффективного подавления ВИЧ-1 в экспериментальной модели. Сочетание препаратов As504+As641 может оказаться эффективным на начальных этапах инфекции, когда присутствуют штаммы ВИЧ, тройные к корецептору CCR5, в то время как сочетание препаратов As337+As645 может оказаться эффективным на поздних этапах инфекции, когда присутствуют штаммы ВИЧ-тропные к корецептору CxCR4.
Активность комплексных мембранотропных соединений As504 и As641 на различных штаммах ВИЧ-1, включая охарактеризованные по корецепторной специфичности HIV-1 SF162(CCR5) и HIV-1 LAV04(C×CR4) свидетельствует об избирательности их антиВИЧ эффективности.
На штамме SF162 работают лучше норборненсодержащий препарат As504 и бинарный препарат с пептидом-имитатором активного домена корецептора CCR5 - As641, что позволяет предположить, что на ранних стадиях ВИЧ-инфекции при инфицировании CCR5 тропными вариантами предпочтительными могут быть норборненсодержащие препараты и пептидсодержащие бинарные соединения. В то время как на поздних стадиях развития СПИДа при доминировании C×CR4 вариантов ВИЧ могут иметь преимущество уже адамантансодержащие препараты.
Преимущества предлагаемого комплекса мембранотропных соединений против ВИЧ-инфекции по сравнению с известным заключаются в том, комбинированное применение мембранотропных соединений обеспечивает блокирование ВИЧ-инфекции на самых ранних этапах взаимодействия вирус-клетка, синергизм препаратов обеспечивается тем, что модификаторы полианионной матрицы - норборнен или адамантан и пептиды-имитаторы корецептора ВИЧ-1/2, связываются с различными сайтами gp120 ВИЧ-1 и тем самым исключается вероятность конкуренции и взаимные стерические затруднения вирусспецифических фармакофоров-модификаторов. При этом заявляемое комплексное соединение воздействуют на более широкий круг мишеней вируса иммунодефицита человека на самых ранних этапах взаимодействия вирус-клетка.
Источники информации
1. Международная заявка (WO) 94/24168, МПК С07К 17/08, опубл. 27.10.1994.
2. Kolocouris N., Foscolos G.B., Kolocouris A. et al. - Synthesis and antiviral activity evaluation of some new aminoadamantane derivatives. J. Med. Chem. 1994; 37: 2896-2902.
3. Сербин А.В., Стоцкая Л.Л., Кренцель Б.А. и др. Сополимеры на основе фурана и малеинового ангидрида и перспективы их использования в медицине. Сб. Полимеры медицинского назначения. - М.: ИНХС, 1988; 127-152.
4. Тимофеев Д.И., Перминова Н.Г., Сербин А.В. и др. Мембранотропные соединения и препараты, воздействующие на ранние стадии ВИЧ-инфекции. Антибиотики и химиотерапия 2003; 48: 2: 29-41.
5. Патент США №6514979, МПК А61К 31/52, опубл. 04.02.2003 г.
6. Патент США №5880154, А, МПК C08F 22/06, опубл. 09.03.1999 (прототип).
7. Патент РФ №2079491, МПК С07С 317/48, опубл. 20.05.1997.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПЛЕКСНОЕ АНТИ-ВИЧ СОЕДИНЕНИЕ | 2004 |
|
RU2270690C1 |
| КОМПЛЕКСНАЯ АУТОЛОГИЧНАЯ ВАКЦИНА ПРОТИВ ВИЧ-ИНФЕКЦИИ И СПИД | 2005 |
|
RU2306950C2 |
| НОВЫЕ Tat-КОМПЛЕКСЫ И ВКЛЮЧАЮЩИЕ ИХ ВАКЦИНЫ | 2005 |
|
RU2432356C2 |
| Генетическая конструкция для экспрессии генов mNG_CD4-CXCR4, рекомбинантная плазмида rVSV_mNG_CD4-CXCR4 и рекомбинантный штамм вируса везикулярного стоматита rVSV_mNG_CD4-CXCR4, обеспечивающий таргетный виролизис клеток, экспонирующих на своей поверхности белки gp120/gp 41 ВИЧ-1 тропности X4 | 2021 |
|
RU2768032C1 |
| Генетическая конструкция для экспрессии генов mNG_CD4-CCR5, рекомбинантная плазмида rVSV_mNG_CD4-CCR5 и рекомбинантный штамм вируса везикулярного стоматита rVSV_mNG_CD4-CCR5, обеспечивающий таргетный виролизис клеток, экспонирующих на своей поверхности белки gp120/gp41 ВИЧ-1 тропности R5 | 2021 |
|
RU2769125C1 |
| ШТАММ 02_AG.RU.09RU2204 ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА 1 ТИПА РЕКОМБИНАНТНОГО СУБТИПА 02_AG, ИСПОЛЬЗУЕМЫЙ ДЛЯ ДИАГНОСТИКИ И ИЗУЧЕНИЯ ЭФФЕКТИВНОСТИ ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2010 |
|
RU2415931C1 |
| ПОЛИАНИОННЫЕ ПРОИЗВОДНЫЕ НОРБОРНАНА, СПОСОБ ПОЛУЧЕНИЯ И ИНГИБИТОРЫ РЕПРОДУКЦИИ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА НА ИХ ОСНОВЕ | 2004 |
|
RU2281297C2 |
| ДВОЙНОЙ ВЕКТОР ДЛЯ ПОДАВЛЕНИЯ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА | 2010 |
|
RU2562868C2 |
| КОНСТРУКЦИИ АНТИТЕЛ И ХЕМОКИНОВ И ИХ ПРИМЕНЕНИЕ ПРИ ИММУНОЛОГИЧЕСКИХ НАРУШЕНИЯХ | 2001 |
|
RU2252786C2 |
| АНТИТЕЛО ПРОТИВ CCR5 | 2003 |
|
RU2322454C2 |
Изобретение относится к биологии и медицине и может быть использовано для профилактики ВИЧ-инфекции и лечения СПИДа, а также в исследовательской работе для изучения лиганд-рецепторных взаимодействий (типа поверхностные вирусные белки - клеточные рецепторы). Изобретение заключается в создание комплекса мембранотропных соединений, обеспечивающих адресную доставку противовирусного препарата к очагу поражения ВИЧ-1/2 и подавление специфической вирусной инфекции на начальных и более поздних этапах ее развития. Данное изобретение обеспечивает воздействие на более широкий круг мишеней вируса иммунодефицита человека и блокирование ВИЧ-инфекции на самых ранних этапах взаимодействия вирус-клетка за счет синергизма входящих в комплекс соединений, который заключается в том, что модификаторы полианионной матрицы-норборнен или адамантан и пептиды-имитаторы корецептора ВИЧ-1/2 связываются с различными сайтами gp120 ВИЧ-1, тем самым исключается вероятность конкуренции и взамные стерические затруднения вирус-специфичных фармакофоров-модификаторов. 2 з.п. ф-лы, 2 ил., 5 табл.
а вторая полианионная матрица и связанный с ней фармакофор норборнен или фармакофор адамантан имеют следующую общую формулу:
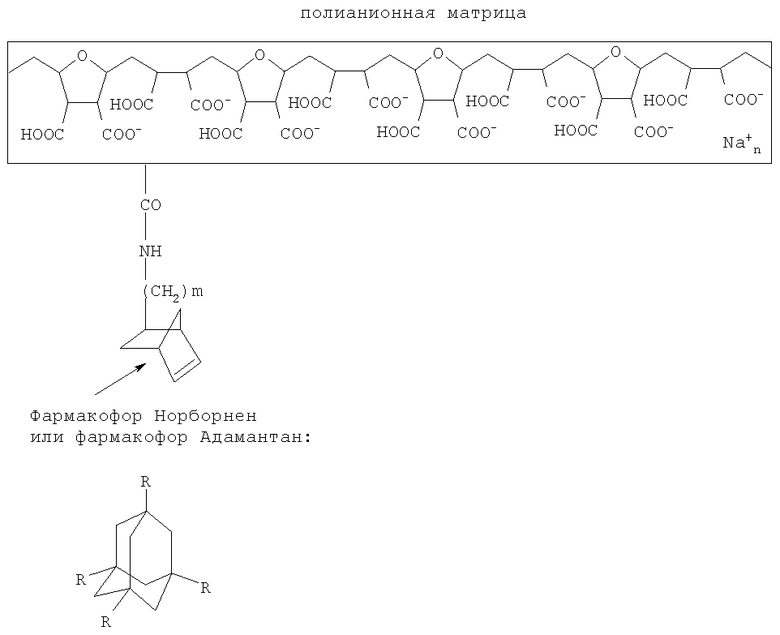
где R - замещенный или незамещенный NH2,
причем соотношение первой полианионной матрицы с химически с ней связанным пептидным фрагментом корецептора ВИЧ-1/2 CCR5 или CXCR4 и второй полианионной матрицы с химически с ней связанным фармакофором норборненом или фармакофором адамантаном находится в пределах от 1:10 до 1:1.
| US 5880154 A, 09.03.1999 | |||
| JP 2002338600 А, 27.11.2002 | |||
| СПОСОБ СЕЛЕКТИВНОЙ КРИСТАЛЛИЗАЦИИ Z-ИЗОМЕРА ИОПРОМИДА | 2009 |
|
RU2481325C2 |
| US 2003139571 A1, 24.07.2003 | |||
| КИСЕЛЕВА Я.Ю | |||
| и др | |||
| "Противовирусная активность мембранотропных соединений, модифицированных адамантановыми и норборненовыми фармакофорами, в отношении различных штаммов ВИЧ-1", Молекулярная генетика, микробиология и вирусология, 2005, | |||
Авторы
Даты
2008-01-27—Публикация
2005-09-29—Подача