Перекрестная ссылка на родственную заявку
Данная заявка основывается на предварительной заявке США 60/337927, поданной 8 ноября 2001, которая полностью включена в данное описание в качестве ссылки.
Область изобретения
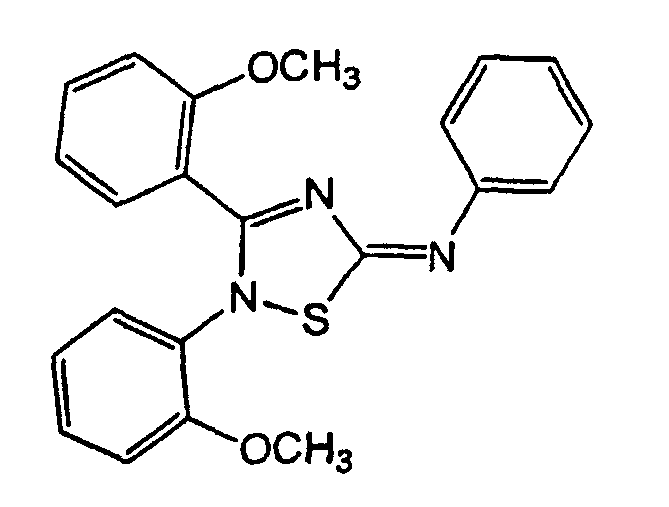
Настоящее изобретение относится к новым производным 1,2,4-тиадиазола, которые могут применяться для лечения нарушения, опосредованного рецептором меланокортина. Более конкретно, соединения настоящего изобретения могут применяться для лечения метаболических нарушений, нарушений, связанных с ЦНС, и дерматологических нарушений, таких, как ожирение, пониженная толерантность к глюкозе при пероральном применении, повышенные уровни глюкозы в крови, диабет типа II, синдром X, диабетическая ретинопатия, острые нейродегенеративные нарушения, хронические нейродегенеративные нарушения, плексопатии, эректильная дисфункция у самцов, сухие глаза, угри, сухая кожа, старая кожа, себорейный дерматит, розовые угри, избыточная ушная сера, заболевание мейбомиевой железы, псевдофолликулит, дрожжевые инфекции, перхоть, гнойный гидраденит, красные глаза и заболевание эккринной железы.
Предпосылки создания изобретения
Меланокортины представляют собой нейропептиды, образующиеся из проопиомеланокортина (POMC - pro-opiomelanocortin), который преимущественно экспрессируется в аркуатном ядре гипоталамуса, долях гипофиза и в ядре отдельного пучка ствола головного мозга. [Gantz, I., et al., Molecular Cloning, Expression, and Gene Localization of a Fourth Melanocortin Receptor, J. Biolog. Chem., 1993, 268, 15174-15179]. Данные пептиды включают ACTH, α-MSH, β-MSH, γ1-3-MSH, а также синтетический аналог NDP-αMSH (Wikberg, J E S, Melanocortin receptors: new opportunities in drug discovery, Exp. Opin. Ther. Patents, 2000, 11(1), 61-76).
Данные пептиды связываются с пятью типами рецепторов меланокортина (MC1-MC5), представляющими собой рецепторы, сопряженные с G-белком, все из которых положительно модулируют аденилатциклазу. Рецепторы MC4 и MC5 широко распространены в мозге и спинном мозге, тогда как рецептор MC3 преимущественно локализован в гипоталамусе [Gantz,I., et al., supra]. Рецептор MC4 избирательно активируется αMSH и может вызывать рост аксонов в клетках Neuro 2A. (Adan R. A. H, et al., Molecular Brain Research, 1996, 36, pp 37-44; Mountjoy, K. G., Mortud, M. T., Low, M. J., Simerly, R. B. and Cone, R. D., Mol. Endocrinol., 1994, 8, pp. 1298-1308). ACHT является менее эффективным активатором рецептора MC4, чем αMSH (Adan, R. A. H., Cone, R. D., Burbach, J. P. H. and Gispen, W. H., mol. pharmacol., 1994, 46, pp. 1182-1190). Рецептор MC5 активируется, в порядке возрастания, под действием NDP ≈ α-MSH > ACHT (1-24) ≥ αMSH ACHT (1-39) = βMSH >> γMSH (The Melanocortin Receptors, Cone, R. D., Editor, Human Press Inc., Totowa, N. J., 2000, Chen, W., pp. 449-472).
Проводимые на интактных животных исследования модели измельченного седалищного нерва крысы показали, что α-MSH увеличивает рост аксонов и, как наиболее активный из производных от ACTH пептидов, в значительной степени стимулирует ветвление нервных окончаний, обуславливает величину площади и периметра концевой области. [Bijlsma, W. A., et al., The Enhanced Recovery of Sensorimotor Function in Rats is Related to the Melantropic Moiety of ACTH/MSH Neuropeptides, Eur. J. Pharmacol, 1983, 92, 231-236; Van der Neut. R., et al., Stimulation by Melanocortins of Neurite Outgrowth from Spinal and Sensory Neurons In Vitro, Peptides, 1992, 13, 1109-1115; Van Der Zee, C. E. E. M., et al., α-MSH and Org 2766 in Peripheral Nerve Regeneration: Different Route of Delivery, Eur. J. Pharmacol., 1988, 147, 351-357; Strand, F. L., et al., Melanocortins as Factors in Somatic Neuromuscular Growth and Regrowth, Pharmac. Ther., 1994, 62, 1-27]. Кроме того, при применении αMSH и других меланокортинов восстановление двигательной функции после повреждения нерва происходит быстрее [Strand, F. L., et al., supra].
Мыши, у которых рецептор MC4 приведен в неактивное состояние путем направленного воздействия на ген, становятся тучными, что позволяет предположить, что рецептор MC4 участвует в процессе усвоения пищи. [Huszar, D., et al., Targeted Disruption of the Melanocortin-4 Receptor Results in Mice, Cell, 1997, 88, 131-141]. Это подтверждается тем фактом, что различные агонисты пептида MC4 ингибируют пищевое поведение у агутиевых мышей. [Fan, W., et al., Role of Melanocortingenic Neurons in Feeding and the Agouti Obesity Syndrome, Nature, 1997,385, 165-168]. α-MSH вызывает груминг у крыс, значение данного факта неясно и, возможно, этот процесс не опосредуется рецептором MC4. [Adan, R. A. H., et al., Differential Effects of Melanocortin Peptides on Neural Melanocortin Receptors, Molecular Pharmacology, 1994, 46, 1182-1190].
Также известно, что меланокортины αMSH и ACTH способны стимулировать пигментацию и секрецию глюкокортикоидов в надпочечниках, соответственно. Роль меланокортинов, особенно αMSH, в регуляции активности сальной железы (экзокринная железа с голокринным типом секреции) первоначально была продемонстрирована на крысах. Более конкретно, исследования показали, что удаление промежуточной доли гипофиза (которая продуцирует пептиды POMC) приводит к уменьшению продукции сальных липидов, с полным возвращением к нормальным уровням после заместительной терапии αMSH (Thody, A. J. and Shuster, Nature, 237, 346-347, 1972). В эксперименте на крысах после тотальной гипофизэктомиии обработка αMSH приводит к увеличению продукции кожного сала, хотя полное восстановление продукции кожного сала достигается только после обработки сочетанием αMSH с тестостероном (Thody, A. J., Shuster, S., J. Endocr. 64, 503-510, 1975; Ebling, F. J., Ebling, E., Randall, V. and Skinner, J., J. Endocr. 66, 407-412, 1975). Было обнаружено, что мыши с выбитым геном, у которых отсутствует рецептор MC5, обладают тяжелым дефектом водоотталкивания и терморегуляции вследствие уменьшения продукции сальных липидов (Chen, W. Kelly, M. A., Opitz-Araya, X., Thomas, R. E., Low, M. J., and Cone, R., Cell, 91, 788-798, 1997).
Известно, что рецептор MC5 экспрессируется в сальных железах человека, и что он может участвовать в регуляции синтеза сальных липидов. Человеческий MC5-R клонировали и охарактеризовали (Chhajlani, V., Muceniece, R., Wikberg, JES., Biochem. Biophys. Res. Commun. 195, 866-873, 1993). Кроме того, методом ревертазо-ПЦР было показано, что в человеческих сальных железах присутствует мРНК MC5-R, белок определяли методами иммуногистохимии и вестерн-блоттинга (Thiboutot, D., Sivarajah, Gililand, K., Cong, Z. and Clawson, G., J. Invest. Dermatol. 115 (4), 614-619, 2000).
Человеческое кожное сало отличается по составу от кожного сала других млекопитающих. Основными липидами человеческого кожного сала являются триглицериды, сложные эфиры воска и сквален (Greene, R. S., Downing, D. T., Poci, P. E., Strauss, J. S., JID 54, 240-247, 1970). Например, сквален не обнаружен у многих млекопитающих, за исключением выдры и бобра. Триглицерид, который представляет собой основной компонент человеческого кожного сала, плохо представлен у других видов, а у многих (например, у шимпанзе), по-видимому, совсем отсутствует (Thody, A. J., Shuster, S., Physiolog. Rev. 69, 383-415, 1989). Кроме того, действие меланокортинов на клетки может различаться у разных видов. Например, и αMSH (EC50=3,7 нМ), и ACTH (EC50=16,4 нМ) являются активными липолитическими агентами для кроличьих адипоцитов, тогда как у крыс только ACTH (EC50=1,34 нМ) обладает высокой липолитической активностью (Ramachadran, J., Lee, V., 428, 339-346, 1987; Richter, W. O., Schwandt, P., Neuropeptides 9, 59-74, 1987). Несмотря на липолитическую активность, проявляемую у грызунов и кроликов, ACTH оказывает очень слабое воздействие на липолиз в выделенных адипоцитах человека и отличных от человека приматов, даже при таких высоких концентрациях, как 1 мкМ (Ng, T. B. Comparative Biochem. 97, 441-446, 1990). Таким образом, установление роли меланокортинов и их рецепторов на животных модельных системах сальных желез не всегда позволяет предсказать их роль в регуляции человеческих сальных липидов.
Недавно Basu et. al. в публикации WIPO WO99/55679 описали изохинолиновые производные, небольшие молекулы непептидных соединений, которые обладают низким микромолярным сродством к рецепторам MC1 и MC4, уменьшают воспаление кожи, вызванное арахидоновыми кислотами, а также уменьшают массу тела и потребление пищи.
Nargund et.al., в публикации WIPO WO99/64002 описали производные спиропиперидина в качестве агонистов рецептора меланокортина, которые могут применяться для лечения таких заболеваний и нарушений как ожирение, диабет и половая дисфункция.
Таким образом, существует потребность в низкомолекулярных модуляторах рецепторов меланокортина, более конкретно, рецепторов меланокортина-3, меланокортина-4 и/или меланокортина-5.
Краткое описание изобретения
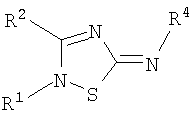
Настоящее изобретение относится к соединениям общей формулы (II)
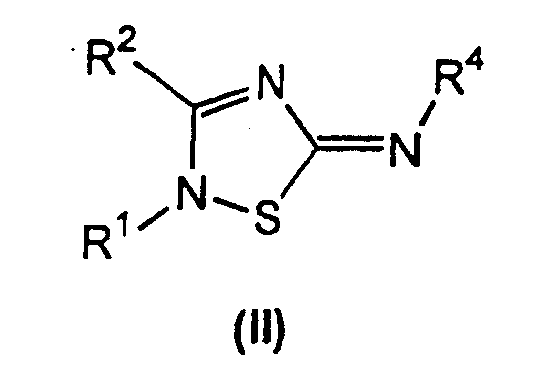
где
R1 выбран из группы, включающей гетероарил, гетероарилалкил, гетероциклоалкил, гетероциклоалкилалкил, циклоалкил, циклоалкилалкил, замещенный арил и замещенный аралкил (R1 не является незамещенным арилом или незамещенным аралкилом);
где гетероарильная, гетероарилалкильная, гетероциклоалкильная, гетероциклоалкилалкильная, циклоалкильная или циклоалкилалкильная группа необязательно замещена одним или несколькими заместителями, независимо выбранными из галогена, гидрокси, алкила, алкокси; галогенированного алкила, галогенированного алкокси, амино, алкиламино или ди(алкил)амино;
где арильная или аралкильная группа замещена одним или несколькими заместителями, независимо выбранными из галогена, гидрокси, алкила, алкокси; галогенированного алкила, галогенированного алкокси, амино, алкиламино или ди(алкил)амино;
R2 выбран из группы, включающей гетероарил, гетероарилалкил, гетероциклоалкил, гетероциклоалкилалкил, циклоалкил, циклоалкилалкил, замещенный арил и замещенный аралкил; (R2 не является незамещенным арилом или незамещенным аралкилом);
где гетероарильная, гетероарилалкильная, гетероциклоалкильная, гетероциклоалкилалкильная, циклоалкильная или циклоалкилалкильная группа необязательно замещена одним или несколькими заместителями, независимо выбранными из галогена, гидрокси, алкила, алкокси; галогенированного алкила, галогенированного алкокси, амино, алкиламино или ди(алкил)амино;
где арильная или аралкильная группа замещена одним или несколькими заместителями, независимо выбранными из галогена, гидрокси, алкила, алкокси; галогенированного алкила, галогенированного алкокси, амино, алкиламино или ди(алкил)амино;
R4 выбран из группы, включающей арил, аралкил, гетероарил, гетероциклоалкил и циклоалкилалкил; где арильная, аралкильная, гетероарильная, гетероциклоалкильная или циклоалкилалкильная группа необязательно замещена одним или несколькими заместителями, независимо выбранными из галогена, гидрокси, алкила, алкокси; галогенированного алкила, галогенированного алкокси, амино, алкиламино или ди(алкил)амино;
при условии, что если R1 представляет собой арил, замещенный одним атомом галогена, и R4 представляет собой арил, замещенный одним атомом галогена, то R2 не является морфолинилом;
и их фармацевтически приемлемые соли.
Настоящее изобретение также касается соединений общей формулы (II)

где
R1 выбран из группы, включающей гетероарил, гетероарилалкил, гетероциклоалкил, гетероциклоалкилалкил, циклоалкил, циклоалкилалкил, замещенный арил и замещенный аралкил (R1 не является незамещенным арилом или незамещенным аралкилом);
где гетероарильная, гетероарилалкильная, гетероциклоалкильная, гетероциклоалкилалкильная, циклоалкильная или циклоалкилалкильная группа необязательно замещена одним или несколькими заместителями, независимо выбранными из галогена, гидрокси, алкила, алкокси; галогенированного алкила, галогенированного алкокси, амино, алкиламино или ди(алкил)амино;
где арильная или аралкильная группа замещена одним или несколькими заместителями, независимо выбранными из галогена, гидрокси, алкила, алкокси; галогенированного алкила, галогенированного алкокси, амино, алкиламино или ди(алкил)амино;
R2 выбран из группы, включающей арил, аралкил, гетероарил, гетероарилалкил, гетероциклоалкил, гетероциклоалкилалкил, циклоалкил, циклоалкилалкил, замещенный арил и замещенный аралкил;
где арильная, аралкильная, гетероарильная, гетероарилалкильная, гетероциклоалкильная, гетероциклоалкилалкильная, циклоалкильная или циклоалкилалкильная группа необязательно замещена одним или несколькими заместителями, независимо выбранными из галогена, гидрокси, алкила, алкокси; галогенированного алкила, галогенированного алкокси, амино, алкиламино или ди(алкил)амино;
R4 выбран из группы, включающей гетероарил, гетероциклоалкил, циклоалкилалкил, замещенный арил и замещенный аралкил (R4 не является незамещенным арилом или незамещенным аралкилом);
где гетероарильная, гетероциклоалкильная или циклоалкилалкильная группа необязательно замещена одним или несколькими заместителями, независимо выбранными из галогена, гидрокси, алкила, алкокси; галогенированного алкила, галогенированного алкокси, амино, алкиламино или ди(алкил)амино;
где арильная или аралкильная группа замещена одним или несколькими заместителями, независимо выбранными из галогена, гидрокси, алкила, алкокси; галогенированного алкила, галогенированного алкокси, амино, алкиламино или ди(алкил)амино;
при условии, что если R1 представляет собой арил, замещенный одним атомом галогена, и R4 представляет собой арил, замещенный одним атомом галогена, то R2 не является морфолинилом;
а также при условии, что если R1 представляет собой метилфенил и R4 представляет собой метоксифенил, то R2 выбран из группы, включающей аралкил, гетероарил, гетероарилалкил, гетероциклоалкил, гетероциклоалкилалкил, циклоалкил, циклоалкилалкил и замещенный арил;
где аралкильная, гетероарильная, гетероциклоалкильная или циклоалкильная группа необязательно замещена одним или несколькими заместителями, независимо выбранными из галогена, гидрокси, алкила, алкокси; галогенированного алкила, галогенированного алкокси, амино, алкиламино или ди(алкил)амино;
где арильная группа замещена одним или несколькими заместителями, независимо выбранными из галогена, гидрокси, алкила, алкокси; галогенированного алкила, галогенированного алкокси, амино, алкиламино или ди(алкил)амино;
и их фармацевтически приемлемые соли.
Настоящее изобретение также касается способа лечения нарушений, опосредованных рецептором меланокортина, включающего введение субъекту, нуждающемуся в лечении, терапевтически эффективного количества соединения формулы (II)

где
R1 выбран из группы, включающей алкил, арил, аралкил, гетероарил, гетероарилалкил, гетероциклоалкил, гетероциклоалкилалкил, циклоалкил и циклоалкилалкил; где арильная, аралкильная, гетероарильная, гетероарилалкильная, гетероциклоалкильная, гетероциклоалкилалкильная, циклоалкильная или циклоалкилалкильная группа необязательно замещена одним или несколькими заместителями, независимо выбранными из галогена, гидрокси, алкила, алкокси; галогенированного алкила, галогенированного алкокси, амино, алкиламино или ди(алкил)амино;
R2 выбран из группы, включающей алкил, арил, аралкил, гетероарил, гетероциклоалкил и циклоалкилалкил; где арильная, аралкильная, гетероарильная, гетероарилалкильная, гетероциклоалкильная, гетероциклоалкилалкильная, циклоалкильная или циклоалкилалкильная группа необязательно замещена одним или несколькими заместителями, независимо выбранными из галогена, гидрокси, алкила, алкокси; галогенированного алкила, галогенированного алкокси, амино, алкиламино или ди(алкил)амино;
R4 выбран из группы, включающей водород, алкил, арил, аралкил, гетероарил, гетероциклоалкил и циклоалкилалкил; где арильная, аралкильная, гетероарильная, гетероциклоалкильная или циклоалкилалкильная группа необязательно замещена одним или несколькими заместителями, независимо выбранными из галогена, гидрокси, алкила, алкокси; галогенированного алкила, галогенированного алкокси, амино, алкиламино или ди(алкил)амино;
и его фармацевтически приемлемых солей.
Иллюстративным примером данного изобретения является фармацевтическая композиция, включающая фармацевтически приемлемый носитель и любое из описанных выше соединений. Иллюстрацией данного изобретения является фармацевтическая композиция, полученная путем смешивания любого из описанных выше соединений с фармацевтически приемлемым носителем. Иллюстрацией данного изобретения является способ получения фармацевтической композиции, включающий смешивание любого из описанных выше соединений с фармацевтически приемлемым носителем.
Иллюстрацией данного изобретения являются способы лечения нарушений, опосредованных рецептором меланокортина, у субъекта, нуждающегося в таком лечении, включающие введение субъекту терапевтически эффективного количества любого из описанных выше соединений или фармацевтических композиций.
Воплощением настоящего изобретения является применение любого из описанных здесь соединений для лечения нарушения, выбранного из группы, включающей метаболические нарушения, нарушения, связанные с ЦНС, и дерматологические нарушения.
Примером данного изобретения является способ лечения нарушения, выбранного из группы, включающей ожирение, пониженную толерантность к глюкозе при пероральном применении, повышенные уровни глюкозы в крови, диабет типа II, синдром X, диабетическую ретинопатию, повреждение спинного мозга, повреждение нерва, острые нейродегенеративные нарушения, хронические нейродегенеративные нарушения, плексопатию, эректильную дисфункцию у самцов, сухие глаза, угри, сухую кожу, старую кожу, себорейный дерматит, розовые угри, избыточную ушную серу, заболевание мейбомиевой железы, псевдофолликулит, дрожжевые инфекции, перхоть, гнойный гидраденит, красные глаза и заболевание эккринной железы, у субъекта, нуждающегося в таком лечении, который включает введение субъекту любого из описанных выше соединений или фармацевтических композиций в терапевтически эффективном количестве.
Другим примером данного изобретения является применение любого из описанных здесь соединений в производстве лекарственного средства для лечения: (a) ожирения, (b) пониженной толерантности к глюкозе при пероральном применении, (c) повышенных уровней глюкозы в крови, (d) диабета типа II, (e) синдрома X, (f) диабетической ретинопатии, (g) острого нейродегенеративного нарушения, (h) хронического нейродегенеративного нарушения, (i) плексопатии, (j) эректильной дисфункции у самцов, (k) сухих глаз,(l) угрей, (m) сухой кожи, (n) старой кожи, (o) себорейного дерматита, (p) розовых угрей, (q) избыточной ушной серы, (r) заболевания мейбомиевой железы, (s) псевдофолликулита, (t) дрожжевых инфекций, (u) перхоти, (v) гнойного гидраденита, (w) красных глаз или (x) заболевания эккринной железы, у субъекта, нуждающегося в таком лечении.
Подробное описание изобретения
Настоящее изобретение относится к новым замещенным производным 1,2,4-тиадиазола, которые могут применяться для лечения нарушений, опосредованных рецептором меланокортина. Более конкретно, настоящее изобретение касается соединений формулы (II)

где R1, R2 и R4 такие, как указано выше, которые могут использоваться как агонисты или антагонисты рецептора меланокортина.
Настоящее изобретение также относится к способу лечения нарушения, опосредованного рецептором меланокортина, предпочтительно, нарушения, чувствительного к лечению агонистом или антагонистом рецептора меланокортина. Предпочтительно рецептор меланокортина выбран из группы, включающей рецептор меланокортина-3, меланокортина-4 и меланокортина-5, более предпочтительно, рецептор меланокортина представляет собой рецептор меланокортина-4 или меланокортина-5.
В одном воплощении настоящего изобретения R1 выбран из группы, включающей арил, аралкил и гетероарил; где арильная, аралкильная или гетероарильная группа необязательно замещена одним или несколькими заместителями, независимо выбранными из галогена, гидрокси, алкила, алкокси; тригалогенметила, тригалогенметокси, амино, алкиламино или ди(алкил)амино. Предпочтительно, R1 выбран из группы, включающей арил; где арильная группа необязательно замещена одним или несколькими заместителями, независимо выбранными из галогена, алкила и алкокси. Более предпочтительно, R1 выбран из группы, включающей фенил, 2-хлорфенил, 4-хлорфенил, 2-метилфенил, 4-метилфенил, 2-метоксифенил и 4-метоксифенил. Наиболее предпочтительно R1 представляет собой 2-метоксифенил.
В другом воплощении настоящего изобретения R1 выбран из группы, включающей замещенный арил и замещенный аралкил, где арил или аралкил замещен одним или двумя заместителями, независимо выбранными из галогена, гидрокси, алкила, алкокси, тригалогенметила, тригалогенметокси, амино, алкиламино или ди(алкил)амино. Предпочтительно, R1 выбран из группы, включающей замещенный арил; где арильная группа замещена заместителем, выбранным из галогена, алкила или алкокси. Более предпочтительно, R1 представляет собой 2-метоксифенил.
В следующем воплощении настоящего изобретения, R1 выбран из группы, включающей замещенный арил и замещенный аралкил; где арильная или аралкильная группа замещена одним или несколькими заместителями, независимо выбранными из галогена, гидрокси, алкила, алкокси; галогенированного алкила, галогенированного алкокси, амино, алкиламино или ди(алкил)амино.
В одном воплощении настоящего изобретения, R2 выбран из группы, включающей арил, аралкил и гетероарил; где арильная, аралкильная или гетероарильная группа необязательно замещена одним или несколькими заместителями, независимо выбранными из галогена, гидрокси, алкила, алкокси; тригалогенметила, тригалогенметокси, амино, алкиламино или ди(алкил)амино. Предпочтительно, R2 выбран из группы, включающей арил; где арильная группа необязательно замещена одним или несколькими заместителями, независимо выбранными из алкила и алкокси. Более предпочтительно, R2 выбран из группы, включающей фенил, 4-метилфенил, 2-метоксифенил и 4-метоксифенил. Наиболее предпочтительно, R2 выбран из группы, включающей фенил и 2-метоксифенил.
В другом воплощении настоящего изобретения R2 выбран из группы, включающей замещенный арил и замещенный аралкил, где арил или аралкил замещен одним или двумя заместителями, независимо выбранными из галогена, гидрокси, алкила, алкокси, тригалогенметила, тригалогенметокси, амино, алкиламино или ди(алкил)амино. Предпочтительно, R2 выбран из группы, включающей замещенный арил; где арильная группа замещена заместителем, выбранным из алкила или алкокси. Более предпочтительно, R2 представляет собой 2-метоксифенил.
В следующем воплощении настоящего изобретения, R2 выбран из группы, включающей арил и аралкил; где арильная или аралкильная группа необязательно замещена одним или несколькими заместителями, независимо выбранными из галогена, гидрокси, алкила, алкокси; галогенированного алкила, галогенированного алкокси, амино, алкиламино или ди(алкил)амино.
В одном воплощении настоящего изобретения R4 выбран из группы, включающей арил, аралкил и гетероарил; где арильная, аралкильная или гетероарильная группа необязательно замещена одним или несколькими заместителями, независимо выбранными из галогена, гидрокси, алкила, алкокси; тригалогенметила, тригалогенметокси, амино, алкиламино или ди(алкил)амино. Предпочтительно, R4 выбран из группы, включающей арил, аралкил и гетероарил; где арильная или аралкильная группа необязательно замещена одним или несколькими заместителями, независимо выбранными из галогена, алкила и алкокси. Более предпочтительно, R4 выбран из группы, включающей фенил, 2-хлорфенил, 4-хлорфенил, 4-бромфенил, 2-метилфенил, 4-метилфенил, 2-метоксифенил, 4-метоксифенил, бензил, 2-хлорбензил, 4-хлорбензил, 2-метилбензил, 4-метилбензил, 2-метоксибензил, 4-метоксибензил, 2,6-дифторфенил, 3,5-дифторфенил, 2-хлор-6-метилфенил и 3-пиридил. Наиболее предпочтительно, R4 выбран из группы, включающей фенил, 2-метилфенил, 4-метилфенил, 2-метоксифенил и 4-метоксифенил.
В другом воплощении настоящего изобретения R4 выбран из группы, включающей арил, аралкил или гетероарил; где арильная, аралкильная или гетероарильная группа необязательно замещена одним или несколькими заместителями, независимо выбранными из галогена, гидрокси, алкила, алкокси, тригалогенметила, тригалогенметокси, амино, алкиламино, ди(алкил)амино. Предпочтительно, R4 выбран из группы, включающей арил и замещенный арил; где арил имеет один или два заместителя, независимо выбранных из галогена, алкила или алкокси. Более предпочтительно, R4 выбран из группы, включающей фенил, 4-метоксифенил, 2,6-дифторфенил, 2-хлор-6-метилфенил и 3,5-дифторфенил.
В следующем воплощении настоящего изобретения R4 выбран из группы, включающей замещенный арил и замещенный аралкил; где арильная или аралкильная группа замещена одним или несколькими заместителями, независимо выбранными из галогена, гидрокси, алкила, алкокси; галогенированного алкила, галогенированного алкокси, амино, алкиламино или ди(алкил)амино.
В данном описании, если не указано иначе, термин "нарушения, опосредованные рецептором меланокортина" включает, не ограничиваясь ими, ожирение, пониженную толерантность к глюкозе при пероральном применении, повышенные уровни глюкозы в крови, диабет типа II, синдром X, диабетическую ретинопатию, острые нейродегенеративные нарушения, хронические нейродегенеративные нарушения, плексопатии, эректильную дисфункцию у самцов, сухие глаза, угри, сухую кожу, старую кожу, себорейный дерматит, розовые угри, избыточную ушную серу, заболевание мейбомиевой железы, псевдофолликулит, дрожжевые инфекции, перхоть, гнойный гидраденит, красные глаза и заболевание эккринной железы.
В данном описании, если не указано иначе, термин "метаболические нарушения" включает, не ограничиваясь ими, ожирение, пониженную толерантность к глюкозе при пероральном применении, повышенные уровни глюкозы в крови, диабет типа II и синдром X.
В данном описании, если не указано иначе, термин "нарушения, связанные с ЦНС" включает, не ограничиваясь ими, диабетическую ретинопатию, острые нейродегенеративные нарушения, хронические нейродегенеративные нарушения и плексопатии.
В данном описании, если не указано иначе, термин "дерматологические нарушения" включает, не ограничиваясь ими, сухие глаза, угри, сухую кожу, старую кожу, себорейный дерматит, розовые угри, избыточную ушную серу, заболевание мейбомиевой железы, псевдофолликулит, дрожжевые инфекции, перхоть, гнойный гидраденит, красные глаза и заболевание эккринной железы.
В данном описании острые нейродегенеративные нарушения включают разные типы острых нейродегенеративных нарушений, связанные с гибелью или нарушением нормального функционирования нервных клеток, включая цереброваскулярную недостаточность, очаговую или диффузную мозговую травму, диффузное повреждение мозга и повреждение спинного мозга, то есть, ишемию или инфаркт головного мозга, в том числе эмболическую окклюзию и тромбозную окклюзию, реперфузию после острой ишемии, перинатальное гипоксическое ишемическое повреждение, остановку сердца, а также внутричерепное кровоизлияние любого типа (включая, не ограничиваясь ими, эпидуральное, сабдуральное, субарахноидальное и внутримозговое), внутричерепные и внутрипозвоночные повреждения (включая, не ограничиваясь ими, контузию, проникающее повреждение, повреждение в результате сдвига, сжатия и разрыва), и детский синдром хлыстового потрясения.
В данном описании к хроническим нейродегенеративным нарушениям, включенным в способы настоящего изобретения, относятся болезнь Альцгеймера, болезнь Пика, деменция, ассоциированная с тельцами Леви, синдром прогрессирующего супрануклеарного паралича (синдром Стила-Ричардсона), сочетанное вырождение (синдром Шая-Дрейджера), хронические эпилептические состояния, связанные с нейродегенерацией, заболевания мотонейронов, в том числе боковой амиотрофический склероз, дегенеративная атаксия, корковая базальная дегенерация, гуамский комплекс ALS-болезнь Паркинсона-слабоумие, подострый склерозирующий панэнцефалит, болезнь Хантингтона, болезнь Паркинсона, синуклеинопатии (в том числе множественная атрофия), первичная прогрессирующая афазия, стриатонигральное вырождение, болезнь Мачадо-Джозефа/спинально-церебральная атаксия типа 3 и оливомостомозжечковые вырождения, болезнь Жилль де ла Туретта, бульбарный и псевдобульбарный паралич, спинальная и спинобульбарная мышечная атрофия (болезнь Кеннеди), первичный латеральный склероз, семейная спастическая параплегия, болезнь Верднига-Хоффмана (Werdnig-Hoffmann), болезнь Кугельберга-Веландера, болезнь Тей-Сача (Tay-Sach), болезнь Сэндхоффа (Sandhoff), семейное спастическое заболевание, болезнь Вохлфарта-Кугельберга-Веландера (Wohlfart-Kugelberg-Welander), спастический парапарез, прогрессирующая мультифокальная лейкоцеребральная дистрофия, семейная вегетативная дисфункция (синдром Райли-Дея), и прионные заболевания (включающие, без ограничения, болезнь Крейтцфельда-Якоба, болезнь Герстманна-Страусстера-Шейнкера (Gerstmann-Strausster-Scheinker), куру-куру и летальную семейную инсомнию).
В данном описании плексопатии включают параличи сплетений, многофокальные невропатии, сенсорные невропатии, двигательные невропатии, сенсорно-двигательные невропатии, инфекционные невропатии, автономные невропатии, сенсорно-автономные невропатии, демиелинизирующие невропатии (включающие, без ограничения, синдром Гийена-Барре и хроническую воспалительную демиелинизирующую полирадикулоневропатию), другие воспалительные и иммунные невропатии, невропатии, вызванные лекарственными средствами, невропатии, вызванные фармакологическим лечением, невропатии, вызванные токсинами, травматические невропатии (включающие, без ограничения, компрессионную невропатию, невропатию, связанную с раздроблением, разрывом, и сегментационную невропатию), метаболические невропатии, эндокринные и паранеопластические невропатии, а также другие невропатии, такие как наследственная невральная амиотрофия (связанная с типами 1a, 1b, 2, 4a, 1-X), атаксия Фридрейха, метахроматическая лейкодистрофия, болезнь Рефсума, адреномиелоневропатия, атаксия-телеангиэктазия, наследственная гипертрофическая невропатия Дежерина-Сотта (типы A и B), синдром Итона-Ламберта, а также заболевания черепных нервов.
В данном описании, если не указано иначе, термин "галоген" включает иод, бром, хлор и фтор.
В данном описании термин "алкил", используемый либо отдельно, либо как часть замещающей группы, включает прямые и разветвленные цепи, содержащие от одного до восьми атомов углерода. Например, алкильные радикалы включают метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил и т.п. Если не указано иначе, "низший", в применении к алкилу, означает углеродную цепь, содержащую от одного до четырех атомов углерода.
Термин "алкенил", используемый либо отдельно, либо как часть замещающей группы, включает прямые и разветвленные алкеновые цепи, содержащие от двух до восьми атомов углерода. Подходящие примеры включают винил, 1-пропенил, 2-пропенил, 1-бутенил, 2-бутенил, 1-пентенил, 2-пентенил, 1-изобутрет-2-енил и т.п. Аналогично, термин "алкинил", используемый либо отдельно, либо как часть замещающей группы, включает прямые и разветвленные алкиновые цепи, содержащие от двух до восьми атомов углерода. Подходящие примеры включают 2-пропинил, 2-бутинил, 1-бутинил, 1-пентинил и т.п.
В данном описании, если не указано иначе, "алкокси" относится к кислородсодержащему радикалу простого эфира описанных выше алкильных групп с прямой или разветвленной цепью. Например, метокси, этокси, н-пропокси, втор-бутокси, трет-бутокси, н-гексилокси и т.п.
В данном описании, если не указано иначе, термин "циклоалкил" обозначает насыщенные моноциклические замкнутые структуры, содержащие от трех до восьми атомов углерода в цикле, предпочтительно от 5 до 7 атомов углерода. Подходящие примеры включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил.
В данном описании термин "арил" относится к ароматическим карбоциклическим структурам, таким как фенил, нафтил и т.п.
В данном описании, если не указано иначе, "аралкил" обозначает любую низшую алкильную группу, замещенную арильной группой, например бензил, фенилэтил, фенилпропил, нафтилметил и т.п.
В данном описании, если не указано иначе, "гетероарил" обозначает любую пяти- или шестичленную моноциклическую ароматическую структуру, содержащую по меньшей мере один гетероатом, выбранный из группы, включающей O, N и S, необязательно содержащую от одного до трех других гетероатомов, независимо выбранных из группы, включающей O, N и S; или девяти- или десятичленную бициклическую ароматическую структуру, содержащую по меньшей мере один гетероатом, выбранный из группы, включающей O, N и S, необязательно содержащую от одного до четырех других гетероатомов, независимо выбранных из группы, включающей O, N и S. Гетероарильная группа может быть присоединена по любому атому углерода цикла, при условии, что в результате получается стабильная структура.
Примеры подходящих гетероарильных групп включают, не ограничиваясь ими, пирролил, фурил, тиенил, оксазолил, имидазолил, пуразолил, изоксазолил, изотиазолил, триазолил, тиадиазолил, пиридил, пиридазинил, пиримидинил, пиразинил, пиранил, фуразанил, индолизинил, индолил, изоиндолинил, индазолил, изоксазолил, бензофурил, бензотиенил, бензимидазолил, бензтиазолил, пуринил, хинолизинил, хинолинил, изохинолинил; изотиазолил, циннолинил, фталазинил, хиназолинил, хиноксалинил, нафтиридинил, птеридинил и т.п. Предпочтительные гетероарильные группы включают пиридил, тиенил и имидазолил.
В данном описании термин "гетероциклоалкил" обозначает любую пяти-семичленную моноциклическую, насыщенную, частично ненасыщенную или частично ароматическую замкнутую структуру, содержащую по меньшей мере один гетероатом, выбранный из группы, включающей O, N и S, необязательно содержащую от одного до трех других гетероатомов, независимо выбранных из группы, включающей O, N и S; или девяти-десятичленную, насыщенную, частично ненасыщенную или частично ароматическую бициклическую замкнутую систему, содержащую по меньшей мере один гетероатом, выбранный из группы, включающей O, N и S, необязательно содержащую от одного до четырех других гетероатомов, независимо выбранных из группы, включающей O, N и S. Гетероциклоалкильная группа может быть присоединена по любому атому углерода цикла, при условии, что в результате получается стабильная структура.
Примеры подходящих гетероциклоалкильных групп включают, не ограничиваясь ими, пирролинил, пирролидинил, диоксаланил, имидазолинил, имидазолидинил, пиразолинил, пиразолидинил, пиперидинил, диоксанил, морфолинил, дитианил, тиоморфолинил, пиперазинил, тритианил, индолинил, хроменил, 3,4-метилендиоксифенил, 2,3-дигидробензофурил, и т.п.
В данном описании символ "*" означает наличие центра стерической изомерии.
Если соединения данного изобретения имеют по меньшей мере один хиральный центр, они, соответственно, могут существовать в виде энантиомеров. Если соединения имеют два или более хиральных центров, они могут также существовать в виде диастереомеров. Следует понимать, что все указанные изомеры и их смеси включены в объем настоящего изобретения. Кроме того, некоторые из кристаллических форм содинений могут существовать в виде полиморфов, которые специально включены в настоящее изобретение. В дополнение к вышесказанному, некоторые из соединений могут образовывать сольваты с водой (т. е. гидраты) или с традиционными органическими растворителями, и такие сольваты также специально включены в объем данного изобретения.
Если конкретная группа является "замещенной" (например, циклоалкил, арил, аралкил, гетероарил, гетероциклоалкил), данная группа может иметь один или несколько заместителей, предпочтительно, от одного до пяти заместителей, более предпочтительно, от одного до трех заместителей, наиболее предпочтительно, от одного до двух заместителей, независимо выбранных из списка заместителей.
Предполагается, что определение какого-либо заместителя или вариабельного фрагмента в конкретном положении молекулы является независимым по отношению к его определениям в других участках данной молекулы. Следует понимать, что специалист в данной области должен выбирать заместители и замещающие фрагменты так, чтобы получить химически стабильное соединение, которое можно легко синтезировать с помощью известных в данной области методов, а также приведенных в данном описании способов.
В соответствии со стандартной номенклатурой, используемой в данном описании, первым описывается концевой фрагмент определяемой боковой цепи, затем соседняя функциональная группа по направлению к месту присоединения. Так, например, заместитель "фенилC1-C6алкиламинокарбонилC1-C6алкил" обозначает группу формулы
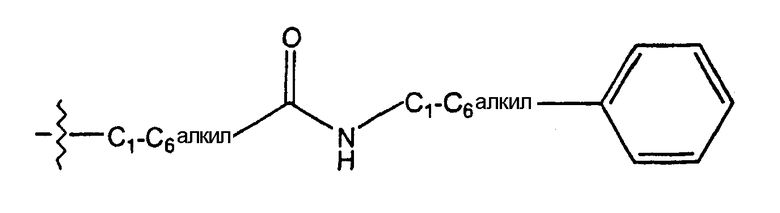
Термин "субъект" в данном описании относится к животному, предпочтительно млекопитающему, наиболее предпочтительно человеку, которое является или являлось объектом лечения, наблюдения или исследования.
В данном описании подразумевается, что термин "композиция" относится к продукту, содержащему определенные ингредиенты в заданных количествах, а также к любому продукту, который получается, непосредственно или косвенно, в результате сочетания определенных ингредиентов в заданных количествах.
Термин "терапевтически эффективное количество" в данном описании означает количество активного соединения или фармацевтического средства, которое вызывает такой биологический или медицинский ответ в тканевой системе, у животного или у человека, определяемый исследователем, ветеринаром, врачом или другим клиницистом, который вызывает облегчение симптомов заболевания или нарушения, подлежащего лечению.
Из солей соединений данного изобретения в медицине используются нетоксичные "фармацевтически приемлемые соли". Другие соли, однако, можно использовать для получения соединений данного изобретения или их фармацевтически приемлемых солей. Подходящие фармацевтически приемлемые соли соединений данного изобретения включают кислотно-аддитивные соли, которые, например, могут быть получены путем смешивания раствора соединения с раствором фармацевтически приемлемой килоты, такой, как хлористоводородная кислота, серная кислота, фумаровая кислота, малеиновая кислота, янтарная кислота, уксусная кислота, бензойная кислота, лимонная кислота, винная кислота, угольная кислота или фосфорная кислота.
В объем настоящего изобретения входят пролекарственные формы соединений данного изобретения. Как правило, такие пролекарственные формы представляют собой функциональные производные соединений, легко превращающиеся in vivo в целевое соединение. Так, в способах лечения настоящего изобретения, термин "введение" охватывает лечение различных описанных нарушений с использованием конкретного описанного соединения, или с использованием соединения, которое может не быть конкретно описанным, но которое преобразуется в желаемое соединение in vivo после введения пациенту. Традиционные методы отбора и получения подходящих пролекарственных производных описаны, например, в "Design of Prodrugs", ed. H. Bundgaard, Elsevier, 1985.
В настоящем описании, в частности, в схемах и примерах, используются следующие сокращения:
BHT = 2,6-бис-(трет-бутил)-4-метил-фенол
БСА = бычий сывороточный альбумин
цАМФ или циклический АМФ = циклический аденозинмонофосфат
ДХЭ = 1,2-дихлорэтан
DEAD = диэтилазодикарбоксилат
DM = дифференцировочная среда
ДМФ = диметилформамид
DMEM = минимальная поддерживающая среда Дульбекко
ДМСО = диметилсульфоксид
DPBS = физиологический раствор с фосфатным буфером по Дульбекко
EDTA = этилендиаминтетрауксусная кислота
FBS = фетальная бычья сыворотка
GDP = гуанозиндифосфат
GTP = гуанозинтрифосфат
GM = среда для выращивания
HBSS = забуференный солевой раствор Хенкса
HEPES = 4-(2-гидроксиэтил)-1-пиперизинэтансульфоновая кислота
HS = человеческая сыворотка
IgG = иммуноглобулин G
% Инг. = процент ингибирования
MEM = минимальная поддерживающая среда
NBS = N-бромсукцинимид
NCS = N-хлорсукцинимид
NDP αMSH = [Nle4, D-Phe7]αMSH, аналог αMSH
PBS = физиологический раствор с фосфатным буфером
ПЭГ = полиэтиленгликоль
PNC = пенициллин
кт или КТ = комнатная температура
SPA = сцинтилляционный проксимальный анализ (Scintillation Proximity Assay)
STM = стрептомицин
ТСХ = тонкослойная хроматография
TM = переходная среда
TMS = триметилсилил
Соединения формулы (I), где R3 обозначает водород, могут быть получены по способу, изображенному на схеме 1.

Схема 1
Более конкретно, подходящим образом замещенное цианосоединение формулы (III), известное соединение или соединение, полученное известными методами, подвергают взаимодействию с подходящим образом замещенным первичным амином формулы (IV), известным соединением или соединением, полученным известными методами, в присутствии такого основания как NaNH2, NaH, NaN(TMS)2 и т.п., предпочтительно NaNH2, при повышенной температуре, предпочтительно приблизительно при температуре кипения с обратным холодильником, с получением соответствующего соединения формулы (V).
Соединение формулы (V) подвергают взаимодействию с подходящим образом замещенным тиоцианатом формулы (VI), известным соединением или соединением, полученным известными методами, в присутствии DCE, при повышенной температуре, предпочтительно приблизительно при 45°C, с получением соответствующего соединения формулы (VII).
Соединение формулы (VII) подвергают циклизации/окислению в присутствии Br2, при комнатной температуре, с получением соответствующего соединения формулы (Ia).
Соединения формулы (II) могут быть получены из подходящим образом замещенного соединения формулы (I), где R3 представляет собой водород, по способу, изображенному на схеме 2.
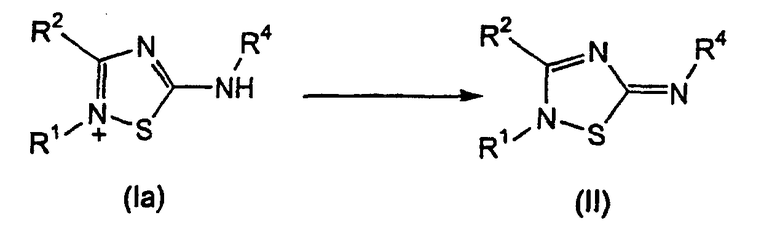
Схема 2
Более конкретно, подходящим образом замещенное соединение формулы (Ia) обрабатывают основанием, например, NaHCO3, Na2CO3, NaOH и т.п., предпочтительно NaHCO3, при комнатной температуре, с получением соответствующего соединения формулы (II).
Соединения формулы (II) также могут быть получены из подходящим образом замещенного соединения формулы (VII) по способу, изображенному на схеме 3.
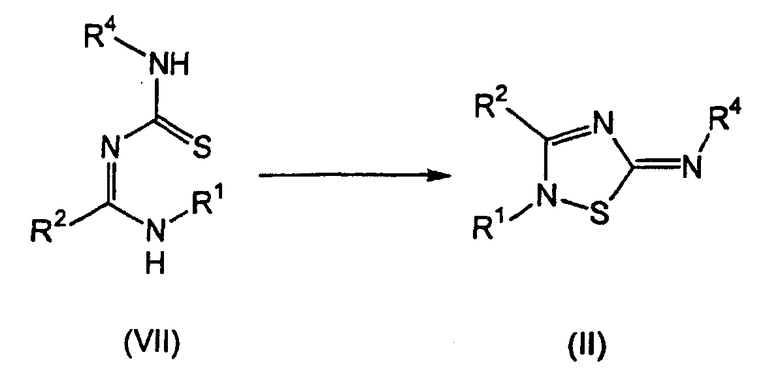
Схема 3
Более конкретно, подходящим образом замещенное соединение формулы (VII) подвергают взаимодействию с окисляющим агентом, например, NBS, NCS, DEAD и т.п., предпочтительно NBS, при комнатной температуре, с получением соответствующего соединения формулы (II). Предпочтительно соединение формулы (II) экстрагируют из водного раствора основания, например, NaHCO3, Na2CO3, NaOH и т.п.
Соединения формулы (I), где R3 обозначает алкил, могут быть получены из подходящим образом замещенного соединения формулы (II) по способу, изображенному на схеме 4.

Схема 4
Соответственно, подходящим образом замещенное соединение формулы (II) подвергают взаимодействию с подходящим образом замещенным соединением формулы (VIII), известным соединением или соединением, полученным известными методами, где X- обозначает трифторметилсульфонат, Br- и I-, при комнатной температуре, с получением соответствующего соединения формулы (I).
Соединения формулы (I), где R3 обозначает водород, могут быть получены из подходящим образом замещенного соединения формулы (II) по способу, изображенному на схеме 5.
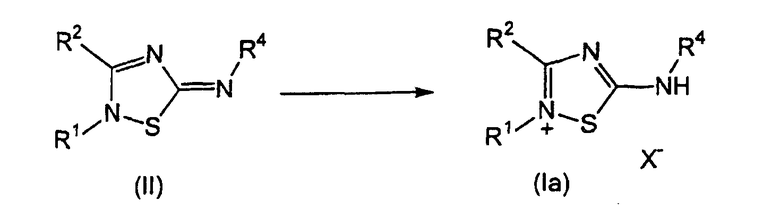
Схема 5
Соответственно, подходящим образом замещенное соединение формулы (II) подвергают взаимодействию с фармацевтически приемлемой кислотой, такой как HCl, HBr, HNO3, и т.п., предпочтительно HCl, при комнатной температуре, с получением соответствующего соединения формулы (Ia), где X- обозначает Cl-, Br-, NO3 - и т.п.
Если способы получения соединений данного изобретения приводят к образованию смеси стереоизомеров, данные изомеры можно разделить с помощью традиционных методов, таких как препаративная хроматография. Соединения могут быть получены в виде рацемической смеси, или индивидуальные энантиомеры можно получить либо путем энантиоспецифичного синтеза, либо в результате разделения. Например, соединения можно разделить на энантиомеры с помощью стандартных методов, таких как получение диастереомерных пар в результате образования соли с оптически активной кислотой, такой как (-)-ди-п-толуоил-d-винная кислота и/или (+)-ди-п-толуоил-l-винная кислота, с последующей фракционной кристаллизацией и получением свободного основания. Соединения также можно разделить путем получения диастереомерных сложных эфиров или амидов с последующим хроматографическим разделением и удалением вспомогательного хирального соединения. Альтернативно, соединения могут быть разделены методом ВЭЖХ с использованием хиральной колонки.
В процессе протекания любого из способов получения соединений настоящего изобретения может возникнуть необходимость в защите чувствительных или реакционноспособных групп на любой из участвующих в реакции молекул, или такая защита может быть желательной. Защиту можно осуществить с помощью традиционных защитных групп, таких как описанные в Protective Groups in Organic Chemistry, ed. J. F. W. McOmie, Plenum Press, 1973; и T. W. Greene & P. G. M. Wuts, Protective Groups in Organic Synthesis, John Wliey & Sons, 1991. Защитные группы могут быть удалены на соответствующей очередной стадии с помощью известных в данной области методов.
Пригодность соединений настоящего изобретения для лечения нарушений, опосредованных рецептором меланокортина, можно установить с помощью методов, приведенных в примерах 4-11 данного описания. Следовательно, настоящее изобретение касается способа лечения таких нарушений, который включает введение какого-либо из соединений, определенных в данном описании, в количестве, эффективном для лечения нарушения (т. е. в терапевтически эффективном количестве). Соединение может быть введено пациенту, страдающему от такого нарушения, любым традиционным способом, включая, без ограничения, внутривенный, пероральный, подкожный, внутримышечный, внутридермальный, парентеральный и чрезкожный.
Настоящее изобретение также относится к фармацевтическим композициям, содержащим одно или несколько соединений данного изобретения в сочетании с фармацевтически приемлемым носителем.
Для получения фармацевтических композиций данного изобретения одно или несколько соединений формулы (I) и/или (II), или их соли (активный ингредиент), тщательно перемешивают с фармацевтическим носителем с помощью традиционных методов получения фармацевтических смесей, данный носитель может находиться в виде широкого ряда форм в зависимости от вида препарата, желательного для введения, например, перорального или парентералного, такого как внутримышечное. Для получения композиций в виде лекарственной формы для перорального применения можно использовать любую из обычных фармацевтических сред. Таким образом, в случае жидких пероральных препаратов, таких как, например, суспензии, эликсиры и растворы, подходящие носители и добавки включают воду, гликоли, масла, спирты, ароматизирующие средства, консерванты, окрашивающие средства и т.п.; в случае твердых пероральных препаратов, таких как, например, порошки, капсулы, таблетки в форме капсулы, гелевые капсулы и таблетки, подходящие носители и добавки включают крахмалы, сахара, разбавители, гранулирующие средства, смазывающие средства, связующие средства, дезинтегрирующие средства и т.п. Из-за простоты введения наиболее предпочтительной стандартной лекарственной формой являются таблетки и капсулы, в данном случае, несомненно, используются твердые фармацевтические носители. При желании, таблетки могут быть покрыты с помощью стандартных методов сахарным или энтеросолюбильным покрытием. В случае парентеральных препаратов, носитель, как правило, включает стерильную воду, хотя могут быть включены другие ингредиенты, например, для облегчения растворимости или для консервации. Также могут быть получены суспензии для инъекций, для которых можно использовать соответствующие жидкие носители, суспендирующие средства и т.п.
Композиции для местного применения, относящиеся к настоящему изобретению, включают, не ограничиваясь ими, кремы, лосьоны, гетерогенные эмульсии, микроэмульсии, липосомальные кремы или гели, гели, растворы, суспензии, мази, пенящиеся аэрозоли, твердые или мягкие желатиновые капсулы, маски, карандаши, роликовые препараты, порошки, спреевые формы и т.п. Композиции для местного применения кроме активного(ых) ингредиента(ов) могут содержать один или несколько неактивных компонентов, включающих, не ограничиваясь ими, хелатообразующие средства, забуферивающие средства, красители, консерванты, отдушки, эмульгаторы, поверхностно-активные вещества, замутняющие средства, мягчительные средства, растворители, солнцезащитные средства, средства, модифицирующие вязкость, антиоксиданты, увлажняющие средства, усилители проницания, средства, образующие пленку, и т.п.
Композиции для местного применения, относящиеся к настоящему изобретению, предназначенные для лечения угрей, могут также содержать один или несколько из нижеследующих компонентов, включая противоугревые/кератолитические средства, противомикробные средства и стероидные или нестероидные противовоспалительные средства (Противоугревыми средствами называются любые соединения, способные разрушать угри. Кератолитическими средствами называются любые соединения, способные разъединять кератиноциты и, как следствие, приводящие к отслаиванию эпидермиса). Подходящие противоугревые/кератолитические средства включают, не ограничиваясь ими, ретиноиды, салициловую кислоту, гликолевую кислоту, цетилбетаин и т.п. Подходящие противомикробные средства включают, не ограничиваясь ими, бензоилпероксид, эритромицин, тетрациклин, клиндамицин, азелаиновую кислоту и т.п. Композиции для местного применения обычно содержат 0,01-1% активного ингредиента.
В данном описании фармацевтические композиции содержат, в стандартной лекарственной форме, например таблетке, капсуле, порошке, инъекционном препарате, чайной ложке и т.п., количество активного ингредиента, необходимое для доставки эффективной дозы, как описано выше. Не предназначенные для местного применения фармацевтические композиции в данном описании содержат, в стандартной лекарственной форме, например таблетке, капсуле, порошке, инъекционном препарате, чайной ложке и т.п., приблизительно от 0,03 мг до 100 мг/кг (предпочтительно 0,1-30 мг/кг) и могут приниматься в количестве, составляющем приблизительно 0,1-300 мг/кг/день (предпочтительно 1-50 мг/кг/день). Данные дозы, однако, можно варьировать в зависимости от потребностей пациентов, тяжести состояния, подлежащего лечению и используемого соединения. Может применяться либо ежедневное введение, либо пострет-периодический дозировочный режим.
Предпочтительно, данные композиции находятся в виде стандартных лекарственных форм, таких как таблетки, пилюли, капсулы, порошки, гранулы, стерильные растворы или суспензии для парентерального введения, дозированные аэрозольные или жидкие спреи, капли, ампулы, автоинжекторные устройства или суппозитории; для перорального, парентерального, интраназального, подъязычного или ректального введения, или для введения путем вдыхания или вдувания. Альтернативно, композиция может находиться в форме, подходящей для введения один раз в неделю или один раз в месяц; например нерастворимая соль активного соединения, такая как деканоат, может играть роль депо препарата для внутримышечного введения. Для получения твердых композиций, таких как таблетки, основной активный ингредиент смешивают с фармацевтическим носителем, например ингредиентами, традиционно использующимися при таблетировании, такими как кукурузный крахмал, лактоза, сахароза, сорбитол, тальк, стеариновая кислота, стеарат магния, дикальцийфосфат или смолы, а также с другими фармацевтическими разбавителями, например с водой, с получением твердой первичной композиции, представляющей собой гомогенную смесь, содержащую соединение настоящего изобретения, или его фармацевтически приемлемую соль. Называя данные первичные композиции гомогенными, авторы подразумевают, что активный ингредиент равномерно распределен по всей композиции так, что композицию можно легко разделить на равноэффективные лекарственные формы, такие как таблетки, пилюли и капсулы. Данную твердую первичную композицию затем разделяют на стандартные лекарственные формы описанного выше типа, содержащие от 0,1 до приблизительно 500 мг активного ингредиента настоящего изобретения. Таблетки или пилюли, полученные с использованием новой композиции, могут быть покрытыми, или могут быть произведены иным образом, с получением лекарственной формы, обладающей преимуществом пролонгированного действия. Например, таблетка или пилюля может содержать внутренний дозированный и внешний дозированный компонент, причем последний находится в виде оболочки, покрывающей первый. Два компонента могут быть разделены энтеросолюбильным слоем, который препятствует распадению в желудке и позволяет внутреннему компоненту проходить в двенадцатиперстную кишку в исходном виде или высвобождаться с задержкой во времени. Для таких энтеросолюбильных слоев или покрытий можно использвать различные вещества, которые включают ряд полимерных кислот с такими веществами как шеллак, цетиловый спирт и ацетат целлюлозы.
Жидкие формы для перорального введения или для инъекции, которые могут содержать новые композиции настоящего изобретения, включают водные растворы, соответствующим образом ароматизированные сиропы, водные или масляные суспензии, ароматизированные эмульсии с пищевыми маслами, такими, как хлопковое масло, кунжутное масло, кокосовое масло или арахисовое масло, а также эликсиры и подобные фармацевтические среды. Диспергирующие или суспендирующие средства, подходящие для водных суспензий, включают синтетические и природные смолы, такие как трагакант, гуммиарабик, альгинат, декстран, карбоксиметилцеллюлоза натрия, метилцеллюлоза, поливинилпирролидон или желатин.
Описанный в настоящем изобретении способ лечения нарушений, опосредованных рецептором меланортина, может быть осуществлен с использованием фармацевтической композиции, содержащей любое из описанных здесь соединений и фармацевтически приемлемый носитель. Не предназначенная для местного введения фармацевтическая композиция может содержать приблизительно от 0,01 мг до 100 мг, предпочтительно приблизительно от 5 до 50 мг, соединения, и может быть представлена в виде любой формы, подходящей для выбранного способа введения. Носители включают необходимые инертные фармацевтические наполнители, включающие, не ограничиваясь ими, связующие средства, суспендирующие средства, смазывающие средства, ароматизаторы, подсластители, консерванты, красители и средства для покрытия. Композиции, подходящие для перорального введения, включают твердые формы, такие, как пилюли, таблетки, таблетки в форме капсул, капсулы (каждая из них включает композиции с незамедлительным высвобождением, регулируемым во времени высвобождением и замедленным высвобождением), гранулы и порошки, а также жидкие формы, такие как растворы, сиропы, эликсиры, эмульсии и суспензии. Формы, пригодные для парентерального введения, включают стерильные растворы, эмульсии и суспензии.
Соединения настоящего изобретения преимущественно могут быть введены в виде разовой дневной дозы, или общая дневная доза может быть введена отдельными дозами два, три или четыре раза в день. Кроме того, соединения настоящего изобретения могут быть введены в интраназальной форме посредством местного применения подходящих интраназальных сред, или чрезкожным способом с помощью пластырей, хорошо известных специалистам в данной области. Введение дозы посредством чрезкожной системы доставки является в большей степени непрерывным, чем перемежающимся, на протяжении всего режима дозировки.
Например, для перорального введения в форме таблетки или капсулы активный лекарственный компонент может быть объединен с нетоксичным фармацевтически приемлемым инертным носителем для перорального применения, таким как этанол, глицерин, вода и т.п. Кроме того, при желании или при необходимости, в смесь также могут быть включены связующие средства, смазывающие средства, дезинтегрирующие средства и окрашивающие средства. Подходящие связующие средства включают, без ограничения, крахмал, желатин, природные сахара, такие как глюкоза или бета-лактоза, кукурузные подсластители, природные и синтетические смолы, такие как гуммиарабик, трагакант или олеат натрия, стеарат натрия, стеарат магния, бензоат натрия, ацетат натрия, хлорид натрия и т.п. Дезинтегрирующие средства включают, без ограничения, крахмал, метилцеллюлозу, агар, бентонит, ксантановую смолу и т.п.
Жидкие формы включают подходящим образом ароматизированные суспендирующие или диспергирующие средства, такие как природные и синтетические смолы, например, трагакант, гуммиарабик, метилцеллюлоза и т.п. Для парентерального введения требуются стерильные суспензии и растворы. Изотонические препараты, которые обычно содержат подходящие консерванты, применяются, если требуется внутривенное введение.
Соединение настоящего изобретения можно также вводить в форме липосомальной системы доставки, такой как маленькие моноламеллярные везикулы, большие моноламеллярные везикулы и мультиламеллярные везикулы. Липосомы могут быть получены из ряда фосфолипидов, таких как холестерин, стеариламин или фосфатидилхолины.
Соединения настоящего изобретения также могут быть доставлены с помощью моноклональных антител, как индивидуальных носителей, к которым присоединены молекулы соединения. Соединения настоящего изобретения также могут быть присоединены к растворимым полимерам, как наводимым на цель носителям лекарственных средств. Такие полимеры могут включать поливинилпирролидон, сополимер пирана, полигидроксипропилметакриламидофенол, полигидроксиэтиласпартамидофенол или полиэтиленоксидполилизин, замещенный остатком пальмитоила. Кроме того, соединения настоящего изобретения могут быть присоединены к полимерам, биодеградируемого типа, которые можно использовать для достижения контролируемого высвобождения лекарственного средства, таких как полимолочная кислота, полиэпсилонкапролактон, полигидроксимасляная кислота, полиортоэфиры, полиацетали, полидигидропираны, полицианоакрилаты и поперечно сшитые или амфипатические блок-сополимеры гидрогелей.
Соединения данного изобретения могут быть введены в составе любой из вышеописанных композиций и в соответствии с дозировочными режимами, принятыми в данной области, если требуется лечение нарушений, опосредованных рецептором меланокортина.
Суточная доза продуктов может варьироваться в широком интервале от 0,01 до 1000 мг в день для взрослого человека. Для перорального введения композиции предпочтительно предоставляются в виде таблеток, содержащих 0,01, 0,05, 0,1, 0,5, 1,0, 2,5, 5,0, 10,0, 15,0, 25,0, 50,0, 100, 150, 200, 250 и 500 миллиграмм активного ингредиента для симптоматического подбора дозы для пациента, подвергающегося лечению. Эффективное количество лекарственного средства обычно поставляется на дозировочном уровне, составляющем приблизительно от 0,01 мг/кг до 100 мг/кг массы тела в день. Предпочтительно в интервале приблизительно от 0,03 до 10 мг/кг массы тела в день. Соединения могут быть введены в режиме от 1 до 4 раз в день.
Специалисты в данной области могут легко установить оптимальные для введения дозы, которые варьируют в зависимости от конкретного используемого соединения, способа введения, эффективности препарата и развития болезненного состояния. Кроме того, наличие факторов, связанных с конкретным пациентом, подвергающимся лечению, включающих возраст пациента, массу, диету и время введения, приводит к необходимости корректировки дозы.
Нижеследующие примеры приведены для облегчения понимания изобретения и их не следует истолковывать как предназначенные для ограничения каким-либо образом изобретения, сформулированного ниже в формуле изобретения.
ПРИМЕР 1
2-(2-метоксифенил)-3-фенил-5-п-толиламино-[1,2,4]тиадиазол-2-ий
Соединение #31
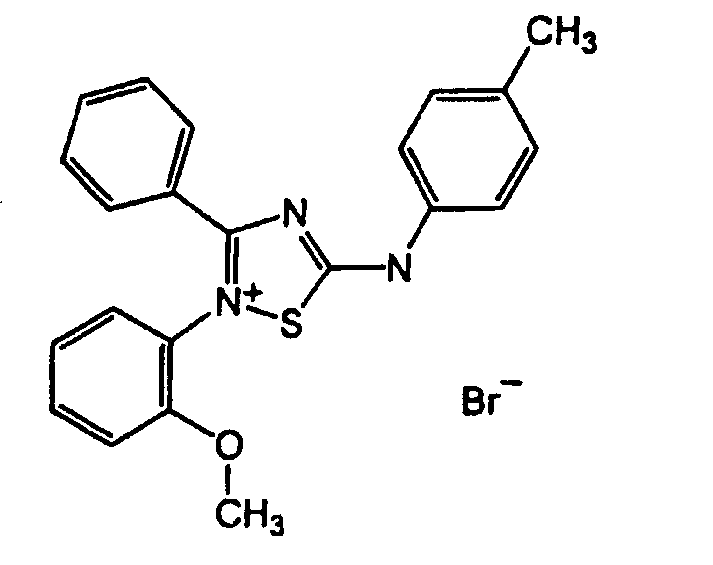
Стадия A:
Смесь o-анизидина (15,0 г, 121,8 ммоль) и амида натрия (50 % (мас.) суспензия в толуоле) (11,40 г, 146,2 ммоль) в безводном толуоле (200 мл) перемешивают 1 час при комнатной температуре. К смеси добавляют бензонитрил (9,86 мл, 96,6 ммоль) и нагревают с обратным холодильником 16 часов. Реакционную смесь охлаждают и реакцию гасят, добавляя 1,0 н HCl (150 мл). Добавляют активированный уголь и реакционную смесь фильтруют через рыхлый слой целита. pH смеси доводят приблизительно до 14 путем добавления 1,0 н. NaOH (200 мл). Водный слой экстрагируют хлороформом (3x150 мл). Объединенный органический слой сушат над безводным MgSO4 и упаривают. Полученное твердое вещество промывают гексаном и сушат в вакууме, получая продукт в виде тусклого белого твердого вещества.
1H ЯМР (300 МГц, CDCl3)™ 3,83 (с, 3H), 4,79 (с, 2H), 6,96 (м, 3H), 7,04 (м, 1H), 7,43 (м, 3H), 7,93 (д, 2H)
МС (APCI, MH+) 227
Стадия B:
Смесь N-арилбензамидина (3,0 г, 13,27 ммоль), полученного на стадии A, и 4-толилизотиоцианата (2,18 г, 14,60 ммоль) в безводном хлороформе (30 мл) нагревают с обратным холодильником в течение 16 часов. Реакционную смесь охлаждают и растворитель упаривают. Полученный остаток очищают колоночной флэш-хроматографией с использованием в качестве подвижной фазы 25% гексана в дихлорметане. Объединенные фракции упаривают и полученное твердое вещество сушат в вакууме, получая продукт в виде твердого вещества желтого цвета.
1H ЯМР (300 МГц, CDCl3)™ 2,36 (с, 3H), 3,66 (с, 3H), 6,76 (м, 1H), 6,97 (т, 1H), 7,17-7,39 (м, 7H), 7,47 (д, 2H), 7,60 (д, 2H), 8,20 (с, 1H), 14,18 (с, 1H)
МС (ES, MH+) 376,29
Стадия C:
К раствору тиомочевины (2,90 г, 7,73 ммоль), полученной на стадии B, в безводном хлороформе (15 мл) медленно добавляют бром (438 мкл, 8,51 ммоль). После перемешивания в течение 16 часов растворитель упаривают. Полученное твердое вещество промывают безводным этиловым эфиром. Неочищенный твердый продукт перекристаллизовывают из 20% раствора воды в этаноле, получая продукт в виде твердого вещества желтого цвета.
1H ЯМР (300МГц, CDCl3) ™ 2,39 (с, 3H), 3,66 (с, 3H), 6,96 (д, 1H), 7,06 (т, 1H), 7,20-8,07 (м, 7H), 7,61 (д, 2H), 7,80 (д, 2H), 12,40 (с, 1H)
МС (ES, MH+) 374,25
ПРИМЕР 2
2-(2-метоксифенил)-3-(2-метоксифенил)-5-фениламино-[1,2,4]тиадиазол-2-ий
Соединение #74
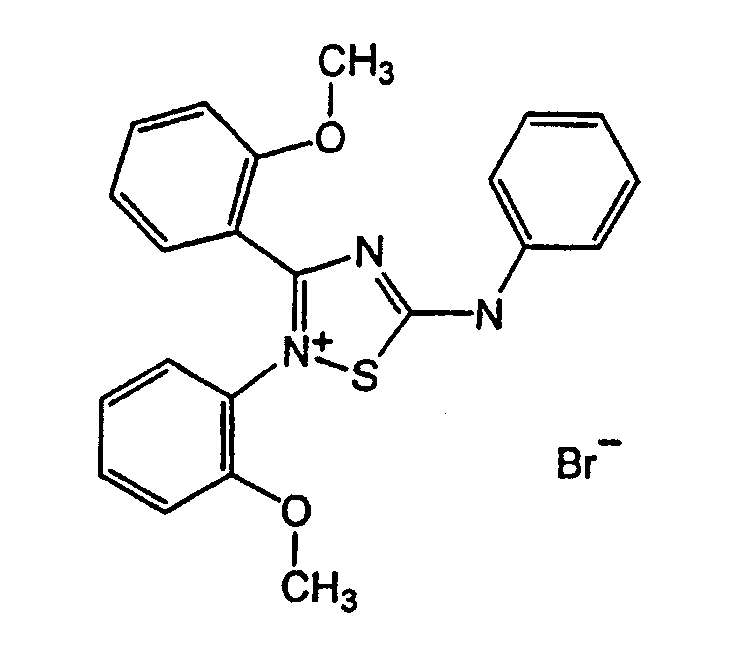
Стадия A:
Смесь o-анизидина (13,5 г, 110,0 ммоль) и амида натрия (50 % (мас.) суспензия в толуоле) (9,40 г, 120,0 ммоль) в безводном толуоле (200 мл) перемешивают 1 час при комнатной температуре. К смеси добавляют 2-метоксибензонитрил (16 мл, 131,0 ммоль) и реакционную смесь затем нагревают с обратным холодильником 16 часов. Реакционную смесь охлаждают и реакцию гасят, добавляя 1,0н. HCl (150 мл). Добавляют активированный уголь и реакционную смесь фильтруют через рыхлый слой целита. pH смеси доводят приблизительно до 14 путем добавления 1,0н. NaOH (200 мл). Водный слой экстрагируют хлороформом (3x150 мл). Объединенный органический слой сушат над безводным MgSO4 и упаривают. Полученное твердое вещество промывают гексаном и сушат в вакууме, получая продукт в виде тусклого белого твердого вещества.
МС(APCI, MH+) 257
Стадия B:
Смесь N-арилбензамидина (15,5 г, 60,6 ммоль), полученного на стадии A, и фенилизотиоцианата (8,70 мл, 72,7 ммоль) в безводном хлороформе (30 мл) нагревают при 45°С в течение 16 часов. Реакционную смесь охлаждают и растворитель упаривают. Полученный остаток очищают колоночной флэш-хроматографией с использованием в качестве подвижной фазы 25% гексана в дихлорметане. Объединенные фракции упаривают и полученное твердое вещество сушат в вакууме, получая продукт в виде твердого вещества желтого цвета.
МС(ES, MH+) 391,50
Стадия C:
К раствору тиомочевины (12,95 г, 33,1 ммоль), полученной на стадии B, в безводном хлороформе (15 мл) медленно добавляют бром (1,78 мл, 34,75 ммоль). После перемешивания в течение 16 часов растворитель упаривают. Полученное твердое вещество промывают безводным этиловым эфиром. Неочищенный твердый продукт перекристаллизовывают из 20% раствора воды в этаноле, получая продукт в виде твердого вещества желтого цвета.
МС(ES, MH+) 390,1
Используя раскрытые в данном описании методы, получают характерные соединения формулы (I) настоящего изобретения, приведенные в таблице 1.
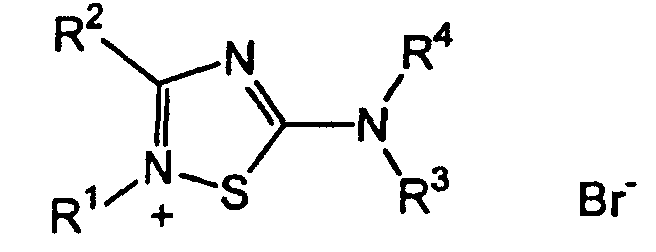
ПРИМЕР 3
2-(2-метоксифенил)-3-(2-метоксифенил)-5-фениламино-[1,2,4]-тиадиазол
Соединение #89
К раствору соединения, полученного на стадии B примера 2 (0,921 г, 2,36 ммоль) в безводном хлороформе (10 мл) добавляют N-хлорсукцинимид (326 мг, 2,71 ммоль). Затем реакционную смесь перемешивают в течение 16 часов, после чего реакцию останавливают и реакционную смесь промывают дважды водным раствором NaHCO3. Органический слой сушат над безводным сульфатом магния и оставшийся растворитель удаляют под вакуумом, получая указанный в заголовке продукт в виде твердого вещества.
МС (ES, MH+) 390,1
Используя раскрытые в данном описании методы, получают характерные соединения формулы (II) настоящего изобретения, приведенные в таблице 2.
Если не указано иначе, спектры ЯМР снимают на ЯМР-спектрометре Bruker Avance, 300 мГц. Если не указано иначе, молекулярные массы определяют с помощью масс-спектрометра с платформенным электрораспылением Micromass LC, результаты приведены в таблице 3.
ПРИМЕР 4
Анализ связывания рецептора меланокортина MC-4
Меланокортин [MC-4]-мембрану [полученную от Receptor Biology Inc.] инкубируют с поливинилтолуольными шариками для сцинтилляционного проксимального анализа, покрытыми агглютинином зародышей пшеницы [полученными от Amersham Pharmacia Inc.], в течение 30 мин при 25°C. В каждой лунке 96-луночного планшета Opti [полученного от Packard, CA] смешивают 2,5 мкг мембраны и 0,25 мг шариков в 100 мкл среды. В качестве среды используют 50 мМ HEPES, pH 7,4, содержащую 0,1% бычьего сывороточного альбумина, 2 мМ CaCl2, 2 мМ MgCl2 и ингибиторы протеаз. В отдельные лунки планшета добавляют анализируемые соединения (1,5 мкл 1 мМ раствора в буфере 30% DMSO-50 мМ HEPES, pH 7,4). В каждую лунку добавляют радиоактивный лиганд 125I-NDP-меланоцитостимулирующий гормон [NEN, 2000 Ки/ммоль] (48,5 мкл на лунку, конечная концентрация 40 пМ). Затем планшет закрывают и оставляют стоять в течение 16 ч при 25°C. Для определения неспецифического связывания (N) в качестве ингибиторных соединений сравнения используют пептид NDP-меланоцитостимулирующий гормон и пептид α-меланоцитостимулирующий гормон [полученные от Palomar Research Inc., 1 мкМ]. Общее связывание (T) определяют, испольуя буфер 30% DMSO-50 мМ HEPES, pH 7,4. Связанную радиоактивность в каждой лунке (Y), выраженную как число импульсов в минуту (cpm), измеряют на TopCount [Packard, CA]. Процент ингибирования рассчитывают следующим образом:
[(T-Y)/(T-N)] · 100%.
ПРИМЕР 5
Анализ стимуляции продукции циклического аденозинмонофосфата [цАМФ]
Клетки человеческой меланомы Бовиса (Bowes), экспрессирующие рецептор меланокортина MC-4, выращивают до слияния в 24-луночном культуральном планшете. Питательную среду отбрасывают и к каждой лунке добавляют 0,5 мл раствора Хэнкса. Анализируемые соединения добавляют в лунки 96-луночного планшета. В лунки положительного контроля добавляют пептид NDP-меланоцитостимулирующий гормон (1 мкМ), тогда как в лунки отрицательного контроля добавляют буфер 30% DMSO-50 мМ HEPES, pH 7,4. Планшет инкубируют при 37°C, в атмосфере 5% CO2 в течение 30 мин. Супернатант отбрасывают и клетки дважды промывают раствором Хэнкса. К каждой лунке добавляют этанол (80%, 0,5 мл) и планшеты инкубируют при 4°C в течение 30 мин. Концентрацию циклического АМФ измеряют, используя набор NEN Flashplate [NEN]. Агонист рецептора меланокортина определяют как анализируемое соединение, которое в данном анализе приводит к увеличению продукции цАМФ.
ПРИМЕР 6
Анализ активации G-белка
В каждом анализе мембраны, экспрессирующие рецептор меланокортина MC-4 (5 мкг), инкубируют в течение 5 мин при 25°C с 0,5 нМ 35S-GTPγS в 100 мкл буфера 25 мМ HEPES, pH 7,5, содержащего 100 мМ NaCl, ингибиторы протеаз, 0,5 мкМ GDP, 5 мМ 2-меркаптоэтанол, 1 мМ MgCl2, вместе с анализируемым соединением, 1 мкМ NDP-меланоцитостимулирующим гормоном, или сочетанием NDP-меланоцитостимулирующего гормона и анализируемого соединения. Базальное связывание 35S-GTPγS определяют, используя буфер 10 мМ HEPES, pH 7,4, содержащий 30% DMSO. Реакцию останавливают добавлением 50 мкл терминирующего буфера, содержащего 25 мМ HEPES, pH 7,5, 20 мМ MgCl2, ингибиторы протеаз, 100 мкМ GDP, 100 мкМ GTP, 5 мМ 2-меркаптоэтанол и детергенты (0,5% дигитонин, 0,2% дезоксихолат натрия и 0,5% NP-40). Мембраны солюбилизируют в течение 30 минут при 25°C. Связанный с 35S-GTPγS Gαs-белок подвергают иммунопреципитации, используя антитела против Gαs (0,5 мкг), которые связываются с антителами против кроличьих IgG или с белком А, конъюгированными с SPA шариками. Связанную радиоактивность измеряют с помощью Topcount [Packard]. Неспецифическое связывание 35S-GTPγS определяют, подвергая 35S-GTPγS иммунопреципитации с нормальными кроличьими IgG (0,5 мкг).
Базальное связывание (B) = Среднее число импульсов/минуту (cpm), обусловленное соединением, подвергшимся иммунопреципитации под действием антител против Gαs.
Неспецифическое связывание (NSB) = Среднее значение cpm, обусловленное соединением, подвергшимся иммунопреципитации под действием нормальных кроличьих IgG.
Специфическое базальное связывание (SB) = B-NSB
Cpm в каждой лунке = C
Истинное значениие cpm в каждой лунке (N) = C-NSB
% Стимуляции = [(N-SB)/SB]×100%
Методы, описанные выше для рецептора меланокортина MC-4, используют для рецептора меланокортина MC-3. С помощью описанных методов характерные соединения настоящего изобретения анализируют на связывание в MC-4 и/или MC-3 анализах, результаты приведены в таблице 4.
ПРИМЕР 7
Питание грызунов: потребление пищи лишенными еды крысами (MC-4)
Самцов крыс Long-Evans (180-200 грамм) размещают индивидуально и держат на одноразовом питании (т. е. кормят один раз в день в интервале между 10 часами утра и 4 часами дня) в течение пяти дней после карантина, чтобы дать животным привыкнуть к порошковой пище (сертифицированная пища для грызунов #5002 PMI) в течение отведенного времени. Пищу оставляют доступной в открытой емкости, укрепленной в клетке с помощью проволоки и снабженной металлическим подавателем, закрывающим еду, для минимизации рассыпания. Вода находится в свободном доступе.
Перед анализом животных не кормят в течение 18 часов. В конце периода голодания животным вводят либо анализируемое соединение, либо среду. Среду и анализируемое соединение вводят или перорально (5 мл/кг) за 60 минут до эксперимента, или подкожно (1 мл/кг) за 30 минут до эксперимента, или внутрибрюшинно (1 мл/кг) за 30 минут до эксперимента. Анализируемые соединения вводят перорально в виде суспензии в водном растворе 0,5% метилцеллюлозы-0,4% Tween 80, или внутрибрюшинно в виде раствора или суспензии в ПЭГ 200; концентрации соединений, как правило, варьируют от 1 мг/кг до 100 мг/кг, предпочтительно от 10-30 мг/кг. Потребление пищи определяют через 2, 4 и 6 часов после введения путем взвешивания специальной емкости, содержащей пищу, перед экспериментом и через определенные промежутки времени. После завершения эксперимента всех животных оставляют на однонедельный период выведения перед повторным анализом.
С помощью описанной выше процедуры анализируют отдельные соединения настоящего изобретения для определения их влияния на потребление пищи голодными крысами, результаты приведены в таблицах 5 и 6.
ПРИМЕР 8
Анализ роста клетки с нейритами
Клеточная культура:
Культуры разобщенных гиппокампальных и корковых клеток создают из 18-дневных эмбрионов крыс, как описано в Mattson, M. P., Barger, S. W., Begley, J, and Mark, R.J., Methods Cell Biol., 1994, 46: 087-216. Если говорить кратко, эмбрионы удаляют из беременных самок (Sprague-Dawley) через кесарево сечение и анестезируют галотаном в соответствии с перечнем Американской ассоциации ветеринаров (AVMA) по эвтаназии. Зародышей декапитируют, мозги удаляют и помещают в сбалансированный солевой раствор Хэнкса, забуференный HEPES (HBSS; Gibco). Выделяют гиппокампы и кору головного мозга и объединяют в соответствии с типом ткани. Ткань трипсинизируют 15 мин (1 мг/мл трипсин-HBSS; Worthington), промывают свежим HBSS, инкубируют с ингибитором трипсина (1 мг/мл; Sigma) 5 мин, снова промывают свежим HBSS и затем растирают в 1 мл свежего HBSS с помощью оплавленной стеклянной пипетки. Разобщенные клетки высевают в количестве 30000 клеток/лунку в 96-луночные планшеты, покрытые поли-D-лизином (Collaborative BioScience). Каждая лунка содержит 100 мкл минимальной поддерживающей среды Игла (MEM; Gibco), содержащей дополнительно 26 мМ NaHCO3 (Sigma), 56 мМ глюкозы (Sigma), 15 мМ KCl (Sigma), 1 мМ пирувата натрия (Sigma), 1,1 мМ L-глютамина (Sigma), 10% (об/об) инактивированной нагреванием фетальной бычьей сыворотки (Hyclone) и 0,001% сульфата гентамицина (Sigma) (pH 7,4). Перед экспериментальной обработкой клетки оставляют прикрепляться в течение 24 ч во влажном инкубаторе при 37°C и 5% CO2. Каждые 3 дня культуральную среду отсасывают и заменяют свежей средой.
Анализ:
Через двадцать четыре часа после помещения в планшеты культуры обрабатывают средой (PBS+0,1% БСА), альфа-меланоцитостимулирующим гормоном (α-MSH) или анализируемым соединением (разбавленным DPBS). Все экспериментальные параметры существуют с четырьмя повторами. На третий день культивирования среду отсасывают и заменяют свежей средой, содержащей анализируемое соединение. Через неделю культивирования клетки фиксируют 10% формалином с фосфатным буфером в течение 15 минут, затем промывают DPBS (Sigma) и помещают в блокирующую сыворотку на 30 мин (лощадиная сыворотка; разведение 1:50 в DPBS; Vector Labs). Культуры снова промывают DPBS и затем инкубируют с первичными антителами в течение 2 ч (белок-2, ассоциированный с микротрубочками (MAP-2) является селективным маркером для процессов, протекающих в дендритах; моноклональные антитела против мышиных иммуноглобулинов (Chemicon); разбавление MAP-2 1:1000 в разбавителе для антител (Zymed)). Лунки отрицательного контроля инкубируют только с разбавителем для антител. Фоновый сигнал определяют по пустым лункам (не содержащим клетки), которые инкубируют с антителами или без антител. Культуры снова промывают DPBS и затем помещают во флуоресцеин на 1 ч (FITC; антитела против мышиных IgG; после адсорбции крысиной сывороткой; разведение 1:50 в DPBS; Vector Labs). Культуры промывают последний раз DPBS и планшеты затем считывают на флюоресцентном планшетрет-ридере Cytofluor 4000. Рост нейритов выражают как процент изменения по отношению к контролю (среде).
Отдельные соединения настоящего изобретения анализируют с помощью вышеописанного метода, результаты которого приведены в таблице 7. Данные выражают как процент изменения по отношению к ответу среды. Все соединения анализируют в концентрации 50 нМ. Аббревиатура NA указывает на отсутствие изменения/активности; аббревиатура ND указывает, что соединение не анализируется/ответ не определяется.
Рост нейритов
Приведенные выше данные показывают, что обработка культур отдельными соединениями настоящего изобретения приводит к значительному увеличению роста нейритов, как определено с помощью иммунофлюоресценции MAP2-FITC. Сравнение анализируемых соединений и α-MSH показывает, что многие из анализируемых соединений превосходят α-MSH по стимуляции роста нейритов в тестируемых концентрациях. Кроме того, некоторые из анализируемых соединений обладают избирательным влиянием на рост нейритов в клетках гиппокампа или коры головного мозга.
ПРИМЕР 9
In vivo модель сжатия лицевого нерва
Способность анализируемого соединения проявлять нейропротективные или нейрорегенеративные свойства исследуют на модели сжатия лицевого нерва. Двигательные аксоны лицевого нерва образуются исключительно из нейронов в мосте в четко определенном центре. Сжатие лицевого нерва приводит к дегенеративным реакциям вблизи участка повреждения и к уоллеровскому перерождению в отдаленной области, что вызывает уменьшение движения усов на поврежденной стороне.
Самцов крыс Long-Evans (150-180 г) анестезируют 3-5% изофлораном для индукции и 2% для поддержания наркоза в течение хирургических операций. Правый лицевой нерв оголяют и сжимают пинцетом в течение 30 сек на выходе из шилососцевидного отверстия. Левый лицевой нерв подвергается фиктивной операции и служит внутренним контролем. Сжатие нерва вызывает паралич мышц, отвечающих за движение усов, и следовательно, уменьшает движение усов на поврежденной стороне, что наблюдается сразу после окончания действия анестезии. Наблюдаются следующие морфологические нарушения, связанные с функциональной недостаточностью:
(1) увеличение числа окружающих нервную ткань глиальных клеток в лицевом центре поврежденной стороны, причем наблюдаемый максимум увеличения составляет приблизительно D3-6;
(2) утоньшение миелиновой оболочки и уменьшение окрашивания основного миелинового белка в подвергавшемся сжатию лицевом нерве приблизительно через одну неделю после повреждения;
(3) морфологические изменения в области N-M соединения и в участках волосяных сумок усов, а также постепенная дегенерация двигательных нейронов в лицевом центре.
После прекращения действия анестезии крыс произвольно делят на группы, которым вводят среду, αMSH или анализируемое соединение, по 6 животных в группе. αMSH (п.к. 70 мкг/каждые 48 ч) используют в качестве положительного контроля. Анализируемые соединения вводят п.о. в количестве 20 мг/кг в течение 14 дней. Восстановление движения усов определяют ежедневно после операции, используя два критерия:
(1) частоту движения усов на поврежденной стороне по сравнению с другой стороной (подвергшейся фиктивной операции), которая служит фоновым контролем
(2) полуколичественные определения (от 0 до 4+) напряжения мышц усов, которое характеризуется процентом движущихся усов, тонусом мышц усов и положением носа, определяемыми наблюдением. При всех наблюдениях организация эксперимента была неизвестна для наблюдателя за поведением.
Результаты поведенческого эксперимента показали, что оба анализируемые соединения, соединения #31 и #84, ускоряют время восстановления двигательной функции мышечного волокна у крыс с повреждением по сравнению с контрольной средой (p<0,05). Скорость восстановления двигательной функции волокна выражают в виде процента от внутреннего контроля (с фиктивной операцией), результаты приведены в таблице 8.
Функциональное восстановление движения усов после перорального введения соединения #31 и #84 у модели сжатия лицевого нерва
15,9
8,3
(246377)
(153791)
ПРИМЕР 10
Анализ in Vitro: Исследование регуляции синтеза сальных липидов.
Стадия A: Получение питающего подслоя
Полуконфлюэнтные культуры мышиных фибробластов 3T3 (мышь Swiss Albino, ATCC CCL-92) обрабатывают митомицином C(4 мкг/мл) в течение 3 часов, трипсинизируют и высевают с плотностью 2,5x105/чашку для культивирования тканей площадью 9,5 см2 в минимальной поддерживающей среде Дульбекко (DMEM), содержащей 10% колорадской телячьей сыворотки, PNC (100 ЕД/мл), STM (100 мкг/мл), L-глютамин (0,3 мг/мл), пируват натрия (1 мМ) и заменимые аминокислоты (100 мкМ). Клетки инкубируют при 37°C в течение 24 часов перед применением в качестве питающего подслоя для себоцитов.
Стадия B: Выделение человеческих себоцитов
Человеческие себоциты выделяют из дерматомных фрагментов послеоперационных кусочков человеческой кожи глубиной 0,4-0,8 мм (ранее было показано, что данная часть кожи обогащена сальными железами). Полученные таким образом фрагменты обрабатывают 1% диспазой в среде Iscoves, содержащей 10% сыворотки, в течение 20 мин при 37°C. Затем ткань помещают в раствор, содержащий 0,3% трипсина/1% EDTA в физиологическом растворе с фосфатным буфером (PBS), на 10 минут при 37°C. После данной инкубации клетки осторожно соскабливают с ткани в питательной среде (GM), включающей смесь сред DMEM/F12 (3:1), и дополнительно содержащей 8% инактивированную нагреванием FBS, 2% инактивированную нагреванием человеческую сыворотку (HS), 1 мМ пируват натрия, эпидермальный фактор роста (10 нг/мл), инсулин (10 мкг/мл), гидрокортизон (0,4 мкг/мл) и +/-холерный токсин (100 мкг/мл), L-глютамин и антибиотики. Полученные таким образом клетки фильтруют через нейлоновое сито (размер пор 100 микрон), центрифугируют при 750 об/мин, снова суспендируют в GM и считают.
Стадия C: Культуры человеческих себоцитов
Клетки, полученные по описанному выше методу выделения, помещают на питающие подслои 3T3 с плотностью 2x105/9,5 см2 в питательной среде и держат при 37°C и 5% CO2 в течение 3 дней (фаза I). После начального периода роста их переносят в переходную среду (TM), которая состоит из сред DMEM/F12, дополнительно содержащую 1 мМ пируват натрия, инсулин (10 мкг/мл), трансферрин (6,7 нг/мл) и селен (5,5 мкг/мл) (ITS), 2% инактивированную нагреванием FBS и 2% инактивированную нагреванием человеческую сыворотку, а также +/-холерный токсин (ch. t.)(100 мкг/мл), L-глютамин и антибиотики (фаза II). Через три дня среду меняют на дифференцировочную среду (DM), DMEM/F12, дополнительно содержащую ITS, 3,3',5-триидо-L-тиронин натрия (3 нМ), 1% (об./об.) смеси микроэлементов и конкретный дифференцировочный агент, т. е. экстракт бычьего гипофиза (10 мкг/мл). Данную среду меняют каждые три дня (фаза III).
Стадия D: Выявление стимуляторов или ингибиторов дифференциации себоцитов и продукции липидов
Гормоны, смесь гормонов, т. е. экстракт бычьего гипофиза, или анализируемые соединения добавляют к культуре в начале фазы III. Для оценки влияния данных веществ на культуры сальных желез используют два критерия: 1) визуальные наблюдения и 2) определение аккумуляции и синтеза липидов в сальных железах. Аккумуляцию липидов определяют, используя нильский красный. Данный метод основан на визуализации нейтральных липидов с помощью нильского красного и определении их количества путем считывания флуоресценции на планшетрет-ридере при длине волны возбуждения 535 нм и длине волны эмиссии 580 нм. Синтез липидов оценивают путем радиоактивного мечения с использованием 14C-ацетата, количество радиоактивности определяют с помощью Bio Rad Phosphoimager (Molecular Imager, FX), используя программное обеспечение 4.1.
Стадия E: Определение аккумуляции липидов путем визуальных наблюдений и с помощью нильского красного
Морфологическое определение аккумуляции липидов легко осуществить, так как клетки укрупняются и образуют липидные гранулы, которые в светлом поле оптического микроскопа выглядят как желтоватые круги внутри клеток. Количественное определение аккумуляции/ингибирования синтеза нейтральных липидов в себоцитах проводят с помощью анализа связывания с использованием нильского красного. Коротко говоря, после обработки себоцитов анализируемыми соединениями, клетки оставляют взаимодействовать с 1 мкМ нильского красного в забуференном солевом растворе Хэнкса, содержащем ДМСО и Pluronic F127. После 4 часов инкубации, промывания и инкубации в течение ночи, флуоресценцию считывают на планшетрет-ридере при длине волны возбуждения 535 нм и длине волны эмиссии 580 нм. Для того чтобы определить, ингибируют ли соединения рост клеток, считают клетки.
С помощью описанного выше метода путем визуального наблюдения и с использованием нильского красного анализируют влияние отдельных соединений настоящего изобретения, результаты приведены в таблице 9.
0,4 мкМ
0,8 мкМ
IC50
Стадия F: Оценка синтеза сальных липидов в клетках сальных желез
Ha 11 день культивирования себоциты метят 14С-ацетатом с конечной концентрацией 2 мкКи/мл в течение 24 часов в питательной среде, не содержащей сыворотки. Затем клетки соскабливают с чашек и замораживают при -80°С в стекляных флаконах. Липиды экстрагируют по методу Bligh-Dyer (Bligh, E.G. and Dyer, W.J., Can. J. Biochem. Physiol., 1959, 37, pp. 911-916) с небольшим изменением, подробно описанным в данном документе. Коротко говоря, клетки гомогенизируют в смеси хлороформ:метанол 2:1 в присутствии KCl. Органическую фазу удаляют из смеси, выделенные липиды сушат в атмосфере аргона и наносят на пластинки для тонкослойной хроматографии высокого разрешения (ТСХВР). Для ТСХВР используют три отдельные мобильные фазы. В качестве первой используют гексан (до верхнего края пластины), затем толуол (до верхнего края) и наконец смесь гексан:эфир:уксусная кислота 70:30:1 (до середины пластины - 10 см). Затем пластины экспонируют с радиографической пленкой для визуализации радиоактивных образцов липидов. Для визуализации немеченных липидов пластины обрабатывают кислотой, содержащей 8% меди II, и обугливают на горячей плите. Количественную обработку результатов проводят с помощью Image Pro Plus 3.0 (Media Cybernetics, Silver Springs, MD).
С помощью описанного выше метода анализируют способность отдельных соединений настоящего изобретения ингибировать дифференцировку человеческих себоцитов. На окрашенных клеточных культурах, обработанных соединением #74, визуально обнаружено, что в культурах себоцитов через семь дней после обработки полностью исчезают липидные гранулы. При анализе синтеза липидов в тех же клетках, проводимом с использоованием радиоактивномеченных липидов, разделяемых с помощью ТСХВР, обнаружено, что происходит ингибирование синтеза сквалена, эфиров холестерина и сложных эфиров воска. Количественную оценку клеточных панелей проводят, измеряя интенсивность полос с помощью Image Pro Plus (версия 5.0). % Ингибирования рассчитывают на основании разницы между обработанными образцами и контролями, обработанными средой, результаты приведены в таблице 10.
0,4 мкМ
0,6 мкМ
ПРИМЕР 11
Оценка влияния анализируемого соединения на продукцию кожного сала in vivo: человеческая кожа-мышиная химерная модель SCID
Мыши с тяжелым комбинированным иммунодефицитом (SCID - Severe combined immunodeficient) являются бесценной моделью для ксенотрансплантации кожи. У данных животных отсутствует как T-, так и B-клеточный иммунитет. Трансплантаты человеческой кожи у мышей SCID сохраняют компоненты человеческой клеточной ткани, в том числе иммунные клетки кожи, т. е. клетки Лангерганса, макрофаги и лимфоциты, а также часть пересаженного эндотелия (Kaufman R., et al., Exp. Dermatol. 1993: 2: 209-216, 1993). Данные свойства позволяют изучать физиологические и/или патологические ответы клеток человеческой кожи на анализируемое соединение.
Стадия A: Метод трансплантации:
Для трансплантации используют мышей C.B-17 scid/scid (Taconic, Germantown, N. Y.) возрастом 5-6 недель. Полнослойную кожу лица человека срезают до толщины ˜0,4 мм с помощью дерматома Формана (Forman Dermatome). Срезы кожи промывают 3 раза в растворе антибиотиков и фунгицидов (пенициллин, стрептомицин, фунгизон) (Life technologies) в модифицированной по Дульбекко среде Игла (DMEM, Life Technologies). Овальные кусочки кожи размером ˜ 2,0-2,5x1,0-1,5 пересаживают на подготовленный для трансплантации участок и накладывают швы, используя шелковые нити 4,0. В процессе хирургической операции мышей анестезируют смесью Ketaset (0,16 мг/г массы тела) и Rompun (8,0 мкг/г массы тела).
Хорошо известно, что процесс заживления раны при трансплантации кожи мышам SCID длится один месяц, в это время человеческую кожу можно использовать для экспериментальных целей. Авторы данного избретения также обнаружили, что в трансплантированной человеческой коже происходит постепенная регенерация сальных желез, и что через 7 недель указанные железы полностью регенерируются и секретируют кожное сало, что подтверждено с помощью Sebutape и гистоморфометрии. Железы достигают максимального размера через 3 месяца после трансплантации. Железы сохраняют способность продуцировать специфическое человеческое кожное сало, а железистая ткань экспрессирует специфические человеческие маркеры, в том числе MC5-R. Так как железы достигают максимального размера через 2-3 месяца после трансплантации, влияние ингибиторов на секрецию кожного сала анализируют в данный момент времени.
Стадия B: Способ обработки:
Для экспериментов используют мышей спустя 2-3 месяца после трансплантации кожи лица человека. Область трансплантата обрабатывают раствором анализируемого соединения с желательной(ыми) концентрацией(ями) в полиэтиленгликоле-этаноле (20 мкл/2 см2). Контроли обрабатывают только средой. Анализируемые соединения наносят ежедневно, включая выходные. Секрецию кожного сала определяют с помощью Sebutape через 15 и 30 дней после обработки.
Стадия C: Окончание эксперимента.
Окончание эксперимента определяют путем предварительной клинической оценки продукции кожного сала с помощью SEBUTAPE. В это время трансплантаты человеческой кожи удаляют и репрезентативные образцы собирают для гистологического анализа. Более конкретно, получают образцы пункционной биопсии размером 2 мм и используют их для анализа синтеза липидов и общей аккумуляции липидов в обработанных тканях.
Стадия D: Анализ синтеза липидов и общей аккумуляции липидов в исследуемых тканях.
Собранные образцы пункционной биопсии размером 2 мм помещают отдельно в 96-луночные планшеты в буфере Кребса и метят 10 мкКи 14C-ацетата в течение 3 часов. По окончании периода мечения образцы промывают в среде, объединяют по 5 образцов, взвешивают и используют для экстракции липидов. Экстракцию липидов и анализ методом ТСХВР проводят по способу, описанному для клеток, полученных из тканевой культуры.
С помощью описанного выше метода соединение #74 настоящего изобретения анализируют на способность ингибировать активность сальной железы через 11 дней после обработки человеческой кожи, трансплантированной мыши SCID.
Визуальное наблюдение за сальной железой показывает, что местная обработка 0,1% раствором соединения #74 приводит к видимому уменьшению размеров сальной железы и к понижению регуляции синтеза сальных липидов. Местная обработка в течение 15 дней 0,05% и 0,005% растворами не является достаточной для обнаружения понижения регуляции синтеза липидов. Количественное определение ингибирования синтеза человеческих сальных липидов в данных клетках осуществляют с помощью ТСХВР, результаты приведены в таблицах 11, 12 и 13. Значения % ингибирования приведены по отношению к контролю.
Влияние соединения #74 на синтез человеческих сальных липидов (11 день обработки)
Влияние соединения #74 на аккумуляцию липидов (30 день обработки)
Влияние соединения #74 на синтез сальных липидов (30 день обработки)
Как показано в приведенных выше таблицах 12 и 13, и общая аккумуляция сальных липидов, и синтез сальных липидов de novo, значительно уменьшаются после 30 дней местной обработки 0,05% и 0,01% раствором соединения #74.
ПРИМЕР 12
Пероральная композиция
Для получения конкретного воплощения пероральной композиции 100 мг соединения #74 примера 2 смешивают с достаточно тонко измельченной лактозой, получая в общей сложности 580 - 590 мг для заполнения твердой гелевой капсулы размером 0.
ПРИМЕР 13
Композиции для местного применения
A: Микроэмульсия
Для получения конкретного воплощения микроэмульсионной композиции смешивают следующие компоненты, используя при необходимости нагревание:
Затем к полученной смеси медленно добавляют воду (42,9 массовых частей), перемешивают до необходимой степени, получая эмульсию.
B: Водно-спиртовой гель
Для получения конкретного воплощения водно-спиртовой гелевой композиции полипропиленгликоль (10 массовых частей), бутиленгликоль (10 массовых частей), бензиловый спирт (2 массовые части), EDTA (0,05 массовых частей) и BHT (0,05 массовых частей) смешивают с водой (74,85 массовых частей по отношению к общей массе). Смесь перемешивают, пока компоненты не растворятся. Затем медленно добавляют карбомер (например, Carbopol 934P от фирмы Goodrich) (3 массовые части) при постоянном вращении, получая гель. После чего соединение #74 (0,05 массовых частей) диспергируют в геле при перемешивании. рН геля доводят приблизительно до 3-4.
C: Безводный гель
Для получения конкретного воплощения безводного геля изопропанол (20 массовых частей) добавляют к бутиленгликолю (20 массовых частей). Затем к смеси изопропанол/бутиленгликоль добавляют BHT (0,05 массовых частей) и бензиловый спирт (1,0 массовых частей). После чего к полученной смеси при непрерывном перемешивании добавляют циклотетрасилоксан (D4) и органополисилоксан-11 (например, Gransil GSM Gel от Grant Industries) (58,85 массовых частей). Соединение #74 (0,1 массовых частей) измельчают и диспергируют в геле при непрерывном перемешивании до однородного распределения.
D: Крем
Для получения конкретного воплощения м/в (масло/вода) крема, следующие компоненты смешивают в указанных количествах (в массовых частях). рН Конечной смеси доводят до 2, используя соляную кислоту.
В то время как вышеприведенное описание разъясняет принципы настоящего изобретения, причем примеры предлагаются для иллюстрации, следует понимать, что на практике данное изобретение охватывает все традиционные вариации, адаптации и/или модификации, входящие в объем нижеследующей формулы изобретения, а также их эквиваленты.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ 1, 2, 4-ТИАДИАЗОЛИЯ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ МОДУЛЯТОРОВ РЕЦЕПТОРОВ МЕЛАНОКОРТИНА | 2002 |
|
RU2323932C2 |
| ПРИМЕНЕНИЕ МОДУЛЯТОРОВ РЕЦЕПТОРА S1P В ОФТАЛЬМОЛОГИИ | 2006 |
|
RU2497513C2 |
| НОВЫЕ ЗАМЕЩЕННЫЕ СУЛЬФАМАТНЫЕ ПРОТИВОСУДОРОЖНЫЕ ПРОИЗВОДНЫЕ | 2003 |
|
RU2328502C2 |
| ИСПОЛЬЗОВАНИЕ МОДУЛЯТОРА РЕЦЕПТОРА S1P | 2008 |
|
RU2498796C2 |
| НОВЫЕ ИНГИБИТОРЫ 17β-ГИДРОКСИСТЕРОИД-ДЕГИДРОГЕНАЗЫ ТИПА I | 2004 |
|
RU2369614C2 |
| КОМПОЗИЦИЯ С ДЛИТЕЛЬНЫМ ВЫСВОБОЖДЕНИЕМ, СОДЕРЖАЩАЯ В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА ПЕПТИДЫ | 2012 |
|
RU2633483C2 |
| ЖИДКИЕ СОСТАВЫ | 2006 |
|
RU2470631C2 |
| ЖИДКИЕ СОСТАВЫ | 2006 |
|
RU2428180C2 |
| СПОСОБ ЛЕЧЕНИЯ ДИАБЕТА | 2003 |
|
RU2320343C2 |
| ЗАМЕЩЕННЫЕ 3-ЦИАНОТИОФЕНАЦЕТАМИДЫ В КАЧЕСТВЕ АНТАГОНИСТОВ РЕЦЕПТОРА ГЛЮКАГОНА | 2004 |
|
RU2336274C2 |
Настоящее изобретение относится к новым производным 1,2,4-тиадиазола формулы (II)
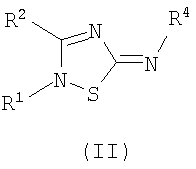
где R1, R2 и R4 представляют собой радикалы, содержащие циклические фрагменты, которые могут использоваться в качестве агонистов или антагонистов рецептора меланокортина. Целью настоящего изобретения является получение фармацевтических композиций, включающих заявляемые соединения, взятые в терапевтически эффективном количестве, которые могут применяться для лечения заболеваний, опосредованных рецептором меланокортина, например, таких как метаболические нарушения, нарушения, связанные с ЦНС, и дерматологические нарушения. 7 н. и 13 з.п. ф-лы, 13 табл., 5 сх.
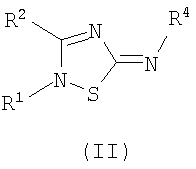
где R1 представляет собой замещенный фенил,
где фенильная группа замещена одним или несколькими заместителями, независимо выбранными из галогена, низшего алкила или низшего алкокси;
R2 представляет собой замещенный фенил,
где фенильная группа замещена одним или несколькими заместителями, независимо выбранными из низшего алкила или низшего алкокси;
R4 представляет собой фенил,
где фенильная группа необязательно замещена одним или несколькими заместителями, независимо выбранными из галогена, низшего алкила или низшего алкокси,
и его фармацевтически приемлемые соли.
R1 представляет собой замещенный фенил, где фенильная группа замещена одним или двумя заместителями, выбранными из галогена, низшего алкила и низшего алкокси;
R2 представляет собой замещенный фенил, где фенильная группа замещена одним или двумя заместителями, выбранными из низшего алкила и низшего алкокси;
R4 представляет собой фенил, где фенил имеет один или два заместителя, независимо выбранных из галогена, низшего алкила и низшего алкокси,
и его фармацевтически приемлемые соли.
R1 представляет собой 2-метоксифенил; R2 представляет собой 2-метоксифенил;
R4 выбран из группы, включающей фенил, 4-метоксифенил, 2,6-дифторфенил, 3,5-дифторфенил и 2-хлор-6-метилфенил, и его фармацевтически приемлемые соли.

где R1 представляет собой замещенный фенил,
где фенильная группа замещена одним или несколькими заместителями, независимо выбранными из галогена, низшего алкила и низшего алкокси;
R2 представляет собой фенил,
где фенильная группа замещена одним или несколькими заместителями, независимо выбранными из низшего алкила и низшего алкокси;
R4 представляет собой замещенный фенил,
где фенильная группа замещена одним или несколькими заместителями, независимо выбранными из галогена, низшего алкила и низшего алкокси, и его фармацевтически приемлемые соли.

где R1 представляет собой замещенный фенил,
где фенильная группа замещена одним или несколькими заместителями, независимо выбранными из галогена, низшего алкила или низшего алкокси;
R2 представляет собой замещенный фенил,
где фенильная группа замещена одним или несколькими заместителями, независимо выбранными из низшего алкила или низшего алкокси;
R4 представляет собой фенил,
где фенильная группа замещена одним или несколькими заместителями, независимо выбранными из галогена, низшего алкила или низшего алкокси,
и его фармацевтически приемлемых солей.
R1 представляет собой замещенный фенил, где фенильная группа замещена одним заместителем, выбранным из галогена, низшего алкила и низшего алкокси;
R2 представляет собой замещенный фенил, где фенильная группа замещена одним заместителем, выбранным из низшего алкила и низшего алкокси;
R4 представляет собой фенил, где фенил имеет один или два заместителя, независимо выбранных из галогена, низшего алкила и низшего алкокси,
и его фармацевтически приемлемых солей.
R1 представляет собой 2-метоксифенил;
R2 представляет собой 2-метоксифенил;
R4 выбран из группы, включающей фенил, 2,6-дифторфенил, 3,5-дифторфенил и 2-хлор-6-метилфенил,
и его фармацевтически приемлемых солей.
| RU 2000101856 А, 10.11.2001 | |||
| W.Abraham, G.Barnikow | |||
| "Formamidinoylisothionate-III | |||
| Addition nucleophiler partner an formamidinoylisothiocyanate" | |||
| Tetrahedron, 29 (5), 699-705 (German) 1973 | |||
| WO 200155107 A, 02.08.2001. |
Авторы
Даты
2008-02-20—Публикация
2002-11-04—Подача