Данное изобретение относится к бифосфонатам, в особенности к новым их применениям и композициям, содержащим бифосфонаты.
Бифосфонаты широко применяются для подавления активности остеокластов при разнообразных как доброкачественных, так и злокачественных заболеваниях, которые включают чрезмерную и нецелесообразную резорбцию костей. Эти аналоги пирофосфатов не только снижают распространенность явлений, связанных со скелетом, но они также приносят пациентам пользу в клинических условиях и улучшают выживаемость. Бифосфонаты способны предупреждать резорбцию костей in vivo; терапевтическая эффективность бифосфонатов продемонстрирована при лечении остеопороза, остеопении, костной болезни Педжета, индуцированной опухолью гиперкальциемии (TIH) и совсем недавно костных метастазов (ВМ) и множественной миеломы (ММ) (для обзора смотри Fleisch H., 1997. Bisphosphonates clinical. В: «Bisphosphonates in Bone Disease. From the Laboratory to the Patient». Изд-во: The Parthenon Publishing Group, New York/London, стр.68-163). Механизмы, по которым бифосфонаты подавляют резорбцию костей еще не полностью ясны и, по-видимому, изменяются по мере изучения бифосфонатов. Показано, что бифосфонаты прочно связываются с кристаллами гидроксиапатита кости, понижая костный обмен и резорбцию, уменьшая уровни гидроксипролина или щелочной фосфатазы в крови и, кроме того, ингибируя образование, восстановление, активацию и активность остеокластов.
Недавние исследования показали также, что некоторые бифосфонаты могут оказать непосредственное воздействие на опухолевые клетки. Так, например, было найдено, что относительно высокие концентрации бифосфонатов, включая золедронат, индуцируют апоптоз карциномы молочной и предстательной желез и миеломных клеток in vitro (Senaratne и др., Br. J. Cancer, 82: 1459-1468, 2000; Lee и др., Cancer Res., 61: 2602-2608, 2001, Shipman и др., Br. J. Cancer, 98: 665-672 (1997).
В настоящее время найдено, что если некоторые типы бифосфонатов применяются в комбинации с некоторыми типами ингибиторов циклооксигеназы-2 (СОХ-2) для обработки клеток злокачественных опухолей in vitro, то достигается усиленное и в некоторых случаях взаимно усиливающее ингибирование роста клеток по сравнению с применением по отдельности или бифосфоната, или ингибитора СОХ-2.
Соответственно настоящее изобретение обеспечивает фармацевтическую композицию для лечения злокачественных новообразований, которая включает в комбинации бифосфонат и ингибитор СОХ-2, для одновременного, последовательного или раздельного применения.
Далее изобретение обеспечивает применение ингибитора СОХ-2 при получении лекарственного средства для применения в комбинации с бифосфонатом при лечении злокачественного заболевания.
В качестве альтернативы изобретение обеспечивает применение бифосфоната при получении лекарственного средства для применения в комбинации с ингибитором СОХ-2 при лечении злокачественного заболевания.
В дальнейшем аспекте изобретение обеспечивает способ лечения пациента, страдающего злокачественным заболеванием, включающий введение пациенту эффективного количества бифосфоната и эффективного количества ингибитора СОХ-2.
Еще дополнительно изобретение обеспечивает применение ингибитора СОХ-2 в комбинации с бифосфонатом, чтобы подавить рост злокачественных опухолевых клеток или индуцировать апоптоз злокачественных опухолевых клеток.
Соответственно настоящее изобретение в дальнейшем также обеспечивает фармацевтическую композицию для подавления роста злокачественных клеток или индуцирования апоптоза злокачественных клеток, которая включает в комбинации бифосфонат и ингибитор СОХ-2, для одновременного, последовательного или раздельного применения.
Далее изобретение обеспечивает применение бифосфоната в получении лекарственного средства для применения в комбинации с ингибитором СОХ-2 при ингибировании роста злокачественных клеток или индуцировании апоптоза злокачественных клеток.
В предпочтительных вариантах осуществления изобретения бифосфонат и ингибитор СОХ-2 применяют в комбинации с таксолом или его производным.
Соответственно еще в дальнейшем аспекте настоящее изобретение обеспечивает также фармацевтическую композицию для лечения злокачественных новообразований, которая включает в комбинации бифосфонат, таксол или его производное и ингибитор СОХ-2, для одновременного, последовательного или раздельного применения.
Далее изобретение обеспечивает применение таксола или его производного при получении лекарственного средства для применения в комбинации с бифосфонатом и ингибитором СОХ-2 при лечении злокачественного новообразования.
Еще в дальнейшем изобретение обеспечивает способ лечения пациента, страдающего злокачественным заболеванием, включающий введение пациенту эффективного количества бифосфоната, эффективного количества ингибитора СОХ-2 и эффективного количества таксола или его производного.
В соответствии с настоящим изобретением было найдено, что все возможные двойные комбинации (а) бифосфонатов, (б) ингибитора СОХ-2 и (в) таксола или его производного, как исследовано, проявляют усиленное ингибирование опухолевых клеток при сравнении с применением каждого агента в отдельности.
Таким образом, еще в дальнейших вариантах воплощения изобретение обеспечивает: способ лечения пациента, страдающего злокачественным заболеванием, включающий введение пациенту эффективного количества таксола или его производного в комбинации с эффективным количеством бифосфоната или эффективным количеством ингибитора СОХ-2; соответствующую фармацевтическую композицию для одновременного, последовательного или раздельного применения; применение соответствующих двойных комбинаций, т.е. таксола или его производного+бифосфонат либо таксол или его производное+ингибитор СОХ-2, для получения противоопухолевых лекарственных средств.
В настоящем описании термин «лечение» включает одновременно профилактическое или превентивное лечение, а также целительное или модифицирующее заболевание лечение, включая терапию пациентов при опасности заражения болезнью или подозреваемых в заражении болезнью, так же как больных пациентов.
Изобретение, как правило, применимо к лечению злокачественных заболеваний, для которых показана терапия бифосфонатами. Так, обычно заболевание означает злокачественное заболевание, которое ассоциировано с развитием костных метастазов или чрезмерной резорбцией костей. Примеры таких заболеваний включают злокачественные опухоли, такие как злокачественные опухоли молочной и предстательной желез, множественную миелому (ММ), индуцированную опухолью гипертензию (TIH) и подобные заболевания и состояния. В особенности изобретение применимо к лечению костных метастазов (ВМ), ассоциируемых с такими злокачественными опухолями, как рак молочной железы, рак легкого, рак ободочной кишки или рак предстательной железы.
Композиции, применения и способы по настоящему изобретению представляют собой усовершенствование существующей терапии злокачественных заболеваний, при которых бифосфонаты применяются для предупреждения или подавления развития костных метастазов или чрезмерной костной резорбции и при которых (как было обнаружено в соответствии с настоящим изобретением) терапия бифосфонатами подавляет также рост опухолевых клеток или индуцирует апоптоз опухолевых клеток. Комбинация бифосфоната с ингибитором СОХ-2, особенно также с таксолом или его производным успешно вызывает повышенные или даже взаимно усиленные уровни ингибирования роста опухолевых клеток или апоптоза опухолевых клеток.
Бифосфонаты для применения по настоящему изобретению являются предпочтительно N-бифосфонатами.
Для целей настоящего описания N-бифосфонат означает соединение, которое в добавление к характеристической геминальной бифосфонатной части включает азот, содержащий боковую цепь, например соединение формулы I
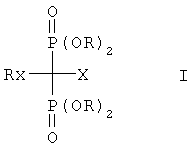
где
Х означает водород, гидроксил, амино, алканоил или аминогруппу, замещенную (С1-С4)алкилом или алканоилом;
R означает водород или (С1-С4)алкил, и
Rx означает боковую цепь, которая содержит необязательно замещенную аминогруппу, или азотсодержащий гетероцикл (включая ароматические азотсодержащие гетероциклы) и
его фармацевтически приемлемые соли или любой его гидрат.
Так, например, соответствующие N-бифосфонаты для применения по изобретению могут включать следующие соединения или их фармацевтически приемлемую соль, или любой их гидрат: 3-амино-1-гидроксипропан-1,1-дифосфоновая кислота (памидроновая кислота), например памидронат (APD); 3-(N,N-диметиламино)-1-гидроксипропан-1,1-дифосфоновая кислота, например диметил-APD; 4-амино-1-гидроксибутан-1,1-дифосфоновая кислота (алендроновая кислота), например алендронат; 1-гидрокси-3-(метилпентиламино)пропилиденбисфосфоновая кислота, ибандроновая кислота, например ибандронат; 6-амино-1-гидроксигексан-1,1-дифосфоновая кислота, например, аминогексил-ВР; 3-(N-метил-N-н-пентиламино)-1-гидроксипропан-1,1-дифосфоновая кислота, например метилпентил-APD (=ВМ 21.0955); 1-гидрокси-2-(имидазол-1-ил1)этан-1,1-дифосфоновая кислота, например золедроновая кислота; 1-гидрокси-2-(3-пиридил)этан-1,1-дифосфоновая кислота (ризедроновая кислота), например ризедронат, включая их N-метилпиридиниевые соли, например йодиды N-метилпиридиния, такие как NE-10244 или NE-10446; 3-[N-(2-фенилтиоэтил)-N-метиламино]-1-гидроксипропан-1,1-дифосфоновая кислота; 1-гидрокси-3-(пирролидин-1-ил)пропан-1,1-дифосфоновая кислота, например ЕВ 1053 (Leo); 1-(N-фениламинотиокарбонил)метан-1,1-дифосфоновая кислота, например FR 78844 (Fujisawa); тетраэтиловый эфир 5-бензоил-3,4-дигидро-2H-пиразол-3,3-дифосфоновой кислоты, например U-81581 (Upjohn); и 1-гидрокси-2-(имидазо[1,2-а]пиридин-3-ил)этан-1,1-дифосфоновая кислота, например YM 529.
В одном варианте воплощения особенно предпочтительный N-бифосфонат для применения по изобретению включает соединение формулы II
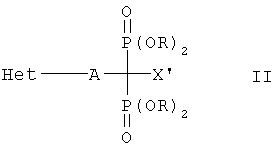
где
Het означает имидазол, оксазол, изоксазол, оксадиазол, тиазол, тиадиазол, пиридин, 1,2,3-триазол, 1,2.4-триазол или бензимидазольный радикал, который необязательно замещен алкилом, алкокси, галоидом, гидроксилом, карбоксилом, аминогруппой, необязательно замещенной алкильным или алканоильным радикалами, или бензильный радикал, необязательно замещенный алкилом, нитро, амино или аминоалкилом;
А означает линейную или разветвленную, насыщенную или ненасыщенную углеводородную часть, содержащую от 1 до 8 атомов углерода;
X' означает атом водорода, необязательно замещенный алканоилом или аминогруппой, необязательно замещенной алкильным или алканоильным радикалами, и
R означает атом водорода или алкильный радикал, и его фармакологически приемлемую соль.
В дальнейшем варианте воплощения особенно предпочтительный бифосфонат для применения по изобретению включает соединение формулы III
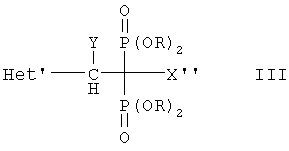
где
Het' означает замещенное или незамещенное гетероароматическое пятичленное кольцо, выбранное из группы, состоящей из имидазолила, имидазолинила, изоксазолила, оксазолила, оксазолинила, тиазолила, тиазолинила, триазолила, оксадиазолила или тиадиазолила, где упомянутое кольцо может быть частично гидрированным и где упомянутый заместитель выбирают по крайней мере из одной группы, состоящей из (С1-С4)алкила, (C1-С4)алкокси, фенила, циклогексила, циклогексилметила, галоида и амино и где два смежных алкильных заместителя Het' могут вместе образовать второе кольцо;
Y означает водород или (С1-С4)алкил;
X'' означает водород, гидроксил, амино или аминогруппу, замещенную (С1-С4)алкилом, и
R означает водород или (С1-С4)алкил; а также
его фармакологически приемлемые соли.
Еще в одном варианте воплощения особенно предпочтительный бифосфонат для применения по изобретению включает соединение формулы IV
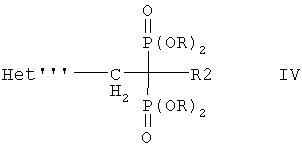
где
Het'''означает имидазолил, 2H-1,2,3-, 1H-1,2,4- или 4H-1,2,4-триазолил, тетразолил, оксазолил, изоксазолил, оксадиазолил, тиазолил или тиазолильный радикал, который является незамещенным или С-моно- либо дизамещенным (низш.)алкилом, (низш.)алкокси и/или галоидом, гидрокси, ди(низш.)алкиламино, (низш.)алкилтио и N-замещенным по замещаемому атому азота (низш.)алкилом или фенил(низш.)алкилом, который, в свою очередь, может быть моно- либо дизамещенным в фенильной части (низш.)алкилом, (низш.)алкокси и/или галоидом, и
R2 означает водород, гидрокси, амино, (низш.)алкилтио или галоид, причем низшие радикалы содержат до и включая 7 углеродных атомов, или его фармакологически приемлемую соль.
Примерами особенно предпочтительных N-бифосфонатов для применения по изобретению являются:
2-(1-метилимидазол-2-ил)-1-гидроксиэтан-1,1-дифосфоновая кислота;
2-(1-бензилимидазол-2-ил)-1-гидроксиэтан-1,1-дифосфоновая кислота;
2-(1-метилимидазол-4-ил)-1-гидроксиэтан-1,1-дифосфоновая кислота;
1-амино-2-(1-метилимидазол-4-ил)этан-1,1-дифосфоновая кислота;
1-амино-2-(1-бензилимидазол-4-ил)этан-1,1-дифосфоновая кислота;
2-(1-метилимидазол-2-ил)этан-1,1-дифосфоновая кислота;
2-(1-бензилимидазол-2-ил)этан-1,1-дифосфоновая кислота;
2-(имидазол-1-ил)-1-гидроксиэтан-1,1-дифосфоновая кислота;
2-(имидазол-1-ил)этан-1,1-дифосфоновая кислота;
2-(4H-1,2,4-триазол-4-ил)-1-гидроксиэтан-1,1-дифосфоновая кислота;
2-(тиазол-2-ил)этан-1,1-дифосфоновая кислота;
2-(имидазол-2-ил)этан-1,1-дифосфоновая кислота;
2-(2-метилимидазол-4(5)-ил)этан-1,1-дифосфоновая кислота;
2-(2-фенилимидазол-4(5)-ил)этан-1,1-дифосфоновая кислота;
2-(4,5-диметилимидазол-1-ил)-1-гидроксиэтан-1,1-дифосфоновая кислота,
2-(2-метилимидазол-4(5)-ил)-1-гидроксиэтан-1,1-дифосфоновая кислота,
и их фармакологически приемлемые соли.
Наиболее предпочтительным N-бифосфонатом для применения по изобретению является 2-(имидазол-1-ил)-1-гидроксиэтан-1,1-дифосфоновая кислота (золедроновая кислота) или ее фармакологически приемлемая соль.
Все производные N-бифосфоновой кислоты, упомянутые выше, хорошо известны из литературы. Это включает их получение (смотри, например ЕР-А-513760, стр.13-48). Например, 3-амино-1-гидроксипропан-1,1-дифосфоновую кислоту получают, как описано в патенте US 3962432, а также ее динатриевую соль, как описано в патентах US 4639338 и 4711880, и 1-гидрокси-2-(имидазол-1-ил)этан-1,1-дифосфоновую кислоту получают, как описано, например, в патенте US 4939130. Смотри также патенты US 4777163 и 4687767.
N-Бифосфонаты могут применяться в форме изомера или, где уместно, смеси изомеров, обычно оптических изомеров, таких как энантиомеры либо диастереоизомеры, или геометрических изомеров, обычно цис-транс-изомеров. Оптические изомеры получают в форме чистых антиподов и/или рацематов.
N-Бифосфонаты могут также применяться в форме их гидратов или включать другие растворители, использованные для их кристаллизации.
Ингибиторы СОХ-2, применяемые в фармацевтических композициях и способах лечения по настоящему изобретению, обычно являются такими, которые имеют значение IC50 при ингибировании СОХ-2 меньше, чем примерно 2 мкМ, и значение IC50 при ингибировании СОХ-1 выше, чем примерно 5 мкМ, например при измерении в анализе, описанном Brideau и др., Inflamm. Res. 45:68-74 (1996). Предпочтительно ингибитор СОХ-2 имеет коэффициент избирательности действия по меньшей мере 10, более предпочтительно по меньшей мере 40 для ингибирования СОХ-2 при сравнении с ингибированием СОХ-1.
Так, например, соответствующие ингибиторы СОХ-2 для применения по изобретению могут включать следующие соединения или их производные, или их фармацевтически приемлемые соли, или их гидраты: рофекоксиб, эторикоксиб, целекоксиб, вальдекоксиб, парекоксиб или ингибитор СОХ-2 на основе производного 5-алкил-2-ариламинофенилуксусной кислоты, например формулы V, как представлено ниже.
В варианте воплощения ингибитор СОХ-2 для применения по настоящему изобретению включает соединение формулы V

где
R означает метил или этил;
R1 означает хлор или фтор;
R2 означает водород или фтор;
R3 означает водород, фтор, хлор, метил, этил, метокси, этокси или гидрокси;
R4 означает водород или фтор;
R5 означает хлор, фтор, трифторметил или метил;
его фармацевтически приемлемые соли; и
его фармацевтически приемлемые сложноэфирные депо-формы.
Особыми соединениями формулы V являются те,
где
R означает метил или этил;
R1 означает хлор или фтор;
R2 означает водород;
R3 означает водород, фтор, хлор, метил или гидрокси;
R4 означает водород;
R5 означает хлор, фтор или метил;
их фармацевтически приемлемые соли;
их фармацевтически приемлемые сложные эфиры.
Особый вариант воплощения изобретения относится к соединениям формулы V,
R означает метил или этил;
R1 означает фтор;
R2 означает водород;
R3 означает водород, фтор или гидрокси;
R4 означает водород;
R5 означает хлор;
их фармацевтически приемлемым солям;
их фармацевтически приемлемым сложноэфирным депо-формам.
Другой особый вариант воплощения изобретения относится к соединениям формулы V
R означает метил или этил;
R1 означает фтор;
R2 означает водород или фтор;
R3 означает водород, фтор, этокси или гидрокси;
R4 означает водород или фтор;
R5 означает хлор, фтор или метил;
их фармацевтически приемлемым солям;
их фармацевтически приемлемым сложноэфирным депо-формам.
Далее упоминаются соединения,
R означает метил или этил;
R1 означает фтор;
R2-R4 означают водород или фтор;
R5 означает хлор или фтор;
их фармацевтически приемлемые соли;
их фармацевтически приемлемые сложноэфирные депо-формы.
Дальнейший вариант воплощения изобретения относится к соединениям формулы V,
R означает метил или этил;
R1 означает фтор;
R2 означает фтор;
R3 означает водород, этокси или гидрокси;
R4 означает водород или фтор;
R5 означает фтор;
их фармацевтически приемлемым солям;
их фармацевтические приемлемым сложноэфирным депо-формам.
Другой вариант воплощения изобретения относится к соединениям формулы V,
R означает метил;
R1 означает фтор;
R2 означает водород;
R3 означает водород или фтор;
R4 означает водород;
R5 означает хлор;
их фармацевтически приемлемым солям;
их фармацевтически приемлемым сложноэфирным депо-формам.
Особые варианты воплощения изобретения относятся к соединениям формулы V,
(а) где
R означает метил;
R1 означает фтор;
R2 означает водород;
R3 означает водород;
R4 означает водород;
R5 означает хлор;
его фармацевтически приемлемым солям;
его фармацевтически приемлемым сложноэфирным депо-формам.
(б) где
R означает метил;
R1 означает фтор;
R2 означает водород;
R3 означает фтор;
R4 означает водород;
R5 означает хлор;
его фармацевтически приемлемым солям;
его фармацевтически приемлемым сложноэфирным депо-формам.
(в) где
R означает этил;
R1 означает фтор;
R2 означает фтор;
R3 означает водород;
R4 означает фтор;
R5 означает фтор;
его фармацевтически приемлемым солям;
его фармацевтически приемлемым сложноэфирным депо-формам.
(г) где
R означает этил;
R1 означает хлор;
R2 означает водород;
R3 означает хлор;
R4 означает водород;
R5 означает метил;
его фармацевтически приемлемым солям;
его фармацевтически приемлемым сложноэфирным депо-формам.
Фармакологически приемлемые соли бифосфонатов и ингибиторов СОХ-2 являются предпочтительно солями с основаниями, удобно солями с металлами из групп Ia, Ib, IIa и IIb Периодической таблицы элементов, включая соли щелочных металлов, например, калиевые и особенно натриевые соли, предпочтительно соли кальция или магния и также аммониевые соли с аммиаком или органическими аминами.
Особенно предпочтительными фармацевтически приемлемыми солями N-бифосфонатов являются такие, где один, два, три или четыре, в особенности один или два, кислотных атома водорода бифосфоновой кислоты заменены на фармацевтически приемлемый катион, в особенности натрия, калия или аммония, в первую очередь - натрия.
Чрезвычайно предпочтительная группа фармацевтически приемлемых солей N-бифосфонатов отличается тем, что содержит один кислотный атом водорода и один фармацевтически приемлемый катион, особенно натриевый, в каждой их фосфоновых кислотных групп.
Альтернативный класс ингибиторов СОХ-2 для применения по изобретению составляет класс ингибиторов, относящихся к метансульфонанилидам, из которых NS-398, флосулид, нимесулид и соединение (i) являются приводимыми в качестве примера членами.
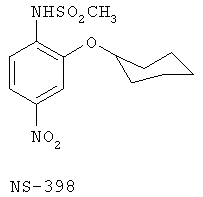
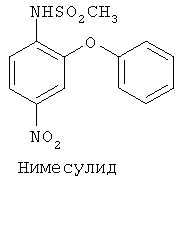
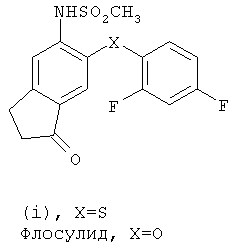
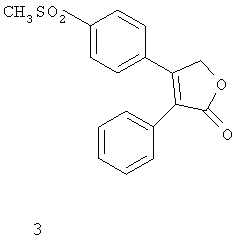
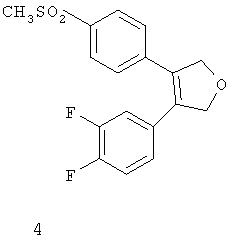
Другим классом ингибиторов СОХ-2 является класс трициклических ингибиторов, который далее может быть разделен на подклассы трициклических ингибиторов с центральным карбоциклическим кольцом (примеры включают SC-57666, 1 и 2; трициклических ингибиторов с центральным моноциклическим гетероциклическим кольцом (примеры включают DuP 697, SC-58125, SC-58635, SC-236 и 3, 4, 5); трициклических ингибиторов с центральным бициклическим гетероциклическим кольцом (примеры включают 6, 7, 8, 9 и 10). Соединения 3, 4 и 5 описаны в патенте US 5474995.
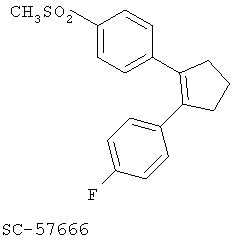
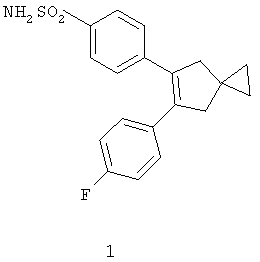
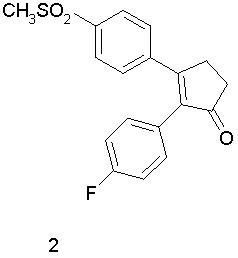
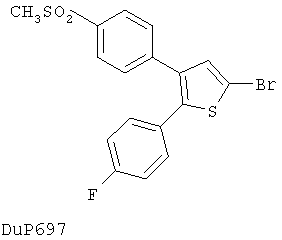
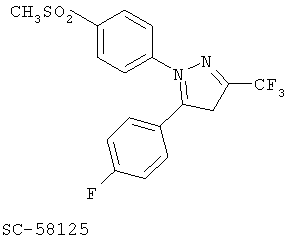
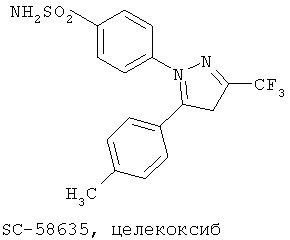
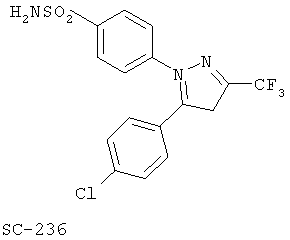
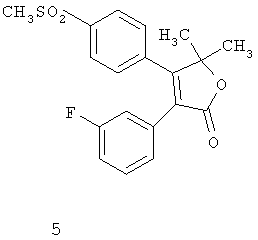
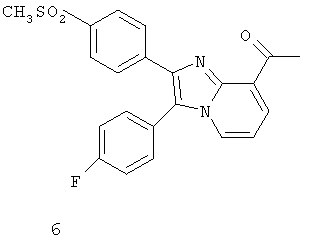
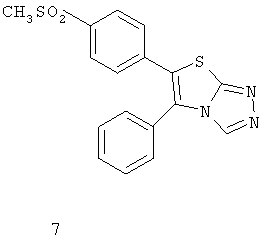
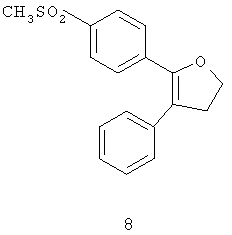

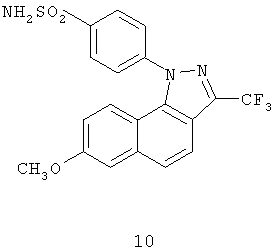
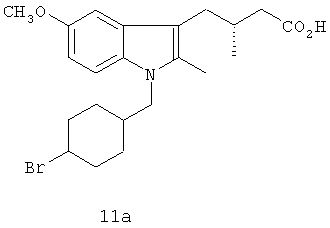
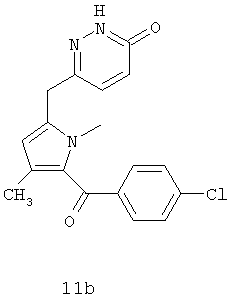
Еще другой класс ингибиторов СОХ-2 может быть отнесен к ингибиторам, которые представляют собой структурно модифицированные нестероидные противовоспалительные препараты (NSAIDs), и включает в качестве примера структуры членов 11а и 11в.
Кроме структурных классов, подклассов, приводимых примеров специфических ингибиторов СОХ-2, примеры соединений, которые избирательно ингибируют циклооксигеназу-2, описаны также в следующих патентных публикациях, которые все включены в изобретение путем цитирования: патенты US 5344991, 5380738, 5393790, 5409944, 5434178, 5436265, 5466823, 5474995, 5510368, 5536752, 5550142, 5552422, 5604253, 5604260, 5639780; и описания изобретений к международным патентам 94/13635, 94/15932, 94/20480, 94/26731, 94/27980, 95/00501, 95/15316, 96/03387, 96/03388, 96/06840; и заявки WO 94/20480, WO 96/21667, WO 96/31509, WO 96/36623, WO 97/14691, WO 97/16435.
Дополнительные ингибиторы СОХ-2, которые входят в объем данного изобретения, включают
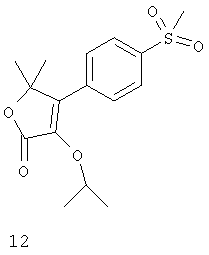
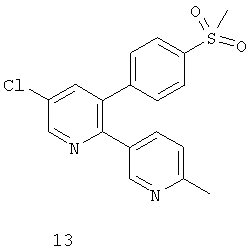
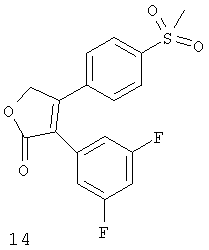
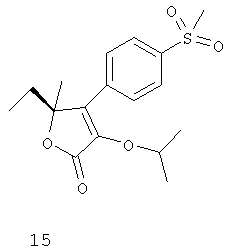
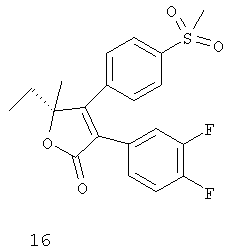
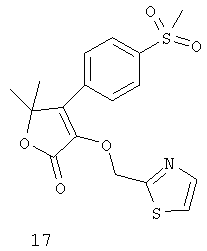
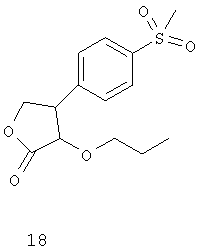
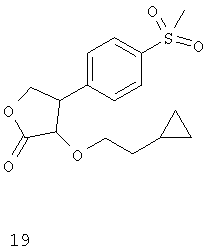
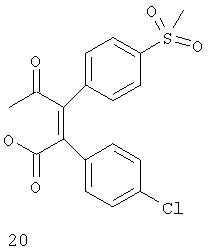
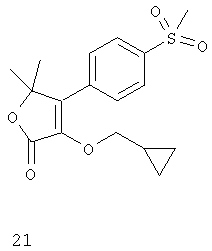
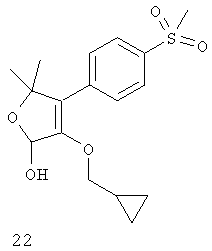
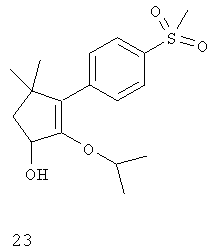
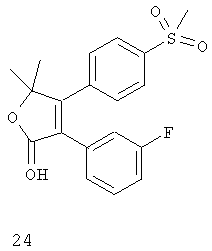
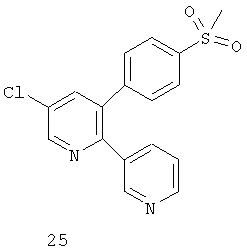
Некоторые из соединений, приведенных выше, могут быть также идентифицированы с помощью следующих химических названий:
3: 3-фенил-4-(4-(метилсульфонил)фенил)-2-(5H)-фуранон;
4: 3-(3,4-дифторфенил)-4-(4-(метилсульфонил)фенил)-2-(5H)-фуранон;
5: 5,5-диметил-4-(4-(метилсульфонил)фенил)-3-(3-фторфенил)-H-фуран-2-он;
12: 5,5-диметил-4-(4-(метилсульфонил)фенил)-3-(2-пропокси)-5H-фуран-2-он;
13: 5-хлор-3-(4-(метилсульфонил)фенил)-2-(2-метил-5-пиридинил)пиридин;
14: 2-(3,5-дифторфенил)-3-(4-(метилсульфонил)фенил)-2-циклопентен-1-он;
15: 5(S)-5-этил-5-метил-4-(4-метилсульфонил)фенил)-3-(2-пропокси)-5H-фуран-2-он;
16: 5-этил-5-метил-4-(4-(метилсульфонил)фенил)-3-(3,4-дифторфенил)-5H-фуран-2-он;
17: 3-((2-тиазолил)метокси)-4-(4-метилсульфонил)фенил)-5,5-диметил-5H-фуран-2-он;
18: 3-пропилокси-4-(4-метилсульфонил)фенил)-5,5-диметил-5H-фуран-2-он;
19: 3-(1-циклопропилэтокси)-5,5-диметил-4-(4-метилсульфонил)фенил)-5H-фуран-2-он;
20: 2-(4-хлорфенил)-3-(4-метилсульфонил)фенил)-4-оксо-2-пентеноат натрия;
21: 3-(циклопропилметокси)-5,5-диметил-4-(4-метилсульфонил)фенил)-5Н-фуран-2-он;
22: 3-(циклопропилметокси)-5,5-диметил-4-(4-метилсульфонил)фенил)-2,5-дигидрофуран-2-ол;
23: 3-изопропокси-5,5-диметил-4-(4-метилсульфонил)фенил)-2,5-дигидрофуран-2-ол;
24: 5,5-диметил-3-(3-фторфенил)-2-гидрокси-4-(4-метилсульфонил)фенил)-2,5-дигидрофуран;
25: 5-хлор-3-(4-метилсульфонил)фенил)-2-(3-пиридинил)пиридин.
Следующие публикации описывают и/или предусматривают способы получения соединений, как указано: соединения 12, 15, 17, 18, 19 и 21, WO 97/14691; соединения 22, 23 и 24, WO 97/16435; соединение 20, WO 96/36623; соединение 14, патент US 5536752; соединение 16, патент US 5474995. Смотри примеры в контексте для соединений 13 и 25. Включены также в контекст путем цитирования те соединения, которые описаны в WO 96/41645 как имеющие структурную формулу VI, приведенную ниже, и обозначения, и предпочтительные обозначения, и разновидности описаны там.
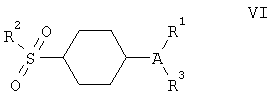
Особенно предпочтительные соединения формулы (VI) включают:
5-(4-фторфенил)-1-[4-(метилсульфонил)фенил]-3-(трифторметил)пиразол;
4-(4-фторфенил)-5-[4-(метилсульфонил)фенил]-1-фенил-3-(трифторметил)пиразол;
4-(5-(4-хлорфенил)-3-(4-метоксифенил)-1H-пиразол-1-ил)бензолсульфонамид;
4-(3,5-бис(4-метилфенил)-1H-пиразол-1-ил)бензолсульфонамид;
4-(5-(4-хлорфенил)-3-фенил-1H-пиразол-1-ил)бензолсульфонамид;
4-(3,5-бис(4-метоксифенил)-1H-пиразол-1-ил)бензолсульфонамид;
4-(5-(4-хлорфенил)-3-(4-метилфенил)-1H-пиразол-1-ил)бензолсульфонамид;
4-(5-(4-хлорфенил)-3-(4-нитрофенил)-1H-пиразол-1-ил)бензолсульфонамид;
4-(5-(4-хлорфенил)-3-(5-хлор-2-тиенил)-1H-пиразол-1-ил)бензолсульфонамид;
4-(4-хлор-3,5-дифенил-1H-пиразол-1-ил)бензолсульфонамид;
4-(5-(4-хлорфенил)-3-(трифторметил)-1H-пиразол-1-ил)бензолсульфонамид;
4-(5-фенил)-3-(трифторметил)-1H-пиразол-1-ил)бензолсульфонамид;
4-(5-(4-фторфенил)-3-(трифторметил)-1H-пиразол-1-ил)бензолсульфонамид;
4-(5-(4-метоксифенил)-3-(трифторметил)-1H-пиразол-1-ил)бензолсульфонамид;
4-(5-(4-хлорфенил)-3-(дифторметил)-1H-пиразол-1-ил)бензолсульфонамид;
4-(5-(4-метилфенил)-3-(трифторметил)-1H-пиразол-1-ил)бензолсульфонамид;
4-(4-хлор-5-(4-хлофенил)-3-(трифторметил)-1H-пиразол-1-ил)бензолсульфонамид;
4-(3-(дифторметил)-5-(4-метилфенил)-1H-пиразол-1-ил)бензолсульфонамид;
4-(3-(дифторметил)-5-фенил-1H-пиразол-1-ил)бензолсульфонамид;
4-(3-(дифторметил)-5-(4-метоксифенил)-1H-пиразол-1-ил)бензолсульфонамид;
4-(3-циано-5-(4-фторфенил)-1H-пиразол-1-ил)бензолсульфонамид;
4-(3-(дифторметил)-5-(3-фтор-4-метоксифенил)-1H-пиразол-1-ил)бензолсульфонамид;
4-(5-(3-фтор-4-метоксифенил)-3-(трифторметил)-1H-пиразол-1-ил)бензолсульфонамид;
4-(4-хлор-5-фенил-1H-пиразол-1-ил)бензолсульфонамид;
4-(5-(4-хлорфенил)-3-(гидроксифенил)-1H-пиразол-1-ил)бензолсульфонамид;
4-(5-(N,N-диметиламино)фенил)-3-(трифторметил)-1H-пиразол-1-ил)бензолсульфонамид;
5-(4-фторфенил)-6-(4-(метилсульфонил)фенил)спиро[2.4]гепт-5-ен;
4-(6-(4-фторфенил)спиро[2.4]гепт-5-ен-5ил)бензолсульфонамид;
6-(4-фторфенил)-7-(4-(метилсульфонил)фенил)спиро[3.4]окт-6-ен;
5-(3-хлор-4-метоксифенил)-6-(4-(метилсульфонил)фенил)спиро[2.4]гепт-5-ен;
4-(6-(3-хлор-4-метоксифенил)спиро[2.4]гепт-5-ен-5-ил)бензолсульфонамид;
5-(3,5-дихлор-4-метоксифенил)-6-(4-(метилсульфонил)фенил)спиро[2.4]гепт-5-ен;
5-(3-хлор-4-фторфенил)-6-(4-(метилсульфонил)фенил)спиро[2.4]гепт-5-ен;
4-(6-(3,4-дихлорфенил)спиро[2.4]гепт-5-ен-5-ил)бензолсульфонамид;
2-(3-хлор-4-фторфенил)-4-(4-фторфенил)-5-(4-метилсульфонилфенил)тиазол;
2-(2-хлорфенил)-4-(4-фторфенил)-5-(4-метилсульфонилфенил)тиазол;
5-(4-фторфенил)-4-(4-метилсульфонилфенил)-2-метилтиазол;
4-(4-фторфенил)-5-(4-метилсульфонилфенил)-2-трифторметилтиазол;
4-(4-фторфенил)-5-(4-метилсульфонилфенил)-2-(2-тиенил)тиазол;
4-(4-фторфенил)-5-(4-метилсульфонилфенил)-2-бензолсульфонамид;
4-(4-фторфенил)-5-(4-метилсульфонилфенил)-2-(1-пропиламино)тиазол;
2-((3,5-дихлорфенокси)метил)-4-(4-фторфенил)-5-(4-(метилсульфонил)фенил)тиазол;
5-(4-фторфенил)-4-(4-метилсульфонилфенил)-2-трифторметилтиазол;
1-метилсульфонил-4-(1,1-диметил-4-(4-фторфенил)циклопента-2,4-диен-3-ил)бензол;
4-(4-(4-фторфенил-1,1-диметилциклопента-2,4-диен-3-ил)бензолсульфонамид;
5-(4-фторфенил)-6-(4-(метилсульфонил)фенил)спиро[2.4]гепта-4,6-диен;
4-(6-(4-фторфенил)спиро[2.4]гепта-4,6-диен-5-ил)бензолсульфонамид;
6-(4-фторфенил)-2-метокси-5-(4-(метилсульфонил)фенил)пиридин-3-карбонитрил;
2-бром-6-(4-фторфенил)-5-(4-(метилсульфонил)фенил)пиридин-3-карбонитрил;
6-(4-фторфенил)-5-(4-(метилсульфонил)фенил)-2-фенилпиридин-3-карбонитрил;
4-(2-(4-метилпиридин-2-ил)-4-(трифторметил)-1H-имидазол-1-ил)бензолсульфонамид;
4-(2-(5-метилпиридин-3-ил)-4-(трифторметил)-1H-имидазол-1-ил)бензолсульфонамид;
4-(2-(2-метилпиридин-3-ил)-4-(трифторметил)-1H-имидазол-1-ил)бензолсульфонамид;
3-(1-(4-(метилсульфонил)фенил)-4-(трифторметил)-1H-имидазол-2-ил)бензолсульфонамид;
2-(1-(4-(метилсульфонил)фенил)-4-(трифторметил)-1H-имидазол-2-ил)пиридин;
2-метил-4-(1-(4-(метилсульфонил)фенил)-4-(трифторметил)-1H-имидазол-2-ил)пиридин;
2-метил-6-(1-(4-(метилсульфонил)фенил)-4-(трифторметил)-1H-имидазол-2-ил)пиридин;
4-(2-(6-метилпиридин-3-ил)-4-(трифторметил)-1H-имидазол-1-ил)бензолсульфонамид;
2-(3,4-дифторфенил)-1-(4-(метилсульфонил)фенил)-4-(трифторметил)-1Н-имидазол;
4-(2-(4-метилфенил)-4-(трифторметил)-1H-имидазол-1-ил)бензолсульфонамид;
2-(4-хлорфенил)-1-(4-метилсульфонил)фенил)-4-метил-1H-имидазол;
2-(4-хлорфенил)-1-(4-(метилсульфонил)фенил)-4-фенил-1H-имидазол;
2-(4-хлорфенил)-4-(4-фторфенил)-1-(4-(метилсульфонил)фенил)-1H-имидазол;
2-(3-фтор-4-метоксифенил)-1-(4-(метилсульфонил)фенил)-4-(трифторметил)-1H-имидазол;
1-(4-метилсульфонил)фенил)-2-фенил-4-трифторметил-1H-имидазол;
2-(4-метилфенил)-1-(4-(метилсульфонил)фенил)-4-трифторметил-1H-имидазол;
4-(2-(3-хлор-4-метилфенил)-4-(трифторметил-1H-имидазол-1-ил)бензолсульфонамид;
2-(3-фтор-5-метилфенил)-1-(4-метилсульфонил)фенил)-4-(трифторметил)-1H-имидазол;
4-(2-(3-фтор-5-метилфенил)-4-(трифторметил)-1H-имидазол-1-ил)бензолсульфонамид;
2-(3-метилфенил)-1-(4-(метилсульфонил)фенил)-4-(трифторметил)-1H-имидазол;
4-(2-(3-метилфенил)-4-(трифторметил)-1H-имидазол-1-ил)бензолсульфонамид;
1-(4-(метилсульфонил)фенил)-2-(3-хлорфенил)-4-(трифторметил)-1Н-имидазол;
4-(2-(3-хлорфенил)-4-(трифторметил)-1H-имидазол-1-ил)бензолсульфонамид;
4-(2-фенил-4-(трифторметил)-1H-имидазол-1-ил)бензолсульфонамид;
4-(2-(4-метокси-3-хлорфенил)-4-(трифторметил)-1H-имидазол-1-ил)бензолсульфонамид;
1-аллил-4-(4-фторфенил)-3-(4-(метилсульфонил)фенил)-5-(трифторметил)-lH-пиразол;
4-(1-этил-4-(4-фторфенил)-5-(трифторметил)-1H-пиразол-3-ил)бензолсульфонамид;
N-фенил-(4-(4-фторфенил)-3-(4-(метилсульфонил)фенил)-5-(трифторметил)-1H-пиразол-1-ил)ацетамид;
этиловый эфир (4-(4-фторфенил)-3-(4-(метилсульфонил)фенил)-5-(трифторметил)-1H-пиразол-1-ил)уксусной кислоты;
4-(4-фторфенил)-3-(4-метилсульфонил)фенил)-1-(2-фенилэтил)-1H-пиразол;
4-(4-фторфенил)-3-(4-(метилсульфонил)фенил)-1-(2-фенилэтил)-5-(трифторметил)пиразол;
1-этил-4-(4-фторфенил)-3-(4-метилсульфонил)фенил)-5-(трифторметил)-1H-пиразол;
5-(4-фторфенил)-4-(4-метилсульфонил)фенил)-2-(трифторметил)-1H-имидазол;
4-(4-метилсульфонил)фенил)-5-(2-тирфенил)-2-(трифторметил)-1H-имидазол;
5-(4-фторфенил)-2-метокси-4-(метилсульфонил)фенил)-6-(трифторметил)пиридин;
2-этокси-5-(4-фторфенил)-4-(4-(метилсульфонил)фенил)-6-(трифторметил)пиридин;
5-(4-фторфенил)-4-(4-(метилсульфонил)фенил)-2-(2-пропинилокси)-6-(трифторметил)пиридин;
2-бром-5-(4-фторфенил)-4-(4-метилсульфонил)фенил)-6-(трифторметил)пиридин;
4-(2-(3-хлор-4-метоксифенил)-4,5-дифторфенил)бензолсульфонамид;
1-(4-фторфенил)-2-(4-метилсульфонил)фенил)бензол;
5-дифторметил-4-(4-метилсульфонил)фенил)-3-фенилизоксазол;
4-(3-этил-5-фенилизоксазол-4-ил)бензолсульфонамид;
4-(5-дифторметил-3-фенилизоксазол-4-ил)бензолсульфонамид;
4-(5-гидроксиметил-3-фенилизоксазол-4-ил)бензолсульфонамид;
4-(5-метил-3-фенилизоксазол-4-ил)бензолсульфонамид;
1-(2-(4-фторфенил)циклопентен-1-ил)-4-(метилсульфонил)бензол;
1-(2-(4-фтор-2-метилфенил)циклопентен-1-ил)-4-(метилсульфонил)бензол;
1-(2-(4-хлорфенил)циклопентен-1-ил)-4-(метилсульфонил)бензол;
1-(2-(2,4-дихлорфенил)циклопентен-1-ил)-4-(метилсульфонил)бензол;
1-(2-(4-трифторметилфенил)циклопентен-1-ил)-4-(метилсульфонил)бензол;
1-(2-(4-метилтиофенил)циклопентен-1-ил)-4-(метилсульфонил)бензол;
1-(2-(4-фторфенил)-4,4-диметилциклопентен-1-ил)-4-(метилсульфонил)бензол;
4-(2-(4-фторфенил)-4,4-диметилциклопентен-1-ил)бензолсульфонамид;
1-(2-(4-хлорфенил)-4,4-диметилциклопентен-1-ил)-4-(метилсульфонил)бензол;
4-(2-(4-хлорфенил)-4,4-диметилциклопентен-1-ил)бензолсульфонамид;
4-(2-(4-фторфенил)циклопентен-1-ил)бензолсульфонамид;
4-(2-(4-хлорфенил)циклопентен-1-ил)бензолсульфонамид;
1-(2-(4-метоксифенил)циклопентен-1-ил)-4-(метилсульфонил)бензол;
1-(2-(2,3-дифторфенил)циклопентен-1-ил)-4-(метилсульфонил)бензол;
4-(2-(3-фтор-4-метоксифенил)циклопентен-1-ил)бензолсульфонамид;
1-(2-(3-хлор-4-метоксифенил)циклопентен-1-ил)-4-(метилсульфонил)бензол;
4-(2-(3-хлор-4-фторфенил)циклопентен-1-ил-бензолсульфонамид;
4-(2-(2-метилпиридин-5-ил)циклопентен-1-ил)бензолсульфонамид;
этиловый эфир 2-(4-(4-фторфенил)-5-(4-метилсульфонил)фенил)оксазол-2-ил)-2-бензилуксусной кислоты;
2-(4-(4-фторфенил)-5-(4-(метилсульфонил)фенил)оксазол-2-ил)уксусная кислота;
2-(трет-бутил)-4-(4-фторфенил)-5-(4-метилсульфонил)фенил)оксазол;
4-(4-фторфенил)-5-(4-(метилсульфонил)фенил)-2-фенилоксазол;
4-(4-фторфенил)-2-метил-5-(4-метилсульфонил)фенил)оксазол; и
4-(5-(3-фтор-4-метоксифенил)-2-трифторметил-4-оксазолил)бензолсульфонамид;
или их фармацевтически приемлемые соли.
N-Бифосфонаты предпочтительно применяются в форме фармацевтических композиций, которые содержат терапевтически эффективное количество активного ингредиента необязательно вместе или в смеси с неорганическими или органическими, твердыми или жидкими фармацевтически приемлемыми носителями, которые пригодны для введения.
Фармацевтические композиции N-бифосфонатов могут быть, например, композициями для энтерального введения, такого как пероральное, ректальное, вдыхание аэрозоля или назальное, композициями для парентерального введения, такого как внутривенное, или подкожное, или композициями для чрескожного введения (например, пассивного или ионофоретического).
Считается, что особенно важным является внутривенное и пероральное введение, в первую очередь и основное - внутривенное. Предпочтительно N-бифосфонатный активный ингредиент находится в парентеральной форме, наиболее предпочтительно во внутривенной форме.
Особый способ введения и доза могут быть выбраны практикующим врачом, принимающим во внимание отличительные признаки пациента, главным образом возраст, массу, образ жизни, уровень активности и соответствующее болезненное состояние. Однако наиболее предпочтительно N-бифосфонаты вводят внутривенно.
Доза N-бифосфоната для применения по изобретению зависит от разнообразных факторов, таких как эффективность и продолжительность действия активного ингредиента, способа введения, вида теплокровного и/или пола, возраста, массы и индивидуального состояния теплокровного млекопитающего.
Таксол представляет собой сложный 6,12b-бис(ацетилокси)-12-(бензоилокси)-2α,3,4,4а,5,6,9,10,11,12,12а,12b-додекагидро-4,11-дигидрокси-4а,8,13,13-тетраметил-5-оксо-7,11-метано-1H-циклодека[3,4]бенз[1,2-b]оксет-9-иловый эфир [2aR-[2aα, 4β, 4αβ, 6β, 9α(αR*, βS*), 11α,12α, 12аα, 12bα]]-β-(бензоиламино)-α-гидроксибензолпропановой кислоты, альтернативно известный как паклитаксел, который является противолейкозным и противоопухолевым агентом, впервые выделенным в виде 1-формы из коры тихоокеанского тиса, Taxus brevifolia, Taxaceae. Соответствующие производные таксола для применения по настоящему изобретению включают таксотер (т.е. сложный 12b-(ацетилокси)-12-(бензоилокси)-2α,3,4,4а,5,6,9,10,11,12,12а,12b-додекагидро-4,6,11-тригидрокси-4а,8,13,13-тетраметил-5-оксо-7,11 -метано-1Н-циклодека[3,4]бенз[1,2-b]оксет-9-иловый эфир [2аR-[2аα, 4β, 4αβ, 6β, 9α(αR*, βS*),11α,12α, 12aα, 12bα]]-β-[[(1,1-диметилэтокси)карбонил]амино]-α-гидроксибензолпропановой кислоты, альтернативно известный как доцетаксел), таксаны, таксины (например, таксин I, таксин II, таксин А или таксин В) или какие-либо другие соответствующие производные таксола. Таксол и соответствующие его производные могут применяться в комбинации с бифосфонатом и ингибитором СОХ-2 по настоящему изобретению. Предпочтительным производным таксола по настоящему изобретению является таксотер. Фармацевтические композиции таксола или производного таксола могут быть, например, композициями для энтерального введения, такого как пероральное, ректальное вдыхание аэрозоля или назальное, композициями для парентерального введения, такого как внутривенное или подкожное, или композициями для чрескожного введения (например, пассивного или ионофоретического).
Агенты по изобретению: (а) ингибитор СОХ-2 и (б) бифосфонат. Ингибитор СОХ-2, бифосфонат и таксол или его производное предпочтительно применяются в форме фармацевтических препаратов, которые содержат необходимое терапевтически эффективное количество каждого активного ингредиента (или отдельно, или в комбинации), необязательно вместе или в смеси с неорганическими или органическими, твердыми или жидкими фармацевтически приемлемыми носителями, которые пригодны для введения. Активные ингредиенты в виде ингибитора СОХ-2 и бифосфоната могут присутствовать в одной и той же фармацевтической композиции, хотя предпочтительно они присутствуют в отдельных фармацевтических композициях. Таким образом, активные ингредиенты могут вводиться в одно и то же время (например, одновременно) или в различное время (например, последовательно) или в течение различных периодов времени, которые могут отделяться один от другого или перекрываться.
Фармацевтические композиции ингибитора СОХ-2 могут быть, например, композициями для энтерального введения, такого как пероральное, ректальное, вдыхание аэрозоля или назальное, композициями для парентерального введения, такого как внутривенное или подкожное, или композициями для чрескожного введения (например, пассивного или ионофоретического).
Предпочтительно фармацевтические композиции ингибитора СОХ-2 адаптируются к пероральному или парентеральному (особенно пероральному) введению. Считается, что особенно важным является внутривенное и пероральное введение, в первую очередь и основное - пероральное. Предпочтительно активный ингредиент в виде ингибитора СОХ-2 находится в пероральной форме.
Особый способ введения и доза могут быть выбраны практикующим врачом, принимающим во внимание отличительные признаки пациента, главным образом возраст, массу, образ жизни, уровень активности и т.д.
Доза агентов по изобретению может зависеть от разнообразных факторов, таких как эффективность и продолжительность действия активного ингредиента, способа введения, вида теплокровного и/или пола, возраста, массы и индивидуального состояния теплокровного млекопитающего.
Более конкретно, фармацевтические композиции включают эффективное, ингибирующее циклооксигеназу-2 количество ингибитора СОХ-2 или соединения формулы I, которое фактически лишено ингибирующей циклооксигеназу-1 активности и связанных с этим побочных эффектов.
Фармакологически активные соединения по изобретению применимы в производстве фармацевтических композиций, включающих их эффективное количество в объединении или смеси с наполнителями или носителями, пригодными или для энтерального или для парентерального применения. Предпочтительными являются таблетки и желатиновые капсулы, включающие активный ингредиент вместе с (а) разбавителями, например, лактозой, декстрозой, сахарозой, маннитом, сорбитом, целлюлозой и/или глицином; (б) смазывающими веществами, например, диоксидом кремния, тальком, стеариновой кислотой, ее магниевой или кальциевой солью и/или полиэтиленгликолем; для таблеток также с (в) связывающими веществами, силикатом магния-алюминия, крахмальной пастой, желатином, трагакантом, метилцеллюлозой, карбоксиметилцеллюлозой и/или поливинилпирролидоном; при необходимости с (г) дезинтегрирующими веществами, например, крахмалами, агаром, альгиновой кислотой или ее натриевой солью или шипучими смесями; и/или с (д) абсорбентами, ароматизаторами и подсластителями. Композиции для инъекций являются предпочтительно водными изотоническими растворами или суспензиями, а суппозитории удобно получать из жирных эмульсий или суспензий. Упомянутые композиции могут стерилизоваться и/или содержать адъюванты, такие как консервирующие, стабилизирующие, смачивающие или эмульгирующие агенты, способствующие растворению вещества, соли для регулирования осмотического давления и/или буферы. Кроме того, они могут также содержать другие терапевтически ценные вещества. Соответственно, упомянутые композиции получают согласно способам стандартного смешивания, грануляции или нанесения покрытия и содержат примерно 0,1-75%, предпочтительно примерно 1-50% активного ингредиента.
Таблетки могут быть покрыты или пленкой, или растворимой в кишечнике оболочкой в соответствии со способами, известными в данной области.
Соответствующие составы для чрескожного применения включают эффективное количество соединения по изобретению с носителем. Преимущественные носители включают абсорбируемые фармакологически приемлемые растворители, чтобы способствовать прохождению через кожу пациента. Например, устройства для чрескожной доставки имеют форму повязки, включающей каркасный элемент, резервуар, содержащий соединение, необязательно с носителями, необязательно контролирующий скорость барьер для доставки соединения в кожу пациента при регулируемой или заданной скорости в течение продолжительного периода времени и средства для прикрепления устройства к коже.
Соответствующие составы для местного применения, например для кожи и глаз, включают водные растворы, суспензии, мази, кремы, гели или распыляемые составы, например, для доставки аэрозоля или тому подобного. Такие системы местной доставки будут особенно удобны для нанесения на кожу, к примеру для лечения рака кожи, например для профилактического применения в кремах, лосьонах, аэрозолях и тому подобном.
Доза вводимого ингибитора СОХ-2 зависит от вида теплокровного животного (млекопитающего), массы тела, возраста, индивидуального состояния и типа введения. Стандартная доза для перорального введения млекопитающему с массой примерно 50-70 кг содержит примерно 5-1000 мг, например, 100-800 мг, предпочтительно 200-400 мг активного ингредиента.
Композиции ингибитора СОХ-2 в однократной лекарственной форме содержат предпочтительно от примерно 1% до примерно 90%, а композиции не в однократной лекарственной форме содержат предпочтительно от примерно 0,1% до примерно 20% активного ингредиента. Однократные лекарственные формы, такие как капсулы, таблетки или драже, содержат, например, от примерно 1 мг до примерно 1000 мг активного ингредиента.
Фармацевтическими препаратами на основе ингибитора СОХ-2 для энтерального и парентерального введения являются, например, препараты в лекарственных формах, таких как драже, таблетки или капсулы и также ампулы. Они получаются известным по сути способом, например посредством стандартных способов смешивания, грануляции, приготовления лекарств, растворения или лиофилизации. Например, фармацевтические препараты для перорального введения могут быть получены объединением активного ингредиента и твердых носителей, где уместно - гранулированием образующейся смеси и обработкой смеси или гранулята, если желательно или необходимо, после прибавления соответствующих добавок в таблетки или сердцевины драже.
Другими перорально вводимыми фармацевтическими препаратами являются капсулы сухого заполнения, сделанные из желатина, и также мягкие герметизированные капсулы, сделанные из желатина и пластифицирующей добавки, такой как глицерин или сорбит. Капсулы сухого заполнения могут содержать активный ингредиент в форме гранулята, например, в смеси с наполнителями, такими как лактоза, связующими веществами, такими как крахмалы, и/или скользящими веществами, такими как тальк или стеарат магния, и, где уместно, стабилизаторами. В мягких капсулах активный ингредиент предпочтительно растворяют или суспендируют в соответствующих жидкостях, таких как жировые масла, парафиновое масло или жидкие полиэтиленгликоли, возможно также добавление стабилизаторов.
Парентеральными композициями являются главным образом инъецируемые жидкости, которые эффективны разнообразными способами, такими как введение внутривенно, внутримышечно, внутрибрюшинно, интраназально, внутрикожно или подкожно. Такие жидкости представляют собой предпочтительно изотонические водные растворы или суспензии, которые могут быть получены перед применением, например, из лиофилизированных препаратов, которые содержат активный ингредиент, один или вместе с фармацевтически приемлемым носителем. Фармацевтические препараты могут стерилизоваться и/или содержать дополнительные вещества, например консерванты, стабилизаторы, смачивающие агенты и/или эмульгаторы, способствующие растворению вещества, соли для регулирования осмотического давления и/или буферы.
Соответствующие композиции для чрескожного применения включают эффективное количество активного ингредиента с носителем. Преимущественные носители включают абсорбируемые фармакологически приемлемые растворители, чтобы способствовать прохождению через кожу пациента. Характерно, что устройства для чрескожной доставки имеют форму повязки, включающей каркасный элемент, резервуар, содержащий соединение, необязательно с носителями, необязательно контролирующий скорость барьер для доставки соединения в кожу пациента при регулируемой или заданной скорости в течение продолжительного периода времени и средства для прикрепления устройства к коже.
Подразумевается, что следующие примеры иллюстрируют изобретение и не должны рассматриваться как его ограничения.
Примеры
А. Примеры композиций
Пример 1
Прочность таблетки с дозой между 5 и 125 мг может быть обеспечена изменением общей массы и соотношения первых трех ингредиентов. Обычно для микрокристаллической целлюлозы и моногидрата лактозы предпочтительно поддерживать соотношение 1:1.
Пример 2
Пример 3
Пример 4
Пример 5
Прочность таблетки с дозой между 5 мг и 125 мг может быть обеспечена изменением общей массы и соотношения первых трех ингредиентов. Обычно для микрокристаллической целлюлозы и моногидрата лактозы предпочтительно поддерживать соотношение 1:1.
Пример 6
Пример 7
Пример 8
Пример 9
Прочность капсулы с дозой между 1 и 50 мг может быть обеспечена изменением общей массы заполнения и соотношения первых трех ингредиентов. Обычно для микрокристаллической целлюлозы и моногидрата лактозы предпочтительно поддерживать соотношение 1:1.
Пример 10
Пример 11
Прочность суспензии с дозой между 1 и 50 мг/5 мл может быть обеспечена изменением соотношения первых двух ингредиентов.
Пример 12
Пример 13
Получение комбинированной таблетки
Таблетки, содержащие 25,0, 50,0 и 100,0 мг таксола, соответственно, и 25 мг ингибитора СОХ-2, получали, как показано ниже.
Таблетки для доз, содержащих 25-200 мг таксола и 25 мг ингибитора COX-2.
Оба активных соединения, целлюлозу и часть кукурузного крахмала смешивали и гранулировали в пасту, содержащую 10% кукурузного крахмала. Полученный гранулят просеивали, сушили и смешивали с оставшимся кукурузным крахмалом и стеаратом магния. Затем полученный гранулят прессовали в таблетки, содержащие соответственно 25,0, 50,0 и 100,0 мг таксола на таблетку и 25 мг ингибитора СОХ-2 на таблетку.
Пример 14
*** Удаляется при обработке.
**** Включает избыток 50% на потерю при нанесении покрытия.
Выше таблица 1 представляет композицию серии из примерно 250000 таблеток незамедлительного высвобождения с нанесенным покрытием для 5-метил-2-(2'-хлор-6'-фторанилино)фенилуксусной кислоты. Для получения таблеток диоксид титана диспергировали в воде, затем добавляли повидон и перемешивали в течение 20 мин, чтобы образовать суспензию повидон/диоксид титана. Субстанцию препарата, лактозу, микрокристаллическую целлюлозу и кроскармеллозу смешивали в миксере с большой срезывающей силой (например, Collette Gral) в течение 5 мин, чтобы образовать лекарственную смесь. Лекарственную смесь гранулировали с суспензией повидон/диоксид титана в миксере с большой срезывающей силой. Суспензию качали насосом со скоростью 3 кг/мин в лекарственную смесь. Полученную смесь перемешивали дополнительные 90 сек после добавления всей суспензии. Влажный гранулят сушили в аппарате с кипящим слоем при температуре воздуха на входе 50°С. Показатель остаточной воды составил 3,5% (при допустимом интервале 2,5-4,5%). Высушенный гранулят пропускали через сито, используя измельчитель (вибратор) и сито 30 меш. Предыдущие этапы повторяли, чтобы получить второй гранулят.
Диоксид титана экстрагранулярной фазы пропускали через ручное сито 60 меш. Сухие грануляты смешивали с микрокристаллической целлюлозой экстрагранулярной фазы, кроскармеллозой в натриевой форме и диоксидом титана в миксере с двойным кожухом в течение 300 оборотов, чтобы получить предпоследнюю смесь. Стеарат магния пропускали через ручное сито 60 меш и смешивали с предпоследней смесью в миксере с двойным кожухом в течение 50 оборотов, чтобы образовать смесь для таблетирования. Смесь для таблетирования прессовали в таблетки, используя таблеточный пресс и овальные штампы.
Порошки для покрытия (опадри) смешивали с очищенной водой для получения 15% об./об. суспензии для нанесения покрытия. Таблетки покрывали пленкой с помощью покрывающей суспензии в аппарате для нанесения покрытий, используя температуру воздуха на входе 60-75°С.
Таблица 2 представляет состав таблетки с нанесенным покрытием, содержащей 200 мг 5-метил-2-(2'-хлор-6'-фторанилино)фенилуксусной кислоты.
в-во
Кроме того, композиции таблетки могут содержать 5-метил-2-(2'-хлор-6'-фторанилино)бензиловый спирт и/или 5-метил-2-(2'-хлор-6'-фторанилино)бензойную кислоту в количестве между примерно 0,01 и 2 мас.%, более конкретно между примерно 0,1 и 1 мас.%.
Пример 15
Капсулы, содержащие гранулы активного ингредиента с покрытием, например, пентагидрата динатриевой соли памидроновой кислоты в качестве активного ингредиента
Смесь динатриевой соли памидроновой кислоты и авицеля® РН 105 увлажняли водой и разминали, экструдировали и формировали в сферы. Затем высушенные гранулы последовательно покрывали в кипящем слое внутренним покрытием, состоящим из целлюлозы НР-М 603, полиэтиленгликоля (PEG) 8000 и талька, и устойчивым к желудочному соку покрытием, состоящим из эудрагита® L 30 D, триэтилцитрата и пеногасителя® AF. Гранулы с нанесенным покрытием измельчали в порошок с тальком и заполняли капсулы (размер капсулы 0) посредством имеющейся в продаже машины для заполнения капсул, например, Höfliger и Karg.
Пример 16
Монолитная адгезивная система чрескожной доставки, содержащая в качестве активного ингредиента, например, 1-гидрокси-2-(имидазол-1-ил)этан-1,1-дифосфоновую кислоту.
Получение
Упомянутые выше компоненты растворяли вместе в 150 г специальной нефтяной фракции с температурой кипения 100-125°С путем раскатывания на роликовом зубчатом настиле. Раствор наносили на полиэфирную пленку (Hostaphan, Kalle) посредством растекающего устройства, используя ракельный нож 300 мм, дающий покрытие примерно 75 г/м. После высушивания (15 мин при 60°С) наносили обработанную силиконом полиэфирную пленку (толщиной 75 мм, Laufenberg) в качестве отслаивающейся пленки. Конечные системы 2 отштамповывали по размерам в требуемой форме от 5 до 30 см2, используя перфоратор. Укомплектованные системы герметизировали по отдельности в пакеты-саше из алюминизированной бумаги.
Пример 17
Флакон, содержащий 1,0 мг лиофильно высушенной 1-гидрокси-2-(имидазол-1-ил)этан-1,1-дифосфоновой кислоты (ее смешанных натриевых солей). После разбавления 1 мл воды получали раствор (концентрация 1 мг/мл) для внутривенной инфузии.
Композиция
В 1 мл воды активный ингредиент титровали дигидратом тринатриевой соли лимонной кислоты до рН 6,0. Затем прибавляли маннит, раствор лиофилизовали, и лиофилизат насыпали во флакон.
Пример 18
Ампула, содержащая активный ингредиент, например пентагидрат динатриевой соли памидроновой кислоты, растворенный в воде. Раствор (концентрация 3 мг/мл) для внутривенной инфузии после разбавления.
Композиция
Пример 19
Ингибирование роста клеточных линий рака молочной железы человека комбинацией золедроновой кислоты и ингибитора СОХ-2.
Цель
Циклооксигеназа (СОХ) это простагландин-Н-синтаза, которая является основным ферментом, опосредующим образование простаноидов (коллективный термин для простациклинов, простагландинов и тромбоксанов). СОХ-2 подвергается «верхней» регуляции в большом проценте распространенных человеческих злокачественных опухолей и ассоциируется с инвазивным и метастатическим поведением опухоли. Ингибиторы СОХ-2 подавляют рост рака ободочной кишки in vitro, индуцируя апоптоз. Золедроновая кислота, представитель нового поколения бифосфонатов, примененная в лечении поражений костей, вызванных раком молочной железы, значительно снижает число клеток и индуцирует апоптоз в клетках рака молочной железы человека. Цель данного исследования состояла в том, чтобы оценить влияние комбинации ингибитора СОХ-2 и золедроновой кислоты на рост клеток рака молочной железы.
Методики
Влияние комбинации ингибитора СОХ-2 и золедроновой кислоты по сравнению с любым из двух агентов в отдельности исследовали на трансфицированной HER-2/neu линии клеток рака молочной железы человека (MCF/18) и трансфицированной контрольным вектором линии (MCF/neo). Число клеток определяли после трехдневной инкубации, используя анализ с красителем 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолийбромид (МТТ).
Результаты
Обработка трансфицированной HER-2/neu линии клеток MCF/18 и контрольной линии клеток MCF/neo с SC236 - ингибитором СОХ-2- (1-10 мкМ) привела к дозозависимому подавлению роста клеток (15-41% ингибирования и 18-53% ингибирования соответственно). Обработка с золедроновой кислотой (1-10 мкМ) также привела к дозозависимому подавления роста. Однако сверхэкспрессирующие HER-2/neu клетки MCF/18 были менее чувствительны к золедроновой кислоте (9-53% ингибирования), чем клетки MCF/neo (8-67% ингибирования). Комбинация золедроновой кислоты (5 мкМ) и ингибитора SC236 (5 мкМ), по-видимому, оказывала усиленное (менее чем аддитивное) ингибиторное воздействие на клетки MCF/neo и аддитивное воздействие на клетки MCF/18.
Заключение
Обработка с одним ингибитором COX-2 (SC236) или с одной золедроновой кислотой дала дозозависимое подавление роста как трансфицированной HER-2/neu линии клеток рака молочной железы человека (MCF/18), так и трансфицированной вектором контрольной линии (MCF/neo). Однако линия клеток MCF/18 была менее чувствительна к золедроновой кислоте. Комбинация золедроновой кислоты с SC236 (ингибитором СОХ-2) оказала усиленное воздействие на контрольные клетки рака молочной железы MCF/neo и аддитивное воздействие на трансфицированные HER-2/neu клетки MCF/18 по сравнению с каждым из двух агентов в отдельности.
Пример 20
Подавление роста линий клеток рака молочной железы человека комбинацией ингибитора СОХ-2, золедроновой кислоты и доцетаксела.
Доцетаксел представляет собой противоопухолевый агент, принадлежащий к семейству таксанов. Доцетаксел индуцирует фосфорилирование белка bcl-2 и последующий апоптоз и эффективен в лечении пациентов, страдающих раком молочной железы. Цель данного исследования состояла в том, чтобы оценить воздействие комбинации ингибитора СОХ-2 с золедроновой кислотой и/или таксотером на рост клеток рака молочной железы.
Методики
Воздействие комбинации ингибитора СОХ-2 (SC 236) с золедроновой кислотой и/или таксотером исследовали на трансфицированной HER-2/neu линии клеток рака молочной железы человека (MCF/18) и трансфицированной контрольным вектором линии (MCF/neo). Число клеток определяли после трехдневной инкубации, используя анализ с красителем 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолийбромид (МТТ).
Результаты
Обработка трансфицированной HER-2/neu линии клеток MCF/18 и контрольной трансфицированной линии клеток каждым из агентов приводила к дозозависимому ингибированию роста. Однако трансфицированные HER-2/neu клетки MCF/18 были менее чувствительны к золедроновой кислоте, чем контрольные клетки MCF/neo, 9%-53% ингибирования и 18%-67% ингибирования соответственно. Обработка комбинацией SC236 (5 мкМ) и таксотера (2 нМ) дала усиленное подавление роста в линиях MCF/18 и MCF/neo.
Обработка золедроновой кислотой (5 мкМ) и таксотером (2 нМ) также привела к усиленному подавлению роста в обеих линиях клеток. Комбинация SC236 (5 мкМ) и золедроновой кислоты (5 мкМ) оказала усиленное ингибиторное действие на клетки MCF/neo и аддитивное воздействие на клетки MCF/18. Тройная комбинация трех агентов приводила к незначительному усилению подавления роста сверх того, которое проявлялось с любой из двойных комбинаций.
Заключение
Все возможные двойные комбинации ингибитора СОХ-2, золедроновой "кислоты и/или таксотера давали усиленное подавление роста по сравнению с каждым агентом в отдельности на линиях клеток рака молочной железы MCF/18, трансфицированных HER-2/neu, и MCF/neo, трансфицированных контрольным вектором. Комбинация ингибитора СОХ-2 (SC236) с золедроновой кислотой имела аддитивное действие на линии трансфицированных HER-2/neu клеток. Тройная комбинация приводила к небольшому усилению подавления роста сверх того, которое проявлялось с любой из двойных комбинаций.
Пример 21
Подавление роста линии клеток рака предстательной железы человека комбинацией ингибитора СОХ-2 и золедроновой кислоты
Цель
Цель данного исследования состояла в том, чтобы оценить воздействие комбинации ингибитора СОХ-2 с золедроновой кислотой на рост клеток рака предстательной железы.
Методики
Воздействие комбинации ингибитора СОХ-2 (SC236) и золедроновой кислоты по сравнению с каждым из двух агентов в отдельности исследовали на линии клеток DU-145 карциномы предстательной железы человека. Число клеток определяли после трехдневной обработки, используя анализ с красителем 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолийбромид (МТТ).
Результаты
Обработка с ингибитором СОХ-2 (SC236) (1-25 мкМ) приводила к дозозависимому подавлению роста клеток (0-77%). Обработка с золедроновой кислотой (1-10 мкМ) также давала дозозависимое подавление роста (8-70%). Комбинация 3 мкМ золедроновой кислоты (23% подавления) и 5 мкМ SC236 (40% подавления) приводила к аддитивному ингибиторному воздействию (60% подавления) на линии клеток DU-145 карциномы предстательной железы человека.
Заключение
Бифосфонат золедроновая кислота и ингибитор COX-2 (SC236) оба давали дозозависимое подавление роста клеток в качестве единственных агентов. Обработка линии клеток DU-145 карциномы предстательной железы человека комбинацией этих двух агентов приводила к аддитивному ингибиторному воздействию по сравнению с тем, которое проявлялось с каждым из двух агентов в отдельности.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРИМЕНЕНИЯ ИНГИБИТОРОВ ЦИКЛООКСИГЕНАЗЫ-2 ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ НЕОПЛАЗИИ | 1997 |
|
RU2239429C2 |
| СПОСОБ ПРИМЕНЕНИЯ ИНГИБИТОРОВ ЦИКЛООКСИГЕНАЗЫ-2 В КАЧЕСТВЕ АНТИАНГИОГЕННЫХ СРЕДСТВ | 1997 |
|
RU2268716C2 |
| НОВЫЕ ГЕТЕРОЦИКЛЫ | 2009 |
|
RU2572616C2 |
| СПОСОБ ЛЕЧЕНИЯ ВОСПАЛЕНИЯ ИЛИ СВЯЗАННОГО С ВОСПАЛЕНИЕМ ЗАБОЛЕВАНИЯ У СОБАК | 1996 |
|
RU2253456C2 |
| СОЕДИНЕНИЯ И КОМПОЗИЦИИ В КАЧЕСТВЕ ИНГИБИТОРОВ ITPKb | 2007 |
|
RU2425826C2 |
| МОРФОЛИНИЛПИРИДОНЫ | 2018 |
|
RU2803158C2 |
| ТРИАЗОЛОПИРИДИНОВЫЕ СОЕДИНЕНИЯ-ИНГИБИТОРЫ JAK И СПОСОБЫ | 2009 |
|
RU2561104C2 |
| ПИРАЗОЛИЛЗАМЕЩЕННЫЙ БЕНЗОЛСУЛЬФОНАМИД ИЛИ ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМАЯ СОЛЬ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЛЕЧЕНИЯ ОТ ВОСПАЛЕНИЯ ИЛИ СВЯЗАННОГО С ВОСПАЛЕНИЕМ ЗАБОЛЕВАНИЯ | 1994 |
|
RU2139281C1 |
| ПРОИЗВОДНЫЕ N-(1,5-ДИФЕНИЛ-1Н-ПИРАЗОЛ-3-ИЛ)СУЛЬФОНАМИДА СО СРОДСТВОМ К РЕЦЕПТОРАМ CB | 2005 |
|
RU2366657C2 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1999 |
|
RU2233272C2 |
Настоящее изобретение относится к области лекарственных средств, в частности к фармацевтической композиции для лечения рака молочной железы, которая включает бисфосфонат, ингибитор СОХ-2 и таксотер для одновременного, последовательного или раздельного применения, где бисфосфонат представляет собой 2-(имидазол-1-ил)-1-гидроксиэтан-1,1-дифосфоновую кислоту (золедроновую кислоту) или ее фармакологически приемлемую соль и где ингибитором СОХ-2 является SC236. 2 н.п. ф-лы, 20 табл.
| САМОРЕГУЛИРУЮЩИЕСЯ ЛОПАСТИ ВЕНТИЛЯТОРА | 1933 |
|
SU38730A1 |
| SENARATNE S.G | |||
| et al | |||
| Bisphosphonates induce apoptosis in human breast cancer cell lines | |||
| Br | |||
| J | |||
| Cancer | |||
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| JAGDEV S.P | |||
| et al | |||
| The bisphosphonate, zoledronic acid, induces apoptosis of breast cancer cells: evidence for synergy with paclitaxel | |||
| Br | |||
| J | |||
| Cancer | |||
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
| Прибор для промывания газов | 1922 |
|
SU20A1 |
Авторы
Даты
2008-02-27—Публикация
2002-10-18—Подача