Изобретение относится к области отбеливания и дезинфекции различных материалов, в частности природных и текстильных волокнистых материалов, бумаги, а также дезинфекции воды и водных растворов, различных материалов, в том числе медицинских инструментов и оборудования и, кроме того, может использоваться как антисептик.
Для дезинфекции и отбеливания известно применения гипогалогенов, а самым предпочтительным из них в силу малой стоимости и наименьшего вреда для окружающей среды является гипохлорид натрия. При этом действие составов на его основе, заключающееся в эффективной отбелке и дезинфекции, происходит при низких температурах - 15-25 градусов С (См., напр., В.А.Слипченко. Совершенствование технологии очистки и обеззараживания воды хлорированием. Киев. 1988 г. Стр. 12.) Указанное вещество широко используется в качестве отбеливающего средства, при хлорировании и окислении органических соединений, для очистки питьевой воды и обезвреживания стоков. Однако при использовании составов, основанных на гипогалогенах, возникает проблема низкой скорости отбеливания и дезинфекции материалов. Низкая скорость обработки жидких сред, включающих воду и водные растворы, а также волокон животного и растительного происхождения гипогалогенами является лимитирующим фактором при индустриальной обработке материалов. Например, при температурах 25-35 градусов С деструкция окрашенных примесей под воздействием гипохлорита натрия протекает в течение 1-2 часов (см., напр., Н.Б.Мельников и др. Физические основы процессов отделочного производства. Москва. 1982 г. Стр. 19). Повышение температуры отбеливания и дезинфицирования приводит к деструкции гипогалогенов вследствие их ускоренного саморазложения. Саморазложение снижается при увеличении щелочности растворов гипогалогенов. Наиболее устойчивым является раствор с рН (водородный показатель раствора) более 11, чего можно добиться, например, при избытке щелочи в количестве 20-30 г/л раствора. Но при таких высоких показателях рН растворы теряют свойство эффективно отбеливать материалы, а также теряют свои свойства дезинфектантов.
Наиболее близким к заявляемому изобретению является патент РФ №2165453, в котором приводится состав, содержащий источник гипохлорита, рН-поддерживающий буферный компонент, выбранный из группы, включающей средние соли щелочных металлов, например карбонат натрия, фосфаты и их смеси, сильный источник щелочности в качестве факультативного ингредиента. рН-поддерживающий компонент состава обеспечивает то, что значение рН поддерживается в определенном интервале значений рН, в том числе и после разбавления. Недостатком этого состава, а также подобных ему является то, что процессы отбеливания и дезинфекции при их применении в условиях рН более 10 резко замедляются по причине снижения химической активности гипохлорита натрия в среде высокой щелочности. (См., Б.Н.Мельников и др. Физико-химические основы процессов отделочного производства. Москва, 1982 г. Стр. 19).
Задачей изобретения является создание содержащего гипогалоген состава с рН-поддерживающей смесью для отбеливания и дезинфекции при температурах более 35 градусов С с водородным показателем рН раствора более 7,5.
Изобретение направлено на ускорение отбеливания и дезинфекции предложенным составом за счет повышения температуры раствора данных составов более 35 градусов С, вплоть до 150 градусов С при рН 7,5-12, более предпочтительно 9-10.
Автором настоящего изобретения было найдено, что в щелочных растворах с источником гипогалогена, например гипохлорита натрия или хлорированного тринатрий-орто-фосфата, происходит спонтанное понижении рН, то есть снижение щелочности, а вслед за этим показателем происходит потеря активного хлора в растворе. Процесс тем интенсивнее, чем выше температура раствора. Удалось установить, что процесс связан со степенью диссоциации воды как источников гидроксил-ионов. Известно, что NaOH по протонной теории является основанием не потому, что он способен отщеплять ОН-, а потому, что ОН- способен присоединять протон 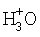 с образованием молекулы воды. В растворе всегда присутствуют молекулы гипохлористой кислоты в недиссоциированной HClO в тем меньшем количестве, чем более щелочной раствор. При рН более 9 в растворе большая часть молекул HClO диссоциирована на
с образованием молекулы воды. В растворе всегда присутствуют молекулы гипохлористой кислоты в недиссоциированной HClO в тем меньшем количестве, чем более щелочной раствор. При рН более 9 в растворе большая часть молекул HClO диссоциирована на 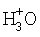 и OCl-, образуя NaOCl-. Новое, обнаруженное автором изобретения, состоит в том, что недиссоциированные молекулы гипохлористой кислоты при рН более 8,5-9,0 в условиях плюсовой температуры раствора диссоциируют, образуя воду путем захвата гидроксильных групп свободной щелочи, что соответственно приводит к уменьшению щелочности и соответственно уменьшению стабильности раствора.
и OCl-, образуя NaOCl-. Новое, обнаруженное автором изобретения, состоит в том, что недиссоциированные молекулы гипохлористой кислоты при рН более 8,5-9,0 в условиях плюсовой температуры раствора диссоциируют, образуя воду путем захвата гидроксильных групп свободной щелочи, что соответственно приводит к уменьшению щелочности и соответственно уменьшению стабильности раствора.
Удалось также обнаружить, что технический результат, обеспечивающий ускорение отбеливания и дезинфицирования материалов в области высоких температур процесса за счет усиления химической устойчивости растворов гипогалогенов, например гипохлорида натрия, может быть достигнут путем создания состава, содержащего источник гипогалогена с рН-поддерживающей буферной смесью, выбранной из группы средних солей щелочных металлов угольной и фосфорной кислот, например карбоната натрия, фосфата натрия и их смесей, кроме того, состав дополнительно содержит и кислые соли различной основности, например гидрокарбонат натрия, дигидрофосфат натрия, гидрофосфат натрия, и их смеси в количестве, обеспечивающем стабильность состава при рабочей температуре раствора 35 -150 градусов С.
Оптимальное количественное отношение средней соли к кислой составляет от 0,03 мас.%: 20 мас.% до 20 мас.%: 0,01 мас.%.
В качестве гипогалогенного отбеливателя и дезинфектанта выбран гипохлорит щелочного металла. Предпочтительным является гипохлорит натрия.
Указанный гипогалогенный отбеливатель и дезинфектант присутствует в количестве 0,03-20 мас.%, предпочтительно 2-8%.
Состав дополнительно может содержать также сильный источник щелочности.
Под химической устойчивостью имеют в виду то, что содержащие источники гипогалогена составы по настоящему изобретению не должны терять больше, чем 15% активного хлора после их хранения в течение 5 дней при 50 градусах С±5 градусов С. Процент активного хлора может быть измерен с помощью метода, описанного, например, в "Analyses des Taux et Extracts de Javel", опубликованном в "La chambre Sindicate nationale de Lear de Javel et des products connexes", стр. 9-10, 1984 г. Указанный метод состоит в измерении активного хлора в свежем состоянии, например, сразу после его приготовления и в том же самом составе через 5 дней при 50 градусах С. Дополнительно проводилась проверка наличия у состава по настоящему изобретению химической стойкости к более высоким температурам - до 120-150 градусов С в течение от 2 часов до 24 часов. Потери активного хлора при этом составляют не более 10-15%.
Наличие в рН-поддерживающей буферной смеси наряду с источником гипогалогена и средней солью, например карбонатом натрия, фосфатом натрия, также кислых солей, например гидрокарбоната натрия, дигидрофосфата натрия, гидрофосфата натрия и их смесей в количественном соотношении средней соли к кислой от 0,03 мас.%: 20 мас.% до 20 мас.%: 0,01 мас.% обеспечивает следующие преимущества: неожиданно обнаружилось, что кислая соль обратимо связывает ионы гидроксила в растворе, поставляемые средней солью, например гидрокарбонат натрия в паре с карбонатом натрия или дигидрофосфат натрия в паре с карбонатом натрия или гидрокарбонат натрия в паре с фосфатом натрия или дигидрофосфат натрия в паре с гидрофосфатом натрия или дигидрофосфат натрия, гидрокарбонат натрия с карбонатом натрия и т.п., поставляя при последующем нагреве раствора эти гидроксил-ионы в раствор, и этим предотвращают падение рН, вызванное распадом недиссоциированной гипохлористой кислоты либо иными причинами.
При этом следует отметить, что поскольку указаны пределы оптимального состава, постольку выход за указанные пределы содержания компонентов в составе, как это было экспериментально подтверждено, несколько ухудшает показатели, однако технический результат не исчезает и по сравнению с прототипом проявляется практически при любом соотношении средних и кислых слой в рамках условий водного раствора.
Способность предложенной смеси увеличивать химическую устойчивость и активность может быть продемонстрирована следующим сравнительным тестом.
Для эксперимента выбираем раствор гипохлоританатрия, полученный нейтрализацией хлорноватистой кислоты щелочью. Свободная щелочь практически отсутствует, то есть имеются следы, которые не учитываем. Водородный показатель рН раствора гипохлорита натрия в воде при концентрации гипохлорита 19 мас.% равен 7,5-8,5.
рН-поддерживающий компонент приготовляемого состава как по изобретению, так и контроль, обеспечивает то, что значение рН составляет в данном случае 9, но в реальном исполнении возможно другое значение рН, например, для условий дезинфекции предпочтительно значение рН, равное 7,5-8,5, а для целей отбеливания необходимо, то есть более предпочтительно значение рН, равное 8,5-12, еще более предпочтительно 9-10, так как в этом интервале отбеливание наиболее эффективно. В то же время в интервале рН, равном 9-10, раствор существующих в настоящее время гипохлоритных отбеливателей не обладает достаточной химической устойчивостью при температурах более 100 градусов С, в особенности более 120 градусов С.
Раствор гиполорита натрия с концентрацией 19 мас.% доводим водой до 5 мас.%. Этот раствор используем в дальнейшем для приготовления растворов контроля и опыта.
Контроль 1. Добавление гидроксида натрия до рН 9,0 менее 0,3 мас.%.
Контроль 2. Добавление карбоната натрия до рН 9,0 менее 0,75 мас.%
Опыт 1. Добавление карбоната натрия+гидрокарбоната натрия в количестве (Na2CO3=5 мас.% NaHCO3=1,3 мас.% г) до рН 9,0.
Опыт 2. Добавление фосфата натрия+дигидрофосфата натрия в количестве (Na3PO4=7,5 мас.% NaH2PO4=0,9 мас.% г) до рН 9,0.
Предпочтительно составы по настоящему изобретению используют в разбавленной форме при их приготовлении как для дезинфекции, так и для отбеливания. Выражение "использовать в разбавленном виде" в данном случае означает, что разбавление производится пользователем, и его проводят, например, в случае ручной стирки или перед индустриальным использованием или перед употреблением для дезинфекции помещения и т.п. Предпочтительно состав разбавляют от 100 до 200 раз, доведя концентрацию гипохлорита до 0,1-0,2 мас.% в конечном растворе. Именно такой раствор активного хлора используется для целей отбеливания и дезинфекции. Для целей дезинфекции используется и менее активный раствор, то есть раствор с меньшей концентрацией активного хлора, например от 0,05 до 0,06 мас.%. В данном случае раствор также разбавляем от 5 мас.% до 0,1 мас.%.
Контроль 3. Добавление фосфата натрия до рН 9,0 менее 0,62 мас.%.
Опыт 3. Разбавление раствора из опыта 2 до 0,06 мас.%
Контроль 4. Раствор Амукин французской лаборатории Жифрер Барбеза с концентрацией 0,06 мас.%.
Контроль 5. Раствор от контроля 1, разбавленный до 0,06 мас.%. Пояснение: Амукин представляет антисептик-гипохлорит натрия раствор с концентрацией активного хлора 0,06 мас.%. Срок хранения при температуре 25 градусов С в закрытой полиэтиленовой упаковке составляет 3 года. Применение в качестве антисептической обработке наружных ран в медицине и ветеринарии. В качестве стабилизатора применяются боратные соединения, достаточно токсичные. В описываемом эксперименте применяется в качестве образца сравнения, имеющего известный срок хранения, что позволяет экстраполировать данные, полученные при высоких температурах, на сохранность растворов при температурах 20-25 градусов С.
Экспериментальные данные.
Контрольные и опытные растворы переносят в стандартные стеклянные флаконы на 500 мл из-под физиологического раствора. Запечатывают резиновыми (силиконовыми) пробками и закатывают алюминиевыми колпачками герметично. Переносят флаконы в автоклав (духовой шкаф фирмы "Memmert"). Температуру устанавливают на уровне 90 градусов С. Время эксперимента - 6 суток (144 часа).
Контроль 1. Потеря активного хлора составила 436 мг/литр (NaOH).
Контроль 2. Потеря активного хлора составила 337 мг/литр (Na2CO3).
Контроль 3. Потеря активного хлора составила 407 мг/литр (Na3PO4).
Опыт 1. Потеря активного хлора составила 138 мг/литр (Na2CO3/NaHCO3).
Опыт 2. Потеря активного хлора составила 173 мг/литр (Na3PO4/NaH2PO4).
Опыт 3. Потеря активного хлора составила 125 мг/литр (Na2CO3/NaHCO3).
Контроль 4. Потеря активного хлора составила 138 мг/литр (Амукин).
Контроль 5. Потеря активного хлора составила 410 мг/литр (NaOH)
Концентрация гипохлорита в исследуемых образцах оценивалась следующим образом: 5 мл исследуемого раствора переносились в коническую колбу емкостью 200 мл. Затем в нее переносилось 5 мл 10% раствора калия иодида и 5 мл 5% серной кислоты. Колба ставится в темное место на 5 минут. Затем колба с исследуемым раствором ставилась под бюретку емкостью 25 мл с 0,01 мас.% тиосульфата натрия. Раствор тиосульфата натрия путем закапывания вводится в исследуемый раствор. Интенсивно красная окраска раствора постепенно бледнеет, превращаясь в бледно-розовую. На завершающем этапе в раствор вводится 1% раствор крахмала. Раствор окрашивается в интенсивно синий цвет. В раствор добавляется несколько капель тиосульфата натрия из бюретки и раствор полностью обесцвечивается. Точность при единичном измерении - плюс-минус 50 мг на литр раствора. Затем число 74,5 умножается на объем в мл использованного тиосульфата натрия. Полученный результат есть количество гипохлорита натрия на единицу объема. Например, на нейтрализацию гипохлорита внесено 8 куб. см тиосульфата натрия. Тогда 74,5×8=596 мг/литр раствора..
Контрольные и опытные образцы переносят в соответствующие флаконы и помещают в духовой шкаф при температуре 125 градусов С на срок 24 часа.
Контроль 1. Потеря активного хлора - 640 мг/л (NaOH).
Контроль 2. Потеря активного хлора - 570 мг/л (Na2CO3).
Контроль 3. Потеря активного хлора - 605 мг/л (Na3PO4).
Опыт 1. Потеря активного хлора - 72 мг/л (Na2CO3/NaHCO3).
Опыт 2. Потеря активного хлора - 90 мг/л (Na3PO4/NaH2PO4).
Опыт 3. Потеря активного хлора - 85 мг/л (Na2CO3/NaHCO3).
Контроль 4. Потеря активного хлора - 210 мг/л (Амукин).
Контроль 5. Потеря активного хлора - 360 мг/л (NaOH).
Комментарий.
Полученные данные свидетельствуют о неожиданном усилении химической устойчивости составов с источником гипогалогена и рН-поддерживающей буферной смесью, выбранной из группы, включающей средние соли щелочных металлов угольной и фосфорной кислот, например карбонат натрия, фосфат натрия и их смесей при дополнительном содержании в нем кислый солей различной основности, например гидрокарбоната натрия, дигидрофосфата натрия, гидрофосфата натрия и их смесей.
Данные также свидетельствуют о высокой химической активности раствора, отличающей от таковой контроль при температуре 25 градусов С. Об этом свидетельствует следующий эксперимент: в бак с баранчиком помещают текстильное волокно в количестве 2 кг, заливают водой, добавляют щелочь в количестве 25-30 грамм/литр, силикат натрия в количестве 305 грамм/литр, сульфит натрия - 2-3 грамма/литр, завинчивают баранчик и помещают бак в духовой шкаф при температуре 120-130 градусов С. Таким образом, производим отварку волокна. После этого охлаждаем раствор, вынимаем волокно, которое приобретает после отварки серый цвет и промываем его для удаления щелочи и продуктов, адсорбировавшихся силикатом натрия. Затем вновь помещаем волокно в бак, заливаем его составом по изобретению, например раствором гипохлорита натрия с концентрацией 1-2 грамма/литр (0,1-0,2 мас.%) с рН-поддерживающей смесью, например раствором карбоната натрия с гидрокарбонатом натрия в процентном соотношении 0,1-0,2 мас.%: 0,02-0,05 мас.%, завинчиваем баранчик и поднимаем температуру до 125 градусов С. После того как температура состава в баке поднимется до 125 градусов С, время проведения процесса отбеливания устанавливаем в 15 минут, после чего сбрасываем температуру и ускоренно охлаждаем бак. Затем вынимаем из бака текстильное волокно и производим визуальный осмотр, производя тем самым оценку белизны волокна сравнительно с контролем.
Контроль. Вышеупомянутые действия по отварке и отбелке. Отличия состоят в температуре, которая не превышает 35 градусов С, времени отбелки, которое составляет 2 часа и состава смеси. В составе смеси для отбелки присутствуют раствор гипохлорита натрия с рН 10 для усиления устойчивости раствора гипохлорита натрия к температуре.
Произведенное сравнение свидетельствует о явном преимуществе высокотемпературной отбелки перед низкотемпературной как в скорости отбелки, так и в ее качестве. Степень отбеливания может определяться также инструментальными методами, например, с помощью колориметра, такого как "Ganz Grisser" или других, например, "Zeiss Elrepho".
Изобретение предназначено не только для отбеливания, но и для применения в медицине, санитарии в качестве дезинфицирующего и антисептического средства, имеющего повышенную сохранность, в том числе не только в кристаллической форме, но и в растворах при повышенной температуре. Известно (см., напр., А.П.Красильников. Справочник по антисептике. Москва. 1995 г. Стр. 96. стр. 70, стр. 60-62) применение гипохлоритов натрия и калия в качестве антисептиков за счет своего окислительного действия при бактериальных, вирусных и грибковых заболеваниях. Оказывают микробоцидное действие на широкий спектр микроорганизмов, в том числе на стафилококки, кишечную палочку, псевдомонады, вирусы, дрожжи в концентрациях 100-200 мг/литр; 2-5% раствор рекомендуют для промывки вагины, полости рта, носа, глотки и т.п. Применяется в растворе с рН 12 для повышения срока хранения. Для увеличения щелочности применяются гидроксиды натрия и калия. Таким образом, применение предлагаемого решения позволит достичь усиления антисептического действия: а) снижение величины водородного показателя рН по крайней мере до 9,0-8,5 увеличивает срок хранения по крайней мере до 3-х лет, о чем свидетельствует сравнение по температурной устойчивости с препаратом Амукин; б) снижение рН раствора гипохлорита натрия при прочих условиях усиливает микробоцидность раствора за счет увеличения в растворе доли гипохлористой кислоты, что при высокой температурной устойчивости раствора позволяет усиливать обеззараживание воды и водных растворов в зимнее время, что актуально, а также обеззараживать воду в протяженных водных сетях, обеззараживать воду в теплообменниках ТЭС и АЭС, то есть эффективно производить борьбу с биологическим обрастанием теплообменников (см., напр., С.В.Костюченко и др. Обеззараживание при подготовке питьевой воды из поверхностных источников. Водоснабжение и санитарная техника. 1999г. №2, стр. 11). Это тем более актуально, что другие хлорсодержащие соединения (гипохлорит натрия, двуокись хлора и т.д.), используемые для обеззараживания воды, в практике обработки оборотной воды для подавления биологических обрастании применения в настоящее время не находят (см., напр., Д.И.Кучеренко и др. Оборотное водоснабжение (системы водяного охлаждения). Москва. 1980 г. Стр. 93).
Что касается применения гипохлорита натрия в медицине, то известно также применение аппаратов ЭДО-4 и ЭДО-01 для выработки на этих аппаратах растворов гипохлорита натрия, пригодных для внутривенного введения в организм человека для интоксикации крови и уничтожения бактерий. Срок хранения гипохлорита для внутривенного введения с рН 9,0 составляет 20-30 дней. Для увеличения химической устойчивости гипохлорита медицинского назначения никакие химикаты не применяются. В то же время известно, что гидрокарбонат натрия и гидрофосфат натрия составляют основу буферной системы крови и тканей человека и животных. Существуют различные препараты, основу которых составляют гидрокарбонат и гидрофосфат натрия как буферные элементы, не являющиеся токсичными в концентрациях, применяющихся для увеличения химической устойчивости раствора гипохлорита натрия. Например, в препарате под торговой маркой «Трисоль», предназначенном как раствор солевой для регидратации и дезинтокссикации, препятствующий развитию метаболитического апидоза, активные вещества натрия хлорид, калия хлорид и натрия бикарбонат (гидрокарбонат), концентрация веществ составляет 5 г:1 г:4 г соответственно. То есть концентрация бикарбоната сопоставима с концентрацией гидрокарбоната в растворе с гипохлоритом по изобретению. В дальнейшем вполне допустимо сочетание раствора «Трисоль» с раствором гипохлорита по изобретению, поскольку введение раствора гипохлорита, вырабатываемого установками ЭДО-01 и ЭДО-4, предусматривает дезинтоксикацию крови, но другим путем, а именно: путем окисления токсинов в крови и уничтожения бактерий также за счет окисления. Дополнительный элемент композиции - карбонат натрия не накладывает ограничений на существование лекарств, в которых содержатся гипохлорит натрия, карбонат натрия, гидрокарбонат натрия и, возможно, калия хлорид. Раствор может быть приготовлен на физиологическом растворе, поскольку проведенные опыты не показывают снижение химической устойчивости при наличии 0,9 мас.% хлорида натрия.
Предпочтительными галогеновыми отбеливателями и дезинфектантами для составов по данному изобретению являются гипохлориты щелочных и щелочноземельных металлов, выбранные из группы, включающей гипохлориты натрия, калия, магния, лития, кальция и их смесей. Наиболее предпочтительным является гипохлорит натрия.
Предпочтительно составы содержат указанный галогеновый отбеливатель и дезинфектант в таком количестве, чтобы содержание активного галоида в составе составляло от 0,3 мас.% до 20 мас.%, более предпочтительно от 2 до 8 мас.%. рН-поддерживающий компонент состава обеспечивает то, что значение рН состава поддерживается в интервале значений рН от 7,5 до 12, предпочтительно от 8, до 12, более предпочтительно от 9 до 10, после того как состав был разбавлен водой или физиологическим раствором от 100 до 200 раз его массы к воде. Именно щелочной диапазон от 9 до 10 является оптимальным для отбеливания, скорости отбеливания и химической устойчивости галогенида. В то же время для дезинфекции оптимальным является диапазон рН 8,0-9,0. Диапазон рН вполне обеспечивается буферной смесью и галогенидным отбеливателем и дезинсектантом, приведенными выше. Однако в добавление к этим компонентам можно также использовать сильный источник щелочности. Подходящими источниками щелочности являются каустические щелочи, такие как гидроксид натрия, гидроксид калия, гидроксид лития, оксиды щелочных металлов, такие как оксид натрия или калия. Предпочтительными источниками сильной щелочности являются каустические щелочи, более предпочтительно гидроксид натрия и гидроксид калия. Типичные концентрации таких каустических щелочей, когда они присутствуют, составляют от 0,1 до 1,5 мас.%, но в данном случае предпочтительно не более 0,1 мас.% от массы состава.
Состав может содержать и другие необязательные компоненты, такие как отдушки, устойчивые к отбеливателю и дезинфектанту, поверхностно-активные вещества, органические и неорганические щелочи, пигментные красители, оптические блескообразователи, растворители, хелатирующие агенты, гасители радикалов и их смеси.
Приготовление предлагаемого состава осуществляют либо путем растворения кислых солей угольной и фосфорной кислот в водном жидком растворе гипогалогена, либо путем сорастворения рН-поддерживающей смеси с твердым или жидким гипогалогеном, либо путем смешивания отдельных компонентов состава и в случае необходимости одновременного размалывания смеси в шаровой мельнице. Процесс размола является чисто механическим, и при нем не происходят химические реакции отдельных компонентов друг с другом.
Изобретение иллюстрируется следующими не ограничивающими его примерами, в которых все процентные концентрации указаны на основе массы, пока нет указаний на другое.
Пример 1.
В соответствии с изобретением были приготовлены составы, приведенные в таблице 1.
Пример 2.
Приготовленные в соответствии с настоящим изобретением составы даны в таблице 2.
Пример 3.
В соответствии с изобретением составы даны в таблице 3.
| название | год | авторы | номер документа |
|---|---|---|---|
| СТАБИЛЬНАЯ ОТБЕЛИВАЮЩАЯ КОМПОЗИЦИЯ | 2015 |
|
RU2693486C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОТБЕЛИВАЮЩИХ СОСТАВОВ, СОДЕРЖАЩИХ ИСТОЧНИКИ ХЛОРА И БРОМА, И ЕГО ПРОДУКТ | 1996 |
|
RU2160769C2 |
| ВОДНЫЙ ЖИДКИЙ ОТБЕЛИВАЮЩИЙ СОСТАВ | 1994 |
|
RU2143021C1 |
| ОТБЕЛИВАЮЩИЕ СОСТАВЫ | 1997 |
|
RU2165453C2 |
| ВОДНАЯ ЖИДКАЯ КОМПОЗИЦИЯ ДЛЯ ОТБЕЛИВАНИЯ | 2006 |
|
RU2394880C2 |
| ВОДНЫЕ ЖИДКИЕ ОТБЕЛИВАЮЩИЕ КОМПОЗИЦИИ | 2005 |
|
RU2387705C2 |
| СОСТАВ ДЛЯ ОБЕЗЗАРАЖИВАНИЯ ВОДЫ | 2005 |
|
RU2299862C2 |
| КОМПОЗИЦИЯ (ВАРИАНТЫ) И СПОСОБЫ ОБРАБОТКИ МАТЕРИАЛА (ВАРИАНТЫ) | 2007 |
|
RU2423049C2 |
| МНОГОКОМПОНЕНТНЫЕ КОМПОЗИЦИИ ДЛЯ ЧИСТКИ ТВЕРДЫХ ПОВЕРХНОСТЕЙ | 2000 |
|
RU2208627C1 |
| Способ получения отбеливателя на основе гипохлорита кальция | 1990 |
|
SU1736918A1 |
Изобретение относится к отбеливанию природных волокнистых материалов и бумаги, а также волокон текстильных материалов. Состав содержит гипогалоген а также pH-поддерживающую буферную смесь, выбранную из группы средних солей щелочных металлов угольной и фосфорной кислот и их смесей, дополнительно содержит кислые соли различной основности, например гидрокарбонат натрия, дигидрофосфат натрия, гидрофосфат натрия и их смеси в количестве, обеспечивающем стабильность состава при рабочей температуре раствора 35 градусов С и выше. Оптимальное количественное отношение средней соли к кислым солям составляет от 0,03 мас.% : 20 мас.% до 20 мас.% : 0,01 мас.%. Состав обладает высокой химической активностью и обеспечивает высокую степень белизны и дезинфекции материалов. 3 з.п. ф-лы, 3 табл.
| ОТБЕЛИВАЮЩИЕ СОСТАВЫ | 1997 |
|
RU2165453C2 |
| ВОССТАНОВИТЕЛЬНАЯ ОТБЕЛИВАЮЩАЯ КОМПОЗИЦИЯ, СПОСОБ ОТБЕЛИВАНИЯ | 1994 |
|
RU2143022C1 |
| СОСТАВ ДЛЯ ОТБЕЛИВАНИЯ ТЕКСТИЛЬНЫХ МАТЕРИАЛОВ | 2000 |
|
RU2179208C2 |
| RU 2004659 A, 30.03.1994. | |||
Авторы
Даты
2008-05-10—Публикация
2003-06-10—Подача