Настоящее изобретение относится к новому способу получения динитрилов фенилмалоновой кислоты.
Способы синтеза динитрилов арилмалоновой кислоты путем образования связи С-С между незамещенными и замещенными арилгалогенидами и динитрилами малоновой кислоты описаны в Chem. Commun. 1984, 932, JP-A-60197650 и WO 00/78712. Синтез проводят в присутствии палладиевых катализаторов и оснований в инертных растворителях. В качестве предпочтительных оснований описаны гидриды щелочных металлов, амиды щелочных металлов и алкоголяты щелочных металлов.
Согласно изобретению неожиданно было обнаружено, что образования связи С-С между динитрилами малоновой кислоты и моно- или полизамещенными фенилпроизводными можно осуществить с хорошим выходом и при хорошей степени чистоты получаемых динитрилов фенилмалоновой кислоты, если вместо оснований, указанных в предшествующем уровне техники, использовать гидроксид щелочного металла.
В соответствии с этим настоящее изобретение относится к способу получения соединений формулы I
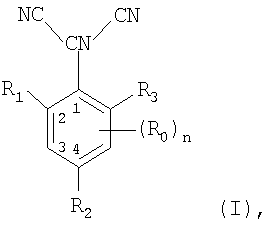
в которой
все R0 независимо один от другого обозначают галоген, C1-С6алкил, С2-С6алкенил, С2-С6алкинил, C1-С6галогеналкил, циано-С1-С6алкил, С2-С6галогеналкенил, циано-С2-С6алкенил, С2-С6галогеналкинил, циано-С2-С6алкинил, гидроксигруппу, гидрокси-C1-С6алкил, C1-С6алкоксигруппу, нитрогруппу, аминогруппу, C1-С6алкиламиногруппу, ди(С1-С6алкил)аминогруппу, C1-С6алкилкарбониламиногруппу, C1-С6алкилсульфониламиногруппу, C1-С6алкиламиносульфонил, C1-С6алкилкарбонил, С1-С6алкилкарбонил-С1-С6алкил, С1-С6алкоксикарбонил-С1-С6алкил, С1-С6алкилкарбонил-С2-С6алкенил, C1-С6алкоксикарбонил, C1-С6алкоксикарбонил-С2-С6алкенил, С1-С6алкилкарбонил-С2-С6алкинил, C1-С6алкоксикарбонил-С2-С6алкинил, цианогруппу, карбоксигруппу, фенил или ароматическое кольцо, содержащее 1 или 2 гетероатома, выбранные из группы, включающей азот, кислород и серу, где 2 последних ароматических кольца могут содержать в качестве заместителей C1-С3алкил, C1-С3галогеналкил, C1-С3алкоксигруппу, C1-С3галогеналкоксигруппу, галоген, циано- или нитрогруппу; или
R0 совместно с соседними заместителями R1, R2 и R3 образует насыщенный или ненасыщенный С3-С6углеводородный мостик, который может содержать 1 или 2 гетероатома, выбранные из группы, включающей азот, кислород и серу, и/или содержать в качестве заместителей С1-С4алкил;
все R1, R2 и R3 независимо один от другого обозначают водород, галоген, C1-С6алкил, С2-С6алкенил, С2-С6алкинил, С3-С6циклоалкил, C1-С6галогеналкил, С2-С6галогеналкенил, C1-С6алкоксикарбонил-С2-С6алкенил, C1-С6алкилкарбонил-С2-С6алкенил, циано-С2-С6алкенил, нитро-С2-С6алкенил, С2-С6галогеналкинил, С1-С6алкоксикарбонил-С2-С6алкинил, С1-С6алкилкарбонил-С2-С6алкинил, циано-С2-С6алкинил, нитро-С2-С6алкинил, С3-С6галогенциклоалкил, гидрокси-С1-С6алкил, С1-С6алкокси-С1-С6алкил, C1-С6алкилтио-С1-С6алкил, цианогруппу, С1-С4алкилкарбонил, C1-С6алкоксикарбонил, гидроксигруппу, C1-С10алкоксигруппу, С3-С6алкенилоксигруппу, С3-С6алкинилоксигруппу, C1-С6галогеналкоксигруппу, С3-С6галогеналкенилоксигруппу, С1-С6алкокси-С1-С6алкоксигруппу, меркаптогруппу, C1-С6алкилтиогруппу, C1-С6галогеналкилтиогруппу, C1-С6алкилсульфинил, C1-С6алкилсульфонил, нитрогруппу, аминогруппу, C1-С6алкиламиногруппу, ди(С1-С6алкил)аминогруппу или феноксигруппу, где фенильное кольцо может содержать в качестве заместителей C1-С3алкил, C1-С3галогеналкил, C1-С3алкоксигруппу, C1-С3галогеналкоксигруппу, галоген, циано- или нитрогруппу;
R2 дополнительно может обозначать фенил, нафтил или 5- или 6-членное ароматическое кольцо, которое может содержать 1 или 2 гетероатома, выбранные из группы, включающей азот, кислород и серу, где фенильное кольцо, нафтильное кольцо или 5- или 6-членное ароматическое кольцо могут содержать в качестве заместителей галоген, С3-С8циклоалкил, гидроксигруппу, меркаптогруппу, аминогруппу, цианогруппу, нитрогруппу или формил; и/или
фенильное кольцо, нафтильное кольцо или 5- или 6-членное ароматическое кольцо могут содержать в качестве заместителей C1-С6алкил, C1-С6алкоксигруппу, гидрокси-С1-С6алкил, С1-С6алкокси-С1-С6алкил, C1-С6алкокси-С1-С6алкоксигруппу, C1-С6алкилкарбонил, C1-С6алкилтиогруппу, Ci-С6алкилсульфинил, C1-С6алкилсульфонил, моно-С1-С6алкиламиногруппу, ди-C1-С6алкиламиногруппу, C1-С6алкилкарбониламиногруппу, C1-С6алкилкарбонил(С1-С6алкил)аминогруппу, С2-С6алкенил, С3-С6алкенилоксигруппу, гидрокси-С3-С6алкенил, С1-С6алкокси-С2-С6алкенил, C1-С6алкокси-С3-С6алкенилоксигруппу, С2-С6алкенилкарбонил, С2-С6алкенилтиогруппу, С2-С6алкенилсульфинил, С2-С6алкенилсульфонил, моно- или ди-С2-С6алкениламиногруппу, С1-С6алкил(С3-С6алкенил)аминогруппу, С2-С6алкенилкарбониламиногруппу, С2-С6алкенилкарбонил(С1-С6алкил)аминогруппу, С2-С6алкинил, С3-С6алкинилоксигруппу, гидрокси-С3-С6алкинил, C1-С6алкокси-С3-С6алкинил, С1-С6алкокси-С4-С6алкинилоксигруппу, С2-С6алкинилкарбонил, С2-С6алкинилтиогруппу, С2-С6алкинилсульфинил, C2-С6алкинилсульфонил, моно- или ди-С3-С6алкиниламиногруппу, С1-С6алкил(С3-С6алкинил)аминогруппу, С2-С6алкинилкарбониламиногруппу или С2-С6алкинилкарбонил(С1-С6алкил)аминогруппу; и/или
фенильное кольцо, нафтильное кольцо или 5- или 6-членное ароматическое кольцо могут содержать в качестве заместителей галогензамещенный C1-С6алкил, C1-С6алкоксигруппу, гидрокси-С1-С6алкил, С1-С6алкокси-С1-С6алкил, С1-С6алкокси-С1-С6алкоксигруппу, C1-С6алкилкарбонил, C1-С6алкилтиогруппу, C1-С6алкилсульфинил, C1-С6алкилсульфонил, моно-С1-С6алкиламиногруппу, ди-C1-С6алкиламиногруппу, C1-С6алкилкарбониламиногруппу, С1-С6алкилкарбонил(С1-С6алкил)аминогруппу, С2-С6алкенил, С3-С6алкенилоксигруппу, гидрокси-С3-С6алкенил, С1-С6алкокси-С2-С6алкенил, C1-С6алкокси-С3-С6алкенилоксигруппу, С2-С6алкенилкарбонил, С2-С6алкенилтиогруппу, С1-С6алкенилсульфинил, С2-С6алкенилсульфонил, моно- или ди-С2-С6алкениламиногруппу, С1-С6алкил(С3-С6алкенил)аминогруппу, С2-С6алкенилкарбониламиногруппу, С2-С6алкенилкарбонил(С1-С6алкил)аминогруппу, С2-С6алкинил, С3-С6алкинилоксигруппу, гидрокси-С3-С6алкинил, C1-С6алкокси-С3-С6алкинил, С1-С6алкокси-С4-С6алкинилоксигруппу, С2-С6алкинилкарбонил, С2-С6алкинилтиогруппу, С2-С6алкинилсульфинил, С2-С6алкинилсульфонил, моно- или ди-С3-С6алкиниламиногруппу, С1-С6алкил(С3-С6алкинил)аминогруппу, С2-С6алкинилкарбониламиногруппу или С2-С6алкинилкарбонил(С1-С6алкил)аминогруппу; и/или
фенильное кольцо, нафтильное кольцо или 5- или 6-членное ароматическое кольцо могут содержать в качестве заместителей радикал формулы COOR50, CONR51, SO2NR53R54 или SO2OR55, где все R50, R51, R52, R53, R54 и R55 независимо друг от друга обозначают C1-С6алкил, С2-С6алкенил или С3-С6алкинил или галоген-, гидрокси-, алкокси-, меркапто-, амино-, циано-, нитро-, алкилтио-, алкилсульфинил- или алкилсульфонилзамещенный C1-С6алкил, С2-С6алкенил или С3-С6алкинил; и n равно 0, 1 или 2, по реакции соединения формулы II
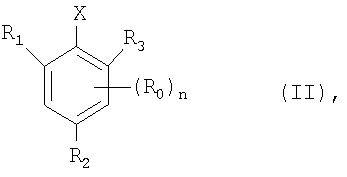
в которой
R0, R1, R2, R3 и n являются такими, как определено, и Х обозначает отщепляющуюся группу с динитрилом малоновой кислоты в инертном разбавителе в присутствии палладиевого катализатора и основания, и в этом способе в качестве основания используется гидроксид щелочного металла или смесь гидроксидов щелочных металлов.
Настоящий способ отличается следующим:
а) высокой объемной концентрацией реагентов,
б) возможностью применения большого количества палладиевых катализаторов, которые имеются в продаже или могут быть легко получены in situ из имеющихся в продаже солей палладия, например, раствора палладий(II)хлорида (20%) в концентрированной хлористоводородной кислоте, и соответствующих лигандов,
в) возможностью применения в качестве исходных соединений в особенности фенилпроизводных, замещенных в 2- и 6-положениях, которые могут содержать разные и стерически заторможенные отщепляющиеся группы,
г) легкой доступностью исходных веществ,
д) простой методикой проведения реакции,
е) простой обработкой и
ж) обычно очень высокими выходами и чистотой продуктов.
В связи с этим предложенный в настоящем изобретении способ получения является особенно подходящим для крупномасштабного получения производных динитрилов фенилмалоновой кислоты формулы I.
В приведенных выше определениях заместителей в соединениях формул I и II под галогеном следует понимать фтор, хлор, бром или йод, предпочтительно - фтор, хлор или бром.
Алкильными группами в определениях заместителей являются, например, метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил или трет-бутил, и изомеры пентила, гексила, гептила, октила, нонила, децила, ундецила и додецила.
Галогеналкильные группы предпочтительно обладают цепью, содержащей от 1 до 6 атомов углерода. Галогеналкил означает, например, фторметил, дифторметил, дифторхлорметил, дифторметил, хлорметил, дихлорметил, дихлорфторметил, трихлорметил, 2,2,2-трифторэтил, 2-фторэтил, 2-хлорэтил, 2,2-дифторэтил, 2,2-дихлорэтил, 2,2,2-трихлорэтил или пентафторэтил, предпочтительно - трихлорметил, дифторхлорметил, дифторметил, дифторметил или дихлорфторметил.
Алкоксигруппы предпочтительно обладают цепью, содержащей от 1 до 6 атомов углерода. Алкоксигруппа означает, например, метокси-, этокси-, н-пропокси-, изопропокси-, н-бутокси-, изобутокси-, втор-бутокси-, трет-бутокси- или изомеры пентилокси- и гексилоксигрупп; предпочтительно - метокси-, этокси- или н-пропоксигруппу.
Галогеналкоксигруппа означает, например, фторметокси-, дифторметокси-, трифторметокси-, 2,2,2-трифторэтокси-, 1,1,2,2-тетрафторэтокси-, 2-фторэтокси-, 2-хлорэтокси- или 2,2,2-трихлорэтоксигруппу.
Примерами алкенилов, которые можно отметить, являются винил, аллил, металлил, 1-метиловинил, бут-2-ен-1-ил, пентенил и 2-гексенил и предпочтение отдается алкенильным радикалам, которые обладают цепью, содержащей от 3 до 6 атомов углерода.
Примерами алкинилов, которые можно отметить, являются этинил, пропаргил, 1-метилпропаргил, 3-бутинил, бут-2-ин-1-ил, 2-метилбут-3-ин-2-ил, бут-3-ин-2-ил, 1-пентинил, пент-4-ин-1-ил и 2-гексинил, предпочтение отдается алкинильным радикалам, которые обладают цепью, содержащей от 3 до 6 атомов углерода.
В качестве галогеналкенила рассматриваются алкенильные группы, один или большее количество раз замещенные галогеном, галогеном предпочтительно являются бром или йод, а особенно предпочтительно - фтор или хлор, например, 2- и 3-фторпропенил, 2- и 3-хлорпропенил, 2- и 3-бромпропенил, 2,2-дифтор-1-метиловинил, 2,3,3-трифторпропенил, 3,3,3-трифторпропенил, 2,3,3-трихлорпропенил, 4,4,4-трифторбут-2-ен-1-ил и 4,4,4-трихлорбут-2-ен-1-ил. Из алкенильных радикалов, моно-, ди- или тризамещенных галогеном, предпочтение отдается таким, которые обладают цепью, содержащей от 3 до 6 атомов углерода. Алкенильные группы могут содержать галогены в качестве заместителей у насыщенных или ненасыщенных атомов углерода.
Алкоксиалкильные группы предпочтительно содержат от 1 до 6 атомов углерода. Алкоксиалкил означает, например, метоксиметил, метоксиэтил, этоксиметил, этоксиэтил, н-пропоксиметил, н-пропоксиэтил, изопропоксиметил или изопропоксиэтил.
Галогеналкоксигруппа означает, например, фторметокси-, дифторметокси-, трифторметокси-, 2,2,2-трифторэтокси-, 1,1,2,2-тетрафторэтокси-, 2-фторэтокси-, 2-хлорэтокси- или 2,2,2-трихлорэтоксигруппу.
Алкенилоксигруппа означает, например, аллилокси-, металлилокси- или бут-2-ен-1-илоксигруппу.
В качестве галогеналкенилоксигрупп рассматриваются алкенилоксигруппы, один или большее количество раз замещенные галогеном, галогеном предпочтительно являются бром или йод, а особенно предпочтительно - фтор или хлор, например, 2- и 3-фторпропенилокси-, 2- и 3-хлорпропенилокси-, 2- и 3-бромпропенилокси-, 2,3,3-трифторпропенилокси-, 2,3,3-трихлорпропенилокси-, 4,4,4-трифторбут-2-ен-1-илокси- и 4,4,4-трихлорбут-2-ен-1-илоксигруппы.
Алкинилоксигруппа означает, например, пропаргилокси или 1-метилпропаргилоксигруппу.
Подходящие циклоалкильные заместители содержат от 3 до 8 атомов углерода и представляют собой, например, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил или циклооктил, каждый из которых может один или большее количество раз быть замещен галогеном, предпочтительно - фтором, хлором или бромом.
Алкоксикарбонилом предпочтительно являются ацетил или пропионил.
Алкоксикарбонил означает, например, метоксикарбонил, этоксикарбонил, н-пропоксикарбонил, изопропоксикарбонил или изомеры бутоксикарбонила, пентилоксикарбонила и гексилоксикарбонила; предпочтительно - метоксикарбонил или этоксикарбонил.
Алкилтиогруппы предпочтительно обладают цепью, содержащей от 1 до 6 атомов углерода. Алкилтиогруппа означает, например, метилтио-, этилтио-, пропилтио-, бутилтио-, пентилтио- или гексилтиогруппы или их разветвленные изомеры; предпочтительно - метилтио- или этилтиогруппы.
Галогеналкилтиогруппа означает, например, 2,2,2-трифторэтилтио- или 2,2,2-трихлорэтилтиогруппу.
Алкилсульфинил означает, например, метилсульфинил, этилсульфинил, н-пропилсульфинил, изопропилсульфинил, н-бутилсульфинил, изобутилсульфинил, втор-бутилсульфинил или трет-бутилсульфинил; предпочтительно - метилсульфинил или этилсульфинил.
Алкилсульфонил означает, например, метилсульфонил, этилсульфонил, н-пропилсульфонил, изопропилсульфонил, н-бутилсульфонил, изобутилсульфонил, втор-бутилсульфонил или трет-бутилсульфонил; предпочтительно - метилсульфонил или этилсульфонил.
Алкиламиногруппа означает, например, метиламино-, этиламино-, н-пропиламино-, изопропиламиногруппу или изомеры бутил-, пентил- и гексиламиногрупп.
Диалкиламиногруппа означает, например, диметиламино-, метилэтиламино-, диэтиламино-, н-пропилметиламино-, дибутиламино- или диизопропиламиногруппу.
Алкилтиоалкил означает, например, метиламино-метил, метиламино-этил, этиламинометил, этиламиноэтил, н-пропиламинометил, н-пропиламиноэтил, изопропиламинометил или изопропиламиноэтил.
Фенил и нафтил в определении R2 и феноксигруппа в определении R1, R2 и R3 могут находиться в замещенной форме. В этом случае в соответствии с необходимостью заместители могут находиться в орто-, мета- и/или пара-положениях и дополнительно - в 5-, 6-, 7- и/или 8-положениях нафтильного кольца.
Примерами подходящих 5- или 6-членных ароматических колец, которые содержат 1 или 2 гетероатома, выбранных из группы, включающей азот, кислород и серу, в определении R0 и R2 являются пирролидильное, пиридильное, пиримидильное, триазинильное, тиазолильное, триазолильное, тиадиазолильное, имидазолильное, оксазолильное, изоксазолильное, пиразинильное, фурильное, тиенильное, пиразолильное, бензоксазолильное, бензотиазолильное, хиноксалильное, индолильное и хинолильное. Эти гетероароматические кольца также могут быть замещенными.
Определения, соответствующие приведенным выше, также можно применить к заместителям в определениях объединенных терминов, например, к алкоксиалкокси-, алкилсульфониламино-, алкиламиносульфонильной, фенилалкильной, нафтилалкильной и гетероалкильной группам.
В определениях алкилкарбонила и алкоксикарбонила карбонильный атом углерода не включен в нижние и верхнее предельные значения количеств атомов углерода, приведенные в каждом конкретном случае.
Предпочтение отдается соединениям формулы I, в которой n равно 0, 1 или 2; все R0 независимо один от другого обозначают галоген, C1-С6алкил, C1-С6галогеналкил, гидроксигруппу, C1-С6алкоксигруппу, нитрогруппу, аминогруппу, C1-С6алкиламиногруппу, ди(С1-С6алкил)аминогруппу, C1-С6алкилкарбониламиногруппу, C1-С6алкилсульфониламиногруппу, C1-С6алкиламиносульфонил, С1-С4алкилкарбонил, C1-С6алкоксикарбонил или карбоксил; и все R1, R2 и R3 независимо один от другого обозначают водород, галоген, C1-С6алкил, С2-С6алкенил, С2-С6алкинил, С2-С6циклоалкил, C1-С6галогеналкил, С2-С6галогеналкенил, С2-С6галогеналкинил, С3-С6галогенциклоалкил, С1-С6алкокси-С1-С6алкил, С1-С6алкилтио-С1-С6алкил, цианогруппу, С1-С4алкилкарбонил, C1-С6алкоксикарбонил, гидроксигруппу, С1-С10алкоксигруппу, С3-С6алкенилоксигруппу, С3-С6алкинилоксигруппу, C1-С6галогеналкоксигруппу, С3-С6галогеналкенилоксигруппу, С1-С6алкокси-С1-С6алкоксигруппу, меркаптогруппу, C1-С6алкилтиогруппу, C1-С6галогеналкилтиогруппу, C1-С6алкилсульфинил, C1-С6алкилсульфонил, нитрогруппу, аминогруппу, С1-С4алкилмино- или ди(С1-С4алкил)аминогруппу.
Предпочтение также отдается соединениям формулы I, в которой все R1, R2 и R3 независимо один от другого обозначают водород, галоген, С1-С4алкил, C1-С4галогеналкил, С2-С4алкенил, С2-С4галогеналкенил, С2-С4алкинил, С3-С6циклоалкил, С1-С4алкилкарбонил, C1-С6алкоксикарбонил, гидроксигруппу, С1-С4алкоксигруппу, С3- или С4-алкенилоксигруппу, С3- или С4-алкинилоксигруппу, С1-С4галогеналкоксигруппу, нитро- или аминогруппу.
Особым значением обладают соединения формулы I, в которой n равно 0 и все R1, R2 и R3 независимо друг от друга обозначают С1-С4алкил.
Получение соединений формулы I проиллюстрировано на приведенной ниже схеме реакций 1.
Схема реакций 1
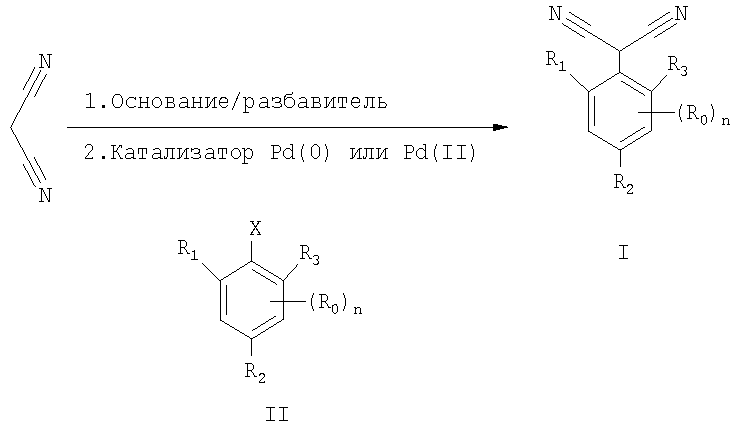
В соответствии со схемой реакций 1 соединения формулы I получают из динитрила малоновой кислоты путем введения последнего на первой стадии реакции в подходящем разбавителе в реакцию с основанием при температуре, равной от 0 до 250°С, предпочтительно - при температуре, равной от 20 до 100°С, в зависимости от разбавителя. На второй стадии реакции образование связи С-С осуществляется путем прибавления соединений формулы II и палладиевого катализатора при температуре, равной от 0 до 250°С, предпочтительно - от 90 до 150°С, в зависимости от разбавителя.
Отщепляющимися группами X, предпочтительными для реакции образование связи С-С соединения формулы II с динитрилом малоновой кислоты в присутствии палладиевых катализаторов, являются галоген; R10S(O)2O-, в котором R10 обозначает С1-С4алкил, предпочтительно - метил, C1-С4галогеналкил, предпочтительно - галогенметил или C4F9-(n), арил, предпочтительно - фенил или фенил, от одного до трех раз замещенный галогеном, метилом или галогенметилом; и моно-, ди- и триарилметоксигруппы.
Арильными радикалами моно-, ди- и триарилметоксигрупп предпочтительно являются фенильные радикалы, которые могут быть замещены, например, от одного до трех раз метилом, предпочтительно, чтобы заместители находились в 2-, 4- и/или 6-положениях фенильного кольца.
Примерами таких отщепляющихся групп являются метилсульфонилокси-(мезилат), дифторметилсульфонилокси- (трифлат), п-толилсульфонилокси-(тозилат), CF3(CF2)3S(O)2O- (нонафлат), дифенилметокси-, ди(метилфенил)метокси-, трифенилметокси- (тритил) и три(метилфенил)метоксигруппа.
Отщепляющимися группами, которые особенно предпочтительны, являются хлор, бром, йод, CF3(O)2O- (трифлат), CF3(CF2)3S(O)2O- (нонафлат), п-толил-S(O)2O- (тозилат), (С6Н5)2СНО-, (СН3-С6Н4)2СНО-, (С6Н5)3СО- (тритил) и (СН3-С6Н4)3СО-. Еще более предпочтительными являются хлор, бром и йод.
Палладиевыми катализаторами, которые рассматриваются для реакции образования связи С-С между соединением формулы II и анионом динитрила малоновой кислоты, обычно являются комплексы палладия(II) или палладия(0), например, палладий(II)дигалогениды, палладий(II)ацетат, палладий(II)сульфат, бис(трифенилфосфин)палладий(II)дихлорид, бис(трициклопентилфосфин)палладий(II)дихлорид, бис(трициклогексилфосфин)палладий(II)дихлорид, бис(дибензилиденацетон)палладий(0) или тетракис(трифенилфосфин)палладий(0).
В особенно предпочтительно варианте выполнения способа, предлагаемого в настоящем изобретении, палладиевый катализатор также можно получить in situ из соединений палладия(II) иди палладия (0) путем образования комплексов с необходимыми лигандами, например, путем введения соли палладия(II), комплекс которой необходимо образовать, например, палладий(II)дихлорида (PdCl2) или палладий(II)ацетата (Pd(OAc)2), вместе с необходимым лигандом, например, трифенилфосфином (PPh3) или трициклогексилфосфином (PCy3), вместе с выбранным разбавителем, динитрилом малоновой кислоты и основанием. Палладий(II)дихлорид можно использовать в качестве недорогостоящей соли палладия также в виде 20% раствора PdCl2 в концентрированной хлористоводородной кислоте. Необходимый лиганд предпочтительно прибавлять в реакционную среду в избытке, составляющем до 10 моль в пересчете на соль палладия. При нагревании реакционной среды затем in situ образуется комплекс палладия(II) или палладия(0), необходимый для реакции сочетания с образованием связи С-С, и затем этот комплекс инициирует реакцию сочетания с образованием связи С-С.
Примерами лигандов, подходящих для комплексов палладия(II) или палладия(0), являются триметилфосфин, триэтилфосфин, трис(трет-бутил)фосфин, трициклопентилфосфин, трициклогексилфосфин (PCy3), три(метилциклогексил)фосфин, метил(тетраметилен)фосфин, трет-бутил(пентаметилен)фосфин, трифенилфосфин (PPh3), три(метилфенил)фосфин, 1,2-дифенилфосфинциклогексан, 1,2-дифенилфосфинциклопентан, 2,2'-(дифенилфосфин)бифенил, 1,2-бис(дифенилфосфин)этан, 1,3-бис(дифенилфосфин)пропан, 1,4-бис(дифенилфосфин)бутан, 3,4-бис(дифенилфосфин)пирролидин, 2,2'-(дифенилфосфин)биснафтил (бинаф), 1,1'-бис(дифенилфосфин)ферроцен, 1,1'-бис(ди-трет-бутилфосфин)ферроцен, дифениловый эфир бисдифенилфосфина
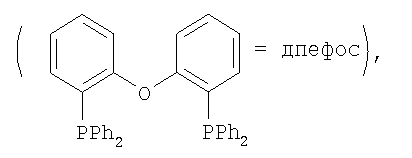
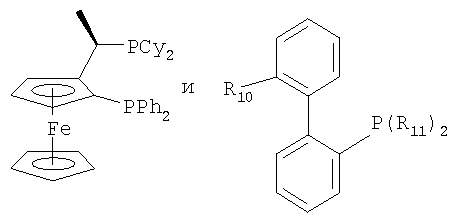 ,
,
где R10 обозначает водород или диметиламиногруппу и R11 обозначает циклогексил или трет-бутил.
Такие палладиевые катализаторы используются в количестве, составляющем от 0,001 до 100 мол.%, предпочтительно - в количестве, составляющем от 0,01 до 10 мол.%, а более предпочтительно - в количестве, составляющем от 0,1 до 1 мол.%, в пересчете на соединение формулы II.
Разбавители, пригодные для образования аниона динитрила малоновой кислоты, (стадия 1) на схеме реакций 1), а также для катализируемой палладием реакции образования связи С-С с соединением формулы II (стадия 2) на схеме реакций 1), являются алифатические, циклоалифатические и ароматические углеводороды, например, пентан, гексан, петролейный эфир, циклогексан, метилциклогексан, бензол, толуол и ксилолы, алифатические галогенуглеводороды, например, метиленхлорид, хлороформ и ди- и тетрахлорэтан, нитрилы, например, ацетонитрил, пропионитрил и бензонитрил, простые эфиры, например, диэтиловый эфир, дибутиловый эфир, трет-бутилметиловый эфир, диметиловый эфир этиленгликоля, диэтиловый эфир этиленгликоля, диметиловый эфир диэтиленгликоля, тетрагидрофуран и диоксан, спирты, например, метанол, этанол, пропанол, бутанол, этиленгликоль, диэтиленгликоль, монометиловый и моноэтиловый эфиры диэтиленгликоля, кетоны, например, ацетон и метилизобутилкетон, сложные эфиры и лактоны, например, этил- и метилацетат и валеролактон, N-замещенные лактамы, например, N-метилпирролидон (НМП), амиды, например, N,N-диметилформамид (ДМФ) и диметилацетамид (ДМА), ациклические мочевины, например, N,N'-диметилэтиленмочевина (ДММ), сульфоксиды, например, диметилсульфоксид и смеси таких разбавителей. Из них особое предпочтение отдается ароматичексим углеводородам, простым эфирам, сульфоксидам, N-замещенным лактамам и ациклическим мочевинам.
Более предпочтительным является N-метилпирролидон.
В качестве разбавителя также применима вода, если целесообразно, то в смеси с одним из указанных выше разбавителей.
Для получения аниона динитрила малоновой кислоты в контексте настоящего изобретения рассматриваются гидроксиды щелочных металлов и смеси гидроксидов щелочных металлов, предпочтительно - гидроксид натрия и гидроксид калия и смеси этих гидроксидов, предпочтительно - гидроксид натрия.
Основание предпочтительно использовать в эквивалентных количествах или в избытке, составляющем от 2 до 10 эквивалентов в пересчете на динитрил малоновой кислоты.
Получение аниона динитрила малоновой кислоты и его реакцию с соединением формулы II в присутствии палладиевого катализатора предпочтительно проводить при температурах реакции, составляющих от 0 до 250°С, предпочтительно - при температурах от 50 до 200°С в зависимости от используемой реакционной среды и давления при проведении реакции.
Если это целесообразно, то реакцию сочетания с образованием связи С-С между анионом динитрила малоновой кислоты и соединением формулы II можно проводить при повышенном давлении, предпочтительно - при давлении от 1,1 до 10 бар. Такая процедура, выполняемая в закрытой системе при повышенном давлении, является особенно подходящей для реакций, проводимых при температурах, которые выше температуры кипения использующегося растворителя, например, при температуре 140°С в случае толуола.
Вследствие того, что для реакции образования связи С-С используется очень небольшое количество палладиевого катализатора (который легко разлагается), катализатор предпочтительно дозировать в реакционную смесь в атмосфере инертного газа и в самом конце последовательности прибавления реагентов (стадия 2) на схеме реакций 1).
Соединения формулы II, в которой Х означает, например, галоген, известны или их можно получить по известным методикам, например, по реакции Сандмайера, из соответствующим образом замещенных аминов формулы VIII
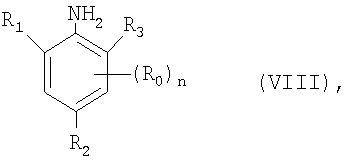
в которой R0, R1, R2, R3 и n являются такими, как это определено для формулы I, через соответствующие соли диазония.
Соединения формулы II, в которой Х означает, например, R10S(O)2O- или моно-, ди- или триарилметоксигруппу, можно получить по стандартным методикам из соответствующих фенолов формулы IX
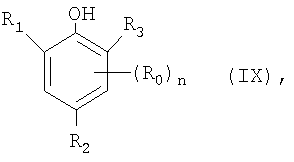
в которой R0, R1, R2, R3 и n являются такими, как это определено.
Замещенные анилины формулы VIII или известны, или их можно получить по известным методикам, как это описано, например, в ЕР-А-0362667, путем алкилирования анилинов с использованием олефинов.
Аналогичным образом, замещенные фенолы формулы IX или известны, или их можно получить по обычным методикам, например, из соответствующих анилинов VIII или их диазониевых солей с помощью так называемого "кипячения с фенолом".
На приведенной ниже схеме реакций 2 проиллюстрированы возможные способы получения соединений формулы II.
Схема реакций 2
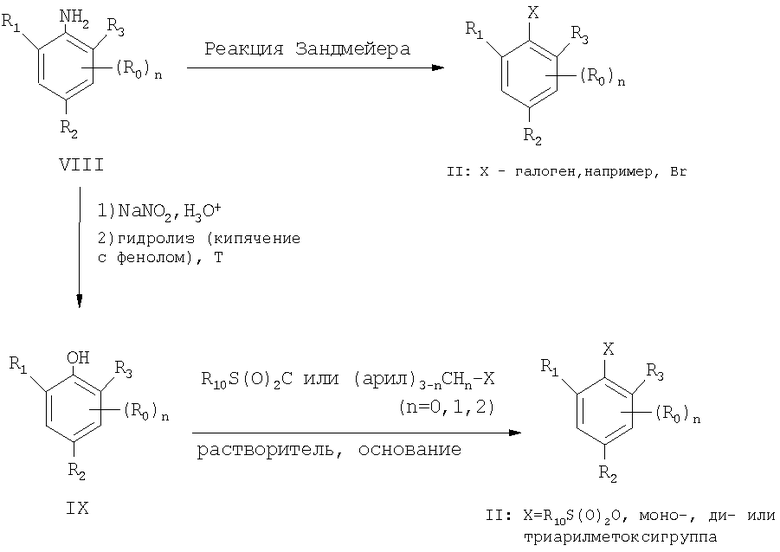
Замещенные арилдинитрилы формулы I используются в качестве предпочтительных промежуточных продуктов при получении замещенных производных 3-гидрокси-4-арил-5-оксопиразолина, которые известны, например, как гербициды, из WO 99/47525.
В приведенных ниже примерах настоящее изобретение проиллюстрировано дополнительно. Они не ограничивают настоящее изобретение.
Примеры получения:
Пример Р1: Получение динитрила 2-(2,6-диэтил-4-метилфенил)малоновой кислоты
В атмосфере азота 13,9 г динитрила малоновой кислоты при нормальном давлении и комнатной температуре прибавляют к 20,4 г порошкообразного гидроксида натрия в 240 г 1-метил-2-пирролидона. После прибавления 45,5 г 2-бром-1,3-диэтил-5-метилбензола реакционную смесь при перемешивании нагревают до 125°С. При этой температуре прибавляют смесь 1,3 г трифенилфосфина, 1,06 г имеющегося в продаже раствора палладий(II)хлорида в концентрированной хлористоводородной кислоте (20% содержания Pd соответствует 0,354 г хлорида Pd(II) и 0,708 г концентрированной хлористоводородной кислоты) и 97,6 г 1-метил-2-пирролидона. Перемешивание проводят в течение еще 3 ч при температуре от 125 до 130°С и 283 г разбавителя отгоняют при пониженном давлении (от 17 до 100 мбар). После охлаждения до комнатной температуры реакционную смесь прибавляют к 70 г воды. После прибавления 38 г концентрированной хлористоводородной кислоты (после этого устанавливается значение рН, меньшее, чем 5) осадившееся твердое вещество отфильтровывают и промывают с помощью 60 г воды. После сушки получают 42,4 г динитрила 2-(2,6-диэтил-4-метилфенил)малоновой кислоты (содержание 92,3%, выход 92,3%), обладающего температурой кипения, равной от 74 до 78°С.
Пример Р2: Получение динитрила 2-(2,6-диэтил-4-метилфенил)малоновой кислоты
В атмосфере азота 14,2 г динитрила малоновой кислоты при нормальном давлении и комнатной температуре прибавляют к смеси 48 г 50% водного раствора гидроксида натрия и 300 г 1-метил-2-пирролидона. Реакционную смесь нагревают до температуры от 60 до 100°С и 98 г разбавителя отгоняют при пониженном давлении (от 25 до 30 мбар). В атмосфере азота при нормальном давлении прибавляют 45,5 г 2-бром-1,3-диэтил-5-метилбензола. Затем реакционную смесь нагревают до 130°С при перемешивании. При этой температуре прибавляют смесь 0,26 г трифенилфосфина, 0,2 г имеющегося в продаже раствора палладий(II)хлорида в концентрированной хлористоводородной кислоте (20% содержания Pd соответствует 0,071 г хлорида Pd(II) и 0,142 г концентрированной хлористоводородной кислоты) и 19,5 г 1-метил-2-пирролидона. Смесь перемешивают при температуре от 125 до 130°С в течение еще 3 ч и затем 199 г разбавителя отгоняют при пониженном давлении (от 20 до 25 мбар) при температуре от 90 до 100°С. После охлаждения до комнатной температуры реакционную смесь прибавляют к 126 г воды. К ней прибавляют 4,5 г Hyflo (целит) и смесь перемешивают в течение 30 мин при 40°С, а затем фильтруют. Осадок на фильтре промывают с помощью 114 г воды. После прибавления к фильтрату 45 г 32% хлористоводородной кислоты (после этого устанавливается значение рН, меньшее, чем 5) осадившееся твердое вещество отфильтровывают и промывают с помощью 120 г воды. После сушки получают 42,8 г (содержание 97,3%, выход 98,0%) динитрила 2-(2,6-диэтил-4-метилфенил)малоновой кислоты, обладающего температурой кипения, равной от 79 до 82°С.
Пример Р3: Получение динитрила 2-фенилмалоновой кислоты
В атмосфере азота и при нормальном давлении 14 г динитрила малоновой кислоты, растворенного в 7 мл 1-метил-2-пирролидона, в течение 30 мин при температуре от 20 до 25°С при механическом перемешивании по каплям прибавляют к смеси 24,1 г гидроксида натрия (гранулы) с 300 мл 1-метил-2-пирролидона. Проводят откачку до давления, составляющего от 10 до 30 мбар, и при температуре от 80 до 100°С отгоняют примерно 100 мл разбавителя. После установления нормального давления прибавляют 32 г бромбензола и реакционную смесь нагревают до 125°С. При этой температуре прибавляют смесь 0,26 г трифенилфосфина, 0,21 г имеющегося в продаже раствора палладий(II)хлорида в концентрированной хлористоводородной кислоте (20% содержания Pd соответствует 0,071 г палладий(II)хлорида в 0,142 г концентрированной хлористоводородной кислоты) и 19,5 г 1-метил-2-пирролидона. Реакционную смесь перемешивают в течение 2-3 ч при температуре от 125 до 140°С, а затем при давлении от 20 до 60 мбар отгоняют еще 180 мл разбавителя. 3 г Hyflo и 150 мл воды прибавляют к остатку, который был охлажден до 50°С. Реакционную смесь энергично перемешивают в течение 10 мин и затем осветляют путем фильтрования через Hyflo. Затем фильтр промывают с помощью 120 мл воды (разделенной на 3 порции). Реакцию объединенных водных фаз доводят до рН <3 с использованием концентрированной хлористоводородной кислоты и затем экстрагируют с помощью трет-бутилметилового эфира (2×200 мл). Органические фазы один раз промывают водой (80 мл), сушат над сульфатом натрия и концентрируют. Получают 27,6 г (95%) динитрила 2-фенилмалоновой кислоты в виде масла, которое после выдерживания в течение некоторого времени кристаллизуется; температура плавления 66-68°С.
Следующие соединения получают аналогично примеру получения Р3:
Исходя из 35 г 4-бромтолуола, получают 31,2 г (99%) динитрила 2-(п-толил)малоновой кислоты, температура плавления 57-59°С;
исходя из 40,6 г 2,4,6-триметилбромбензола, получают 37,2 г (98%) динитрила 2-(2,4,5-триметилфенил)малоновой кислоты, температура плавления 91-93°С;
исходя из 37,8 г 2,6-диметилбромбензола, получают 34 г (96%) динитрила (2,6-диметилфенил)малоновой кислоты, температура плавления 83-85°С и,
исходя из 37,4 г 2-этилбромбензола, получают 25,6 г (72%) динитрила (2-этилфенил)малоновой кислоты, в виде масла, nD 20 1,518.
Пример Р4: Получение динитрила 2-(2,6-диэтил-4-метилфенил)малоновой кислоты
В атмосфере азота и при нормальном давлении 14 г (217 ммоль) динитрила малоновой кислоты, растворенного в 7 мл 1-метил-2-пирролидона, в течение 30 мин при температуре от 20 до 25°С при механическом перемешивании по каплям прибавляют к смеси 24,1 г (600 ммоль) гидроксида натрия (гранулы) с 300 мл 1-метил-2-пирролидона. Проводят откачку до давления, составляющего от 10 до 30 мбар, и при температуре от 80 до 100°С отгоняют 113 г разбавителя. После установления нормального давления прибавляют 48 г (содержание 94,9%; 200 ммоль) 2-бром-1,3-диэтил-5-метилбензола и реакционную смесь нагревают до 130°С. При этой температуре прибавляют смесь 0,26 г (1 ммоль) трифенилфосфина, 0,21 г имеющегося в продаже раствора палладий(II)хлорида в концентрированной хлористоводородной кислоте (20% содержания Pd соответствует 0,071 г (400 мкмоль) палладий(II)хлорида в 0,142 г концентрированной хлористоводородной кислоты) и 19,5 г 1-метил-2-пирролидона. Реакционную смесь перемешивают в течение 2-3 ч при температуре от 125 до 140°С, подавая под поверхность азот. Еще 165 г разбавителя отгоняют при давлении от 20 до 60 мбар. 2,3 г Hyflo и 150 мл воды прибавляют к остатку, который был охлажден до 50°С. Реакционную смесь энергично перемешивают в течение 10 мин и затем осветляют путем фильтрования через Hyflo. Затем фильтр промывают с помощью 55 мл воды. Объединенные водные фазы один раз экстрагируют с помощью 91 г толуола. Органическую фазу отделяют и отбрасывают. 30 г Смеси толуол/вода отгоняют из водной фазы при температуре от 20 до 70°С и давлении от 200 до 250 мбар. В приемник для перегонки при температуре от 20 до 25°С в течение 60-80 мин прибавляют 45,7 г 32% хлористоводородной кислоты и за это время продукт кристаллизуется и значение рН снижается до 4,0-4,5. Выполняют фильтрование отсасыванием, а затем промывают с помощью 120 мл воды (разделенной на 2 порции). Продукт сушат в вакуумной сушильной камере в течение 16 ч при давлении от 100 до 250 мбар. Получают 42,2 г (содержание 98,2%; выход 97,6%) динитрила 2-(2,6-диэтил-4-метилфенил)малоновой кислоты.
Пример Р5: Получение динитрила 2-(2,6-диэтил-4-метилфенил)малоновой кислоты
а) В атмосфере азота и при нормальном давлении 7 г динитрила малоновой кислоты, растворенного в 3,5 мл 1-метил-2-пирролидона, в течение 30 мин при температуре от 20 до 30°С при механическом перемешивании по каплям прибавляют к смеси 12 г гидроксида натрия (гранулы) с 150 мл диметилсульфоксида. Проводят откачку до давления, составляющего от 10 до 30 мбар, и 79,1 г разбавителя отгоняют при температуре от 80 до 100°С. После установления нормального давления прибавляют 24 г (содержание 94,9%) 2-бром-1,3-диэтил-5-метилбензола и реакционную смесь нагревают до 130°С. При этой температуре прибавляют смесь 0,13 г трифенилфосфина, 0,1 г имеющегося в продаже раствора палладий(II)хлорида в концентрированной хлористоводородной кислоте (20% содержания Pd соответствует 0,035 г палладий(II)хлорида в 0,071 г концентрированной хлористоводородной кислоты) и 9,6 г 1-метил-2-пирролидона. Реакционную смесь перемешивают в течение 2-3 ч при температуре от 125 до 140°С. Еще 59,5 г разбавителя отгоняют при давлении от 20 до 60 мбар. 1,5 г Hyflo и 75 мл воды прибавляют к остатку, который был охлажден до 50°С. Реакционную смесь энергично перемешивают в течение 10 мин и затем осветляют путем фильтрования через Hyflo. Затем фильтр промывают с помощью 50 мл воды. К фильтрату в течение 60-80 мин при температуре от 20 до 25°С прибавляют 23,3 г 32% хлористоводородной кислоты и за это время продукт кристаллизуется и значение рН снижается до 4,0-4,5. Выполняют фильтрование отсасыванием, а затем промывают с помощью 100 мл воды (разделенной на 2 порции). Продукт сушат в вакуумной сушильной камере в течение 16 ч при давлении от 100 до 250 мбар. Получают 20,6 г (содержание 97,9%; выход 95,1%) динитрила 2-(2,6-диэтил-4-метилфенил)малоновой кислоты.
б) В атмосфере азота и при нормальном давлении 14 г динитрила малоновой кислоты, растворенного в 7 мл 1-метил-2-пирролидона, в течение 30 мин при температуре от 20 до 30°С при механическом перемешивании по каплям прибавляют к смеси 24,1 г гидроксида натрия (гранулы) с 300 г N,N-диметилацетамида. Проводят откачку до давления, составляющего от 10 до 30 мбар, и при температуре от 80 до 100°С отгоняют 100 г разбавителя. После установления нормального давления прибавляют 48 г (содержание 94,9%) 2-бром-1,3-диэтил-5-метилбензола и реакционную смесь нагревают до 130°С. При этой температуре прибавляют смесь 0,26 г трифенилфосфина, 0,21 г имеющегося в продаже раствора палладий(II)хлорида в концентрированной хлористоводородной кислоте (20% содержания Pd соответствует 0,071 г палладий(II)хлорида в 0,142 г концентрированной хлористоводородной кислоты) и 19,5 г 1-метил-2-пирролидона. Реакционную смесь перемешивают в течение 2-3 ч при температуре от 125 до 140°С. Еще 181 г разбавителя затем отгоняют при давлении от 20 до 60 мбар. 2 г Hyflo и 150 мл воды прибавляют к остатку, который был охлажден до 50°С. Реакционную смесь энергично перемешивают в течение 10 мин и затем осветляют путем фильтрования через Hyflo. Затем фильтр промывают с помощью 50 мл воды. Объединенные водные фазы один раз экстрагируют с помощью 91 г толуола. Органическую фазу отделяют и отбрасывают. 30 г Смеси толуол/вода отгоняют из водных фаз при температуре от 20 до 70°С и давлении от 200 до 250 мбар. В приемник для перегонки при температуре от 20 до 25°С в течение 60 - 80 мин прибавляют 41,3 г 32% хлористоводородной кислоты и за это время продукт кристаллизуется и значение рН снижается до 4,0-4,5. Выполняют фильтрование отсасыванием, а затем промывают с помощью 120 мл воды (разделенной на 2 порции). Продукт сушат в вакуумной сушильной камере в течение 16 ч при давлении от 100 до 250 мбар. Получают 41,9 г (содержание 97,8%; выход 96,6%) динитрила 2-(2,6-диэтил-4-метилфенил)малоновой кислоты.
в) В атмосфере азота и при нормальном давлении 14 г динитрила малоновой кислоты, растворенного в 7 мл 1-метил-2-пирролидона, в течение 30 мин при температуре от 20 до 30°С при механическом перемешивании по каплям прибавляют к смеси 24,1 г гидроксида натрия (гранулы) с 300 г 1,3-диметилимидазолин-2-она. Проводят откачку до давления, составляющего от 10 до 30 мбар, и при температуре от 80 до 120°С отгоняют 136 г разбавителя. После установления нормального давления прибавляют 48 г (содержание 94,9%) 2-бром-1,3-диэтил-5-метилбензола и реакционную смесь нагревают до 130°С. При этой температуре прибавляют смесь 0,26 г трифенилфосфина, 0,21 г имеющегося в продаже раствора палладий(П)хлорида в концентрированной хлористоводородной кислоте (20% содержания Pd соответствует 0,071 г палладий(II)хлорида в 0,142 г концентрированной хлористоводородной кислоты) и 19,5 г 1-метил-2-пирролидона. Реакционную смесь перемешивают в течение 2-3 ч при температуре от 125 до 140°С. Еще 167 г разбавителя затем отгоняют при давлении от 20 до 60 мбар. 2 г Hyflo и 155 мл воды прибавляют к остатку, который был охлажден до 50°С. Реакционную смесь энергично перемешивают в течение 10 мин и затем осветляют путем фильтрования через Hyflo. Затем фильтр промывают с помощью 50 мл воды. Объединенные водные фазы один раз экстрагируют с помощью 91 г толуола. Органическую фазу отделяют и отбрасывают. 30 г Смеси толуол/вода отгоняют из водной фазы при температуре от 20 до 70°С и давлении от 200 до 250 мбар. В приемник для перегонки при температуре от 20 до 25°С в течение 60-80 мин прибавляют 42,9 г 32% хлористоводородной кислоты и за это время продукт кристаллизуется и значение рН снижается до 4,0-4,5. Выполняют фильтрование отсасыванием, а затем промывают с помощью 120 мл воды (разделенной на 2 порции). Продукт сушат в вакуумной сушильной камере в течение 16 ч при давлении от 100 до 250 мбар. Получают 41,4 г (содержание 97,5%; выход 95,2%) динитрила 2-(2,6-диэтил-4-метилфенил)малоновой кислоты.
Пример Р6: Получение динитрила 2-(2,6-диэтил-4-метилфенил)малоновой кислоты
В атмосфере азота 14,2 г динитрила малоновой кислоты прибавляют при нормальном давлении и комнатной температуре к смеси 67,3 г 50% раствора гидроксида калия и 300 мл 1-метил-2-пирролидона. Реакционную смесь нагревают до температуры от 60 до 100°С и 106 г разбавителя отгоняют при пониженном давлении (от 20 до 30 мбар). В атмосфере азота и при нормальном давлении прибавляют 45,5 г 2-бром-1,3-диэтил-5-метилбензола. Затем реакционную смесь нагревают до 120°С при перемешивании. При этой температуре прибавляют смесь 0,26 г трифенилфосфина, 0,2 г имеющегося в продаже раствора палладий(II)хлорида в концентрированной хлористоводородной кислоте (20% содержания Pd соответствует 0,071 г палладий(II)хлорида и 0,142 г концентрированной хлористоводородной кислоты) и 19,5 г 1-метил-2-пирролидона. Перемешивание проводят при температуре от 120 до 125°С в течение 1 ч, а затем повторно прибавляют смесь 0,26 г трифенилфосфина, 0,2 г имеющегося в продаже раствора палладий(II)хлорида в концентрированной хлористоводородной кислоте (20% содержания Pd соответствует 0,071 г палладий(II)хлорида и 0,142 г концентрированной хлористоводородной кислоты) и 19,5 г 1-метил-2-пирролидона. Реакционную смесь перемешивают в течение 3 ч при температуре от 120 до 125°С и затем еще 237 г разбавителя отгоняют при пониженном давлении (от 20 до 30 мбар) и при температуре от 80 до 120°С. После охлаждения реакционной смеси до 45°С прибавляют 100 мл толуола и 220 г воды и интенсивное перемешивание проводят в течение 15 мин. Эту двухфазную смесь переносят в делительную воронку для разделения. Органическую фазу отбрасывают. Водную фазу отделяют и 43,4 г вещества отгоняют при пониженном давлении (от 250 до 300 мбар) и при температуре от 70 до 110°С. В приемник для перегонки при температуре от 20 до 25°С в течение 60-80 мин прибавляют 48,5 г 32% хлористоводородной кислоты и за это время продукт кристаллизуется и значение рН снижается до 4,0-4,5. Выполняют фильтрование отсасыванием, а затем промывают с помощью 130 мл воды (разделенной на 2 порции). Продукт сушат в вакуумной сушильной камере в течение 16 ч при давлении от 100 до 250 мбар. Получают 37,2 г (содержание 97,7%; выход 85,7%) динитрила 2-(2,6-диэтил-4-метилфенил)малоновой кислоты.
Сравнительное исследование С1: Получение динитрила 2-(2,6-диэтил-4-метилфенил)малоновой кислоты с использованием гидрида натрия
В атмосфере азота и при нормальном давлении 4,8 г (120 ммоль) 60% гидрида натрия суспендируют в 60 мл гексана. Суспензию оставляют стоять. Отделяющийся растворитель сливают. К твердому веществу прибавляют 100 г 1-метил-2-пирролидона и в течение 30 мин при комнатной температуре прибавляют смесь 3,7 г (54 ммоль) динитрила малоновой кислоты и 4 г 1-метил-2-пирролидона. Смесь нагревают до 65°С и прибавляют 11,4 г (50 ммоль) 2-бром-1,3-диэтил-5-метилбензола. Затем реакционную смесь нагревают до 125-130°С и прибавляют смесь 0,065 г трифенилфосфина, 0,4 г имеющегося в продаже раствора палладий(II)хлорида в концентрированной хлористоводородной кислоте (20% содержания Pd соответствует 0,018 г палладий(II)хлорида в 0,035 г концентрированной хлористоводородной кислоты) и 4,8 г 1-метил-2-пирролидона. Затем реакционную смесь перемешивают в течение 75 мин при температуре от 120 до 130°С. Повторно прибавляют смесь 0,13 г трифенилфосфина, 0,1 г имеющегося в продаже раствора палладий(II)хлорида в концентрированной хлористоводородной кислоте (20% содержания Pd соответствует 0,035 г палладий(II)хлорида в 0,071 г концентрированной хлористоводородной кислоты) и 9,7 г 1-метил-2-пирролидона. Затем реакционную смесь перемешивают в течение 3 ч при температуре от 120 до 130°С. После охлаждения смеси до комнатной температуры прибавляют 1,3 г воды. 100 мл растворителя затем отгоняют при пониженном давлении (от 20 до 25 мбар) при температуре от 70 до 110°С. К остатку прибавляют 95 г воды и 100 мл толуола. Интенсивное перемешивание проводят в течение 30 мин. Эту двухфазную смесь разделяют в делительной воронке. Органическую фазу отбрасывают. Водную фазу отделяют и 30 г вещества отгоняют при пониженном давлении (от 100 до 150 мбар) и при температуре от 40 до 60°С. В приемник для перегонки при температуре от 20 до 25°С в течение 60-80 мин прибавляют 7,7 г 32% хлористоводородной кислоты за это время продукт кристаллизуется и значение рН снижается до 4,0-4,5. Выполняют фильтрование отсасыванием, а затем промывают с помощью 40 мл воды (разделенной на 2 порции). Продукт сушат в вакуумной сушильной камере в течение 16 ч при давлении от 100 до 250 мбар. Получают 7,7 г (содержание 98,6%; выход 72%) динитрила 2-(2,6-диэтил-4-метилфенил)малоновой кислоты.
Сравнительное исследование С2: Получение динитрила 2-(2,6-диэтил-4-метилфенил)малоновой кислоты с использованием карбоната натрия
В атмосфере азота и при нормальном давлении 14 г динитрила малоновой кислоты, растворенного в 7 мл 1-метил-2-пирролидона, в течение 30 мин при температуре от 20 до 25°С при механическом перемешивании по каплям прибавляют к смеси 64 г карбоната натрия с 200 мл 1-метил-2-пирролидона. Реакционную смесь нагревают до 100°С и прибавляют 45,5 г 2-бром-1,3-диэтил-5-метилбензола, а затем смесь нагревают до 120°С. При этой температуре прибавляют смесь 0,26 г трифенилфосфина, 0,21 г имеющегося в продаже раствора палладий(II)хлорида в концентрированной хлористоводородной кислоте (20% содержания Pd соответствует 0,071 г палладий(II)хлорида в 0,142 г концентрированной хлористоводородной кислоты) и 19,5 г 1-метил-2-пирролидона. Реакционную смесь перемешивают в течение от 2 до 3 ч при температуре от 125 до 140°С. Газовая хроматография образца (1 мл реакционной смеси подвергают распределению между 2 мл 1 н. хлористоводородной кислоты и 2 мл трет-бутилметилового эфира) показывает, что продукт (динитрил 2-(2,6-диэтил-4-метилфенил)малоновой кислоты) не образовался.
Сравнительное исследование С3: Получение динитрила 2-(2,6-диэтил-4-метилфенил)малоновой кислоты с использованием этанолята натрия
21,5 г Этанолята натрия и 150 г 1-метил-2-пирролидона механически перемешивают в атмосфере азота при нормальном давлении. К ним порциями прибавляют 7,3 г динитрила малоновой кислоты. 58 г Растворителя отгоняют при температуре от 100 до 120°С при пониженном давлении (от 20 до 30 мбар). В атмосфере азота и при нормальном давлении при 110°С прибавляют 22,7 г 2-бром-1,3-диэтил-5-метилбензола. Реакционную смесь нагревают до 125°С. При этой температуре прибавляют смесь 0,13 г трифенилфосфина, 0,1 г имеющегося в продаже раствора палладий(II)хлорида в концентрированной хлористоводородной кислоте (20% содержания Pd соответствует 0,035 г палладий(II)хлорида в 0,071 г концентрированной хлористоводородной кислоты) и 9,6 г 1-метил-2-пирролидона. Реакционную смесь нагревают при температуре от 120 до 130°С в течение 1 ч. Повторно прибавляют смесь 0,13 г трифенилфосфина, 0,1 г имеющегося в продаже раствора палладий(II)хлорида в концентрированной хлористоводородной кислоте (20% содержания Pd соответствует 0,035 г палладий(II)хлорида в 0,071 г концентрированной хлористоводородной кислоты) и 9,6 г 1-метил-2-пирролидона. Реакционную смесь перемешивают в течение 2 ч при температуре от 120 до 130°С. Газовая хроматография образца (1 мл реакционной смеси подвергают распределению между 2 мл 1 н. хлористоводородной кислоты и 2 мл трет-бутилметилового эфира) показывает, что продукт (динитрил 2-(2,6-диэтил-4-метилфенил)малоновой кислоты) не образовался.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ГЕРБИЦИДНЫХ ПРОИЗВОДНЫХ И ПРОМЕЖУТОЧНОЕ СОЕДИНЕНИЕ | 2000 |
|
RU2244715C2 |
| МОЛЕКУЛА, ПЕСТИЦИДНАЯ КОМПОЗИЦИЯ НА ЕЕ ОСНОВЕ (ВАРИАНТЫ) И СПОСОБ ПРИМЕНЕНИЯ МОЛЕКУЛЫ (ВАРИАНТЫ) | 2010 |
|
RU2543806C2 |
| 6-АМИНО-2-ЗАМЕЩЕННЫЕ-5- ВИНИЛСИЛИЛПИРИМИДИН-4-КАРБОНОВЫЕ КИСЛОТЫ И СЛОЖНЫЕ ЭФИРЫ И 4-АМИНО-6-ЗАМЕЩЕННЫЕ-3-ВИНИЛСИЛИЛПИРИДИН-ПИКОЛИНОВЫЕ КИСЛОТЫ И СЛОЖНЫЕ ЭФИРЫ КАК ГЕРБИЦИДЫ | 2012 |
|
RU2556000C2 |
| ЦИКЛИЧЕСКИЕ ДИОНЫ В КАЧЕСТВЕ ГЕРБИЦИДНЫХ СОЕДИНЕНИЙ | 2020 |
|
RU2822391C2 |
| ГЕРБИЦИДНЫЕ ПИРИДИНО-/ПИРИМИДИНОТИАЗОЛЫ | 2015 |
|
RU2720093C2 |
| ГЕРБИЦИДНЫЕ ЦИКЛОГЕКСАНДИОНОВЫЕ ПРОИЗВОДНЫЕ | 2020 |
|
RU2830286C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИКЛИЧЕСКИХ ДИКЕТОНОВ | 2005 |
|
RU2384562C2 |
| ГЕРБИЦИДЫ | 2017 |
|
RU2739914C2 |
| СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ ОПОСРЕДОВАННЫХ КОМПЛЕМЕНТОМ НАРУШЕНИЙ | 2015 |
|
RU2703995C2 |
| ГЕРБИЦИДНЫЕ СОЕДИНЕНИЯ | 2020 |
|
RU2839723C2 |
Изобретение относится к способу получения соединения формулы I
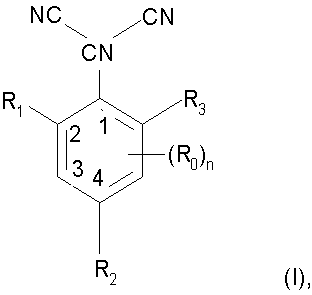
в которой R1, R2, R3 независимо один от другого обозначают водород или С1-С6алкил и n равно 0, включающий реакцию соединения формулы II
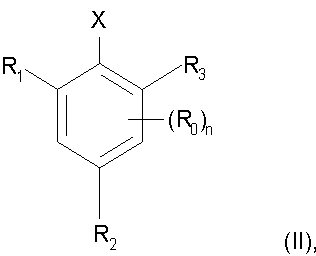
в которой R0, R1, R2, R3 и n являются такими, как определено выше, а X обозначает уходящую группу с динитрилом малоновой кислоты в инертном разбавителе при температуре, равной от 0 до 250°С, в присутствии палладиевого катализатора и основания, отличающийся тем, что в качестве основания используют гидроксид щелочного металла или смесь гидроксидов щелочных металлов, а в качестве палладиевого катализатора используют палладий(II)дигалогенид, палладий(II)ацетат, палладий(II)сульфат, бис(трифенилфосфин)палладий(II)дихлорид, бис(трициклопентилфосфин) палладий(II)дихлорид, бис(трициклогексилфосфин)палладий(II)дихлорид, бис(дибензилиденацетон)палладий(0) или тетракис(трифенилфосфин) палладий(0). Способ позволяет увеличить выход и степень чистоты получаемых динитрилов фенилмалоновой кислоты. 12 з.п. ф-лы.
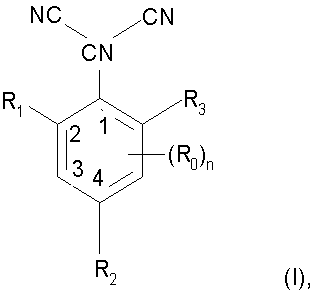
в которой R1, R2, R3 независимо один от другого обозначают водород или С1-С6алкил,
и n равно 0,
включающий реакцию соединения формулы II
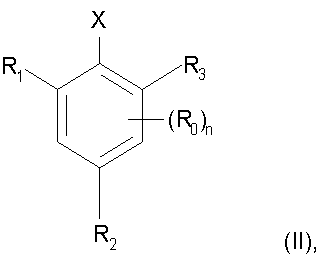
в которой R0, R1, R2, R3 и n являются такими, как определено выше, а X обозначает уходящую группу, с динитрилом малоновой кислоты в инертном разбавителе при температуре, равной от 0° до 250°С, в присутствии палладиевого катализатора и основания, отличающийся тем, что в качестве основания используют гидроксид щелочного металла или смесь гидроксидов щелочных металлов, а в качестве палладиевого катализатора используют палладий(II)дигалогенид, палладий(II)ацетат, палладий(II)сульфат, бис(трифенилфосфин)палладий(II)дихлорид, бис(трициклопентилфосфин)палладий(II)дихлорид, бис(трициклогексилфосфин)палладий(II)дихлорид, бис(дибензилиденацетон)палладий(0) или тетракис(трифенилфосфин)палладий(0).
| JP 2000281636 А, 10.10.2000 | |||
| Способ безостаточной переработки сланца на бытовой газ, ароматизированное искусственное жидкое топливо или легкую смолу | 1948 |
|
SU78712A1 |
| JP 60197650 А, 07.10.1985 | |||
| RU 99105594 А, 20.01.2001. | |||
Авторы
Даты
2008-05-20—Публикация
2003-12-04—Подача