Изобретение относится к медицине, а именно к клинической иммунологии.
Проблема подбора специализированных продуктов детского питания (СПДП) у детей актуальна в связи с тем, что практически все дети нуждаются в прикорме, а некоторые из них и в замене грудного вскармливания искусственным. При этом у 15% детей в возрасте до 1 года, получающих СПДП, отмечены различные сомато-аллергические реакции (САР) - атопический дерматит, гастро-интестинальный, метаболический синдромы и др.
В настоящее время существует широкий ассортимент СПДП, который постоянно пополняется. Известно, что способность вызывать аллергические реакции обусловлена главным образом белковыми компонентами пищевых продуктов (В кн.: «Лечебное питание детей с пищевой аллергией». Пособие для врачей. 3-е изд., переработанное и дополненное под ред. проф. В.А.Ревякиной и проф. Т.Э.Боровик. М.:, Издательский Дом «Династия», 2005, с.4-6), обладающими свойствами антигенов. Антигенами называют химические соединения, способные вызывать иммунный ответ. В свою очередь, аллергенами называют такие антигены, которые способны вызывать аллергические реакции. Поскольку практически все белковые компоненты СПДП способны вызывать аллергические реакции, в настоящем описании слова антиген и аллерген будут использоваться как синонимы. Наряду с продуктами, приготовленными на основе нативных белков с практически неизмененными физико-химическими свойствами (белки цельного молока, сыворотки молока, казеин и др.), производятся также продукты, в которых нативные белки целенаправленно подвергают различным физико-химическим воздействиям (ферментативный гидролиз разной степени, ультрафильтрация, термическая обработка, ультрафиолетовое облучение и др.), изменяющим их антигенные свойства, что приводит к снижению их аллергенности. Эти продукты получили название лечебных и лечебно-профилактических СПДП.
Однако даже при высокой степени ферментативного гидролиза в этих СПДП обнаруживают высокомолекулярные белковые компоненты, сохраняющие антигенные свойства исходных белков и способные вызывать аллергические реакции у сенситизированных детей. Следует отметить также, что входящие в состав СПДП разнообразные небелковые ингредиенты (жиры, липиды, углеводы, эмульгаторы, загустители и др.) могут содержать в виде примесей способные вызывать САР белковые компоненты тех природных продуктов, из которых они были приготовлены. Разнообразие ингредиентного состава и технологических процессов обработки определяют разную переносимость ребенком различных СПДП (даже если состав их белковых компонентов сходен). Поэтому, основываясь на компонентном составе конкретного СПДП, приводимом фирмой-изготовителем, часто не удается предсказать переносимость данного продукта ребенком. Это в значительной мере осложняет работу практического врача при индивидуальном подборе питания ребенку.
Все это указывает на необходимость разработки объективного, надежного и безопасного способа диагностики индивидуальной переносимости ребенком конкретного вида СПДП.
Известен способ диагностики риска развития САР при применении СПДП путем проведения клинического исследования - сбор аллергологического анамнеза, ведение пищевого дневника, наблюдение и осмотр пациента (В кн.: «Лечебное питание детей с пищевой аллергией». Пособие для врачей. 3-е изд., переработанное и дополненное под редакцией проф. В.А.Ревякиной и проф. Т.Э.Боровик. М.: Издательский Дом «Династия», 2005, с.10).
Недостатком этого способа является субъективная оценка состояния пациента, зависящая от квалификации врача, полноты информации, а также необходимость длительного срока наблюдений.
Известен способ диагностики риска развития САР при применении СПДП путем проведения кожных тестов и провокационных проб с пищевыми аллергенами (прик-тест, скарификация или внутрикожное введение) - в кн.: «Лечебное питание детей с пищевой аллергией». Пособие для врачей. 3-е изд., переработанное и дополненное под редакцией проф. В.А.Ревякиной и проф. Т.Э.Боровик. М.: Издательский Дом «Династия», 2005, с.10-12.
Недостатками этого способа являются невозможность проведения кожных проб в острой стадии заболевания, необходимость условий специализированного медицинского учреждения, ограничения по возрасту (с 3-х лет), возможность провоцирования САР после проб (В кн.: «Клиническая аллергология», Руководство для практических врачей. Под ред. акад. РАМН проф. Р.М.Хаитова, М.: МЕДпресс-информ, 2002, с.148).
Наиболее близким к предлагаемому решению является способ in vitro диагностики риска развития САР при применении СПДП, основанный на иммунологической реакции антиген-антитело, с определением концентрации специфических антител классов IgG и IgE, иммунореактивных по отношению к отдельным нативным белковым компонентам пищевых продуктов, с помощью методов иммунохимического анализа (PACT, ИФА, иммунофлуоресцентный анализ, иммуноблоттинг и др.) - к белкам коровьего молока (бета-лактоглобулин, альфа-лактоальбумин, бычий сывороточный альбумин, казеин и др.), куриного яйца (овальбумин, овомукоид, лизоцим, фосвитин и др.), сои (глицинии, бета-конглицинин и др.), пшеницы (глиадин, глютенин и др.) и др. (В кн.: «Лечебное питание детей с пищевой аллергией». Пособие для врачей. 3-е изд., переработанное и дополненное под ред. проф. В.А.Ревякиной и проф. Т.Э.Боровик. М.: Издательский Дом «Династия», 2005, с.12).
Недостатками этого способа является невозможность оценки индивидуальной переносимости конкретного СПДП в целом, имеющего сложный многокомпонентный состав и подвергшегося при изготовлении различным видам технологической обработки, в том числе и таким, которые изменяют физико-химические и антигенные свойства компонентов СПДП.
Наиболее близкой к предлагаемой тест-системе является тест-система, производимая фирмой "Dr.Fooke" (Германия), предназначенная для диагностики пищевой аллергии и непереносимости ряда пищевых продуктов и представляющая собой набор аллергенов, выделенных из натуральных пищевых продуктов и иммобилизованных на твердом носителе (полистироловые микропланшеты, полимерные диски), позволяющая определять методом ИФА в крови пациента антитела класса IgG и IgE, специфичные в отношении пищевых антигенов (Аллергодиагностика in vitro компании Dr.Fooke Laboratorien GmbH. Layout©Blechmann miblArtwork, 2004, Germany).
Недостатком этой тест-системы является то, что она предназначена для диагностики пищевой аллергии и непереносимости натуральных пищевых продуктов у лиц в возрасте старше шести лет и не позволяет выявлять пищевую непереносимость, аллергические реакции и риск их возникновения при применении СПДП - многокомпонентных смесей, содержащих технологически переработанные пищевые продукты со специально измененными физико-химическими и антигенными свойствами, применяемых в основном для питания детей в возрасте до 3 лет, в результате чего эта тест-система не может быть использована для выявления аллергических реакций и пищевой непереносимости конкретных видов СПДП.
Таким образом, в настоящее время отсутствуют способы и средства (тест-системы, наборы реагентов и др.) in vitro диагностики риска развития САР при применении конкретных СПДП, в частности пищевых смесей лечебного и лечебно-профилактического назначения, в которых белковые компоненты были подвергнуты в процессе технологической обработки различным физико-химическим воздействиям, изменяющим их антигенные свойства с целью снижения аллергенности.
Техническим результатом предлагаемого решения является разработка тест-системы (рабочее название «Лакттест»), позволяющей диагностировать с большей точностью и надежностью риск развития САР при применении конкретных видов СПДП и дающей возможность индивидуальной оценки переносимости конкретного продукта в целом при отсутствии побочных явлений и осложнений для испытуемого.
Этот результат достигается тем, что для выявления специфических антител классов IgG и IgE используют тест-систему, содержащую набор антигенов - суммарные белково-пептидные фракции, выделенные методом экстракции из СПДП различных типов, а именно: из лечебных (высокогидролизованных) смесей, из профилактических смесей (частично-гидролизованных молочных и на основе растительных белков), из молочных смесей на основе нативных белков и из грудного молока. Способы (экстракции, применяемые в биомедицинских исследованиях, предназначены для выделения определенного набора веществ из конкретного исходного материала и состоят из нескольких стадий, отличающихся составом и свойствами растворов (рН, ионная сила, наличие комплексонов, детергентов и др.), условиями проведения процесса (продолжительность операций, температура, перемешивание, диспергирование и др.). Существует определенный набор применяемых приемов и способов, из которых в каждом отдельном случае складывается конкретный метод экстракции. Метод экстракции, разработанный для получения входящих в состав предлагаемой тест-системы антигенов, по совокупности используемых процедур, их последовательности, параметров их проведения, состава используемых растворов уникален. Риск развития сомато-аллергических реакций в отношении конкретного вида СПДП диагностируют при увеличении концентрации специфических IgG более 10 мкг/мл и/или при выявлении специфических IgE в концентрации выше 5 нг/мл.
Способ осуществляют следующим образом:
Способ, основанный на проведении иммунологической реакции антиген-антитело in vitro с помощью метода ИФА, включает следующие этапы:
1. Изготовление тест-системы «ЛАКТТЕСТ».
2. Получение сыворотки крови ребенка.
3. Проведение иммуно-ферментного анализа с помощью тест-системы «ЛАКТТЕСТ» для выявления специфических IgG и IgE.
4. Оценка и интерпретация полученных данных.
1. Изготовление тест-системы «ЛАКТТЕСТ».
Тест-система «ЛАКТТЕСТ» представляет собой набор иммобилизованных на твердом носителе антигенов - суммарных белково-пептидных фракций, выделенных из СПДП трех типов, каждый из которых представлен на отдельной панели.
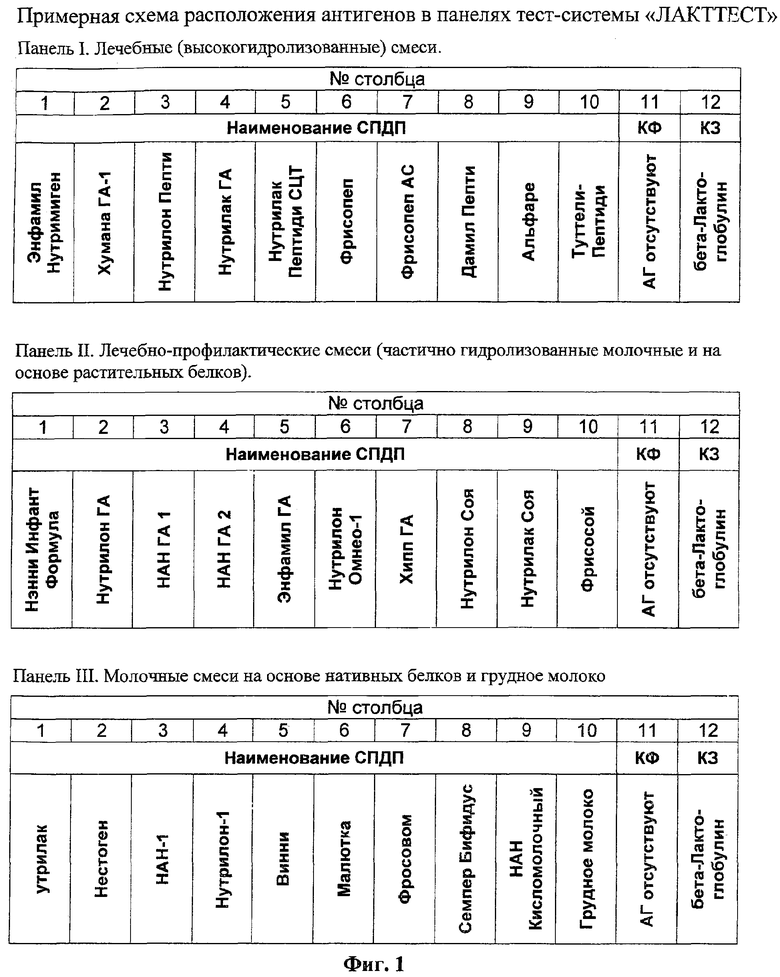
Первая панель содержит антигены из любых лечебных (высокогидролизованных) смесей, например - Энфамил Нутрамиген, Хумана ГА-1, Нутрилон Пепти, Нутрилак ГА, Нутрилак Пептиди СЦТ, Фрисопеп, Фрисопеп АС, Дамил Пепти, Альфаре, Туттели-Пептиди.
Вторая панель содержит антигены из любых лечебно-профилактических смесей (частично-гидролизованных молочных и на основе растительных белков), например - Нэнни Инфант Формула, Нутрилон ГА, НАН ГА 1, НАН ГА 2, Энфамил ГА, Нутрилон Омнео-1, Хипп ГА, Нутрилон Соя, Нутрилак Соя, Фрисосой.
Третья панель содержит антигены из любых молочных смесей на основе нативных белков, например - Нутрилак, Нестоген, НАН-1, Нутрилон-1, Винни, Малютка, Фрисовом, Семпер Бифидус, НАН Кисломолочный и из грудного молока.
1.1. Выделение суммарных белково-пептидных фракций из отдельных видов СПДП и грудного молока.
Суммарные белково-пептидные фракции выделяют из СПДП по следующей схеме:
- обезжиривание образца СПДП (экстракция жиров органическими растворителями);
- высушивание;
- экстракция белково-пептидных компонентов водно-солевым буферным раствором;
- центрифугирование;
- количественное определение концентрации белково-пептидных компонентов.
К навеске сухой смеси СПДП (1 г) добавляют 10 мл н-гексана и в течение 60 мин. встряхивают при комнатной температуре. Затем центрифугируют 15 мин при 1500 g. Надосадочную жидкость удаляют, а осадок дважды обрабатывают гексаном (порциями по 10 мл), как описано выше. Затем к осадку добавляют 10 мл диэтилового эфира, встряхивают в течение 60 мин при комнатной температуре и переносят в стеклянную воронку на стекловолокнистый фильтр. Диэтиловый эфир отфильтровывают, осадок дважды промывают диэтиловым эфиром (порциями по 10 мл). Обезжиренный осадок высушивают при 35-40°С до исчезновения запаха эфира.
Белково-пептидные компоненты экстрагируют из обезжиренной смеси водно-солевым буферным раствором (ВСБР) следующего состава: 0,15 М NaCl, 10 мМ натрий-фосфатный буфер, 10 мМ 2-меркаптоэтанол, 1 мМ ЭДТА·Na2, 0,05% азид натрия, рН 7,6. Для этого к обезжиренной смеси добавляют ВСБР (из расчета - 10 мл ВСБР на 1 г обезжиренной смеси), гомогенизируют в стеклянном шариковом гомогенизаторе Даунса, переносят в полипропиленовую пробирку и перемешивают в течение 16-18 часов при 4-8°С путем переворачивания пробирки. Нерастворимый материал отделяют центрифугированием в течение 45 мин при 250000 g и температуре 4-8°С. В надосадочной жидкости определяют концентрацию белка и используют ее в качестве препарата суммарных белково-пептидных компонентов смеси.
Для получения препарата белково-пептидных компонентов грудного молока объединяют равные части грудного молока пяти здоровых кормящих женщин. Полученную смесь центрифугируют 30 мин. при 25000 g и температуре 4-8°С. Флотировавший жировой слой удаляют и аккуратно отбирают находящуюся под ним водную фазу, так, чтобы в нее не попали частицы осадка. Полученную таким образом водную фазу используют в качестве препарата суммарных белково-пептидных антигенов грудного молока.
Концентрацию белково-пептидных компонентов определяют с помощью биуретовой реакции с использованием в качестве стандарта триглицина и детектированием при длине волны 540 нм.
1.2. Сенсибилизация иммунологических планшетов.
Каждую панель антигенов СПДП изготавливают в виде двух идентичных иммунологических планшетов: первый планшет - для определения специфических IgG, второй - для определения специфических IgE.
Стандартные 96-луночные (12×8) плоскодонные планшеты для иммуноферментного анализа сенсибилизируют антигенами суммарных белково-пептидных фракций, выделенных из СПДП и грудного молока: два планшета первой панели - антигенами из лечебных (высокогидролизованных) смесей, например - Энфамил Нутрамиген, Хумана ГА-1, Нутрилон Пепти, Нутрилак ГА, Нутрилак Пептиди СЦТ, Фрисопеп, Фрисопеп АС, Дамил Пепти, Альфаре, Туттели-Пептиди; два планшета второй панели - антигенами из лечебно-профилактических (частично-гидролизованных молочных смесей и смесей на основе растительных белков), например - Нэнни Инфант Формула, Нутрилон ГА, НАН ГА 1, НАН ГА 2, Энфамил ГА, Нутрилон Омнео-1, Хипп ГА, Нутрилон Соя, Нутрилак Соя, Фрисосой; два планшета третьей панели - антигенами из молочных смесей на основе нативных белков, например - Нутрилак, Нестоген, НАН-1, Нутрилон-1, Винни, Малютка, Фрисовом, Семпер Бифидус, НАН Кисломолочный и из грудного молока.
Примерная схема сенсибилизации лунок планшетов приведена на Фиг.1. В каждом планшете антигенами отдельного вида СПДП сенсибилизируют 8 вертикально расположенных друг над другом (в столбец) лунок - всего 10 столбцов (№1-10). Столбец №11 предназначен для контроля фонового окрашивания (КФ). Лунки столбца №12, предназначенные для построения калибровочной зависимости (КЗ), сенсибилизируют бета-лактоглобулином коровьего молока. Каждый планшет предназначен для анализа сывороток четырех пациентов в дупликатах.
Препараты суммарных белково-пептидных фракций разводят 0,05 М карбонатным буфером (КБ) рН 9,0-10,0 так, чтобы концентрация белка составляла 1-10 мкг/мл. В лунки столбцов №1-10 планшета вносят по 100 мкл растворов белково-пептидных антигенов СПДП, в лунки столбца №11 (КФ) - по 100 мкл КБ, в лунки столбца №12 (КЗ) - по 100 мкл раствора бета-лактоглобулина (1 мг/мл в КБ).
Планшеты инкубируют в течение 16-18 часов при 2-4°С. После этого растворы антигенов удаляют из лунок и добавляют в них по 300 мкл раствора блокирующего агента. В качестве блокирующего агента предпочтительно использовать препараты, содержащие смесь низкомолекулярных синтетических полипептидов, типа MegaBloc™3. Концентрация блокирующего агента - 0,5-1,0% или - в соответствии с рекомендациями производителя. Планшеты инкубируют с блокирующим агентом 1-2 часа при 37°С.
Затем лунки планшета промывают несколькими порциями фосфатно-солевого буферного раствора (ФСБР, например, 0.15 М NaCl, 10 мМ фосфатный буфер, рН 7,2-7,4), содержащего 0,05-0,1% детергента (например - Твин-20™).
2. Получение сыворотки крови ребенка.
Для получения сыворотки крови у детей берут венозную кровь (у грудных детей - обычно из лобной, височной или яремной вены) в количестве до 1 мл. Препараты сыворотки готовят в соответствии с рекомендациями, приведенными в Кн.: Обеспечение качества лабораторных исследований. Преаналитический этап. Справочное пособие. Под ред. В.В.Меньшикова. М.: Лабинформ, 1999, с.263-264.
3. Проведение иммуно-ферментного анализа с помощью тест-системы «ЛАКТТЕСТ» для выявления специфических IgG и IgE.
3.1. Приготовление для анализа исследуемых сывороток (ИС) и калибровочных образцов (КО).
- в качестве калибратора для определения специфических IgG и IgE используют сыворотку донора с установленным референсным методом высоким содержанием IgG и IgE, специфических в отношении бета-лактоглобулина (БЛГ);
- для определения специфических IgG сыворотку-калибратор разводят ФСБР таким образом, чтобы в КО2, КО3, КО4 содержалось соответственно 20, 50 и 100 мкг/мл анти-БЛГ IgG. В качестве КО1 используют сыворотку здорового донора, не содержащую анти-БЛГ IgG, разведенную ФСБР в такое же количество раз, как и КО2;
- для определения специфических IgG сыворотку-калибратор разводят ФСБР таким образом, чтобы в КО2, КО3, КО4 содержалось соответственно 10, 20 и 50 нг/мл анти-БЛГ IgE. В качестве КО1 используют сыворотку здорового донора, не содержащую анти-БЛГ IgE, разведенную ФСБР в такое же количество раз, как и КО2;
- для определения специфических IgG ИС и соответствующие КО разводят ФСБР в отношении 1:200-1:400,
- для определения специфических IgE ИС и соответствующие КО разводят ФСБР в отношении 1:2-1:5.
3.2. Внесение ИС и КО в лунки планшетов:
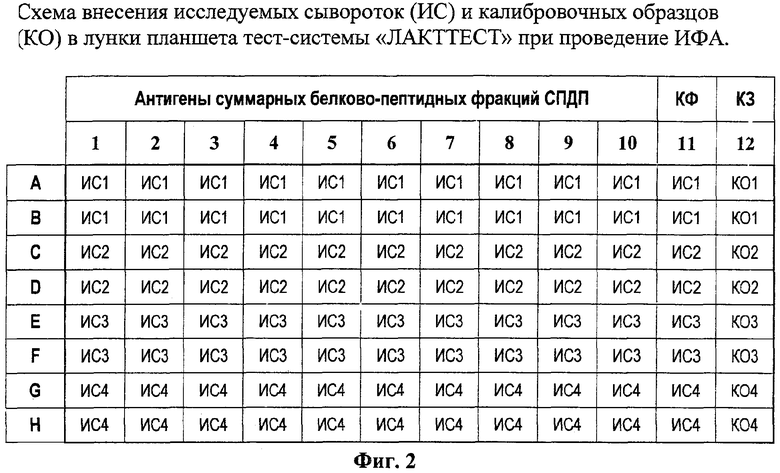
- в лунки планшета вносят по 100 мкл разведенных ИС и КО в дупликатах в соответствии со схемой, приведенной на Фиг.2;
- планшеты инкубируют 1 час при 37°С.
3.3 Планшет промывают 3-5 раз порциями ФСБР, содержащего 0,05-0,1% Твин-20™.
3.4 Визуализация реакции АГ-АТ:
- исходный раствор конъюгата моноклональных антител к иммуноглобулинам IgG, IgE человека с пероксидазой хрена (или иным ферментом) разводят в необходимое число раз (в зависимости от его активности) ФСБР;
- раствор конъюгата вносят во все лунки планшета;
- планшет инкубируют 60-90 мин при 37°С. После этого коньюгат удаляют из лунок и планшеты промывают 3-5 раз порциями ФСБР, содержащего 0,05-0,1% Твин-20™;
- после этого для визуализации реакции АГ-АТ во все лунки планшета вносят раствор хромогенного субстрата, например, 0,005% 3,3′,5,5′-тетраметилбензидин (ТМБ), 0,005-0,01% перекись водорода в 0,1М цитрат-фосфатном буфере, рН 4,5-5,0 (в случае применения пероксидазных конъюгатов). Планшет инкубируют 15-20 мин при комнатной температуре в темноте.
3.5. По достижению оптимального уровня окрашивания (обычно через 10-20 мин) реакцию останавливают добавлением стоп-раствора (например, 2 N серной кислоты).
3.6. Оптическую плотность (ОП) раствора в лунке регистрируют фотометрически с помощью ИФА-фотометра с детекцией при длине волны 450 нм (при использовании в качестве хромогена ТМБ).
3.7. Обработка полученных данных:
- вычисляют среднее арифметическое значение ОП для дубликатов проб каждого КО-ОПKOi ср., где i - номер калибровочной пробы;
- используя значения (ОПKOi ср. - ОПКO1 ср.), строят калибровочную зависимость;
- вычисляют среднее арифметическое значение ОП для дубликатов проб ИС (ОПИС ср.) и соответствующих проб КФ (ОПКФ ср.);
- используя значения (ОПИС ср. - ОПКФ ср.), по калибровочной зависимости определяют концентрацию специфических антител к антигенам тест-системы.
4. Оценка и интерпретация полученных данных.
4.1 Если концентрация в сыворотке специфических IgG к данному виду СПДП не превышает 10 мкг/мл, а концентрация специфических IgE к этому виду СПДП не превышает 5 нг/мл, иммунореактивность сыворотки к этому виду СПДП считают нормальной, риск развития САР при применении конкретного вида СПДП отсутствует.
4.2 При увеличении концентрации специфических IgG более 10 мкг/мл и (или) при выявлении специфических IgE в концентрации выше 5 нг/мл к данному виду СПДП диагностируют риск развития САР в отношении этого вида СПДП.
ПРИМЕРЫ
Пример 1
Пациент Б., Возраст: 6 мес., Пол: Жен., Амбулаторная карта № 3.
Поступил на обследование в Медицинский научно-исследовательский центр «МЕДИАН» 16.01.2006
Клинический диагноз:
основной: атопический дерматит;
сопутствующий: дисфункция ЖКТ, дисбактериоз кишечника.
Из анамнеза известно, что практически сразу после рождения (с 2 нед.) ребенок находился на искусственном вскармливании. Через 3 недели после введения в рацион питания смеси «Малютка» у ребенка появились кожные высыпания на лице, а затем - по всему телу, в связи с чем участковым педиатром была рекомендована замена молочной смеси.
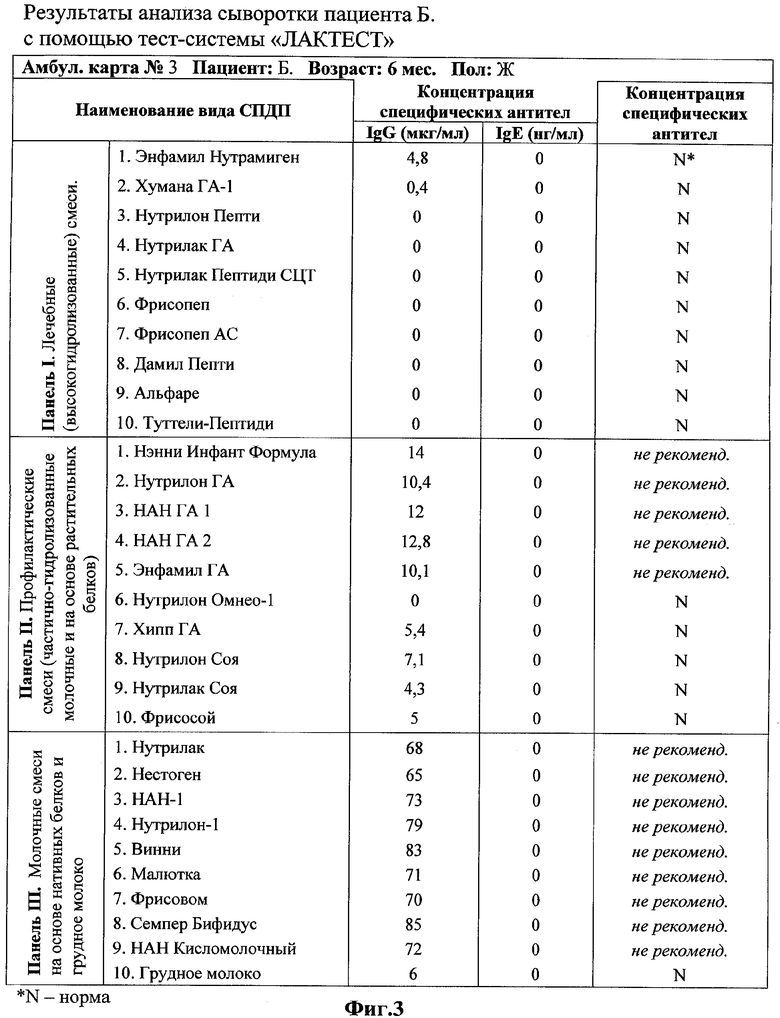
Ребенок получал следующие продукты Нэнни Инфант Формула, Нутрилон Пепти ТСЦ, Энфамил Нутрамиген, Фрисопеп. Выраженность дерматита существенно уменьшилась, но ребенок стал более беспокойным, хуже прибавлял в весе. В связи с этим ребенок был направлен на иммунологические исследования с использованием тест-системы «ЛАКТТЕСТ». Результаты исследования отражены на Фиг.3.
Исследования выявили у этого ребенка увеличение специфических IgG свыше 10 мкг/мл к следующим СПДП: Нэнни Инфант Формула, Нутрилон ГА, НАН ГА 1, НАН ГА 2, Энфамил ГА, Нутрилак, Нестоген, НАН-1, Нутрилон-1, Винни, Малютка, Фрисовом, Семпер Бифидус, НАН Кисломолочный при отсутствии специфических IgE. Это свидетельствуют о риске развития САР при применении данных СПДП.
Пример 2.
Пациент X., Возраст: 6 мес., Пол: Муж., Амбулаторная карта № 8.
Поступил на обследование в Медицинский научно-исследовательский центр «МЕДИАН» 1.03.2006
Клинический диагноз:
основной: атопический дерматит (начало заболевания в 3 мес.);
сопутствующий: дисфункция желудочно-кишечного тракта, дисбактериоз кишечника.
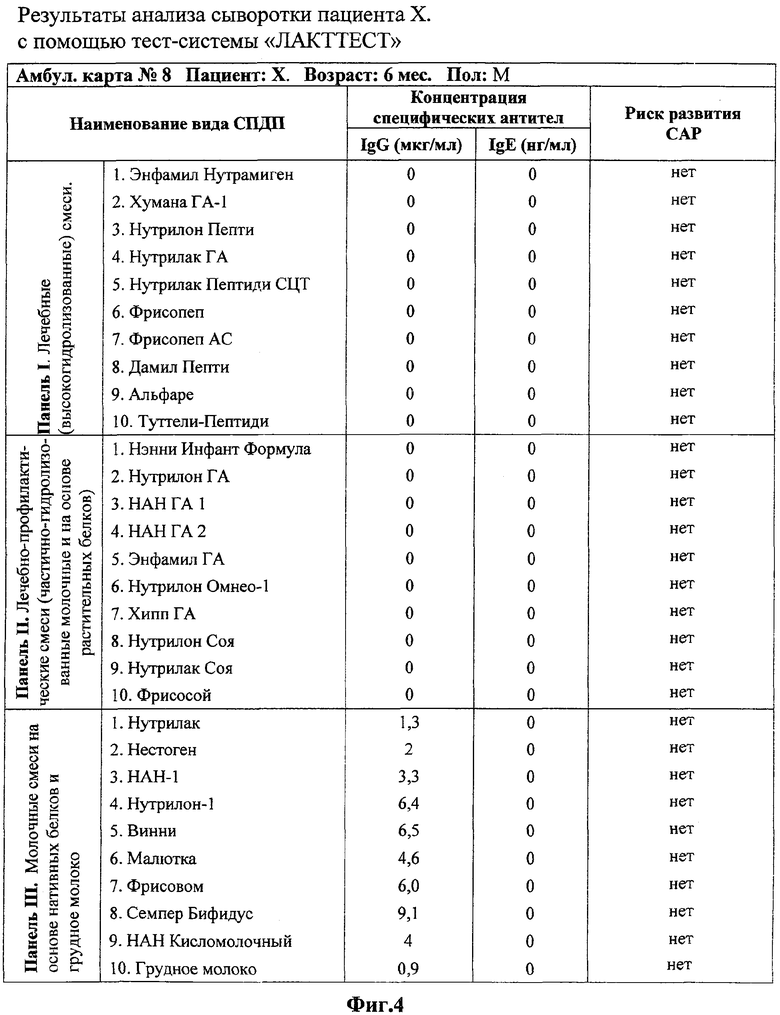
Из анамнеза известно, что ребенок находится только на естественном вскармливании. Из перенесенных заболеваний отмечены гнойный менингит, развившийся на фоне родовой травмы, гипохромная анемия смешанного генеза, три прививки АКДС по графику прошли с повышением температуры до 37°С. В 3 мес.начали вводить яблочный сок, а затем яблочное и кабачковое пюре. Вскоре после этого у ребенка появились кожные высыпания на щеках. Матери была назначена гипоаллергенная диета, но состояние ребенка не улучшилось. Дерматит стал распространенным (практически вся кожа) с тенденцией к мокнутию, нарушилось опорожнение кишечника. Педиатр связал появление дерматита с непереносимостью грудного молока. Содержание в сыворотке крови специфических антител класса IgG и IgE к белкам коровьего молока (БСА, казеину и бета-лактоглобулину) не превышало границ нормы для данного возраста. Встал вопрос об отмене грудного вскармливания и подборе СПДП для данного ребенка. Ребенок был направлен на иммунологическое исследование сыворотки крови с помощью тест-системы «ЛАКТТЕСТ».
Результаты исследования (Фиг.4) показали, что концентрация специфических IgG не превышает 10 мкг/мл, специфических IgE в концентрации свыше 5 нг/мл не выявлено. Это свидетельствует о том, что ни один из исследованных видов СПДП и грудное молоко для данного пациента не имеют противопоказаний, риск развития САР при применении этих продуктов отсутствует.
Данный случай также иллюстрирует возможность использования предлагаемого нами способа для дифференциальной диагностики САР, не связанных с питанием.
Пример 3
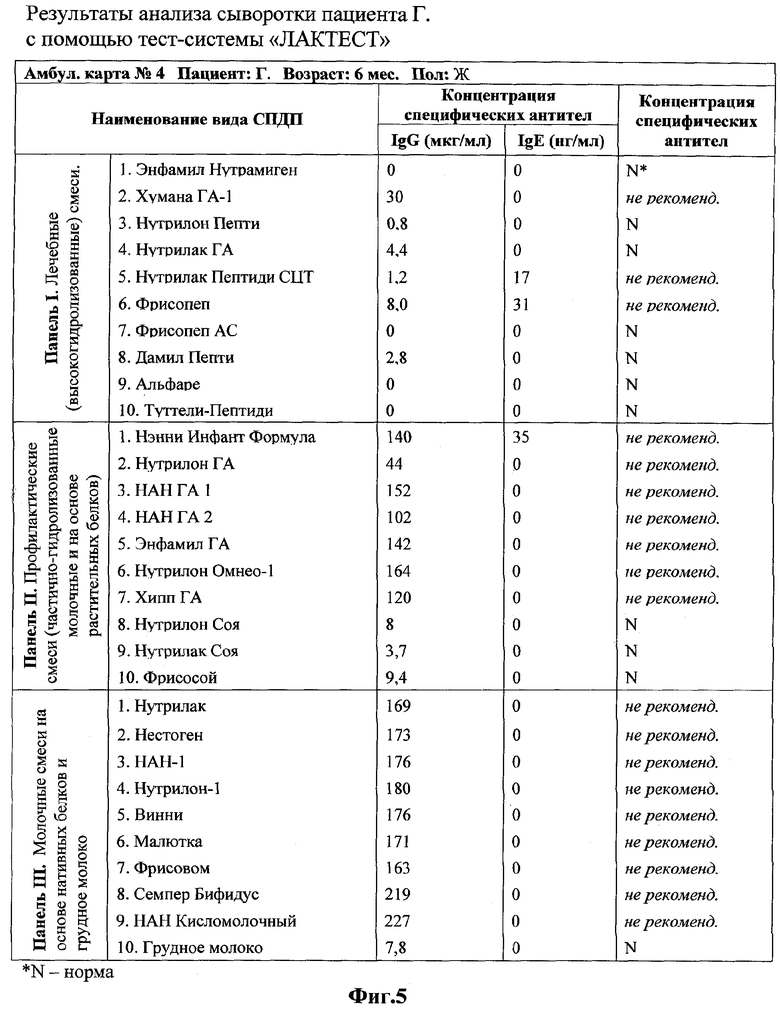
Пациент Г. Возраст: 6 мес. Пол: Жен., Амбулаторная карта № 4.
Поступил на обследование в Медицинский научно-исследовательский центр «МЕДИАН» 2.02.2006.
Клинический диагноз: атонический дерматит, расширенная форма, подострое течение (начало заболевания в 2 мес.).
Ребенок до 2 мес. находился на смешанном вскармливании, затем грудное вскармливание было отменено, и ребенок был переведен на искусственное вскармливание: Нэнни Инфант Формула, Фрисовом, Фрисосой, Нутрилон Омнео-1, Хумана ГА. Затем вернули в рацион СПДП Нэнни Инфант Формулу. Дерматит усилился и стал более распространенным. Состояние ребенка прогрессивно ухудшалось: нарушилось опорожнение кишечника: самостоятельное опорожнение отсутствовало, стул стал густым, серо-зеленым. При этом ребенок стал очень беспокойным, хуже прибавлял в весе, отставал в физическом развитии, отмечался выраженный атопический дерматит с мокнутием. К этому времени не было сделано ни одной профилактической прививки. Имеются данные по отягощенному семейному анамнезу: у матери - пищевая аллергия, у отца - бронхиальная астма. Анализ на специфические антитела к антигенам коровьего молока выявил очень высокое содержание специфических IgG к бычьему сывороточному альбумину - 162 мкг/мл, казеину - 143 мкг/мл, бета-лактоглобулину - 92 мкг/мл при отсутствии специфических IgE к этим антигенам. По этим данным был сделан вывод о непереносимости ребенком белков коровьего молока. На фоне тяжелого клинического состояния ребенок был направлен на иммунологическое исследование с помощью тест-системы «ЛАКТТЕСТ» для подбора питания, не вызывающего развития САР.
Результаты исследования (Фиг.5) показали увеличение концентрации специфических IgG свыше 10 мкг/мл и/или наличие специфических IgE в концентрации, превышающей 5 нг/мл, к следующим видам СПДП: Хумана ГА-1, Нутрилак пептиди СЦТ, Фрисопеп, Нэнни Инфант Формула, Нутрилон ГА, НАН ГА 1, НАН ГА 2, Энфамил ГА, Нутрилон Омнео-1, Хипп ГА, Нутрилак, Нестоген, НАН-1, Нутрилон-1, Винни, Малютка, Фрисовом, Семпер Бифидус, НАН Кисломолочный.
Это свидетельствует о риске развития САР при применении данных СПДП.
Пример 4
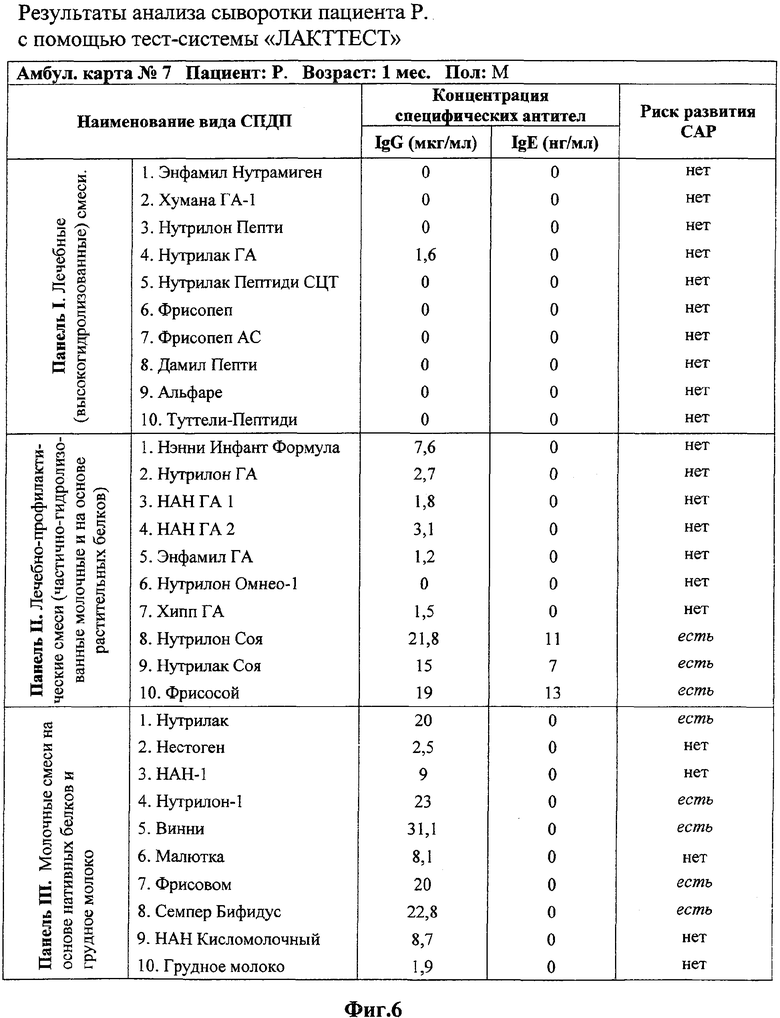
Пациент Р., Возраст: 1 мес., Пол: Муж., Амбулаторная карта № 7.
Поступил на обследование в Медицинский научно-исследовательский центр «МЕДИАН» 20.02.2006.
Клинический диагноз: практически здоров.
Ребенок до 1 мес. находился на естественном вскармливании, затем возникла необходимость перевода ребенка на искусственное вскармливание из-за потери лактации у матери на фоне психологического стресса. С целью подбора диеты и оценки индивидуальной переносимости ребенком некоторых видов заменителей грудного молока были проведены иммунологические исследования сыворотки данного пациента с использованием тест-системы «ЛАКТТЕСТ». Результаты исследования отражены на Фиг.6.
Результаты исследования выявили увеличение специфических IgG более 10 мкг/мл и наличие специфических IgE в концентрации, превышающей 5 нг/мл, к некоторым видам смесей, что свидетельствует о риске развития САР при приеме смесей Нутрилон Соя, Нутрилак Соя, Фрисосой, Нутрилак, Нутрилон-1, Винни, Фрисовом, Семпер Бифидус данных видов СПДП.
Совпадение клинических и иммунологических результатов исследования, полученных с использованием тест-системы «ЛАКТТЕСТ», отмечено у 85% пациентов.
Предлагаемый способ имеет следующие преимущества перед известными:
1. Применение тест-системы «ЛАКТТЕСТ» в клинико-лабораторных исследованиях позволяет повысить точность и надежность диагностики риска развития САР.
2. Получена возможность количественной индивидуальной оценки переносимости конкретного вида СПДП в целом.
3. Применение «ЛАКТТЕСТ»а позволяет провести дифференциальную диагностику пищевой и других видов аллергии у детей.
4. Выполнение исследования производится в условиях in vitro, требует не более 1 мл крови обследуемого лица и безопасно в отношении возможности провоцирования САР после проб.
5. Проведение исследования не требует специальной сложной и дорогостоящей аппаратуры и реактивов, может производиться специалистом-лаборантом; нет необходимости в условиях специализированного медицинского учреждения.
6. Отсутствуют возрастные ограничения для проведения обследования детей, исследования могут быть проведены у ребенка любого возраста.
7. Возможность проведения исследования в любой фазе заболевания, в том числе и острой, является важным достоинством предлагаемого способа.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СОСТАВЛЕНИЯ РАЦИОНА ПИТАНИЯ ДЕТЕЙ С ПИЩЕВОЙ АЛЛЕРГИЕЙ | 2007 |
|
RU2362168C2 |
| Специализированный продукт с пробиотиком на основе полного гидролизата сывороточных белков для питания детей с рождения | 2020 |
|
RU2761534C1 |
| Способ профилактики нутритивной недостаточности у детей с болезнью Гиршпрунга | 2018 |
|
RU2694839C1 |
| СПОСОБ ПОЛУЧЕНИЯ БАКТЕРИАЛЬНОЙ ЗАКВАСКИ ДЛЯ КИСЛОМОЛОЧНОГО ПРОДУКТА | 2000 |
|
RU2169472C2 |
| ВНОВЬ ИДЕНТИФИЦИРОВАННЫЕ ПЕПТИДЫ ДЛЯ ПРИМЕНЕНИЯ ПРИ ИНДУКЦИИ ТОЛЕРАНТНОСТИ ПРИ ПЕРОРАЛЬНОМ ВВЕДЕНИИ У МОЛОДЫХ МЛЕКОПИТАЮЩИХ | 2013 |
|
RU2668155C1 |
| Способ лечения и профилактики заболеваний желудочно-кишечного тракта и других иммунозависимых болезней с хроническим воспалительным синдромом | 2018 |
|
RU2708373C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФЕРМЕНТАТИВНОГО ГИДРОЛИЗАТА СЫВОРОТОЧНЫХ БЕЛКОВ СО СРЕДНЕЙ СТЕПЕНЬЮ ГИДРОЛИЗА | 2008 |
|
RU2375910C1 |
| Способ обследования детей с дистрофической формой врожденного буллезного эпидермолиза | 2017 |
|
RU2657542C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ БЕРЕМЕННОСТИ И ОПРЕДЕЛЕНИЯ СТЕПЕНИ РИСКА НАРУШЕНИЙ РАЗВИТИЯ ЭМБРИОНА/ПЛОДА И РОЖДЕНИЯ РЕБЕНКА С РАЗЛИЧНОЙ НЕ ГЕНЕТИЧЕСКОЙ ПАТОЛОГИЕЙ | 2022 |
|
RU2808266C1 |
| Рекомбинантная плазмидная ДНК pET21-VP40VE, содержащая ген матриксного белка VP40 вируса Эбола и рекомбинантный белок VP40-ВЭ, полученный в результате экспрессии гена белка VP40 вируса Эбола с использованием рекомбинантной плазмидной ДНК pET21-VP40VE и обладающий иммуногенными и антигенными свойствами | 2020 |
|
RU2742511C1 |
Изобретение относится к области медицины, а именно к клинической иммунологии. Способ основан на иммунологической реакции антиген-антитело с определением концентрации специфических антител классов IgG и/или IgE с помощью иммуноферментного анализа. Проводят определение концентрации IgG и/или IgE, специфичных в отношении аллергенов, содержащихся в СПДП различных типов, с использованием тест-системы, содержащей набор антигенов - суммарные белково-пептидные фракции, выделенные методом экстракции из СПДП различных типов, а именно: из лечебных (высокогидролизованных) смесей, из лечебно-профилактических смесей (частично-гидролизованных молочных и на основе растительных белков), из молочных смесей на основе нативных белков и из грудного молока, и при увеличении концентрации специфических IgG более 10 мкг/мл и/или при выявлении специфических IgE в концентрации выше 5 нг/мл диагностируют риск развития сомато-аллергических реакций (САР) в отношении конкретного вида СПДП. Изобретение обеспечивает возможность количественно оценить индивидуальную переносимость конкретного вида СПДП в целом, что позволяет повысить точность и надежность диагностики риска развития САР. 2 н.п. ф-лы, 6 ил.
| MEHL A | |||
| et al | |||
| Utility of the ratio of food-specific IgE/total IgE in predicting symptomatic food allergy in children, Allergy, 2005 Aug 60(8),p.1034-1039 | |||
| SAMPSON HA Utility of food-specific IgE concentrations in predicting symptomatic food allergy, Allergy Clin Immunol, 2001 May 107(5),p 891-896 | |||
| AZABO I et al | |||
| Allergenicity of major cow′s |
Авторы
Даты
2008-06-20—Публикация
2006-07-24—Подача