Данное изобретение относится к области лечения злокачественных опухолей и представляет собой противоопухолевую композицию, содержащую замещенное производное акрилоилдистамицина, точнее α-бром- или α-хлоракрилоилдистамициновое производное, и ингибитор протеинкиназ (серин-/треонин- и тирозинкиназ), проявляющих синергическое противоопухолевое действие.
Дистамицин А и его аналоги, в дальнейшем называемые дистамицин и дистамицин-подобные производные, известны из уровня техники как цитотоксические агенты, используемые в противоопухолевой терапии.
Дистамицин А является антибиотиком с противовирусной и противопротозойной активностью, имеющим полипиррольный аспект [Nature 203: 1064 (1964); J. Med. Chem. 32: 774-778 (1989]). В международных патентных заявках WO 90/11277, WO 98/04524, WO 98/21202, WO 99/50265, WO 99/50266 и WO 01/40181 на имя заявителя включены в описание цитированием, раскрыты производные акрилоилдистамицина, в которых амидино-фрагмент дистамицина возможно замещен содержащими азот концевыми группами, такими как, например, цианамидино, N-метиламидино, гуанидино, карбамоил, амидоксим, циано и тому подобные, и/или в которых полипиррольная структура дистамицина или ее часть замещена различными карбоциклическими или гетероциклическими фрагментами.
В первом аспекте данного изобретения представляют фармацевтическую композицию для применения в противоопухолевой терапии у млекопитающих, включая человека, содержащую фармацевтически приемлемый носитель или наполнитель;
- производное акрилоилдистамицина формулы (I):
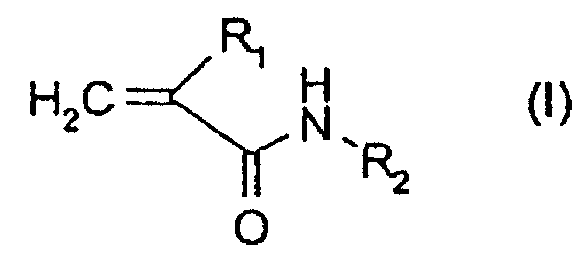 ,
,
в которой:
R1 представляет собой атом брома или хлора;
R2 представляет собой дистамициновый или дистамициноподобный скелет; или его фармацевтически приемлемую соль; и
- ингибитор протеинкиназы.
В рамки данного изобретения включены фармацевтические композиции, содержащие любой из возможных изомеров соединений формулы (I) по отдельности или в смеси, а также метаболиты и фармацевтически приемлемые биопредшественники (известные также как пролекарства) соединений формулы (I).
В данном описании, если не указано особо, под термином «дистамицин» или «дистамициноподобная структура R2» имеют в виду любой фрагмент, структурно близкородственный самому дистамицину, например необязательно замещающий концевой амидиновый фрагмент дистамицин и/или его полипиррольного скелета, или его части, например, как описано ниже.
Протеинкиназы, в дальнейшем кратко называемые PK, представляют собой большое семейство гомологичных белков [смотри ссылку на J. Clin. Invest. 105: 3 (2000); Cancer Chemotherapy and Biological Response Modifiers, Annual 19, Chapter 11, 236 (2001)].
PK как компоненты путей передачи сигнала играют центральную роль в разнообразных биологических процессах, таких как контроль роста, метаболизм, дифференцировка и апоптоз клеток. Разработку селективных ингибиторов РК, которые могут прекращать или изменять развитие заболеваний с дефектами в упомянутых путях передачи сигналов, рассматривают как перспективный подход к созданию новых противораковых лекарственных средств. Подбор названных средств представлен в таблице 1.
Низкомолекулярные АТФ-конкурентные ингибиторы протеинкиназ в клинической разработке
OSI-774 (Тарцева)
PKI 166
EKB-569
GW572016
GCP 41251 (STI 412)
Сафингол
Перифозин
CGP 79787
CP-564959
ZD 6474
ZD 2171
SU-11248
CI-202
Таким образом, композиции изобретения могут содержать упомянутое выше производное акрилоилдистамицина формулы (I) и ингибитор протеинкиназ, которые приведены в Таблице 1.
В соответствии с предпочтительным аспектом изобретения ингибитор PK выбирают из STI571 (Глеевек; иматиниб - ингибитор тирозинкиназы Bcr-Abl), ZD-1839 (Иресса - ингибитор тирозинкиназы рецептора 1 эпидермального фактора роста), OSI-774 (Тарцева - ингибитор тирозинкиназы рецептора 1 эпидермального фактора роста), и SU 5416 (Семаксаниб -ингибитор тирозинкиназы, который ингибирует три отдельные мишени-рецепторы ростовых факторов).
В соответствии с другим предпочтительным аспектом изобретения раскрыты вышеупомянутые фармацевтические композиции, в которых в производном акрилоилдистамицина формулы (I) R1 имеет описанные выше значения, а R2 является группой формулы (II), ниже:
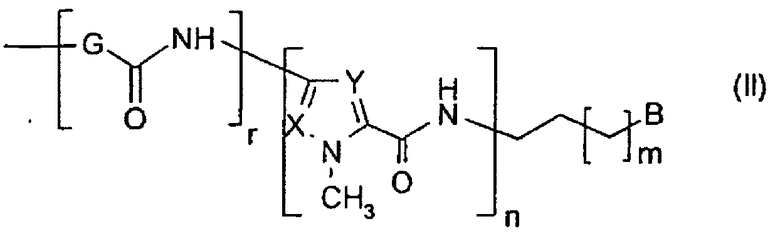 ,
,
в которой
m означает целое число от 0 до 2;
n означает целое число от 2 до 5;
r равно 0 или 1;
X и Y, одинаковые или разные и независимо для каждого гетероциклического кольца являются атомом азота или группой СН;
G представляет собой фенилен, 5- или 6-членное насыщенное или ненасыщенное гетероциклическое кольцо с 1 - 3 гетероатомами, выбранными из N, O или S, или он представляет собой группу формулы (III), ниже:
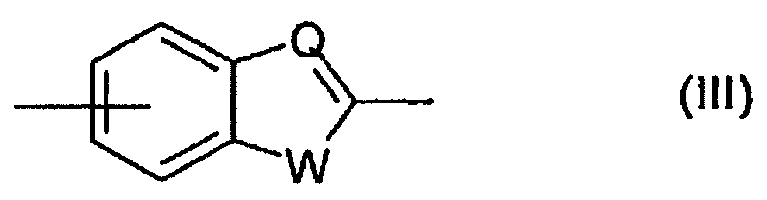 ,
,
в которой Q является атомом водорода или группой СН, а W означает атом кислорода или серы или он означает группу NR3, в которой R3 представляет собой водород или С1-С4-алкил;
В выбирают из группы, состоящей из
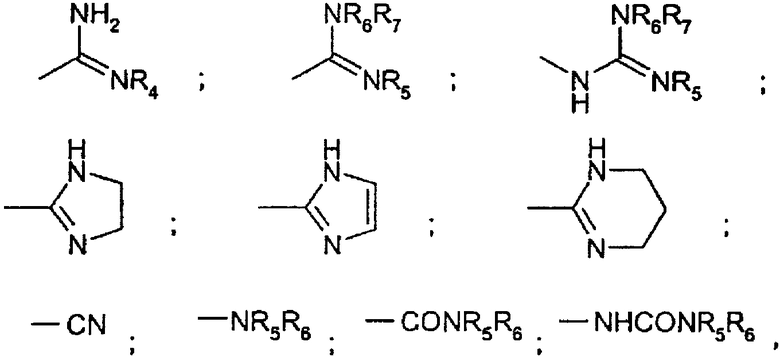
в которых R4 означает циано, гидрокси или С1-С4-алкокси; R5, R6 и R7, одинаковые или разные, представляют собой водород или С1-С4-алкил.
В данном описании, если не указано особо, под термином С1-С4-алкил или группа алкокси имеют в виду группу с прямой или разветвленной цепью, выбранную из метила, этила, н-пропила, изопропила, н-бутила, изобутила, втор-бутила, трет-бутила, метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутила, втор-бутокси или трет-бутокси.
Предпочтительно фармацевтические композиции изобретения содержат упомянутое выше производное акрилоилдистамицина формулы (I), в которой R1 является бромом или хлором; R2 представляет собой упомянутую выше группу формулы (II), в которой r равно 0, m равно 0 или 1, n равно 4, а В имеет описанные выше значения.
В названном классе более предпочтительными являются фармацевтические композиции, содержащие соединения формулы (I), в которых R1 является бромом или хлором; R2 представляет собой упомянутую выше группу формулы (II), в которой r равно 0, m равно 0 или 1, n равно 4, X и Y представляют собой группы СН, а В выбирают из:
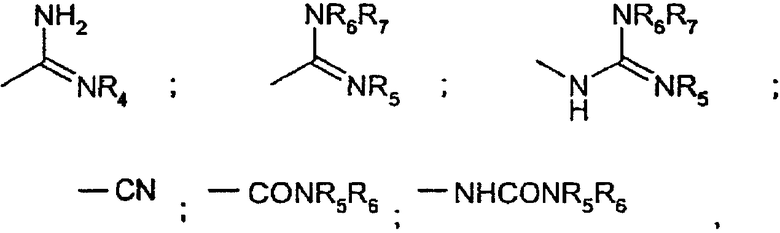
в которых R4 представляет собой циано или гидрокси, а R5, R6 и R7, одинаковые или разные, представляют собой водород или С1-С4-алкил.
Еще более предпочтительными композициями изобретения являются композиции, содержащие соединение формулы (I), в которой R1 является бромом, R2 представляет собой упомянутую выше группу формулы (II), в которой r и m означают 0, n равно 4, X и Y являются СН, В представляет собой группу формулы:
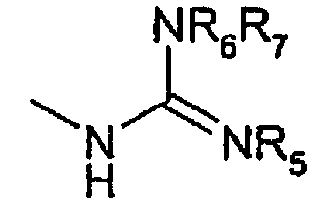 ,
,
в которой R5, R6 и R7 являются атомами водорода, возможно, в виде его фармацевтически приемлемой соли.
Фармацевтически приемлемыми солями соединений формулы (I) являются соли фармацевтически приемлемых неорганических или органических кислот, таких как, например, хлористоводородная, бромистоводородная, серная, азотная, уксусная, пропионовая, янтарная, малоновая, лимонная, винная, метансульфоновая, п-толуолсульфоновая кислота и тому подобные.
Примерами предпочтительных производных акрилоилдистамицина формулы (I) в композициях изобретения, например, в виде фармацевтически приемлемых солей, предпочтительно хлористоводородной кислоты, являются:
1. N-[5-[[[5-[[[2-[(аминоиминометил)амино]этил]амино]карбонил]-1-метил-1Н-пиррол-3-ил]амино]карбонил]-1-метил-1Н-пиррол-3-ил]-4-[[[4-[(2-бромо-1-оксо-2-пропенил)амино]-1-метил-1Н-пиррол-2-ил[карбонил]амино]-1-метил-1Н-пиррол-2-карбоксамид гидрохлорид (Бросталлицин);
2. N-(5-{[(5-{[(5-{[(2-{[амино(имино)метил]амино}пропил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)-4-[(2-бромакрилоил)амино]-1-метил-1Н-пиррол-2-карбоксамид гидрохлорид;
3. N-(5-{[(5-{[(5-{[(3-амино-3-иминопропил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)-4-[(2-бромакрилоил)амино]-1-метил-1Н-пиррол-2-карбоксамид гидрохлорид;
4. N-(5-{[(5-{[(5-{[(3-амино-3-иминопропил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)-4-[(2-бромакрилоил)амино]-1-метил-1Н-имидазол-2-карбоксамид гидрохлорид;
5. N-(5-{[(5-{[(5-{[(3-амино-3-иминопропил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)-3-[(2-бромакрилоил)амино]-1-метил-1Н-пиразол-5-карбоксамид гидрохлорид;
6. N-(5-{[(5-{[(5-{[(3-амино-3-оксопропил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)-3-[(2-бромакрилоил)амино]-1-метил-1Н-пиразол-5-карбоксамид гидрохлорид;
7. N-(5-{[(5-{[(5-{[(2-{[амино(имино)метил]амино}этил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)-4-[(2-хлоракрилоил)амино]-1-метил-1Н-пиррол-2-карбоксамид гидрохлорид;
8. N-(5-{[(5-{[(3-{[амино(имино)метил]амино}пропил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)-4-[(2-бромакрилоил)амино]-1-метил-1Н-пиррол-2-карбоксамид гидрохлорид;
9. N-(5-{[(5-{[(3-амино-3-иминопропил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)-4-[(2-бромакрилоил)амино]-1-метил-1Н-пиррол-2-карбоксамид гидрохлорид; и
10. N-{5-[({5-[({5-[({3-[(аминокарбонил)амино]пропил}амино]карбонил}-1-метил-1Н-пиррол-3-ил}амино)карбонил]-1-метил-1Н-пиррол-3-ил}амино)карбонил]-1-метил-1Н-пиррол-3-ил}-4-[(2-бромакрилоил)амино]-1-метил-1Н-пиррол-2-карбоксамид.
Упомянутые выше соединения формулы (I), или конкретно идентифицированные как таковые или по общей формуле, являются известными, или их легко получают по известным способам, которые описаны, например, в вышеупомянутых международных патентных заявках WO 90/11277, WO 98/04524, WO 98/21202, WO 99/50265 и WO 99/50266, а также в WO 01/40181.
Кроме того, в данном изобретении предоставляют продукт, иначе называемый набор компонентов, содержащий производное акрилоилдистамицина формулы (I), которая описана выше, и ингибитор РК, в виде комбинированного препарата для одновременного, раздельного или последовательного применения в противоопухолевой терапии.
Следующий аспект данного изобретения состоит в способе лечения млекопитающего, включая человека, страдающего опухолевым болезненным состоянием, причем способ предусматривает введение указанному млекопитающему вышеупомянутого производного акрилоилдистамицина формулы (I) и ингибитора РК в количестве, эффективном для достижения синергического противоопухолевого действия.
Данное изобретение также относится к способу снижения побочных эффектов, вызванных противоопухолевым агентом при противоопухолевой терапии у млекопитающего, включая человека, нуждающегося в этом, причем способ предусматривает введение указанному млекопитающему комбинированного препарата, содержащего ингибитор РК и производное акрилоилдистамицина формулы (I), которая описана выше, в количестве, эффективном для достижения синергического противоопухолевого действия.
Используемый в описании термин «синергический противоопухолевой эффект» означает ингибирование роста опухоли, предпочтительно полную регрессию опухоли, введением эффективного количества комбинации, содержащей производное акрилоилдистамицина формулы (I) и ингибитор РК, млекопитающему, включая человека.
Используемый в описании термин «вводимый» или «введение» означает парентеральное и/или пероральное введение; термин «парентеральный» подразумевает внутривенное, подкожное и внутримышечное введение.
По способу данного изобретения производное акрилоилдистамицина можно вводить одновременно с ингибитором РК или, альтернативно, оба соединения можно вводить последовательно в любом порядке.
В этом отношении следует отдать должное тому, что данный предпочтительный способ и порядок введения будет варьироваться в зависимости от, между прочим, определенного используемого препарата акрилоилдистамицина формулы (I), определенного используемого препарата ингибитора РК, конкретного типа опухоли, подвергаемой лечению, а также определенного хозяина, получающего лечение.
Для введения производного акрилоилдистамицина формулы (I) согласно способу изобретения курс обычно применяемой терапии содержит дозы, колеблющиеся приблизительно от 0,05 до 100 мг/м2 поверхности тела и более предпочтительно приблизительно от 0,1 до 50 мг/м2 поверхности тела.
Для введения ингибитора РК по способу изобретения курс обычно применяемой терапии может быть следующим.
Для введения STI571 (Иматиниб) дозы колеблются приблизительно от 5 мг/сутки до 5000 мг/сутки и более предпочтительно приблизительно от 30 до 1000 мг/сутки.
Для введения ZD 1839 (Иресса) дозы колеблются приблизительно от 5 мг/сутки до 10000 мг/сутки и более предпочтительно от 50 до 1000 мг/сутки.
Для введения OSI-774 (Тарцева) дозы составляют приблизительно от 5 мг/сутки до 10000 мг/сутки и более предпочтительно от 50 до 1000 мг/сутки.
Для введения SU 5416 (Семаксаниб) дозы колеблются приблизительно от 1 мг/м2 до 1000 мг/м2 поверхности тела и более предпочтительно от 10 до 500 мг/м2 поверхности тела.
Противоопухолевая терапия по данному изобретению особенно подходит для лечения опухолей молочной железы, яичников, легкого, ободочной кишки, почек, желудка, поджелудочной железы, печени, меланомы, лейкоза и опухолей головного мозга у млекопитающих, включая человека.
В следующем аспекте данное изобретение относится к фармацевтической композиции, содержащей эффективное количество производного акрилоилдистамицина формулы (I), которая описана выше, и ингибитора РК в препарате лекарственного средства для применения для профилактики или лечения метастаза или лечения опухолей ингибированием ангиогенеза.
В то время как действия производного акрилоилдистамицина формулы (I) и ингибитора РК значительно усиливаются без параллельного увеличения токсичности, комбинированная терапия данного изобретения повышает противоопухолевые эффекты производного акрилоилдистамицина и ингибитора РК и, следовательно, обеспечивает наиболее эффективное и наименее токсичное лечение опухолей.
ЦИТОТОКСИЧЕСКАЯ АКТИВНОСТЬ IN VITRO
Экспоненциально растущие клетки засевали и инкубировали при 37°С во влажной атмосфере 5% СО2. Через 24 часа в среду добавляли скалярные дозы бросталлицина и ингибитора киназы и клетки выдерживали в течение 72 часов. По окончании обработки пролиферацию клеток определяли системой мониторинга клеточного аденозинтрифосфата. Пролиферацию клеток сравнивали с контрольными клетками. Все исследованные клеточные линии были чувствительны к бросталлицину. Для каждой комбинации была выбрана клеточная линия, наиболее чувствительная к ингибитору киназы: CML K562 (BCR-ABL положительная) человека для STI571 (Gleevec); NCI-H322M рака легких человека для ZD1839 (Iressa) и MDA-MB-468 рака молочной железы человека для OSI-774 (Tarceva).
Индексы комбинации (C.I.) рассчитывали с использованием компьютерной программы для множественного анализа эффекта лекарственного средства, основанного на уравнении Chou-Talalay (Enzyme Regul. 1984; 22: 27-55), для взаимно не исключающих лекарственных средств, где C.I.<1 in vitro указывает на более чем просто аддитивный (кумулятивный) эффект.
Результаты, полученные с лекарственными средствами в виде отдельных агентов и в комбинации, представлены в таблицах 2-4.
in vitro комбинация бросталлицина и STI571 на клеточной линии человека CML K562
in vitro комбинация бросталлицина и ZD 1839 на клеточной линии рака легкого человека NCI-H322M
in vitro комбинация бросталлицина и OSI-774 на клеточной линии рака молочной железы человека MDA-MB-468
Полученные результаты показывают, что в случае опухолевых клеток человека бросталлицин можно эффективно комбинировать с STI 571 (Gleevec), ZD 1839 (Iressa) или OSI-774 (Tarceva) с получением более чем аддитивного, а именно, синергетического эффекта.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМБИНИРОВАННАЯ ПРОТИВООПУХОЛЕВАЯ ТЕРАПИЯ, ВКЛЮЧАЮЩАЯ ИСПОЛЬЗОВАНИЕ ЗАМЕЩЕННЫХ АКРИЛОИЛПРОИЗВОДНЫХ ДИСТАМИЦИНА И ЛУЧЕВОЙ ТЕРАПИИ | 2003 |
|
RU2314807C2 |
| СОЕДИНЕНИЯ И СПОСОБЫ МОДУЛИРОВАНИЯ КИНАЗЫ И ПОКАЗАНИЯ К ИХ ПРИМЕНЕНИЮ | 2013 |
|
RU2666146C2 |
| КОМБИНАЦИЯ, ВКЛЮЧАЮЩАЯ А) ПИРИМИДИЛАМИНОБЕНЗАМИД И Б) ИНГИБИТОР КИНАЗЫ Thr315lle | 2007 |
|
RU2481840C2 |
| КОМБИНАЦИИ, ВКЛЮЧАЮЩИЕ ИНГИБИТОРЫ Bcr-Abl/c-Kit/PDGF-R TK, ДЛЯ ЛЕЧЕНИЯ РАКА | 2007 |
|
RU2452492C2 |
| КОМБИНАЦИИ ТЕРАПЕВТИЧЕСКИХ АГЕНТОВ ДЛЯ ЛЕЧЕНИЯ РАКА | 2007 |
|
RU2449788C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ | 2016 |
|
RU2744897C2 |
| КОМБИНАЦИИ ТЕРАПЕВТИЧЕСКИХ СРЕДСТВ, ПРЕДНАЗНАЧЕННЫЕ ДЛЯ ЛЕЧЕНИЯ РАКА | 2007 |
|
RU2447891C2 |
| ХРОМЕНОНОВЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ РI3-КИНАЗЫ ДЛЯ ЛЕЧЕНИЯ РАКА | 2012 |
|
RU2598028C2 |
| СОЕДИНЕНИЯ, ИСПОЛЬЗУЕМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗЫ ATR | 2013 |
|
RU2689996C2 |
| АКРИЛОИЛЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ПИРРОЛА И ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ КИСЛОТНО-АДДИТИВНЫЕ СОЛИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1990 |
|
RU2094430C1 |
Изобретение относится к области фармакологии и медицины и касается фармацевтической композиции для лечения опухолей, содержащей производное акрилоилдистамицина формулы (1) и ингибитор протеинкиназы, продукта, содержащего производное акрилоилдистамицина формулы (1) и ингибитор протеинкиназы, применения производного акрилоилдистамицина формулы (1) и ингибитора протеинкиназы в комбинированной терапии при лечении опухолей а также способа лечения опухолевого заболевания. Изобретение обеспечивает высокую эффективность лечения. 9 н. и 18 з.п. ф-лы, 4 табл.
- производное акрилоилдистамицина формулы (I)
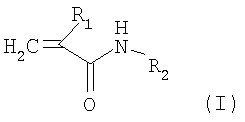
в которой R1 представляет собой атом брома или хлора;
R2 является дистамицином или дистамицинподобной структурой,
или его фармацевтически приемлемую соль; и
ингибитор протеинкиназы.

где R1 представляет собой атом брома или хлора;
R2 представляет собой группу формулы (II)
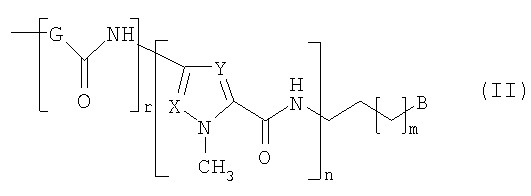
в которой m означает целое число от 0 до 2;
n означает целое число от 2 до 5;
r равно 0 или 1;
Х и Y, одинаковые или разные и независимо для каждого гетероциклического кольца представляют собой атом азота или группу СН;
G представляет собой фенилен, 5- или 6-членное насыщенное или ненасыщенное гетероциклическое кольцо с 1-3 гетероатомами, выбранными из N, О или S, или он является группой формулы (III)
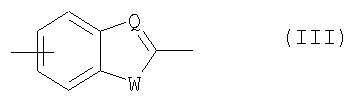
в которой Q является атомом азота или группой СН, a W представляет собой атом кислорода или серы, или Q является группой NR3, в которой R3 означает водород или С1-С4-алкил;
В выбирают из группы, состоящей из
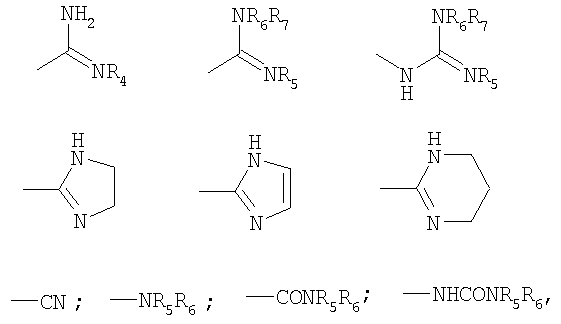
в которых R4 означает циано, амино, гидрокси или C1-C4-алкокси; R5, R6 и R7, одинаковые или разные, представляют собой водород или С1-С4-алкил.
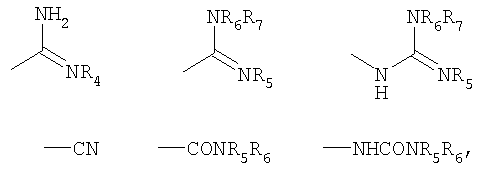
в которой R4 представляет собой циано или гидрокси, a R5, R6 и R7, одинаковые или разные, представляют собой водород или C1-C4-алкил.
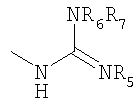
в которой R5, R6 и R7, одинаковые или разные, представляют собой атомы водорода,
возможно в виде фармацевтически приемлемой соли.
{[амино(имино)метил]амино}пропил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)-4-[(2-бромакрилоил)амино]-1-метил-1Н-пиррол-2-карбоксамида гидрохлорида;
иминопропил)амино]карбонил}-1-метил-1H-пиррол-3-ил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)амино]карбонил}-1-метил-1H-пиррол-3-ил)-4-[(2-бромакрилоил)амино]-1-метил-1H-пиррол-2-карбоксамида гидрохлорида;
{[амино(имино)метил]амино}этил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)-4-[(2-хлоракрилоил)амино]-1-метил-1H-пиррол-2-карбоксамида гидрохлорида;
{[амино(имино)метил]амино}пропил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)амино]карбонил}-1-метил-1Н-пиррол-3-ил)-4-[(2-бромакрилоил)амино]-1-метил-1Н-пирроле-2-карбоксамида гидрохлорида;
[(аминокарбонил)амино]пропил}амино]карбонил}-1-метил-1Н-пиррол-3-ил}амино)карбонил]-1-метил-1Н-пиррол-3-ил}амино)карбонил]-1-метил-1Н-пиррол-3-ил}-4-[(2-бромакрилоил)амино]-1-метил-1Н-пиррол-2-карбоксамида.
N-[5-[[[5-[[[2-[(аминоиминометил)амино]этил]амино]карбонил]-1-метил-1Н-пиррол-3-ил]амино]карбонил]-1-метил-1Н-пиррол-3-ил]-4-[[[4-[(2-бром-1-оксо-2-пропенил)амино]-1-метил-1Н-пиррол-2-ил[карбонил]амино]-1-метил-1Н-пиррол-2-карбоксамид гидрохлорид (Бросталлицин) и
ингибитор протеинкиназ, выбранный из группы, состоящей из STI571, ZD-1839, OSI-774 и SU 5416.

в которой R1 представляет собой атом брома или хлора;
R2 является дистамицином или дистамицинподобной структурой; или его фармацевтически приемлемой солью; и ингибитор протеинкиназ, используемых в препарате для одновременного, раздельного или последовательного применения при лечении опухолей.

в которой R1 представляет собой атом брома или хлора;
R2 представляет собой группу формулы (II)

в которой m является целым числом от 0 до 2;
n является целым числом от 2 до 5;
r равно 0 или 1;
Х и Y, одинаковые или разные и независимо для каждого гетероциклического кольца, представляют собой атом азота или группу СН;
G представляет собой фенилен, 5- или 6-членное насыщенное или ненасыщенное гетероциклическое кольцо с 1-3 гетероатомами, выбранными из N, О и S, или G является группой формулы (III)

в которой Q представляет собой атом азота или группу СН, а W означает атом кислорода или серы или он является группой NR3, в которой R3 представляет собой водород или С1-С4-алкил;
В выбирают из группы, состоящей из
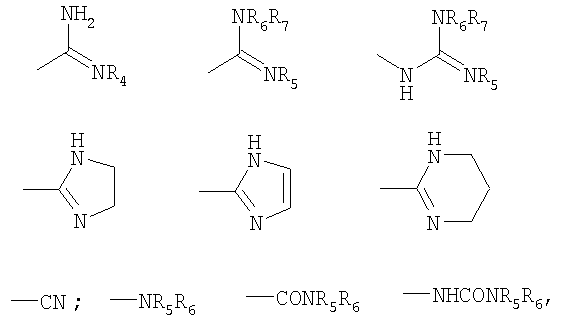
в которой R4 означает циано, амино, гидрокси или C1-C4-алкокси; R5, R6 и R7, одинаковые или разные, представляют собой водород или С1-С4-алкил.
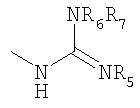
в которой R5, R6 и R7 являются атомами водорода, возможно в виде фармацевтически приемлемой соли.
| Пожарный двухцилиндровый насос | 0 |
|
SU90A1 |
| АКРИЛОИЛЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ПИРРОЛА И ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ КИСЛОТНО-АДДИТИВНЫЕ СОЛИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1990 |
|
RU2094430C1 |
| US 5821072 А, 13.10.1998 | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2008-07-10—Публикация
2002-12-18—Подача