Изобретение относится к фармацевтической промышленности, а именно к способам выделения биологически активных веществ из растительного сырья, в частности к технологии получения агарициновой кислоты. Она используется для проведения анализа и получения лекарственных препаратов [Garcia, N. Agaric acid induces mitochondrial permeability transition through its interaction with the adenine nucleotide translocase. Its dependence on membrane fluidity. / Garcia N., Zazueta C., Pavon N., Chavez E. // Mitochondrion. - 2005. - V.5. - Is. 4. - P.272-281; Chavez, E. The effect of agaric on citrate transport in rat liver mitochondria. / Chavez E., Chavez R., Carrasco N. // Life Sciences. - 1978. - V.23. - Is. 14. - P.1423-1429].
Известен способ получения агарициновой кислоты из гриба трутовика (Fomitopsis of ficinalis Will. Bond. Et Sing.) (Патент RU 2257222 C1 от 02.07.2004, A61K 35/84 Комплексная переработка гриба трутовика лекарственного, авторы Ушанова В.М., Ооржак У.С., Канзай В.И.), который принят за прототип. Способ основан на том, что сырье сначала экстрагируют сжиженным диоксидом углерода с выделением углекислотного экстракта, содержащего эфирное масло, жирные ненасащенные кислоты, каротиноиды, витамины Е, А и стерины, затем остаток экстрагируют диэтиловым эфиром при температуре 34-36°С в течение 2-3 часов с выделением экстракта, содержащего агарициновую кислоту и липидно-каротиноидный комплекс.
Недостатками способа являются: использование экстракции диоксидом углерода, требующей сложного герметичного оборудования, использование дорогостоящего диэтилового эфира в качестве растворителя, получение готового продукта с примесью липидно-каротиноидного комплекса.
Задачей предлагаемого изобретения является упрощение способа с одновременным сокращением до минимума потерь агарициновой кислоты в процессе выделения, получение чистого, без примесей других веществ вещества, а также: замена более токсичного органического растворителя (диэтиловый эфир) на менее токсичный (95% этанол), удешевление способа за счет использования более дешевого экстрагента (95% этанола) и более дешевого оборудования.
Отличительными существенными признаками являются использование 95% этанола в качестве растворителя на стадии первичной экстракции и очистки, одновременность осуществления процесса разделения и очистки.
Экстракция исходного растительного сырья 95% этанолом с нагреванием с последующей перекристаллизацией агарициновой кислоты позволяет:
- увеличить выход агарициновой кислоты;
- получить агарициновую кислоту в чистом виде без примеси липидов и каротиноидов.
Применение 95% этанола позволяет осуществить процесс выделения агарициновой кислоты без стадии экстракции сырья диоксидом углерода и последующей экстракции диэтиловым эфиром.
Способ осуществляется следующим образом.
100,0 г гриба трутовика лекарственного (Fomitopsis officinalis Will. семейства трутовиковых - Polyporaceae, класса базидиомицетов - Basidiomycetes), измельченного не более 3 мм, экстрагируют в аппарате Сокслета 95%-ным этанолом при суммарном соотношении сырья и экстрагента 1:25 при нагревании на водяной бане при температуре +78°С до истощения сырья.
Полноту извлечения агарициновой кислоты контролируют хроматографическим методом. Раствор выделенного вещества наносят на пластинки «Сорбфил ПТСХ-А-УФ». Система для хроматографии - хлороформ : уксусная кислота : вода 13:2,5:1. Пятна рассматривают в УФ-свете при длине волны 365 нм. При полном извлечении агарициновой кислоты должно отсутствовать пятно с Rf=0,67±0,02.
Полученный экстракт упаривают до суммарного соотношения сырье и экстракт 1 мас.ч. сырья : 6 об.ч. экстракта, оставляют при температуре -4°С - -5°С, на 12 часов до образования осадка. Осадок отделяют и промывают на фильтре 95% этанолом при суммарном соотношении сырье : этанол 95% 1 мас.ч. осадка : 0,5 об.ч. этанола (температура этанола не более +5°С), получают техническую агарициновую кислоту.
Техническую агарициновую кислоту растворяют при нагревании, при +50 - +55°С, в 95% этаноле, взятом в соотношении агарициновая кислота : растворитель 1:10, охлаждают, выдерживают при -4°С - -5°С в течение 2 часов, отделяют осадок фильтрованием через стеклянный фильтр. Перекристаллизацию повторяют еще четыре раза - получают очищенную агарициновую кислоту. Полученный продукт высушивают в сушильном шкафу до постоянной массы при +50°С - +55°С. Взвешивают. Выход 9,5%-14,2% в пересчете на абсолютно сухое сырье.
Пример 1.
Аналитическую пробу сырья гриба трутовика лекарственного (Fomitopsis officinalis Will. семейства трутовиковых - Polyporaceae, класса базидиомицетов - Basidiomycetes) измельчают до размера частиц не более 3 мм. Около 100 г (точная навеска) сырья упаковывают в патрон из фильтровальной бумаги и загружают в аппарат Сокслета, заливают 95%-ным этанолом при суммарном соотношении сырья и экстрагента 1:25, экстрагируют при нагревании на водяной бане при температуре +78°С до истощения сырья. Полноту извлечения агарици новой кислоты контролируют хроматографическим методом, как описано выше. Параллельно определяют влажность сырья. Все измерения проводят с точностью до 0,0001 г.
Полученный экстракт упаривают до суммарного соотношения сырье и экстракт 1 мас.ч. сырья : 6 об. ч. экстракта, оставляют при температуре -4°С - -5°С, на 12 часов до образования осадка. Надосадочную жидкость сливают, остаток фильтруют через стеклянный фильтр, осадок промывают на фильтре 95% этанолом при суммарном соотношении сырье: этанол 95% 1 мас.ч. осадка : 0,5 об.ч. этанола (температура этанола не более +5°С), получают техническую агарициновую кислоту.
Техническую агарициновую кислоту растворяют при нагревании, при +50 - +55°С, в 95% этаноле, взятом в соотношении агарициновая кислота : растворитель 1:10, охлаждают, выдерживают при -4°С - -5°С в течение 12 часов, отделяют осадок фильтрованием через стеклянный фильтр. Осадок опять растворяют при нагревании, при +50 - +55°С, в 95% этаноле, взятом в соотношении агарициновая кислота : растворитель 1:10, охлаждают, выдерживают при -4°С - -5°С в течение 12 часов, отделяют осадок фильтрованием через стеклянный фильтр. Данную операцию повторяют еще три раза, получают очищенную агарициновую кислоту.
Полученный продукт (образец 1) высушивают в сушильном шкафу до постоянной массы при 50°С. Взвешивают. Выход очищенной агарициновой кислоты в пересчете на абсолютно сухое сырье составляет 14,2%.
Пример 2.
Аналитическую пробу сырья гриба трутовика лекарственного (Fomitopsis officinalis Will. семейства трутовиковых - Polyporaceae, класса базидиомицетов - Basidiomycetes) измельчают до размера частиц не более 3 мм. Около 100 г (точная навеска) сырья упаковывают в патрон из фильтровальной бумаги и загружают в аппарат Сокслета, заливают 95%-ным этанолом при суммарном соотношении сырья и экстрагента 1:25, экстрагируют при нагревании на водяной бане при температуре +78°С до истощения сырья. Полноту извлечения агарициновой кислоты контролируют хроматографическим методом, как описано выше. Параллельно определяют влажность сырья. Все измерения проводят с точностью до 0,0001 г. Полученный экстракт упаривают до суммарного соотношения сырье и экстракт 1 мас.ч. сырья: 6 об. ч. экстракта, оставляют при температуре -4°С - -5°С, на 12 часов до образования осадка. Надосадочную жидкость сливают, остаток фильтруют через стеклянный фильтр, осадок промывают на фильтре 95% этанолом при суммарном соотношении сырье : этанол 95% 1 мас.ч. осадка : 0,5 об.ч. этанола (температура этанола не более +5°С), получают техническую агарициновую кислоту.
Техническую агарициновую кислоту растворяют при нагревании, при +50° - +55°С, в 95% этаноле, взятом в соотношении агарициновая кислота : растворитель 1:10, охлаждают, выдерживают при -4°С - -5°С в течение 12 часов, отделяют осадок фильтрованием через стеклянный фильтр. Осадок повторно растворяют при нагревании, при +50 - +55°С, в 95% этаноле, взятом в соотношении агарициновая кислота : растворитель 1:10, охлаждают, выдерживают при -4°С - -5°С в течение 12 часов, отделяют осадок фильтрованием через стеклянный фильтр. Данную операцию повторяют еще три раза, получают очищенную агарициновую кислоту.
Полученный продукт (образец 2) высушивают в сушильном шкафу до постоянной массы при 50°С. Взвешивают. Выход очищенной агарициновой кислоты в пересчете на абсолютно сухое сырье составляет 9,5%.
Физические и физико-химические свойства выделенного вещества (образец 1 и образец 2) сравнивали со свойствами достоверного стандартного образца агарициновой кислоты (получен по каталогу фирмы «Sigma-Aldrich» №666-99-9). Исследование показало, что это - кристаллические порошки белого цвета с легким желтоватым оттенком, без запаха, горько-сладкого вкуса, практически не растворимые в воде, очень мало растворимые в 1 моль/л растворе натрия гидроксида, растворимые при нагревании в этаноле 95% в соотношении 1:10, в этаноле 95% при температуре +5°С в соотношении 1:130, спирте изопропиловом, диметилсульфоксиде.
Затем с целью идентификации полученного вещества как агарициновой кислоты были определены: его температура плавления, Rf, УФ-спектр, ИК-спектр, ЯМР-спектр.
Температура плавления выделенного вещества (образец 1 и образец 2) составила 134°С - 136°С, температура плавления достоверного образца агарициновой кислоты - 134-136°С, температура плавления пробы смешения выделенного вещества с достоверным образцом агарициновой кислоты - 134-136°С, (т.е. депрессии температуры плавления не произошло). Таким образом, можно сделать вывод об идентичности стандарта агарициновой кислоты (SIGMA ALDRICH) и вещества, полученной из лиственничной губки.
0,5% раствор выделенного вещества (образец 1 и образец 2), раствор достоверного стандартного образца агарициновой кислоты (каталог «Sigma» № 666-99-9 FC № 211-566-5), раствор из смеси равных количеств выделенного вещества и достоверного стандартного образца наносили на пластинки «Сорбфил ПТСХ-А-УФ» в количестве 5 мкл. Система для хроматографии - хлороформ : уксусная кислота : вода 13:2,5:1. Пятна рассматривали в УФ-свете при длине волны 365 нм. В результате анализа, на хроматограмме выделенного вещества было обнаружено одно пятно с Rf=0,67±0,02, достоверный стандартный агарициновой кислоты дал одно пятно с Rf=0,67±0,02, проба смешения выделенного вещества и достоверного стандартного образца дала одно пятно с Rf=0,67±0,02. Это подтверждает идентичность стандарта агарициновой кислоты (SIGMA ALDRICH) и вещества, полученного из лиственничной губки.
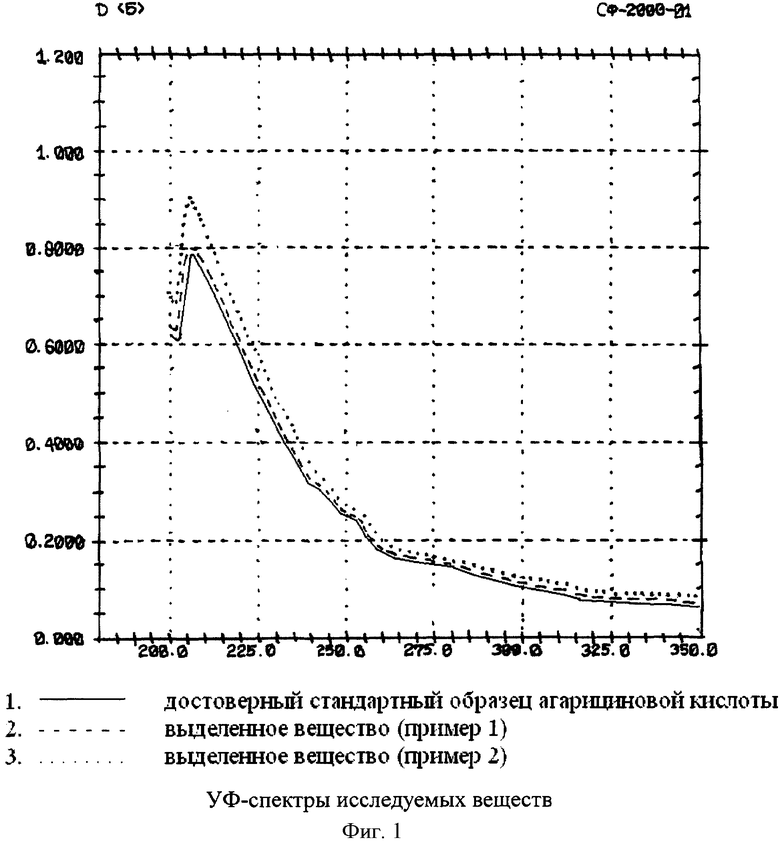
УФ-спектры 0,05% растворов выделенного вещества (образец 1 и образец 2) и достоверного стандартного образца агарициновой кислоты в 95% этаноле измеряли на саморегистрирующем спектрофотометре СФ-56 в области 200-350 нм. Максимум светопоглощения всех образцов находился в области 206±2 нм. УФ-спектры представлены на фиг.1.
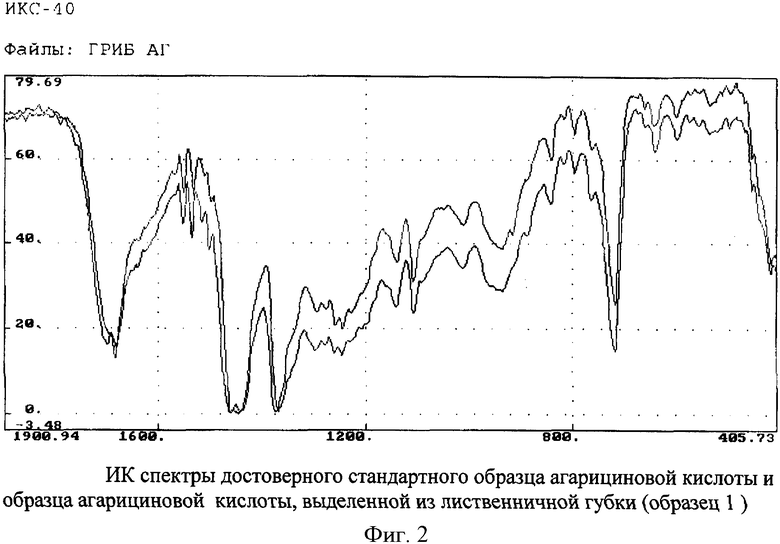
Подготовку проб веществ для снятия ИК-спектра осуществляли в соответствии с требованиями Государственной фармакопеи XI издания [Государственная фармакопея СССР. - М.: Медицина, 1987. - Вып.1. - С.37]. Навески веществ (выделенного и достоверного стандартного образца агарициновой кислоты) массой по 15 мг измельчали в агатовой ступке и растирали с 1-2 каплями вазелинового масла качества для ПК - спектроскопии. Полученную пасту наносили между двумя пластинками из калия бромида (KBr) и измеряли ИК - спектр образца.
В работе использовали спектрофотометр инфракрасный ИКС - 40 (ОАО «Ломо», Россия). Параметры записи спектров: диапазон 4000-400 см-1, шаг дискретизации 2,7 см-1, скорость сканирования 225 см-1/мин, коэффициент щели - 1, аподизация стандартная. Фоновый спектр (воздух) получали непосредственно перед записью каждого спектра испытуемой субстанции. Управление прибором и обработку спектров осуществляли с использованием программы на языке ФОРТ, поставляемую вместе с комплексом. Полученные данные свидетельствуют о том, что два образца, выделенных из лиственничной губки (образец 1 и образец 2) и стандарт агарициновой кислоты (SIGMA), полностью идентичны.
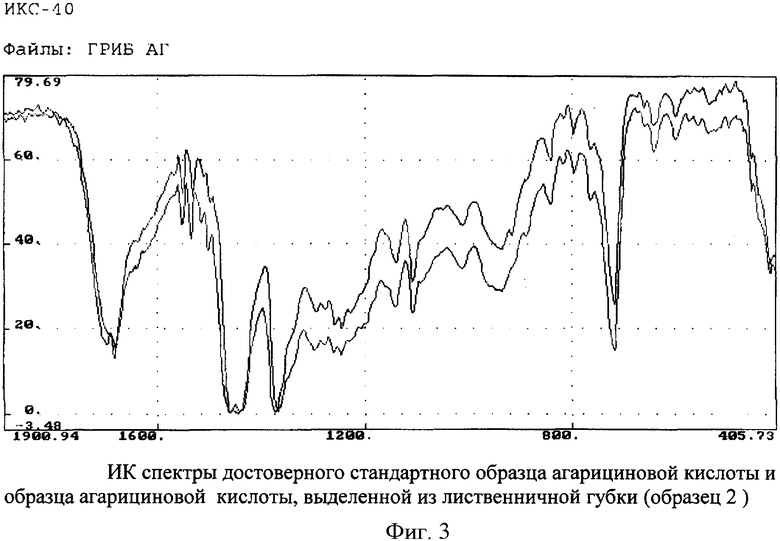
На фиг.2,3 представлены ИК-спектры стандарта агарициновой кислоты и этой же кислоты, выделенной гриба трутовика (образец 1 и образец 2). Анализ спектров стандартного образца и выделенного вещества показал их идентичность.
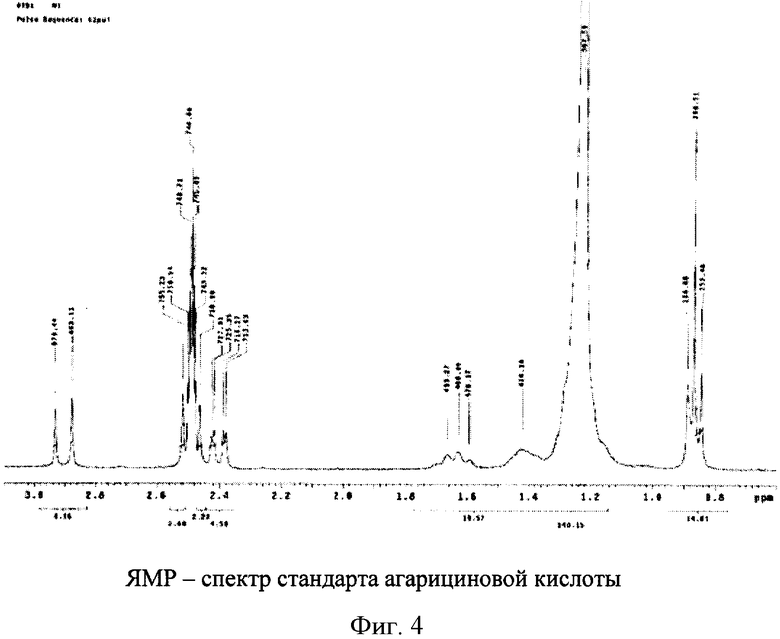
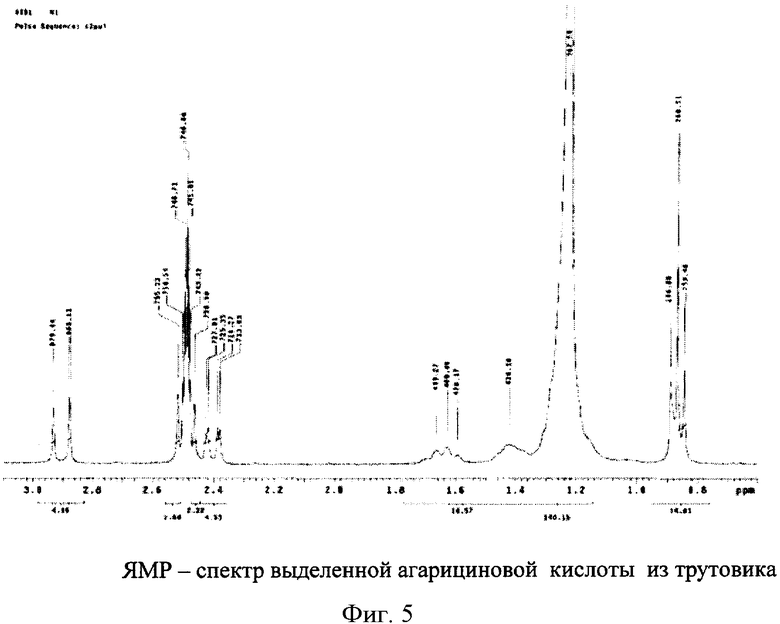
На фиг.4 и 5 представлены ЯМР-спектры стандарта агарициновой кислоты и этой же кислоты, выделенной гриба трутовика.
Образец выделенного вещества и достоверный стандартный образец агарициновой кислоты исследовали с помощью одномерной ЯМР 1H и 13С-спектроскопии. Спектр ЯМР 1Н стандарта агарициновой кислоты (фиг.4) и агарициновой кислоты, полученной из двух партий лиственничной губки, в области резонанса атомов углерода содержал три интенсивных (260,51; 367,59 и 746,88) и двадцать минорных сигналов (253,48-879,44). Так как при данном методе использовали такой растворитель как диметилсульфоксид (ДМСО), то сразу исключаем пик этого растворителя (746,88). Наиболее интенсивными сигналами в спектре были пики от СН3- и (CH2)n-групп (при соответственно 260,51 и 367,59), что свидетельствует о наличии в молекуле агарициновой кислоты длинной углеродной цепи (C18H40O7). Спектры ЯМР - снимали на спектрометре UNITY - 300 выпуск 1990 г, фирмы «VARIAN» США. Для получения 1Н спектров ЯМР использовали стандартную 2-импульсную последовательность с последующим Фурье преобразованием. Химические сдвиги ЯМР сигналов определялись относительно сигнала остаточных протонов соответствующего дейтеро-растворителя (ДМСО - d6). Спектры ЯМР 1Н растворов указанных образцов с концентрацией веществ 10% регистрировали на спектрометре высокого разрешения WP-200 (50,3 МГц) с сверх проводящим магнитом и широкополостным датчиком 1Н/13С в режиме полного подавления спин-спинового взаимодействия ядер углерода 13С с протонами.
Анализ ЯМР-спектров стандартного образца и выделенного вещества показал их идентичность.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения агарициновой кислоты из мицелия трутовика лекарственного | 2019 |
|
RU2708034C1 |
| Способ комплексной переработки гриба трутовика лекарственного | 2016 |
|
RU2619551C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДОРАСТВОРИМЫХ ПОЛИСАХАРИДОВ ИЗ ПЛОДОВОГО ТЕЛА ТРУТОВИКА ЛЕКАРСТВЕННОГО, ОБЛАДАЮЩИХ ИММУНОТРОПНОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2404249C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИММОБИЛИЗОВАННОГО МИЦЕЛИЯ БАЗИДИОМИЦЕТА FOMITOPSIS OFFICINALIS | 2017 |
|
RU2707541C2 |
| ШТАММ БАЗИДИАЛЬНОГО ГРИБА Fomitopsis officinalis, ПРОЯВЛЯЮЩИЙ АНТИБАКТЕРИАЛЬНУЮ АКТИВНОСТЬ В ОТНОШЕНИИ БАКТЕРИЙ Yersinia pseudotuberculosis | 2008 |
|
RU2375439C1 |
| КОМПЛЕКСНАЯ ПЕРЕРАБОТКА ГРИБА ТРУТОВИКА ЛЕКАРСТВЕННОГО (FOMITOPSIS OFFICINALIS (VILL.: FR.) BOND. ET SING.) | 2004 |
|
RU2257222C1 |
| ШТАММ БАЗИДИОМИЦЕТА Fomitopsis Tyv-2006, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПОЛУЧЕНИЯ ПРОТИВООПУХОЛЕВЫХ ПРЕПАРАТОВ | 2007 |
|
RU2360960C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО АНТИМИКРОБНОЙ, ПРОТИВОВОСПАЛИТЕЛЬНОЙ И ПРОТИВООЖОГОВОЙ АКТИВНОСТЬЮ ИЗ ПЛОДОВОГО ТЕЛА ГРИБА ТРУТОВИКА (FOMITOPSIS OFFICINALIS BOND.) | 2009 |
|
RU2409378C2 |
| КОСМЕТИЧЕСКОЕ СРЕДСТВО | 2007 |
|
RU2319478C1 |
| ПРОТИВОВИРУСНОЕ СРЕДСТВО НА ОСНОВЕ СУХОГО ЭКСТРАКТА ПЛОДОВОГО ТЕЛА КСИЛОТРОФНОГО БАЗИДИОМИЦЕТА Bjerkandera adusta | 2015 |
|
RU2580296C1 |
Изобретение относится к фармацевтической промышленности, в частности к способу получения агарициновой кислоты из гриба трутовика лекарственного. Способ получения агарициновой кислоты из гриба трутовика лекарственного (Fomitopsis officinalis Will., семейство трутовиковых - Polyporaceae, класс базидиомицетов - Basidiomycetes), включающий экстракцию измельченного сырья этанолом при определенных условиях, упаривание экстракта до определенного значения, отделение агарициновой кислоты, очищение, перекристаллизацию при определенных условиях. Вышеописанный способ позволяет получить агарициновую кислоту в чистом виде без примесей и повысить выход конечного продукта. 5 ил.
Способ получения агарициновой кислоты из гриба трутовика лекарственного (Fomitopsis officinalis Will., семейство трутовиковых -Polyporaceae, класс базидиомицетов - Basidiomycetes), включающий экстракцию измельченного сырья, разделение конечного продукта и сопутствующих веществ и очистку, отличающийся тем, что сырье, измельченное до размеров не более 3 мм, многократно экстрагируют 95%-ным этанолом при суммарном соотношении сырья и экстрагента 1 мас.ч. сырья: 25 об.ч. экстрагента при температуре 78°С; полученный экстракт упаривают до 6 об.ч. экстракта; отделение агарициновой кислоты проводят выдерживанием экстракта при температуре (-4) - (-5)°С в течение 12 ч с последующим отделением осадка агарициновой кислоты, а затем проводят очистку продукта промыванием 95%-ным этанолом, имеющим температуру (-4) - (-5)°С, с последующей 5-кратной перекристаллизацией агарициновой кислоты с использованием 95%-ного этанола.
| КОМПЛЕКСНАЯ ПЕРЕРАБОТКА ГРИБА ТРУТОВИКА ЛЕКАРСТВЕННОГО (FOMITOPSIS OFFICINALIS (VILL.: FR.) BOND. ET SING.) | 2004 |
|
RU2257222C1 |
| US 20060171958 А1, 03.08.2006 | |||
| Вещество, обладающее гипотермическим действием | 1990 |
|
SU1827257A1 |
| US 6852484, 08.02.2005 | |||
| Вещество, повышающее стрессоустойчивость | 1990 |
|
SU1813446A1 |
| Вещество, стимулирующее регенерацию тканей при комбинированном радиационном поражении и действии цитостатиков | 1990 |
|
SU1827258A1 |
Авторы
Даты
2008-08-10—Публикация
2007-01-09—Подача