Изобретение относится к области медицины, а именно к хирургии пищевода, и может быть использовано при пластике пищевода толстой кишкой после удаления пищевода и части желудка по поводу рубцовой стриктуры пищевода и рубцовой деформации желудка в связи с химическим ожогом пищевода и желудка.
Известны способы формирования толстокишечно-желудочного анастомоза, выполняемые при толстокишечной пластике пищевода, в которых предусматривается анастомозирование трансплантата с передней стенкой неизмененного желудка [1, 3]. Ряд авторов предлагают использовать при наложении кологастрального соустья при пластике пищевода по поводу его поражения антирефлюксный механизм [2, 4].
Однако данные способы не до конца удовлетворяют требованиям современной хирургической гастроэнтерологии. В отдаленном периоде самым неблагоприятным осложнением являются пептические поражения трансплантата вследствие рефлюкса агрессивного содержимого из желудка в искусственный пищевод и даже в глотку. К этому приводит отсутствие у анастомозов арефлюксных свойств или их недостаточной выраженности. Развивающиеся стеноз области анастомоза и сужение трансплантата выше места анастомозирования являются не только плохим функциональным результатом операции, но и требуют реконструктивных вмешательств.
Сложной задачей является наложение соустья между трансплантатом и культей желудка при резекции пищевода и части желудка по поводу рубцовых изменений вследствие химического ожога не только пищевода, но и желудка. Операцией выбора остается наложение соустья с культей желудка, создавая при этом «искусственную кардию».
Наиболее близким (прототипом) к предлагаемому способу является способ формирования анастомоза искусственного пищевода из толстой кишки с культей желудка, выполняемый А.Ф.Черноусовым и соавт. [5]. Кологастроанастомоз по типу «конец в бок» накладывают с передней стенкой антрального отдела в поперечном направлении. Поперечный анастомоз обеспечивает антирефлюксный эффект, кроме того, щелочная среда в антральном отделе предотвращает образование пептических язв трансплантата.
Недостатком этого метода является возможность возникновения рефлюкса содержимого желудка за счет недостаточного антирефлюксного механизма и отсутствия как такового клапана и смыкания его створок. В ряде случаев может возникать несостоятельность швов анастомоза вследствие нарушения кровоснабжения в трансплантате. Кроме того, присутствует недостаточный функциональный результат операции вследствие того, что выключается большая часть желудка из процесса пищеварения и отсутствует естественное прохождение пищи по всему желудку.
Задачей, решаемой данным изобретением, является исключение патологического воздействия рефлюкса содержимого желудка на толстокишечный трансплантат и пептических осложнений в нем, снижение риска развития несостоятельности швов пищеводно-толстокишечного анастомоза и достижение адекватного функционального результата операции.
Новый технический результат достигается применением нового способа формирования толстокишечно-желудочного анастомоза при пластике пищевода путем субтотальной резекции пищевода и проксимальной резекции желудка, формирования трансплантата из левой половины толстой кишки в антиперистальтической позиции, питаемого за счет брыжеечных сосудов, причем выполняют резекцию желудка с наложением трех механических швов, располагающихся под тупым углом друг к другу и большой кривизне желудка, моделируя свод желудка, поворачивают трансплантат вдоль своей оси на 90° против часовой стрелки, на аборальном конце толстокишечного трансплантата наносят циркулярный разрез серозно-мышечной оболочки в косом направлении, отступив 10 мм со стороны брыжеечных сосудов и 35-40 мм со стороны противобрыжеечного края, накладывают два ряда швов между трансплантатом и малой кривизной культи желудка, инвагинируя дистальный фрагмент кишки ниже циркулярного разреза в просвет культи желудка в виде дубликатуры, создают угол Гиса путем фиксации образованного свода к толстокишечному трансплантату.
В проанализированной авторами научно-медицинской и патентной литературе не найдено данных отличительных признаков, и они явным образом не следуют для специалиста из уровня техники. Данный способ прошел клинические испытания в НИИ гастроэнтерологии Сибирского государственного медицинского университета. Таким образом, данное техническое решение соответствует критериям изобретения "новизна", "изобретательский уровень" и "промышленно применимо".
Способ осуществляют следующим образом.
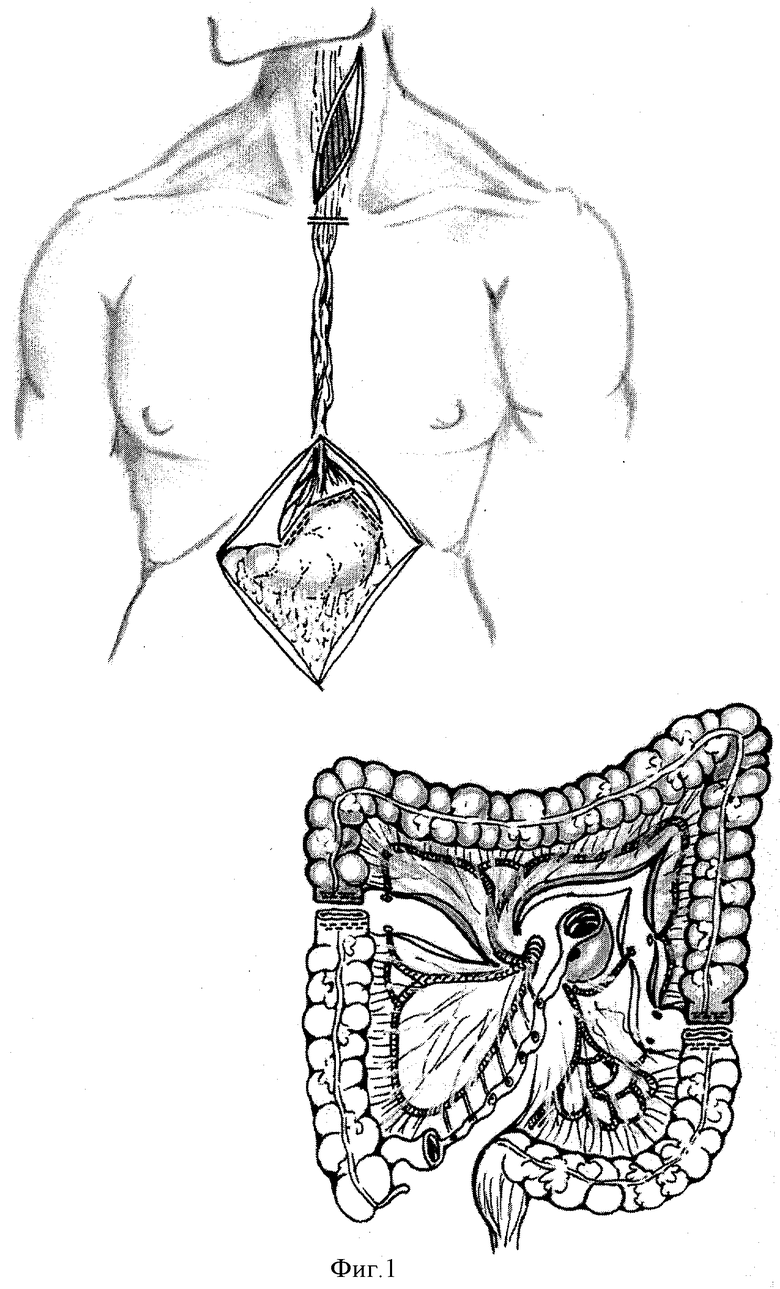
Производят верхнесрединную лапаротомию. Выполняют сагиттальную диафрагмокруротомию, мобилизуют пищевод до верхней трети грудного отдела. Косопоперечным разрезом на шее слева выделяют шейный отдел пищевода, сдвигая грудино-ключично-сосцевидную мышцу и трахею, лигируют сосуды пищевода и резецируют его. Выполняют резекцию желудка. Формируют трансплантат из левой половины толстой кишки, выкраивая антиперистальтический трансплантат на средней ободочной артерии (фиг.1).
Сформированный толстокишечный трансплантат проводят в заднем средостении и выводят в рану на шее. Накладывают колоэзофагоанастомоз «конец в конец» на шее.
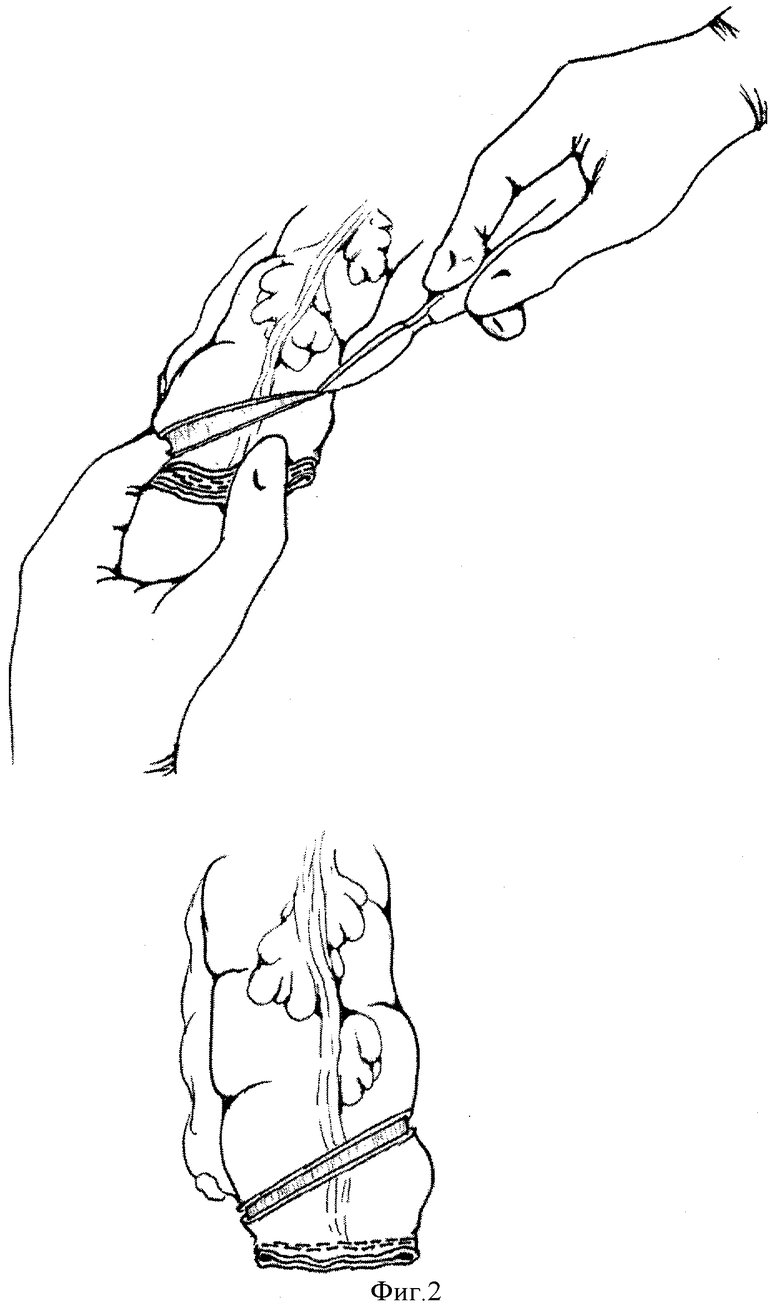
Проводят мобилизацию аборального края толстокишечного трансплантата на протяжении 35-40 мм со стороны противобрыжеечного края и 1 см со стороны брыжеечного края. Наносят на аборальном конце трансплантата циркулярный разрез серозно-мышечной оболочки в косом направлении, на брыжеечной части проходящий как можно ближе к месту резекции, на противобрыжеечной части располагающийся на 35-40 мм оральнее конца трансплантата, формируя таким образом две створки клапана и увеличивая их подвижность при функционировании клапана (фиг.2).
Выполняют резекцию желудка с помощью аппаратов УО-40. Для этого удаляют пораженную часть органа с захватом здоровых тканей и накладывают аппараты таким образом, чтобы сформировать свод желудка, образовывая тупой угол между большой кривизной и первым механическим швом, а также между первым и вторым механическим швами. Третий механический шов накладывают по направлению к двенадцатиперстной кишке, отступя на расстояние до 3 см от второго механического шва, оставляя место для выполнения анастомоза (фиг.3).
Поворачивают трансплантат вдоль своей оси на 90° против часовой стрелки таким образом, чтобы брыжеечная часть трансплантата располагалась по направлению механического шва в сторону двенадцатиперстной кишки.
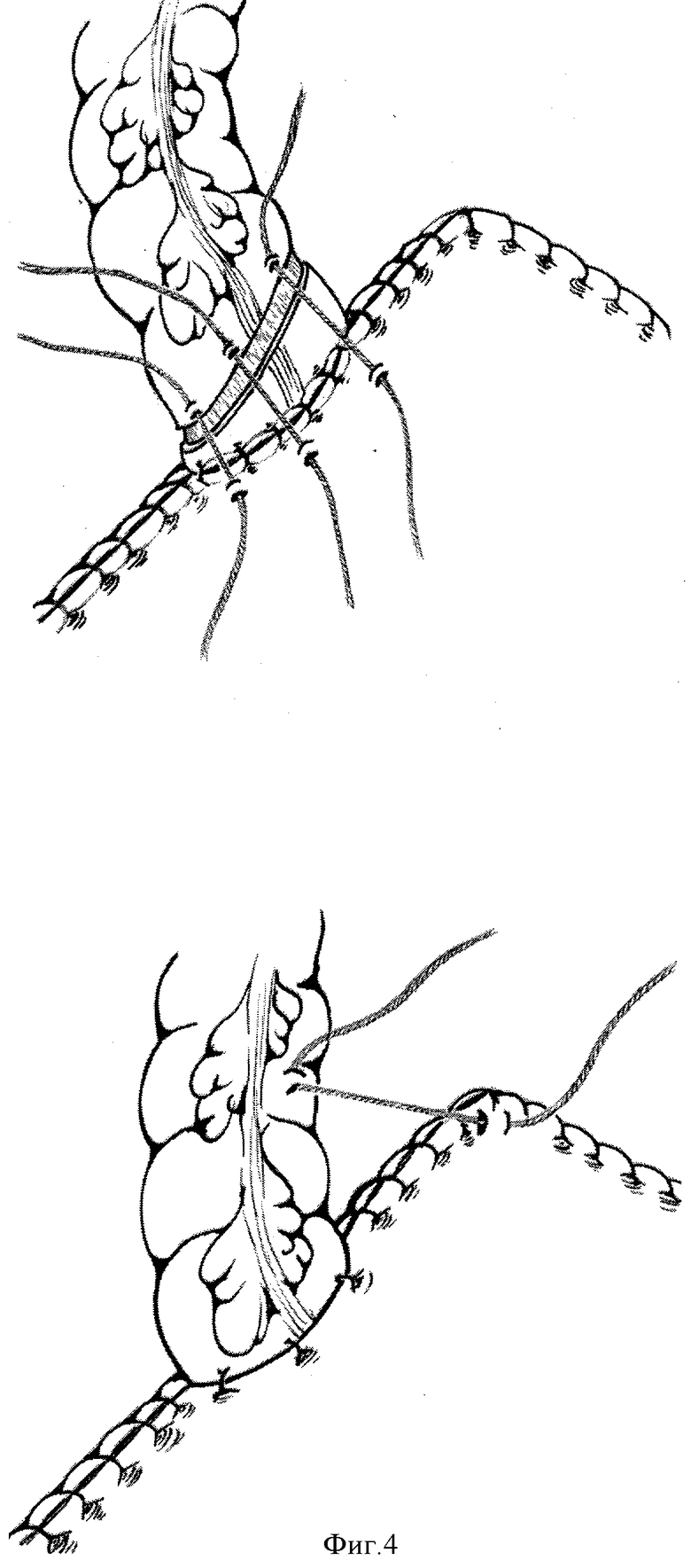
Накладывают два ряда швов между трансплантатом и культей желудка на участке между вторым и третьим механическими швами длиной до 3 см, формируя анастомоз. При этом формируют клапан путем инвагинации мобилизованного участка трансплантата в просвет культи желудка в виде дубликатуры с помощью наложения узловых швов на переднюю губу анастомоза с захватом края серозно-мышечной оболочки трансплантата, образовавшегося в результате циркулярного разреза, и серозно-мышечной оболочки культи желудка. Накладывают серозно-мышечные швы, укрывая механические швы линий резекции (фиг.4).
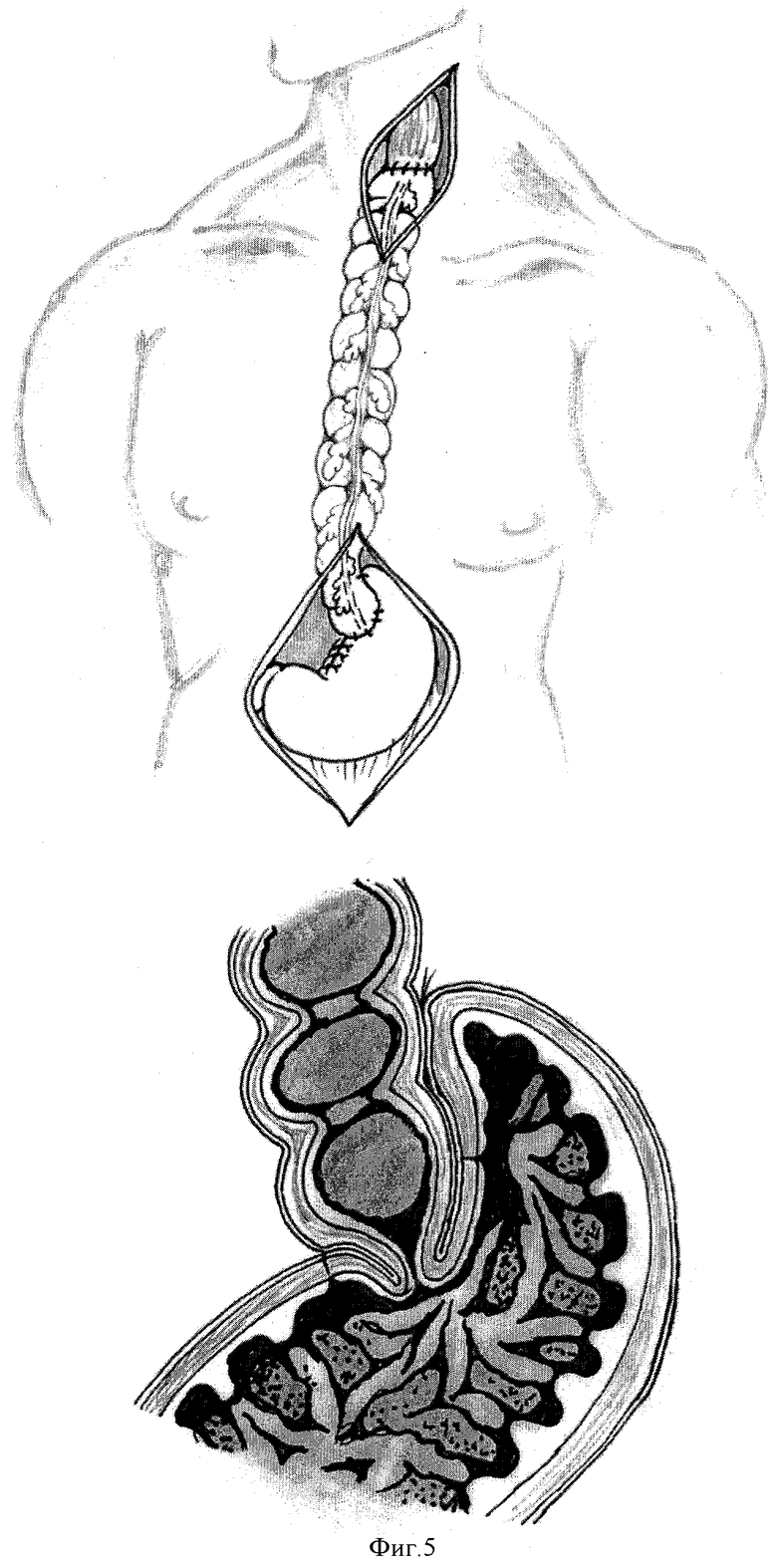
Создается свод желудка, который с помощью 2-4 швов подшивается к толстокишечному трансплантату, укрывая, таким образом, шов анастомоза и формируя острый угол Гиса (фиг.4, 5).
Пример выполнения данной операции.
Больная Шарова Алевтина Яковлевна, 1940 года рождения, поступила в клинику 08.01.2002 года с клиническим диагнозом:
Основное заболевание: Рубцовая стриктура шейного отдела пищевода. Состояние после химического ожога пищевода (уксусом) 1983 г. Состояние после экстирпации пищевода, пластики желудочным стеблем от 28.03.01 г. Наложение арефлюксной еюностомы от 12.04.01 в связи с некрозом шейного отдела трансплантата.
Целью госпитализации явился реконструктивный этап операции, закрытие еюностомы.
Данные инструментального исследования в предоперационном периоде:
УЗИ от 9.01.02: Осмотрен фрагмент шейного отдела пластики пищевода. Поперечник по наружному диаметру на различных участках от 6,7 мм до 11 мм (норма по ультразвуковым параметрам для пищевода). По контуру участка "пищевода" с малым размером фиброз окружающих тканей.
ФГС от 10.01.02: В устье пищевода рубцовая циркулярная стриктура с просветом до 4 мм.
Заключение: Рубцовая стриктура пищевода.
Рентгеноскопия пищевода от 3.10.01: Отмечается дисфагия при прохождении водорастворимого контраста и бария на уровне I физиологического сужения. Маленький глоток контрастного вещества проходит за несколько глотательных движений. Дисфагия смешанного генеза: имеется рубцовое сужение и психогенная. Затеков контрастного вещества не выявлено.
Заключение: Состояние после пластики пищевода желудочным стеблем, осложненное в раннем периоде несостоятельностью, в позднем - рубцовым сужением.
15.01.02 пациентке выполнена операция по предлагаемой методике с закрытием питающей еюностомы. Из верхнесрединного лапаротомного доступа выполнили сагиттальную диафрагмокруротомию, мобилизовали пищевод до верхней трети грудного отдела. Косо-поперечным разрезом на шее слева выделили шейный отдел пищевода, сдвигая грудино-ключично-сосцевидную мышцу и трахею, легировали сосуды пищевода и резецировали его. Дополнительно выполнили проксимальную резекцию желудка. Сформировали трансплантат из левой половины толстой кишки, выкроив антиперистальтический трансплантат на средней ободочной артерии.
Сформированный толстокишечный трансплантат провели в заднем средостении и вывели в рану на шее. Наложили колоэзофагоанастомоз «конец в конец» на шее.
Произвели мобилизацию аборального края толстокишечного трансплантата на протяжении 35-40 мм со стороны противобрыжеечного края и 1 см со стороны брыжеечного края. Нанесли на аборальном конце трансплантата циркулярный разрез серозно-мышечной оболочки в косом направлении, на брыжеечной части проходящий как можно ближе к месту резекции, на противобрыжеечной части располагающийся на 35-40 мм оральнее конца трансплантата.
Выполнили резекцию желудка с помощью аппаратов УО-40. При этом накладывали аппараты таким образом, чтобы сформировать свод желудка, образовывая тупой угол между большой кривизной и первым механическим швом, а также между первым и вторым механическим швами. Третий механический шов наложили по направлению к двенадцатиперстной кишке, отступя на расстояние до 3 см от второго механического шва, оставив место для выполнения анастомоза.
Повернули трансплантат вдоль своей оси на 90° против часовой стрелки таким образом, чтобы брыжеечная часть трансплантата располагалась по направлению механического шва в сторону двенадцатиперстной кишки.
Наложили два ряда швов между трансплантатом и культей желудка на участке между вторым и третьим механическими швами длиной до 3 см, формируя анастомоз. При этом сформировали клапан путем инвагинации мобилизованного участка трансплантата в просвет культи желудка в виде дубликатуры с помощью наложения узловых швов на переднюю губу анастомоза с захватом края серозно-мышечной оболочки трансплантата, образовавшегося в результате циркулярного разреза, и серозно-мышечной оболочки культи желудка. Наложили серозно-мышечные швы, укрывая механические швы линий резекции.
Созданный свод желудка подшили к толстокишечному трансплантату, укрыв, таким образом, шов анастомоза и сформировав острый угол Гиса. Ранний послеоперационный период протекал без осложнений, декомпрессионный желудочный зонд удален на 6 сутки, кормление через рот начато на 10 сутки.
При контрольном исследовании через полгода после операции пациентка субъективно жалоб не предъявляет. При объективном обследовании:
ФГС от 19.08.02: В области устья пищевода находится анастомоз, сомкнут, проходим свободно тубусом аппарата 10 мм, слизистая розовая без воспалительных и рубцовых изменений. Слизистая толстокишечного «пищевода» обычной окраски, на 48 см от резцов клапанный толстокишечно-желудочный анастомоз, свободно проходим, по линии анастомоза дефектов нет, слизистая без воспалительных изменений. Также аппарат проведен в культю желудка. Слизистая желудка с признаками атрофии, дефектов слизистой нет. Пилорус сомкнут, свободно проходим, ДПК б\о.
Заключение: Состояние после пластики пищевода. ТКЖ-анастомоз с нормальной функцией. Атрофический гастрит.
Рентгеноскопия желудка №1491 от 20.08.02: Загрудинно располагается толстокишечный трансплантат пищевода. Пищеводно-толстокишечный анастомоз конец в конец на уровне устья. Хорошо пропускает контраст. Трансплантат больше напоминает тонкую кишку по рельефу слизистой и контурам стенок, перистальтика в основном поступательная, но имеются и антиперистальтические редкие волны с обратным забросом контраста.
Заключение: Состояние после загрудинной пластики пищевода толстокишечным трансплантантом.
При обследовании через 3 года:
Рентгеноскопия желудка №96 от 22.02.06: Пищеводно-толстокишечный анастомоз конец в конец на уровне устья, широкий, свободно пропускает барий. Толстокишечный трансплантат располагается загрудинно, в виде трубки, с неровным контуром из-за складок, которые больше напоминают утолщенные складки тонкой кишки, чем гаустрацию толстой. Имеется передаточная пульсация сердца на н/3 трансплантата с кратковременной задержкой контраста под этим участком. Перистальтика поступательная без антиперистальтических волн. Клапанный толстокишечно-желудочный анастомоз раскрывается до 19-20 мм, поступление контраста в желудок порционное.
Заключение: Состояние после загрудинной пластики пищевода толстокишечным трансплантатом.
По предлагаемому способу оперировано 6 пациентов с указанной патологией. Сроки наблюдения составляют до 3,5 лет. Осложнений в ближайшем отдаленном периодах не отмечено, отмечена хорошая функция арефлюксного механизма.
Таким образом, предлагаемый способ формирования толстокишечно-желудочного анастомоза при пластике пищевода позволяет уменьшить риск развития рефлюкса в толстокишечный трансплантат и его осложнений с помощью создания инвагинационного клапана из мобилизованного аборального конца трансплантата со стороны противобрыжеечного края и нанесения на аборальном конце трансплантата циркулярного разреза серозно-мышечной оболочки в косом направлении, улучшающего функцию клапана. Усиление арефлюксных свойств достигается за счет формирования свода желудка, а также образования угла Гиса с помощью наложения серозно-мышечных швов между культей желудка (сформированным сводом) и трансплантатом. Методика формирования соустья, заключающаяся в наложении двух рядов швов, укреплении линии швов анастомоза в области противобрыжеечной части с помощью наложения швов при формировании угла Гиса значительно уменьшают риск несостоятельности анастомоза. Моделирование желудка позволяет включить в процесс пищеварения весь орган, что благоприятно сказывается на состоянии пациента в отдаленном послеоперационном периоде.
Список литературы
1. Витебский Я.Д. Клапанные анастомозы в хирургии пищеварительного тракта. М.: Медицина, 1988. - 112 с. (С.21-23).
2. Оноприев В.И., Дурлештер В.М., Сиюхов Р.Ш. Двадцатилетний опыт загрудинной тотальной колоэзофагопластики с использованием арефлюксного анастомоза. Хирургия. - 2003, №6. - С.50-54.
3. Симич П. Хирургия кишечника. Бухарест: Медицинское издательство, 1979, 399 с. (С.360).
4. Степанов Э.А., Разумовский А.Ю. Антирефлюксная защита трансплантата при колоэзофагопластике. Грудная хирургия. - 1987, №4. - С.87-92.
5. Черноусов А.Ф., Богопольский П.М., Курбанов Ф.С. Хирургия пищевода: Руководство для врачей. - М.: Медицина, 2000. - 352 с. (С.177-179).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЕЮНОГАСТРОПЛАСТИКИ ПРИ ГАСТРЭКТОМИИ | 1994 |
|
RU2121304C1 |
| СПОСОБ ВЫПОЛНЕНИЯ ОПЕРАЦИЙ НА ЖЕЛУДКЕ И ПИЩЕВОДЕ ПРИ НАЛИЧИИ ДОБАВОЧНОЙ ПЕЧЕНОЧНОЙ АРТЕРИИ | 2006 |
|
RU2302825C1 |
| СПОСОБ ЛЕЧЕНИЯ СОЧЕТАННОЙ ЯЗВЕННОЙ БОЛЕЗНИ ЖЕЛУДКА, ОСЛОЖНЕННОЙ ПИЛОРОБУЛЬБАРНЫМ СТЕНОЗОМ | 2000 |
|
RU2173093C1 |
| СПОСОБ ФОРМИРОВАНИЯ АРЕФЛЮКСНОГО ШЕЙНОГО ПИЩЕВОДНО-ТОЛСТОКИШЕЧНОГО АНАСТОМОЗА | 2001 |
|
RU2207069C2 |
| СПОСОБ ТОЛСТОКИШЕЧНОЙ ГАСТРОПЛАСТИКИ ПОСЛЕ ГАСТРЭКТОМИИ | 2004 |
|
RU2278619C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РЕФЛЮКС-ЭЗОФАГИТА ПРИ ОПЕРАЦИИ РЕКОНСТРУКТИВНОЙ ЕЮНОГАСТРОПЛАСТИКИ ПОСЛЕ ГАСТРЭКТОМИИ | 1999 |
|
RU2148958C1 |
| СПОСОБ ФОРМИРОВАНИЯ АРЕФЛЮКСНОГО ШЕЙНОГО ПИЩЕВОДНО-ЖЕЛУДОЧНОГО АНАСТОМОЗА | 1999 |
|
RU2143849C1 |
| СПОСОБ ДУОДЕНОПИЛОРОГАСТРОПЛАСТИКИ В ХИРУРГИИ ГАСТРОДУОДЕНАЛЬНЫХ ЯЗВ, ОСЛОЖНЕННЫХ ПРОТЯЖЕННЫМ ПИЛОРОБУЛЬБАРНЫМ СТЕНОЗОМ | 2001 |
|
RU2199279C1 |
| СПОСОБ РЕЗЕКЦИИ ЖЕЛУДКА ПРИ ТРУДНЫХ ЯЗВАХ ДВЕНАДЦАТИПЕРСТНОЙ КИШКИ | 2001 |
|
RU2206278C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ПИЛОРОБУЛЬБАРНЫХ ЯЗВ, ОСЛОЖНЕННЫХ СТЕНОЗОМ ПРИВРАТНИКА | 2000 |
|
RU2177731C2 |

Изобретение относится к области медицины, а именно к хирургии пищевода, может быть использовано при пластике пищевода толстой кишкой после удаления пищевода и части желудка по поводу рубцовой стриктуры пищевода и рубцовой деформации желудка в связи с химическим ожогом пищевода и желудка. Выполняют субтотальную резекцию пищевода и проксимальную резекцию желудка с наложением трех механических швов. Первый механический шов располагают под тупым углом к большой кривизне желудка и ко второму механическому шву. При этом формируют свод желудка. Третий механический шов накладывают по направлению к двенадцатиперстной кишке. Отступают при этом от второго механического шва с оставлением места для наложения анастомоза. Поворачивают трансплантат так, чтобы его брыжеечная часть располагалась по направлению механического шва в сторону двенадцатиперстной кишки. На аборальном конце толстокишечного трансплантата наносят циркулярный разрез серозно-мышечной оболочки в косом направлении, отступив 10 мм со стороны брыжеечных сосудов и 35-40 мм со стороны противобрыжеечного края. Накладывают два ряда швов между трансплантатом и малой кривизной культи желудка, инвагинируя дистальный фрагмент кишки ниже циркулярного разреза в просвет культи желудка в виде дупликатуры. Создают угол Гиса путем фиксации образованного свода желудка к толстокишечному трансплантату. Способ позволяет предупредить рефлюкс содержимого желудка в толстокишечный трансплантат и связанные с ним осложнения, снизить риск развития несостоятельности швов желудочно-толстокишечного анастомоза, обеспечивает адекватный функциональный результат операции. 5 ил.
Способ формирования толстокишечно-желудочного анастомоза при пластике пищевода, включающий субтотальную резекцию пищевода и проксимальную резекцию желудка, с последующим формированием трансплантата из левой половины толстой кишки в антиперистальтической позиции, питаемого за счет брыжеечных сосудов, отличающийся тем, что выполняют резекцию желудка с наложением трех механических швов, при этом первый механический шов располагают под тупым углом к большой кривизне и ко второму механическому шву, формируя свод желудка, а третий механический шов накладывают по направлению к двенадцатиперстной кишке, отступя от второго механического шва с оставлением места для наложения анастомоза, поворачивают трансплантат так, чтобы его брыжеечная часть располагалась по направлению механического шва в сторону двенадцатиперстной кишки, на аборальном конце толстокишечного трансплантата наносят циркулярный разрез серозно-мышечной оболочки в косом направлении, отступив 10 мм со стороны брыжеечных сосудов и 35-40 мм со стороны противобрыжеечного края, накладывают два ряда швов между трансплантатом и малой кривизной культи желудка, инвагинируя дистальный фрагмент кишки ниже циркулярного разреза в просвет культи желудка в виде дупликатуры, создают угол Гиса путем фиксации образованного свода желудка к толстокишечному трансплантату.
| ЧЕРНОУСОВ А.Ф | |||
| и др | |||
| Хирургия пищевода | |||
| Руководство для врачей | |||
| - М.: Медицина, 2000, с.177-179 | |||
| СПОСОБ ФОРМИРОВАНИЯ КОЛО-ГАСТРАЛЬНОГО АНАСТОМОЗА ПРИ ТОЛСТОКИШЕЧНОЙ ПЛАСТИКЕ ПИЩЕВОДА | 1999 |
|
RU2156611C1 |
| Способ толстокишечной эзофагопластики | 1989 |
|
SU1806620A1 |
| RU 2004116416 A, 10.11.2005 | |||
| KZ 990006, 06.01.1999 | |||
| HADIDI A.T | |||
| et al | |||
| A technique to improve vascularity in colon replacement of the esophagus, Eur | |||
| J | |||
| Pediatr | |||
| Surg., 2006, 16(1), 39-44. | |||
Авторы
Даты
2008-10-20—Публикация
2007-05-23—Подача