Изобретение относится к способу получения никотинальдегидов путем восстановления соответствующих морфолинамидов никотиновой кислоты.
Никотинальдегиды являются важными промежуточными продуктами или конечными продуктами в промышленной органической химии. Подходяще замещенные производные, такие как, например, арилникотинальдегиды, являются, в частности, ценными промежуточными продуктами для синтеза чрезвычайно ценных конечных продуктов или сами являются такими конечными продуктами, в частности, для защиты растений, такими как, например, фунгициды, инсектициды, гербициды или пестициды, или для получения высокоактивных фармацевтических веществ.
Таким образом, существует потребность в чрезвычайно экономном способе получения этих соединений со значительным промышленным выходом.
Альдегиды, как нестабильное окисленное состояние между спиртом и карбоновой кислотой, как правило, достигаются с трудностями. Ароматические альдегиды, в частности, легко окисляются в соответствующие карбоновые кислоты или диспропорционируют в щелочных условиях с образованием спирта и карбоновой кислоты. При восстановительном получении производных никотинальдегидов в качестве дополнительной побочной реакции встречается восстановление дигидропиридина.
Из литературы известны способы получения, в которых описано селективное восстановление производных карбоновой кислоты до альдегидной стадии. Для этих способов, как правило, требуется охлаждение реакционной смеси для сведения к минимуму излишнего восстановления.
Также известные специфические способы восстановления производных никотиновой кислоты. Таким образом, например, в DE-A 10005150 описан способ получения 5-арилникотинальдегидов путем восстановления соответствующих 5-арилникотинникотиновых кислот при помощи каталитической гидрогенизации.
Н.С.Brown и A.Tsukamoto в J. Am. Chem. Soc. 81, стр.502 (1959) описали восстановление никотинаминов при помощи триэтоксилитийалюминийгидрида. Однако для него, как необходимое условие, указана низкая температура реакции, и выход составляет меньше 90% от теории.
Другие известные способы получения никотинальдегидов путем восстановления приведены в следующем обзоре:
Из обзора видно, что известные способы или требуют дорогостоящих реагентов (примеры 1, 3, 10), применения неочищенных веществ, которые не являются доступными в промышленных количествах (примеры 1, 3, 11), могут осуществляться только с нитрилом, который сам получают в три стадии (примеры 2, 3, 4, 7, 9), или требуют низких температур (примеры 2, 4, 11). С точки зрения выхода, только примеры 1, 2 и 3 являются экономично выгодными. Если стоимость реагентов включить в общий баланс, то остается только способ из примера 2. Тем не менее, для последнего требуется три стадии реакции, исходя из никотиновой кислоты, и он зависит от поддержания низких температур.
Сейчас изобретателями настоящего изобретения неожиданно было обнаружено, что никотинальдегиды могут быть получены в эффективных количественных выходах путем восстановления в стандартных условиях (комнатная температура, атмосферное давление), если применяемыми исходными веществами являются соответствующие морфолинамиды.
Морфолинамиды никотиновой кислоты и их производные не были ранее известны в качестве предшественников альдегидов.
Таким образом, настоящее изобретение относится к способу получения никотинальдегидов, который характеризуется тем, что применяемыми исходными веществами для восстановления являются соответствующие морфолинамиды. Указанный способ предпочтительно осуществляют при комнатной температуре и без давления (при атмосферном давлении).
Восстановителями, которые являются предпочтительными в соответствии с настоящим изобретением, являются литийалкоксиалюминийгидриды, содержащие один - три алкокси радикала. Общая формула представляет собой LiAlH(4-n)(OR)n, где n может представлять собой =1, 2 или 3. Подходящими радикалами являются прямоцепочечные или разветвленные алифатические радикалы, такие как, например метил, этил и трет-бутил. Восстановление наиболее успешно селективно осуществляется с LiAlH(OEt)3. Также подходящим в качестве восстановителя в способе получения в соответствии с изобретением является LiAlH3(OEt), который значительно дешевле.
В предпочтительном варианте осуществления изобретения, морфолинамиды никотиновой кислоты формулы I

, в которой
R1', R1" каждый, независимо друг от друга, представляет собой Н, Hal, A, ОА, CH2R2 или Ar,
R2 представляет собой ОА или NA2,
А представляет собой неразветвленный или разветвленный алкил, содержащий 1-10 атомов углерода, в котором одна или две СН2 группы могут быть заменены атомами О или S и/или -СН=СН- группами, и/или также 1-7 атомов водорода могут быть заменены F.
Ar представляет собой ненасыщенную, частично или полностью насыщенную, моно- или полициклическую гомо- или гетероциклическую систему с гетероатомами О, N, S, которая незамещена или моно- или полизамещена Hal, A, OA, NA2, NO2, NASO2A, SO2NA, SO2A, и
Hal представляет собой F, Cl, Br или I, в качестве исходных веществ восстанавливаются до никотинальдегидов формулы II
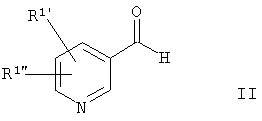 .
.
Вышеуказанные радикалы предпочтительно имеют значения, указанные далее:
R1', R1" каждый, независимо друг от друга, представляет собой Н, Hal, A, OA, CH2R2 или Аг, где A, Ar, Hal и R2 имеют одно из значений, указанных далее. R1', R1" представляет собой, в частности, водород, метокси, этокси, пропокси, бутокси, фтор, хлор, бром, йод, фенил или о-, м или n-замещенный фенил. R1' более предпочтительно представляет собой и-фторфенил или бром и R1" одновременно представляет собой водород.
Hal представляет собой фтор, хлор, бром или йод, предпочтительно фтор, хлор или бром.
R2 представляет собой OA или NA2, где А имеет значения, указанные выше и в дальнейшем.
А представляет собой алкил, который является неразветвленным (линейным) или разветвленным, и имеет 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 атомов углерода.
А предпочтительно представляет собой метил, кроме того, этил, пропил, изопропил, бутил, изобутил, втор-бутил или трет-бутил, кроме того, также пентил, 1-, 2- или 3-метилбутил, 1,1-, 1,2- или 2,2-диметилпропил, 1-этилпропил, гексил, 1-, 2-, 3- или 4-метилпентил, 1,1-, 1,2-, 1,3-, 2,2-, 2,3- или 3,3-диметилбутил, 1- или 2-этилбутил, 1-этил-1-метилпропил, 1-этил-2-метилпропил, 1,1,2- или 1,2,2-триметилпропил, кроме того, предпочтительно, например, трифторметил.
А наиболее предпочтительно представляет собой алкил, содержащий 1-6 атомов углерода, предпочтительно метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил, гексил, трифторметил, пентафторэтил или 1,1,1-трифторэтил. Кроме того, А представляет собой циклоалкил, предпочтительно циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил или 2,6,6-триметилбицикло-[3.1.1]гептил, но также моно- или бициклические терпены, предпочтительно n-ментан, ментол, пинан, борнан или камфора, куда включены каждая известная стереоизомерная форма или адамантил. Для камфоры это обозначение включает как L-камфору, так и D-камфору.
Ar представляет собой ненасыщенную, частично или полностью насыщенную, моно- или полициклическую гомо- или гетероциклическую систему с гетероатомами О, N, S, которая незамещена или моно- или полизамещена Hal, A, OA, NA2, NO2, NASO2A, SO2NA2, SO2А.
Предпочтительными циклическими системами являются незамещенный или замещенный фенил, нафтил или бифенил, более предпочтительно фенил, о-, м- или n-толил, о-, м- или n-цианофенил, о-, м- или n-метоксифенил, о-, м- или n-фторфенил, о-, м- или n-бромфенил, о-, м- или n-хлорфенил, более предпочтительно 2,3-, 2,4-, 2,5-, 2,6-, 3,4- или 3,5-дифторфенил, 2,3-, 2,4-, 2,5-, 2,6-, 3,4- или 3,5-дихлорфенил, 2,3-, 2,4-, 2,5-, 2,6-, 3,4- или 3,5-дибромфенил, 2-фтор-4-бромфенил, 2,5-дифтор-4-бромфенил.
Более предпочтительными исходными веществами для синтеза альдегида в соответствии с изобретением являются морфолинамид 5-(4-фторфенил)никотиновой кислоты и морфолинамид 3-бромникотинникотиновой кислоты.
Настоящее изобретение также относится к применению морфолинамидов никотиновой кислоты, предпочтительно морфолинамида 5-(4-фторфенил)никотиновой кислоты или морфолинамида 5-бромникотиновой кислоты, для получения соответствующих никотинальдегидов.
Кроме того, настоящее изобретение относится к морфолинамиду 5-(4-фторфенил)никотиновой кислоты и морфолинамиду 5-бромникотиновой кислоты в качестве исходных веществ при синтезе в соответствии с изобретением.
Взаимодействие в соответствии с изобретением, как правило, осуществляют в инертном растворителе. Примерами подходящих инертных растворителей для вышеописанных реакций являются углеводороды, такие как гексан, петролейный эфир, бензол, толуол или ксилол; простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, тетрагидрофуран (ТГФ) или диоксан; гликолевые эфиры, такие как этиленгликольдиметиловый эфир (диглим); или смеси указанных растворителей. Более предпочтительными являются простые эфиры, в частности тетрагидрофуран.
Количество растворителя не является решающим, как правило, от 5 г до 500 г, предпочтительно от 10 г до 100 г растворителя можно прибавлять на грамм исходного вещества.
Температура реакции для вышеописанных реакций, в зависимости от применяемых условий, находится в интервале приблизительно от -10° до 200°, обычно от -10° до 100°, в частности, от 0° до 50°, однако предпочтительно 10°-40°, более предпочтительной является комнатная температура.
Время реакции, в зависимости от применяемых условий, составляет от нескольких секунд до нескольких часов, предпочтительно от 1 минуты до 3 часов. Тем не менее, взаимодействие в соответствии с изобретением обычно завершается через 0,1-1,5 часа.
Для целей настоящего изобретения под "применяемыми условиями" подразумевают способ замещения морфолинамида никотиновой кислоты, тип и количество растворителя, тип и количество восстановителя, длительность реакции, температуру реакции и другие детали осуществления взаимодействия, такие как, например, скорость мешалки или другие характеристики реакционного сосуда.
Как правило, окончание восстановления в соответствии с изобретением до альдегида определяют при помощи подходящих аналитических способов, например тонкослойной хроматографии или ВЭЖХ, и восстановление прекращают.
Никотинальдегиды в соответствии с изобретением могут быть получены после удаления растворителя при помощи стадий обычной обработки, таких как, например, добавление к реакционной смеси воды или кислоты и экстракцию. Может являться благоприятной дальнейшая перегонка или кристаллизация для дополнительной очистки продукта.
Морфолинамиды никотиновой кислоты, которые применяются в качестве исходных веществ для способа в соответствии с изобретением, могут быть получены при помощи методов, известных per se, как описано в литературе (например, в стандартных работах, таких как Houben-Weyl, Methoden der organischen Chemie [Методы органической химии], Georg-Thieme-Verlag, Штутгарт), в соответствии с условиями реакций, которые известны и приемлемы для указанных реакций. Также при этом можно применять разнообразные модификации, которые известны per se, но о которых здесь подробно не упоминается.
Как правило, применяют следующую методику.
Никотиновую кислоту превращают, используя подходящий реагент, такой как, например, тионилхлорид, в хлорангидрид, который затем подвергают взаимодействию с желательным амином с получением амида.
Для защиты заместителей от нежелательных взаимодействий при восстановлении в соответствии с изобретением и/или последующих этапах обработки, применяют защитные группы, если это является подходящим, и удаляют после восстановления морфолинамида никотиновой кислоты. Способы применения защитных групп описаны, например, в Theodora W.Green, Peter G.M. Wuts: Protective Groups in Organic Synthesis, 3-е издание John Wiley & Sons (1999).
Даже без дополнительных вариантов осуществления изобретения предполагается, что специалист в данной области техники способен использовать вышеприведенное описание в самом широком объеме. Следовательно, предпочтительные варианты осуществления изобретения приведены только в качестве описательных раскрытий, которые никоим образом не ограничивают изобретение.
Пример 1: Получение 5-(4-фторфенил)никотинальдегида из морфолинамида 5-(4-фторфенил)пиридин-3-карбоновой кислоты
(а) Синтез предшественника 5-(4-фторфенил)пиридин-3-карбоновой кислоты
Сначала, 5-(4-фторфенил)пиридин-3-карбоновую кислоту получали путем сочетания Сузуки (N.Miyaura, A.Suzuki, Chem. Rev. 95, 2457 (1995)) путем взаимодействия 5-бромникотиновой кислоты с n-фторбензолбороновой кислотой (обе являются коммерчески доступными) в условиях реакции, которые известны per se, получая 5-(4-фторфенил)пиридин-3-карбоновую кислоту.
(b1) Синтез морфолинамида 5-(4-фторфенил)пиридин-3-карбоновой кислоты - Вариант 1
В начальной стадии 25,6 г 5-(4-фторфенил)никотиновой кислоты вносили в 200 мл толуола и затем добавляли 25,1 г тионилхлорида при комнатной температуре. После этого смесь нагревали при 90°С в течение 18 часов и затем непрореагировавший тионилхлорид и некоторое количество растворителя отгоняли. Затем отогнанный объем восстанавливали толуолом, добавляли 12,4 г морфолина при 80-100°С, и реакционную смесь охлаждали через 2 часа. Значение рН устанавливали на 8 путем добавления раствора гидроксида натрия и продукт отделяли путем экстрагирования толуолом. После обесцвечивания при помощи активированного угля и удаления растворителя путем перегонки оставалось 27,7 г морфолинамида 5-(4-фторфенил)пиридин-3-карбоновой кислоты в виде твердого вещества (точка плавления: 100-102°С, выход: 81% теории).
(b2) Синтез морфолинамида 5-(4-фторфенил)пиридин-3-карбоновой кислоты - Вариант 2
1,2 г Pd[Р(Ph)3]4 и 7,6 г n-фторбензолбороновой кислоты добавляли к раствору 14,3 г морфолинамида 5-бромникотиновой кислоты в 100 г ТГФ. После этого по каплям добавляли раствор 8,0 г Na2CO3 в 25 г воды при перемешивании при 65°С. Через 16 часов реакционную смесь охлаждали и упаривали на роторном испарителе. Остаток ресуспендировали в дихлорметане, добавляли активированный уголь и смесь фильтровали. При повторной экстракции фильтрата водой и упаривании на роторном испарителе получали остаток 15,7 г, который, согласно ВЭЖХ; содержал 89% морфолинамида 5-(4-фторфенил)пиридин-3-карбоновой кислоты (чистый выход 93% теории). При перекристаллизации из этилацетата получали 8,0 г морфолинамида 5-(4-фторфенил)пиридин-3-карбоновой кислоты, который имеет чистоту 99,6% при анализе ВЭЖХ (53,3% теории).
(с) Получение 5-(4-фторфенил)никотинальдегида
6,0 г морфолинамида 5-(4-фторфенил)пиридин-3-карбоновой кислоты из примера 1(b) растворяли в 30 мл ТГФ и добавляли 57 г 13,6% раствора LiAlH-(OEt)3 в ТГФ в течение 10 минут при 30°С-35°С. Через 1 час добавляли 30 мл 12,5% серной кислоты и органическую фазу отделяли. Значение рН водной фазы доводили до рН 1 при помощи серной кислоты и несколько раз экстрагировали метил трет-бутиловым эфиром. Затем органические фазы объединяли, один раз экстрагировали водой и после этого упаривали, получая остаток 4,3 г, который содержал 97% по весу 5-(4-фторфенил)пиридин-3-карбальдегида (выход = 98% теории).
Пример 2 (сравнительный пример относительно примера 1, с применением пиперидинамида вместо морфолинамида): получение 5-(4-фторфенил)-никотинальдегида из пиперидинамида 5-(4-фторфенил)пиридин-3-карбоновой кислоты
36,7 г 10% раствора LiAlH4 разводили 75 г ТГФ и затем добавляли смесь 8,88 г этилацетата и 75 г ТГФ при 0°С. При -7°С добавляли раствор пиперидинамида 6,8 г 5-(4-фторфенил)пиридин-3-карбоновой кислоты в 24,7 мл ТГФ. Через три часа смесь добавляли к 190 г 10% серной кислоты. Значение рН устанавливали на 3 при помощи раствора гидроксида натрия и после этого ТГФ в основном удаляли путем перегонки. При экстрагировании метил трет-бутиловым эфиром и упаривании получали 2,6 г твердого вещества (содержание в соответствии с ВЭЖХ 67% площади, что соотв. 36% теории).
Пример 3: Получение 5-бромникотинальдегида из морфолинамида 5-бромпиридин-3-карбоновой кислоты
(а) Синтез морфолинамида 5-бромпиридин-3-карбоновой кислоты
50,4 г 5-бромникотиновой кислоты и 87,5 г морфолина нагревали в колбе с обратным холодильником в 200 мл ксилола и образованную воду отгоняли. После охлаждения реакционную смесь трижды экстрагировали 10% раствором гидроксида натрия и затем дважды водой. После этого ксилол отгоняли, остаток перекристаллизовывали из этилацетата. Выход после высушивания составил 19,2 г (28,3% теории). Точка плавления 80°С.
(b) Получение 5-бромникотинальдегида
1,75 г порошка литийалюминийгидрида суспендировали в 64 г ТГФ. Затем по каплям добавляли смесь 5,9 г этилацетата и 28 г ТГФ при охлаждении. Через 30 минут эту реакционную смесь по каплям при 0°С-10°С добавляли к раствору 5,0 г морфолинамида 5-бромпиридин-3-карбоновой кислоты из примера 3(а) в 30 г ТГФ (это соответствует 150% избытку восстановителя). Через 1 час реакционную смесь вливали в 35 мл 12% серной кислоты и органическую фазу выпаривали насухо. При перекристаллизации из МТВ эфира и высушивании получали 1,91 г продукта (= 55,7% теории). Точка плавления 95°С.
Как можно видеть при сравнении соответствующих выходов реакций из примеров 1 и 2, применение пиперидинамида никотиновой кислоты, как альтернатива никотинамиду, но который по своей структуре очень сходен с морфолинамидом - приводит к значительному ухудшению реакции.
В противоположность этому, лучшего выхода можно достичь при применении морфолинамида, даже при большом избытке восстановителя (пример 3), по сравнению со случаем с надлежащей стехиометрией в примере 2, в котором в качестве аминового компонента применяют пипередин.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 5-(4-ФТОРФЕНИЛ)НИКОТИНАЛЬДЕГИДА СОЕДИНЕНИЯ | 2001 |
|
RU2256653C2 |
| СПОСОБ КРИСТАЛЛИЗАЦИИ СОЛЕЙ ГУАНИДИНИЯ | 2004 |
|
RU2374224C2 |
| ПРОИЗВОДНЫЕ ПИПЕРАЗИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1997 |
|
RU2180660C2 |
| ПРОИЗВОДНЫЕ ФЕНОКСИ-N-[4-(1,1-ДИОКСОИЗОТИАЗОЛИДИН-2-ИЛ)ФЕНИЛ]-ВАЛЕРАМИДА И ДРУГИЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ ФАКТОРА КОАГУЛЯЦИИ Ха ДЛЯ ЛЕЧЕНИЯ ТРОМБЭМБОЛИЧЕСКИХ БОЛЕЗНЕЙ И ОПУХОЛЕЙ | 2002 |
|
RU2301228C2 |
| 3-БЕНЗИЛПИПЕРИДИНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1998 |
|
RU2194047C2 |
| ПРОИЗВОДНЫЕ ПИПЕРИДИНИЛМЕТИЛОКСАЗОЛИДИН-2-ОНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1996 |
|
RU2175970C2 |
| ТИЕНОПИРИДИНЫ | 2006 |
|
RU2415859C2 |
| ПРОИЗВОДНЫЕ ПИПЕРАЗИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1998 |
|
RU2194048C2 |
| ПРОИЗВОДНЫЕ АМИНО(ТИО)ЭФИРОВ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1995 |
|
RU2155753C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3-АЛКАНОИЛ- И 3-АЛКИЛИНДОЛОВ | 1999 |
|
RU2260589C2 |
Изобретение относится к способу получения никотинальдегидов реакцией восстановления, который характеризуется тем, что в качестве исходных эдуктов в реакции восстановления используют морфолинамиды никотиновой кислоты формулы I, 
в которой R1', R1" каждый, независимо друг от друга, представляет собой Н, Hal, А, ОА, СН2R2 или Ar, R2 представляет собой ОА или NA2, А представляет собой неразветвленный или разветвленный алкил, содержащий 1-10 атомов углерода, в которой одна или две СН2 группы могут быть заменены атомами О или S и/или -СН=СН-группами и/или также 1-7 атомов водорода могут быть заменены F, Аг, представляет собой ненасыщенную, частично или полностью насыщенную, моно- или полициклическую гомо- или гетероциклическую систему с гетероатомами О, N, S, которая незамещена или моно- или полизамещена Hal, А, ОА, NA2, NO2, NASO2A, SO2NA, SO2A и Hal представляет собой F, Cl, Br или I, также к применению морфолинамидов никотиновой кислоты формулы I, в реакции восстановления, для получения соответствующих никотинальдегидов, и к исходным эдуктам формулы I. Технический результат: увеличение выхода никотинальдегидов. 3 н. и 5 з.п. ф-лы, 1 табл.

в которой R1', R1" каждый, независимо друг от друга, представляет собой Н, Hal, A, ОА, CH2R2 или Ar,
R2 представляет собой ОА или NA2,
А представляет собой неразветвленный или разветвленный алкил,
содержащий 1-10 атомов углерода, в которой одна или две СН2 группы могут быть заменены атомами О или S и/или -СН=СН- группами и/или также 1-7 атомов водорода могут быть заменены F,
Ar представляет собой ненасыщенную, частично или полностью насыщенную, моно- или полициклическую гомо- или гетероциклическую систему с гетероатомами О, N, S, которая незамещена или моно- или полизамещена Hal, А, ОА, NA2, NO2, NASO2A, SO2NA, SO2А, и Hal представляет собой F, Cl, Br или I.
 ,
,
в которой R1', R1" каждый, независимо друг от друга, представляет собой Н, Hal, A, ОА, CH2R2 или Ar,
R2 представляет собой ОА или NA2,
А представляет собой неразветвленный или разветвленный алкил, содержащий 1-10 атомов углерода, в которой одна или две СН2 группы могут быть заменены атомами О или S и/или -СН=СН- группами и/или также 1-7 атомов водорода могут быть заменены F,
Ar представляет собой ненасыщенную, частично или полностью насыщенную, моно- или полициклическую гомо- или гетероциклическую систему с гетероатомами О, N, S, которая незамещена или моно- или полизамещена Hal, А, ОА, NA2, NO2, NASO2A, SO2NA, SO2A, и
Hal представляет собой F, Cl, Br или I,
в реакции восстановления для получения соответствующих никотинальдегидов.
а) морфолинамид 5-(4-фторфенил)никотиновой кислоты,
б) морфолинамид 5-бромникотиновой кислоты.
| DOUAT, CELINE et al | |||
| "Synthesis of N-protected | |||
| Alpha-, aminoaldehydes from their morfoline amide derivatives", TETRAHEDRON LETTERS, 41(1), 37-40, Seite 39 - Seite 40; tabelle 1 | |||
| SAMMAKIA, TAREK et al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2008-11-27—Публикация
2004-03-27—Подача