Изобретение относится к способу кристаллизации соединений формулы I или их кислото-аддитивных солей
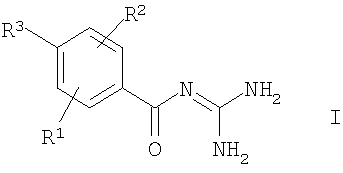
в которой
R1 - R4SO2- или А;
R2 и R3, независимо друг от друга, Н, Hal, алкил, содержащий 1-12 атомов углерода, R4SO2-, Ar или Het;
R4 - арил или алкил, содержащий 1-12 атомов углерода;
Het - насыщенный, ненасыщенный или ароматический, моно- или бициклический, гетероциклический или линейный или разветвленный органический радикал, содержащий один или несколько гетероатомов, который незамещен или моно- или полизамещен A, COAr, COHet и/или Hal;
Ar - фенильный радикал, который незамещен или моно- или полизамещен А и/или Hal, ОН, ОА, СООН, СООА, CONH2, CONA2, CONHA, CN, NO2, NH2, NHA, NA2, NHCOA, CF3 или SO2A;
А - прямоцепочечный или разветвленный алкил или гидроксиалкил, содержащий 1-10 атомов углерода, алкенил или алкоксиалкил, содержащий 2-10 атомов углерода,
и
Hal - F, Cl, Br, I,
который отличается тем, что соответствующие соединения формулы I или их смеси с примесями растворяют при данной температуре в воде, которая фактически насыщена по крайней мере одним несмешивающимся с водой растворителем и необязательно содержит один или несколько смешивающихся с водой растворителей, и соединения формулы подвергают кристаллизации I при низшей температуре.
Соединения формулы I могут иметь один или несколько хиральных центров. Следовательно, они могут встречаться в различных энантиомерных формах и существовать в рацемической или оптически активной форме. Таким образом, изобретение также относится к оптически активным формам (стереоизомерам), энантиомерам, рацематам, диастереомерам и гидратам и сольватам этих соединений. Таутомерные формы соединений формулы I также подпадают под объем изобретения.
Сульфонилбензоилгуанидины известны и описаны, например, в ЕР 0758644 A1. Эти вещества являются ингибиторами клеточного Na+/H+ антипортера, то есть активными компонентами, которые ингибируют механизм обмена Na+/H+ в клетках (Dusing и др., Med. Klin. 1992, 87, 367-384) и, соответственно, являются хорошими антиаритмическими средствами, которые пригодны, в частности, для лечения аритмии, возникающей в результате кислородной недостаточности.
Эти вещества обладают хорошим кардиозащитным действием и поэтому чрезвычайно пригодны для лечения острого инфаркта миокарда, профилактики инфаркта, послеинфарктного лечения, хронической сердечной недостаточности и для лечения стенокардии. Кроме того, они противодействуют всем патологическим гипоксическим и ишемическим повреждениям, обеспечивая возможность лечения заболеваний, вызванных первично или вторично таким повреждением. Эти активные компоненты также чрезвычайно пригодны для профилактического применения.
Благодаря профилактическому действию этих веществ на патологические гипоксические или ишемические состояния обеспечиваются дополнительные возможные применения при хирургических вмешательствах для профилактики временного недостаточного кровоснабжения органов, при пересадке органов для защиты удаленных органов, при ангиопластических сосудистых или сердечных вмешательствах, при ишемии нервной системы, при лечении шоковых состояний и для предотвращения гипертонической болезни.
Кроме того, эти соединения также могут применяться в качестве терапевтических средств при заболеваниях, вызванных пролиферацией клеток, таких как артериосклероз, диабет и поздние осложнения диабета, опухолевые заболевания, фиброзные заболевания, в частности легких, печени и почек, гипертрофии и гиперплазии органов. Дополнительно, соединения пригодны для диагностического применения для выявления заболеваний, сопровождающихся повышенной активностью Na+/H+ антипортера, например, в эритроцитах, тромбоцитах или лейкоцитах.
Соответственно, соединения могут применяться в качестве активных компонентов лекарственных средств для лечения людей и в ветеринарии. Они также могут применяться в качестве промежуточных продуктов для приготовления дальнейших фармацевтически активных компонентов.
Соединения формулы I могут быть получены, например, в соответствии с ЕР 0758644. В этих способах, активные компоненты обычно получают в количестве 95-99% ВЭЖХ площади, что не соответствует требованиям для активных компонентов лекарственных средств. При этом необходима дополнительная очистка.
Однако перекристаллизация продуктов из воды или обычных органических растворителей практически невозможна. Поскольку продукты характеризуются исключительно низкой растворимостью (даже при повышенных температурах), то это вызывает плохую кристаллизацию и получение кристаллов недостаточной чистоты. Даже повторная кристаллизация из воды или обычных органических растворителей не приводит к получению вещества достаточной чистоты.
Возможно осуществлять очистку неочищенного продукта путем растворения в большом количестве воды и затем концентрировать водный раствор при пониженном давлении до фракции исходного объема, при этом продукт выкристаллизовывается. Недостатком такого способа является очень большая продолжительность процесса (для концентрации водных растворов необходимо несколько дней в случае больших партий) и потеря последующего продукта вследствие гидролиза.
Таким образом, задачей настоящего изобретения является обеспечение улучшенного способа кристаллизации соединений формулы I и их кислото-аддитивных солей, который может применяться в значительных промышленных масштабах.
Эта задача решается при помощи способа в соответствии с изобретением кристаллизации соединений формулы I, который характеризуется тем, что соответствующие соединения формулы I или их смеси с примесями растворяют при данной температуре в воде, которая фактически насыщена по крайней мере одним несмешивающимся с водой растворителем и необязательно содержит один или несколько смешивающихся с водой растворителей, и соединения формулы I подвергают кристаллизации при низшей температуре.
В соединениях формул I радикалы имеют следующие предпочтительные значения.
R1 предпочтительно представляет собой R4SO2- или А.
R2 в соединениях формулы I предпочтительно находится в орто-положении к гуанидиновому радикалу и предпочтительно представляет собой Н или алкил, содержащий 1-7 атомов углерода, в особенности Н или метил.
R3 предпочтительно представляет собой Н, алкил, содержащий 1-7 атомов углерода, R4SO2- или Het, в частности R4SO2- или Het.
R4 предпочтительно представляет собой фенил, м-, о- или n-толил или метил, этил, изопропил, н-бутил или н-пентил. Наиболее предпочтительным является метил или этил, в особенности метил.
Ar предпочтительно представляет собой фенил, м-, о- или n-метил или метоксифенил.
Het предпочтительно представляет собой
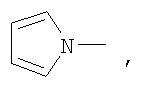
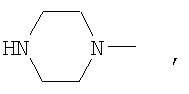
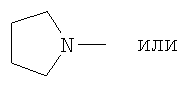
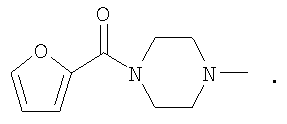
Hal предпочтительно представляет собой Cl или Br, в особенности F или Cl.
Способ в соответствии с изобретением чрезвычайно пригоден для кристаллизации соединений формулы Ia-Ie или их кислото-аддитивных солей:
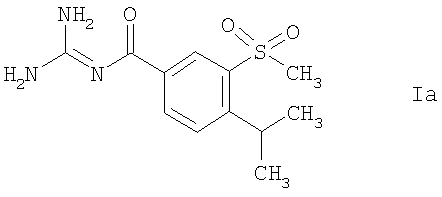
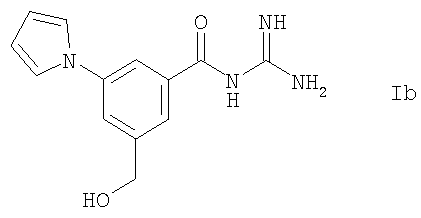

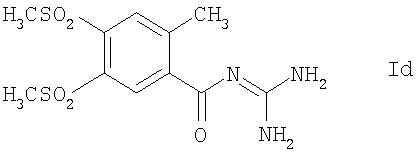
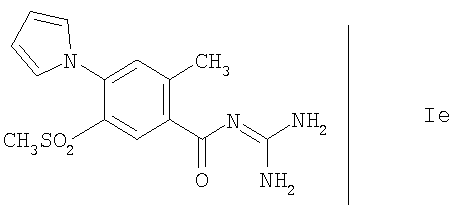
Реакцию способа в соответствии с изобретением легко осуществлять, так как соединения формулы I можно перекристаллизовывать, если применяемым растворителем является вода, которая фактически насыщена несмешивающимся с водой растворителем. Это является совершенно неожиданным, так как растворимость соединений формулы I в чистых растворителях, то есть в воде или одном или более несмешивающихся с водой растворителях, является недостаточной для обеспечения эффективной кристаллизации. Тем не менее, с системой растворителей в соответствии с изобретением можно достичь отличного объемного выхода, и при этом обеспечить очень хорошую чистоту (>99,7% ВЭЖХ площади), даже в случае больших партий.
Для практического осуществления не является необходимым точно устанавливать насыщенное соотношение компонентов смеси двух растворителей. Предпочтительно применять избыток несмешивающегося с водой растворителя. После растворения продукта в смеси растворителей при повышенных температурах избыток несмешивающегося с водой растворителя предпочтительно удаляют и раствор оставляют охладиться для выкристаллизации. Так как неполное удаление избытка несмешивающегося с водой растворителя не обладает отрицательным влиянием на кристаллизацию, то кристаллизацию также можно осуществлять непосредственно из двухфазной смеси.
Подходящими несмешивающимися с водой растворителями для способа в соответствии с изобретением являются, как правило, все известные растворители, которые не смешиваются с водой в первом приближении. Они предпочтительно представляют собой относительно длинноцепочечные несмешивающиеся с водой кетоны, такие как, например, метилэтилкетон, или алкилалканоаты, такие как, например, этилацетат, изопропилацетат, метилацетат или этилпропионат. Кроме того, предпочтительно могут применяться ароматические растворители или высшие спирты, такие как, например, бутанол. Особенно предпочтительным является толуол или ксилол. Тем не менее, после сравнения всех значимых параметров (выход, чистота, цена, приемлемость для окружающей среды и т.д.) предпочтительными по сравнению с другими растворителями являются алкилалканоаты, в особенности этилацетат.
Способ в соответствии с изобретением дополнительно может быть усовершенствован при применении на практике при использовании многокомпонентных смесей. Предпочтительной является смесь воды, несмешивающегося с водой растворителя и спирта, в частности смесь воды, этанола и этилацетата. Предпочтительными диапазонами концентраций являются те концентрации, при которых добавляемый к смеси растворителей спирт не содействует полному смешиванию воды и несмешивающегося с водой растворителя.
Спиртами, которые могут применяться, являются, в частности, предпочтительно этанол, метанол или н- или изопропанол.
Вместо спирта также можно применять кетоны и нитрилы. Предпочтительными являются растворимые в воде кетоны, в особенности ацетон.
Соединения формулы I предпочтительно растворяют в соответствующей смеси растворителей при повышенных температурах, предпочтительно при 30-180°С, в особенности при 60-100°С и чрезвычайно предпочтительно при 60-70°С, и осуществляют кристаллизацию при пониженных температурах, предпочтительно при комнатной температуре.
Продолжительность реакции кристаллизации зависит от выбранных условий реакции. Как правило, кристаллизация продолжается от 30 минут до 2 дней, предпочтительно 1-15 часов.
В предпочтительном варианте осуществления способа кристаллизации в соответствии с изобретением, значение рН устанавливают равным 1-3,5; в частности 1-2, при помощи подходящей кислоты (например, используя HCl в случае гидрохлоридов, используя метансульфоновые кислоты в случае метансульфоната) перед кристаллизацией или при кристаллизации.
Кислотами, которые добавляются перед кристаллизацией или при кристаллизации, также являются те, которые образуют физиологически приемлемые и переносимые соли с соединениями формулы I.
Для этой цели предпочтительным может являться применение неорганических кислот, например серной кислоты, азотной кислоты, галогенводородных кислот, таких как соляная кислота или бромистоводородная кислота, фосфорных кислот, таких как ортофосфорная кислота, сульфаминовой кислоты, кроме того, органических кислот, в частности алифатических, алициклических, аралифатических, ароматических или гетероциклических одно- или многоосновных карбоновых, сульфоновых или серных кислот, например муравьиной кислоты, уксусной кислоты, пропионовой кислоты, пивалиновой кислоты, диэтилуксусной кислоты, малоновой кислоты, янтарной кислоты, пимелиновой кислоты, фумаровой кислоты, малеиновой кислоты, молочной кислоты, винной кислоты, яблочной кислоты, бензойной кислоты, салициловой кислоты, 2- или 3-фенилпропионовой кислоты, лимонной кислоты, глюконовой кислоты, аскорбиновой кислоты, никотиновой кислоты, изоникотиновой кислоты, метан- или этансульфоновой кислоты, этандисульфоновой кислоты, 2-гидроксиэтансульфоновой кислоты, бензосульфоновой кислоты, n-толуолсульфоновой кислоты, нафталинмоно- и дисульфоновых кислот, лаурилсерной кислоты.
Более предпочтительной является соляная кислота или метансульфоновая кислота.
Количество смесей растворителей для кристаллизации в соответствии с изобретением не является решающим, для растворения предпочтительно можно применять 10 г - 500 г смесей растворителей на 1 г соединений формулы I.
Даже без дополнительных вариантов осуществления изобретения предполагается, что специалист в данной области техники способен использовать вышеприведенное описание в наиболее широком объеме. Следовательно, предпочтительные варианты осуществления изобретения могут рассматриваться только как описательное раскрытие, которое никоим образом не ограничивает изобретение.
Последующие примеры предназначены для пояснения изобретения без его ограничения. Если специально не указано иначе, то проценты обозначают мас.%. Все температуры приведены в градусах Цельсия.
Пример 1

30,00 г соединения 1 очищали и 300 мл этилацетата добавляли к 550 мл воды при перемешивании около 73°С. Смесь перемешивали при 75°С в течение 40 минут с образованием двух прозрачных фаз. Водную фазу отделяли и пропускали через обогреваемый паром фильтр Зейтца 2 I (фильтр К 900). Водную фазу оставляли охладиться при перемешивании в течение ночи и дополнительно перемешивали в течение 3-х часов при охлаждении на льду. Образованные кристаллы отделяли, промывали охлажденной водой и высушивали при 50°С, получая соединение 1 с чистотой 99,9%.
Пример 2
65 г загрязненного соединения 1 из примера 1 и 300 мл этилацетата добавляли к смеси 550 мл воды и 100 мл этанола при 71°С. Смесь перемешивали при 70°С в течение 30 минут с образованием двух прозрачных фаз. Водную фазу отделяли и фильтровали через обогреваемый паром фильтр Зейтца (Весо SD30). Значение рН доводили до 1,5 путем добавления 1,5 г метансульфоновой кислоты. Водную фазу оставляли охладиться при перемешивании в течение ночи и дополнительно перемешивали в течение 3-х часов при охлаждении на льду. Образованные кристаллы отделяли, промывали охлажденной водой и высушивали при 50°С, получая соединение 1 с чистотой 99,9% и с улучшенным выходом по сравнению с примером 1.
Пример 3

17,80 г соединения 2 очищали и 454 мл этилацетата добавляли к 182 мл воды при перемешивании приблизительно при 70°С. Смесь перемешивали при 65°С в течение 40 минут с образованием двух прозрачных фаз. Водную фазу отделяли и значение рН устанавливали на 1,0 при помощи водной соляной кислоты. Водную фазу оставляли охладиться при перемешивании в течение ночи и дополнительно перемешивали в течение 3-х часов при охлаждении на льду. Образованные кристаллы отделяли, промывали охлажденной водой и высушивали при 50°С, получая соединение 2 в виде его гидрата с чистотой 99,9%.
Пример 4
35,80 г соединения 2 очищали и 456 мл этилацетата добавляли к 501 мл воды при перемешивании приблизительно при 70°С. Смесь перемешивали при 65°С в течение 40 минут с образованием двух прозрачных фаз. Водную фазу отделяли и значение рН устанавливали на 1,4 при помощи водной соляной кислоты. Водную фазу оставляли охладиться при перемешивании в течение ночи и дополнительно перемешивали в течение 3-х часов при охлаждении на льду. Образованные кристаллы отделяли, промывали охлажденной водой и высушивали при 50°С, получая соединение 2 в виде его гидрата с чистотой 99,9%.
Пример 5
40,00 г соединения 2 очищали и 113,2 г этилацетата добавляли к смеси 282 мл воды и 51,7 г этанола при перемешивании приблизительно при 70°С. Смесь перемешивали приблизительно при 65°С в течение 10 минут с образованием двух фаз. Затем для очистки вносили дополнительно 30,00 г соединения 2 в течение 15 минут при перемешивании. Водную фазу отделяли и значение рН устанавливали на 1,2 при помощи водной соляной кислоты. Водную фазу оставляли охладиться и перемешивали дополнительно в течение 1 часа при охлаждении на льду. Образованные кристаллы отделяли, промывали охлажденной водой и высушивали при 50°С, получая соединение 2 в виде его гидрата с чистотой 99,9%.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ НИКОТИНАЛЬДЕГИДОВ | 2004 |
|
RU2339619C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-АРИЛМОРФОЛИНОНОВ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2004 |
|
RU2343149C2 |
| СПОСОБ ПОЛУЧЕНИЯ 5-(1-ПИПЕРАЗИНИЛ)БЕНЗОФУРАН-2-КАРБОКСАМИДА И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ | 2000 |
|
RU2266292C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОЧИСТОГО ДИАЛКИЛПЕМЕТРЕКСЕДА | 2010 |
|
RU2552519C2 |
| ПРОИЗВОДНЫЕ ТРИАЗОЛА | 2006 |
|
RU2416605C2 |
| ЗАМЕЩЕННЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1996 |
|
RU2157807C2 |
| Способ получения производных цефалоспорина с | 1973 |
|
SU499812A3 |
| ПРОИЗВОДНЫЕ ФЕНОКСИ-N-[4-(1,1-ДИОКСОИЗОТИАЗОЛИДИН-2-ИЛ)ФЕНИЛ]-ВАЛЕРАМИДА И ДРУГИЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ ФАКТОРА КОАГУЛЯЦИИ Ха ДЛЯ ЛЕЧЕНИЯ ТРОМБЭМБОЛИЧЕСКИХ БОЛЕЗНЕЙ И ОПУХОЛЕЙ | 2002 |
|
RU2301228C2 |
| ПРОИЗВОДНЫЕ 1,10b-ДИГИДРО-2-(АМИНОКАРБОНИЛФЕНИЛ)-5Н-ПИРАЗОЛО[1,5-c][1,3]БЕНЗОКСАЗИН-5-ИЛ)ФЕНИЛМЕТАНОНА В КАЧЕСТВЕ ИНГИБИТОРОВ РЕПЛИКАЦИИ ВИЧ ВИРУСА | 2005 |
|
RU2382789C2 |
| ПРОИЗВОДНЫЕ 3-ФЕНИЛПИРАЗОЛА, СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 3-ФЕНИЛПИРАЗОЛА И ФУНГИЦИДНАЯ КОМПОЗИЦИЯ | 1992 |
|
RU2072991C1 |
Изобретение относится к способу кристаллизации соединений формулы I или их кислото-аддитивных солей
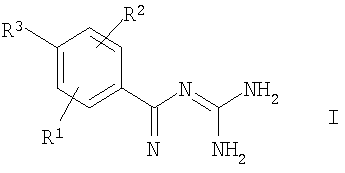
в которой R1, R2 и R3 имеют значения, указанные в п.1 формулы изобретения. В процессе соответствующие соединения формулы I или их смеси с примесями растворяют при повышенной температуре в воде, которая насыщена, по крайней мере, одним несмешивающимся с водой растворителем, выбранным из алкилалканоатов, и необязательно содержит один или несколько смешивающихся с водой растворителей, и подвергают кристаллизации при более низкой температуре. Технический результат - увеличение чистоты продукта. 6 з.п. ф-лы.
1. Способ кристаллизации соединений формулы I или их кислото-аддитивных солей,

в которой R1 R4SO2- или А,
R2 и R3, независимо друг от друга, Н, Hal, алкил, содержащий 1-12 атомов углерода, R1SO2-, Ar или Het,
R4 арил или алкил, содержащий 1-12 атомов углерода,
Het насыщенный, ненасыщенный или ароматический, моно- или бициклический, гетероциклический или линейный или разветвленный органический радикал, содержащий один или несколько гетероатомов, который незамещен или моно- или полизамещен A, COAr, COHet и/или Hal, Ar фенильный радикал, который незамещен или моно- или полизамещен А и/или Hal, ОН, ОА, СООН, СООА, CONH2, CONA2, CONHA, CN, NO2, NH2, NHA, NA2, NHCOA, CF3 или SO2A,
А прямоцепочечный или разветвленный алкил или гидроксиалкил, содержащий 1-10 атомов углерода, алкенил или алкоксиалкил, содержащий 2-10 атомов углерода, и
Hal F, Cl, Br, I,
отличающийся тем, что соответствующие соединения формулы I или их смеси с примесями растворяют при повышенной температуре в воде, которая насыщена, по крайней мере, одним несмешивающимся с водой растворителем, выбранным из алкилалканоатов, и необязательно содержит один или несколько смешивающихся с водой растворителей, и соединения формулы I подвергают кристаллизации при более низкой температуре.
2. Способ по п.1 для кристаллизации соединений формулы Ia-Ie
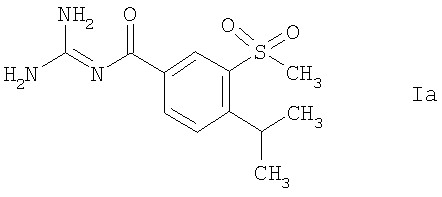
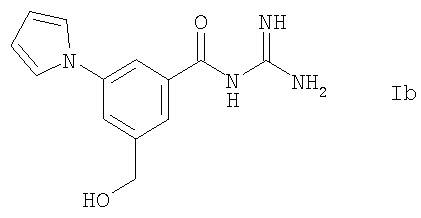
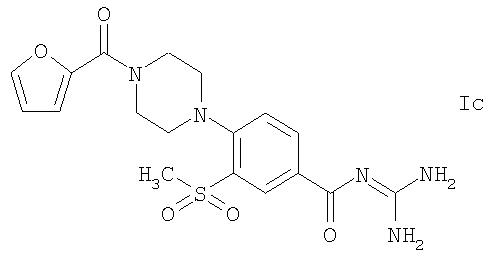
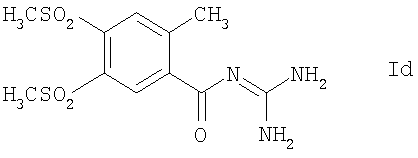
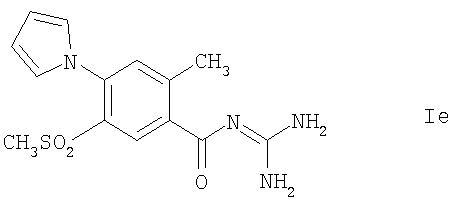
или их кислотоаддитивных солеи.
3. Способ по п.1, отличающийся тем, что применяют избыток несмешивающегося с водой растворителя.
4. Способ в соответствии с п.1, отличающийся тем, что используют смесь воды, одного или нескольких несмешивающихся с водой растворителей и одного или нескольких спиртов.
5. Способ по п.4, отличающийся тем, что используемый спирт представляет собой этанол, метанол или н- или изопропанол.
6. Способ по п.4, отличающийся тем, что спирт прибавляют к смеси растворителей в количестве, которое не вызывает полного смешивания воды и несмешивающегося с водой растворителя.
7. Способ по п.1, отличающийся тем, что значение рН устанавливают равным 1-3,5 с помощью подходящей кислоты перед кристаллизацией или при кристаллизации.
| ЕР 0758644 А1, 19.02.1997 | |||
| US 3975533 А, 17.08.1976 | |||
| US 5840761 А, 24.11.1998 | |||
| Способ получения производных 2-гуанидино-4-гетероарилтиазола или их фармацевтически приемлемых кислотно-аддитивных солей | 1982 |
|
SU1217258A3 |
Авторы
Даты
2009-11-27—Публикация
2004-04-10—Подача