Изобретение относится к химико-фармацевтической промышленности и касается получения риккардина С - соединения бисбибензильного типа структурной формулы I:
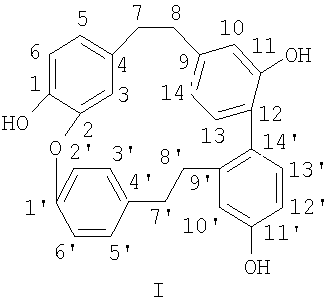
Указанное соединение может найти применение в качестве фармацевтического средства.
Соединение (I) впервые было выделено из мха Reboulia hemispherica в 1982 году [Asakawa, Y. and Matsuda, R. Riccardin C, a novel cyclic bibenzyl derivative from Reboulia hemispherica. / Phytochemistry. 1982. N21. P.2143-1244]. Из литературных данных известно, что риккардин С (I) (Riccardin С) и подобные ему бисбибензильные системы (Perrottetins, Marchantins, Plagiochins), представляющие собой фенольные соединения, ранее выделялись только из бриофитов - мхов-печеночников (из родов Riccardia, Marchantia, Plagiochila и др.) [Wu, С., Lin, H. Labdanoids and bis(bibenzyls) from Jungermannia species / Phytochemistry. - 1995. - V.44. - N1. - P.101-105; Martini, U., Zapp, J., Becker, H.. Chlorinated macrocyclic bis(bibenzyls) from the liverwort Bazzania trilobata / Phytochemistry. - 1998. - V.47. - N1. - P.89-96; Toyota, M., Yoshida, Т., Matsunam, J., Asakawa, Y. Sesquiterpene and other constituents of the liverwort Dumortiera hirsuta // Phytochemistry. - 1997. - V.44. - N2. - P.293-298], а в высших растениях, водорослях и грибах, обнаружены не были.
Из литературных данных известно, что такие соединения проявляют широкий спектр цитотоксической, антибактериальной и фунгицидной активности и используются как ингибиторы 5-липоксигеназы [Zinsmeister, H.D.; Becker, H.; Eicher, Т.. Bryophytes, a source of biologically active, naturally occuring material. / Angew. Chem. 1991, 103, 134-151; Asakawa, Y. Progress in the Chemistry of Organic Natural Products / Eds.: Herz, E., Kirby, G.W., Moore, R.E., Steglich, W., Tamm, C. - New York: Springer, Wien, 1995. - P.5]. Кроме того, обнаружено, что риккардин С (I) и близкие ему по структуре соединения являются ингибиторами индуцибельной NO-синтазы [Harinantenaina, D.N. Quang, N. Takeshi et. al. Bis(bibenzyls) from liverworts inhibit lipopolysaccaharide-induced inducible NOS in RAW 264.7 cells: a study of structure-activity relartionships and molecular mechanism // L. J. Nat. Prod. - 2005. - N6. - P.1779-1781]. Выделение веществ, отвечающих за ингибирование NO-синтаз, создание новых препаратов соответствующего действия - одна из важнейших проблем в медицине, так как чрезмерный выброс NO приводит к целому ряду различных, зачастую тяжелых патологических состояний. К ним относятся септический шок, нейродегенеративные заболевания - болезни Паркинсона и Альцгеймера, различные воспалительные процессы [Граник, В.Г., Григорьев, H.Б. Ингибиторы синтаз оксида азота - биология и химия // Известия АН. сер. хим. - 2002. - N11 - С.1819-1841].
Известен способ получения риккардина С с низким выходом (0.0015%) путем выделения из мха-печеночника [Anton, H., Shoeneborn, R., Mues, R. Bibenzils and bisbibenzyls from a neotropical Plagiochila species. / Phytochemistry. 1999. N8. P.1639-1645]. Способ заключается в экстракции воздушно-сухого сырья последовательно хлористым метиленом и 80%-ным водным метиловым спиртом с последующим фракционированием метанольного экстракта на твердофазном экстракторе с фазой RP-18, и далее, двукратной хроматографией соответствующих фракций на сефадексе LH-20 и хроматографией на препаративной колонке ВЭЖХ.
В качестве прототипа выбран способ получения риккардина С путем экстрагирования мха-печеночника Reboulia hemispherica этилацетатом и метанолом с последующим разделением экстракта колоночной хроматографией на силикагеле и тонкослойной хроматографией [Asakawa, Y. and Matsuda, R. Riccardin С, a novel cyclic bibenzyl derivative from Reboulia hemispherica. / Phytochemistry. 1982. N21. P.2143-1244], выход вещества (I) - 0.00153%.
Недостатком обоих способов является низкий выход риккардина С и малодоступное сырье, используемое для его получения - японские мхи-печеночники, растения, имеющие небольшой ареал и сложные в интродукции.
Задачей изобретения является создание простого технологичного способа получения риккардина С с высоким выходом из доступного сырья.
Задача решается выделением риккардина С (I) из высших цветковых растений, а именно из примулы крупночашечковой (Primula macrocalyx Bge.) последовательной экстракцией надземной части и корней растения органическим растворителем (петролейный эфир, гексан, ацетон) с последующим выделением целевого продукта путем хроматографирования. Примула крупночашечковая - многолетнее травянистое растение с толстым корневищем, несущим многочисленные мочки корней и до 10 и более розеток листьев. Растение встречается в Крыму, на Кавказе, на Южном Урале, широко распространено на юге Западной Сибири и Красноярского края. Культивируется в Центральном Сибирском Ботаническом саду (Новосибирск). Предлагаемый способ позволяет извлекать риккардин С (I) с высоким выходом как из надземной части, так и из корней примулы, причем как из диких растений, так и интродуцированных.
Исходное сырье: в работе использовали надземную часть и корневища первоцвета крупночашечкового (Primula macrocalyx Bge.), собранные экспедицией на Алтае в окрестностях села Амос, Чемальский район, в августе 2004 г., а также интродуцированную примулу, выращенную на участках Центрального Сибирского ботанического сада СО РАН. Определение вида примулы и интродукция были проведены сотрудниками лаборатории лекарственных растений ЦСБС СО РАН.
Общая методика выделения риккардина С.
Для максимально полного удаления липофильных веществ, наличие которых в экстрактах значительно осложняет хроматографическое выделение индивидуальных соединений, проводят экстракцию настаиванием воздушно-сухого растительного сырья в гексане или петролейном эфире при комнатной температуре. Настаивание проводят многократно до обесцвечивания растворителя. Именно настаивание, а не кипячение в растворителе, позволяет отделить красящие пигменты, воска и другие липофильные вещества из сырья, причем риккардин С холодным гексаном или петролейным эфиром не извлекается.
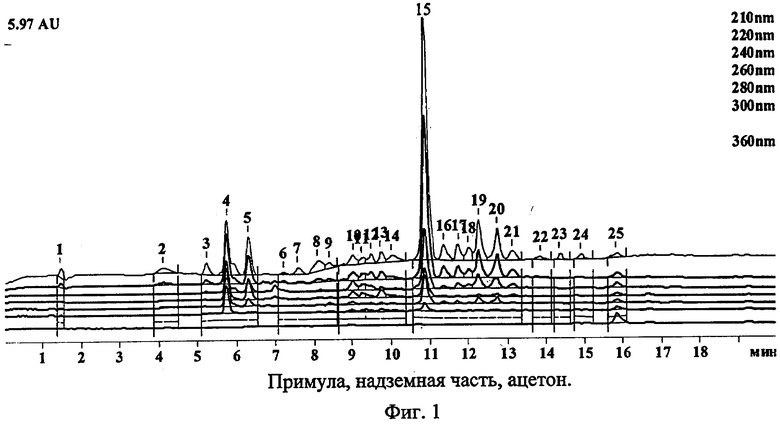
Дальнейшую обработку растительного сырья проводят настаиванием в ацетоне при комнатной температуре. В результате настаивания растительного сырья в ацетоне получают довольно простой по составу экстракт, содержащий одно основное вещество - риккардин С (пик 15, фиг.1).
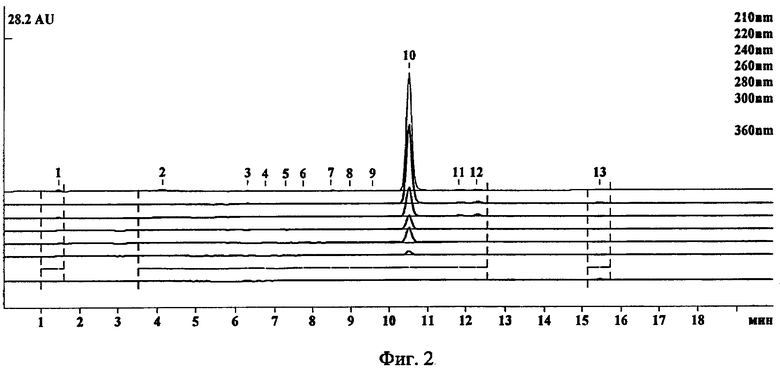
Ацетоновый экстракт делят на колонке с силикагелем (соотношение экстракт:адсорбент 1:40), получают фракции, обогащенные риккардином С. Либо - предварительно ацетоновый экстракт последовательно обрабатывают хлороформом и этанолом, весь риккардин С отделяется хлороформом. Затем обогащенные веществом (I) фракции делят на силикагеле и колонке с обращенной фазой (Art. 9334 LiChrosorb RP-18, 10 мкм, Merck), получают риккардин С (фиг.2).
На основании сравнения полученных спектральных данных с литературными [Anton, H., Shoeneborn, R., Mues, R. Bibenzils and bisbibenzyls from a neotropical Plagiochila species. / Phytochemistry. 1999. N8. P.1639-1645.] выделенному соединению была приписана структура риккардина С (I).
Изобретение иллюстрируется следующими примерами.
Пример 1. В колонку диаметром 5 см с краном внизу загружают 94.24 г растительного сырья (воздушно-сухие измельченные листья и стебли), шестикратно заливают по 0.5 л гексана и настаивают в общей сложности 48 часов до бесцветного экстракта. Масса гексанового экстракта 0.65 г (0.7% от массы сырья), этот экстракт отбрасывают. Затем сырье настаивают ацетоном 4 раза по 24 часа, масса экстракта - 2.11 г (2.24% от массы сырья).
2.11 г ацетонового экстракта разделяют на колонке с силикагелем (100/160μ, соотношение вещество: адсорбент ˜ 1:40, элюент - хлороформ с градиентом этилового спирта от 1%), выделяют в сумме 0.045 г фракций, обогащенных веществом (I).
Фракции, обогащенные веществом (I) (0.045 г; 2.13% от массы ацетонового экстракта) делят на обращенной фазе. В стеклянный фильтр насыпают 3 г SiO2 (L 60/200 μ), 10 г обращенной фазы (Art. 9334 LiChrosorb RP-18, 10 мкм, Merck), несколько раз промывают дистиллированной водой, метанолом, наносят фракцию соединения (I) в метаноле и элюируют вещество (I) 90% метанолом. Масса выделенного чистого вещества (I) составляет 0.020 г (0.95% - от массы экстракта; 0.021% - от массы сухого сырья).
ИК-спектр соединения (I) (C28H24O4; ν, см-1, CHCl3): 3597, 3550, 2928, 2860, 1740, 1706, 1606, 1566, 1506, 1482, 1433, 1333, 1269, 1188, 1105, 1050, 978, 914.
УФ-спектр соединения (I) (метанол): 279 нм.
Спектр ЯМР 1Н соединения (I) DMSO-d6, +55°С, δ, м.д. (J, Гц): 5.34 д (H3, J3,5 2.0), 6.65 д.д (H5, J5,6 8.0 J5,3 2.0), 6.77 д (H6, J6,5 8.0), 6.77 д (Н6, J6,5 8.0), 2.61 м (2Н7), 2.55 м (2Н8), 6.32 д (H10, J10,14 1.7), 6.70 д (H13, J13,14 7.6), 6.09 д.д (Н14, J14,13 7.6 J14,10 1.7), 6.68 ш.д (Н2', Н6'), 6.82 ш.д (Н3', Н5', J3',2' 7.7), 2.80 ш.с (2Н7', 2Н8'), 6.80 д (Н10', J10',12' 2.6), 6.63 д.д (Н12', J12',13' 8.3 J12',10 2.6), 6.85 д (H13', J13',12' 8.3), 8.65 с (С11-ОН), 8.78 ш.с (С1-ОН), 9.09 ш.с (С11'-ОН).
Спектр ЯМР 13С соединения (I) (DMSO, δC, м.д.): 34.8 т (С7'), 36.1 т (С7), 37 (С8), 37.3 (С8'), 112.7 д (С12'), 115.6 д (С10), 116 д (С6), 116.03 д (С10'), 116.6 д (С3), 119.5 д (С14), 121.5 д (С5), 121.5 д (С2', С6'), 125.6 с (С12), 129 д (С3', С5'), 129.2 с (С14'), 131.7 с (С4), 132 д (С13'), 132 д (С13), 139.1 с (С4'), 139.9 с (С9'), 142.7 с (С9), 144.1 с (С1), 147 с (С2), 152.7 с (С1'), 153.4 с (С11), 156.3 с (С11').
MS; m/z (%): 424 (100), 225 (7.6), 212 (46), 211 (93.5), 197 (8), 152 (4), 120 (7), 107 (18), 941 (14), 77 (8), 56 (5).
Пример 2. Из 100 г воздушно сухого сырья (надземная часть примулы, измельченные листья и стебли) получают 2.23 г (2.23% от массы сырья) ацетонового экстракта, как описано в примере 1. Экстракт разделяют растворителями - в хлороформ экстрагируется 1.56 г экстракта (70%), этанолом - 0.67 г (30%). Колоночной хроматографией хлороформного извлечения (SiO2 100/160μ, соотношение вещество:адсорбент ˜1:40; диаметр колонки 1.0 см, элюент - хлороформ с градиентом этилового спирта от 1 до 10%) выделяют 0.049 г фракции вещества (I). Ход хроматографии контролируют с помощью пластинок ТСХ в системе растворителей 5% этанола в хлороформе. Обогащенные фракции вещества (I) (0.049 г; 2.20% от массы ацетонового экстракта). В стеклянный фильтр насыпают 3 г SiO2 (L 60/200 μ), 10 г обращенной фазы (Art. 9334 LiChrosorb RP-18, 10 мкм, Merck), несколько раз промывают дистиллированной водой, метанолом, наносят объединенную фракцию соединения (I) в метаноле и элюируют вещество (I) 90% метанолом. Масса выделенного чистого вещества (I) составляет 0.022 г (0.97% - от массы экстракта; 0.022% - от массы сухого сырья).
Пример 3. Воздушно-сухие измельченные корни примулы крупночашечковой массой 199 г настаивают в колбе в 1.5 л петролейного эфира 3 раза по двое суток до бесцветного экстракта. Эти экстракты отбрасывают. Далее настаивают сырье в 1.5 л ацетона (5 раз по двое суток до полного извлечения риккардина С, контроль методом ВЭЖХ). Получают 3.85 г экстракта (1.93% от массы сухого сырья). Экстракт хроматографируют на колонке с силикагелем (100/160μ, соотношение вещество:адсорбент ˜ 1:40, элюент - хлороформ с градиентом этилового спирта от 1 до 10%), выделяют в сумме 0.45 г фракций, обогащенных веществом (I). Проводят рехроматографию на колонке с силикагелем (100/160μ, соотношение вещество:адсорбент ˜ 1:80, элюент - хлороформ с градиентом этилового спирта от 1 до 10%), выделяют в сумме 0.046 г вещества (I) (0.023% от массы сухого сырья).
Пример 4. Воздушно-сухие экземпляры целого растения примулы измельчают, образец массой 100 г настаивают в колбе, в 1.0 л петролейного эфира 3 раза по двое суток. Эти экстракты отбрасывают. Далее настаивают сырье в 1.0 л ацетона (5 раз по двое суток до полного извлечения риккардина С, контроль методом ВЭЖХ). Получают 2.02 г экстракта (2.02% от массы сухого сырья). Экстракт хроматографируют на колонке с силикагелем (100/160μ, соотношение вещество:адсорбент ˜1:40, элюент - хлороформ с градиентом этилового спирта от 1 до 10%), выделяют в сумме 0.22 г фракций, обогащенных веществом (I). Проводят рехроматографию на колонке с силикагелем (100/160μ, соотношение вещество:адсорбент ˜ 1:80, элюент - хлороформ с градиентом этилового спирта от 1 до 10%), выделяют в сумме 0.022 г вещества (I) (0.022% от массы сухого сырья).
Таким образом, предлагаемый способ получения риккардина С позволяет получить чистое вещество (I) из доступного возобновляемого сырья с достаточно высоким выходом после экстракции органическими растворителями настаиванием при комнатной температуре и последовательных хроматографий на силикагеле и обращенной фазе или двукратной колоночной хроматографией на силикагеле. Он имеет ряд преимуществ по сравнению с известными способами:
- экстракция целевого продукта проводится из доступного сырья - высшего цветкового растения примулы крупночашечковой, которая может быть достаточно легко заготовлена как в дикой природе, так и на культурных площадках в отличие от сбора мхов-печеночников, используемых в прототипе;
- для извлечения риккардина С используются различные растворители; отогнанный из экстракта растворитель не требует дополнительной очистки или регенерации для использования в повторных экстракциях, что весьма технологично;
- растворители и метод экстракции подобраны таким образом, что извлекаемый из сырья риккардин С выделяется с выходом, большим, чем в способах-аналогах. Выход целевого продукта по предлагаемому способу составляет 0.021-0.023%, против 0.00153% по известному способу-прототипу.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ РЕЗВЕРАТРОЛА ИЗ РАСТИТЕЛЬНОГО СЫРЬЯ | 2005 |
|
RU2294919C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ГИДРОКСИ-2,3,5-ТРИМЕТОКСИКСАНТОНА, ОБЛАДАЮЩЕГО ЖЕЛЧЕГОННЫМ И ГЕПАТОПРОТЕКТОРНЫМ ДЕЙСТВИЕМ | 2004 |
|
RU2264211C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ГИДРОКСИ-2,3,4,5-ТЕТРАМЕТОКСИКСАНТОНА, ОБЛАДАЮЩЕГО ЖЕЛЧЕГОННЫМ И ГЕПАТОПРОТЕКТОРНЫМ ДЕЙСТВИЕМ | 2000 |
|
RU2178302C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТОВ ИЗ РАСТИТЕЛЬНОГО ЛЕКАРСТВЕННОГО СЫРЬЯ | 1999 |
|
RU2176919C2 |
| СПОСОБ ПОЛУЧЕНИЯ УСНИНОВОЙ КИСЛОТЫ | 2006 |
|
RU2317076C1 |
| СПОСОБ ПОЛУЧЕНИЯ 4-ГИДРОКСИАЦЕТОФЕНОН-4-О-БЕТА-D-ГЛЮКОПИРАНОЗИДА (ПИЦЕИНА) ИЗ РАСТИТЕЛЬНОГО СЫРЬЯ | 2012 |
|
RU2532167C2 |
| СПОСОБ ОДНОВРЕМЕННОГО ПОЛУЧЕНИЯ ГИПЕРИЦИНА И ПСЕВДОГИПЕРИЦИНА | 2015 |
|
RU2623084C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА ЛЮТЕНУРИНА ИЗ КУБЫШКИ ЖЕЛТОЙ (Nuphar lutea (L.) Smith) | 2016 |
|
RU2615356C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТИМОСАПОНИНА ВII | 2005 |
|
RU2395518C2 |
| СПОСОБ ВЫДЕЛЕНИЯ 3-ОКСО-8-ГИДРОКСИ-1,5,7А,4,8В(Н)-ГВАЙ-10(14),11(13)-ДИЕН-12,6-ОЛИДА | 2017 |
|
RU2665975C1 |
Изобретение относится к химико-фармацевтической промышленности. Осуществляют обработку надземной части и корней растения примула крупночашечковая (Primula macrocalyx Bge.) органическим растворителем - петролейным эфиром или гексаном с последующей экстракцией ацетоном и выделением целевого продукта путем хроматографирования. Изобретение позволяет повысить выход продукта. 2 ил.
Способ получения риккардина С формулы I:

из растительного сырья путем экстракции органическим растворителем с последующим выделением целевого продукта хроматографией, отличающийся тем, что в качестве исходного сырья используется примула крупночащечковая (Primula macrocalyx Bge.), в качестве органического растворителя - ацетон, и экстракция проводится при комнатной температуре с предварительной обработкой сырья гексаном или петролейным эфиром.
| Acakawa, Y, and Matsuda, R | |||
| Riccardin C, a novel cyclic bibenzyl derivative from Reboulia hemispherica | |||
| Phytochemistry | |||
| Устройство для видения на расстоянии | 1915 |
|
SU1982A1 |
| Anton, H., Shoenebom, R., Mues, R | |||
| Bibenrils and bisbibenryls from a neotropical Plagiochila species | |||
| Phytochemistry | |||
| Металлический водоудерживающий щит висячей системы | 1922 |
|
SU1999A1 |
Авторы
Даты
2008-12-10—Публикация
2007-07-30—Подача