Изобретение относится к фармацевтической промышленности и касается способа производства субстанций препаратов, содержащих нафтодиантроновые пигменты растений - гиперицин и псевдогиперицин для медицины, ветеринарии, биотехнологии и научных исследований.
В научной и патентной литературе есть известные сведения о способах экстракции указанных пигментов из растительного сырья, способах разделения указанных пигментов. В связи с этим коллектив авторов считает необходимым привести сравнительный анализ уже известных способов экстракции и разделения указанных пигментов.
В описании изобретения имеются следующие сокращения и обозначения:
- H - гиперицин;
- РН - псевдогиперицин;
- МАЭ - микроволновая активация процесса экстракции;
- (об/об/об) - объемные отношения;
- ТСХ - тонкослойная хроматография;
- УЗВ - ультразвуковая ванна;
- ВЭЖХ - высокоэффективная жидкостная хроматография;
- ГЖХ - газожидкостная хроматография;
- ТМС-производных - триметилсилильных производных;
- ИК-спектры - инфракрасные спектры;
- спектры поглощения в УФ-(ультрафиолетовой) области.
Известен способ экстракции гиперицина и псевдогиперицина в аппаратах Сокслета и хроматографического выделения псевдогиперицина [Zotou Α., Loukou Ζ. Determination of Hypericin and Pseudohypericin in Extracts from Hypericum perforatum L. and Pharmaceutical Preparations by Liquid Chromatography-Fluorescence Detection // Chromatographia, 2001. - V. 54. - P. 218-224]. Способ осуществляют путем экстракции пигментов смесью метанол-ацетон (1:1) в течение 6 часов, при постоянном кипячении экстрагента, концентрирования экстракта пигментов до сухого остатка, растворения сухого экстракта в метаноле и выделения РН препаративной жидкостной хроматографией в течение десяти дней, концентрирования фракций, содержащих по данным ВЭЖХ анализа РН, методом лиофильной сушки.
Недостатками указанного способа экстракции пигментов и выделения РН являются: применение высокотоксичных растворителей: метанол и смесь метанола с ацетоном (1:1). Большая продолжительность экстракции пигментов на аппарате Сокслета (6 ч) и высокие трудозатраты на стадии выделения РН методом жидкостной хроматографии в течение 10 дней.
Известен способ экстракции пигментов зверобоя и обогащения экстракта гиперицинами [Стасевич О.В., Леонтьев В.Н., Коваленко Н.А., Супиченко Г.Н. Хроматографический анализ и разделение гиперицинсодержащего экстракта зверобоя // Труды БГТУ, 2012. - №4 (151). - С. 183-185]. Способ осуществляют экстракцией пигментов в аппарате Сокслета этанолом, препаративным разделением экстракта жидкостной хроматографией на сорбенте Diaion НР-20, элюированием пигментов с сорбента водными растворами спирта концентрации (0, 20, 40, 60, 80 и 100%), а также смесью этанолоа и хлороформа (1:1). Установлено, что при этом гиперицины концентрируются при элюировании 80%-ным этанолом в объеме 304-356 мл, а также смесью этанола с хлороформом в объеме 540-564 мл. В результате авторам удалось повысить концентрацию H в полученных фракциях с 0,08% до 0,34%.
Недостатками указанного способа экстракции пигментов и выделения H являются: применение высокотоксичных растворителей - смесь этанола с хлороформом (1:1). Применение сорбента для хроматографического обогащения пигментов, не обеспечивающего селективное разделение H и РН с получением препаративно чистых соединений. Большая продолжительность процесса хроматографического разделения пигментов на сорбентах с полистирольной матрицей, типа «Diaion НР-20».
Известен способ получения H и РН, приведенный в патенте [US Patent 5047435 Antiviral compositions containing aromatic polycyclic diones and method for treating retrovirus infections / Lavie; David (Rehovot, IL); Meruelo; Daniel (Scarborough, NY); Lavie; Gad (New York, NY); Revel; Michel (Rehovot, IL); Vande Velde; Vincent (Boncelles, BE); Rotman; Dalia (Rehovot, IL) Assignee: New York University (New York, NY); Yeda Research and Development Company, Ltd. (Rehovot, IL), Foreign Application Priority Data: Aug 08, 1986. Intern'l Class: A61K 031/015; A61K 045/08; A61L 002/18; A61L 015/00/], заключающийся в сушке растительного сырья при 55°С, измельчении сырья, экстракции 1 кг травы зверобоя ацетоном (около 5-10 л на кг) в аппарате Сокслета до обесцвечивания растворителя в извлечении (9-55 ч), концентрирования ацетонового экстракта выпариванием в вакууме досуха с получением остатка 95 г, хроматографического фракционирования полученного сухого экстракта на колонке, заполненной силикагелем 60 (0,06-0,20 мм). Для этого авторы патента растворяют 25 г полученного сухого экстракта в 500 мл ацетона, добавляют равное количество силикагеля 60 и упаривают на роторном испарителе с перемешиванием до получения однородной и сухой смеси, которую затем помещают в верхнюю часть хроматографической колонки, содержащей один кг силикагеля 60 и элюируют хлороформом до тех пор, пока растворитель не достигнет дна колонки. Затем колонку промывают смесью растворителей, включающей хлороформ-ацетон-метанол, 75:15:10 (об/об/об). После снижения интенсивности красной окраски элюата промывают колонку смесью растворителей хлороформ-ацетон-метанол, 55:15:10 (об/об/об). Собирают фракции по 250 мл. Каждую фракцию анализируют методом ТСХ. Дальнейшую очистку и разделение H и РН достигают последовательно двукратной флеш-хроматографией с использованием силикагеля 60 (меш 0,04-0,06) под давлением. Получают два основных компонента: H с выходом 0,19 г и РН с выходом 0,73 г.
Недостатками указанного способа экстракции пигментов и выделения H и РН являются: применение высокотоксичных растворителей - хлороформ, ацетон, метанол. Применение сорбента для хроматографического обогащения пигментов силикагеля 60, не обеспечивающего селективное разделение гиперицина и псевдогиперицина с получением препаративно чистых соединений в одну стадию флеш-хроматографии. Большая продолжительность процесса экстракции сырья ацетоном в аппарате Сокслета и хроматографического разделения пигментов на сорбентах типа силикагель 60.
Наиболее близким по технической сущности и достигаемому результату является способ экстракции H и РН из лекарственной фитомассы зверобоя продырявленного, описанный в статье [Пунегов В.В., Костромин В.И., Фомина М.Г., Зайнуллин В.Г., Юшкова Е.А., Белых Д.В., Чукичева И.Ю., Зайнуллин Г.Г. Экстрагирование гиперицина и псевдогиперицина из зверобоя продырявленного в условиях микроволновой активации процесса // Химия растительного сырья, 2014. - №1. - С. 125-130] и принимаемого за прототип в части стадии экстракции целевых пигментов. Способ экстракции H и РН заключается в измельчении лекарственной фитомассы зверобоя продырявленного до травяной муки, проходящей через сито с ячейкой 0,5 мм, трехкратной экстракции липофильных веществ хлороформом при гидромодуле, равном тридцати, с активацией процесса массопереноса обработкой суспензии сырье-хлороформ ультразвуком в течение 30 с, выдержки суспензии при комнатной температуре в течение 30 мин, фильтрования хлороформного экстракта хлорофилла и липидов через слой ваты и бумажного фильтра, сушки обезжиренного сырья в вакууме в токе воздуха с целью полного удаления паров хлороформа из сырья, трехкратной экстракции суммы H и РН из обезжиренного сырья в течение 60 с водным раствором этилового спирта или изопропанола при гидромодуле от 20 до 48 в условиях микроволновой активации процесса экстракции (далее по тексту МАЕ (э)) с нагреванием суспензии в микроволной камере до 65°С при частоте СВЧ излучения 2450 МГц, удельной мощности СВЧ в условиях эксперимента 0,0205 Вт/см3. Полученные экстракты объединяют и концентрируют в вакууме на роторном испарителе с целью рекуперации растворителей.
Недостатками указанного способа экстракции H и РН являются: применение в качестве экстрагента липофильных веществ токсичного хлороформа. Для полного удаления паров хлороформа из обезжиренного сырья требуется много времени. При этом пары хлороформа не подвергаются улавливанию и загрязняют атмосферу. Кроме того, как правило, технический хлороформ содержит в следовых количествах диоксины, которые могут вызвать контаминацию растительного сырья при использовании хлороформа.
Экстракцию H и РН осуществляют быстрым нагреванием суспензии спирт-сырье в СВЧ камере до 65°С за 60 с, но при температуре более 60°С происходит интенсивная экстракция гликозидов флавоноидов и крахмала из фитомассы в раствор и загрязнение экстракта пигментов балластными, в данном случае, веществами. Эти вещества в дальнейшем снижают селективность хроматографического разделения H и РН в условиях флеш-хроматографии. Кроме того, в условиях постоянного быстрого нагревания суспензии сырье-экстрагент в СВЧ камере возможен локальный перегрев, сопровождающийся частичным разрушением целевых пигментов, а также при этом есть реальная опасность внезапного теплового выброса экстракционной массы из экстрактора.
Технический результат заключается в упрощении и сокращении затрат, повышении вариабельности экстракции растительного сырья и условий проведения экстракции, повышении эффективности стадии глубокой очистки гиперицина и псевдогиперицина методом препаративной жидкостной флеш-хроматографии от сопутствующих экстрактивных веществ растения.
Изобретение поясняется рисунками:
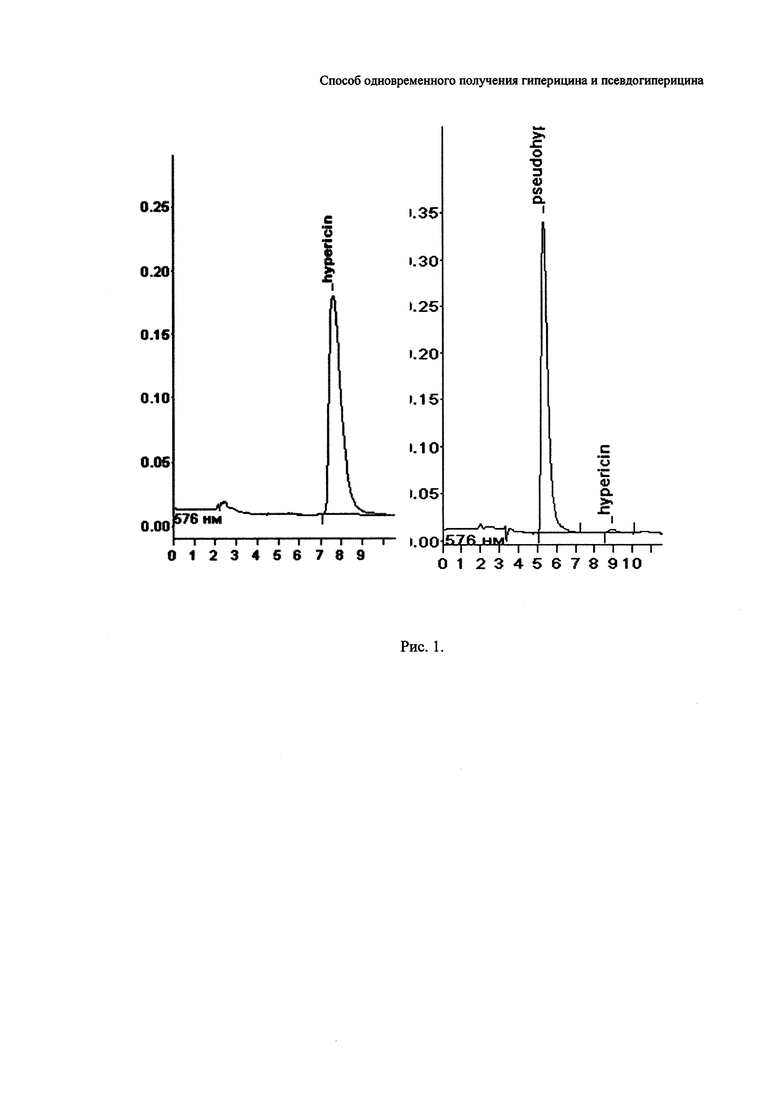
- на рис. 1 приведена хроматограмма ВЭЖХ анализа полученных пигментов. ВЭЖ хроматограммы чистых пигментов зверобоя продырявленного - гиперицина и псевдогиперицина, по вертикали: единицы оптической плотности (Б (бел.)), по горизонтали - время хроматографического удерживания компонентов, мин. Хроматограф «Милихром-5», VIS-детектор, колонка 80*2 мм, сорбент «Нуклеосил С18», 5 мкм, элюент ацетонитрил-этанол с линейным градиентом возрастания концентрации этанола, подкисленного уксусной кислотой (1%).
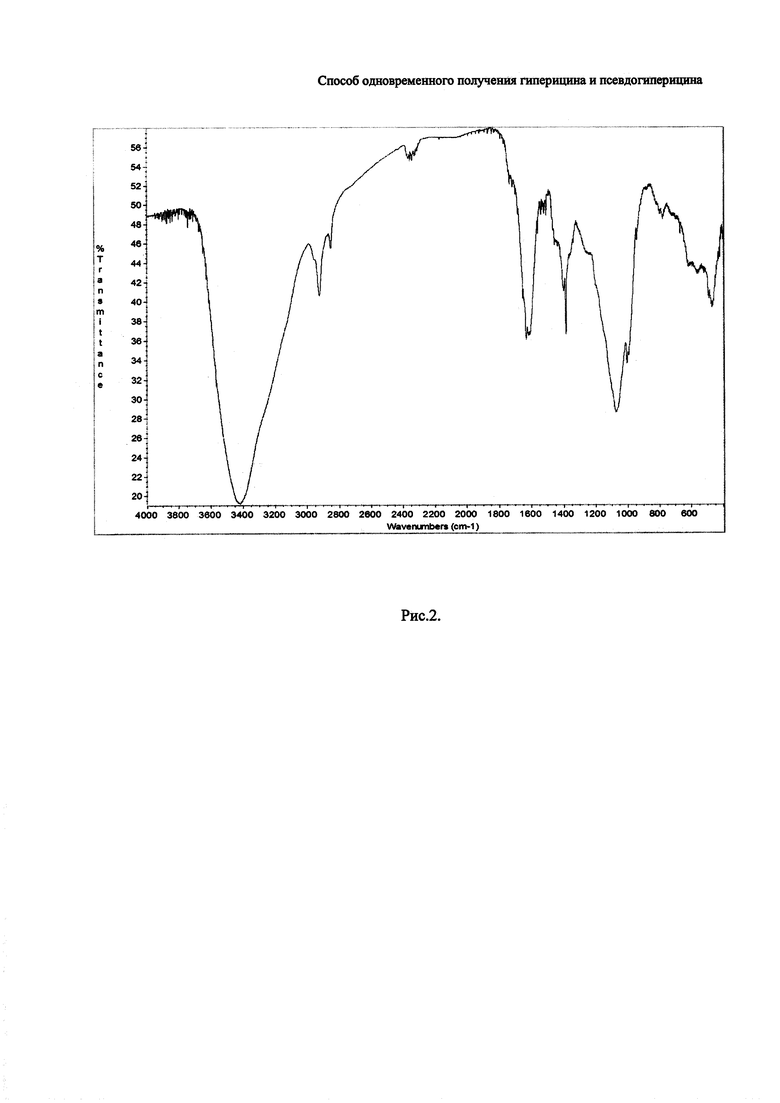
- на рис. 2 приведены ИК-спектры (ИК-спектр гиперицина (тонкая пленка на диске KBr), идентичный с ИК-спектром псевдогиперицина. Фурье спектрометр «Инфралюм ФТ-02».
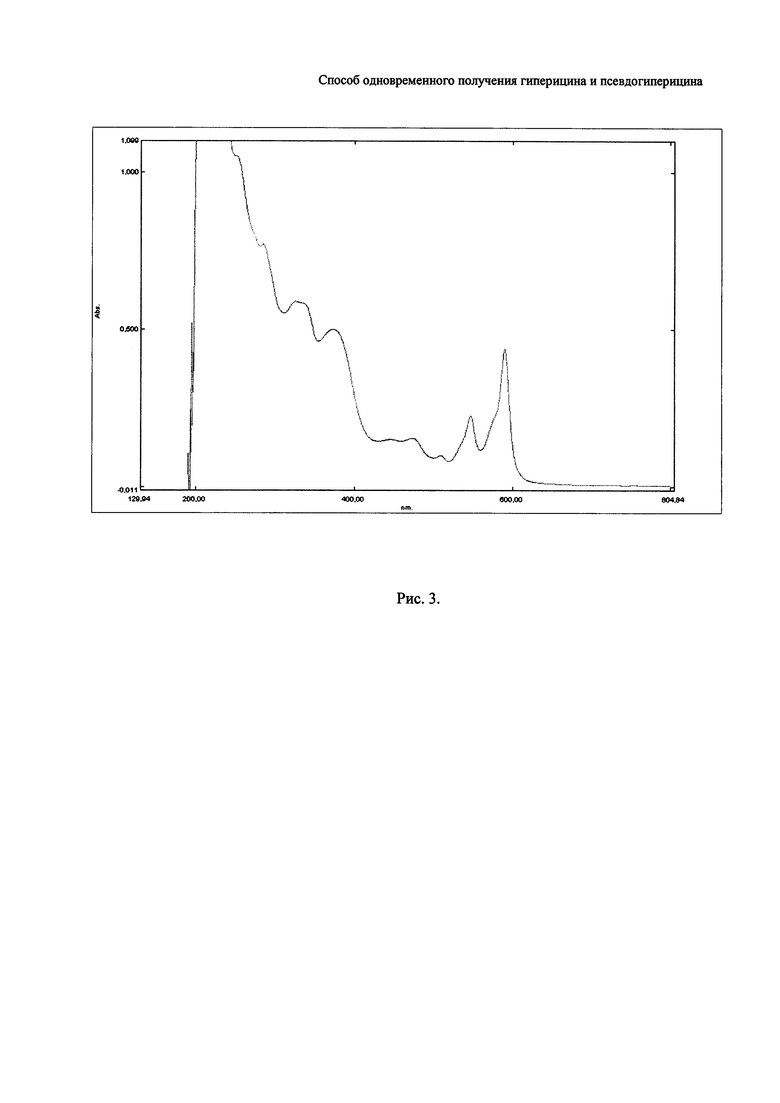
- на рис. 3 приведен спектр поглощения в УФ- и видимой области спиртовых растворов полученных образцов гиперицина и псевдогиперицина. Спектрометр Shimadzu UV1700 (Япония).
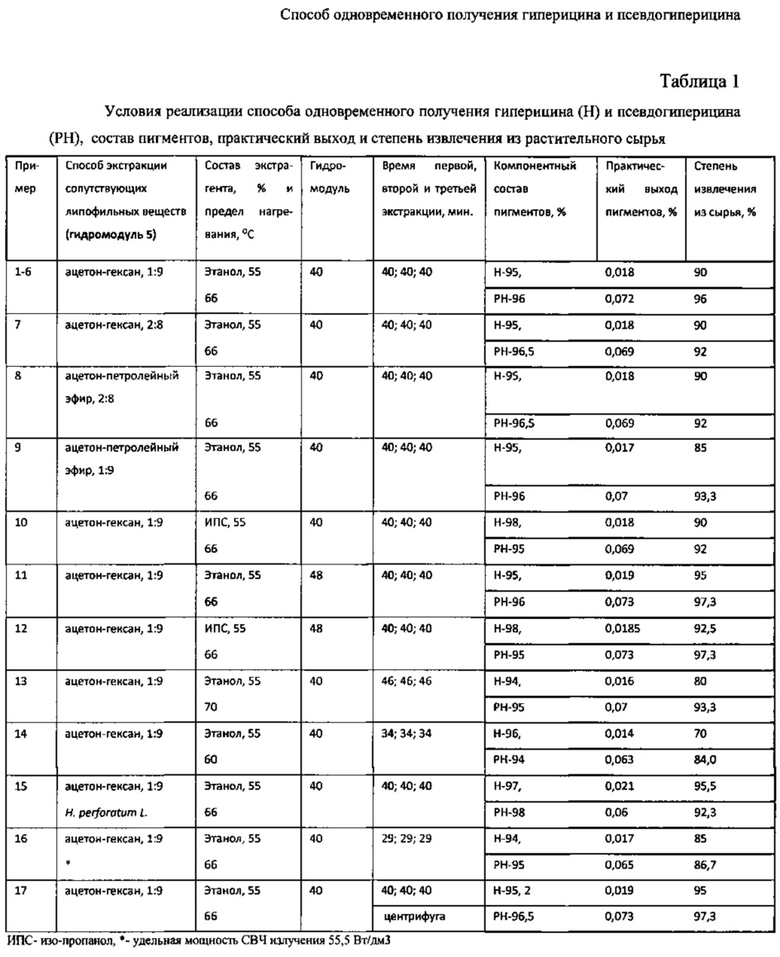
В таблице 1 отражены условия реализации способа одновременного получения гиперицина (Н) и псевдогиперицина (РН), состав пигментов, практический выход и степень извлечения из растительного сырья.
Способ осуществляется следующим образом: сырьем для производства гиперицина и псевдогиперицина является измельченная лекарственная фитомасса растений Hypericum maculatum Crantz и Hypericum peforatum L., заготавливаемая в фазе бутонизации или массового цветения растений.
Верхнюю часть олиственных стеблей зверобоя в фазе бутонизации-массового цветения длиной 20-25 см срезают и высушивают вне действия прямого солнечного света. Высушенное сырье перемалывают до частиц, проходящих через сито с ячейкой 0,5 мм. Травяную муку зверобоя вносят в стеклянную колбу объемом 1 л и экстрагируют липофильные вещества (хлорофиллы, каротиноиды, липиды) гексаном или петролейным эфиром, содержащим 10-20% (объемная доля) ацетона, при гидромодуле 4,8. Интенсивно перемешивают суспензию в течение 20 мин и выдерживают в ультразвуковой ванне в течение 5 мин при удельной мощности ультразвукового излучателя 39 Вт/дм3. Полученный экстракт отделяют фильтрованием. Сырье на фильтре дополнительно промывают раствором гексан-ацетон предпочтительно при объемном отношении 8:2 три раза по 0,1 л. Сырье, очищенное от липофильных веществ, высушивают в вакууме водоструйного насоса для удаления следов растворителей. Экстракт липофильных веществ концентрируют на ротационном испарителе в вакууме при температуре 45°С досуха для рекуперации гексана (или петролейного эфира) и ацетона. Полученная хлорофилльно-каротиноидная паста является сопутствующим продуктом при производстве гиперицина и псевдогиперицина. Пасту извлекают из кубовой емкости и фасуют в герметичные пластиковые емкости. Обезжиренное сырье вносят в экстрактор, снабженный обратным холодильником, и приливают 55%-ного этанола или изопропанола в таком количестве, чтобы гидромодуль был в интервале 40-48. Суспензию выдерживают 30 мин для набухания сырья и трехкратно экстрагируют гиперицин и псевдогиперицин в СВЧ камере с частотой излучения 2450 МГц, с удельной мощностью 41,6 Вт/дм3 при гидромодуле 40-48 с нагреванием суспензии сырье-экстрагент до 60-70°С (предпочтительно 66°С) за 29-46 мин (предпочтительно за 42 мин), с периодическим перемешиванием суспензии в условиях широтно-импульсной модуляции СВЧ излучения со скважностью пачек импульсов, равной 1,3, длительностью пачек импульсов СВЧ 23 с. Полученный после фильтрации (или центрифугирования) суммарный экстракт в объеме 14,3 л концентрируют в вакууме с одновременным облучением экстракта в отгонной колбе емкостью 10 л лампой накаливания в 95 Вт на ротационном испарителе при температуре 50°С досуха. Получают 60 г сухого экстракта фиолетового цвета. При облучении экстракта в процессе концентрирования в вакууме в течение 2,5 ч происходит фотоциклизация сопутствующих соединений: протогиперицина и протопсевдогиперицина соответственно до H и PH. Фотоциклизация указанных веществ позволяет повысить практический выход целевых пигментов. С целью дальнейшего фракционирования методом флеш-хроматографии суммарный экстракт пигментов смешивают с водой (0,25 л), диспергируют в УЗВ и смешивают с 300 г сорбента «Диасорб 130 С16Т». Для преципитации сорбент с экстрактом высушивают в вакууме при перемешивании на ротационном испарителе при температуре 50°С. Досушивают преципитат в вакууме масляного насоса при остаточном давлении 0,05-0,08 Па. Преципитат H и РН на «Диасорбе С16» представляет собой порошок коричнево-фиолетового цвета в количестве 360 г. В форколонку системы для препаративной флеш-хроматографии «FLASH150» вносят преципитат пигментов и элюируют псевдогиперицин и гиперицин через хроматографическую колонку внутренним диаметром 160 мм и высотой слоя сорбента 320 мм, заполненную сорбентом, фракции 40-64 мкм, содержащим на поверхности пор силикагеля функциональный покров из диметилоктадецилсилильных групп. Колонка снабжена пневматической системой для радиального сжатия сорбента в колонке, а также входным и выходным радиальным распределителем потока элюента вдоль колонки. В качестве элюента используют водные растворы этилового спирта с возрастанием концентрации от 5% до 60%. Для подавления диссоциации пигментов и увеличения селективности хроматографического разделения используют элюенты, подкисленные уксусной кислотой. Элюируют пигменты с колонки в режиме ступенчатого градиента концентрации этилового спирта. Псевдогиперицин элюируется из колонки 20 и 30%-ным этанолом. Гиперицин элюируется 40 и 45%-ным этанолом. Полученные фракции по 5 л каждая анализируются методом ВЭЖХ по тексту на аналитическом хроматографе «Милихром 5» и по результатам анализа объединяются отдельно фракции, содержащие псевдогиперицин и гиперицин. Фракции красного цвета, содержащие целевые пигменты концентрируются в вакууме на ротационном испарителе. В результате получают фракцию концентрата псевдогиперицина и гиперицина. Полученные концентраты псевдогиперицина и гиперицина растворяют соответственно в 800 мл и 300 мл 95%-ного этилового спирта при кипячении. Растворы фильтруют через мембранный фильтр из фторопласта с порами 0,2 мкм и концентрируют с одновременной вакуумной кристаллизацией на ротационном испарителе ИР-1М при остаточном давлении 33-13 кПа (25-10 мм рт. ст.) до остатка объемом соответственно 5 и 2 мл. Остаток, содержащий целевые продукты, отфильтровывают через мембранный фильтр из фторопласта с порами 0,2 мкм. Получают, после сушки в вакууме при 60°С, на фильтре в кристаллическом виде 0,06-0,073 г псевдогиперицина и 0,014-0,21 г гиперицина. По данным ВЭЖХ анализа массовая доля псевдогиперицина и гиперицина в полученных образцах 94-98%.
Маточные растворы, содержащие этанол упаривают досуха. Твердый остаток, представляющий собой смесь минорных диантроновых соединений зверобоя и следов каротиноидов растения, является сопутствующим продуктом производства гиперицина и псевдогиперицина. Его извлекают из отгонной колбы и после сушки в вакууме фасуют в герметичную тару. Смесь ацетон-гексан и ацетон-петролейный эфир перегоняют на ректификационной установке и после обезвоживания синтетическим цеолитом CaX, используют многократно для производства опытных партий пигментов зверобоя с целью медико-биологических исследований их свойств. Растительное сырье после экстракции целевых пигментов помещают в кубовую емкость лабораторной ретификационной установки и путем перегонки производят рекуперацию этилового спирта или изопропанола, сорбированного растительным жомом. Растительный остаток утилизируют.
Данный способ можно с успехом использовать в фармацевтической промышленности, поэтому он соответствует критерию «промышленно применимо», «новизна» и «изобретательский уровень».
Способ одновременного производства гиперицина и псевдогиперицина конкретизируется следующими примерами:
Пример 1. Подготовка растительного сырья. Верхнюю часть олиственных стеблей зверобоя пятнистого (Hypericum maculatum Crantz) в фазе бутонизации-массового цветения длиной 20-25 см срезали и высушивали вне действия прямого солнечного света. Сырье было заготовлено в Сыктывдинском районе Республики Коми, а сырье зверобоя продырявленного (Hypericum perforatum L.) заготавливали с экспериментальных делянок Ботанического сада Института биологии Коми НЦ УрО РАН. Высушенное сырье перемалывали на мельнице до частиц, проходящих через сито с ячейкой 0,5 мм. По результатам ВЭЖХ анализа, в полученной травяной муке из зверобоя пятнистого содержится 0,095% суммы гиперицина и псевдогиперицина, в том числе 0,075% псевдогиперицина и 0,020% гиперицина. Травяная мука из зверобоя продырявленного содержит 0,087% суммы гиперицина и псевдогиперицина, в том числе 0,065% псевдогиперицина и 0,022% -гиперицина.
Пример 2. Экстракция сопутствующих липофильных веществ (хлорофиллы и каротиноиды, триглицериды). 124 г воздушно-сухой травяной муки зверобоя пятнистого внесли в стеклянную колбу объемом 1 л и прилили 0,6 л гексана, содержащего 10% (объемная доля) ацетона. Гидромодуль 5. Интенсивно перемешивали суспензию на магнитной мешалке в течение 20 мин и выдерживали в УЗВ-2/150-ТН (ООО «Рэлтек», Россия) в течение 5 мин при удельной мощности ультразвукового излучателя 39 Вт/дм3. Полученный экстракт фильтровали на нутч-фильтре. Сырье на фильтре дополнительно промывали раствором гексан-ацетон (9:1) три раза по 0,1 л. Сырье, очищенное от липофильных веществ, высушивали в вакууме водоструйного насоса для удаления следов растворителей. Экстракт концентрировали на ротационном испарителе ИР-1 (ОАО «Химлаборприбор», г. Клин, Россия) в вакууме при температуре 45°С досуха для рекуперации гексана и ацетона. Полученная хлорофилльно-каротиноидная паста является сопутствующим продуктом при производстве гиперицина и псевдогиперицина. Пасту извлекали из кубовой емкости и фасовали в герметичные пластиковые емкости.
Пример 3. Экстракция гиперицина и псевдогиперицина. Обезжиренное сырье вносили в полипропиленовый экстрактор объемом 6 л, снабженный обратным холодильником, и прилили 4960 мл 55%-ного этанола. Суспензию выдерживали 30 мин для набухания сырья и трехкратно экстрагировали пигменты в СВЧ камере с частотой излучения 2450 МГц, с удельной мощностью 41,6 Вт/дм3 при гидромодуле 40 с нагреванием суспензии сырье-экстрагент до 66°С за 42 мин, с периодическим перемешиванием суспензии в условиях широтно-импульсной модуляции СВЧ излучения со скважностью пачек импульсов, равной 1,3, длительностью пачек импульсов СВЧ 23 с. Полученный после фильтрации суммарный экстракт в объеме 14,3 л концентрировали в вакууме с одновременным облучением экстракта в отгонной колбе емкостью 10 л лампой накаливания в 95 Вт на ротационном испарителе ИР-10М (ОАО «Химлаборприбор», г. Клин, Россия) при температуре 50°С досуха. Получили 60 г сухого экстракта фиолетового цвета. При облучении экстракта в процессе концентрирования в вакууме в течение 2,5 ч происходит фотоциклизация сопутствующих соединений: протогиперицина и протопсевдогиперицина соответственно до Н и РН. Фотоциклизация указанных веществ позволяет повысить практический выход целевых пигментов. С целью дальнейшего фракционирования методом флеш-хроматографии суммарный экстракт пигментов смешивали с водой (0,25 л), диспергировали в УЗВ и смешивали со 300 г сорбента «Диасорб 130 С16Т» (ЗАО БиоХимМак СТ» г. Москва, Россия) фракции 160-250 мкм. Для преципитации сорбент с экстрактом высушивали в вакууме при перемешивании на ротационном испарителе ИР-1 при температуре 50°С. Досушивали в вакууме масляного насоса при остаточном давлении 0,05-0,08 Па. Преципитат пигментов на «Диасорбе С16» представлял собой порошок коричнево-фиолетового цвета в количестве 360 г.
Пример 4. Фракционирование пигментов флеш-хроматографией. В форколонку системы для препаративной флеш-хроматографии «FLASH150», (Biotage, USA) внесли полученный по примеру 3, преципитат пигментов в количестве 360 г и элюировали псевдогиперицин и гиперицин через хроматографическую колонку внутренним диаметром 160 мм и высотой слоя сорбента 320 мм, заполненную сорбентом, фракции 40-64 мкм, содержащим на поверхности пор силикагеля функциональный покров из диметилоктадецилсилильных групп. Колонка снабжена пневматической системой для радиального сжатия сорбента в колонке, а также входным и выходным радиальным распределителем потока элюента вдоль колонки. В качестве элюента использовали водные растворы этилового спирта с возрастанием концентрации от 5% до 60%. Для подавления диссоциации пигментов и увеличения селективности хроматографического разделения использовали элюенты, подкисленные уксусной кислотой с объемной долей 1%. Элюировали пигменты с колонки в режиме ступенчатого градиента концентрации этилового спирта. Расход элюента на выходе колонки составлял 850 см3/мин при давлении на входе колонки 6 атм (607,95 кПа). В первых фракциях, элюированных этанолом 5-15% целевые пигменты не были обнаружены методом ВЭЖХ анализа. Методом ГЖХ-анализа ТМС-производных в этих фракциях обнаружены моно- и дисахариды, гликозиды флавоноидов, преимущественно рутин. Псевдогиперицин элюировали из колонки 20 и 30%-ным этанолом. Гиперицин элюировался 40 и 45%-ным этанолом. Полученные 17 фракций по 5 л каждая анализировали методом ВЭЖХ на аналитическом хроматографе «Милихром 5» (ООО «Медикант», г. Орел, Россия) и по результатам анализа объединяли отдельно фракции, содержащие псевдогиперицин и гиперицин. Фракции красного цвета, содержащие целевые пигменты, концентрировали в вакууме на ротационном испарителе ИР-10М. В результате получена фракция концентрата псевдогиперицина в количестве 0,0883 г (практический выход 0,072%) и гиперицина 0,0221 г (практический выход 0,018%). По данным ВЭЖХ анализа содержание псевдогиперицина в полученном образце составляло 95%, а гиперицина во втором образце 96% (см. табл. 1).
Пример 5. Очистка методом перекристаллизации образцов гиперицина и псевдогиперицина, полученных по примеру 4. 0,0883 г псевдогиперицина и 0,0221 г гиперицина растворяли соответственно в 800 мл и 300 мл 95%-ного этилового спирта при кипячении в конических колбах, полученные растворы фильтровали через мембранный фильтр из фторопласта с порами 0,2 мкм (ЗАО «БиоХимМак СТ», г. Москва, Россия) и концентрировали с одновременной вакуумной кристаллизацией на ротационном испарителе ИР-1М (ОАО «Химлаборприбор», г. Клин, Россия) при остаточном давлении 33-13 кПа (25-10 мм рт. ст.) до остатка объемом соответственно 5 и 2 мл. Остаток, содержащий целевые продукты, отфильтровывали через мембранный фильтр из фторопласта с порами 0,2 мкм. Получили, после сушки в вакууме при 60°С, на фильтре в кристаллическом виде 0, 0879 г псевдогиперицина и 0,0218 г гиперицина. По данным ВЭЖХ анализа массовая доля псевдогиперицина в полученном образце составляет 98, 6%, гиперицина - 99,5% (табл. 1). В виде примеси псевдогиперицин содержит 1,4% гиперицина, а образец гиперицина содержит 0,5% псевдогиперицина. Полученные пигменты исследовали физико-химическими методами, показаными на рисунках. На рис. 1 приведена хроматограмма ВЭЖХ анализа полученных пигментов. На рис. 2 приведены ИК-спектры, а на рис. 3 спектры поглощения в УФ- и видимой области спектра спиртовых растворов полученных пигментов.
По результатам хромато-масс-спектрометрического анализа растворов полученных пигментов, установлено, в масс-спектре, фиксирующем отрицательные ионы, для образца псевдогиперицина характерен сигнал молекулярного иона со значением m/z 519, для образца гиперицина соответствующий сигнал регистрируется со значением m/z 503.
Пример. 6. Рекуперация растворителей, утилизация маточных растворов и отработанного сырья. Маточные растворы, содержащие этанол, упаривали досуха. Твердый остаток, представляющий собой смесь минорных диантроновых соединений зверобоя и следов каротиноидов растения, является сопутствующим продуктом производства гиперицина и псевдогиперицина. Его извлекали из отгонной колбы и после досушки в вакууме фасовали в герметичную тару. Смесь ацетон-гексан и ацетон-петролейный эфир перегоняли на ректификационной установке и после обезвоживания синтетическим цеолитом СаХ использовали многократно для производства опытных партий пигментов зверобоя с целью медико-биологических исследований их свойств. Растительное сырье после экстракции целевых пигментов помещали в кубовую емкость лабораторной ретификационной установки и путем перегонки производили рекуперацию этилового спирта, сорбированного растительным жомом. Растительный остаток утилизировали.
Пример 7. Получение гиперицина и псевдогиперицина осуществляли согласно примерам 1-6, но для обезжиривания сырья использовали смесь ацетона и гексана в объемном соотношении 2:8 при гидромодуле 5. Практический выход и состав пигментов отражен в табл. 1.
Пример 8. Получение гиперицина и псевдогиперицина осуществляли согласно примерам 1-6, но растительное сырье обезжиривают органическим растворителем состава гексан: ацетон (8:2) или петролейный эфир: ацетон (8:2) при гидромодуле 5 в течение 5 минут. Практический выход и состав пигментов отражен в табл. 1.
Пример 9. Получение гиперицина и псевдогиперицина осуществляли согласно примерам 1-6, но растительное сырье обезжиривают органическим растворителем состава гексан: ацетон (9:1) или петролейный эфир: ацетон (9:1) при гидромодуле 5 в течение 5 минут. Практический выход и состав пигментов отражен в табл. 1.
Пример 10. Получение гиперицина и псевдогиперицина осуществляли согласно примерам 1-6, но СВЧ экстракцию пигментов осуществляли с применением 55%-ного изопропанола при гидромодуле 40. Практический выход и состав пигментов отражен в табл. 1.
Пример 11. Получение гиперицина и псевдогиперицина осуществляли согласно примерам 1-6, но СВЧ экстракцию пигментов осуществляли с применением 55%-ного этилового спирта, но при гидромодуле 48. Практический выход и состав пигментов отражен в табл. 1.
Пример 12. Получение гиперицина и псевдогиперицина осуществляли согласно примерам 1-6, но СВЧ экстракцию пигментов осуществляли с применением 55%-ного изопропанола при гидромодуле 48. Практический выход и состав пигментов отражен в табл. 1.
Пример 13. Получение гиперицина и псевдогиперицина осуществляли согласно примерам 1-6, но СВЧ экстракцию пигментов осуществляли с применением 55%-ного этилового спирта при гидромодуле 40 с нагреванием до 70°С за 46 мин. Практический выход и состав пигментов отражен в табл. 1.
Пример 14. Получение гиперицина и псевдогиперицина осуществляли согласно примерам 1-6, но СВЧ экстракцию пигментов осуществляли с применением 55%-спирта при гидромодуле 40 с нагреванием до 60°С. Практический выход и состав пигментов отражен в табл. 1.
Пример 15. Получение гиперицина и псевдогиперицина осуществляли согласно примерам 1-6, но в качестве сырья использовали 124 г травяной муки зверобоя пятнистого (Hypericum perforatum L). Практический выход и состав пигментов отражен в табл. 1.
Пример 16. Получение гиперицина и псевдогиперицина осуществляют согласно примерам 1-6, но СВЧ экстракцию пигментов осуществляют с в режиме широтно-импульсной модуляции СВЧ излучения частотой 2450 МГц с удельной мощностью 55,5 Вт/дм3 три раза при гидромодуле 40 с нагреванием суспензии сырье-экстрагент до 66°С за 29 мин. Практический выход и состав пигментов отражен в табл. 1.
Пример 17. Получение гиперицина и псевдогиперицина осуществляют согласно примерам 1-6, но вместо фильтрования экстракта целевых пигментов используют центрифугирование суспензии сырье-экстракт на центрифуге Т230 в течение 10 мин при скорости вращения ротора центрифуги до 10000 об/мин.
Супернатант сливают с осадка, объединяют с получением 15 л суммарного экстракта и концентрируют в вакууме. Практический выход и состав пигментов отражен в табл. 1.
Таким образом предполагаемый объект позволяет упростить технологию получения целевых веществ - гиперицина и псевдогиперицина за счет отказа от применения высокотоксичного хлороформа, сократить продолжительность всех технологических стадий способа, уменьшить затраты электроэнергии и трудозатраты по сравнению с аналогом и прототипом, повысить экологическую безопасность производства целевых пигментов.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ НА ОСНОВЕ ЗВЕРОБОЯ, ВКЛЮЧАЮЩАЯ СОЕДИНЕНИЯ ДИАНТРОНОВОГО РЯДА, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2010 |
|
RU2436586C1 |
| СПОСОБ ПОЛУЧЕНИЯ СУММЫ ФЛАВОНОИДОВ, ОБЛАДАЮЩЕЙ РАДИОЗАЩИТНЫМ ДЕЙСТВИЕМ | 1999 |
|
RU2152794C1 |
| Способ выделения гиперфорина и адгиперфорина из травы зверобоя продырявленного | 2019 |
|
RU2720457C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИНДИВИДУАЛЬНЫХ КАРОТИНОИДОВ | 2016 |
|
RU2648452C1 |
| СПОСОБ ЭКСТРАКЦИИ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ ИЗ ЗВЕРОБОЯ ПРОДЫРЯВЛЕННОГО (Hypericum perforatum L.) | 2014 |
|
RU2568912C1 |
| Способ установления подлинности и качества зверобоя продырявленного (Hypericum perforatum L.) | 2015 |
|
RU2614200C1 |
| СРЕДСТВО "ЭКДИСТЕРОН-80", ОБЛАДАЮЩЕЕ КАРДИОПРОТЕКТОРНОЙ, АДАПТОГЕННОЙ, АНТИГИПОКСИЧЕСКОЙ, ГАСТРОПРОТЕКТОРНОЙ, ТЕРМОПРОТЕКТОРНОЙ, АНАБОЛИЧЕСКОЙ И АКТОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ, И СПОСОБ ЕГО ПРОИЗВОДСТВА | 2006 |
|
RU2321420C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭКСТРАКТОВ ИЗ РАСТИТЕЛЬНОГО СЫРЬЯ ВОДНО-ЖИРОВОЙ ЭКСТРАКЦИЕЙ НАТУРАЛЬНЫМИ ЭКСТРАГЕНТАМИ | 2011 |
|
RU2491947C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭКДИСТЕРОИДОВ РАСТЕНИЯ РОДА SERRATULA αЭКДИЗОНА, βЭКДИЗОНА И ИНОКОСТЕРОНА | 1997 |
|
RU2138509C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ЭКСТРАКТА ТРАВЫ ЗВЕРОБОЯ, СБРОЖЕННОГО МОЛОЧНОКИСЛЫМИ БАКТЕРИЯМИ, И ТЕХНОЛОГИЧЕСКАЯ ЛИНИЯ ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2021 |
|
RU2779115C1 |
Изобретение относится к фармацевтической промышленности и касается способа получения гиперицина и псевдогиперицина из сырьевой фитомассы растений видов зверобой пятнистый и зверобой продырявленный. Способ получения гиперицина и псевдогиперицина из сырьевой фитомассы растений видов зверобой пятнистый и зверобой продырявленный, включающий измельчение растительного сырья, обезжиривание сырья органическим растворителем, отделение экстракта липофильных веществ растений, сушку сырья, повторную экстракцию обезжиренного сырья водными растворами органического растворителя, фильтрацию полученных экстрактов, концентрирование экстрактов, хроматографическое разделение целевых пигментов на колонке, содержащей силикагель с использованием элюентов, содержащих органический растворитель и воду, концентрирование полученных фракций элюатов, объединение фракций, кристаллизацию гиперицина и псевдогиперицина с применением растворов полярного органического растворителя в неполярном, сушку готовых пигментов, при этом надземную массу растений Hypericum perforatim L. и Hypericum maculatum Crantz., собранную в фазу массовой бутонизации и начала цветения предварительно обезжиривают органическим растворителем, трехкратно экстрагируют настаиванием 40-55% спиртом формулы CnH2nOH, где n=2 или n=3, процесс ведут в СВЧ камере, отделяют экстракт фильтрованием или центрифугированием и упаривают в вакууме досуха, затем экстракт подвергают преципитации на силикагеле с функциональным покровом пор из диметилоктадецилсилильных групп, с последующей сушкой в вакууме, далее преципитат помещают в форколонку для флэш-хроматографии поверх сорбента и элюируют нафтодиантроновые пигменты водными растворами этилового спирта, кристаллизацию гиперицина и псевдогиперицина осуществляют из смеси этанол-вода в режиме вакуумной кристаллизации с одновременным концентрированием маточного раствора на роторном испарителе, сушку гиперицина и псевдогиперицина осуществляют в вакууме, при определенных условиях. Вышеописанный способ является упрощенным, повышает вариабельность экстракции растительного сырья, повышает эффективность стадии глубокой очистки гиперицина и псевдогиперицина. 3 ил., 17 пр., 1 табл.
Способ получения гиперицина и псевдогиперицина из сырьевой фитомассы растений видов зверобой пятнистый и зверобой продырявленный, включающий измельчение растительного сырья, обезжиривание сырья органическим растворителем, отделение экстракта липофильных веществ растений, сушку сырья, повторную экстракцию обезжиренного сырья водными растворами органического растворителя, фильтрацию полученных экстрактов, концентрирование экстрактов, хроматографическое разделение целевых пигментов на колонке, содержащей силикагель с использованием элюентов, содержащих органический растворитель и воду, концентрирование полученных фракций элюатов, объединение фракций, кристаллизацию гиперицина и псевдогиперицина с применением растворов полярного органического растворителя в неполярном, сушку готовых пигментов, отличающийся тем, что надземную массу растений Hypericum perforatim L. и Hypericum maculatum Crantz., собранную в фазу массовой бутонизации и начала цветения, предварительно обезжиривают органическим растворителем состава гексан и ацетон при соотношении гексан : ацетон 8-9:2-1 или состава петролейный эфир и ацетон при соотношении петролейный эфир и ацетон 8-9:2-1, соответственно, при гидромодуле 5 в течение 5 минут, последовательно трехкратно экстрагируют настаиванием 40-55% спиртом формулы CnH2nOH, где n=2 или n=3, при гидромодуле 40-48 в течение 29-46 минут, процесс ведут в СВЧ камере в условиях широтно-импульсной модуляции СВЧ излучения со скважностью пачек импульсов, равной 1,3, длительностью пачек импульсов СВЧ 23 секунд, частотой излучения 2450 МГц, с удельной мощностью 41,6 Вт/дм3 с нагреванием суспензии сырье-экстрагент до 66°С с периодическим перемешиванием суспензии, отделяют экстракт фильтрованием или центрифугированием и упаривают в вакууме досуха при температуре 50°С с одновременным облучением экстракта лампой накаливания 95 Вт, затем экстракт подвергают преципитации на силикагеле с функциональным покровом пор из диметилоктадецилсилильных групп при соотношении сухой остаток-сорбент 1:5 с последующей сушкой в вакууме 0,05-0,08 Па, далее преципитат помещают в форколонку для флэш-хроматографии поверх сорбента дисперсности 40-64 мкм и элюируют нафтодиантроновые пигменты водными растворами этилового спирта с градиентом концентрации спирта от 5% до 60%, кристаллизацию гиперицина и псевдогиперицина осуществляют из смеси этанол-вода в режиме вакуумной кристаллизации с одновременным концентрированием маточного раствора на роторном испарителе в вакууме с остаточным давлением 33-13 кПа (25-10 мм рт.ст.), сушку гиперицина и псевдогиперицина осуществляют в вакууме при температуре 60°С.
| ПУНЕГОВ В.В | |||
| и др | |||
| Экстрагирование гиперицина и псевдогиперицина из зверобоя продырявленного в условиях микроволновой активации процесса // Химия растительного сырья, 2014 | |||
| CN 1883520 A, 27.12.2006 | |||
| Безопасная бритва типа "Жиллет" | 1927 |
|
SU8087A1 |
| Приспособление к суппорту токарного станка для автоматического выключения самохода | 1928 |
|
SU17972A1 |
| СОСТАВНАЯ РАМА ПОВОРОТНОГО КРУГА ИЛИ ПЕРЕДВИЖНОЙ ТЕЛЕЖКИ | 1924 |
|
SU948A1 |
| ЕР 13456114 А1, 24.09.2003 | |||
| СТАСЕВИЧ О.В | |||
| и др | |||
| Хроматографический анализ и разделение гиперицинсодержащего экстракта зверобоя //Труды БГТУ, 2012. | |||
Авторы
Даты
2017-06-21—Публикация
2015-06-23—Подача