Изобретение относится к области медицины и касается способа получения биологически активного соединения из растительного сырья, обладающего желчегонным и гепатопротекторным действием.
Известно несколько способов получения 1-гидрокси-2,3,5-триметоксиксантона.
Способ 1. Из корней растения Frasera caroliniensis Walt. (5500 г) был выделен 1-гидрокси-2,3,5-триметоксиксантон следующим образом: экстракция растительного сырья ацетоном, жидкофазная экстракция СН2Cl2/пентаном, концентрирование полученного извлечения (29 г) с последующей кристаллизацией из МеОН (18.5 г смеси ксантонов), колоночная хроматография на силикагеле смеси ксантонов (элюирование проводили смесью растворителей - гексан/этилацетат - 3:1) и перекристаллизация из СН2Cl2/гексана и МеОН. Выход 1-гидрокси-2,3,5-триметоксиксантона составил 0.11% от массы абсолютно сухого сырья [Stout G.H., Balkenhol W.J. Xanthones of the Gentianaceae. - I. Frasera caroliniensis Walt. / G.H.Stout, W.J.Balkenhol. // Tetrahedron. - 1969. - v.25. - p.1947].
Способ 2. Из корней растения Frasera albicaulis Dougl. ex Griesb. (1644 г) также был выделен 1-гидрокси-2,3,5-триметоксиксантон. Выделение проводили путем экстракции растительного сырья МеОН, жидкофазной экстракцией 20%-ным CH2Cl2 в пентане, концентрированном полученного извлечения (31.73 г) с последующей колоночной хроматографией на силикагеле (элюирование проводили смесью растворителей - гексан/этилацетат - 2:1) и перекристаллизацией из СН2Cl2/гексана. Выход 1-гидрокси-2,3,5-триметоксиксантона составил 0.04%, от массы абсолютно сухого сырья [Stout G.H., Christensen E.N., Balkenhol W.J., Stevens K.L. Xanthones of the Gentianaceae.- II. Frasera albicaulis Dougl. ex Griesb. / G.H.Stout, E.N. Christensen, W.J. Balkenhol, K.L. Stevens. // Tetrahedron.- 1969.- v. 25.-p. 1961].
Способ 3. 1-гидрокси-2,3,5-триметоксиксантон был выделен из корней и надземной части растения Halenia asclepidea (HBK) Don (422 г) в результате экстракции растительного сырья гексаном, концентрированием полученного извлечения (15.5 г) с последующим растворением в CH2Cl2, фильтрованием, экстрагированием водно-метанольным раствором КОН, разбавлением водой, подкислением и экстракцией CH2Cl2. Извлечение (2.55 г) подвергли препаративной тонкослойной хроматографии на силикагеле (в качестве подвижной фазы использовали систему растворителей - петролейный эфир/этилацетат - 8:1) с последующей перекристаллизацией из МеОН. Выход 1-гидрокси-2,3,5-триметоксиксантона составил 0.06% от массы абсолютно сухого сырья [Stout G.H., Fries J.L. The xanthones of a Halenia species. / G.H.Stout, J.L.Fries. // Phytochemistry. - 1970. - v.9. - p.235].
Способ 4. Из корней и надземной части растения Halenia elliptica D. Don (2000 г) также был выделен 1-гидрокси-2,3,5-триметоксиксантон. Выделение проводили путем экстракции растительного сырья этанолом, концентрированием полученного этанольного извлечения (20 г), жидкофазной экстракцией водного остатка хлороформом, колоночной хроматографией на силикагеле (элюирование проводили смесью растворителей - гексан/ацетон - 19:1→18:2) и перекристаллизацией из МеОН. Выход 1-гидрокси-2,3,5-триметоксиксантона составил 0.08% от массы абсолютно сухого сырья [Dhasmana H., Garg H.S., Two xanthone glucosides from Halenia elliptica / H.Dhasmana, H.S. Garg. // Phytochemistry. - 1989. - v.28. - p.2819].
Способ 5. Способ получения 1-гидрокси-2,3,5-триметоксиксантона из корней и надземной части растения Halenia campanulata (52 г): экстракция растительного сырья CH2Cl2 и МеОН, концентрирование полученного извлечения (4 г), колоночная хроматография на силикагеле (в качестве элюента использовали систему растворителей - петролейный эфир/этилацетат - 3:1) с последующей перекристаллизацией из МеОН. Выход 1-гидрокси-2,3,5-триметоксиксантона составил 0.11%, от массы абсолютно сухого сырья [Recio-Iglesias M.-C., Marston A., Hostettmann К.Xanthones and secoiridoid glucosides of Halenia campanulata. / M.-C.Recio-Iglesias, A.Marston, K.Hostettmann. // Phytochemistry. - 1992. - v.31. - p.1387].
Недостатками указанных способов являются низкий выход целевого продукта, длительность и трудоемкость технологического процесса.
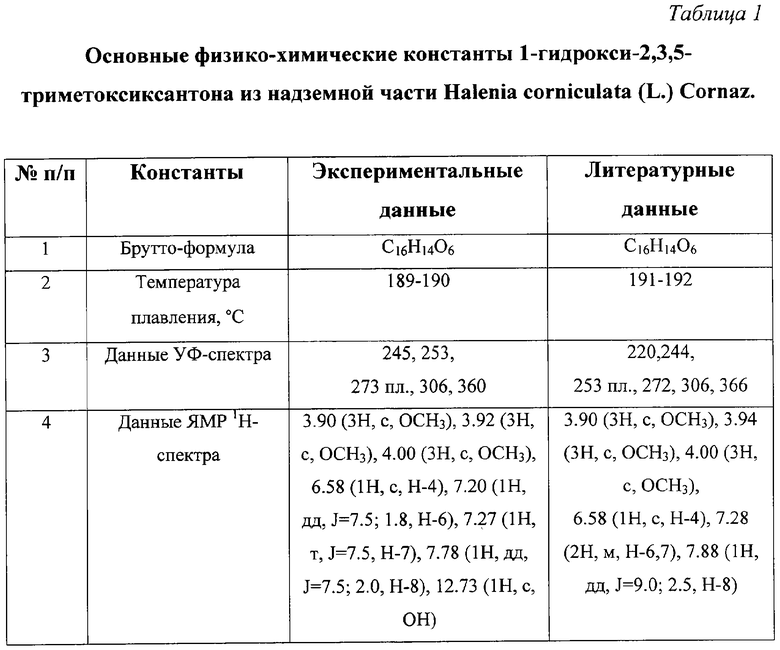
Задачей изобретения является повышение выхода целевого продукта (1-гидрокси-2,3,5-триметоксиксантона) из надземной части Halenia corniculata (L.) Cornaz. с желчегонным и гепатопротекторным действием и расширение сырьевой базы для получения холеритических средств.
Указанная задача решается следующим способом: растительное сырье - надземную часть Halenia corniculata (L.) Cornaz с остаточной влажностью не более 10%, измельченную до размера частиц 1-2 мм, экстрагируют 96%-ным этанолом трижды, отфильтровывают спиртовые извлечения, концентрируют спиртовые извлечения, добавляют дистиллированную воду и последовательно экстрагируют хлороформом (3×1000 мл), упаривают объединенные хлороформные извлечения, добавляют силикагель к хлороформным извлечениям и концентрируют. Хлороформное извлечение хроматографируют на колонке с силикагелем. Элюирование проводят смесью растворителей - гексан/этилацетат (7/3). Фракции, содержащие 1-гидрокси-2,3,5-триметоксиксантон, объединяют, концентрируют досуха и дважды перекристаллизовывают из этанола. Выход составляет 0.15% от массы абсолютно сухого сырья
Нижеследующие примеры иллюстрируют заявляемый способ.
Пример 1. 100 г воздушно-сухого измельченного сырья Halenia corniculata (L.) Cornaz экстрагировали по 1000 мл 96%-ным этанолом три раза, отфильтровывали и концентрировали объединенные этанольные извлечения до 200 мл. Полученное извлечение переносили в делительную воронку, прибавляли 100 мл дистиллированной воды, после чего ксантоновые агликоны извлекали 3-х кратной экстракцией хлороформом (по 1000 мл). Объединенное хлороформное извлечение упаривали до минимального объема (100 мл), добавляли 40 г силикагеля (L 100/250) и концентрировали досуха. Полученную хлороформную фракцию (8.3 г, 8.3% от массы абсолютно сухого сырья) наносили на колонку с силикагелем (L 100/250) и элюировали хлороформом. Фракции, содержащие 1-гидрокси-2,3,5-триметоксиксантон, объединяли, концентрировали досуха и дважды перекристаллизовывали из этанола. В результате было получено 0.02 г 1-гидрокси-2,3,5-триметоксиксантона. Выход составил 0.02% от массы абсолютно сухого сырья.
Пример 2. 100 г воздушно-сухого измельченного сырья Halenia corniculata (L.) Cornaz экстрагировали по 1000 мл 96%-ным этанолом три раза, отфильтровывали и концентрировали объединенные этанольные извлечения до 200 мл. Полученное извлечение переносили в делительную воронку, прибавляли 100 мл дистиллированной воды, после чего ксантоновые агликоны извлекали 3-х кратной экстракцией хлороформом (по 1000 мл). Объединенное хлороформное извлечение упаривали до минимального объема (100 мл), добавляли 40 г силикагеля (L 100/250) и концентрировали досуха. Полученную хлороформную фракцию (8.2 г, 8.2% от массы абсолютно сухого сырья) наносили на колонку с силикагелем (L 100/250) и элюировали смесью растворителей - гексан/этилацетат - 7:3. Фракции, содержащие 1-гидрокси-2,3,5-триметоксиксантон, объединяли, концентрировали досуха и дважды перекристаллизовывали из этанола. В результате было получено 0.15 г 1-гидрокси-2,3,5-триметоксиксантона. Выход составил 0.15% от массы абс. сухого сырья.
Пример 3. 100 г воздушно-сухого измельченного сырья Halenia corniculata (L.) Cornaz экстрагировали по 1000 мл 96%-ным этанолом три раза, отфильтровывали и концентрировали объединенные этанольные извлечения до 200 мл. Полученное извлечение переносили в делительную воронку, прибавляли 100 мл дистиллированной воды, после чего ксантоновые агликоны извлекали 3-х кратной экстракцией хлороформом (по 1000 мл). Объединенное хлороформное извлечение упаривали до минимального объема (100 мл), добавляли 40 г силикагеля (L 100/250) и концентрировали досуха. Полученную хлороформную фракцию (8.0 г, 8.0% от массы абсолютно сухого сырья) наносили на колонку с силикагелем (L 100/250) и элюировали смесью растворителей - гексан/этилацетат - 8:2. Фракции, содержащие 1-гидрокси-2,3,5-триметоксиксантон, объединяли, концентрировали досуха и дважды перекристаллизовывали из этанола. В результате было получено 0.01 г 1-гидрокси-2,3,5-триметоксиксантона. Выход составил 0.01% от массы абсолютно сухого сырья.
Пример 4. 100 г воздушно-сухого измельченного сырья Halenia corniculata (L.) Cornaz экстрагировали по 1000 мл 96%-ным этанолом три раза, отфильтровывали и концентрировали объединенные этанольные извлечения до 200 мл. Полученное извлечение переносили в делительную воронку, прибавляли 100 мл дистиллированной воды, после чего ксантоновые агликоны извлекали 3-х кратной экстракцией хлороформом (по 1000 мл). Объединенное хлороформное извлечение упаривали до минимального объема (100 мл), добавляли 40 г силикагеля (L 100/250) и концентрировали досуха. Полученную хлороформную фракцию (7.8 г, 7.8% от массы абсолютно сухого сырья) наносили на колонку с силикагелем (L 100/250) и элюировали смесью растворителей - гексан/этилацетат - 6:4. Фракции, содержащие 1-гидрокси-2,3,5-триметоксиксантон, объединяли, концентрировали досуха и дважды перекристаллизовывали из этанола. В результате было получено 0.10 г 1-гидрокси-2,3,5-триметоксиксантона. Выход составил 0.10% от массы абсолютно сухого сырья.
Определение желчегонного и гепатопротекторного действия 1-гидрокси-2,3,5-триметоксиксантона.
Желчегонная активность 1-гидрокси-2,3,5-триметоксиксантона.
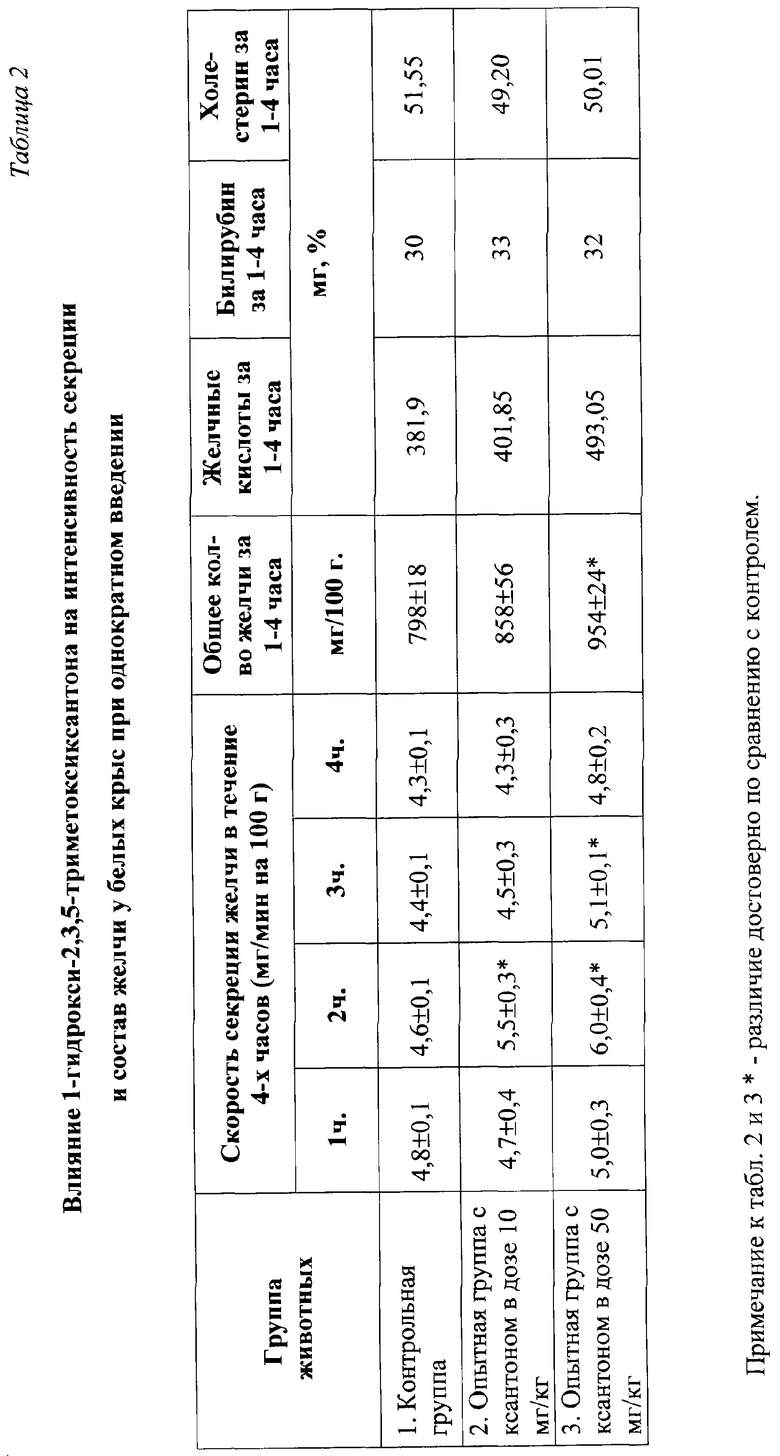
Эксперименты по оценке фармакологических свойств испытуемого ксантона проведены на белых крысах линии Wistar обоего пола с массой 180-200 г. Желчь для исследования получали в условиях острых опытов по общепринятой методике Н.П.Скакуна и А.П.Олейник [Скакун И.П., Олейник А.Н. Сравнительное действие атропина и метацина на внешнесекреторную функцию печени. // Фармакология и токсикология.-1967. - Т.30. - №3. - С.334-337]. Животные находились под наркозом (1% раствор барбамила в объеме 0.8 мл на 100 г массы животных) при комнатной температуре. Желчь собирали в течение 4-х часов с помощью специальной канюли, вставленной в общий желчный проток, через каждый час. Исследуемый ксантон вводили крысам в двенадцатиперстную кишку крыс в дозах 10 и 50 мг/кг в виде водного раствора в объеме 1 мл. Животным контрольной группы вводили эквиобъемное количество дистиллированной воды. О степени желчегонной активности ксантона судили по скорости секреции и общему количеству выделенной желчи у крыс, а также по содержанию в ней основных ее ингредиентов: желчных кислот, холестерина [Мирошниченко В.П., Громашевская Л.Л., Касаткина М.Г. и др. Определение содержания желчных кислот и холестерина в желчи. // Лабораторное дело. - 1978. - №3. - С.149-153] и билирубина [Скакун Н.П. Нейрогуморальный механизм желчегонного действия инсулина. // Проблемы эндокринологии. - 1956. - №6.- С.75-78]. Статистическая обработка полученных данных проведена с использованием критерия Стъюдента [Иванов Ю.И., Погорелюк О.Н. Статистическая обработка результатов медико-биологических исследований на микрокалькуляторах по программам. М.: Медицина, 1990. - 224 с; Монцевичюте-Эрингене Е.В. Упрощенные математико-статистические методы в медицинской исследовательской работе. // Патологическая физиология и экспериментальная терапия. - 1964. - №14. - С.71-78]., что испытуемый ксантон в дозе 10 мг/кг через 1 час после его введения способствует повышению секреции желчи по сравнению с таковой у крыс контрольной группы на 19.5%. Более выраженное желчегонное действие ксантона отмечено при дозе 50 мг/кг. При этом скорость секреции возрастала через 1 час после его введения на 30%, постепенно снижаясь в последующие часы наблюдения. Общее количество выделенной желчи превышало контроль на 19.5%. Наряду с этим, 1-гидрокси-2,3,5-триметоксиксантон способствовал синтезу и выделению желчных кислот, концентрация которых в желчи по сравнению с таковой у крыс контрольной группы повышалась на 29% (таблица 2).
Таким образом, 1-гидрокси-2,3,5-триметоксиксантон обладает желчегонным действием.
Гепатопротекторное действие 1-гидрокси-2,3,5-триметоксиксантона оценивали на модели токсического гепатита, вызванного подкожным введением белым крысам 50%-ного масляного раствора тетрахлорметана в объеме 0.4 мл на 100 г массы, 1 раз в сутки, в течение четырех дней [Николаев С.М. Растительные лекарственные препараты при повреждениях гепатобилиарной системы. - Новосибирск, 1992. - 155 с]. 1-Гидрокси-2,3,5-триметоксиксантон в экспериментально-терапевтической дозе - 30 мг/кг вводили в виде водного раствора внутрижелудочно, начиная со второго дня опыта, 1 раз в сутки, в течение всего эксперимента. Животным контрольной группы вводили дистиллированную воду по аналогичной схеме. Оценку функционального состояния печени крыс проводили на 7, 14, 21 и 28-е сутки опыта по биохимическим показателям сыворотки крови [Меньшиков В.В., Делекторская Л.Н., Золотницкая Р.П. и др. Лабораторные методы исследования в клинике. Справочник. - М., 1987. - 368 с]. Кроме того, оценивали интенсивность процессов перекисного окисления липидов (ПОЛ) по содержанию малонового диальдегида (МДА) в сыворотке крови [Темирбулатов Р.А., Селезнев Е.И. Метод повышения интенсивности свободнорадикального окисления липидсодержащих компонентов крови и его диагностическое значение. // Лабораторное дело. - 1981. - №4. - С.209-211] и антитоксическую функцию печени по бромсульфофталеиновому тесту [Соловьев В.И., Егоренко Г.Г., Фирсов А.А. Использование математической модели фармакокинетики при изучении функции печени у белых крыс методом бромсульфалеиновой пробы. // Лабораторное дело. - 1976. - №9. - С.538-542].
Оценка функции печени у крыс с токсическим гепатитом показала, что курсовое введение испытуемого ксантона оказывает выраженное гепатопротекторное действие. Как следует из таблицы 3, уже в ранние сроки эксперимента у крыс, получавших ксантон, наблюдалось торможение процессов ПОЛ, о чем свидетельствовало снижение содержания МДА в сыворотке крови, наиболее выраженное на 21-е сутки опыта (на 26%). Ингибирование процессов ПОЛ способствовало уменьшению проницаемости клеточных мембран гепатоцитов, что выражалось в снижении уровней активности маркеров цитолиза АлАТ (аланинаминотрансфераза) и АсАТ (аспартатаминотрансфераза) на 7-е сутки опыта на 10 и 18%, на 21-е - 26%, а на 28-е сутки - 38 и 34% соответственно. О степени выраженности холестаза судили на основании комплексной оценки содержания холестерина и β-липопротеидов, концентрации которых под влиянием испытуемого ксантона снижались на 7-е сутки опыта на 19 и 21%, а на 21-е сутки - 23 и 18% соответственно. Показатели тимоловой пробы, отражающие диспротеинемию, также снижались с ранних сроков опыта. Тенденция повышения содержания белка свидетельствовала об улучшении синтетической функции печени у животных. У крыс, получавших 1-гидрокси-2,3,5-триметоксиксантон, снижался коэффициент ретенции бромсульфофталеина (БСФ), являющегося важным показателем состояния антитоксической функции печени. В частности, на 7-е сутки опыта снижение составило 18%, а на 21-е - 28%.
В целом, полученные результаты свидетельствуют о желчегонном и гепатопротекторном действии 1-гидрокси-2,3,5-триметоксиксантона.
Таким образом, предлагается новый способ получения 1-гидрокси-2,3,5-триметоксиксантона, обладающий желчегонным и гепатопротекторным действием, позволяющий увеличить выход целевого продукта (1-гидрокси-2,3,5-триметоксиксантона) и расширить сырьевую базу для получения эффективных холеритических средств.
Влияние 1-гидрокси-2,3,5-триметоксиксантона на функциональное состояние печени при остром токсическом гепатите
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 1-ГИДРОКСИ-2,3,4,5-ТЕТРАМЕТОКСИКСАНТОНА, ОБЛАДАЮЩЕГО ЖЕЛЧЕГОННЫМ И ГЕПАТОПРОТЕКТОРНЫМ ДЕЙСТВИЕМ | 2000 |
|
RU2178302C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ЖЕЛЧЕГОННОЙ, ПРОТИВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЯМИ | 2014 |
|
RU2557990C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕНТИАКАУЛЕИНА, ОБЛАДАЮЩЕГО ХОЛАТОСТИМУЛИРУЮЩИМ ДЕЙСТВИЕМ | 2000 |
|
RU2178301C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ПРОТИВОВОСПАЛИТЕЛЬНОЙ, ГЕПАТОПРОТЕКТОРНОЙ, ЖЕЛЧЕГОННОЙ АКТИВНОСТЯМИ | 2018 |
|
RU2684729C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ГЕПАТОПРОТЕКТОРНЫМ, ЖЕЛЧЕГОННЫМ, ГИПОХОЛЕСТЕРИНЕМИЧЕСКИМ И РАНОЗАЖИВЛЯЮЩИМ ДЕЙСТВИЕМ | 2007 |
|
RU2339391C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИФЕНОЛОВ, ОБЛАДАЮЩИХ ГЕПАТОЗАЩИТНОЙ, ЖЕЛЧЕГОННОЙ, АНТИОКСИДАНТНОЙ И АНАЛЕПТИЧЕСКОЙ АКТИВНОСТЬЮ | 1992 |
|
RU2018315C1 |
| Способ получения пентасахарида | 1983 |
|
SU1694065A3 |
| Способ получения экстракта абортирующих веществ | 1975 |
|
SU651655A3 |
| СПОСОБ ВЫДЕЛЕНИЯ 3-ОКСО-8-ГИДРОКСИ-1,5,7А,4,8В(Н)-ГВАЙ-10(14),11(13)-ДИЕН-12,6-ОЛИДА | 2017 |
|
RU2665975C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПАТУЛЕТИНА И ПАТУЛЕТИН-7-О-β-D-ГЛЮКОПИРАНОЗИДА (ПАТУЛИТРИНА) ИЗ РАСТИТЕЛЬНОГО СЫРЬЯ | 2013 |
|
RU2546298C2 |
Изобретение относится к медицине и касается способа получения биологически активного соединения из растительного сырья, обладающего желчегонным и гепатопротекторным действием. Способ получения 1-гидрокси-2,3,5-триметоксиксантона, обладающего желчегонным и гепатопротекторным действием путем трехкратной экстракции измельченной воздушно-сухой надземной части галении рогатой Halenia comiculata (L.) Cornaz 96%-ным этанолом, отфильтровывания спиртовых извлечений, концентрирования спиртовых извлечений, трехкратной жидкофазной экстракции водного остатка хлороформом, упаривания объединенных хлороформных извлечений, добавления силикагеля и концентрирования, далее хроматографируют на колонке с силикагелем смесью растворителей - гексан/этилацетат, взятые в определенном соотношении, концентрируют и перекристаллизовывают из этанола дважды. Способ позволяет эффективно повысить выход целевого продукта 1-гидрокси-2,3,5-триметоксиксантона. 3 табл.
Способ получения 1-гидрокси-2,3,5-триметоксиксантона, обладающего желчегонным и гепатопротекторным действием путем экстракции растительного сырья этанолом, концентрированием спиртовых извлечений, жидкофазной экстракции остатка хлороформом, с последующей колоночной хроматографией и перекристаллизацией, отличающийся тем, что предварительно измельченное воздушно-сухое растительное сырье - надземную часть галении рогатой Halenia corniculata (L.) Cornaz, трижды экстрагируют 96%-ным этанолом, отфильтровывают спиртовые извлечения с последующим концентрированием спиртовых извлечений, экстрагируют водный остаток хлороформом трижды, упаривают объединенные хлороформные извлечения, добавляют силикагель и концентрируют, хроматографируют на колонке с силикагелем смесью растворителей - гексан/этилацетат (7/3), концентрируют и перекристаллизовывают из этанола дважды.
| Н.Dhasmana, H.S.Garg // Phytochemistry, 1989, v.28, p.2819 | |||
| M.-C.Recio-Iglesias, A.Marston, К.Hostettmann // Phytochemistry, 1992, v.31, p.1387 | |||
| СПОСОБ ПОЛУЧЕНИЯ 1-ГИДРОКСИ-2,3,4,5-ТЕТРАМЕТОКСИКСАНТОНА, ОБЛАДАЮЩЕГО ЖЕЛЧЕГОННЫМ И ГЕПАТОПРОТЕКТОРНЫМ ДЕЙСТВИЕМ | 2000 |
|
RU2178302C1 |
| ИММУНОМОДУЛИРУЮЩЕЕ СРЕДСТВО | 1987 |
|
RU2007178C1 |
Авторы
Даты
2005-11-20—Публикация
2004-07-02—Подача