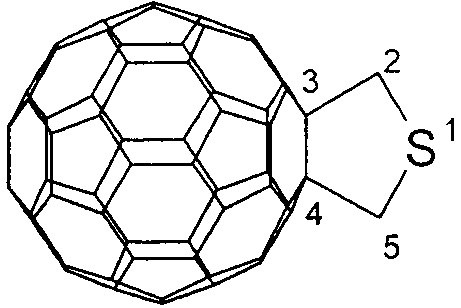
Предлагаемое изобретение относится к органической химии, конкретно к способу получения 3,4-фуллеро[60]тетрагидротиофена (1):
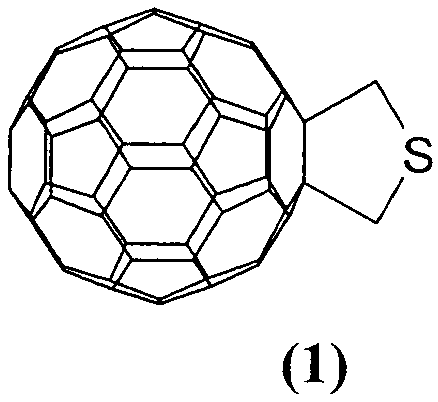
Функционально замещенные фуллерены могут найти применение в качестве комплексообразователей, сорбентов, биологически активных соединений, а также при создании новых материалов с заданными электронными, магнитными и оптическими свойствами.
Известен способ ([1], F.Effenberger, G.Grube. Synthesis, 1998, 1372-1379) получения производного фуллерена с тиофеновым фрагментом формулы (2) взаимодействием С60 с 2,3-бис(бромметил)тиофеном в кипящем толуоле в присутствии дегалогенирующего реагента, состоящего из краун-эфира и KI.
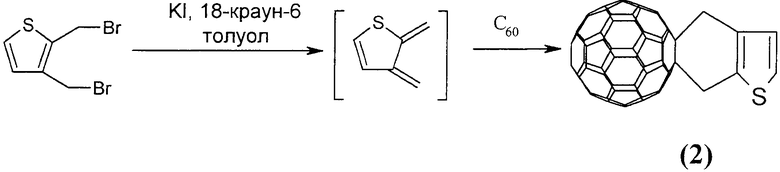
Известным способом не может быть получен 3,4-фуллеро[60]тетрагидротиофен (1).
Известен способ ([2], H.Ishida, K.Itoh, M.Ohno. Tetrahrdron, 2001, 57, 1737-1747) получения 3,4-фуллеро[60]тетрагидротиофена формулы (1) реакцией бис(триметилсилилметил)сульфоксида с С60 в о-дихлорбензоле в качестве растворителя при температуре 110°С по схеме
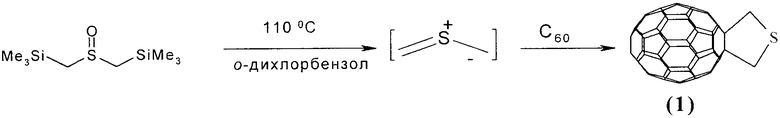
Недостатком известного метода является высокая энергоемкость процесса и пожароопасность, так как реакция может быть осуществлена лишь при повышенной температуре в кипящем толуоле (110°С).
Предлагается новый способ получения 3,4-фуллеро[60]тетрагидротиофена (1).
Сущность способа заключается во взаимодействии фуллерена С60 с диметилсульфидом (Me2S) в присутствии катализатора титанацендихлорида (Cp2TiCl2), взятых в мольном соотношении соответственно 0.01:(0.045-0.055):(0.0015-0.0025), предпочтительно 0.01:0.05:0.0020, при комнатной температуре (˜20°С) в течение 66-78 ч, предпочтительно 72 ч, в растворе толуола. Выход 3,4-фуллеро[60]тетрагидротиофена (1) составляет (по данным ВЭЖХ) 59-82%. Реакция протекает по схеме
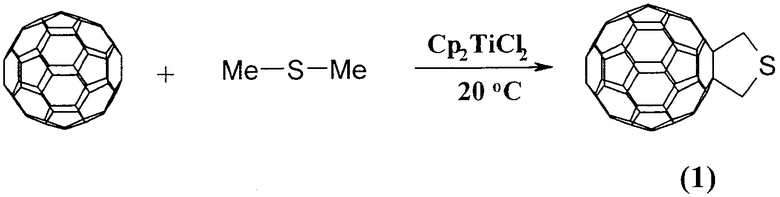
Диметилсульфид берут с избытком по отношению к фуллерену С60 с целью повышения выхода целевого продукта (1). Снижение количества диметилсульфида по отношению к С60 нецелесообразно, так как приводит к уменьшению выхода целевого продукта. Без катализатора данная реакция не идет.
Проведение указанной реакции в присутствии катализатора титаноцендихлорида (Cp2TiCl2) больше 25 мол.% по отношению к С60 не приводит к существенному увеличению выхода целевого продукта (1). Использование катализатора титаноцендихлорида (Cp2TiCl2) менее 15 мол.% по отношению к С60 снижает выход продукта (1), что связано, возможно, со снижением каталитически активных центров в реакционной массе.
Изменение соотношения исходных реагентов в сторону значительного увеличения содержания диметилсульфида по отношению к фуллерену[60] приводит к присоединению дополнительных молекул исходного сульфида к молекуле С60.
Существенные отличия предлагаемого способа
Предлагаемый способ базируется на использовании в качестве исходного реагента диметилсульфида и катализатора титаноцендихлорида (Cp2TiCl2), реакция идет в толуоле при температуре ˜20°С. В известном способе используется бис(триметилсилилметил)сульфоксид в качестве исходного реагента, реакция идет в о-дихлорбензоле при температуре 110°С.
Предлагаемый процесс, в отличие от известного, не является энергоемким и пожароопасным и позволяет получать 3,4-фуллеро[60]тетрагидротиофен (1) уже при комнатной температуре.
Способ поясняется следующими примерами.
ПРИМЕР 1. В стеклянную колбу объемом 50 мл помещают 0.01 ммоля фуллерена С60, 10 мл «сухого» толуола, 0.05 ммоля диметилсульфида и 0.002 ммоль катализатора Cp2TiCl2, перемешивают 72 часа при температуре 20°С, получают 3,4-фуллеро[60]тетрагидротиофен общей формулы (1) с выходом 74% (по данным ВЭЖХ). Спектр ЯМР 13С 3,4-фуллеро[60]тетрагидротиофена (1) (δ, м.д.): 56.46 (С2,5), 74.53 (С3,4). Сигналы углеродных атомов фуллеренового фрагмента располагаются в области 139-158 м.д.
Другие примеры, подтверждающие способ, приведены в таблице.
В качестве растворителя использовали толуол, реакции проводили при комнатной температуре (˜20°С).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 2,5-ДИАЛКИЛ-3,4-ФУЛЛЕРО[60]ТЕТРАГИДРОТИОФЕНОВ | 2007 |
|
RU2342382C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2,5-ДИАЛКИЛ-3,4-ФУЛЛЕРО[60]ТЕТРАГИДРОТИОФЕН-1-ОНОВ | 2007 |
|
RU2342377C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2,5-ДИФЕНИЛ-3,4-ФУЛЛЕРО[60]ТЕТРАГИДРОТИОФЕН-1-ОНА | 2007 |
|
RU2342380C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3,4-ФУЛЛЕРО[60]ТЕТРАГИДРОТИОФЕН-1-ОНА | 2007 |
|
RU2342381C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2,5-ДИФЕНИЛ-3,4-ФУЛЛЕРО[60]ТЕТРАГИДРОТИОФЕНА | 2007 |
|
RU2342379C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2-АЛКИЛ-5-ФЕНИЛ-3,4-ФУЛЛЕРО[60]ТЕТРАГИДРОТИОФЕНОВ | 2007 |
|
RU2342376C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ФУЛЛЕРО-7-ТИАБИЦИКЛО[2.2.1]ГЕПТАНА | 2007 |
|
RU2349593C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,5-ДИАЛКИЛ(2,2,5,5-ТЕТРААЛКИЛ)-3,4-ФУЛЛЕРО[60]ТЕТРАГИДРОФУРАНОВ | 2008 |
|
RU2371441C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ФЕНИЛ-2,5-ДИАЛКИЛ-3,4-ФУЛЛЕРО[60]ФОСФОЛАНОВ | 2006 |
|
RU2310660C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,2,5-ТРИАЛКИЛ-3,4-ФУЛЛЕРО[60]ФОСФОЛАНОВ | 2006 |
|
RU2315055C1 |
Настоящее изобретение относится к области органической химии, конкретно к способу получения 3,4-фуллеро(60)тетрагидротиофена формулы
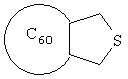
который может найти применение в качестве комплексообразователя, сорбента, биологически активного соединения, а также при создании новых материалов с заданными электронными, магнитными и оптическими свойствами. Сущность способа заключается во взаимодействии фуллерена С60 с диметилсульфидом в присутствии катализатора Cp2TiCl2 в среде толуола при температуре ˜20°С в течение 66-78 часов. Выход целевого продукта составляет 59-82%. 1 табл.
Способ получения 3,4-фуллеро[60]тетрагидротиофена (1)
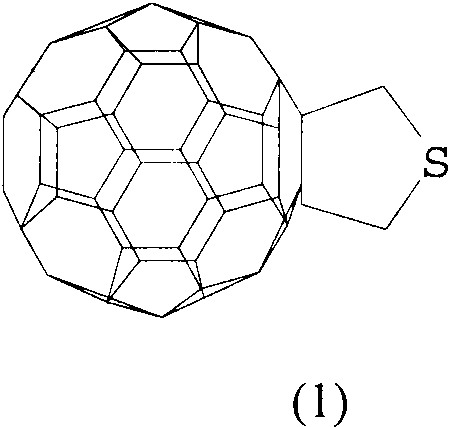
отличающийся тем, что фуллерен С60 подвергают взаимодействию с диметилсульфидом в присутствии катализатора титанацендихлорида при мольном соотношении С60 : диметилсульфид : Ср2TiCl2=0,01:(0,045-0,055):(0,0015-0,0025) в среде толуола при комнатной температуре (˜20°С) в течение 66-78 ч.
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ФУЛЛЕРЕНО[60]-2,3,4,7-ТЕТРАГИДРО-1H λ-ТИЕПИН-1,1-ДИОКСИДА | 2001 |
|
RU2191182C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФУЛЛЕРЕН[60]СУЛЬФОКСИДОВ | 2000 |
|
RU2188154C2 |
| US 5372798, 13.12.1994. | |||
Авторы
Даты
2008-12-27—Публикация
2007-02-05—Подача