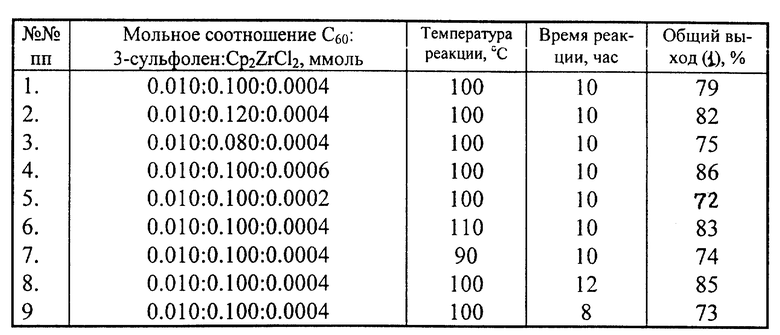
Предлагаемое изобретение относится к области органической химии, конкретнокспособуполучения2,3-фуллерено[60]-2,3,4,7-тетрагидро-1Hλ6-тиепин-1,1-диоксида общей формулы (1):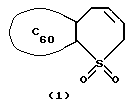
Функционально замещенные фуллерены могут найти применение в качестве комплексообразователей, сорбентов, биологически активных соединений. С их помощью могут быть созданы новые органические молекулы с заданными электронными, магнитными и оптическими свойствами.
Известен способ (W. L. Mock. Stereochemical Consequences of Orbital Symmetry Control in the Reversible Combining of Sulfur Dioxide with Conjugated Systems (Sulfolene Reactions). JACS, 1975, 97, 3666-3672) получения 2,7-диметил-2,7-дигидротиепин-1,1-диоксида (2) реакцией циклоприсоединения двуокиси серы (SO2) к октатриену по схеме: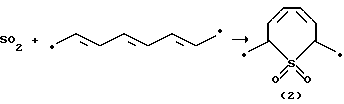
Известным способом не может быть получен 2,3-фуллерено[60]-2,3,4,7-тетрагидро-1Н λ6-тиепин-1,1-диоксид (1).
Известен способ (L.A. Paquette, S. Maiorana. C-C Bond Cleavage Reactions of Episulphones. A Convenient New Synthesis of Thiepin 1,1-Dioxide. Chem. Commun. , 1971, 313-314) получения 3,4-бензо-2,5-дигидротиепин-1-оксида (3) взаимодействием винилдиазометана с бензилиденсульфоном по схеме: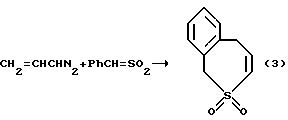
Известный способ не позволяет получать 2,3-фуллерено[60]-2,3,4,7-тетрагидро-1Н λ6-тиепин-1,1-диоксид (1).
Таким образом, в литературе отсутствуют сведения по синтезу 2,3-фуллерено[60]-2,3,4,7-тетрагидро-1Н λ6-тиепин-1,1 -диоксида (1).
Предлагается новый способ синтеза 2,3-фуллерено[60]-2,3,4,7-тетрагидро-1Н λ6-тиепин-1,1-диоксида (1).
Сущность способа заключается во взаимодействии фуллерена [60] с 3-сульфоленом, взятыми в мольном соотношении С60:3-сульфолен=1:(8÷12), предпочтительно 1:10, в присутствии катализатора цирконацендихлорида (Cp2ZrCl2, где Ср= η5-С5Н5), взятого в количестве 2-6 мол.% по отношению к фуллерену [60] , предпочтительно 4 мол.%, в атмосфере аргона при 90-110oС, предпочтительно 100oС, в течение 8-12 ч, предпочтительно 10 ч, в толуоле в качестве растворителя.Выход2,3-фуллерено[60]-2,3,4,7-тетрагидро-1Нλ6-тиепин-1,1-диоксида (1) составляет (по данным ВЭЖХ) 72-86%. Реакция протекает по схеме: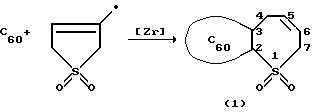
Снижение количества 3-сульфолена по отношению к С60, например С60:3-сульфолен= 1: 5, приводит к снижению выхода целевого продукта (1). Изменение соотношения исходных реагентов в сторону увеличения содержания 3-сульфолена по отношению к С60, например С60:3-сульфолен=1:15, не приводит к существенному повышению выхода целевого продукта (1).
2,3-Фуллерено[60] -2,3,4,7-тетрагидро-1Н λ6-тиепин-1,1-диоксид (1) образуется только с участием фуллерена [60] и 3-сульфолена в присутствии катализатора Cp2ZrCl2.
Проведение реакции при более высокой температуре, например 120oС, не приводит к значительному увеличению выхода целевого продукта (1). При меньшей температуре, например 80oС, снижается скорость реакции.
Существенные отличия предлагаемого способа:
1. Предлагаемый способ базируется на использовании в качестве исходных реагентов 3-сульфолена и фуллерена [60], в качестве катализатора используется Cp2ZrCl2. В известном способе в качестве исходных реагентов используются винилдиазометан с бензилиденсульфоном. Предлагаемый способ в отличие от известного позволяет получать 2,3-фуллерено[60] -2,3,4,7-тетрагидро-1Н λ6-тиепин-1,1-диоксид (1), синтез которого в литературе не описан.
Способ поясняется следующими примерами:
Пример 1. В металлический "пальчиковый" автоклав объемом 17 мл в атмосфере аргона при комнатной температуре помещают 0,010 ммоль фуллерена [60], 6 мл сухого толуола, 0,100 ммоль 3-сульфолена и 0,0004 ммоль Cp2ZrC12, перемешивают 10 ч при 100oС, получают 2,3-фуллерено[60]-2,3,4,7-тетрагидро-1Н λ6-тиепин-1,1-диоксид (1) с выходом 79% (по данным ВЭЖХ).
Спектральные характеристики 2,3-фуллерено[60] -2,3,4,7-тетрагидро-1Н λ6-тиепин-1,1-диоксида (1):
Спектр ЯМР 13С (δ, м.д.): 78,9 (С2), 66,0 (С3), 47,4 (С4), 133,0 (С5), 132,5 (С6), 59,8 (С7), 133,0-159,6 (фуллереновые).
Другие примеры, подтверждающие способ, приведены в таблице.
В качестве растворителя целесообразно использовать толуол, т.к. в нем наибольшая растворимость фуллерена [60].
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ФУЛЛЕРЕНО[60]-6-МЕТИЛ-2,3,4,7-ТЕТРАГИДРО-1H-1λ-ТИЕПИН-1,1-ДИОКСИДА | 2001 |
|
RU2191183C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ЭТИЛ-3,3-ДИАЛКИЛ-6,7-ФУЛЛЕРЕНО[60]ЦИКЛОГЕПТА-2-ОКС-1-АЛАНОВ | 2002 |
|
RU2206570C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-[(2,3-(ФУЛЛЕРЕН[60])-2,3-ДИГИДРО-1H-1,2,3-БЕНЗОТРИАЗОЛ-1-ИЛ)МЕТИЛ]-N,N-Д ИМЕТИЛАМИНА | 2000 |
|
RU2183634C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-АЛКОКСИ-2,3-ФУЛЛЕРЕН[60]АЛЮМАЦИКЛОПРОПАНОВ | 1999 |
|
RU2160274C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ДИАЛКИЛАМИН-2,3-ФУЛЛЕРЕН[60]АЛЮМАЦИКЛОПРОПАНОВ | 1999 |
|
RU2160271C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-[(4,5-(ФУЛЛЕРЕН[60])-4,5-ДИГИДРО-1H-1,2,4-ТРИАЗОЛ-1-ИЛ)МЕТИЛ]-N,N-ДИМЕТИ ЛАМИНА | 2000 |
|
RU2184117C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФУЛЛЕРЕН[60]СУЛЬФОКСИДОВ | 2000 |
|
RU2188154C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ЭТИЛ-2,3-ФУЛЛЕРЕН[60]АЛЮМАЦИКЛОПРОПАНОВ | 1999 |
|
RU2160272C1 |
| СПОСОБ ПОЛУЧЕНИЯ 3,4-ФУЛЛЕРЕН[60]-1,2-ОКСИТИОЭТАН-2-(1',4'-БУТ-2'-ЕН)-2-ОКСИДА | 1999 |
|
RU2164918C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ЭТИЛ-3-АЛКИЛ(ФЕНИЛ)-6,7-ФУЛЛЕРЕНО[60]ЦИКЛОГЕПТА-2-ОКС-1-АЛАНОВ | 2002 |
|
RU2220969C2 |
Изобретение относится к области органической химии, а именно к способу получения функционально замещенного фуллерена формулы I, который может найти применение в качестве комплексообразователя, сорбента, биологически активного соединения. Сущность способа заключается во взаимодействии фуллерена[60] с избытком 3-сульфолена в присутствии катализатора Cp2ZrCl2 в атмосфере аргона в среде толуола при 90-110oС в течение 8-12 ч. Выход целевого продукта составляет 72-86%. 1 табл.
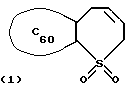
Способполучения2,3-фуллерено[60]-2,3,4,7-тетрагидро-1Нλ6-тиепин-1,1-диоксида (1) общей формулы
отличающийся тем, что фуллерен [60] взаимодействует с избытком 3-сульфолена в присутствии катализатора Cp2ZrCl2, взятыми в мольном соотношении С60: 3-сульфолен: Ср2ZrСl2= 1:(8-12):(0,02-0,06), в атмосфере аргона в среде толуола в качестве растворителя при 90-110oС в течение 8-12 ч.
| СПОСОБ ПОЛУЧЕНИЯ 3,4-ФУЛЛЕРЕН [60]-1,2-ОКСИТИОЭТАН-2(2',3'-ДИМЕТИЛ-1',4'-БУТ-2'-ЕН)-2-ОКСИДА | 1999 |
|
RU2165425C1 |
| СПОСОБ ПОЛУЧЕНИЯ (1+1)-АДДУКТОВ ФУЛЛЕРЕНА С С НОРБОРНАДИЕНОМ И ЕГО 7-СПИРОЦИКЛОПРОПАНЗАМЕЩЕННЫМ ПРОИЗВОДНЫМ | 1998 |
|
RU2137743C1 |
| EP 0919520 A2, 02.06.1999 | |||
| EP 0770577 A1, 02.05.1997. | |||
Авторы
Даты
2002-10-20—Публикация
2001-05-14—Подача