Предлагаемое изобретение относится к микробиологической промышленности и биотехнологии, а именно к биологически активным добавкам на основе молочного сырья и железа.
Известно, что дефицит железа приводит к повышению ломкости волос и ногтей, воспалению органов рото- и носоглотки, изменению характера вкусовых ощущений, снижению функции щитовидной железы и активности иммунной системы, повышению восприимчивости организма к различным инфекциям и, как следствие, к развитию железодефицитной анемии (ЖДА).
Железодефицитные состояния по-прежнему остаются актуальной, и во многих отношениях не решенной проблемой современной медицины. Для профилактики и лечения железодефицитных состояний принимаются препараты, содержащие железо. В медицинской и ветеринарной практике железосодержащие препараты применяются внутрь и парентерально (внутримышечно или внутривенно).
Препараты для парентерального применения представлены комплексными соединениями - декстраном, декстрином, сахаратом, глюконатом и сорбитолом (см.: Чернов В.М. «Применение внутримышечных препаратов железа в клинической практике» // Гематология и трансфузиология, 2004, т.49, № 3, с.27).
Имеются данные, что многократное введение декстрана железа в один и тот же участок мышцы может способствовать канцерогенезу. Кроме того, ионные парентеральные ферропрепараты вызывают достаточно серьезные побочные проявления: боль в месте введения, вкус железа во рту, снижение аппетита, лихорадку, крапивницу, артралгии, астму, тошноту и расстройства кровообращения (см.: «Дефицит железа у детей: проблемы и решения» Т.В.Казаков и др. // Consillium-Medicum приложение, 2002, т.4, № 3, с.15-17). Глюконат железа для внутривенного введения настолько токсичен, что может применяться только в режиме низких доз. Декстранат железа имеет невысокий, но значительный риск анафилаксии (см.: Чернов В.М. «Применение внутримышечных препаратов железа в клинической практике» // Гематология и трансфузиология, 2004, т.49, № 3, с.27).
Препараты для внутреннего применения представлены сульфатом железа (актиферрин, сорбифер дурулес, конферон, тардиферон, ферроплекс), хлоридом железа (гемофер, сироп алоэ с железом), глюконатом железа (апаферроглюконат), фумаратом железа (ферретоаб), а также препаратом трехвалентного железа - мальтофером (см.: Воробьев П.А. Анемичный синдром в клинической практике. - М.: Ньюдиамед, 2001. - 168 с.).
Лечение пероральными препаратами железа, чаще всего солевыми и двухвалентными, эффективно, просто, дешево, но ограничено побочными эффектами, плохой всасываемостью солевых препаратов железа.
Известен железосодержащий препарат Ферпос для профилактики алиментарной анемии, содержащий катионное двухвалентное железо с концентрацией 1,0±0,15% (см.: Заявка РФ № 92006763, кл. А61K 35/24, 1992 г.).
Однако данный препарат имеет невысокую биологическую активность за счет низкого содержания железа.
Известен железосодержащий препарат Ферокс для профилактики алиментарной анемии с концентрацией двухвалентного железа 1,0±0,15% (см.: Заявка РФ № 92006855, кл. А61K 33/26, 1995).
Однако препарат также имеет невысокую биологическую активность за счет низкого содержания железа.
Недостатком вышеназванных известных решений является то, что железо в этих препаратах, хоть и находится в двухвалентной форме, но в процессе усвоения может подвергнуться быстрому химическому окислению, что впоследствии приведет к образованию нерастворимого Fe3+, который не усваивается организмом, накапливается в нем, вызывая тем самым, эффект отравления.
Связывать железо и оставлять его в усвояемой форме способны аминокислоты. Дело в том, что ионы железа, находясь в оболочке аминокислоты, не требуют дополнительных превращений в организме, они являются готовыми к использованию и транспортировке клетками эпителия тонкой кишки, где происходит основной процесс усвоения. Такой процесс называется «хелатированием». Употреблять нехелатированные минеральные вещества (в том числе и железо) означает подвергать организм еще большей нагрузке, так как он пытается выделить дополнительные аминокислоты, необходимые для процесса хелатирования. Другими словами, организм будет пытаться самостоятельно хелатировать минеральные вещества, но этим перегрузит систему и растратит те аминокислоты, которые должны использоваться в других процессах.
Наиболее близким по технической сущности к заявляемому изобретению является получение биологически активной добавки к пище "Magni Fe++", содержащей 20 мг двухвалентного железа в виде аминокислотного хелата (см.: Шарманов Т.Ш. Отчет центра экспертизы БАД по клинической апробации биологически активной добавки "Magni Fe++", 2003 г.).
Недостатком данного препарата является то, что при его изготовлении не предусмотрена подготовка желудочно-кишечного тракта к оптимальному усвоению железа.
Установлено, что существует причинная связь между слизистой желудка и дефицитом железа, что имеет непосредственное отношение к патогенезу железодефицитного состояния. У подавляющего числа больных ЖДА при биопсии слизистой оболочки желудка обнаружены морфологические изменения от поверхностного гастрита до глубокой атрофии железистого аппарата. В настоящее время считается, что морфофункциональные изменения слизистой оболочки желудка при ЖДА носят вторичный характер и являются не причиной, а следствием железодефицита (см.: "Способ лечения железодефицитной анемии" патент RU 2272641 С2, 27.03.2006 Бюл. №9).
С учетом имеющихся недостатков железосодержащих препаратов поиск новых биологически активных добавок для профилактики и лечения железодефицита остается актуальным.
Задачей настоящего изобретения является создание биологически активной добавки к пище, обогащенной усвояемым хелатированным железом, на основе пропионовокислых бактерий для восполнения недостатка железа в организме и профилактики ЖДА.
Технический результат настоящего изобретения состоит в повышении усвояемости железа организмом, сокращении срока усвоения за счет подготовки пропионовокислыми бактериями пищеварительного тракта к приему биодоступного хелатного железа, увеличении количества жизнеспособных клеток пропионовокислых бактерий.
Проведенные исследования по данной проблеме не выявили способов, идентичных предложенному.
Указанный технический результат достигается тем, что согласно изобретению, в приготовленную питательную среду на основе осветленной творожной сыворотки вносят хелатирующий агент в виде раствора казеиновых фосфопептидов в количестве 15-20% от объема питательной среды и сульфат железа в количестве 0,35-0,45 мг/мл, среду стерилизуют, охлаждают, вносят 3-5% активизированных культур пропионовокислых бактерий и проводят культивирование.
Существенными отличительными признаками заявляемого способа являются: использование в качестве хелатирующего агента раствора казеиновых фосфопептидов и культивирование среды активизированными культурами пропионовокислых бактерий. Железо в питательную среду вводится в виде двухвалентной соли (FeSO4).
Пропионовокислые бактерии (ПКБ) являются представителями нормальной микрофлоры желудочно-кишечного тракта человека и животных, обладают морфокинетическим действием, образуют ферменты, участвующие в метаболизме белков, углеводов, липидов и нуклеиновых кислот, продуцируют биологически активные соединения, в частности витамин В12, выполняют иммуногенную и антимутагенную функцию, а также участвуют в детоксикации экзо- и эндогенных токсических агентов. Пропионовокислые бактерии положительно влияют на пристеночное пищеварение, абсорбируя промежуточные метаболиты, в состав которых могут входить и микроэлементы, конкурирующие с железом при всасывании (см.: Воробьева Л.И. Пропионовокислые бактерии. М.: Изд-во МГУ, 1995. 380 с). Поэтому использование ПКБ в заявляемом способе позволит подготовить слизистую оболочку желудочно-кишечного тракта и улучшить всасывание ионов железа и тем самым ускорит темп нормализации гематологических показателей.
В качестве инокулята в заявленном способе использовались активизированные культуры пропионовокислых бактерий разных штаммов: Propionibacterium freudenreichii subsp.shermanii типа AC-2503, Propionibacterium freudenrichii subsp.fredenreichii типа AC-2500 и Propionibacterium cyclohexanicum Kusano типа AC-2260, полученных из фонда BKM Института Биохимии и Физиологии Микроорганизмов (Москва).
Авторами было исследовано влияние различных доз сульфата железа на биохимическую активность указанных микроорганизмов с целью использования их при производстве железосодержащей БАД. Для оценки влияния железа на рост пропионовокислых бактерий сравнивали количество жизнеспособных клеток по окончании процесса культивирования, а также удельные скорости роста культур в каждом варианте опыта. За контроль взята среда без добавления сульфата железа. Результаты представлены в таблице и на фиг.1.
Из данных таблицы видно, что при концентрации железа в среде 0,25-0,45 мг/мл количество жизнеспособных клеток пропионовокислых бактерий повышается и составляет в среднем 2,5·1011 КОЕ/см3, что на порядок выше, чем в среде без железа (см. контроль). Поскольку количество жизнеспособных клеток пропионовокислых бактерий почти во всех опытных образцах было выше контрольного, можно утверждать о возможности интенсификации микробиологического роста ПБК посредством сульфата железа.
Из фиг.1 видно, что повышение концентрации FeSO4 в среде до 0,35 мг/мл для P. freudenrichii subsp. fredenreichii АС-2500 и 0,45 мг/мл для остальных штаммов приводит к значительному увеличению скорости роста (почти в 2 раза). Стимулирующее действие сульфата железа вероятно связано с тем, что при таких концентрациях ионы Fe2+ создают в среде низкий окислительно-восстановительный потенциал - необходимое условие развития пропионовокислых бактерий, а также с детоксикацией продуктов метаболизма кислорода. Увеличение концентрации сульфата железа в среде до 0,55 мг/мл приводит к замедлению скорости роста культур, можно предположить, что происходит перенасыщение среды ионами железа.
Следует отметить, что наибольшее стимулирующее воздействие сульфат железа проявил по отношению к Propionibacterium freudenreichii subsp.shermanii типа AC-2503.
С учетом удовлетворения суточной потребности взрослого человека в железе, количество вносимого в питательную среду FeSO4 установлено из расчета 0,35-0,45 мг/мл, что, при дозированном приеме добавки составляет 30% от суточной нормы потребления железа. При этом наблюдается активный рост пропионовокислых бактерий (см. фиг.1 и табл.1).
Для предотвращения окисления железа и сохранения его в усвояемой двухвалентной форме в заявленном способе используют раствор казеиновых фосфопептидов.
Казеиновые фосфопептиды (CPPS) - это фосфолированные пептиды, образующиеся из казеинов коровьего молока при их переваривании пищеварительными протеинадами. CPPS способны связывать минеральные вещества и поддерживать их в растворимом состоянии в щелочной зоне рН тонкой кишки. Кроме того, казеиновые фосфопептиды устойчивы к интенсивному протеолизу и накапливаются в дистальном отделе тонкой кишки, где усиливают пассивный транспорт минеральных элементов в циркуляцию. Способность CCPS связывать (хелатировать) железо обусловлена присутствием в структуре входящих аминокислот анионного гидрофильного участка (см.: Гаппаров М.М, Стан Е.Я. Влияние казеиновых фосфопептидов на биодоступность алиментарных минералов // Вопросы питания, № 6, 2003, с.41-44).
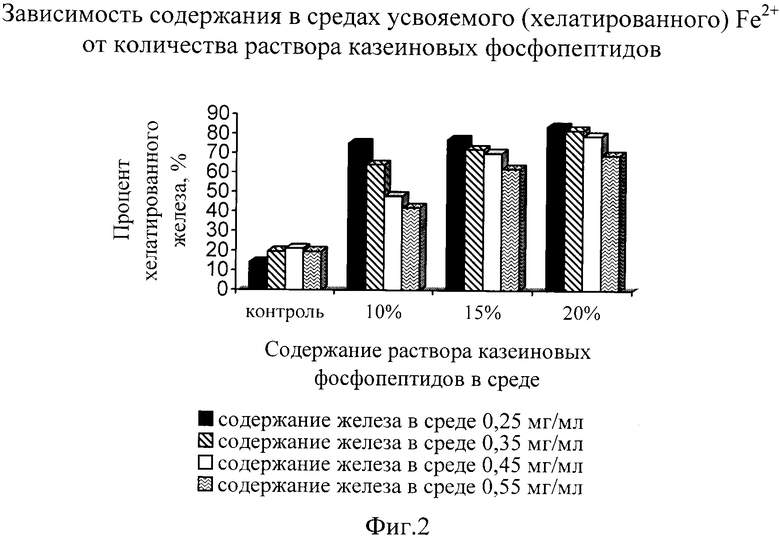
Авторами изучено влияние различного количества в среде раствора CPPS на биодоступность железа (сохранение его в растворенной, хелатной, двухвалентной форме). За процессом связывания железа следили по количеству железа, которое не подвергнулось химическому окислению, а осталось в усвояемой, двухвалентной форме от первоначальной дозы внесения. За контроль взята среда без добавления CPPs. Результаты исследований представлены на фиг.2.
Как видно из фиг.2, наличие в среде казеиновых фосфопептидов значительно способствует хелатированию железа и сохранению его в виде растворимых ионов Fe2+. Так, в средах, содержащих CPPs, в органической растворенной форме осталось почти в 4 раза больше вносимого сульфата железа, чем в среде, не содержащей фосфопептиды. Следовательно, железо в таких БАДах усвоится намного лучше и основное его количество останется в тканях организма.
Следует отметить, что в зависимости от дозы вносимого FeSO4, казеиновые фосфопептиды в средах проявили различную способность связывать железо. Так, было установлено, что добавление в питательную среду 0,45 мг/мл FeSO4 и 15-20% раствора казеиновых фосфопептидов позволит оставить в усвояемой форме до 70-80% вносимого сульфата железа; тогда как при внесении 10% CPPs в усвояемой форме остается только 45-50% вносимого FeSO4. Это объясняется тем, что молекулы CPPs могут связывать только ограниченное число молекул железа, то есть количество ионизированного (свободного) минерала не должно превышать количество имеющихся анионных гидрофильных участков аминокислот казеиновых фосфопептидов.
В качестве основы питательной среды в заявленном способе выбрана осветленная творожная сыворотка, которая является сравнительно дешевым вторичным сырьем при производстве творога. Кроме того, творожная сыворотка содержит необходимые для культивирования пробиотических микроорганизмов факторы роста: аминокислоты, витамины и микроэлементы.
Таким образом, именно выявленная совокупность отличительных признаков изобретения, заключающаяся в ведении в питательную среду раствора казеиновых фосфопептидов и культивировании среды активизированными культурами пропионовокислых бактерий, влияют на достижение технического результата, выражающегося в повышении усвояемости железа организмом, сокращении срока усвоения за счет подготовки ПКБ пищеварительного тракта к приему биодоступного хелатного железа, увеличении количества жизнеспособных клеток ПКБ.
Предлагаемый способ осуществляют следующим образом.
В качестве питательной среды для культивирования пробиотических микроорганизмов используют осветленную творожную сыворотку, в которую добавляют компоненты среды: буферные соли, аскорбиновую кислоту, пептон и агар.
В приготовленную питательную среду вносят заранее приготовленный раствор казеиновых фосфопептидов.
Раствор казеиновых фосфопептидов готовили известным способом (см.: Kunst A. Process to isolate phosphopeptides. European Patent Application EPO 476199 A1 1990). Казеиновые фосфопептиды выделяли из обезжиренного молока путем кислотной коагуляции с последующей обработкой щелочью до получения казеината натрия. Далее казеинат Na подвергали ферментативному гидролизу с последующим подкислением и осаждением. Ниже представлена технологическая схема приготовления раствора казеиновых фосфопептидов:
Обезжиренное молоко (М.д. жира не более 0,05%)
↓
Кислотная коагуляция + CaCI2
↓
Прессование, центрифугирование (влажность зерен 80%)
↓
Обработка реагентом - щелочь (рН 6,6-7,0)
↓
Na-казеинат
↓
Эндопротеиназа переваривание (рН 8,0)
↓
Гидролизат (подкисление рН 4,6)
↓
Удаление непептидного материала (центрифугирование)
↓
CaCI2-агрегация, фильтрация
↓
Раствор, обогащенный CCPs.
Раствор CCPs вносят в количестве 15-20% от объема питательной среды.
Добавляют в подготовленную питательную среду двухвалентную соль сульфата железа FeSO4 из расчета 0,35-0,45 мг/мл.
Устанавливают рН в пределах (7±0,1). Затем стерилизуют при температуре 121±1°С в течение 23±2 мин, охлаждают до 30±2°С, вносят 3-5% активизированных культур пропионовокислых бактерий.
Наращивание клеток пропионовокислых бактерий осуществляют при температуре 30°С в течение 24 часов, в условиях периодического культивирования при однократной нейтрализации среды через 12 часов насыщенным стерильным раствором углекислого натрия (NaCO3). Полученную суспензию клеток охлаждают и разливают в асептических условиях в стерильные флаконы по 10-12 см3.
Укупоривают стерильно в асептических условиях резиновыми пробками, охлаждают до температуры 4±2°С и хранят при этой температуре не более 90 суток.
Пример 1.
В качестве питательной среды для культивирования пробиотических микроорганизмов используют осветленную творожную сыворотку, в которую добавляют компоненты среды: буферные соли, аскорбиновую кислоту, пептон и агар.
В приготовленную питательную среду вносят приготовленный раствор казеиновых фосфопептидов в количестве 20% от объема питательной среды.
Добавляют в подготовленную питательную среду двухвалентную соль сульфата железа FeSO4 из расчета 0,45 мг/мл.
Устанавливают рН в пределах 7,0. Затем стерилизуют при температуре 12°С в течение 23 мин, охлаждают до 30°С, вносят 5% активизированных культур пропионовокислых бактерий штамма Propionibacterium freudenreichii subsp. shermanii AC-2503.
Наращивание клеток пропионовокислых бактерий осуществляют при температуре 30°С в течение 24 часов, в условиях периодического культивирования при однократной нейтрализации среды через 12 часов насыщенным стерильным раствором углекислого натрия (Na2СО3). Полученную суспензию клеток охлаждают и разливают в асептических условиях в стерильные флаконы по 12 см3.
Укупоривают стерильно в асептических условиях резиновыми пробками, охлаждают до температуры 4°С и хранят при этой температуре не более 90 суток.
Пример 2.
В качестве питательной среды для культивирования пробиотических микроорганизмов используют осветленную творожную сыворотку, в которую добавляют компоненты среды: буферные соли, аскорбиновую кислоту, пептон и агар.
В приготовленную питательную среду вносят приготовленный раствор казеиновых фосфопептидов в количестве 15% от объема питательной среды.
Добавляют в подготовленную питательную среду двухвалентную соль сульфата железа FeSO4 из расчета 0,35 мг/мл.
Устанавливают рН в пределах 7,0. Затем стерилизуют при температуре 12°С в течение 23 мин, охлаждают до 30°С, вносят 5% активизированных культур пропионовокислых бактерий штамма Propionibacterium freudenrichii subsp. fredenreichii типа АС-2500.
Наращивание клеток пропионовокислых бактерий осуществляют при температуре 30°С в течение 24 часов, в условиях периодического культивирования при однократной нейтрализации среды через 12 часов насыщенным стерильным раствором углекислого натрия (Na2CO3). Полученную суспензию клеток охлаждают и разливают в асептических условиях в стерильные флаконы по 12 см3.
Укупоривают стерильно в асептических условиях резиновыми пробками, охлаждают до температуры 6°С и хранят при этой температуре не более 90 суток.
Пример 3.
В качестве питательной среды для культивирования пробиотических микроорганизмов используют осветленную творожную сыворотку, в которую добавляют компоненты среды: буферные соли, аскорбиновую кислоту, пептон и агар.
В приготовленную питательную среду вносят приготовленный раствор казеиновых фосфопептидов в количестве 20% от объема питательной среды.
Добавляют в подготовленную питательную среду двухвалентную соль сульфата железа FeSO4 из расчета 0,45 мг/мл.
Устанавливают рН в пределах 7,0. Затем стерилизуют при температуре 12°С в течение 23 мин, охлаждают до 30°С, вносят 5% активизированных культур пропионовокислых бактерий штамма Propionibacterium cyclohexanicum Kusano типа AC-2260.
Наращивание клеток пропионовокислых бактерий осуществляют при температуре 30°С в течение 24 часов, в условиях периодического культивирования при однократной нейтрализации среды через 12 часов насыщенным стерильным раствором углекислого натрия (Na2CO3). Полученную суспензию клеток охлаждают и разливают в асептических условиях в стерильные флаконы по 12 см3.
Укупоривают стерильно в асептических условиях резиновыми пробками, охлаждают до температуры 4°С и хранят при этой температуре не более 90 суток.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ НАНОЧАСТИЦ СЕЛЕНА В КОЛЛОИДНОЙ ФОРМЕ ПРИ ПРОИЗВОДСТВЕ БИОЛОГИЧЕСКИ АКТИВНЫХ ДОБАВОК | 2018 |
|
RU2717997C2 |
| СПОСОБ ПОЛУЧЕНИЯ БАКТЕРИАЛЬНОГО КОНЦЕНТРАТА | 2014 |
|
RU2567813C1 |
| СПОСОБ ПОЛУЧЕНИЯ СЕЛЕНСОДЕРЖАЩЕЙ БИОЛОГИЧЕСКИ АКТИВНОЙ ДОБАВКИ | 2006 |
|
RU2333655C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМОРОЖЕННОЙ КОНЦЕНТРИРОВАННОЙ ЗАКВАСКИ НА ОСНОВЕ СИМБИОЗА ПРОБИОТИЧЕСКИХ БАКТЕРИЙ | 2008 |
|
RU2372782C1 |
| СПОСОБ ПОЛУЧЕНИЯ КИСЛОМОЛОЧНОГО ПРОДУКТА "ЦЕЛЕБНЫЙ", ОБОГАЩЕННОГО СЕЛЕНОМ | 2010 |
|
RU2440768C1 |
| СПОСОБ ПРОИЗВОДСТВА КВАСНОГО НАПИТКА | 2008 |
|
RU2361911C1 |
| СПОСОБ ПРОИЗВОДСТВА ЙОДИРОВАННЫХ ПРОДУКТОВ | 2005 |
|
RU2294645C2 |
| СПОСОБ ПОЛУЧЕНИЯ БАКТЕРИАЛЬНОГО КОНЦЕНТРАТА ПРОПИОНОВО-КИСЛЫХ БАКТЕРИЙ | 2005 |
|
RU2309982C2 |
| СПОСОБ ПРОИЗВОДСТВА ВАРЕНО-КОПЧЕНЫХ КОЛБАС | 2004 |
|
RU2284115C2 |
| СПОСОБ ПОЛУЧЕНИЯ БАКТЕРИАЛЬНОГО КОНЦЕНТРАТА КОНСОРЦИУМА ПРОБИОТИЧЕСКИХ МИКРООРГАНИЗМОВ | 2013 |
|
RU2544052C2 |
Изобретение относится к микробиологической промышленности и биотехнологии, а именно к БАД на основе молочного сырья и железа. В приготовленную питательную среду на основе осветленной творожной сыворотки вносят хелатирующий агент в виде раствора казеиновых фосфопептидов в количестве 15-20% от объема среды и сульфат железа в количестве 0,35-0,45 мг/мл. Среду стерилизуют, охлаждают и вносят 3-5% активизированных культур пропионовокислых бактерий, проводят культивирование. Изобретение позволяет повысить усвояемость железа организмом, сократить срок его усвоения за счет подготовки пропионовокислыми бактериями пищеварительного тракта к приему биодоступного железа, увеличить количество жизнеспособных клеток пропионовокислых бактерий. 2 ил., 1 табл.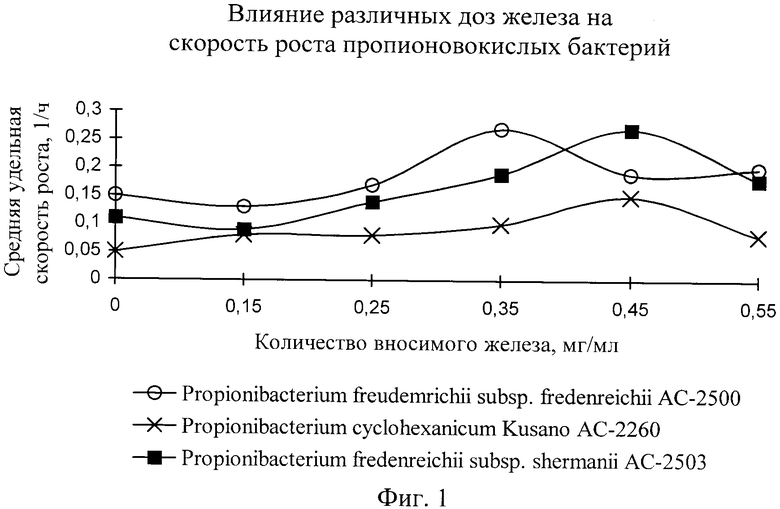
Способ получения железосодержащей биологически активной добавки к пище, характеризующийся тем, что в приготовленную среду на основе осветленной творожной сыворотки вносят хелатирующий агент в количестве 15-20% от объема питательной среды в виде раствора казеиновых фосфопептидов и сульфат железа в количестве 0,35-0,45 мг/мл, среду стерилизуют, охлаждают, вносят 3-5% активизированных культур пропионовокислых бактерий и проводят культивирование.
| ЧЕРНОВ В.М | |||
| и др | |||
| Применение внутримышечных препаратов железа в клинической практике | |||
| - Гематология и трансфузиология, т.49, №3, 2004 | |||
| СПОСОБ ПОЛУЧЕНИЯ ЖЕЛЕЗОСОДЕРЖАЩЕЙ БИОЛОГИЧЕСКИ АКТИВНОЙ ПИЩЕВОЙ ДОБАВКИ | 2005 |
|
RU2286685C1 |
| БИОЛОГИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ ПИЩЕВОГО ПРЕПАРАТА НА ОСНОВЕ ЖЕЛЕЗА ГЕМА, А ТАКЖЕ ПИЩЕВОЙ ПРЕПАРАТ, ПОЛУЧЕННЫЙ ПРИ ИСПОЛЬЗОВАНИИ ЭТОГО СПОСОБА (ВАРИАНТЫ) | 2004 |
|
RU2270576C2 |
| БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА ПРОТИВОАНЕМИЧЕСКОГО ДЕЙСТВИЯ "АНТИ-АНЕМИН" | 2001 |
|
RU2192872C1 |
Авторы
Даты
2009-02-10—Публикация
2007-04-19—Подача