Изобретение относится к сорбентам для хроматографии и может быть использовано для анализа и препаративной очистки оптически активных соединений.
Известны сорбенты для разделения оптически активных соединений на основе силикагеля с привитыми оптически активными соединениями для разделения энантиомеров. Известен, например, сорбент, содержащий на поверхности силикагеля производные хинина (SU 1429016, 1988).
Известен хиральный оптически активный сорбент, содержащий оптически активный полимер, ковалентно связанный с твердым носителем, при этом полимер представляет собой сетчатый полимер, содержащий оптически активные производные дикарбоновых кислот, диаминов, диолов или гидроксикислот, предпочтительно производные винной кислоты, а носитель представляет собой органический или неорганический материал. Способ получения данного сорбента включает закрепление производных винной кислоты на поверхности носителя, которое производят путем сетевой полимеризации через гидроксилирование в присутствии гидросилана и гидросилоксана и закрепляют на носителе в присутствии катализатора (RU 2121395, 1998).
Известен сорбент для разделения рацематов оптически активных соединений, содержащий носитель и хиральный селектор - пер-6-аминопроизводные α-, β-, или γ-циклодекстрина или их ацетилированные аналоги. Способ получения данного сорбента включает ковалентную иммобилизацию хиральных селекторов на носителе, которую осуществляют путем последовательного взаимодействия аминированного носителя с конденсирующим агентом, затем с реагентом, выбранным из группы: пер-6-амино-α-циклодекстрина, пер-6-амино-β-циклодекстрина, пер-6-амино-γ-циклодекстрина, а затем с боргидридом металла (RU 2203730, 2003).
Известен сорбент, проявляющий энантиоселективность в разделении изомеров фенилаланина на основе силикагеля с иммобилизованным хиральным полианилином, полученным путем химической окислительной полимеризации анилина (US 6265615, 2001).
Известны сорбенты на основе силикагеля с химически привитыми гликопептидными антибиотиками, такими как ванкомицин, тейкопланин, тейкопланин агликон и ристомицин (US 6669842, 2003).
Однако известные сорбенты обладают энантиоселективностью лишь к определенным классам веществ или обладают недостаточной энантиоселективностью.
Наиболее близким по технической сущности и достигаемому результату является сорбент на основе силикагеля с химически привитым гликопептидным антибиотиком эремомицином, структурная формула которого приведена на фиг.1, а также способ его получения, описанный в RU 2255802, 2005, выбранный в качестве прототипа изобретения.
Фиг.1 илюстрирует структурную формулу эремомицина.
Сорбент проявляют селективность в разделении широкого круга энантиомеров как в водно-органических, так и в неводных элюентах. Однако не всегда энантиоселективность является достаточно высокой.
Способ получения известного сорбента заключается в обработке силикагеля 3-глицидооксипропилтриалкоксисиланом с последующим взаимодействием с эремомицином в водном или водно-органическом щелочном буферном растворе при температуре не выше 40°С.
Недостатком известного способа получения сорбента является наличие в составе распознающих хиральных центров только производных эремомицина.
Задачей настоящего изобретения является повышение селективности сорбента в разделении оптических изомеров и разработка способа, позволяющего обеспечить введение в состав хирального селектора сорбента спиралевидной хиральности.
Поставленная задача решается описываемым сорбентом для хроматографии оптических изомеров, содержащим силикагель, модифицированный гликопептидным антибиотиком - эремомицином и дополнительно хиральным полианилином.
Поставленная задача решается также описываемым способом получения сорбента для хроматографии оптических изомеров, включающим модифицирование поверхности силикагеля эпоксигруппами, иммобилизацию эремомицина на поверхности силикагеля с привитыми эпоксигруппами, промывку, сушку, в котором силикагель, модифицированный эремомицином, подвергают взаимодействию с анилином в присутствии фермента лакказы и энантиомера сульфокамфорной кислоты. Предпочтительно для модифицирования поверхности силикагеля эпоксигруппами используют обработку 3-глицидоксипропилтриэтоксисиланом.
В заявленном способе наилучшие результаты показал эремомицин, полученный с использованием штамма-продуцента Amicolatopsis orientalis subsp, согласно известному способу по RU 2110578, 1998.
Ниже приведены конкретные примеры осуществления способа.
Пример 1.
50,4 г силикагеля Kromasil KR100-7-SIL суспендировали в 250 мл 0,1 М раствора ацетата натрия, доведенного ледяной уксусной кислотой до рН 5,5. К полученной суспензии добавили 40 мл 3-глицидоксипропилтриэтоксисилана. Реакционную смесь интенсивно перемешивали в течение 2 часов, а затем оставили без нагревания и перемешивания на 4 суток. По окончании реакции модифицированный силикагель промыли водой, этанолом, ацетоном и отфильтровали. Сушили при температуре 105°С. По данным элементного анализа содержание углерода составляет 7,3%.
Получен силикагель, модифицированный эпоксигруппами. Затем 15 г макроциклического антибиотика - эремомицина растворили в 230 мл дистиллированной воды. Довели рН до значения 8,58, прибавляя по каплям 1 М водный раствор КОН. Полученный раствор смешали с 56,1 г силикагеля с привитыми эпоксигруппами. Полученную реакционную смесь выдерживали при комнатной температуре, периодически перемешивая, в течение 1 недели. После окончания реакции сорбент отфильтровали и отмыли последовательно водой, метанолом и ацетоном. Сушили в сушильном шкафу при 50°С в течение 20 часов. По данным элементного анализа содержание углерода составляет 13,9%.
Реакционную смесь объемом 60 мл (рН 2,8), содержащую свежеперегнанный анилин (0,15 М) и S-сульфокамфорную кислоту (0,155 М), перемешивали на магнитной мешалке в течение 10 мин. Затем в раствор добавляли 6 г сорбента с иммобилизованным эремомицином. После этого рН реакционной смеси сдвигалась до значения 3,6. Реакцию окислительной полимеризации анилина инициировали добавлением фермента - лакказы (концентрация в реакционной смеси 1,6·10-7M) в суспензию сорбента. Синтез проводили при 4°С и постоянном перемешивании в течение 24 часов. После окончания синтеза сорбент отделяли центрифугированием (4000 об/мин), промывали бидистиллированной водой (5 раз по 100 мл) для удаления избытка исходных реагентов и 2 раза этиловым спиртом для удаления образовавшихся растворимых олигомеров. Полученные модифицированные сорбенты высушивали под вакуумом в течение 6 часов при непрерывной откачке. По данным элементного анализа содержание углерода составляет 14,4%.
Таким образом, получен силикагель с привитым через спейсер гибридным хиральным селектором:
Силикагель - Si-(СН2)3О-СН2-СН(ОН)-СН2-Эремомицин-хиральный полианилин
Пример 2
Сорбент с иммобилизованным эремомицином получали по примеру 1. Далее реакционную смесь объемом 60 мл (рН 2,8), содержащую свежеперегнанный анилин (0,15 М) и S-сульфокамфорную кислоту (0,155 М), перемешивали на магнитной мешалке в течение 1 часа для установления электростатического равновесия. Затем в раствор добавляли 6 г сорбента и обрабатывали полученную суспензию ультразвуком для увеличения смачиваемости пор сорбента. Значение рН реакционной смеси доводили до 2,8 S-сульфокамфорной кислотой. Полимеризацию анилина и отмывку полученного гибридного сорбента проводили, как описано в примере 1.
По данным элементного анализа содержание углерода составляет 14,5%.
Подтверждение модификации поверхности сорбентов полианилином дополнительно осуществлено с помощью КД-спектров в растворе диметилсульфоксида.
Полученный в соответствии с настоящим изобретением сорбент был испытан при разделении оптических изомеров в следующих условиях.
Сорбент по примеру 1 упаковали суспензионным методом в колонку из нержавеющей стали 2×100 мм и проводили разделение оптических изомеров профенов с использованием метода высокоэффективной жидкостной хроматографии.
Сорбент по примеру 2 упаковали суспензионным методом в колонку из нержавеющей стали размером 4,0×250 мм и проводили разделение оптических изомеров аминокислот и их производных с использованием метода высокоэффективной жидкостной хроматографии.
Хроматографический анализ осуществляли на ВЭЖХ хроматографе фирмы KNAUER (Германия) в составе: насос К-1001, спектрофотометрический детектор К-2501, термостат колонок Jetstream, с возможностью контроля температуры в диапазоне 5-85°С с точностью 0,1°С, ручной кран-дозатор с петлей на 20 мкл. Объем пробы 5-20 мкл. Хроматографические пики детектировали в диапазоне 210-280 нм, в соответствии с максимумами поглощения разделяемых соединений.
Запись хроматограмм и расчеты факторов удерживания разделенных компонентов k, селективности α и разрешения Rs проводили с помощью программно-аппаратного комплекса «Мультихром» (Амперсенд, Россия).
В качестве подвижной фазы использовали метанольные и водно-метанольные буферные растворы.
Пример 3
В таблице 1 представлены результаты хроматографического разделения профенов (значения факторов удерживания (А) и энантиоселективности (α)) на колонке с сорбентом, полученным по примеру 1 с привитым гибридным селектором. Разделение осуществляли в элюенте состава: 40% метанол - 60% фосфатный буфер (рН 6.5). Скорость: 0.3 мл/мин.
Из таблицы видно, что сорбент проявляет высокую энантиоселективность к данному классу соединений (α-оксикислоты).
Пример 4.
В таблице 2 представлены результаты хроматографического разделения аминокислот и некоторых их производных на колонке с сорбентом, полученным по примеру 2 с привитым гибридным селектором в сравнении с сорбентом, полученным известным способом. (RU 2255802, 2004). Разделение осуществляли в элюенте одинакового состава: 20%СН3ОН - 80% 0,1 М NaH2PO4 на колонках 4×250 мм. Поток 0,7 мл/мин.
Из полученных результатов видно, что заявленный сорбент в большинстве случаев обеспечивает более высокие результаты по энантиоселективности (α), чем известный. Хроматограммы разделения некоторых соединений представлены на фиг.3-9.
Фиг.1. Химическая структура эремомицина.
Фиг.2. Химическая структура полианилина.
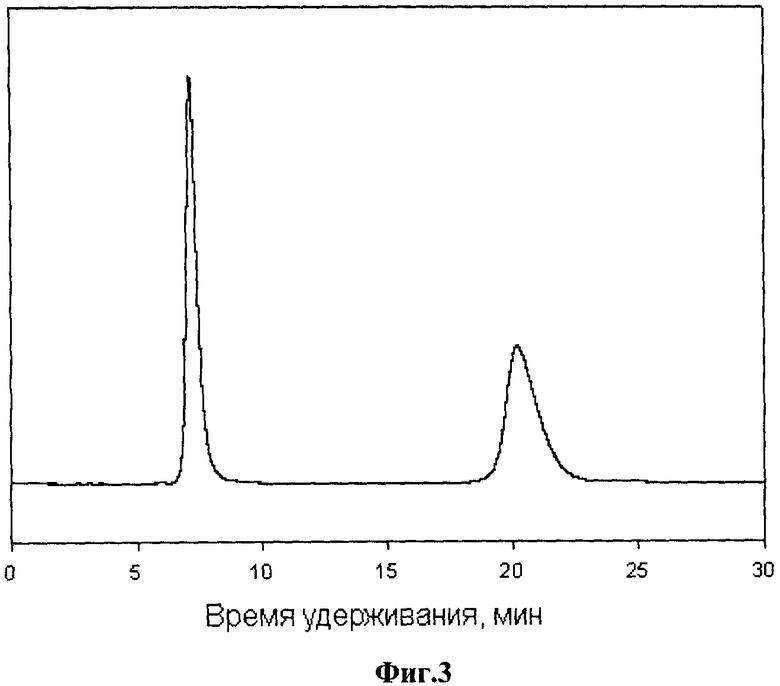
Фиг.3. Хроматограмма разделения DL-DOPA на колонке с иммобилизованным гибридным селектором. Элюент: 20% СН3ОН - 80% 0,1 М NaH2PO4; 0,7 мл/мин. Детектирование: УФ 280 нм. Температура: 22°С.
Фиг.4. Хроматограмма разделения DL-Met на колонке с иммобилизованным гибридным селектором. Элюент: 20% СН3ОН - 80% 0,1 М NaH2PO4; 0,7 мл/мин. Детектирование: УФ 210 нм. Температура: 22°С.
Фиг.5. Хроматограмма разделения DL-His на колонке с иммобилизованным гибридным селектором. Элюент: 20% СН3ОН - 80% 0,1 М NaH2PO4; 0,7 мл/мин. Детектирование: УФ 220 нм. Температура: 22°С.
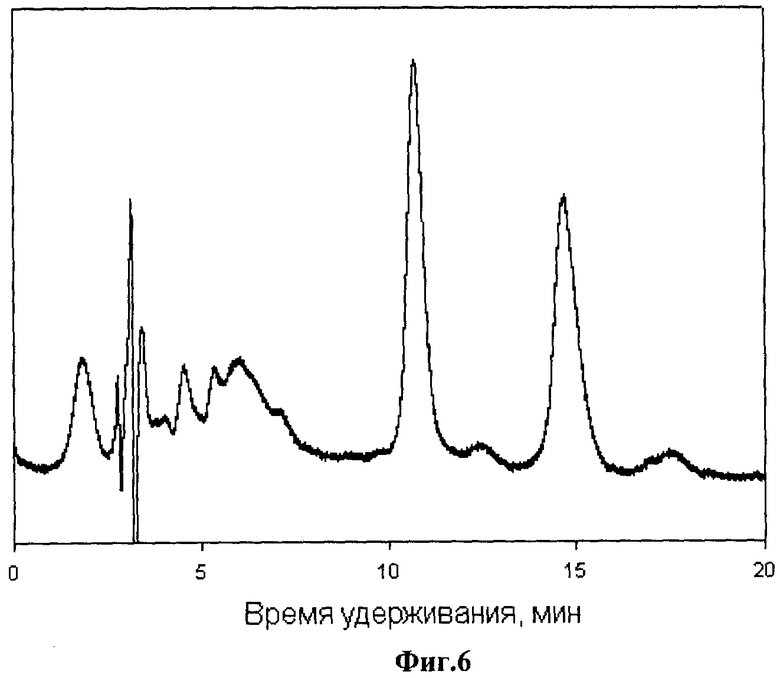
Фиг.6. Хроматограмма разделения DL-Asp на колонке с иммобилизованным гибридным селектором. Элюент: 20% СН3ОН - 80% 0,1 М NaH2PO4; 0,7 мл/мин. Детектирование: УФ 210 нм. Температура: 22°С.
Фиг.7. Хроматограмма разделения DL-Phe на колонке с иммобилизованным гибридным селектором. Элюент: 20% СН3ОН - 80% 0,1 М NaH2PO4; 0,7 мл/мин. Детектирование: УФ 220 нм. Температура: 22°С.
Фиг.8. Хроматограмма разделения DL-Cit на колонке с иммобилизованным гибридным селектором. Элюент: 20% СН3ОН - 80% 0,1 М NaH2PO4; 0,7 мл/мин. Детектирование: УФ 210 нм. Температура: 22°С.
Фиг.9. Хроматограмма разделения DL-Ala на колонке с иммобилизованным гибридным селектором. Элюент: 20% СН3ОН - 80% 0,1 М NaH2PO4; 0,7 мл/мин. Детектирование: УФ 210 нм. Температура: 22°С.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОРБЕНТ ДЛЯ РАЗДЕЛЕНИЯ ОПТИЧЕСКИХ ИЗОМЕРОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2004 |
|
RU2255802C1 |
| СОРБЕНТ ДЛЯ РАЗДЕЛЕНИЯ ОПТИЧЕСКИХ ИЗОМЕРОВ ВЕЩЕСТВ И ИХ АНАЛИЗА В БИОЛОГИЧЕСКИХ ЖИДКОСТЯХ МЕТОДОМ ВЭЖХ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2014 |
|
RU2592893C2 |
| СПОСОБ ПОЛУЧЕНИЯ ХИРАЛЬНОЙ ПЛАНАРНОЙ ПЛАСТИНЫ ДЛЯ ТОНКОСЛОЙНОЙ ХРОМАТОГРАФИИ ОПТИЧЕСКИХ ИЗОМЕРОВ | 2012 |
|
RU2545315C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭНАНТИОСЕЛЕКТИВНОГО СОРБЕНТА | 2008 |
|
RU2363538C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТОНКОСЛОЙНЫХ ХИРАЛЬНЫХ ПЛАСТИН ДЛЯ ПЛАНАРНОЙ ХРОМАТОГРАФИИ СТЕРЕОИЗОМЕРОВ И ИХ РАЦЕМИЧЕСКИХ СМЕСЕЙ | 2013 |
|
RU2541524C2 |
| Способ селективного разделения рацемической смеси сальбутамола | 2017 |
|
RU2667002C1 |
| СПОСОБ ПРЕПАРАТИВНОГО РАЗДЕЛЕНИЯ РАЦЕМИЧЕСКОГО САЛЬБУТАМОЛА ОСНОВАНИЯ С ПРИМЕНЕНИЕМ СВЕРХКРИТИЧЕСКОЙ ФЛЮИДНОЙ ХРОМАТОГРАФИИ | 2019 |
|
RU2727890C1 |
| СПОСОБ РАЗДЕЛЕНИЯ ХИРАЛЬНЫХ СУЛЬФОКСИДОВ С ПОМОЩЬЮ ЭНАНТИОСЕЛЕКТИВНОЙ ХРОМАТОГРАФИИ | 2006 |
|
RU2310505C1 |
| СПОСОБ АНАЛИЗА ОПТИЧЕСКИХ И СТРУКТУРНЫХ ИЗОМЕРОВ | 2009 |
|
RU2413936C2 |
| СОРБЕНТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2001 |
|
RU2203730C1 |







Изобретение относится к сорбентам для хроматографии. Предложен сорбент на основе силикагеля с привитым через спейсер гибридным хиральным селектором, полученный путем модифицирования силикагеля эпоксигруппами, прививки эремомицина и хирального полианилина. Сорбент проявляет повышенную энантиоселективность к различным соединениям. 2 н. и 1 з.п. ф-лы, 2 табл., 9 ил.
| СОРБЕНТ ДЛЯ РАЗДЕЛЕНИЯ ОПТИЧЕСКИХ ИЗОМЕРОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2004 |
|
RU2255802C1 |
| US 6669842 А, 30.12.2003 | |||
| СОРБЕНТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2001 |
|
RU2203730C1 |
| Способ контроля электростатической безопасности объекта | 1987 |
|
SU1429061A1 |
| ХИРАЛЬНЫЕ ОПТИЧЕСКИЕ АКТИВНЫЕ АДСОРБЕНТЫ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, СЕТЧАТЫЙ ПОЛИМЕР, ПРОИЗВОДНЫЕ ВИННОЙ КИСЛОТЫ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 1993 |
|
RU2121395C1 |
| D | |||
| Armstrong et al | |||
| "Macrocyclic antibiotics as a new class of chiral selectors for liquid - chromatography" Analytical Chemistry, vol.66, No.9, May 1994, pp.1473-1484. | |||
Авторы
Даты
2009-03-10—Публикация
2006-10-10—Подача