Изобретение относится к сорбентам для высокоэффективной жидкостной хроматографии и может быть использовано для анализа, препаративной очистки оптически активных соединений, а также определения низкомолекулярных гидрофобных оптически активных примесей (например, лекарств) в биологических жидкостях.
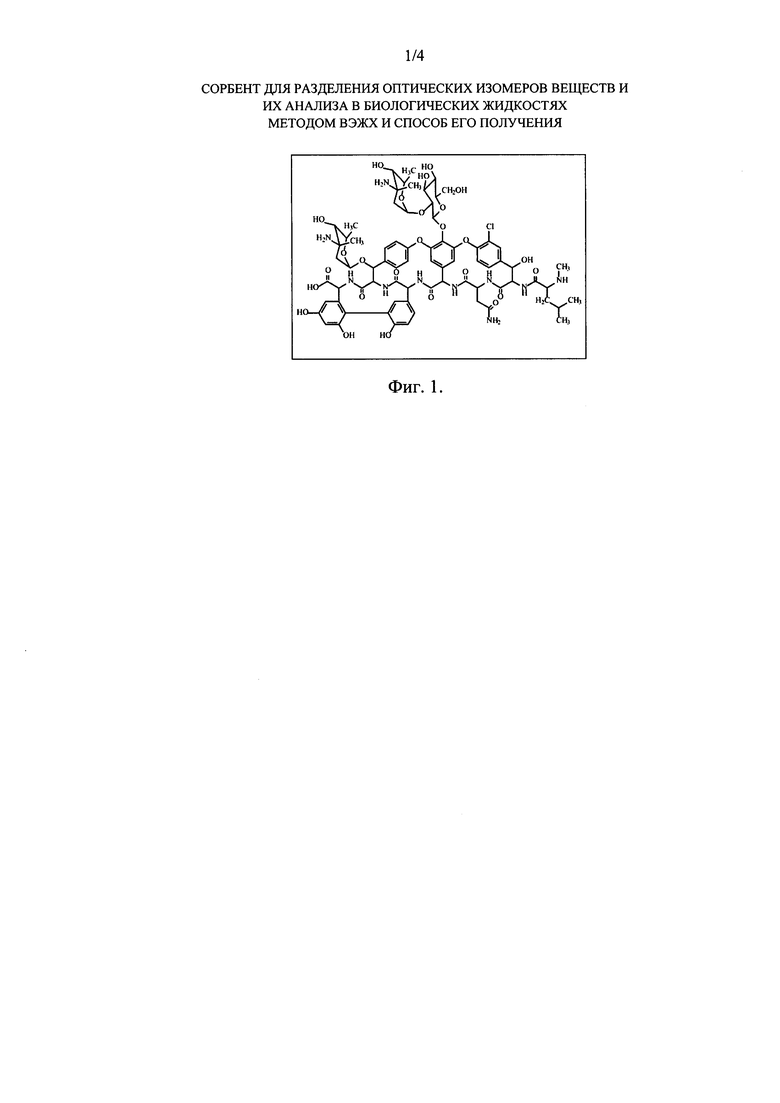
Наиболее близким по технической сущности и достигаемому результату является сорбент на основе силикагеля с химически привитым гликопептидным антибиотиком эремомицином, структурная формула которого приведена на фиг. 1, а также способ его получения, описанный в RU 2255802, 2005, выбранный в качестве прототипа изобретения.
Сорбент проявляет селективность в разделении широкого круга энантиомеров как в водно-органических, так и в неводных элюентах. Однако не всегда энантиоселективность является достаточно высокой.
Способ получения известного сорбента заключается в обработке силикагеля 3-глицидооксипропилтриалкоксисиланом с последующим взаимодействием с эремомицином в водном или водно-органическом щелочном буферном растворе при температуре не выше 40°C.
Одним из недостатков известного способа получения сорбента является наличие в составе распознающих хиральных центров только производных эремомицина. Еще один недостаток сорбента, полученного известным способом, заключается в невозможности определения низкомолекулярных гидрофобных оптически активных примесей (например, лекарств) напрямую в биологических жидкостях.
Еще одним прототипом изобретения, близким по технической сущности и достигаемому результату, является гибридный сорбент на основе силикагеля с химически привитыми гликопептидным антибиотиком эремомицином и хиральным полианилином, способ его получения описан в RU 2348455, 2006.
Энантиоселективность такого сорбента повышена за счет введения в состав хирального сорбента селектора эремомицина и селектора спиралевидной хиральности - хирального полианилина.
Способ получения такого гибридного сорбента заключается в модифицировании поверхности силикагеля эпоксигруппами, иммобилизацию эремомицина на поверхности силикагеля с привитыми эпоксигруппами, промывку, сушку, а затем силикагель, модифицированный эремомицином, подвергают взаимодействию с анилином в присутствии фермента лакказы и энантиомера сульфокамфорной кислоты. Предпочтительно для модифицирования поверхности силикагеля эпоксигруппами используют обработку 3-глицидоксипропилтриэтоксисиланом.
Наилучшие результаты показал сорбент известного способа с эремомицином, полученным с использованием штамма-продуцента Amicolatopsis orientalis subsp, согласно известному способу по RU 2110578, 1998.
Недостатком известного способа получения сорбента является отсутствие в его структуре каркаса из хиральных молекул (например, молекул альбумина) на поверхности силикагеля большего размера, чем размер пор самого силикагеля, что не позволяет определять низкомолекулярные гидрофобные оптически активные примеси (например, лекарств) напрямую в биологических жидкостях.
Задачей настоящего изобретения является повышение селективности сорбента в разделении оптических изомеров и разработка способа, позволяющего обеспечить введение на поверхность хирального сорбента каркаса из молекул большого размера, закрывающего доступ внутрь пор силикагеля белкам, находящимся в растворе.
Поставленная задача решается описываемым сорбентом для хроматографии оптических изомеров, содержащим силикагель, модифицированный гликопептидным антибиотиком - эремомицином и дополнительно бычьим сывороточным альбумином (БСА).
Поставленная задача решается также описываемым способом получения сорбента для хроматографии оптических изомеров, включающим модифицирование поверхности силикагеля эпоксигруппами, иммобилизацию эремомицина на поверхности силикагеля с привитыми эпоксигруппами, промывку, сушку, в котором силикагель, модифицированный эремомицином, после промывки и сушки подвергают взаимодействию с бычьим сывороточным альбумином, последующей обработкой глутаровым альдегидом и восстановление тетрагидроборатом натрия. Обработка глутаровым альдегидом осуществляется для сшивания между собой молекул бычьего сывороточного альбумина и образования каркаса на поверхности силикагеля. Обработка тетрагидроборатом натрия необходима для восстановления всех непрореагировавших групп на поверхности сорбента и устранения их влияния на разделение оптических изомеров. Предпочтительно для модифицирования поверхности силикагеля эпоксигруппами используют обработку 3-глицидоксипропилтриэтрксисиланом.
Сущность изобретения поясняется иллюстративными материалами.
На Фиг. 1 показана структурная формула эремомицина.
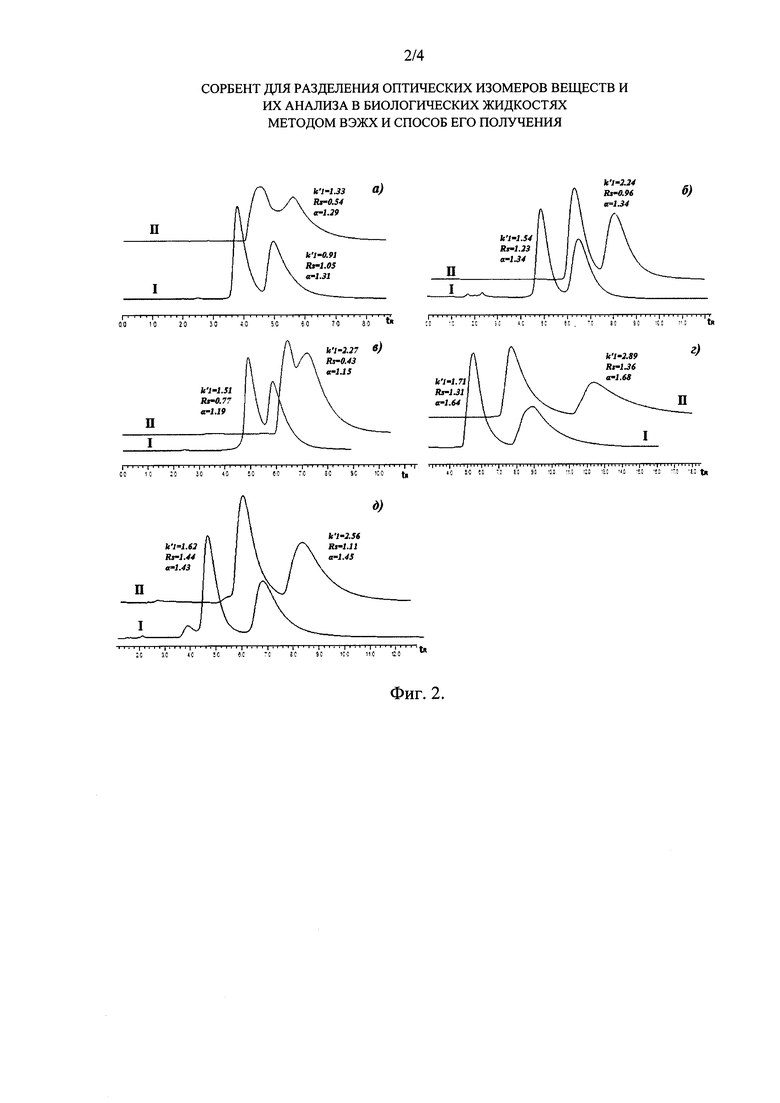
На Фиг. 2 показаны хроматограммы профенов, полученные на колонке с иммобилизованным гибридным сорбентом I (силикагель-эремомицин-БСА) и на колонке с сорбентом, полученным известным способом (RU 2255802, 2005) II. Хроматограмы следующих веществ:
а) ибупрофен
б) кетопрофен
в) фенопрофен
г) флурбипрофен
д) индопрофен.
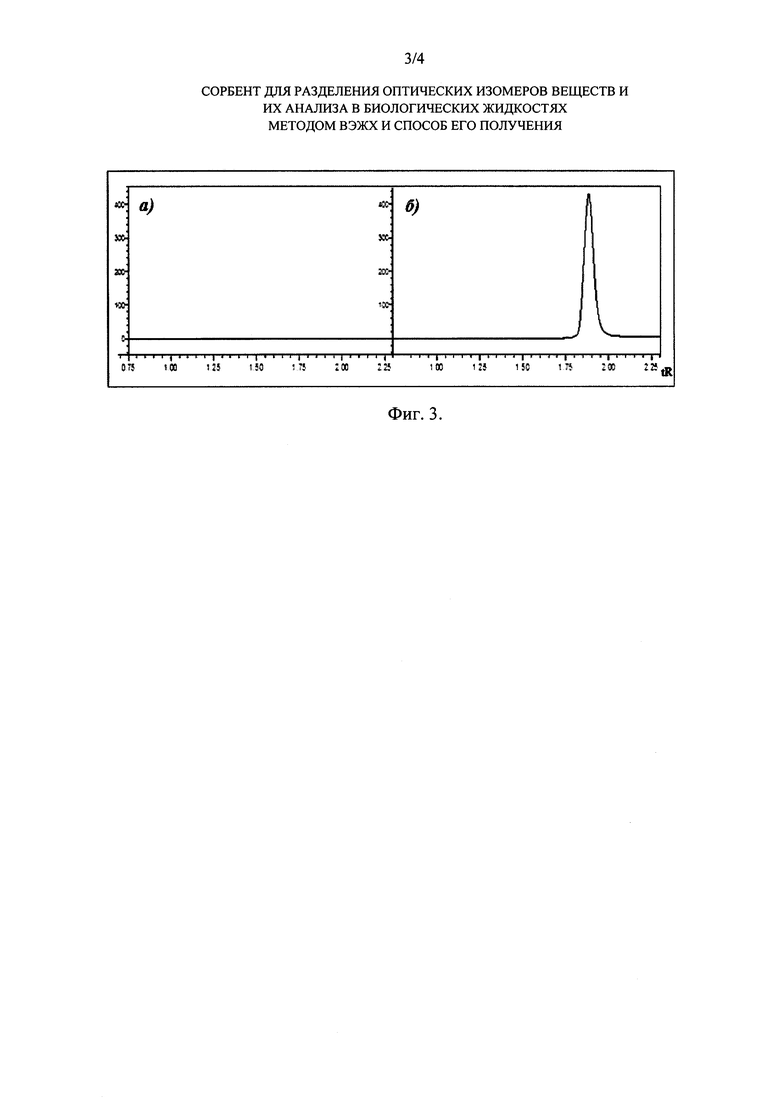
На Фиг. 3 показаны хроматограммы белка, полученные на сорбенте-прототипе (RU 2255802, 2005) (а) и на сорбенте с гибридным селектором (б). Элюент: МеОН/KH2PO4 (0.1М, pH 4.5), 50/50, об/об; 0.5 мл/мин. Детектирование: УФ 280 нм. Температура 24°C.
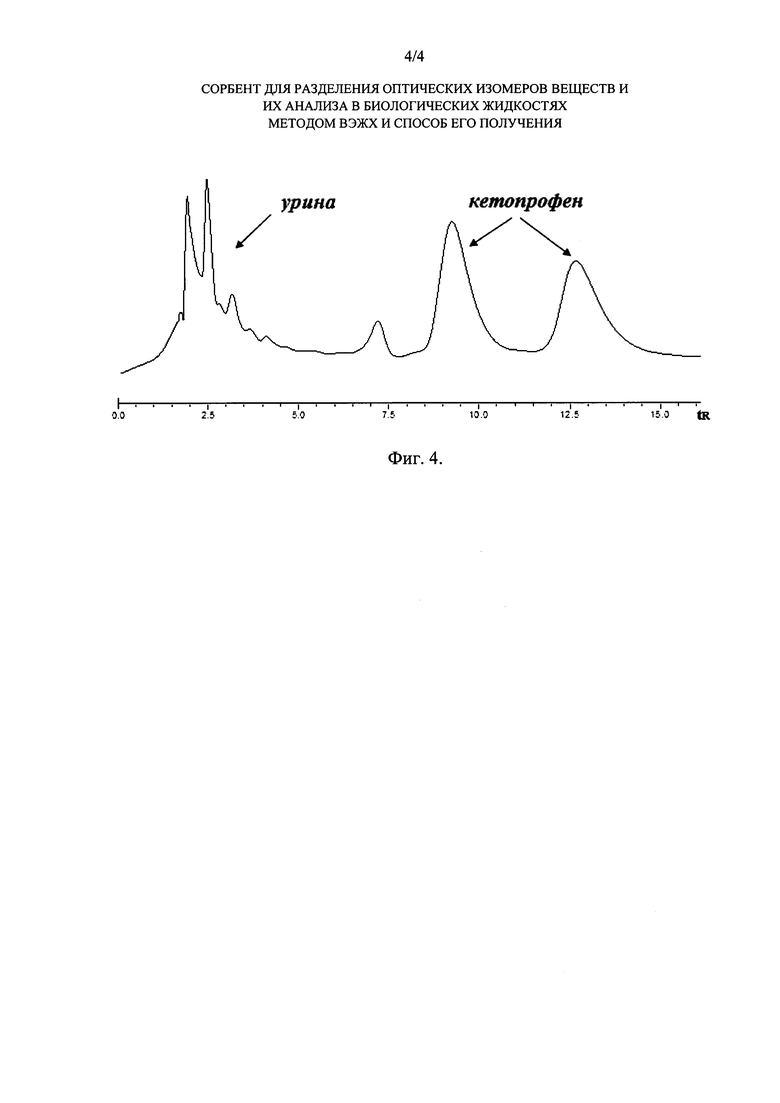
На Фиг. 4 показана хроматограмма кетопрофена на колонке с иммобилизованным гибридным селектором в образце мочи. Элюент: МеОН/KH2PO4 (0.1М, pH 4.5), 50/50, об/об; 0.5 мл/мин. Детектирование: УФ 280 нм. Температура 24°C.
Изобретение иллюстрируется примерами вариантов его выполнения и применения.
Пример 1
5,04 г силикагеля Kromasil KR100-7-SIL суспендировали в 25 мл 0,1 М раствора ацетата натрия, доведенного ледяной уксусной кислотой до pH 5,5. К полученной суспензии добавили 4 мл 3-глицидоксипропилтриэтоксисилана. Реакционную смесь интенсивно перемешивали в течение 2 часов, а затем оставили без нагревания и перемешивания на 4 суток. По окончании реакции модифицированный силикагель промыли водой, этанолом, ацетоном и отфильтровали. Сушили при температуре 105°C. По данным элементного анализа содержание углерода составляет 5,2%.
Получен силикагель, модифицированный эпоксигруппами. Затем 1,5 г макроциклического антибиотика - эремомицина растворили в 23 мл дистиллированной воды. Довели pH до значения 8,58, прибавляя по каплям 1 М водный раствор КОН. Полученный раствор смешали с 5,61 г силикагеля с привитыми эпоксигруппами. Полученную реакционную смесь выдерживали при комнатной температуре, периодически перемешивая, в течение 1 недели. После окончания реакции сорбент отфильтровали и отмыли последовательно водой, метанолом и ацетоном. Сушили в сушильном шкафу при 50°C в течение 20 часов. По данным элементного анализа содержание углерода составляет 9,5%.
Получен силикагель, модифицированный эремомицином. Затем раствор 0,2 г БСА в 25 мл ацетата натрия (доведенного до pH 5,6 уксусной кислотой) добавили к 2 г силикагеля, модифицированного эремомицином. Полученную реакционную смесь выдерживали при комнатной температуре, подвергая ультразвуковой обработке каждые четыре часа, в течение двух дней. После окончания реакции сорбент отфильтровали и отмыли водой. Затем его суспендировали в раствор глутарового альдегида (1,5 мл 25% глутарового альдегида в 25 мл ацетатного буферного раствора с pH 5,6). Полученную реакционную смесь выдерживали при комнатной температуре, периодически перемешивая, в течение одного дня. После окончания реакции сорбент отфильтровали и отмыли водой, добавили к нему раствор 0,16 г NaBH4 в 25 мл дистиллированной воды. Полученную реакционную смесь выдерживали при комнатной температуре, периодически перемешивая, в течение одного дня. После окончания реакции сорбент отфильтровали и отмыли водой, этанолом. Сушили на воздухе в течение 24 часов. По данным элементного анализа содержание углерода составляет 13,8%.
Таким образом, получен силикагель с привитым через спейсер гибридным хиральным селектором:
Силикагель -Si(СН2)3О-СН2-СН(ОН)-СН2-эремомицин-бычий сывороточный альбумин.
Полученный в соответствии с настоящим изобретением сорбент был испытан при разделении оптических изомеров, в том числе в образцах мочи, в следующих условиях.
Сорбент по примеру 1 упаковали суспензионным методом в колонку из нержавеющей стали 4,6×100 мм и проводили разделение оптических изомеров профенов с использованием метода высокоэффективной жидкостной хроматографии.
Хроматографический анализ осуществляли на ВЭЖХ хроматографе фирмы Shimadzu (Япония) в составе: насос LC-20AB, диодно-матричный детектор SPD-M20A, вакуумный дегазатор DGU-20A5, термостат колонок СТО-20А, с возможностью контроля температуры в диапазоне 5-85°C с точностью 0,1°C, ручной кран-дозатор с петлей на 20 мкл. Объем пробы 20 мкл. Хроматографические пики детектировали в диапазоне 210-280 нм, в соответствии с максимумами поглощения разделяемых соединений.
Запись хроматограмм и расчеты факторов удерживания разделенных компонентов к, селективности A и разрешения RS проводили с помощью программно-аппаратного комплекса Laboratory Solution (Shimadzu, Япония).
В качестве подвижной фазы использовали метанольные и водно-метанольные буферные растворы.
Пример 2
В таблице 1 представлены результаты хроматографического разделения профенов (значения факторов удерживания (k) и энантиоселективности (α) на колонке с сорбентом, полученным по примеру 1 с привитым гибридным селектором.
Разделение осуществляли в элюенте состава: 50% метанол - 50% водный раствор дигидрофосфата калия (pH 4.5) с молярной концентрацией 0,02 М, 0,04 М и 0,10 М. Скорость потока подвижной фазы: 0.5 мл/мин.
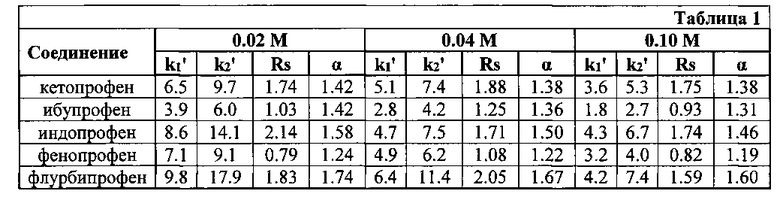
Из таблицы видно, что сорбент проявляет высокую энантиоселективность к данному классу соединений (α-оксикислоты).
Пример 3
В таблице 2 представлены результаты хроматографического разделения энантиомеров профенов на колонке с сорбентом, полученным по примеру 1 с привитым гибридным селектором в сравнении с сорбентом, полученным известным способом (RU 2255802, 2005). Разделение осуществляли в элюенте одинакового состава: 50% СН3ОН - 50% 0,1 М фосфатный буфер (pH 6,5) на колонках 4,6×100 мм. Скорость потока подвижной фазы: 0.5 мл/мин.
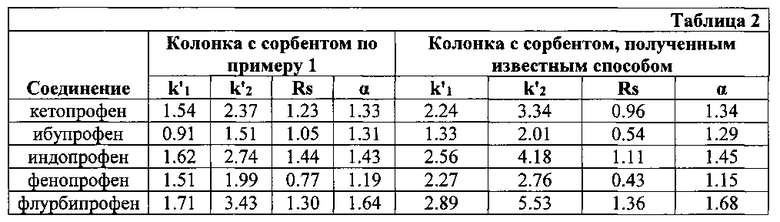
Из полученных результатов видно, что заявленный сорбент в большинстве случаев обеспечивает меньшее удерживание 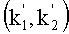
Пример 4
Высокомолекулярные соединения, в частности белки, не удерживаются на сорбенте, полученном по примеру 1, и элюируются с мертвым объемом. С сорбента-прототипа (RU 2255802, 2005) белки не элюируются, оседают на сорбенте, изменяя ее свойства. На Фиг. 3 представлены хроматограммы раствора белка (бычьего сывороточного альбумина), полученные на гибридном сорбенте и на сорбенте-прототипе (RU 2255802, 2005).
Как следует из результатов исследования, на сорбенте, полученном по примеру 1, в отличие от сорбентов-прототипов (RU 2255802, 2005 и RU 2348455, 2006) возможно разделение и определение энантиомеров низкомолекулярных соединений (лекарств, например, профенов) в биологических жидкостях при их прямом вводе на колонку с сорбентом. На Фиг. 4 представлена хроматограмма энантиоразделения кетопрофена в образце мочи при его прямом вводе в колонку с гибридным сорбентом.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОРБЕНТ ДЛЯ ХРОМАТОГРАФИИ ОПТИЧЕСКИХ ИЗОМЕРОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2006 |
|
RU2348455C2 |
| СОРБЕНТ ДЛЯ РАЗДЕЛЕНИЯ ОПТИЧЕСКИХ ИЗОМЕРОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2004 |
|
RU2255802C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХИРАЛЬНОЙ ПЛАНАРНОЙ ПЛАСТИНЫ ДЛЯ ТОНКОСЛОЙНОЙ ХРОМАТОГРАФИИ ОПТИЧЕСКИХ ИЗОМЕРОВ | 2012 |
|
RU2545315C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭНАНТИОСЕЛЕКТИВНОГО СОРБЕНТА | 2008 |
|
RU2363538C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТОНКОСЛОЙНЫХ ХИРАЛЬНЫХ ПЛАСТИН ДЛЯ ПЛАНАРНОЙ ХРОМАТОГРАФИИ СТЕРЕОИЗОМЕРОВ И ИХ РАЦЕМИЧЕСКИХ СМЕСЕЙ | 2013 |
|
RU2541524C2 |
| Способ селективного разделения рацемической смеси сальбутамола | 2017 |
|
RU2667002C1 |
| СПОСОБ АНАЛИЗА ОПТИЧЕСКИХ И СТРУКТУРНЫХ ИЗОМЕРОВ | 2009 |
|
RU2413936C2 |
| НАНОГИБРИДНЫЙ ФУНКЦИОНАЛЬНЫЙ СЕПАРАЦИОННЫЙ МАТЕРИАЛ НА ОСНОВЕ МОДИФИЦИРОВАННОГО НОСИТЕЛЯ И МОДИФИЦИРОВАННЫХ НАНОЧАСТИЦ МЕТАЛЛА | 2012 |
|
RU2555030C2 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОГИБРИДНОГО ФУНКЦИОНАЛЬНОГО СЕПАРАЦИОННОГО МАТЕРИАЛА НА ОСНОВЕ МОДИФИЦИРОВАННОГО НОСИТЕЛЯ И МОДИФИЦИРОВАННЫХ НАНОЧАСТИЦ МЕТАЛЛА | 2012 |
|
RU2543170C2 |
| СПОСОБ ПОЛУЧЕНИЯ ХИРАЛЬНЫХ СОРБЕНТОВ | 2007 |
|
RU2339445C1 |
Изобретение относится к сорбентам для высокоэффективной жидкостной хроматографии (ВЭЖХ), в частности к получению химически модифицированных сорбентов. Предложен сорбент на основе силикагеля с привитым через спейсер гибридным хиральным селектором. Сорбент получен путем модифицирования силикагеля эпоксигруппами, прививки эремомицина и бычьего сывороточного альбумина. Сорбент проявляет повышенную энантиоселективность к различным соединениям, в том числе при их анализе в биологических жидкостях. 2 н.п. ф-лы, 4 ил., 2 табл.
1. Сорбент для разделения оптических изомеров веществ и для их анализа в биологических жидкостях методом ВЭЖХ, содержащий силикагель, модифицированный гликопептидным антибиотиком эремомицином, отличающийся тем, что он дополнительно модифицирован бычьим сывороточным альбумином.
2. Способ получения сорбента для хроматографии оптических изомеров, включающий модифицирование поверхности силикагеля эпоксигруппами, иммобилизацию эремомицина на поверхности силикагеля с привитыми эпоксигруппами, промывку, сушку, отличающийся тем, что силикагель, модифицированный эремомицином, после сушки подвергают взаимодействию с бычьим сывороточным альбумином, глутаровым альдегидом и тетрагидроборатом натрия.
| СОРБЕНТ ДЛЯ РАЗДЕЛЕНИЯ ОПТИЧЕСКИХ ИЗОМЕРОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2004 |
|
RU2255802C1 |
| СОРБЕНТ ДЛЯ ХРОМАТОГРАФИИ ОПТИЧЕСКИХ ИЗОМЕРОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2006 |
|
RU2348455C2 |
| US 7008533 B2 07.03.2006 | |||
| US 20130105396 A1 02.05.2013 | |||
| КУЗНЕЦОВ М.А | |||
| Энантиоселективные сорбенты с иммобилизированными макроциклическими гликопептидными антибиотиками, Автореф | |||
| дисс | |||
| на соиск | |||
| уч | |||
| степ | |||
| кан | |||
| хим | |||
| наук, Москва, 2008. | |||
Авторы
Даты
2016-07-27—Публикация
2014-12-26—Подача