Область изобретения
Настоящее изобретение связано с N-пиридин-3-ил или N-пиразин-2-ил карбоксамидными соединениями, которые являются агентами, повышающими уровень холестерина ЛПВП, их изготовлением, фармацевтическими композициями, содержащими их, и их применением в качестве терапевтически активных веществ.
В частности, изобретение относится к соединениям формулы I

где A, R1-R7 являются такими, как описано ниже, и их изомерным формам и их фармацевтически приемлемым солям.
Соединения по изобретению представляют собой агенты, повышающие уровень холестерина ЛПВП, и, следовательно, могут быть использованы в терапевтическом и/или профилактическом лечении заболеваний и расстройств, таких как дислипидемия, атеросклероз и сердечно-сосудистые заболевания.
Атеросклероз и сопровождающая его ишемическая болезнь сердца являются основной причиной смерти в индустриализованном мире. Установлено, что риск развития ишемической болезни сердца строго коррелирует с уровнями некоторых липидов в плазме. Липиды транспортируются в кровь липопротеинами. Общая структура липопротеинов представляет собой ядро нейтральных липидов (триглицерид и эфир холестерина) и оболочку из полярных липидов (фосфолипиды и неэтерифицированный холестерин). Существует 3 разных класса липопротеинов плазмы с разным содержанием липидов в ядре: липопротеин низкой плотности (ЛПНП), который богат холестериновыми эфирами (ХЭ); липопротеин высокой плотности (ЛПВП), который также богат холестериновыми эфирами (ХЭ); и липопротеин очень низкой плотности (ЛПОНП), который богат триглицеридами (ТГ). Разные липопротеины могут быть разделены исходя из их разной скорости флотации, плотности или размера.
Высокие уровни холестерина ЛПНП (ЛПНП-Х) и триглицеридов находятся в прямой связи, тогда как высокие уровни холестерина ЛПВП (ЛПВП-Х) находятся в обратной связи с риском развития сердечно-сосудистых заболеваний.
Не существует совершенно удовлетворительных приводящих к повышению ЛПВП методов лечения. Ниацин может значительно увеличивать ЛПВП, но имеет серьезные ограничения в плане переносимости, которые ослабляют соблюдение режима лечения. Фибраты и ингибиторы ГМГ-КоА-редуктазы (гидроксиметилглутарил-кофермент А-редуктазы от HMG CoA reductase) повышают уровень холестерина ЛПВП весьма умеренно (-10-12%). В результате существует значительная неудовлетворенная медицинская потребность в хорошо переносимом агенте, который может значительно повышать уровни ЛПВП в плазме.
Таким образом, агенты, повышающие уровень холестерина ЛПВП, могут применяться в качестве лекарственных средств для лечения и/или профилактики атеросклероза, заболевания периферических сосудов, дислипидемии, гипербеталипопротеинемии, гипоальфалипопротеинемии, гиперхолестеринемии, гипертриглицеридемии, семейной гиперхолестеринемии, сердечно-сосудистых заболеваний, стенокардии, ишемии, сердечной ишемии, инсульта, инфаркта миокарда, реперфузионного повреждения, ангиопластического рестеноза, гипертензии и сосудистых осложнений диабета, ожирения или эндотоксикоза.
Кроме того, агенты, повышающие уровень холестерина ЛПВП, могут быть использованы в сочетании с другим соединением, указанное соединение является ингибитором ГМГ-КоА-редуктазы, ингибитором секреции микросомального белка переноса триглицеридов (МТР) / ApoB (Аполипопротеина В), активатором PPAR (рецептора, активируемого пролифераторами пероксисом), ингибитором обратного захвата желчных кислот, ингибитором белка переноса холестериновых эфиров (СЕТР от cholesteryl ester transfer protein), ингибитором абсорбции холестерина, ингибитором синтеза холестерина, фибратом, ниацином, препаратами, содержащими ниацин или другие агонисты НМ74а, ионообменной смолой, антиоксидантом, ингибитором АСАТ (ацил-КоА-холестерин-ацилтрансферазы) или секвестрантом желчных кислот.
Таким образом, предметом настоящего изобретения является создание соединений, которые представляют собой эффективные агенты, повышающие уровень холестерина ЛПВП. Было найдено, что соединения формулы I по настоящему изобретению очень полезны для лечения и/или профилактики заболеваний и расстройств, которые можно лечить агентами, повышающими уровень холестерина ЛПВП, т.е. соединения формулы I особенно полезны для лечения и/или предотвращения дислипидемии, атеросклероза и сердечно-сосудистых заболеваний. Также предметом настоящего изобретения является создание соединений, которые при терапевтически активных концентрациях, что увеличивают ЛПВП-концентрации, не взаимодействуют с рецептором СВ1. Причина состоит в том, что лиганды рецептора СВ1 могут ухудшать терапевтическую ценность агентов, повышающих уровень холестерина ЛПВП, поскольку как агонисты, так и антагонисты рецептора СВ1 способны приводить к побочным эффектам.
Подробное описание изобретения
Если не указано иное, то следующие определения приведены для иллюстрации и определения значений и объема разных терминов, используемых здесь для описания изобретения.
В данном описании термин «низший» используется для обозначения группы, состоящей от одного до семи, особенно от одного до четырех атомов углерода.
Термин «алкил», отдельно или в сочетании с другими группами, относится к разветвленному или неразветвленному одновалентному насыщенному алифатическому углеводородному радикалу от одного до двадцати атомов углерода, особенно от одного до шестнадцати атомов углерода, более конкретно от одного до десяти атомов углерода.
Термин «низший алкил» или «C1-7-алкил», отдельно или в сочетании, означает алкильную группу с прямой цепью или разветвленной цепью от 1 до 7 атомов углерода, в частности алкильную группу с прямой или разветвленной цепью от 1 до 6 атомов углерода и более конкретно алкильную группу с прямой или разветвленной цепью от 1 до 4 атомов углерода. Примерами C1-7 алкильных групп с прямой и разветвленной цепью являются метил, этил, пропил, изопропил, бутил, изобутил, трет-бутил, изомерные пентилы, изомерные гексилы и изомерные гептилы, в частности этил, пропил, изопропил и трет-бутил.
Термин «низший алкокси» или «C1-7-алкокси» относится к группе R'-O-, где R' представляет собой низший алкил, и термин «низший алкил» имеет ранее приведенное значение. Примерами низших алкокси групп являются метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси и трет-бутокси, в частности метокси.
Термин «низший алкоксиалкил» или «С1-7-алкокси-С1-7-алкил» относится к низшей алкильной группе, как определено выше, которая является моно- или полизамещенной низшей алкокси группой, как определено выше. Примерами низших алкоксиалкильных групп являются, например, -СН2-О-СН3, -СН2-СН2-О-СН3, -СН2-O-СН2-СН3 и группы, особо приведенные здесь в качестве примера. Более конкретно низшим алкоксиалкилом является метоксиэтил.
Термин «низший гидроксиалкил» или «гидрокси-С1-7-алкил» относится к низшим алкильным группам, как определено выше, где по меньшей мере один из атомов водорода низшей алкильной группы замещен гидрокси-группой. Особый интерес представляют С3-7-гидроксиалкильные группы. Примерами низших гидроксиалкильных групп являются 2-гидроксибутил, 3-гидрокси-2,2-диметилпропил и группы, особо приведенные здесь в качестве примера.
Термин «низший гидроксиимино-алкил» или «гидроксиимино-С1-7-алкил» относится к низшим алкильным группам, как определено выше, где по меньшей мере один из атомов водорода низшей алкильной группы замещен гидроксиимино группой (=N-ОН). Особый интерес представляет 1-гидроксииминоэтильная группа -С(=N-ОН)-СН3.
Термин «низший алкоксиимино-алкил» или «С1-7-алкоксиимино-С1-7-алкил» относится к низшей алкильной группе, как определено выше, где по меньшей мере один из атомов водорода низшей алкильной группы замещен низшей алкоксиимино группой (=N-OR, R=низший алкил). Примерами низших алкоксиимино-алкильных групп являются 1-метоксииминоэтил или 1-этоксииминоэтил. Более конкретно низшим алкоксиимино-алкилом является 1-метоксииминоэтил (-С(=N-ОСН3)-СН3).
Термин «циклоалкил» или «С3-7-циклоалкил» обозначает насыщенную карбоциклическую группу, содержащую от 3 до 7 атомов углерода, такую как циклопропил, циклобутил, циклопентил, цикпогексил или циклогептил, особенно циклопропил.
Термин «низший циклоалкилалкил» или «С3-7-циклоалкил-С1-7-алкил» относится к низшим алкильным группам, как определено выше, где по меньшей мере один из атомов водорода низшей алкильной группы замещен циклоалкильной группой. Среди низших циклоалкилалкильных групп особый интерес представляет циклопропилметил.
Термин «галоген» относится к фтору, хлору, брому и йоду, особый интерес представляют фтор, хлор и бром. Более конкретно галоген относится к фтору и хлору.
Термин «низший галогеналкил» или «галоген-С1-7-алкил» относится к низшим алкильным группам, которые моно- или полизамещены галогеном, предпочтительно фтором или хлором, наиболее предпочтительно фтором. Примерами низших галогеналкильных групп являются, например, -CF3, -CHF2, -CH2Cl, -CH2CF3, -СН(CF3)2, -CF2-CF3, -СН2-CH2-CF3, -СН(СН3)-CF3 и группы, особо приведенные здесь в качестве примера. Особо интересными группами являются трифторметил (-CF3), 2,2,2-трифторэтил (-CH2CF3) и 1,1,1-трифтор-пропан-2-ил (-СН(СН3)-CF3).
Термин «низший галогеналкокси» или «галоген-С1-7-алкокси» относится к низшим алкокси группам, которые моно- или полизамещены галогеном, предпочтительно фтором или хлором, наиболее предпочтительно фтором. Примерами низших галогеналкильных групп являются, например, -OCF3, -OCHF2, -OCH2Cl, -OCH2CF3, -ОСН(CF3)2, -OCF2-CF3 и -ОСН(СН3)-CF3.
Термин «циано» обозначает группу -CN.
Термин «амино» относится к группе -NH2.
Термин «азидо» обозначает группу -N=N+=N-.
Термин «карбамоил» или «аминокарбонил» относится к группе -CO-NH2.
Термин «низший карбамоилалкил» или «карбамоил-С1-7-алкил» относится к низшим алкильным группам, как определено выше, где один из атомов водорода низшей алкильной группы замещен карбамоильной группой. Примерами низших карбамоилалкильных групп являются 3-карбамоилпропил, 4-карбамоилбутил и 5-карбамоилпентил, более конкретно 4-карбамоилбутил.
Термин «низший алкилкарбонил» относится к группе -CO-R”, где R” представляет собой низший алкил, как определено здесь ранее. «Низший алкилкарбониламино» относится к группе -NH-CO-R”, где R” представляет собой низший алкил, как определено здесь ранее.
Термин «низший алкилкарбониламиноалкил» или «C1-7-алкилкарбониламино-С1-7-алкил» относится к низшим алкильным группам, как определено выше, где один из атомов водорода низшей алкильной группы замещен низшей алкилкарбониламино группой. Примером низшей алкилкарбониламиноалкильной группы является этилкарбониламиноэтил.
Термин «низший алкиламинокарбонил» или «C1-7-алкиламинокарбонил» относится к группе -CO-NH-R, где R представляет собой низшую алкильную группу, как определено выше. Примером низшей алкиламинокарбонильной группы является метиламинокарбонил.
Термин «низший фенилалкил» или «фенил-С1-7-алкил» относится к низшим алкильным группам, как определено выше, где по меньшей мере один из атомов водорода низшей алкильной группы замещен фенильной группой. В частности, низший фенилалкил означает бензил.
Термин «гетероциклил» относится к насыщенному или частично ненасыщенному 3-, 4-, 5-, 6- или 7-членному кольцу, которое может включать один, два или три гетероатома, выбранных из N, О и S. Примеры гетероциклильных колец включают пиперидинил, пиперазинил, азетидинил, азепинил, пирролидинил, пиразолидинил, имидазолинил, имидазолидинил, оксазолидинил, изоксазолидинил, морфолинил, тиазолидинил, изотиазолидинил, оксиранил, тиадиазолилидинил, оксетанил, диоксоланил, дигидрофуранил, тетрагидрофуранил, дигидропиранил, тетрагидропиранил и тиоморфолинил. Особый интерес представляет тетрагидрофуранильная группа.
Термин «низший гетероциклилалкил» или «гетероциклил-С1-7-алкил» относится к низшим алкильным группам, как определено выше, где по меньшей мере один из атомов водорода низшей алкильной группы замещен гетероциклильной группой, как определено выше.
Термин «гетероарил» относится к ароматическому 5- или 6-членному кольцу, которое может включать один, два или три атома, выбранных из N, О и S. Примерами гетероарильных групп являются, например, фуранил, пиридил, пиразинил, пиримидинил, пиридазинил, тиенил, изоксазолил, тиазолил, изотиазолил, тиадиазолил, оксазолил, имидазолил, пиразолил, триазолил, оксадиазолил, оксатриазолил, тетразолил, пентазолил или пирролил. Термин «гетероарил» также включает бициклические группы, содержащие два 5- или 6-членных кольца, в которых одно или оба кольца являются ароматическими и могут содержать один, два или три атома, выбранных из азота, кислорода или серы, такие как хинолинил, изохинолинил, циннолинил, пиразоло[1,5-а]пиридил, имидазо[1,2-а]пиридил, хиноксалинил, бензотиазолил, бензотриазолил, индолил, индазолил и 3,4-дигидро-2Н-пиридо[3,2-b][1,4]оксазинил. Гетероарильная группа может быть моно- или дизамещена низшим алкилом, гидрокси, циано или галогеном. Представляющими особый интерес гетероарильными группами являются фуранил, оксазолил, изоксазолил, пиразолил, тиазолил, изотиазолил, [1,2,3]тиадиазолил, пиридил, пиразинил, пиридазинил, пиримидинил и 3,4-дигидро-2Н-пиридо[3,2-b][1,4]оксазинил.
Термин «низший гетероарилалкил» или «гетероарил-С1-7-алкил» относится к низшим алкильным группам, как определено выше, где по меньшей мере один из атомов водорода низшей алкильной группы замещен гетероарильной группой, как определено выше.
«Изомерными формами» являются все формы соединения, характеризуемые наличием одинаковой молекулярной формулы, но которые отличаются по природе или последовательности соединения их атомов или по расположению их атомов в пространстве. Предпочтительно изомерные формы отличаются по расположению их атомов в пространстве и также могут быть названы «стереоизомерами». Стереоизомеры, которые не являются зеркальными изображениями друг друга, называются «диастереоизомерами», и стереоизомеры, которые являются неналагающимися зеркальными изображениями, называются «энантиомерами», или иногда оптическими изомерами. Атом углерода, соединенный с четырьмя неодинаковыми заместителями, называется «хиральный центр».
Термин «фармацевтически приемлемые соли» относится к тем солям, которые сохраняют биологическую эффективность и свойства свободных оснований или свободных кислот и которые не обладают собственными свойствами, которые не желательны. Соли получают с неорганическими кислотами, такими как соляная кислота, бромисто-водородная кислота, серная кислота, азотная кислота, фосфорная кислота и подобные, предпочтительно соляной кислотой, и органическими кислотами, такими как муравьиная кислота, уксусная кислота, пропионовая кислота, гликолевая кислота, пировиноградная кислота, щавелевая кислота, малеиновая кислота, малоновая кислота, салициловая кислота, янтарная кислота, фумаровая кислота, винная кислота, лимонная кислота, бензойная кислота, коричная кислота, миндальная кислота, метансульфоновая кислота, этансульфоновая кислота, n-толуолсульфоновая кислота, салициловая кислота, N-ацетилцистеин и подобные. Таким образом, предпочтительные «фармацевтически приемлемые соли» включают ацетат, бромид, хлорид, формиат, фумарат, малеат, мезилат, нитрат, оксалат, фосфат, сульфат, тартрат и тозилат соединений формулы I. Кроме того, фармацевтически приемлемые соли могут быть получены при добавлении неорганического основания или органического основания свободной кислоты. Соли, полученные из неорганического основания, включают, но не ограничиваются этим, соли натрия, калия, лития, аммония, кальция, магния и подобные. Соли, полученные из органических оснований, включают, но не ограничиваются этим, соли первичных, вторичных и третичных аминов, замещенных аминов, включая встречающиеся в природе замещенные амины, циклических аминов и основные ионообменные смолы, такие как изопропиламин, триметиламин, диэтиламин, триэтиламин, трипропиламин, этаноламин, диэтиламин, лизин, аргинин, N-этилпиперидин, пиперидин, пиперазин и подобные. Соединение формулы I также может находиться в форме цвиттерионов или в форме гидратов. Особенно предпочтительными фармацевтически приемлемыми солями соединений формулы I являются гидрохлориды.
Настоящее изобретение относится к соединениям формулы
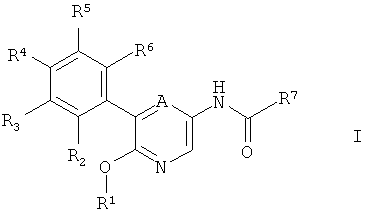
где
А выбран из СН или N;
R1 выбран из группы, состоящей из низшего алкила,
циклоалкила,
низшего циклоалкилалкила,
низшего гидроксиалкила,
низшего алкоксиалкила,
низшего галогеналкила,
низшего карбамоилалкила,
низшего алкилкарбониламиноалкила,
низшего фенилалкила,
низшего гетероциклилалкила, где гетероциклильная группа не замещена или замещена оксо,
низшего гетероарилалкила, где гетероарильная группа не замещена или моно- или ди-замещена низшим алкилом, и
фенила, который не замещен или моно- или ди-замещен галогеном;
R2 и R6 независимо друг от друга представляют собой водород или галоген;
R3 и R5 независимо друг от друга выбраны из группы, состоящей из водорода, низшего алкила, низшего алкокси, галогена, низшего галогеналкила, низшего галогеналкокси и циано;
R4 выбран из группы, состоящей из водорода, низшего алкила, низшего алкокси, галогена, низшего галогеналкила, низшего галогеналкокси, амино, азидо и циано;
R7 выбран из группы, состоящей из низшего алкила,
низшего гидроксиалкила, низшего алкоксиалкила,
низшего гидроксиимино-алкила, низшего алкоксиимино-алкила,
низшего циклоалкила, указанный циклоалкил не замещен или замещен гидрокси,
низшего гетероциклила,
фенила, указанный фенил не замещен или замещен одной или двумя группами, выбранными из группы, состоящей из низшего алкила, гидрокси, низшего алкокси, циано, низшего алкиламинокарбонила и галогена,
гетероарила, указанный гетероарил не замещен или замещен одной или двумя группами, выбранными из группы, состоящей из низшего алкила, гидрокси, низшего алкокси, циано, низшего алкиламинокарбонила и галогена;
и их фармацевтически приемлемым солям.
Соединения формулы I по настоящему изобретению представляют собой те, где R1 выбран из группы, состоящей из низшего алкила, циклоалкила, низшего циклоалкилалкила, низшего гидроксиалкила, низшего алкоксиалкила, низшего галогеналкила, низшего карбамоилалкила, низшего алкилкарбониламиноалкила, низшего фенилалкила, низшего гетероциклилалкила, где гетероциклильная группа не замещена или замещена оксо, или низшего гетероарилалкила, где гетероарильная группа не замещена или моно- или ди-замещена низшим алкилом.
В частности, изобретение относится к соединениям формулы I, где R1 выбран из циклоалкила, низшего циклоалкилалкила, низшего алкоксиалкила и низшего галогеналкила. Более конкретно R1 выбран из циклобутила, циклопропилметила, 2-метоксиэтила и низшего галогеналкила. Даже более конкретно R1 представляет собой циклопропилметил или низший галогеналкил. Наиболее конкретно R1 представляет собой 2,2,2-трифторэтил или 1,1,1-трифтор-пропан-2-ил, наибольший интерес представляет R1, являющийся 2,2,2-трифторэтилом.
Соединения формулы I по изобретению представляют собой те, где R2 и R6 независимо друг от друга представляют собой водород или галоген. Соединения формулы I, где R2 и R6 представляют собой водород, особенно интересны.
Кроме того, изобретение относится к соединениям формулы I, где R3 и R5 независимо друг от друга выбраны из группы, состоящей из водорода, низшего алкила, низшего алкокси, галогена, низшего галогеналкила, низшего галогеналкокси и циано. В частности, изобретение относится к соединениям формулы I, где R3 и R5 выбраны из водорода, галогена и низшего алкила, более конкретно водорода, фтора, хлора и метила.
Кроме того, изобретение связано с соединениями формулы I, где R4 выбран из группы, состоящей из водорода, низшего алкила, низшего алкокси, галогена, низшего галогеналкила, низшего галогеналкокси, амино, азидо и циано. Более конкретно R4 представляет собой низший алкил или галоген. Наиболее конкретно R4 представляет собой галоген, особенно хлор.
Соединения формулы I по изобретению, кроме того, являются теми, где R7 выбран из группы, состоящей из низшего алкила,
низшего гидроксиалкила, низшего алкоксиалкила,
низшего гидроксиимино-алкила, низшего алкоксиимино-алкила,
низшего циклоалкила, указанный циклоалкил не замещен или замещен гидрокси,
низшего гетероциклила,
фенила, указанный фенил не замещен или замещен одной или двумя группами, выбранными из группы, состоящей из низшего алкила, гидрокси, низшего алкокси, циано, низшего алкиламинокарбонила и галогена, и
гетероарила, указанный гетероарил не замещен или замещен одной или двумя группами, выбранными из группы, состоящей из низшего алкила, гидрокси, низшего алкокси, циано, низшего алкиламинокарбонила и галогена.
Одной группой соединений формулы I по изобретению являются те, где R7 представляет собой низший алкил, в частности метил, пропил или бутил.
Другой группой соединений формулы I по настоящему изобретению являются те, где R7 представляет собой фенил, указанный фенил не замещен или замещен одной или двумя группами, выбранными из группы, состоящей из низшего алкила, гидрокси, низшего алкокси, циано, низшего алкиламинокарбонила и галогена, или гетероарил, указанный гетероарил не замещен или замещен одной или двумя группами, выбранными из группы, состоящей из низшего алкила, гидрокси, низшего алкокси, циано, низшего алкиламинокарбонила и галогена.
Особый интерес представляют соединения формулы I по изобретению, где R7 представляет собой гетероарил, указанный гетероарил не замещен или замещен одной или двумя группами, выбранными из группы, состоящей из низшего алкила, гидрокси, низшего алкокси, циано, низшего алкиламинокарбонила и галогена. В частности, изобретение относится к соединениям формулы I, где R7 представляет собой гетероарил, указанный гетероарил не замещен или замещен одной или двумя группами, выбранными из группы, состоящей из низшего алкила, гидрокси, циано, низшего алкиламинокарбонила и галогена. Более конкретно изобретение относится к соединениям формулы I, где R7 представляет собой гетероарил, выбранный из группы, состоящей из фуранила, оксазолила, изоксазолила, пиразолила, тиазолила, изотиазолила, [1,2,3]тиадиазолила, пиридила, пиразинила, пиридазинила, пиримидинила и 3,4-дигидро-2Н-пиридо[3,2-b][1,4]оксазинила, указанный гетероарил не замещен или замещен одной или двумя группами, выбранными из группы, состоящей из низшего алкила, гидрокси, низшего алкокси, циано, низшего алкиламинокарбонила и галогена. Даже более конкретно R7 представляет собой гетероарил, выбранный из группы, состоящей из оксазолила, изоксазолила, пиразолила, пиридила, пиридазинила и пиримидинила, указанный гетероарил не замещен или замещен одной или двумя группами, выбранными из группы, состоящей из низшего алкила, гидрокси, низшего алкокси, циано, низшего алкиламинокарбонила и галогена. Особенно R7 представляет собой пиридил, указанный пиридил не замещен или замещен одной или двумя группами, выбранными из группы, состоящей из низшего алкила, гидрокси, низшего алкокси, циано, низшего алкиламинокарбонила и галогена.
В частности, изобретение относится к соединениям формулы I, где R7 выбран из группы, состоящей из фуран-2-ила, 5-метил-фуран-2-ила, фуран-3-ила, 5-метил-оксазол-4-ила, 2,4-диметил-оксазол-5-ила, изоксазол-5-ила, 3-метил-изоксазол-4-ила, 3,5-диметил-изоксазол-4-ила, 5-метил-изоксазол-3-ила, 1H-пиразол-3-ила, 1-метил-1H-пиразол-3-ила, 1,3-диметил-1Н-пиразол-4-ила, 2-метил-2Н-пиразол-3-ила, 5-метил-2H-пиразол-3-ила, 2,5-диметил-2H-пиразол-3-ила, тиазол-2-ила, 5-метил-тиазол-2-ила, изотиазол-5-ила, 4-метил-[1,2,3]тиадиазол-5-ила, пиридин-2-ила, 3-метилпиридин-2-ила, пиридин-3-ила, 2,4-дифтор-пиридин-3-ила, 2-метил-пиридин-3-ила, 5-метил-пиридин-3-ила, 6-метил-пиридин-3-ила, 5-циано-пиридин-3-ила, 5-бром-пиридин-3-ила, 5-йод-пиридин-3-ила, 5-метокси-пиридин-3-ила, пиридин-4-ила, 2-метил-пиридин-4-ила, 3-метил-пиридин-4-ила, 2-гидрокси-пиридин-4-ила, 5-гидрокси-пиридин-2-ила, пиразин-2-ила, пиридазин-3-ила, пиримидин-4-ила, пиримидин-5-ила и 4-метил-3,4-дигидро-2H-пиридо[3,2-b][1,4]оксазин-7-ила. Более конкретно R7 выбран из пиридин-3-ила, 3-метил-изоксазол-4-ила, пиридазин-3-ила, 1,3-диметил-1H-пиразол-4-ила и 5-метил-оксазол-4-ила. Наиболее конкретно R7 представляет собой пиридин-3-ил.
В частности, изобретение относится к соединениям формулы I, где А представляет собой СН. Соединения представляют собой производные пиридина формулы
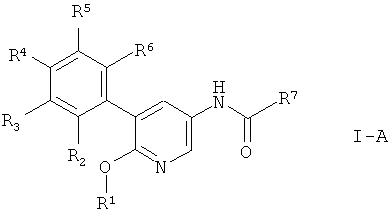
где
R1 выбран из группы, состоящей из низшего алкила,
циклоалкила,
низшего циклоалкилалкила,
низшего гидроксиалкила,
низшего алкоксиалкила,
низшего галогеналкила,
низшего карбамоилалкила,
низшего алкилкарбониламиноалкила,
низшего фенилалкила,
низшего гетероциклилалкила, где гетероциклильная группа не замещена или замещена оксо,
низшего гетероарилалкила, где гетероарильная группа не замещена или моно- или ди-замещена низшим алкилом, и
фенила, который не замещен или моно- или ди-замещен галогеном;
R2 и R6 независимо друг от друга представляют собой водород или галоген;
R3 и R5 независимо друг от друга выбраны из группы, состоящей из водорода, низшего алкила, низшего алкокси, галогена, низшего галогеналкила, низшего галогеналкокси и циано;
R4 выбран из группы, состоящей из водорода, низшего алкила, низшего алкокси, галогена, низшего галогеналкила, низшего галогеналкокси, амино, азидо и циано;
R7 выбран из группы, состоящей из низшего алкила,
низшего гидроксиалкила, низшего алкоксиалкила,
низшего гидроксиимино-алкила, низшего алкоксиимино-алкила,
низшего циклоалкила, указанный циклоалкил не замещен или замещен гидрокси,
низшего гетероциклила,
фенила, указанный фенил не замещен или замещен одной или двумя группами, выбранными из группы, состоящей из низшего алкила, гидрокси, низшего алкокси, циано, низшего алкиламинокарбонила и галогена,
гетероарила, указанный гетероарил не замещен или замещен одной или двумя группами, выбранными из группы, состоящей из низшего алкила, гидрокси, низшего алкокси, циано, низшего алкиламинокарбонила и галогена;
и их фармацевтически приемлемые соли.
Особенно настоящее изобретение относится к соединениям формулы

где
R1 выбран из группы, состоящей из низшего алкила,
циклоалкила,
низшего циклоалкилалкила,
низшего гидроксиалкила,
низшего алкоксиалкила,
низшего галогеналкила,
низшего карбамоилалкила,
низшего алкилкарбониламиноалкила,
низшего фенилалкила,
низшего гетероциклилалкила, где гетероциклильная группа не замещена или замещена оксо,
низшего гетероарилалкила, где гетероарильная группа не замещена или моно- или ди-замещена низшим алкилом, и
фенила, который не замещен или моно- или ди-замещен галогеном;
R2 и R6 независимо друг от друга представляют собой водород или галоген;
R3 и R5 независимо друг от друга выбраны из группы, состоящей из водорода, низшего алкила, низшего алкокси, галогена, низшего галогеналкила, низшего галогеналкокси и циано;
R4 выбран из группы, состоящей из водорода, низшего алкокси, галогена, низшего галогеналкила, низшего галогеналкокси, амино, азидо и циано;
R7 выбран из группы, состоящей из низшего алкила,
низшего гидроксиалкила,
низшего циклоалкила, указанный циклоалкил не замещен или замещен гидрокси,
низшего гетероциклила,
фенила, указанный фенил не замещен или замещен одной или двумя группами, выбранными из группы, состоящей из низшего алкила, гидрокси и галогена,
гетероарила, указанный гетероарил не замещен или замещен одной или двумя группами, выбранными из группы, состоящей из низшего алкила, гидрокси, циано и галогена;
и их фармацевтически приемлемым солям.
Также изобретение относится к соединениям формулы I, где А представляет собой N. Соединения представляют собой производные пиразина формулы
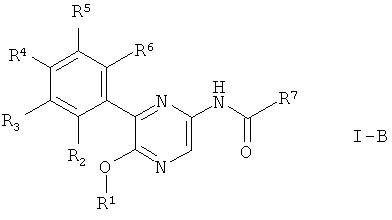
где
R1 выбран из группы, состоящей из низшего алкила,
циклоалкила,
низшего циклоалкилалкила,
низшего гидроксиалкила,
низшего алкоксиалкила,
низшего галогеналкила,
низшего карбамоилалкила,
низшего алкилкарбониламиноалкила,
низшего фенилалкила,
низшего гетероциклилалкила, где гетероциклильная группа не замещена или
замещена оксо,
низшего гетероарилалкила, где гетероарильная группа не замещена или моно- или ди-замещена низшим алкилом, и
фенила, который не замещен или моно- или ди-замещен галогеном;
R2 и R6 независимо друг от друга представляют собой водород или галоген;
R3 и R5 независимо друг от друга выбраны из группы, состоящей из водорода, низшего алкила, низшего алкокси, галогена, низшего галогеналкила, низшего галогеналкокси и циано;
R4 выбран из группы, состоящей из водорода, низшего алкила, низшего алкокси, галогена, низшего галогеналкила, низшего галогеналкокси, амино, азидо и циано;
R7 выбран из группы, состоящей из низшего алкила,
низшего гидроксиалкила, низшего алкоксиалкила,
низшего гидроксиимино-алкила, низшего алкоксиимино-алкила,
низшего циклоалкила, указанный циклоалкил не замещен или замещен гидрокси,
низшего гетероциклила,
фенила, указанный фенил не замещен или замещен одной или двумя группами, выбранными из группы, состоящей из низшего алкила, гидрокси, низшего алкокси, циано, низшего алкиламинокарбонила и галогена,
гетероарила, указанный гетероарил не замещен или замещен одной или двумя группами, выбранными из группы, состоящей из низшего алкила, гидрокси, низшего алкокси, циано, низшего алкиламинокарбонила и галогена;
и их фармацевтически приемлемые соли.
Особые соединения формулы I по настоящему изобретению являются следующими:
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид пентановой кислоты,
N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-бензамид,
N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-никотинамид,
N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-изоникотинамид,
N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-ацетамид,
N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-бутирамид,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид пиридин-2-карбоновой кислоты,
N-[5-(4-хлор-фенил)-6-циклопропилметокси-пиридин-3-ил]-бензамид,
N-[5-(4-хлор-фенил)-6-циклопропилметокси-пиридин-3-ил]-ацетамид,
N-[5-(4-хлор-фенил)-6-циклопропилметокси-пиридин-3-ил]-никотинамид,
N-[5-(4-хлор-фенил)-6-циклопропилметокси-пиридин-3-ил]-изоникотинамид,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид пиразин-2-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид 2,5-диметил-2H-пиразол-3-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид 3-метил-изоксазол-4-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид 1-метил-1Н-пиразол-3-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид 5-метил-изоксазол-3-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид пиридазин-3-карбоновой кислоты,
N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-3-метил-изоникотинамид,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид пиримидин-5-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид 2-метил-2H-пиразол-3-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид 2,4-диметил-оксазол-5-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид изотиазол-5-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид 5-метил-2Н-пиразол-3-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид 1Н-пиразол-3-карбоновой кислоты,
N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-2-метил-изоникотинамид,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид 5-метил-тиазол-2-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид 4-метил-[1,2,3]тиадиазол-5-карбоновой кислоты,
N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-6-метил-никотинамид,
N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-2-метил-никотинамид,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид изоксазол-5-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид 3,5-диметил-изоксазол-4-карбоновой кислоты,
N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-2-гидрокси-изоникотинамид,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид 1,3-диметил-1Н-пиразол-4-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид пиримидин-4-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид тиазол-2-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид 3-метил-пиридин-2-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид 5-метил-оксазол-4-карбоновой кислоты,
N-(5-(3,4-диметилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-никотинамид,
N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-никотинамид, и их фармацевтически приемлемые соли.
Дополнительные соединения формулы I по настоящему изобретению являются следующими:
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид 5-гидрокси-пиридин-2-карбоновой кислоты,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-5-метилникотинамид,
(S)-N-(5-(4-хлорфенил)-6-(1,1,1-трифторпропан-2-илокси)пиридин-3-ил)пиридазин-3-карбоксамид,
(S)-N-(5-(4-хлорфенил)-6-(1,1,1-трифторпропан-2-илокси)пиридин-3-ил)никотинамид,
N-(5-(4-хлор-3-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамид,
N-(5-(3-хлор-4-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамид,
N-(5-(4-хлор-2-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамид,
N-(5-(4-этилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамид,
(S)-N-(6-(4-хлорфенил)-5-(1,1,1-трифторпропан-2-илокси)пиразин-2-ил)никотинамид,
N-(6-(4-хлорфенил)-5-(2,2,2-трифторэтокси)пиразин-2-ил)никотинамид,
N-(6-(4-хлорфенил)-5-циклобутоксипиразин-2-ил)никотинамид,
N-(6-(4-хлорфенил)-5-циклобутоксипиразин-2-ил)пиримидин-5-карбоксамид,
N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиримидин-5-карбоксамид,
N-(5-(4-хлор-3-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиримидин-5-карбоксамид,
N-(5-(3-хлор-4-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиримидин-5-карбоксамид,
N-(5-(4-хлор-2-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиримидин-5-карбоксамид,
N-(5-(4-этилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиримидин-5-карбоксамид,
N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-2-гидроксиизоникотинамид,
N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-1,3-диметил-1H-пиразол-4-карбоксамид,
N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-2,4-дифторникотинамид,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-2-гидроксибензамид,
N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-5-цианоникотинамид,
N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиридазин-3-карбоксамид,
N-(5-(4-хлор-3-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиридазин-3-карбоксамид,
N-(5-(4-хлор-2-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиридазин-3-карбоксамид,
N-(5-(4-этилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиридазин-3-карбоксамид,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)фуран-2-карбоксамид,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)фуран-3-карбоксамид,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-5-метилфуран-2-карбоксамид,
N-(5-(4-хлор-3-метилфенил)-6-(2-метоксиэтокси)пиридин-3-ил)бензамид,
(R)-N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)тетрагидрофуран-2-карбоксамид,
(S)-N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)тетрагидрофуран-3-карбоксамид,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-4-метил-3,4-дигидро-2H-пиридо[3,2-b][1,4]оксазин-7-карбоксамид,
N-(5-(4-амино-3-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-5-йодникотинамид,
N-(5-фенил-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамид,
N-(5-(4-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамид,
N-(5-(3-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамид,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-5-метоксиникотинамид,
N-(5-(4-хлорфенил)-6-циклобутоксипиридин-3-ил)пиразин-2-карбоксамид,
N-(5-(4-хлорфенил)-6-циклобутоксипиридин-3-ил)никотинамид,
N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-4-метил-3,4-дигидро-2H-пиридо[3,2-b][1,4]оксазин-7-карбоксамид,
N-(5-(4-хлор-3-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-4-метил-3,4-дигидро-2H-пиридо[3,2-b][1,4]оксазин-7-карбоксамид,
[5-(4-хлор-фенил)-6-циклобутокси-пиридин-3-ил]-амид 6-метил-оксазол-4-карбоновой кислоты,
N-[5-(4-хлор-фенил)-6-циклобутокси-пиридин-3-ил]-5-метил-никотинамид,
N5-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-N2-метилпиридин-2,5-дикарбоксамид,
5-бром-N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамид,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-2-метоксипропанамид,
N3-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-N5-метилпиридин-3,5-дикарбоксамид,
(+)-N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-2-метоксипропанамид,
(Е)-N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-2-(метоксиимино)пропанамид,
и их фармацевтически приемлемые соли.
Более конкретно соединения формулы I по настоящему изобретению являются следующими:
N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-никотинамид,
N-[5-(4-хлор-фенил)-6-циклопропилметокси-пиридин-3-ил]-никотинамид,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид 3-метил-изоксазол-4-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид пиридазин-3-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид 1,3-диметил-1Н-пиразол-4-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид 5-метил-оксазол-4-карбоновой кислоты,
N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-никотинамид,
N-(5-(4-хлор-3-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамид,
(3)-N-(6-(4-хлорфенил)-5-(1,1,1-трифторпропан-2-илокси)пиразин-2-ил)никотинамид,
N-(6-(4-хлорфенил)-5-циклобутоксипиразин-2-ил)пиримидин-5-карбоксамид,
N-(5-(4-хлор-2-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиримидин-5-карбоксамид,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-2-гидроксибензамид,
N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-5-цианоникотинамид,
N-(5-(4-хлор-2-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиридазин-3-карбоксамид,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-5-метилфуран-2-карбоксамид,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-4-метил-3,4-дигидро-2H-пиридо[3,2-b][1,4]оксазин-7-карбоксамид,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-5-метоксиникотинамид,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-2-метоксипропанамид,
и их фармацевтически приемлемые соли.
Даже более конкретно изобретение относится к соединению формулы I, которое представляет собой N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-никотинамид и его фармацевтически приемлемые соли.
Также более конкретно изобретение относится к соединению формулы I, которое представляет собой N-[5-(4-хлор-фенил)-6-циклопропилметокси-пиридин-3-ил]-никотинамид и его фармацевтически приемлемые соли.
Также более конкретно изобретение относится к соединению формулы I, которое представляет собой N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-5-метоксиникотинамид и его фармацевтически приемлемые соли.
Соединения формулы I могут быть получены способом, согласно которому связывают соединение формулы
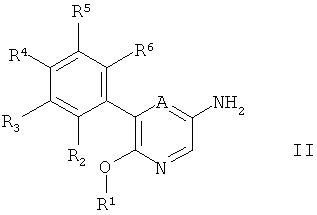
где А и R1 - R6 являются такими, как определено выше, с кислотой формулы
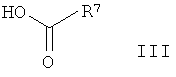
где R7 является таким, как определено выше, с помощью связующего вещества при основных условиях,
и при желании переводят полученное в результате соединение формулы I в его фармацевтически приемлемую соль.
Связующими веществами для реакции соединений формулы II с кислотами формулы III являются, например, N,N'-карбонилдиимидазол (CDI), N,N'-дициклогексилкарбодиимид (DCC), 1-(3-диметиламинопропил)-3-этилкарбодиимида гидрохлорид (EDCI), 1-[бис(диметиламино)-метилен]-1H-1,2,3-триазоло[4,5-b]пиридиний-3-оксида гексафторфосфат (HATU), 1-гидрокси-1,2,3-бензотриазол (НОВТ), O-бензотриазол-1-ил-N,N,N',N'-тетраметилурония тетрафторборат (TBTU) или O-бензотриазол-N,N,N',N'-тетраметил-уроний-гексафторфосфат (HBTU). Более конкретно связующее вещество представляет собой HBTU. Подходящие основания включают триэтиламин, диизопропилэтиламин и особенно N-метилморфолин.
Синтез соединений общей структуры I-A может быть выполнен согласно схеме 1.
Следуя процедуре согласно схеме 1, соединение АА (3-бром-2-хлор-5-нитро-пиридин, CAS RN 5470-17-7) может быть использовано в качестве исходного вещества. АА имеется в продаже.
Соединение АВ можно получить из АА в ходе реакции с подходяще замещенным первичным или вторичным спиртом R1-OH в присутствии основания, например гидрида натрия, в присутствии или отсутствие инертного растворителя, например диметилформамида, при температурах от комнатной температуры до температуры кипения растворителя, предпочтительно при комнатной температуре.
Соединение АС можно получить из АВ в ходе восстановления, используя многочисленные варианты возможностей, известных в данной области техники для восстановления ароматической нитрогруппы. Удобный способ восстановления состоит в использовании хлорида олова в подходящей смеси растворителей, предпочтительно в этаноле с добавленной соляной кислотой, при температурах от комнатной температуры до повышенных температур, предпочтительно при 25°С.
Схема 1

Соединение II можно получить из АС в ходе связывания подходяще замещенных арильных металлических частиц формулы AD, особенно арилбороновой кислоты или эфира арилбороновой кислоты, в присутствии подходящего катализатора, в частности палладиевого катализатора, и более конкретно смесей ацетата палладия (II) / трифенилфосфина или комплексов хлорида палладия (II) - dppf (1,1'-бис(дифенил-фосфино)ферроцена), и основания, такого как триэтиламин, карбонат натрия или фосфат калия, в инертном растворителе, таком как диметилформамид, толуол, тетрагидрофуран, ацетонитрил и диметоксиэтан.
Соединения формулы AD, содержащие функциональные группы, неблагоприятные для палладий-катализируемых реакций Сузуки, могут быть с целью проведения этой реакции защищены подходящей защитной группой (Р). Подходящими аминными защитными группами являются, например, бензилокси-карбонил (Z), трет-бутилоксикарбонил (ВОС), тогда как походящими кислотными защитными группами являются, например, бензил (Вn), бензилоксиметил (ВОМ), метоксиэтоксиметил (MEM) или аллильные группы и силильные группы, такие как триметилсилильный, триэтилсилильный и трет-бутилдиметилсилильный эфиры (дополнительную информацию смотрите у T.W. Greene et al., Protective Groups in Organic Chemistry, John Wiley и Sons Inc. New York 1999, 3rd edition). Удаление защитной группы можно выполнить подходящими способами, известными в данной области техники.
Соединение I-A можно получить из II и соответствующей кислоты формулы III в ходе подходящих реакций образования амидной связи. Эти реакции известны в данной области техники. Например, связующие реагенты, подобные N,N'-карбонил-диимидазолу (CDI), N,N'-дициклогексилкарбодиимиду (DCC), 1-(3-диметиламинопропил)-3-этилкарбодиимида гидрохлориду (EDCI), 1-[бис(диметиламино)-метилен]-1Н-1,2,3-триазоло[4,5-b]пиридиний-3-оксида гексафторфосфату (HATU), 1-гидрокси-1,2,3-бензотриазолу (НОВТ), O-бензотриазол-1-ил-N,N,N',N'-тетраметилурония тетрафторборату (TBTU) и O-бензотриазол-N',N,N',N'-тетраметил-урония-гексафторфосфату (HBTU) можно использовать для осуществления подобного превращения. Удобный способ состоит в использовании, например, HBTU и основания, например N-метилморфолина, в инертном растворителе, таком как, например, диметилформамид, при комнатной температуре.
Следуя альтернативной процедуре согласно схеме 2, соединение АС можно использовать в качестве исходного вещества.
Соединение BD можно получить из АС и соответствующей кислоты формулы III в ходе подходящих реакций образования амидной связи. Эти реакции известны в данной области техники. Например, связующие реагенты, подобные N,N'-карбонил-диимидазолу (CDI), N,N'-дициклогексилкарбодиимиду (DCC), 1-(3-диметиламинопропил)-3-этилкарбодиимида гидрохлориду (EDCI), 1-[бис(диметиламино)-метилен]-1H-1,2,3-триазоло[4,5-b]пиридиний-3-оксида гексафторфосфату (HATU), 1-гидрокси-1,2,3-бензотриазолу (НОВТ), O-бензотриазол-1-ил-N,N,N',N'-тетраметилурония тетрафторборату (TBTU) и O-бензотриазол-N,N,N,N'-тетраметил-урония-гексафторфосфату (HBTU) можно использовать для осуществления подобного превращения. Удобный способ состоит в использовании, например, HBTU и основания, например N-метилморфолина, в инертном растворителе, таком как, например, диметилформамид, при комнатной температуре.
Соединение I-А можно получить из BD в ходе связывания подходяще замещенных арильных металлических частиц формулы AD, особенно арилбороновой кислоты или эфира арилбороновой кислоты, в присутствии подходящего катализатора, в частности палладиевого катализатора, и более конкретно смесей ацетата палладия (II) / трифенилфосфина или комплексов хлорида палладия (II) - dppf (1,1'-бис(дифенил-фосфино)ферроцена), и основания, такого как триэтиламин, карбонат натрия или фосфат калия, в инертном растворителе, таком как диметилформамид, толуол, тетрагидрофуран, ацетонитрил и диметоксиэтан.
Схема 2

Соединения формулы AD, содержащие функциональные группы, неблагоприятные для палладий-катализируемых реакций Сузуки, могут быть с целью проведения этой реакции защищены подходящей защитной группой (Р). Подходящими аминными защитными группами являются, например, бензилокси-карбонил (Z), трет-бутилоксикарбонил (ВОС), тогда как походящими кислотными защитными группами являются, например, бензил (Bn), бензилоксиметил (ВОМ), метоксиэтоксиметил (MEM) или аллильные группы и силильные группы, такие как триметилсилильный, триэтилсилильный и трет-бутилдиметилсилильный эфиры (дополнительную информацию смотрите у T.W. Greene et al., Protective Groups in Organic Chemistry, John Wiley и Sons Inc. New York 1999, 3rd edition). Удаление защитной группы можно выполнить подходящими способами, известными в данной области техники.
Следуя процедуре согласно схеме 3, соединение СА (3-бром-5-хлор-2-фтор-пиридин, CAN 884484-87-5) можно использовать в качестве исходного вещества. СА имеется в продаже.
Соединение СВ можно получить из СА в ходе связывания подходяще замещенных арильных металлических частиц формулы AD, особенно арилбороновой кислоты или эфира арилбороновой кислоты, в присутствии подходящего катализатора, в частности палладиевого катализатора, и более конкретно смесей ацетата палладия (II) / трифенилфосфина или комплексов хлорида палладия (II) - dppf (1,1'-бис(дифенил-фосфино)ферроцена), и основания, такого как триэтиламин, карбонат натрия или фосфат калия, в инертном растворителе, таком как диметилформамид, толуол, тетрагидрофуран, ацетонитрил и диметоксиэтан.
Соединения формулы AD, содержащие функциональные группы, неблагоприятные для палладий-катализируемых реакций Сузуки, могут быть с целью проведения этой реакции защищены подходящей защитной группой (Р). Подходящими аминными защитными группами являются, например, бензилокси-карбонил (Z), трет-бутилоксикарбонил (ВОС), тогда как походящими кислотными защитными группами являются, например, бензил (Bn), бензилоксиметил (ВОМ), метоксиэтоксиметил (MEM) или аллильные группы и силильные группы, такие как триметилсилильный, триэтилсилильный и трет-бутилдиметилсилильный эфиры (дополнительную информацию смотрите у T.W. Greene et al., Protective Groups in Organic Chemistry, John Wiley и Sons Inc. New York 1999, 3rd edition). Удаление защитной группы можно выполнить подходящими способами, известными в данной области техники.
Соединение СС можно получить из СВ в ходе реакции с подходяще замещенным первичным или вторичным спиртом R1-OH в присутствии основания, например гидрида натрия, в присутствии или отсутствие инертного растворителя, например диметилформамида, при температурах от комнатной температуры до температуры кипения растворителя, предпочтительно при комнатной температуре.
Соединения общей формулы CD можно получить из соединений общей формулы СС в ходе катализируемой переходным металлом, а именно катализируемой палладием, предпочтительно катализируемой хлоридом палладия (II) - dppf реакции с монооксидом углерода в подходящем растворителе, таком как первичный спирт, особенно метанол, под давлением монооксида углерода от 1 до 200 бар, в частности от 1 до 70 бар и температурах от 0 до 150°С, особенно от 1 до 100°С.
Омыление полученного в результате эфира CD способами, хорошо известными квалифицированному специалисту в данной области техники, приводит к кислотам общей формулы СЕ.
Соединения общей формулы CF можно получить из соединений общей формулы СЕ посредством перегруппировки Курциуса, предпочтительно при обработке с дифенилфосфорил азидом и основанием, особенно триэтиламином, в кипящем трет-бутаноле. Удалить защитные группы у карбаматов общей формулы CF можно способами, хорошо известными в данной области техники, что даст амины общей формулы II. Альтернативно амины общей формулы II можно получить из кислот общей формулы СЕ в ходе синтеза соответствующего первичного амида с последующей перегруппировкой Гофмана.
Схема 3
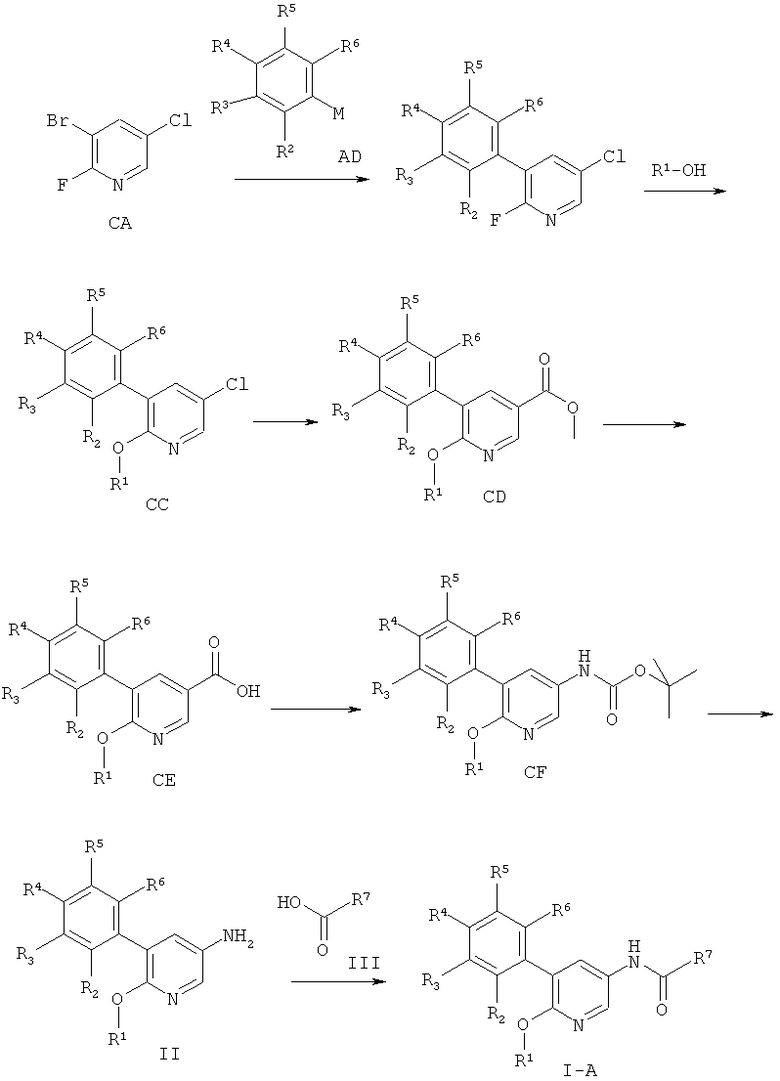
Соединение I-А можно получить из II и соответствующей кислоты формулы III в ходе подходящих реакций образования амидной связи. Эти реакции известны в данной области техники. Например, связующие реагенты, подобные N,N'-карбонил-диимидазолу (CDI), N,N'-дициклогексилкарбодиимиду (DCC), 1-(3-диметиламинопропил)-3-этилкарбодиимида гидрохлориду (EDCI), 1-[бис(диметиламино)-метилен]-1H-1,2,3-триазоло[4,5-b]пиридиний-3-оксида гексафторфосфату (HATU), 1-гидрокси-1,2,3-бензотриазолу (НОВТ), O-бензотриазол-1-ил-N,N,N',N'-тетраметилурония тетрафторборату (TBTU) и O-бензотриазол-N,N,N',N'-тетраметил-урония-гексафторфосфату (Н BTU) можно использовать для осуществления подобного превращения. Удобный способ состоит в использовании, например, HBTU и основания, например N-метилморфолина, в инертном растворителе, таком как, например, диметилформамид, при комнатной температуре.
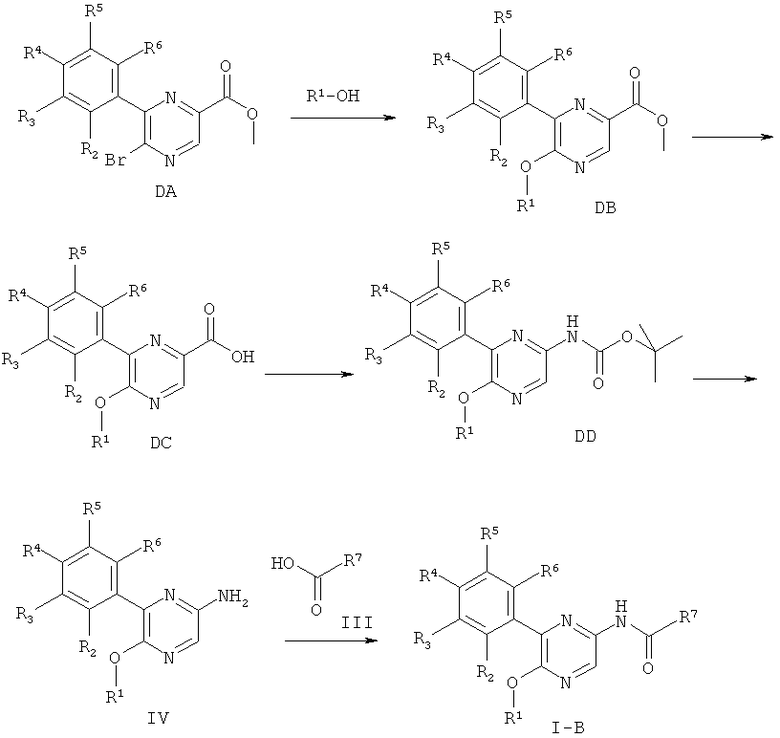
Следуя процедуре согласно схеме 4, соединения общей формулы DA (синтез которых описан, например. в WO 2008040651 и WO 2008040649) можно использовать в качестве исходных веществ, чтобы получить соединения общей формулы I-В.
В частности, соединения общей формулы DB можно получить из соединений общей формулы DA в ходе реакции с подходяще замещенным первичным или вторичным спиртом R1-OH в присутствии основания, например карбоната цезия, в присутствии или отсутствие инертного растворителя, например диметилсульфоксида, при температурах от комнатной температуры до температуры кипения растворителя, особенно при комнатной температуре.
Омыление полученного в результате эфира общей формулы DB способами, хорошо известными квалифицированному специалисту в данной области техники, приводит к кислотам общей формулы DC.
Соединения общей формулы DD можно получить из соединений общей формулы DC посредством перегруппировки Курциуса, предпочтительно при обработке с дифенилфосфорил азидом и основанием, особенно триэтиламином, в кипящем трет-бутаноле. Удалить защитные группы у карбаматов общей формулы DD можно способами, хорошо известными в данной области техники, что даст амины общей формулы IV. Альтернативно амины общей формулы IV можно получить из кислот общей формулы DC в ходе синтеза соответствующего первичного амида с последующей перегруппировкой Гофмана.
Соединения общей формулы I-В можно получить из IV и соответствующих кислот формулы III в ходе подходящих реакций образования амидной связи. Эти реакции известны в данной области техники. Например, связующие реагенты, подобные N,N-карбонил-диимидазолу (CDI), N,N-дициклогексилкарбодиимиду (DCC), 1-(3-диметиламинопропил)-3-этилкарбодиимида гидрохлориду (EDCI), 1-[бис(диметиламино)-метилен]-1H-1,2,3-триазоло[4,5-b]пиридиний-3-оксида гексафторфосфату (HATU), 1-гидрокси-1,2,3-бензотриазолу (НОВТ), O-бензотриазол-1-ил-N,N,N',N'-тетраметилурония тетрафторборату (TBTU) и O-бензотриазол-N,N,N',N'-тетраметил-урония-гексафторфосфату (HBTU) можно использовать для осуществления подобного превращения. Удобный способ состоит в использовании, например, HBTU и основания, например N-метилморфолина, в инертном растворителе, таком как, например, диметилформамид, при комнатной температуре.
Схема 4
Соединения общей формулы I-А или I-В могут быть, при необходимости, известными в данной области техники способами подвергнуты дальнейшей обработке до других соединения той же самой общей формулы. Это может, например, включать удаление защитной группы способами, известными в данной области техники (дополнительную информацию смотрите у T.W. Greene et al., Protective Groups in Organic Chemistry, John Wiley и Sons Inc. New York 1999, 3rd edition); или простые преобразования функциональных групп, например преобразование кетогруппы в гидроксиимино или метоксиимино группу.
Как описано выше, соединения формулы I по настоящему изобретению или их фармацевтически приемлемые соли могут быть использованы в качестве лекарственных средств для лечения и/или профилактики заболеваний, которые можно лечить с помощью агентов, повышающих уровень холестерина ЛПВП. Примерами таких заболеваний являются атеросклероз, заболевание периферических сосудов, дислипидемия, гипербеталипопротеинемия, гипоальфалипопротеинемия, гиперхолестеринемия, гипертриглицеридемия, семейная гиперхолестеринемия, сердечно-сосудистые заболевания, такие как стенокардия, ишемия, сердечная ишемия, инсульт, инфаркт миокарда, реперфузионное повреждение, ангиопластический рестеноз, гипертензия, и сосудистые осложнения диабета, ожирение или эндотоксикоз. Особый интерес представляет применение в качестве лекарственного средства для лечения и/или профилактики дислипидемии, атеросклероза и сердечно-сосудистых заболеваний.
Следовательно, изобретение также относится к фармацевтическим композициям, включающим соединение формулы I, как определено выше, или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель и/или вспомогательное вещество. Фармацевтические композиции используются в лечении и/или профилактике заболеваний, которые можно лечить с помощью агентов, повышающих уровень холестерина ЛПВП.
Таким образом, изобретение относится к фармацевтической композиции, как определено выше, для применения в лечении и/или профилактике атеросклероза, заболевания периферических сосудов, дислипидемии, гипербеталипопротеинемии, гипоальфалипопротеинемии, гиперхолестеринемии, гипертриглицеридемии, семейной гиперхолестеринемии, сердечно-сосудистых заболеваний, таких как стенокардия, ишемия, сердечная ишемия, инсульт, инфаркт миокарда, реперфузионное повреждение, ангиопластический рестеноз, гипертензия, и сосудистых осложнений диабета, ожирения или эндотоксикоза.
В другом воплощении изобретение относится к способу лечения и/или профилактики заболеваний, которые можно лечить с помощью агентов, повышающих уровень холестерина ЛПВП, согласно которому вводят терапевтически эффективное количество соединения формулы I или его фармацевтически приемлемой соли пациенту, нуждающемуся в этом. Примерами таких заболеваний являются атеросклероз, заболевание периферических сосудов, дислипидемия, гипербеталипопротеинемия, гипоальфалипопротеинемия, гиперхолестеринемия, гипертриглицеридемия, семейная гиперхолестеринемия, сердечно-сосудистые заболевания, такие как стенокардия, ишемия, сердечная ишемия, инсульт, инфаркт миокарда, реперфузионное повреждение, ангиопластический рестеноз, гипертензия и сосудистые осложнения диабета, ожирение или эндотоксикоз. Предпочтительным является способ лечения и/или профилактики дислипидемии, атеросклероза и сердечно-сосудистых заболеваний.
Также изобретение относится к соединениям формулы I или их фармацевтически приемлемым солям для применения в качестве лекарственных средств. А именно, изобретение относится к соединениям формулы I или их фармацевтически приемлемым солям для применения в качестве агентов, повышающих уровень холестерина ЛПВП. Таким образом, изобретение относится к соединениям формулы I или их фармацевтически приемлемым солям для применения в лечении и/или профилактике атеросклероза, заболевания периферических сосудов, дислипидемии, гипербеталипопротеинемии, гипоальфалипопротеинемии, гиперхолестеринемии, гипертриглицеридемии, семейной гиперхолестеринемии, сердечно-сосудистых заболеваний, таких как стенокардия, ишемия, сердечная ишемия, инсульт, инфаркт миокарда, реперфузионное повреждение, ангиопластический рестеноз, гипертензия, и сосудистых осложнений диабета, ожирения или эндотоксикоза, в частности, для применения в лечении и/или профилактике дислипидемии, атеросклероза и сердечно-сосудистых заболеваний.
Кроме того, изобретение относится к применению соединений формулы I, как определено выше, или их фармацевтически приемлемых солей для получения лекарства для лечения и/или профилактики заболеваний, которые можно лечить с помощью агентов, повышающих уровень холестерина ЛПВП. Примерами таких заболеваний являются атеросклероз, заболевание периферических сосудов, дислипидемия, гипербеталипопротеинемия, гипоальфалипопротеинемия, гиперхолестеринемия, гипертриглицеридемия, семейная гиперхолестеринемия, сердечно-сосудистые заболевания, такие как стенокардия, ишемия, сердечная ишемия, инсульт, инфаркт миокарда, реперфузионное повреждение, ангиопластический рестеноз, гипертензия, и сосудистые осложнения диабета, ожирение или эндотоксикоз. Особый интерес представляет применение соединений формулы I, как определено выше, или их фармацевтически приемлемых солей для получения лекарств для лечения и/или профилактики дислипидемии, атеросклероза и сердечно-сосудистых заболеваний.
Кроме того, агенты, повышающие уровень холестерина ЛПВП, формулы I применяются в сочетании или связи с другим соединением, указанное соединение выбрано из группы, состоящей из ингибитора ГМГ-КоА-редуктазы, ингибитора секреции микросомального белка переноса триглицеридов (МТР)/АроВ, активатора PPAR, ингибитора белка переноса холестериновых эфиров (СЕТР), ингибитора обратного захвата желчных кислот, ингибитора абсорбции холестерина, ингибитора синтеза холестерина, фибрата, ниацина, препарата, содержащего ниацин, или других агонистов НМ74а, ионообменной смолы, антиоксиданта, ингибитора АСАТ или секвестранта желчных кислот.
Следовательно, изобретение также относится к фармацевтическим композициям, включающим соединение формулы I, как определено выше, или его фармацевтически приемлемую соль в сочетании или связи с другим соединением, выбранным из группы, состоящей из ингибитора ГМГ-КоА-редуктазы, ингибитора секреции микросомального белка переноса триглицеридов (МТР)/АроВ, активатора PPAR, ингибитора белка переноса холестериновых эфиров (СЕТР), ингибитора обратного захвата желчных кислот, ингибитора абсорбции холестерина, ингибитора синтеза холестерина, фибрата, ниацина, препарата, содержащего ниацин, или других агонистов НМ74а, ионообменной смолы, антиоксиданта, ингибитора АСАТ или секвестранта желчных кислот, а также фармацевтически приемлемый носитель и/или вспомогательное вещество.
Кроме того, изобретение относится к соединениям формулы I, как определено выше, или их фармацевтически приемлемым солям в сочетании или связи с соединением, выбранным из группы, состоящей из ингибитора ГМГ-КоА-редуктазы, ингибитора секреции микросомального белка переноса триглицеридов (МТР)/АроВ, активатора PPAR, ингибитора белка переноса холестериновых эфиров (СЕТР), ингибитора обратного захвата желчных кислот, ингибитора абсорбции холестерина, ингибитора синтеза холестерина, фибрата, ниацина, препарата, содержащего ниацин, или других агонистов НМ74а, ионообменной смолы, антиоксиданта, ингибитора АСАТ или секвестранта желчных кислот, для применения в лечении и/или профилактике заболеваний, таких как атеросклероз, заболевание периферических сосудов, дислипидемия, гипербеталипопротеинемия, гипоальфалипопротеинемия, гиперхолестеринемия, гипертриглицеридемия, семейная гиперхолестеринемия, сердечно-сосудистые заболевания, такие как стенокардия, ишемия, сердечная ишемия, инсульт, инфаркт миокарда, реперфузионное повреждение, ангиопластический рестеноз, гипертензия, и сосудистые осложнения диабета, ожирение или эндотоксикоз.
Также изобретение относится к способу лечения и/или профилактики заболеваний, которые можно лечить с помощью агентов, повышающих уровень холестерина ЛПВП, согласно которому вводят терапевтически эффективное количество соединения формулы I или его фармацевтически приемлемой соли в сочетании или связи с терапевтически эффективным количеством соединения, выбранного из группы, состоящей из ингибитора ГМГ-КоА-редуктазы, ингибитора секреции микросомального белка переноса триглицеридов (МТР)/АроВ, активатора PPAR, ингибитора белка переноса холестериновых эфиров (СЕТР), ингибитора обратного захвата желчных кислот, ингибитора абсорбции холестерина, ингибитора синтеза холестерина, фибрата, ниацина, препарата, содержащего ниацин, или других агонистов НМ74а, ионообменной смолы, антиоксиданта, ингибитора АСАТ или секвестранта желчных кислот.
Фармацевтические композиции
Соединения формулы I и/или их фармацевтически приемлемые соли могут применяться в форме фармацевтических композиций для энтерального, парентерального или местного введения. Их можно вводить, например, перорально, например в форме таблеток, таблеток, покрытых оболочкой, драже, твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий, орально, например в форме для полости рта, ректально, например в форме суппозиториев, парентерально, например в форме растворов для инъекций или инфузионных растворов для внутримышечной, внутривенной или подкожной инъекции, или местно, например в форме мазей, кремов или масел. Особый интерес представляет оральное введение.
Изготовление фармацевтических препаратов можно осуществлять способом, который знаком любому квалифицированному специалисту в данной области техники, внося описанные соединения формулы I и/или их фармацевтически приемлемые соли, возможно в сочетании с другими терапевтически ценными соединениями, в галеновую лекарственную форму вместе с подходящими, нетоксичными, инертными, терапевтически совместимыми твердыми или жидкими носителями, и, если требуется, обычными фармацевтическими вспомогательными веществами.
Подходящими носителями являются не только неорганические носители, но также и органические носители. Таким образом, например, лактозу, кукурузный крахмал или его производные, тальк, стеариновую кислоту или ее соли можно использовать в качестве носителей для таблеток, таблеток, покрытых оболочкой, драже и твердых желатиновых капсул. Подходящими носителями для мягких желатиновых капсул являются, например, растительные масла, воски, жиры и полутвердые и жидкие полиолы (однако в зависимости от природы активного вещества в случае мягких желатиновых капсул носители обычно не требуются). Подходящими носителями для получения растворов и сиропов являются, например, вода, полиолы, сахароза, инвертный сахар и подобные. Подходящими носителями для инъекционных растворов являются, например, вода, спирты, полиолы, глицерин и растительные масла. Подходящими носителями для суппозиториев являются, например, природные или отвержденные масла, воски, жиры и полужидкие или жидкие полиолы. Подходящими носителями для препаратов местного применения являются глицериды, полусинтетические и синтетические глицериды, гидрогенизированные масла, жидкие воски, жидкие парафины, жидкие жирные спирты, стерины, полиэтиленгликоли и производные целлюлозы.
Обычные стабилизаторы, консерванты, смачивающие и эмульгирующие агенты, улучшающие консистенцию агенты, улучшающие вкус агенты, соли для регулирования осмотического давления, буферные вещества, солюбилизаторы, красители, маскирующие агенты и антиоксиданты рассматриваются в качестве фармацевтических вспомогательных веществ.
Терапевтически эффективное количество или дозировка соединений формулы I может изменяться в широких пределах в зависимости от контролируемого заболевания, возраста и индивидуального состояния пациента и способа введения, и будет, конечно, подбираться по индивидуальным потребностям в каждом конкретном случае. Для взрослых пациентов рассматривается суточная доза приблизительно от 1 до 100 мг, особенно приблизительно от 1 до 50 мг. В зависимости от тяжести заболевания и точности фармакокинетического профиля соединение может вводиться одной или несколькими суточными дозированными единицами, например 1-3 дозированными единицами.
Фармацевтические композиции обычно содержат приблизительно 1-100 мг, предпочтительно 5-50 мг соединения формулы I.
Следующие примеры С1-С3 иллюстрируют обычные композиции по настоящему изобретению и лишь представляют его.
Пример С1
Покрытые пленочной оболочкой таблетки, содержащие следующие ингредиенты, могут быть изготовлены обычным способом:
Активный ингредиент просеивают и смешивают с микрокристаллической целлюлозой и смесь гранулируют с раствором поливинилпирролидона в воде. Гранулят затем смешивают с натрия крахмала гликолятом и стеаратом магния и сжимают, что дает ядра 120 или 350 мг, соответственно. Ядра лакируют водным раствором / суспензией вышеупомянутой пленочной оболочки.
Пример С2
Капсулы, содержащие следующие ингредиенты, могут быть изготовлены обычным способом:
Компоненты просеивают, смешивают и заполняют капсулы размером 2.
Пример С3
Растворы для инъекций могут иметь следующий состав:
Активный ингредиент растворяют в смеси полиэтиленгликоля 400 и воды для инъекции (часть). Доводят рН до 5,0 с помощью уксусной кислоты. Доводят объем до 1,0 мл, добавляя оставшееся количество воды. Раствор фильтруют, заполняют им ампулы, используя допустимый избыток, и стерилизуют.
Фармакологические тесты
Следующие тесты проводили, чтобы определить активность соединений формулы I и их ценные фармакологические свойства.
Детектирование повышение экспрессии белка АВСА1 в клетках
Способность соединений по изобретению увеличивать уровень белка АВСА1 определяют в повторных культурах макрофагов ТНР-1 на 96-луночных микропланшетах. Клетки высеивают при начальной плотности 100,000 клеток/лунка в 100 мкл среды и дифференцируют с липкими макрофагами с добавлением РМА (100 нМ) в течение 68 часов в 10% эмбриональной бычьей сыворотке, 3 мкл/л бета-меркаптоэтанола, RPMI-1640 среде. Затем клетки инкубируют с RPMI-1640 средой, содержащей 1% ЭТС, 25 мкг/мл ацетилированных ЛПНП, в течение 24 часов при 37°С. После инкубации с ацетилированными ЛПНП клетки промывают дважды 50 мкл ФБСР и инкубируют со 100 мкл RPMI-1640 среды, содержащей представляющее интерес соединение, солюбилизированное в ДМСО, в течение дополнительных 24 часов. Конечную концентрацию ДМСО в присутствии клеток поддерживают при 0,5%. Анализ связывания АроА-I при использовании High Content Image Analysis инициируется при замене на свежую среду, RPMI без фенолового красного, 0,2% БСА, содержащий AlexaFluor®647 меченный АроА-I, в течение 2 ч/37°С/5% CO2. Затем клетки фиксируют с 4% формальдегидом в ФБСР (15 мин, к.т.). Затем ядра окрашивают раствором Хехста (3 мкМ ФБСР) и цитоплазму окрашивают Cell Mask Blue (2 мкг/мл ФБСР), 15 минут, к.т. В конце окрашенные клетки фиксируют со второй порцией формальдегида. Фиксированные окрашенные клетки промывают и хранят в ФБСР при 4°С, и они могут быть непосредственно считаны вплоть до одного месяца после получения. То, что связывание АроА-I действительно отражало уровень АВСА1 в клетке, было показано потерей сигнала, когда экспрессия АВСА1 была искусственно уменьшена при трансфекции с малыми интерферирующими РНК.
Alexa Fluor 647-меченный Аполипопротеин A-I (20 нМ) получали следующим образом: Рекомбинантный Аполипопротеин A-I (АроА-I) человека заменяли в буфере 0,02 М NaHCO3 при рН 8,2 на NAP обессоленной колонки (GE Healthcare) и доводили до концентрации 40 мкМ (1,13 мг/мл) при регулировании с тем же самым буфером. АроА-I становится флуоресцентно меченным при инкубации с Alexa Fluor сукцинимидным эфиром карбоновой кислоты (Alexa Fluor 647, Invitrogen A-20006) при молярном соотношении 2:1 (Alexa к ApoA-I) в течение 1 часа при встряхивании при к.т. Оставшуюся несвязанную метку удаляли заменой буфера до 0,02 М NaHCO3 при рН 8,2.
Регистрацию изображений и данных выполняли на конфокальном аппарате для прочтения планшетов OPERA, используя 20х водно-иммерсионный объектив и УФ360 или 405 лазерную установку для идентификации клеточных ядер и 635 лазерную установку для идентификации флуоресцирующего ApoA-I. Восемь зон обзора записывали на лунку. Запись изображений и анализ проводили с помощью программного обеспечения Acapella. Фоновую флуоресценцию, детектируемую на контрольных лунках без ApoA-I, вычитали.
Применяя программу XLfit3 (ID Business Solutions Ltd. UK), модель 205 для Dose Response One Site используют для вычисления значений ЕС50. Соединения по настоящему изобретению увеличивают уровень белка АВСА1 более чем на 45% при концентрации 3 мкМ. Предпочтительно соединения показывают значения ЕС50 в диапазоне от 0,1 мкМ до 10 мкМ в ходе анализа обнаружения белка АВСА1. Даже более предпочтительно соединения по настоящему изобретению имеют значения ЕС50 в диапазоне от 0,1 мкМ до 3 мкМ.
Анализ выведения холестерина
Способность соединений по изобретению стимулировать выведение холестерина определяют в повторных культурах клеток ТНР-1 на 96-луночных микропланшетах. Клетки высеивают при начальной плотности 150,000 клеток/лунка и дифференцируют с макрофагами с добавлением РМА (100 нг/мл) в течение 72 часов в 10% эмбриональной бычьей сыворотке, 3 мкл/л бета-меркаптоэтанола, RPMI-1640 среде. Клетки промывают один раз с RPMI-1640 и загружают с RPMI-1640 средой, содержащей 2% ЭТС, 50 мкг/мл ацетилированных ЛПНП и 10 мкКи/мл [3H]холестерина, в течение 48 часов при 37°С. После загрузки клетки промывают один раз RPMI-1640 и инкубируют с представляющим интерес соединением из растворов ДМСО в течение дополнительных 24 часов в RPMI-1640 среде, содержащей 1 мг/мл альбумина бычьей сыворотки (БСА), не содержащего жирных кислот. После инкубации клетки промывают один раз, и выведение холестерина вызывают добавлением 10 мкг/мл Аполипопротеина AI в RPMI-1640, содержащей 1 мг/мл БСА, и в присутствии соединения в течение дополнительных 6 часов. После инкубации радиоактивность определяют в надосадочных жидкостях, и выведение холестерина выражают в виде процентов стимуляции относительно повторных культур, обработанных только с ДМСО. Сигмоидальные кривые строили, используя программное обеспечение XLfit3 (ID Business Solutions Ltd. UK), и определяли значения ЕС50.
Соединения по настоящему изобретению показывают значения EC50 в диапазоне от 0,1 мкМ до 3,0 мкМ в ходе анализа выведения холестерина. Предпочтительно соединения по настоящему изобретению имеют значения ЕС50 в диапазоне от 0,1 мкМ до 1,5 мкМ.
Сродство к рецепторам СВ1 и СВ2
Сродство соединений по изобретению к каннабиноидным рецепторам определяли, используя мембранные препараты из клеток эмбриональной почки человека (НЕК от human embryonic kidney), в которых рецептор СВ1 человека временно трансфицируют, используя систему вируса леса Семлики в сочетании с [3Н]-СР-55,940 в качестве радиолиганда. После инкубации свежеприготовленного препарата клеточных мембран с [3H]-лигандом, с или без добавления соединений по изобретению, разделение связанного и свободного лиганда осуществляли в ходе фильтрации через стекловолоконные фильтры. Радиоактивность на фильтре измеряли сцинтилляционным методом.
Сродство соединений по изобретению к каннабиноидным рецепторам СВ2 определяли, используя мембранные препараты из клеток эмбриональной почки человека (НЕК), в которых рецептор СВ2 человека временно трансфицируют, используя систему вируса леса Семлики в сочетании с [3Н]-СР-55,940 в качестве радиолиганда. После инкубации свежеприготовленного препарата клеточных мембран с [3H]-лигандом, с или без добавления соединений по изобретению, разделение связанного и свободного лиганда осуществляли в ходе фильтрации через стекловолоконные фильтры. Радиоактивность на фильтре измеряли сцинтилляционным методом.
Способность соединений вытеснять радиолиганд [3H]-СР-55,940 измеряли при концентрации 10 мкМ и приводятся значения в виде [% ингибирования при 10 мкМ] для обоих анализов рецепторов СВ1 и СВ2. Чем ниже % ингибирования, тем ниже вероятность побочных эффектов, основанных на ингибировании рецепторов СВ1 или СВ2.
Соединения по настоящему изобретению показывают значения ниже 50% ингибирования в обоих анализах рецепторов СВ1 и СВ2 при концентрации 10 мкМ. Предпочтительно соединения по настоящему изобретению показывают значения ниже 35% ингибирования в обоих анализах рецепторов СВ1 и СВ2 и даже более предпочтительно ниже 20% в обоих анализах.
Дополнительная демонстрация биологических активностей соединений по настоящему изобретению может быть выполнена посредством следующих анализов in vivo, которые хорошо известны в данной области техники.
Влияние на уровни липидов в плазме на тощих крысах, получающих корм
Влияние соединений формулы I на уровни липидов в плазме определяли на тощих крысах линии Спраг-Доули, получающих корм с соединениями, введенными перорально с искусственным питанием. После одной недели акклиматизации образцы крови собирали у животных, 4 часа не получающих до этого пищу, для определения липидов в плазме. Затем животных закрепляли за экспериментальными группами исходя из уровней холестерина ЛПВП. Соединения формулы I вводили искусственным путем один раз в день в течение пяти дней. Контрольные животные принимали только наполнитель. Кровь собирали на пятый день у крыс, 4 часа не получающих до этого пищу, через 2 часа после окончательного введения для анализа липидов в плазме. Общий холестерин, холестерин ЛПВП и триглицериды определяли, измеряя общий холестерин, холестерин ЛПВП и триглицериды, используя колориметрические ферментные анализы (Roche Diagnostic GmbH, Mannheim, Germany). Количество ЛПВП-Х также определяли, используя эксклюзионную хроматографию на колонке superpose-6, используя систему SMART (Pharmacia). Распределение липопротеинов рассчитывали исходя из распределения Гаусса для каждого пика, используя аппроксимацию нелинейным методом наименьших квадратов для вычисления площади под кривой. Также определяли концентрацию соединений в плазме.
Влияние на уровни липидов в плазме на тучных крысах, получающих корм с высоким содержанием жира
Способность соединений изменять уровни липидов в плазме также определяли на тучных самцах крыс линии Спраг-Доули после 28-29 дней введения соединений. Самцам крыс линии Спраг-Доули в возрасте 10 недель давали корм с высоким содержанием жиров в течение 3 недель. Тучных крыс распределяли по группам в соответствии с однородными BW (вес тела) и FI (фарбиндекс), рассчитанными за неделю до начала обработки. Обработку осуществляли в виде пищевой добавки. На 29 день кровь собирали утром при небольшой анестезии (ретроорбитальный способ) после приема пищи, т.е. 4 часа после еды исключали. Плазму отделяли от крови низкоскоростным центрифугированием, и отобранные органы собирали (например печень, жир). Общий холестерин, холестерин ЛПВП и триглицериды определяли, измеряя общий холестерин, холестерин ЛПВП, холестерин ЛПНП и триглицериды, используя колориметрические ферментные анализы (Roche Diagnostic GmbH, Mannheim, Germany). Количество ЛПВП-Х также определяли, используя эксклюзионную хроматографию на колонке superpose-6, используя систему SMART (Pharmacia). Распределение липопротеинов рассчитывали исходя из распределения Гаусса для каждого пика, используя аппроксимацию нелинейным методом наименьших квадратов для вычисления площади под кривой. Также определяли концентрацию соединений в плазме.
Влияние на уровни липидов в плазме на хомяках
Способность соединений изменять уровни липидов в плазме определяли на хомяках через 5 дней ежедневного введения соединений. В исследованиях использовали самцов хомяков в возрасте 6-8 недель. После одной недели акклиматизации образцы крови собирали у животных, 4 часа не получающих до этого пищу, для определения липидов в плазме. Затем животных закрепляли за экспериментальными группами исходя из уровней холестерина ЛПВП. Соединения вводили искусственным путем один раз в день в течение пяти дней. Контрольные животные принимали только наполнитель. Кровь собирали на пятый день у хомяков, 4 часа не получающих до этого пищу, через 2 часа после окончательного введения для анализа липидов в плазме. Общий холестерин, холестерин ЛПВП, холестерин ЛПНП и триглицериды определяли, используя колориметрические ферментные анализы (Roche Diagnostic GmbH, Mannheim, Germany). Количественно уровни холестерина ЛПВП, холестерина ЛПНП и холестерина ЛПОНП также определяли, используя эксклюзионную хроматографию на колонке superpose-6, используя систему SMART (Pharmacia). Распределение липопротеинов рассчитывали исходя из распределения Гаусса для каждого пика, используя аппроксимацию нелинейным методом наименьших квадратов для вычисления площади под кривой. Также определяли концентрацию соединений в плазме.
Влияние на уровни липидов в плазме на хомяках, получающих корм с холестерином/жиром
Способность соединений изменять уровни липидов в плазме определяли на хомяках через 5 дней ежедневного введения соединений. В исследованиях использовали самцов хомяков в возрасте 6-8 недель. После одной недели акклиматизации образцы крови собирали у животных, 4 часа не получающих до этого пищу, для определения липидов в плазме. Затем животных закрепляли за экспериментальными группами исходя из уровней холестерина ЛПВП. Соединения вводили искусственным путем один раз в день в течение пяти дней. Контрольные животные принимали только наполнитель. Кровь собирали на пятый день у хомяком, 4 часа не получающих до этого пищу, через 2 часа после окончательного введения для анализа липидов в плазме. Общий холестерин, холестерин ЛПВП, холестерин ЛПНП и триглицериды определяли, используя колориметрические ферментные анализы (Roche Diagnostic GmbH, Mannheim, Germany). Холестерин ЛПВП также определяли после селективного осаждения ЛПВП из плазмы стандартными способами.
Примеры
МС = масс-спектрометрия; ЭИ = электронная ионизация; ЭСИ = электрораспыление; данные ЯМР представлены в миллионных долях (5) относительно внутреннего стандарта тетраметилсилана и ссылаются на сигнал захвата дейтерия из образца растворителя (d6-ДМСО, если не указано иное); константы связывания (J) приведены в герцах, т.пл. = температура плавления; т.кип. = тепература кипения; ВЭЖХ=ЖХ = высокоэффективная жидкостная хроматография, Rt = время удерживания, ТСХ = тонкослойная хроматография, к.т. = комнатная температура, ДИПЭА = диизопропилэтиламин, ДФФА = дифенилфосфорилазид, TBTU = O-(бензотриазол-1-yl)-N,N',N'-тетраметил-уроний-тетрафторборат; TEMPO = радикал 2,2,6,6-тетра-метилпиперидин-1-оксил, ДМФА = диметилформамид, ДМСО = диметилсульфоксид, ТГФ = тетрагидрофуран, CAN=регистрационный номер CAS.
Получение промежуточных соединений
Пример А
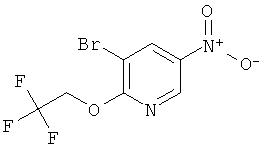
Получение 3-бром-5-нитро-2-(2,2,2-трифтор-этокси)-пиридина
Гидрид натрия (3,2 г, 80,02 ммоль) осторожно добавляли небольшими порциями к 2,2,2-трифторэтанолу (регистрационный № CAS 75-89-8) (60 мл) при 0°С в атмосфере азота и перемешивали при 25°С в течение 30 минут. Затем добавляли 3-бром-2-хлор-5-нитропиридин (регистрационный №CAS 5470-17-7) (2 г, 8,42 ммоль) в трифторэтаноле, и реакционную смесь нагревали с обратным холодильником в течение 16 часов. Растворитель выпаривали в вакууме, и остаток переносили в воду и экстрагировали этилацетатом (3×120 мл). Объединенные органические слои промывали водой и солевым раствором, сушили над Na2SO4 и концентрировали, что давало неочищенный остаток (3 г). Неочищенный остаток очищали с помощью колоночной хроматографии (3% этилацетат/гексан), что давало требуемый продукт (2,4 г, 95%) в виде желтой жидкости. МС (ЖХ/МС): не отвечает, ЯМР находится в соответствии со структурой: 1H-ЯМР (400 МГц, CDCl3):δ 4.90 (m, 2H), 8.68 (d, 1H), 8.98 (d, 1H).
Пример В
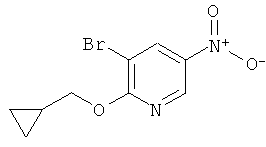
Получение 3-бром-2-циклопропилметокси-5-нитро-пиридина
К раствору гидрида натрия (2,21 г, 55,34 ммоль) в безводном ДМФА (20 мл) добавляли циклопропилметанол (регистрационный № CAS 2516-33-8) (12,45 мл, 153,2 ммоль) в атмосфере азота при 0°С и реакционную смесь перемешивали при 25°С в течение 30 минут. Затем 3-бром-2-хлор-5-нитропиридин (регистрационный № CAS 5470-17-7) (7,3 г, 30,74 ммоль) добавляли по каплям при 0°С и перемешивали в течение двух часов при 25°С. Воду (60 мл) добавляли к реакционной смеси и экстрагировали этилацетатом (3×100 мл). Объединенные органические слои промывали водой и солевым раствором, сушил над Na2SO4 и выпаривали при пониженном давлении, что давало неочищенный остаток (12 г). Неочищенный остаток очищали с помощью колоночной хроматографии (2% этилацетат/гексан), что давало требуемый продукт (2,06 г, 32%) в виде светло-желтого твердого вещества, и 1,7 г не вступившего в реакцию 3-бром-2-хлор-5-нитропиридина выделяли. МС (ЖХ/МС): не отвечает, ЯМР находится в соответствии со структурой: 1H-ЯМР (400 МГц, CDCl2):δ 0.41 (m, 2H), 0.65 (m, 2H), 1.32 (m, 1H), 4.34 (d, 2H), 8.60 (d, 1H), 8.96 (d, 1H).
Пример С
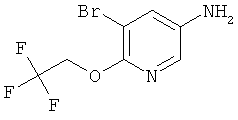
Получение 5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-иламина
К раствору 3-бром-5-нитро-2-(2,2,2-трифтор-этокси)-пиридина (2,4 г, 7,97 ммоль) в этаноле (100 мл) добавляли HCl (0,3 мл) и хлорид олова (10,5 г, 55,81 ммоль) при 25°С и реакционную смесь перемешивали в течение 4 часов при 25°С. После полного расхода исходного вещества (контроль с помощью ТСХ) этанол выпаривали при пониженном давлении, разбавляли этилацетатом, нейтрализовали водным раствором Na2CO3 и фильтровали через прокладку из целита. Органический слой отделяли, и водный слой дополнительного экстрагировали этилацетатом (2×120 мл). Объединенные органические слои промывали солевым раствором, сушили над Na2SO4 и выпаривали в вакууме, что давало требуемое соединение (2,1 г, 97%) в виде коричневой жидкости. Его использовали как таковое на следующей стадии без дополнительной очистки. МС (ЖХ/МС): не отвечает, ЯМР находится в соответствии со структурой: 1H-ЯМР (400 МГц, CDCl3): δ 4.70 (m, 2H), 7.30 (d, 1H), 7.54 (d, 1H).
Пример D

Получение 5-бром-6-циклопропилметокси-пиридин-3-иламина
К раствору 3-бром-2-циклопропилметокси-5-нитро-пиридина (600 мг, 2,19 ммоль) в метаноле (30 мл) добавляли воду (15 мл), цинковую пыль (1 г, 15,37 ммоль) и хлорид аммония (1,28 г, 24,09 ммоль) при 25°С, и реакционную смесь перемешивали в течение 45 минут при 25°С. После полного расхода исходного веществ (контроль с помощью ТСХ) реакционную смесь фильтровали через прокладку из целита, и фильтрат выпаривали при пониженном давлении, что давало неочищенный остаток. Остаток растворяли в дихлорметане и промывали водой и солевым раствором. Органическую часть сушили над Na2SO4 и выпаривали, что давало соединение (507 мг, 95%). Это соединение использовали на следующей стадии без дополнительной очистки. МС (ЖХ/МС): 244,0 (М+Н).
Пример Е

Получение 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламина
К раствору 5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-иламина (2,1 г, 7,74 ммоль) в ДМЭ, этаноле, воде (3:1:1) (50 мл) в закрытой пробирке добавляли 4-хлорфенилбороновую кислоту (регистрационный № CAS 1679-18-1) (1,8 г, 11,62 ммоль) и фосфат калия (4,9 г, 23,22 ммоль), и затем реакционную смесь продували азотов в течение 15 минут. Затем добавляли Pd(dppf)2Cl2 (651 мг, 0,93 ммоль) к реакционной смеси и нагревали при 100°С в течение 4 часов. Реакционную смесь фильтровали, и осадок на фильтре промывали этилацетатом (3×20 мл). Органический слой промывали водой, солевым раствором, сушили над Na2SO4 и выпаривали в вакууме, что давало неочищенное вещество (1,9 г). Неочищенное вещество очищали с помощью колоночной хроматографии (20-25% этилацетат/гексан), что давало требуемый продукт (1,3 г, 56%) в виде коричневой жидкости. МС (ЖХ/МС): 303,0 (М+Н).
Пример F
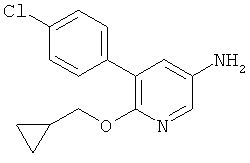
Получение 5-(4-хлор-фенил)-6-циклопропилметокси-пиридин-3-иламина
Указанное в заголовке соединение синтезировали по аналогии с Примером Е, используя 5-бром-6-циклопропилметокси-пирдин-3-иламин и 4-хлорфенилбороновую кислоту (44%). МС (ЖХ/МС): 275,2 (М+Н).
Пример G
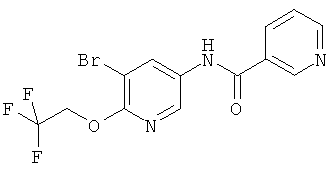
Получение N-[5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-никотинамида
К раствору никотиновой кислоты (454 мг, 3,69 ммоль) в ДМФА (33 мл) последовательно добавляли TBTU (1,18 г, 3,69 ммоль), N,N-диизопропилэтиламин (3,16 мл, 18,4 ммоль) и 5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (1 г, 3,69 ммоль). Коричневую смесь перемешивали в атмосфере аргона в течение 3 часов при комнатной температуре. После выпаривания ДМФА коричневое масло разделяли между этилацетатом (50 мл) и 1 М NaOH (30 мл). Водные слои повторно экстрагировали этилацетатом (1×50 мл). Органические части промывали водой (2×25 мл) и солевым раствором (25 мл), затем сушили над MgSO4 и концентрировали в вакууме. Неочищенное вещество очищали с помощью флэш-хроматографии (силикагель, 40 г, 10% до 100% этилацетата в гептане), что давало требуемый продукт в виде белого твердого вещества (580 мг; 42%); МС (ЭИ): 376,1; 378,0 (М+Н).
Пример 1

Получение [5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида пентановой кислоты
К раствору 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламина (50 мг, 0,165 ммоль) и валериановой кислоты (36 мг, 0,247 ммоль) в ДМФА (5 мл) добавляли N-метил-морфолин (51 мг, 0,5 ммоль) и HBTU (94 мг, 0,247 ммоль), и реакционную смесь перемешивали в течение 16 часов при 25°С. Реакционную смесь выливали в воду и экстрагировали этилцетатом (3×20 мл). Объединенную этилацетатную часть сушили над Na2SO4 и выпаривали, что давало неочищенное вещество (60 мг). Неочищенное вещество очищали с помощью преп. ВЭЖХ и требуемый продукт (30 мг, 47%) получали в виде липкого белого твердого вещества. МС (ЖХ/МС): 387,2 (М+Н).
Пример 2

Получение N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-бензамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и бензойную кислоту в качестве исходных веществ, МС (ЖХ/МС): 407,2 (М+Н).
Пример 3
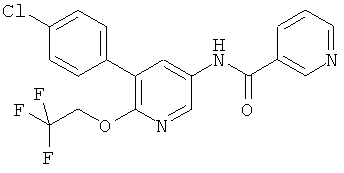
Получение N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-никотинамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и никотиновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 408,0 (М+Н).
Пример 4
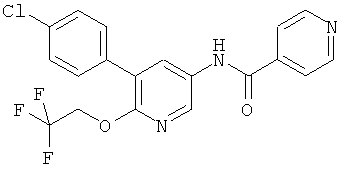
Получение N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-изоникотинамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и изоникотиновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 408,0 (М+Н).
Пример 5

Получение N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-ацетамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и уксусную кислоту в качестве исходных веществ, МС (ЖХ/МС): 345,0 (М+Н).
Пример 6

Получение N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-бутирамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и н-бутановую кислоту в качестве исходных веществ, МС (ЖХ/МС): 373,2 (М+Н).
Пример 7

Получение [5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида пиридин-2-карбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и пиридин-2-карбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 408,0 (М+Н).
Пример 8

Получение N-[5-(4-хлор-фенил)-6-циклопропилметокси-пиридин-3-ил]-бензамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-циклопропилметокси-пиридин-3-иламин и бензойную кислоту в качестве исходных веществ, МС (ЖХ/МС): 379,2 (М+Н).
Пример 9
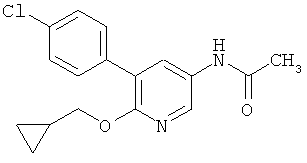
Получение N-[5-(4-хлор-фенил)-6-циклопропилметокси-пиридин-3-ил]-ацетамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-циклопропилметокси-пиридин-3-иламин и уксусную кислоту в качестве исходных веществ, МС (ЖХ/МС): 317,2 (М+Н).
Пример 10

Получение N-[5-(4-хлор-фенил)-6-циклопропилметокси-пиридин-3-ил]-никотинамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-циклопропилметокси-пиридин-3-иламин и никотиновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 380,2 (М+Н).
Пример 11

Получение N-[5-(4-хлор-фенил)-6-циклопропилметокси-пиридин-3-ил]-изоникотинамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-циклопропилметокси-пиридин-3-иламин и изоникотиновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 380,2 (М+Н).
Пример 12
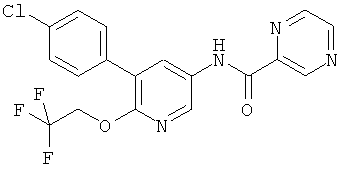
Получение [5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида пиразин-2-карбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 2-пиразинкарбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 409,6 (М+Н).
Пример 13
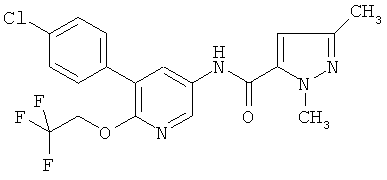
Получение [5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 2,5-диметил-2H-пиразол-3-карбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 1,3-диметил-1H-пиразол-5-карбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 425,6 (М+Н).
Пример 14

Получение [5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 3-метил-изоксазол-4-карбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 3-метил-4-изоксазолкарбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 412,2 (М+Н).
Пример 15

Получение [5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 1-метил-1H-пиразол-3-карбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 1-метил-1H-пиразол-3-карбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 411,0 (М+Н).
Пример 16

Получение [5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 5-метил-3-изоксазолкарбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 5-метил-3-изоксазолкарбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 412,2 (М+Н).
Пример 17
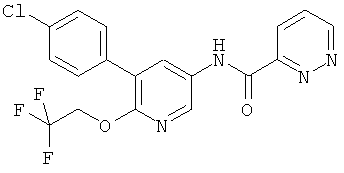
Получение [5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 3-пиридазинкарбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 3-пиридазинкарбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 409,0 (М+Н).
Пример 18

Получение амида N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-3-метил-4-пиридинкарбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 3-метил-4-пиридинкарбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 422,0 (М+Н).
Пример 19
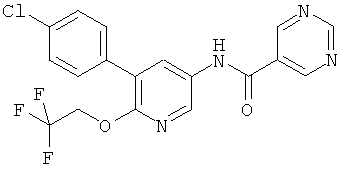
Получение [5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 5-пиримидинкарбононой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 5-пиримидинкарбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 409,0 (М+Н).
Пример 20

Получение [5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 1-метил-1H-пиразол-5-карбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 1-метил-1H-пиразол-5-карбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 409,2 (М-Н).
Пример 21
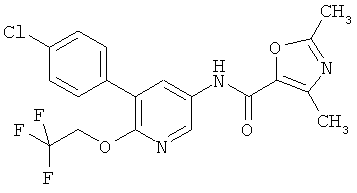
Получение [5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 2,4-диметил-5-оксазолкарбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 2,4-диметил-5-оксазолкарбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 426,2 (М+Н).
Пример 22

Получение [5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 5-изотиазолкарбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 5-изотиазолкарбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 414,0 (М+Н).
Пример 23

Получение [5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 5-метил-1H-пиразол-3-карбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 5-метил-1Н-пиразол-3-карбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 409,2 (М-Н).
Пример 24

Получение [5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 1H-пиразол-3-карбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 1H-пиразол-3-карбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 395,2 (М-Н).
Пример 25
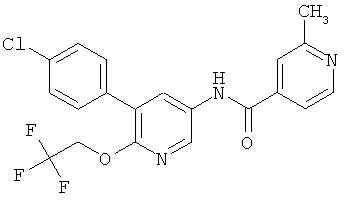
Получение амида N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-2-метил-4-пиридинкарбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 2-метил-4-пиридинкарбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 422,0 (М+Н).
Пример 26
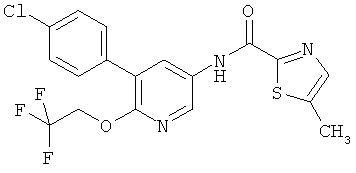
Получение [5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 6-метил-2-тиазол-карбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 5-метил-2-тиазолкарбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС):428,2 (М+Н).
Пример 27
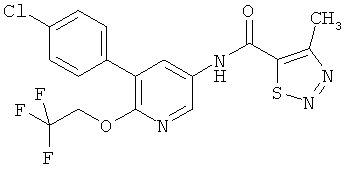
Получение [5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 4-метил-1,2,3-тиадиазол-5-карбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 4-метил-1,2,3-тиадиазол-5-карбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 429,2 (М+Н).
Пример 28

Получение амида N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-6-метил-3-пиридинкарбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 6-метил-3-пиридинкарбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 420,4 (М-Н).
Пример 29

Получение амида N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-2-метил-3-пиридинкарбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 2-метил-3-пиридинкарбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 421,8 (М+Н).
Пример 30

Получение [5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 5-изоксазолкарбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 5-изоксазолкарбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 398,0 (М+Н).
Пример 31
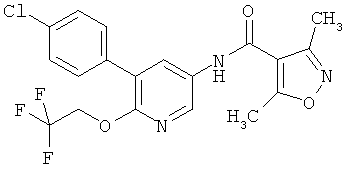
Получение [5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 3,5-диметил-4-изоксазолкарбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 3,5-диметил-4-изоксазолкарбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 426,2 (М+Н).
Пример 32
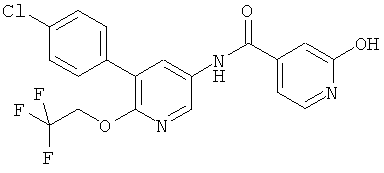
Получение амида N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-1,2-дигидро-2-оксо-4-пиридинкарбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 1,2-дигидро-2-оксо-4-пиридинкарбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 424,0 (М+Н).
Пример 33
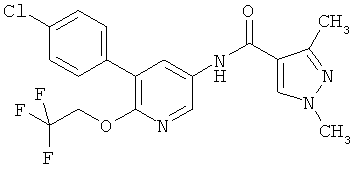
Получение [5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 1,3-диметил-1H-пиразол-4-карбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 1,3-диметил-1H-пиразол-4-карбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 425,0 (М+Н).
Пример 34
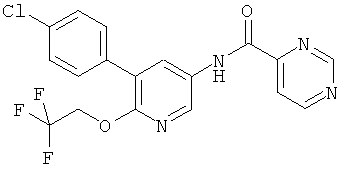
Получение [5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 4-пиримидинкарбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 4-пиримидинкарбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 409,0 (М+Н).
Пример 35

Получение [5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 2-тиазолкарбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 2-тиазолкарбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 414,0 (М+Н).
Пример 36
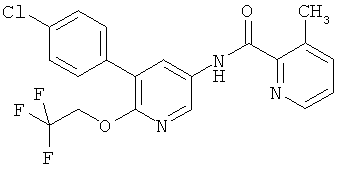
Получение [5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 3-метил-2-пиридинкарбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 3-метил-2-пиридинкарбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 422,0 (М+Н).
Пример 37

Получение [5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 5-метил-4-оксазолкарбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 5-метил-4-оксазолкарбоновую кислоту в качестве исходных веществ, МС (ЖХ/МС): 412,2 (М+Н).
Пример 38

Получение N-(5-(3,4-диметилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамида
В 25 мл закрытой пробирке N-(5-бром-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамид (200 мг, 532 мкмоль) объединяли с толуолом (11 мл). В атмосфере аргона добавляли 3,4-диметилбензолбороновую кислоту (160 мг, 1,06 ммоль), водный раствор карбоната натрия (2 М, 0,53 мл) и Pd(dppf)2Cl2 (12 мг, 0,016 ммоль). После двух часов при 90°С темно-красную суспензию охлаждали до комнатной температуры, разбавляли этилацетатом (10 мл) и промывали водой (10 мл) и солевым раствором (10 мл). Водный слой повторно экстрагировали этилацетатом (15 мл). Органические слои сушили над MgSO4 и концентрировали в вакууме. Кристаллизация из этилацетата/гептана (5 мл, 1/2) давала белое твердое вещество (96 мг), фильтрат выпаривали досуха и очищали с помощью колоночной хроматографии (силикагель, 20 г, 10% до 100% этилацетата в гептане), что давало вторую часть требуемого продукта в виде белого твердого вещества (139 мг). Общий выход составил 65%; МС (ЭИ): 402,3 (М+Н).
Пример 39

Получение N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамида
В 25 мл закрытой пробирке N-(5-бром-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамид (520 мг, 1,38 ммоль) объединяли с толуолом (20 мл). В атмосфере аргона добавляли 4-хлор-3-метилфенилбороновую кислоту (471 мг, 2,77 ммоль), водный раствор карбоната натрия (2 М, 1,38 мл) и Pd(dppf)2Cl2 (30 мг, 0,041 ммоль). После двух часов при 90°C темно-красную суспензию охлаждали до комнатной температуры, разбавляли этилацетатом (10 мл) и промывали водой (10 мл) и солевым раствором (10 мл). Водный слой повторно экстрагировали этилацетатом (15 мл). Орагнические слои сушили над MgSO4 и концентрировали в вакууме. Неочищенное вещество (760 мг) очищали с помощью флэш-хроматографии (силикагель, 20 г, 20% до 100% этилацетата в гептане), что давало указанное в заголовке соединение в виде светло-коричневого твердого вещества (575 мг, 98%); МС (ЭИ): 422,8 (М+Н).
Пример 40

Получение [5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 5-гидрокси-пиридин-2-карбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 5-гидрокси-2-пиридинкарбоновую кислоту (CAN 15069-92-8) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 96,3%, 422,0523 (М-Н)-.
Пример 41
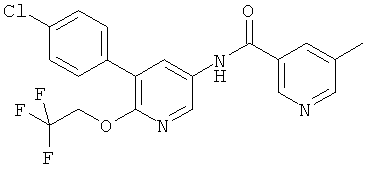
Получение N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-5-метилникотинамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 1, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин и 5-метил-3-пиридинкарбоновую кислоту (CAN 3222-49-9) в качестве исходных веществ; МС (ЭИ) 422,1 (М+Н)+.
Пример 42

Получение (S)-N-(5-(4-хлорфенил)-6-(1,1,1-трифторпропан-2-илокси)пиридин-3-ил)пиридазин-3-карбоксамида
а) 5-Хлор-3-(4-хлор-фенил)-2-фтор-пиридин

Смесь 3-бром-6-хлор-2-фтор-пиридина (CAN 884494-87-5; 2,0 г, 9,50 ммоль), 4-хлорфенилбороновой кислоты (CAN 1679-18-1; 1,5 г, 9,50 ммоль); тетракис(трифенилфосфин)-палладия (0,55 г, 0,48 ммоль) и карбоната калия (2,6 г, 19 ммоль) в воде (50 мл) и ТГФ (50 мл) нагревали с обратным холодильником в течение 18 часов. Реакционную смесь охлаждали, разбавляли этилацетатом, фазы разделяли и водную фазу экстрагировали этилацетатом. Органические фазы объединяли, сушили с MgSO4 и растворитель удаляли в вакууме. Остаток очищали с помощью колоночной хроматографии (на силикагеле с градиентом гептан до гептан:этилацетат = 9:1), что давало указанный в заголовке продукт (2,2 г, 95%) в виде белого твердого вещества; МС (ЭСИ): 241,0 (М)+.
b) 5-Хлор-3-(4-хлор-фенил)-2-((5)-2,2,2-трифтор-1-метил-этокси)-пиридин

К смеси 1,133 г (S)-1,1,1-трифтор-2-пропанола в 10 мл безводного ДМФА добавляли 397 мг гидрида натрия (60%) и смесь перемешивали при комнатной температуре в течение 30 минут. Полученный в результате раствор добавляли по каплям при к.т. к раствору 2,185 г 5-хлор-3-(4-хлор-фенил)-2-фтор-пиридина в 20 мл безводного ДМФА. Затем реакционную смесь перемешивали при комнатной температуре в течение 2 часов. Полученную в результате светло-желтую смесь разделяли между водой и этилацетатом, фазы разделяли. Органическую фазу сушили над MgSO4 и очищали с помощью хроматографии на силикагеле с градиентом гептан до гептан:этилацетат=9:1, что давало 2,330 г (76,80%) указанного в заголовке соединения в виде бесцветной жидкости; МС (ЭСИ) 336,1 (М+Н)+.
с) (S)-Метил 5-(4-хлорфенил)-6-(1,1,1-трифторпропан-2-илокси)никотинат
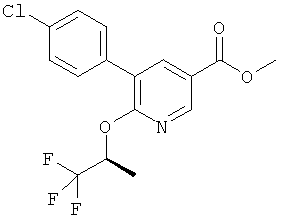
К раствору 2,42 г 5-хлор-3-(4-хлор-фенил)-2-((5)-2,2,2-трифтор-1-метил-этокси)-пиридина в 50 мл метанола добавляли 1,09 г триэтиламина и 0,484 г PdCl2.dppf.CH2Cl2. Смесь нагревали до 150°С в атмосфере 70 бар монооксида углерода в течение 20 часов. Реакционную смесь охлаждали до комнатной температуры. Твердые вещества удаляли фильтрованием, маточный раствор выпаривали и очищали с помощью хроматографии на силикагеле, используя градиент гептан до гептан:этилацетат 85:15, что давало 0,862 г (33%) указанного в заголовке соединения в виде светло-желтого масла; МС (ЭСИ) 359 (М+).
d) (5)-5-(4-Хлорфенил)-6-(1,1,1-трифторпропан-2-илокси)никотиновая кислота
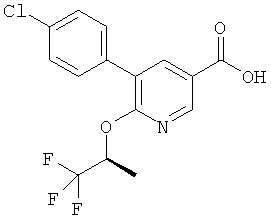
К раствору 0,860 г (S)-метил 5-(4-хлорфенил)-6-(1,1,1-трифторпропан-2-илокси)никотината в 9 мл тетрагидрофурана добавляли 3 мл 1 М раствора гидроксида лития в воде и смесь перемешивали при комнатной температуре в течение ночи. Растворитель выпаривали и остаток подкисляли, добавляя 1 М соляную кислоту до рН 2. Добавляли этилацетат и фазы разделяли. Органическую фазу сушили над MgSO4 и растворитель удаляли, что давало 830 мг (100%) указанного в заголовке соединения в виде светло-желтого твердого вещества; МС (ЭСИ) 344,1 (М-Н)-.
е) трет-Бутиловый эфир [5-(4-хлор-фенил)-6-((8)-2,2,2-трифтор-1-метил-этокси)-пиридин-3-ил]-карбаминовой кислоты

(S)-5-(4-Хлорфенил)-6-(1,1,1-трифторпропан-2-илокси)никотиновую кислоту (0,300 г, 868 мкмоль) суспендировали в трет-бутаноле (3,0 мл). ДФФА (358 мг, 282 мкл) и триэтиламин (87,8 мг, 120 мкл, 868 мкмоль) добавляли и реакционную смесь перемешивали при 100°С в течение ночи. Смесь охлаждали до комнатной температуры, экстрагировали этилацетатом и раствором карбоната натрия, органическую фазу сушили с MgSO4 и концентрировали в вакууме. Неочищенное вещество очищали с помощью флэш-хроматографии (силикагель, 20 г, от 5% до 25% этилацетата в гептане), что давало 0,36 г (99%) указанного в заголовке соединения в виде белого твердого вещества; МС (ЭИ) 417,3 (М+Н)+.
f) 5-(4-Хлор-фенил)-6-((8)-2,2,2-трифтор-1-метил-этокси)-пиридин-3-иламин

Трифторуксусную кислоту (2,74 г, 1,85 мл, 24,0 ммоль) добавляли к (S)-трет-бутил 5-(4-хлорфенил)-6-(1,1,1-трифторпропан-2-илокси)пиридин-3-илкарбамату (0,350 г, 840 мкмоль). Полученный в результате желтый раствор перемешивали при к.т. в течение 1 часа. Растворитель выпаривали. Остаток разделяли между этилацетатом и 1 М раствором Na2CO3, органическую фазу сушили с MgSO4 и концентрировали в вакууме. Неочищенное вещество очищали с помощью флэш-хроматографии (силикагель, 20 г, от 5% до 50% EtOAc в гептане), что давало 0,22 г (82%) указанного в заголовке соединения в виде светло-коричневого масла; МС (ЭИ) 317,1 (М+Н)+.
g) (S)-N-(5-(4-Хлорфенил)-6-(1,1,1-трифторпропан-2-илокси)пиридин-3-ил)пиридазин-3-карбоксамид
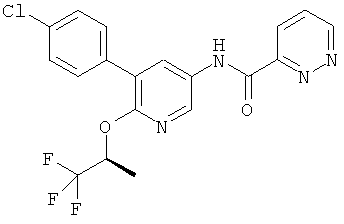
Пиридазин-3-карбоновую кислоту (CAN 2164-61-6; 43,1 мг, 347 мкмоль) суспендировали в ДМФА (1,0 мл). Добавляли TBTU (112 мг, 347 мкмоль), этилдиизопропиламин (102 мг, 131 мкл, 789 мкмоль) и 5-(4-хлор-фенил)-6-((S)-2,2,2-трифтор-1-метил-этокси)-пиридин-3-иламин (0,100 г, 316 мкмоль) и реакционную смесь перемешивали при комнатной температуре в течение 1 часа. Реакционную смесь экстрагировали этилацетатом и 1 М раствором лимонной кислоты; органическую фазу сушили с MgSO4 и концентрировали в вакууме. Неочищенное вещество очищали с помощью флэш-хроматографии (силикагель, 10 г, от 10% до 50% этилацетата в гептане), что давало 0,11 г (83%) указанного в заголовке соединения в виде белого твердого вещества; МС (ЭИ) 423,1 (М+Н)+.
Пример 43
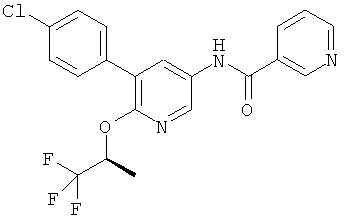
Получение (S)-N-(5-(4-хлорфенил)-6-(1,1,1-трифторпропан-2-илокси)пиридин-3-ил)никотинамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-(4-хлор-фенил)-6-((S)-2,2,2-трифтор-1-метил-этокси)-пиридин-3-иламин (пример 42f) и 3-пиридин-карбоновую кислоту (CAN 59-67-6) в качестве исходных веществ; МС (ЭИ) 422,0 (М+Н)+.
Пример 44
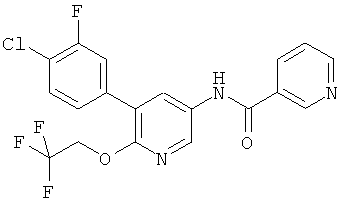
Получение N-(5-(4-хлор-3-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 39, используя N-[5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-никотинамид (пример G) и В-(4-хлор-3-фторфенил)-бороновую кислоту (CAN 137504-86-0) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 96,4%, 424,0482 (M-H)-.
Пример 45

Получение N-(5-(3-хлор-4-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 39, используя N-[5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-никотинамид (пример G) и В-(3-хлор-4-фторфенил)-бороновую кислоту (CAN 144432-85-9) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 98,0%, 424,0483 (М-Н)-.
Пример 46
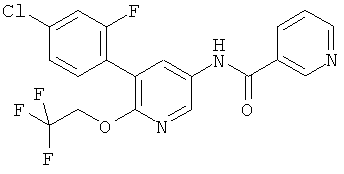
Получение N-(5-(4-хлор-2-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 39, используя N-[5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-никотинамид (пример G) и В-(4-хлор-2-фторфенил)-бороновую кислоту (CAN 160591-91-3) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 97,2%, 424,0483 (М-Н)-.
Пример 47

Получение N-(5-(4-этилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 39, используя N-[5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-никотинамид (пример G) и В-(4-этилфенил)-бороновую кислоту (CAN 63139-21-9) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 100%, 402,1409 (М+Н)+.
Пример 48
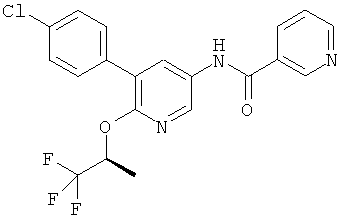
Получение (S)-N-(6-(4-хлорфенил)-5-(1,1,1-трифторпропан-2-илокси)пиразин-2-ил)никотинамида
а) Метиловый эфир 6-(4-хлор-фенил)-5-((S)-2,2,2-трифтор-1-метил-этокси)-пиразин-2-карбоновой кислоты
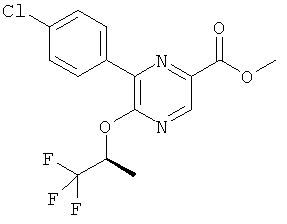
Метиловый эфир 5-бром-6-(4-хлорфенил)-2-пиразинкарбоновой кислоты (CAN 960247-79-4, 2,420 г, 7,39 ммоль) растворяли в безводном ДМСО (25 мл). Добавляли карбонат цезия (4,41 г, 8,13 ммоль) и (8)-1,1,1-трифторпропан-2-ол (927 мг, 8,13 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 2 часов. Смесь разделяли между водой и этилацетатом; органическую фазу сушили с MgSO4 и концентрировали в вакууме. Неочищенный остаток очищали с помощью флэш-хроматографии (силикагель, 100 г, от 10% до 50% этилацетата в гептане), что давало 2,53 г (95%) указанного в заголовке соединения в виде желтого масла; МС (ЭИ) 361,1 (М+Н)+.
b) 6-(4-Хлор-фенил)-5-((S)-2,2,2-трифтор-1-метил-этокси)-пиразин-2-карбоновая кислота
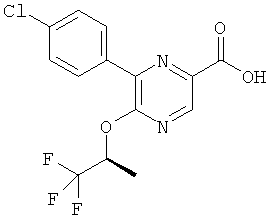
Указанное в заголовке соединение синтезировали по аналогии с Примером 42d, используя метиловый эфир 6-(4-хлор-фенил)-5-((S)-2,2,2-трифтор-1-метил-этокси)-пиразин-2-карбоновой кислоты в качестве исходного вещества; МС (ЭСИ) 345,0 (М-Н)-.
с) трет-Бутиловый эфир [6-(4-хлор-фенил)-5-((S)-2,2,2-трифтор-1-метил-этокси)-пиразин-2-ил]-карбаминовой кислоты
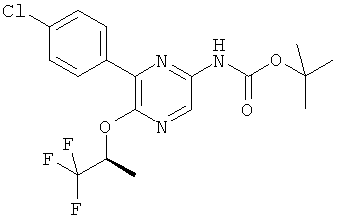
Указанное в заголовке соединение синтезировали по аналогии с Примером 42е, используя 6-(4-хлор-фенил)-5-((S)-2,2,2-трифтор-1-метил-этокси)-пиразин-2-карбоновую кислоту в качестве исходного вещества; МС (ЭИ) 418,2 (М+Н)+.
d) 6-(4-Хлор-фенил)-5-((S)-2,2,2-трифтор-1-метил-этокси)-пиразин-2-иламин
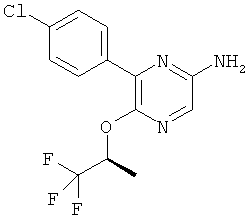
Указанное в заголовке соединение синтезировали по аналогии с Примером 42f, используя трет-бутиловый эфир [6-(4-хлор-фенил)-5-((S)-2,2,2-трифтор-1-метил-этокси)-пиразин-2-ил]-карбаминовой кислоты в качестве исходного вещества; МС (ЭИ) 318,0 (М+Н)+.
е) (S)-N-(6-(4-Хлорфенил)-5-(1,1,1-трифторпропан-2-илокси)пиразин-2-ил)никотинамид

6-(4-Хлор-фенил)-5-((S)-2,2,2-трифтор-1-метил-этокси)-пиразин-2-иламин (0,100 г, 315 мкмоль) растворяли в безводном пиридине (1,0 мл), добавляли никотиноилхлорида гидрохлорид (61,6 мг, 346 мкмоль) и суспензию перемешивали при 140°С в течение 10 минут при микроволновом излучении. Растворитель выпаривали и неочищенное вещество очищали с помощью флэш-хроматографии (силикагель, 10 г, от 0% до 50% CH2Cl2/МеОН/NH3 9/1/0,1), что давало 0,121 г (91%) указанного в заголовке соединения в виде белого твердого вещества; ЖХ-МС (площаль УФ пика / ЭСИ) 100%, 423,0821 (М+Н)+.
Пример 49

Получение N-(6-(4-хлорфенил)-5-(2,2,2-трифторэтокси)пиразин-2-ил)никотинамида
а) Метиловый эфир 6-(4-хлор-фенил)-5-(2,2,2-трифтор-этокси)-пиразин-2-карбоновой кислоты

Указанное в заголовке соединение синтезировали по аналогии с Примером 48а, используя метиловый эфир 5-бром-6-(4-хлорфенил)-2-пиразинкарбоновой кислоты (CAN 960247-79-4) и 2,2,2-трифторэтанол в качестве исходных веществ; МС (ЭИ) 347,1 (М+Н)+.
b) 6-(4-Хлор-фенил)-5-(2,2,2-трифтор-этокси)-пиразин-2-карбоновая кислота

Указанное в заголовке соединение синтезировали по аналогии с Примером 42d, используя метиловый эфир 6-(4-хлор-фенил)-5-(2,2,2-трифтор-этокси)-пиразин-2-карбоновой кислоты в качестве исходного вещества; МС (ЭСИ) 331,1 (М-Н)-.
с) трет-Бутил о вы и эфир [6-(4-хлор-фенил)-5-(2,2,2-трифтор-этокси)-пиразин-2-ил]-карбаминовой кислоты

Указанное в заголовке соединение синтезировали по аналогии с Примером 42е, используя 6-(4-хлор-фенил)-5-(2,2,2-трифтор-этокси)-пиразин-2-карбоновую кислоту в качестве исходного вещества; МС (ЭИ) 404,3 (М+Н)+.
d) 6-(4-Хлор-фенил)-5-(2,2,2-трифтор-этокси)-пиразин-2-иламин

Указанное в заголовке соединение синтезировали по аналогии с Примером 42f, используя трет-бутиловый эфир [6-(4-хлор-фенил)-5-(2,2,2-трифтор-этокси)-пиразин-2-ил]-карбаминовой кислоты в качестве исходного вещества; МС (ЭИ) 304,0 (М+Н)+.
е) N-(6-(4-Хлорфенил)-5-(2,2,2-трифторэтокси)пиразин-2-ил)никотинамид

Указанное в заголовке соединение синтезировали по аналогии с Примером 48е, используя 6-(4-хлор-фенил)-5-(2,2,2-трифтор-этокси)-пиразин-2-иламин (Пример 49d) и никотиноилхлорида гидрохлорид в качестве исходных веществ; ЖХ-МС (площаль УФ пика / ЭСИ) 95,7%, 407,0532 (М-Н)-.
Пример 50
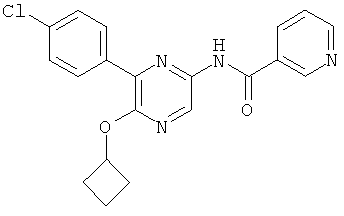
Получение N-(6-(4-хлорфенил)-5-циклобутоксипиразин-2-ил)никотинамида
а) 6-(4-Хлор-фенил)-5-циклопропилметокси-пиразин-2-карбоновая кислота
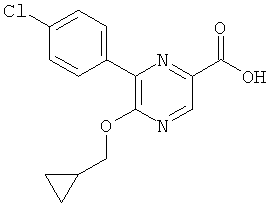
Циклопропилметанол (1,54 г, 1,73 мл, 21,3 ммоль) разбавляли безводным ДМФА (15 мл); частями добавляли гидрид натрия (512 мг, 21,3 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 15 минут. Полученный в результате раствор медленно добавляли при <5°С к раствору 5-бром-6-(4-хлорфенил)пиразин-2-карбоновой кислоты (CAN 960247-80-7; 3,040 г, 9,7 ммоль) в безводном ДМФА (15 мл). Реакционную смесь перемешивали при комнатной температуре в течение 30 минут; добавляли воду и смесь подкисляли 1 М раствором HCl до рН 2. Смесь экстрагировали этилацетатом; органические фазы объединяли, сушили с MgSO4 и концентрировали в вакууме. Неочищенное вещество еще содержало исходное вещество, и его растворяли снова в 15 мл ДМФА; добавляли раствор циклопропилметанола (1,05 г, 1,18 мл, 14,5 ммоль) и гидрида натрия (582 мг, 14,5 ммоль) в 15 мл ДМФА и смесь перемешивали при комнатной температуре в течение 3 часов. Добавляли воду и реакционную смесь подкисляли 1 М раствором HCl до рН 2; продукт осаждали, что давало 2,55 г (86%) указанного в заголовке соединения в виде светло-желтого твердого вещества; МС (ЭСИ) 303,2 (М-Н)-.
b) трет-Бутиловый эфир [6-(4-хлор-фенил)-5-циклопропилметокси-пиразин-2-ил]-карбаминовой кислоты

Указанное в заголовке соединение синтезировали по аналогии с Примером 42е, используя 6-(4-хлор-фенил)-5-циклопропилметокси-пиразин-2-карбоновую кислоту (Пример 50а) в качестве исходного вещества; МС (ЭИ) 376,3 (М+Н)+.
с) 6-(4-Хлор-фенил)-5-циклобутокси-пиразин-2-иламин

ТФК (14,8 г, 10 мл, 130 ммоль) добавляли к трет-бутиловому эфиру [6-(4-хлор-фенил)-5-циклопропилметокси-пиразин-2-ил]-карбаминовой кислоты (Пример 50b, 1,365 г, 3,63 ммоль). Полученный в результате желтый раствор перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали и остаток разделяли между этилацетатом и 1 М раствором Na2CO3; органические фазы объединяли, сушили с MgSO4 и концентрировали в вакууме. Неочищенное вещество очищали с помощью флэш-хроматографии (силикагель, 100 г, от 10% до 50% этилацетата в гептане; затем этилацетат/метанол 9/1, что давало 0,133 г (13%) указанного в заголовке соединения (в ходе перегруппировки) в виде желтого масла; МС (ЭИ) 276,1 (М+Н)+.
d) N-(6-(4-Хлорфенил)-5-циклобутоксипиразин-2-ил)никотинамид

Указанное в заголовке соединение синтезировали по аналогии с Примером 48е, используя 6-(4-хлор-фенил)-5-циклобутокси-пиразин-2-иламин (Пример 50с) и никотиноилхлорида гидрохлорид в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 97,4%, 381,1096 (М+Н).
Пример 51
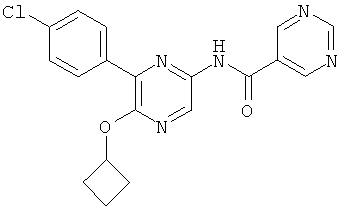
Получение N-(6-(4-хлорфенил)-5-циклобутоксипиразин-2-ил)пиримидин-5-карбоксамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 6-(4-хлор-фенил)-5-циклобутокси-пиразин-2-иламин (Пример 50с) и 5-пиримидинкарбоновую кислоту (CAN 4595-61-3) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 96,3%, 482,1073 (М+Н)+.
Пример 52
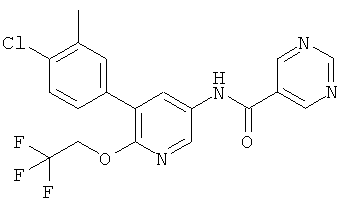
Получение N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиримидин-5-карбоксамида
а) [5-Бром-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид пиримидин-5-карбоновой кислоты

Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (Пример D) и 5-пиримидинкарбоновую кислоту (CAN 4595-61-3) в качестве исходных веществ; МС (ЭСИ) 375,2 (М-Н)-.
b) N-(5-(4-Хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиримидин-5-карбоксамид

Указанное в заголовке соединение синтезировали по аналогии с Примером 39, используя [5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид пиримидин-5-карбоновой кислоты (Пример 52а) и В-(4-хлор-3-метилфенил)-бороновую кислоту (CAN 161950-10-3) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 100%, 421,0698 (М-Н)-.
Пример 53
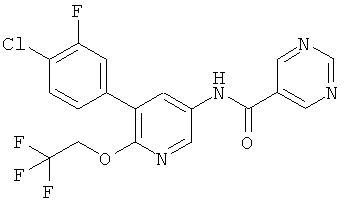
Получение N-(5-(4-хлор-3-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиримидин-5-карбоксамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 39, используя [5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид пиримидин-5-карбоновой кислоты (Пример 52 а) и В-(4-хлор-3-фторфенил)-бороновую кислоту (CAN 137504-86-0) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 97,7%, 425,0448 (М-Н)-.
Пример 54
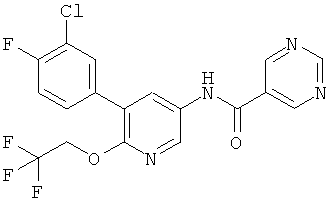
Получение N-(5-(3-хлор-4-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиримидин-5-карбоксамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 39, используя [5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид пиримидин-5-карбоновой кислоты (Пример 52а) и В-(3-хлор-4-фторфенил)-бороновую кислоту (CAN 144432-85-9) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 93,5%, 425,0449 (М-Н)-.
Пример 55

Получение N-(5-(4-хлор-2-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиримидин-5-карбоксамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 39, используя [5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид пиримидин-5-карбоновой кислоты (Пример 52а) и В-(4-хлор-2-фторфенил)-бороновую кислоту (CAN 160591-91-3) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 92,2%, 425,0446 (М-Н)-.
Пример 56
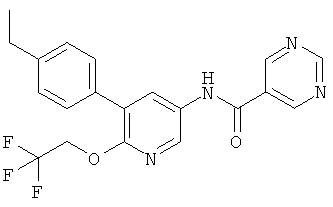
Получение N-(5-(4-этилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиримидин-5-карбоксамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 39, используя [5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид пиримидин-5-карбоновой кислоты (Пример 52а) и В-(4-этилфенил)-бороновую кислоту (CAN 63139-21-9) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 100%, 403,1384 (М+Н)+.
Пример 57
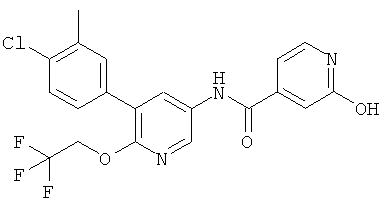
Получение N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-2-гидроксиизоникотинамида
а) 5-(4-Хлор-3-метил-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин

Указанное в заголовке соединение синтезировали по аналогии с Примером 39, используя 5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (Пример D) и В-(4-хлор-3-метилфенил)-бороновую кислоту (CAN 161950-10-3) в качестве исходных веществ; МС (ЭИ) 317,0 (М+H)+.
b) N-(5-(4-Хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-2-гидроксиизоникотинамид
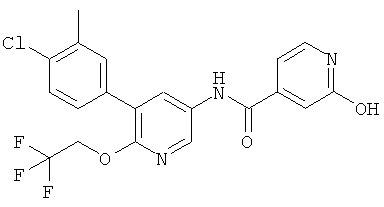
Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-(4-хлор-3-метил-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (Пример 57а) и 1,2-дигидро-2-оксо-4-пиридинкарбоновую кислоту (CAN 22282-72-0) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 100%, 436,0689 (М-Н)-.
Пример 58

Получение N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-1,3-диметил-1Н-пиразол-4-карбоксамида
а) [5-Бром-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид 1,3-диметил-1Н-пиразол-4-карбоновой кислоты

Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (Пример D) и 1,3-диметил-1H-пиразол-4-карбоновую кислоту (CAN 78703-53-4) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 100%, 393,0063 (М-Н)-.
b) N-(5-(4-Хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-1,3-диметил-1H-пиразол-4-карбоксамид

Указанное в заголовке соединение синтезировали по аналогии с Примером 39, используя [5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид 1,3-диметил-1H-пиразол-4-карбоновой кислоты (Пример 58а) и В-(4-хлор-3-метилфенил)-бороновую кислоту (CAN 161950-10-3) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 96,1%, 439,1154 (М+Н)+.
Пример 59

Получение N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-2,4-дифторникотинамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-(4-хлор-3-метил-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (Пример 57а) и 2,4-дифтор-3-пиридинкарбоновую кислоту (CAN 849937-90-2) в качестве исходных веществ; МС (ЭИ) 458,2 (М+Н)+.
Пример 60
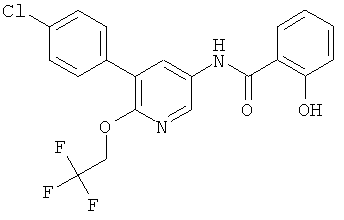
Получение N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-2-гидрокси-бензамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (Пример Е) и 2-гидрокси-бензойную кислоту (CAN 69-72-7) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 97,7%, 421,5080 (М-Н)-.
Пример 61

Получение N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-5-цианоникотинамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-(4-хлор-3-метил-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (Пример 57а) и 5-циано-3-пиридинкарбоновую кислоту (CAN 887579-62-6) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 98,7%, 445,0693 (М-Н)-.
Пример 62
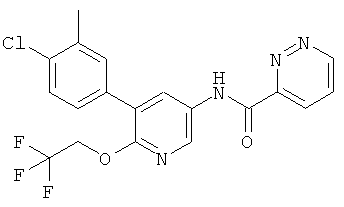
Получение N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиридазин-3-карбоксамида
а) [5-Бром-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид пиридазин-3-карбоновой кислоты
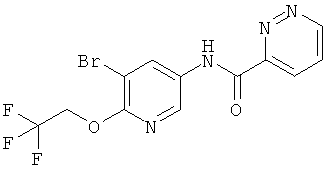
Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (Пример D) и 3-пиридазинкарбоновую кислоту (CAN 2164-61-6) в качестве исходных веществ; МС (ЭСИ) 375,2 (М-Н)-.
b) N-(5-(4-Хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиридазин-3-карбоксамид
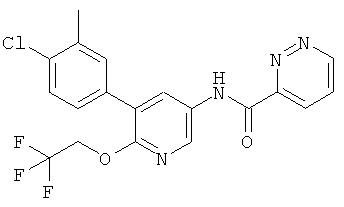
Указанное в заголовке соединение синтезировали по аналогии с Примером 39, используя [5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид пиридазин-3-карбоновой кислоты (Пример 62 а) и В-(4-хлор-3-метилфенил)-бороновую кислоту (CAN 161950-10-3) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 94,2%, 423,0828 (М+Н)+.
Пример 63
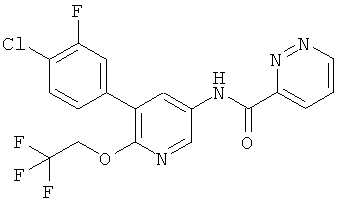
Получение N-(5-(4-хлор-3-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиридазин-3-карбоксамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 39, используя [5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид пиридазин-3-карбоновой кислоты (Пример 62а) и В-(4-хлор-3-фторфенил)-бороновую кислоту (CAN 137504-86-0) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 100%, 425,0438 (М-Н)-.
Пример 64

Получение N-(5-(4-хлор-2-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиридазин-3-карбоксамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 39, используя [5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид пиридазин-3-карбоновой кислоты (Пример 62а) и В-(4-хлор-2-фторфенил)-бороновую кислоту (CAN 160591-91-3) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 98,7%, 427,0587 (М+Н)+.
Пример 65

Получение N-(5-(4-этилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиридазин-3-карбоксамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 39, используя [5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амид пиридазин-3-карбоновой кислоты (Пример 62 а) и В-(4-этилфенил)-бороновую кислоту (CAN 63139-21-9) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 98,9%, 403,1386 (М+Н)+.
Пример 66
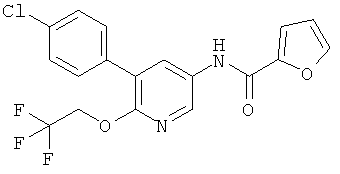
Получение N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)фуран-2-карбоксамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (Пример Е) и 2-фуранкарбоновую кислоту (CAN 88-14-2) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 98,0%, 397,0566 (М+Н)+.
Пример 67

Получение N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)фуран-3-карбоксамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (Пример Е) и 3-фуранкарбоновую кислоту (CAN 488-93-7) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 98,2%, 395,0414 (М-Н)-.
Пример 68

Получение N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-5-метилфуран-2-карбоксамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (Пример Е) и 5-метил-2-фуранкарбоновую кислоту (CAN 1917-15-3) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 98,0%, 409,574 (М-Н)-.
Пример 69

Получение N-(5-(4-хлор-3-метилфенил)-6-(2-метоксиэтокси)пиридин-3-ил)бензамида
а) 3-Бром-2-(2-метокси-этокси)-5-нитро-пиридин

К раствору 2-метоксиэтанола (8,81 г, 9,13 мл, 116 ммоль) в безводном ТГФ (150 мл) добавляли гидрид натрия (4,63 г, 116 ммоль) в атмосфере азота при 5°С или ниже и реакционную смесь перемешивали при 25°С в течение 1 часа. Затем добавляли по каплям 3-бром-2-хлор-5-нитропиридин (CAN 5470-17-7) (25 г, 105 ммоль) при 25°С и перемешивали при 25°С в течение 1 часа. К реакционной смеси добавляли воду со льдом (150 мл) и экстрагировали этилацетатом (500 мл). Объединенные органические слои промывали водой и солевым раствором, сушили над Na2SO4 и выпаривали при пониженном давлении, что давало неочищенный остаток (25,7 г). Неочищенное вещество очищали с помощью колоночной хроматографии (15% этилацетат/гексан), что давало требуемый продукт (21,6 г, 74%) в виде светло-желтого твердого вещества; ГХ/МС (ПИД/ЭТ): 100%, 276,0 (М)+.
b) 5-Бром-6-(2-метокси-этокси)-пиридин-3-иламин

Указанное в заголовке соединение синтезировали по аналогии с Примером С, используя 3-бром-2-(2-метокси-этокси)-5-нитро-пиридин (Пример 69а) в качестве исходного вещества; ЖХ-МС (площадь УФ пика / ЭСИ) 100%, 247,0084 (М+Н)+.
с) 5-(4-Хлор-3-метил-фенил)-6-(2-метокси-этокси)-пиридин-3-иламин

Указанное в заголовке соединение синтезировали по аналогии с Примером Е, используя 5-бром-6-(2-метокси-этокси)-пиридин-3-иламин (Пример 69b) и В-(4-хлор-3-метилфенил)-бороновую кислоту (CAN 161950-10-3) в качестве исходных веществ; ГХ/МС (ПИД/ЭИ):100%, 292 (М)+.
d) N-(5-(4-Хлор-3-метилфенил)-6-(2-метоксиэтокси)пиридин-3-ил)бензамид

Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-(4-хлор-3-метил-фенил)-6-(2-метокси-этокси)-пиридин-3-иламин (Пример 69с) и бензойную кислоту в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 100%, 397,1307 (М+Н)+.
Пример 70
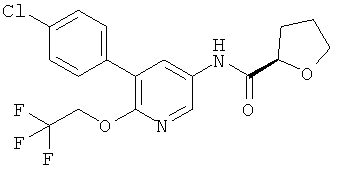
Получение (RS)-N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)тетрагидрофуран-2-карбоксамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (Пример Е) и тетрагидро-2-фуранкарбоновую кислоту (CAN 16874-33-2) в качестве исходных веществ; энантиомеры разделяли с помощью хиральной ВЭЖХ (ChiralPak AD, 30% этанол/н-гептан), выделяли (-) энантиомер; ЖХ-МС (площадь УФ пика / ЭСИ) 100%, 401,0868 (М+Н)+; 
Пример 71

Получение (SR)-N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-тетрагидрофуран-3-карбоксамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (Пример Е) и тетрагидро-3-фуранкарбоновую кислоту (CAN 89364-31-8) в качестве исходных веществ; энантиомеры разделяли с помощью хиральной ВЭЖХ (ChiralPak AD, 30% этанол/н-гептан), выделяли (+) энантиомер; ЖХ-МС (площадь УФ пика/ЭСИ) 98,1%, 401,0869 (М+Н)+; 
Пример 72

Получение N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-4-метил-3,4-дигидро-2Н-пиридо[3,2-b][1,4]оксазин-7-карбоксамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (Пример Е) и 3,4-дигидро-4-метил-2H-пиридо[3,2-b]-1,4-оксазин-7-карбоновую кислоту (CAN 915707-58-3) в качестве исходных веществ; МС (ЭИ) 479,2 (М+Н)+.
Пример 73

Получение N-(5-(4-амино-3-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-5-йодникотинамида
а) Бензиловый эфир {4-[5-амино-2-(2,2,2-трифтор-этокси)-пиридин-3-ил]-2-хлор-фенил}-карбаминовой кислоты

Указанное в заголовке соединение синтезировали по аналогии с Примером Е, используя 5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (Пример С) и фенилметиловый эфир N-[2-хлор-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил]-карбаминовой кислоты (CAN 1218791-42-4) в качестве исходных веществ; МС (ЭИ) 452,1 (М+Н)+.
b) Бензиловый эфир {2-хлор-4-[5-[(5-йод-пиридин-3-карбонил)-амино]-2-(2,2,2-трифтор-этокси)-пиридин-3-ил]-фенил}-карбаминовой кислоты
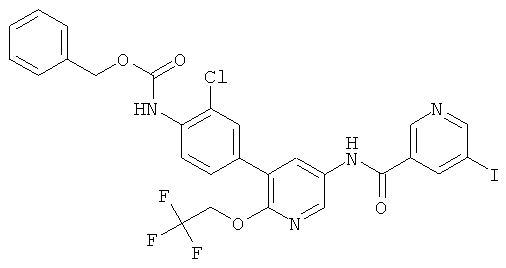
Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя бензиловый эфир {4-[5-амино-2-(2,2,2-трифтор-этокси)-пиридин-3-ил]-2-хлор-фенил}-карбаминовой кислоты (Пример 73а) и 5-йод-3-пиридинкарбоновую кислоту (CAN 15366-65-1) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 68,6%, 683,4 (М+Н)+.
с) N-(5-(4-Амино-3-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-5-йодникотинамид

Бензиловый эфир {2-хлор-4-[5-[(5-йод-пиридин-3-карбонил)-амино]-2-(2,2,2-трифтор-этокси)-пиридин-3-ил]-фенил}-карбаминовой кислоты (87 мг, 127 мкмоль), охлаждая, объединяли с трифторуксусной кислотой (3 мл), что давало коричневый раствор. Реакционную смесь нагревали до комнатной температуры и перемешивали в течение 72 часов. Неочищенную реакционную смесь концентрировали в вакууме, выливали в 50 мл этилацетата и экстрагировали 1 М NaOH (1×25 мл). Водный слой промывали этилацетатом (1×50 мл). Органические слои объединяли, сушили с Na2SO4 и концентрировали в вакууме. Неочищенное вещество очищали с помощью флэш-хроматографии (силикагель, 20 г, от 0% до 40% EtOAc в гептане), что давало указанное в заголовке соединение (59 мг, 84%); ЖХ-МС (площадь УФ пика / ЭСИ) 98,1%, 548,9795 (М+Н)+.
Пример 74

Получение N-(5-фенил-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 39, используя N-[5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-никотинамид (Пример G) и В-фенил-бороновую кислоту (CAN 98-80-6) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 100%, 374,1107 (М+Н)+.
Пример 75

Получение N-(5-(4-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 39, используя N-[5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-никотинамид (Пример G) и В-(4-фторфенил)-бороновую кислоту (CAN 1765-93-1) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 100%, 392,1005 (M+H)+.
Пример 76

Получение N-(5-(3-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 39, используя N-[5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-никотинамид (Пример G) и В-(3-хлорфенил)-бороновую кислоту (CAN 63503-60-6) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 100%, 408,0719 (М+Н)+.
Пример 77
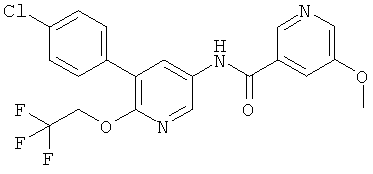
Получение N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-5-метоксиникотинамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (Пример Е) и 5-метокси-3-пиридинкарбоновую кислоту (CAN 20826-03-3) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 97,8%, 438,0812 (М+Н)+.
Пример 78
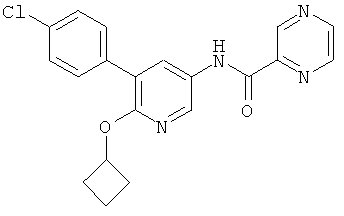
Получение N-(5-(4-хлорфенил)-6-циклобутоксипиридин-3-ил)пиразин-2-карбоксамида
а) 5-Бром-6-циклобутокси-никотиновая кислота

5-Бром-6-хлорникотиновую кислоту (CAN 29241-62-1; 3 г, 12,7 ммоль) растворяли в ДМСО (30 мл); добавляли циклобутанол (1,19 г, 1,29 мл, 16,5 ммоль) и гидроксид калия (порошок) (2,14 г, 38,1 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 5 часов. Добавляли еще циклобутанол (0,5 мл) и КОН (1 г) и реакционную смесь перемешивали при комнатной температуре в течение еще 2 дней. Добавляли воду (30 мл) и смесь подкисляли (охлаждая) 5 мл 37% HCl в воде (рН 2). Суспензию фильтровали и промывали водой. Осадок на фильтре сушили в вакууме, чтобы получить указанное в заголовке соединение (3,1 г, 88,7%) в виде белого твердого вещества; МС (ЭСИ) 270,2 (М-Н)-.
b) 5-(4-Хлор-фенил)-6-циклобутокси-никотиновая кислота

5-Бром-6-циклобутокси-никотиновую кислоту (Пример 78а; 1,531 г, 5,63 ммоль), 4-хлор-фенилбороновую кислоту (968 мг, 6,19 ммоль), карбонат калия (1,56 г, 11,3 ммоль) и тетракис(трифенилфосфин)палладия (325 мг, 281 мкмоль) суспендировали в ТГФ (38 мл) и воде (38 мл). Реакционную смесь перемешивали при нагревании с обратным холодильником (100°С) в течение выходных дней. ТГФ удаляли и остаток разделяли между водой (рН 2) и этилацетатом; органические фазы объединяли, сушили с MgSO4 и концентрировали в вакууме, чтобы получить указанное в заголовке соединение (колич.) в виде твердого вещества белого оттенка; МС (ЭСИ) 302,2 (М-Н)-.
с) трет-Бутиловый эфир [5-(4-хлор-фенил)-6-циклобутокси-пиридин-3-ил]-карбаминовой кислоты

Указанное в заголовке соединение синтезировали по аналогии с Примером 42е, используя 5-(4-хлор-фенил)-6-циклобутокси-никотиновую кислоту (Пример 78b) в качестве исходного вещества; ЖХ-МС (площадь УФ пика / ЭСИ) 92,9%, 375,1456 (М+Н)+.
d) 5-(4-Хлор-фенил)-6-циклобутокси-пиридин-3-иламин

трет-Бутиловый эфир [5-(4-хлор-фенил)-6-циклобутокси-пиридин-3-ил]-карбаминовой кислоты (1,042 г, 2,78 ммоль) растворяли в 4 М HCl в диоксане (10,4 мл, 41,7 ммоль). Реакционная смесь представляла собой светло-желтый раствор, и ее перемешивали при комнатной температуре в течение 1 часа. Смесь разделяли между этилацетатом и 1 М раствором Na2CO3. Органические фазы объединяли, сушили с MgSO4 и концентрировали в вакууме. Неочищенное вещество очищали с помощью флэш-хроматографии (силикагель, 100 г, от 5% до 75% этилацетата в гептане), что давало 0,358 г (46,9%) указанного в заголовке соединения в виде светло-красного масла; ЖХ-МС (площадь УФ пика / ЭСИ) 94,3%, 275,0950 (М+Н)+.
е) N-(5-(4-Хлорфенил)-6-циклобутоксипиридин-3-ил)пиразин-2-карбоксамид

Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-(4-хлор-фенил)-6-циклобутокси-пиридин-3-иламин (Пример 78d) и 2-пиразинкарбоновую кислоту (CAN 98-97-5) в качестве исходных веществ; МС (ЭИ) 381,2 (М+H)+.
Пример 79

Получение N-(5-(4-хлорфенил)-6-циклобутоксипиридин-3-ил)никотинамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 48е, используя 5-(4-хлор-фенил)-6-циклобутокси-пиридин-3-иламин (Пример 78 d) и никотиноилхлорида гидрохлорид в качестве исходных веществ; МС (ЭИ) 380,2 (М+Н)+.
Пример 80

Получение N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-4-метил-3,4-дигидро-2H-пиридо[3,2-b][1,4]оксазин-7-карбоксамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 42f, используя 5-(4-хлор-3-метил-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (Пример 57а) и 3,4-дигидро-4-метил-2H-пиридо[3,2-b]-1,4-оксазин-7-карбоновую кислоту (CAN 915707-58-3) в качестве исходных веществ; МС (ЭИ) 493,1 (М+Н)+.
Пример 81

Получение N-(5-(4-хлор-3-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-4-метил-3,4-дигидро-2H-пиридо[3,2-b][1,4]оксазин-7-карбоксамида
а) 5-(4-Хлор-3-фтор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин
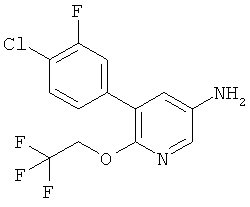
Указанное в заголовке соединение синтезировали по аналогии с Примером Е, используя 5-бром-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (Пример С) и В-(4-хлор-3-фторфенил)-бороновую кислоту (CAN 137504-86-0) в качестве исходных веществ; МС (ЭИ) 379,3 (M+ОАс)+.
b) N-(5-(4-Хлор-3-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-4-метил-3,4-дигидро-2H-пиридо[3,2-b][1,4]оксазин-7-карбоксамид

Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-(4-хлор-3-фтор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (Пример 81а) и 3,4-дигидро-4-метил-2H-пиридо[3,2-b]-1,4-оксазин-7-карбоновую кислоту (CAN 915707-58-3) в качестве исходных веществ; МС (ЭИ) 497,2 (М+Н)+.
Пример 82
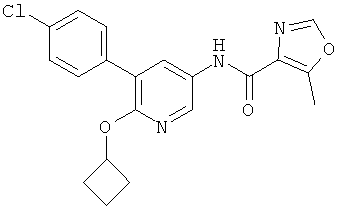
Получение [5-(4-хлор-фенил)-6-циклобутокси-пиридин-3-ил]-амида 5-метил-оксазол-4-карбоновой кислоты
Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-(4-хлор-фенил)-6-циклобутокси-пиридин-3-иламин (Пример 78d) и 5-метил-4-оксазолкарбоновую кислоту (CAN 103879-58-9) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 100%, 384,1102 (М+Н)+.
Пример 83

Получение N-[5-(4-хлор-фенил)-6-циклобутокси-пиридин-3-ил]-5-метил-никотинамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-(4-хлор-фенил)-6-циклобутокси-пиридин-3-иламин (Пример 78d) и 5-метил-3-пиридинкарбоновую кислоту (CAN 40473-04-9) в качестве исходных веществ; МС (ЭИ) 394,1 (М+Н)+.
Пример 84

Получение N5-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-N2-метилпиридин-2,5-дикарбоксамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (Пример Е) и 6-[(метиламино)-карбонил]-3-пиридинкарбоновую кислоту (CAN 170464-32-1) в качестве исходных веществ; МС (ЭИ) 465,2 (М+Н)+.
Пример 85

Получение 5-бром-N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (Пример Е) и 5-бром-3-пиридинкарбоновую кислоту (CAN 20826-04-4) в качестве исходных веществ; ЖХ-МС (площадь УФ пика / ЭСИ) 92,7%, 485,9662 (М-Н)-.
Пример 86
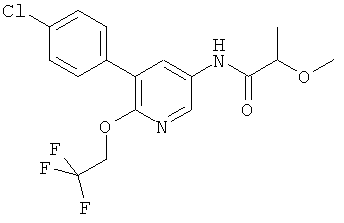
Получение N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-2-метокси-пропанамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (Пример Е) и 2-метокси-пропановую кислоту (CAN 4324-37-2) в качестве исходных веществ; МС (ЭИ) 389,2 (М+Н)+,
Пример 87
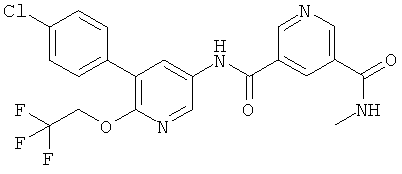
Получение N3-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-N5-метилпиридин-3,5-дикарбоксамида
а) Этиловый эфир 5-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-илкарбамоил]-никотиновой кислоты
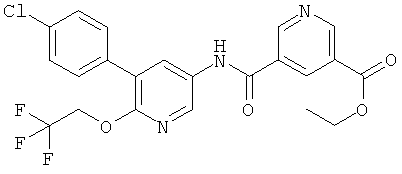
Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (Пример Е) и 3-этиловый эфир 3,5-пиридиндикарбоновой кислоты (CAN 84254-37-5) в качестве исходных веществ; МС (ЭИ) 480,1 (М+Н)+.
b) 5-[5-(4-Хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-илкарбамоил]-никотиновая кислота

Этиловый эфир 5-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-илкарбамоил]-никотиновой кислоты (510 мг, 1,06 ммоль) объединяли с ТГФ (25 мл), метанолом (5 мл) и водой (5 мл), что давало светло-желтую суспензию. Реакционную смесь перемешивали в течение 4 часов и концентрировали в вакууме. Реакционную смесь выливали в 100 мл этилацетата и экстрагировали 1 М HCl (1×25 мл) и солевым раствором (1×25 мл). Водные фазы экстрагировали этилацетатом (1×50 мл). Органические слои объединяли, сушили с Na2SO4 и концентрировали в вакууме. Неочищенное вещество очищали с помощью флэш-хроматографии (силикагель, 40 г, от 0% до 100% этилацетата в гептане), что давало 0,17 г (48,7%) указанного в заголовке соединения в виде белого твердого вещества; МС (ЭСИ) 450,0 (М-Н)-.
с) N3-(5-(4-Хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-N5-метилпиридин-3,5-дикарбоксамид

5-[5-(4-Хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-илкарбамоил]-никотиновую кислоту (120 мг, 260 мкмоль) и метиламина гидрохлорид (140 мг, 2,6 ммоль) растворяли в ДМФА (3 мл). Добавляли TBTU (125 мг, 390 мкмоль) и ДИПЭА (672 мг, 908 мкл, 5,2 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 20 часов. Неочищенную реакционную смесь концентрировали в вакууме и очищали с помощью флэш-хроматографии (силикагель, 10 г, от 0% до 100% этилацетата в гептане), что давало 34 мг (28%) указанного в заголовке соединения в виде белого твердого вещества; ЖХ-МС (площадь УФ пика / ЭСИ) 99,5%, 465,0928 (М+Н)+.
Пример 88
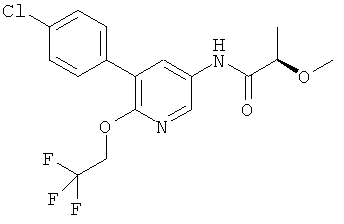
Получение (+)-N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-2-метоксипропанамида
Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (Пример Е) и 2-метокси-пропановую кислоту (CAN 4324-37-2) в качестве исходных веществ; энантиомеры разделяли с помощью хиральной ВЭЖХ (ChiralPak AD, 10% этанол / н-гептан); выделяли (+) энантиомер; ЖХ-МС (площадь УФ пика / ЭСИ) 100%, 389,0874 (М+Н)+; 
Пример 89

Получение (Е)-N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-2-(метоксиимино)пропанамида
а) N-[5-(4-Хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-2-оксо-пропионамид

Указанное в заголовке соединение синтезировали по аналогии с Примером 42g, используя 5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-иламин (Пример Е) и 2-оксо-пропановую кислоту (127-17-3) в качестве исходных веществ; МС (ЭИ) 373,0 (М+Н)+.
b) (Е)-N-(5-(4-Хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-2-(метоксиимино)-пропанамид

N-[5-(4-Хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-2-охо-пропионамид (0,063 г, 169 мкмоль) растворяли в метаноле (1,00 мл). Добавляли O-метил-гидроксиламина гидрохлорид (70,6 мг, 845 мкмоль) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Растворитель выпаривали и остаток разделяли между водой и этилацетатом; органическую фазу сушили с MgSO4 и концентрировали в вакууме, что давало 67 мг (89%) указанного в заголовке соединения в виде белого твердого вещества; ЖХ-МС (площадь УФ пика / ЭСИ) 99,0%, 402,0825 (М+Н)+.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЗАМЕЩЕННЫЕ БЕНЗАМИДНЫЕ ПРОИЗВОДНЫЕ | 2010 |
|
RU2595902C2 |
| ПРОИЗВОДНЫЕ N-(ИМИДАЗОПИРИМИДИН-7-ИЛ)-ГЕТЕРОАРИЛАМИДОВ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ PDE10A | 2011 |
|
RU2562066C2 |
| 2-АМИНО-5,5-ДИФТОР-5,6-ДИГИДРО-4Н-ОКСАЗИНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ВАСЕ 1 И(ИЛИ) ВАСЕ 2 | 2010 |
|
RU2515221C2 |
| ПРОИЗВОДНЫЕ ОКСАЗОЛИНОВ ДЛЯ ЛЕЧЕНИЯ РАССТРОЙСТВ ЦНС | 2010 |
|
RU2569887C2 |
| 2-ОКСА-5-АЗАБИЦИКЛО[2.2.1]ГЕПТАН-3-ИЛЬНЫЕ ПРОИЗВОДНЫЕ | 2015 |
|
RU2697651C2 |
| ПРОИЗВОДНЫЕ АРИЛАМИДОВ В КАЧЕСТВЕ БЛОКАТОРОВ TTX-S | 2011 |
|
RU2535671C1 |
| ПРОИЗВОДНЫЕ ДИГИДРООКСАЗОЛ-2-АМИНА | 2011 |
|
RU2587512C2 |
| ПРОИЗВОДНЫЕ 3-ПИРИДИНКАРБОКСАМИДА И 2-ПИРАЗИНКАРБОКСАМИДА В КАЧЕСТВЕ АГЕНТОВ, ПОВЫШАЮЩИХ УРОВЕНЬ ЛВП-ХОЛЕСТЕРИНА | 2007 |
|
RU2454405C2 |
| ПРОИЗВОДНЫЕ МОРФОЛИН-ПИРИДИНА | 2015 |
|
RU2690154C2 |
| АМИДОПРОИЗВОДНЫЕ КАК БЛОКАТОРЫ TTX-S | 2013 |
|
RU2632899C2 |
Изобретение относится к области органической химии, а именно к гетероциклическим соединениям формулы I и к их фармацевтически приемлемым солям, где А выбран из СН или N; R1 выбран из группы, состоящей из, С3-6-циклоалкила, С3-6-циклоалкил-С1-7-алкила, С1-7-алкокси-С1-7-алкила, галоген-С1-7-алкила; R2 и R6 независимо друг от друга представляют собой водород или галоген; R3 и R5 независимо друг от друга выбраны из группы, состоящей из водорода, C1-7-алкила и галогена; R4 выбран из группы, состоящей из водорода, C1-7-алкила, галогена и амино; R7 выбран из группы, состоящей из C1-7-алкила, С1-7-алкокси-С1-7-алкила, С1-7-алкоксиимино-С1-7-алкила, 4-6-членного гетероциклила, содержащего один гетероатом О, фенила, указанный фенил не замещен или замещен одной группой гидрокси, и 5-10-членного гетероарила, содержащего 1-3 гетероатома, выбранных из N, S и О, указанный гетероарил не замещен или замещен одной или двумя группами, выбранными из группы, состоящей из C1-7-алкила, гидрокси, С1-7-алкокси, циано, C1-7-алкиламинокарбонила и галогена. Также изобретение относится к фармацевтической композиции на основе соединения формулы I и способу получения соединения формулы I. Технический результат: получены новые гетероциклические соединения, которые являются агентами, повышающими уровень холестерина ЛПВП. 3 н. и 14 з.п. ф-лы, 2 табл., 89 пр.

1. Соединения формулы

где
А выбран из СН или N;
R1 выбран из группы, состоящей из
С3-6-циклоалкила,
С3-6-циклоалкил-С1-7-алкила,
С1-7-алкокси-С1-7-алкила,
галоген-С1-7-алкила;
R2 и R6 независимо друг от друга представляют собой водород или галоген;
R3 и R5 независимо друг от друга выбраны из группы, состоящей из водорода, C1-7-алкила и галогена;
R4 выбран из группы, состоящей из водорода, C1-7-алкила, галогена и амино;
R7 выбран из группы, состоящей из C1-7-алкила,
С1-7-алкокси-С1-7-алкила,
С1-7-алкоксиимино-С1-7-алкила,
4-6-членного гетероциклила, содержащего один гетероатом О,
фенила, указанный фенил не замещен или замещен одной группой гидрокси, и
5-10-членного гетероарила, содержащего 1-3 гетероатома, выбранных из N, S и О, указанный гетероарил не замещен или замещен одной или двумя группами, выбранными из группы, состоящей из C1-7-алкила, гидрокси, С1-7-алкокси, циано, C1-7-алкиламинокарбонила и галогена;
и их фармацевтически приемлемые соли.
2. Соединения формулы I по п.1, где R1 представляет собой С3-6-циклоалкил-С1-7-алкил или галоген-С1-7-алкил.
3. Соединения формулы I по п.1, где R1 представляет собой галоген-С1-7-алкил.
4. Соединения формулы I по п.1, где R2 и R6 представляют собой водород.
5. Соединения формулы I по п.1, где R3 и R5 представляют собой водород или c1-7-алкил.
6. Соединения формулы I по п.1, где R4 представляет собой C1-7-алкил или галоген.
7. Соединения формулы I по п.1, где R4 представляет собой галоген.
8. Соединения формулы I по п.1, где R7 представляет собой фенил, указанный фенил не замещен или замещен одним гидрокси, или 5-10-членный гетероарил, содержащий 1-3 гетероатома, выбранных из N, S и О, указанный гетероарил не замещен или замещен одной или двумя группами, выбранными из группы, состоящей из C1-7-алкила, гидрокси, циано, c1-7-алкиламинокарбонила и галогена.
9. Соединения формулы I по п.1, где R7 представляет собой 5-10-членный гетероарил, содержащий 1-3 гетероатома, выбранных из N, S и О, указанный гетероарил не замещен или замещен одной или двумя группами, выбранными из группы, состоящей из C1-7-алкила, гидрокси, циано, C1-7-алкиламинокарбонила и галогена.
10. Соединения формулы I по п.1, где гетероарил выбран из группы, состоящей из фуранила, оксазолила, изоксазолила, пиразолила, тиазолила, изотиазолила, [1,2,3]тиадиазолила, пиридила, пиразинила, пиридазинила, пиримидинила и 3,4-дигидро-2Н-пиридо[3,2-b][1,4]оксазинила, указанный гетероарил не замещен или замещен одной или двумя группами, выбранными из группы, состоящей из C1-7-алкила, гидрокси, циано, C1-7-алкиламинокарбонила и галогена.
11. Соединения формулы I по п.1, где А представляет собой СН.
12. Соединения формулы I по п.1, имеющие формулу
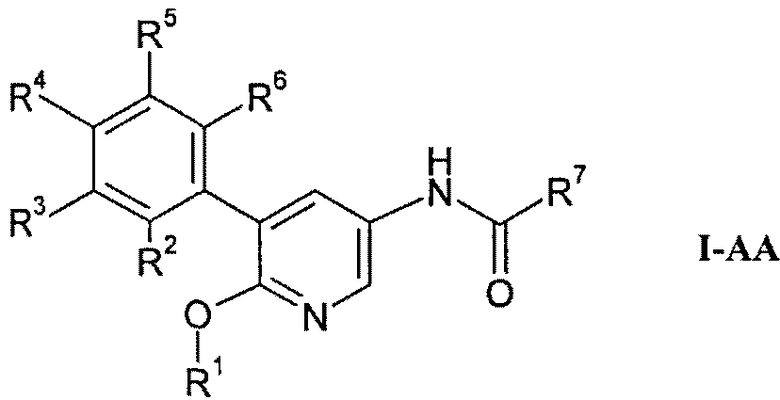
где
R1 выбран из группы, состоящей из
С3-6-циклоалкила,
С3-6-циклоалкил-С1-7-алкила,
С1-7-алкоксиС1-7-алкила,
галоген-С1-7-алкила;
R2 и R6 независимо друг от друга представляют собой водород или галоген;
R3 и R5 независимо друг от друга выбраны из группы, состоящей из водорода, C1-7-алкила и галогена;
R4 выбран из группы, состоящей из водорода, галогена и амино;
R7 выбран из группы, состоящей из C1-7-алкила,
4-6-членного гетероциклила, содержащего один гетероатом О, фенила, указанный фенил не замещен или замещен одним гидрокси, и 5-10-членного гетероарила, содержащего 1-3 гетероатома, выбранных из N, S и О, указанный гетероарил не замещен или замещен одной или двумя группами, выбранными из группы, состоящей из C1-7-алкила, гидрокси, циано и галогена;
и их фармацевтически приемлемые соли.
13. Соединения формулы I по п.1, выбранные из группы, состоящей из
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида пентановой кислоты,
N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-бензамида,
N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-никотинамида,
N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-изоникотинамида,
N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-ацетамида,
N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-бутирамида,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида пиридин-2-карбоновой кислоты,
N-[5-(4-хлор-фенил)-6-циклопропилметокси-пиридин-3-ил]-бензамида,
N-[5-(4-хлор-фенил)-6-циклопропилметокси-пиридин-3-ил]-ацетамида,
N-[5-(4-хлор-фенил)-6-циклопропилметокси-пиридин-3-ил]-никотинамида,
N-[5-(4-хлор-фенил)-6-циклопропилметокси-пиридин-3-ил]-изоникотинамида,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида пиразин-2-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 2,5-диметил-2H-пиразол-3-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 3-метил-изоксазол-4-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 1-метил-1Н-пиразол-3-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 5-метил-изоксазол-3-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида пиридазин-3-карбоновой кислоты,
N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-3-метил-изоникотинамида,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида пиримидин-5-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 2-метил-2Н-пиразол-3-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 2,4-диметил-оксазол-5-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида изотиазол-5-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 5-метил-2Н-пиразол-3-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 1H-пиразол-3-карбоновой кислоты,
N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-2-метил-изоникотинамида,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 5-метил-тиазол-2-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 4-метил-[1,2,3]тиадиазол-5-карбоновой кислоты,
N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-6-метил-никотинамида,
N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-2-метил-никотинамида,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида изоксазол-5-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 3,5-диметил-изоксазол-4-карбоновой кислоты,
N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-2-гидрокси-изоникотинамида,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 1,3-диметил-1Н-пиразол-4-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида пиримидин-4-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида тиазол-2-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 3-метил-пиридин-2-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 5-метил-оксазол-4-карбоновой кислоты,
N-(5-(3,4-диметилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-никотинамида,
N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-никотинамида,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 5-гидрокси-пиридин-2-карбоновой кислоты,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-5-метилникотинамида,
(S)-N-(5-(4-хлорфенил)-6-(1,1,1-трифторпропан-2-илокси)пиридин-3-ил)пиридазин-3-карбоксамида,
(S)-N-(5-(4-хлорфенил)-6-(1,1,1-трифторпропан-2-илокси)пиридин-3-ил)никотинамида,
N-(5-(4-хлор-3-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамида,
N-(5-(3-хлор-4-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамида,
N-(5-(4-хлор-2-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамида,
N-(5-(4-этилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамида,
(S)-N-(6-(4-хлорфенил)-5-(1,1,1-трифторпропан-2-илокси)пиразин-2-ил)никотинамида,
N-(6-(4-хлорфенил)-5-(2,2,2-трифторэтокси)пиразин-2-ил)никотинамида,
N-(6-(4-хлорфенил)-5-циклобутоксипиразин-2-ил)никотинамида,
N-(6-(4-хлорфенил)-5-циклобутоксипиразин-2-ил)пиримидин-5-карбоксамида,
N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиримидин-5-карбоксамида,
N-(5-(4-хлор-3-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиримидин-5-карбоксамида,
N-(5-(3-хлор-4-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиримидин-5-карбоксамида,
N-(5-(4-хлор-2-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиримидин-5-карбоксамида,
N-(5-(4-этилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиримидин-5-карбоксамида,
N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-2-гидроксиизоникотинамида,
N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-1,3-диметил-1Н-пиразол-4-карбоксамида,
N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-2,4-дифторникотинамида,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-2-гидроксибензамида,
N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-5-цианоникотинамида,
N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиридазин-3-карбоксамида,
N-(5-(4-хлор-3-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиридазин-3-карбоксамида,
N-(5-(4-хлор-2-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиридазин-3-карбоксамида,
N-(5-(4-этилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиридазин-3-карбоксамида,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)фуран-2-карбоксамида,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)фуран-3-карбоксамида,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-5-метилфуран-2-карбоксамида,
N-(5-(4-хлор-3-метилфенил)-6-(2-метоксиэтокси)пиридин-3-ил)бензамида,
(R)-N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)тетрагидрофуран-2-карбоксамида,
(S)-N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)тетрагидрофуран-3-карбоксамида,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-4-метил-3,4-дигидро-2H-пиридо[3,2-b][1,4]оксазин-7-карбоксамида,
N-(5-(4-амино-3-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-5-йодникотинамида,
N-(5-фенил-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамида,
N-(5-(4-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамида,
N-(5-(3-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамида,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-5-метоксиникотинамида,
N-(5-(4-хлорфенил)-6-циклобутоксипиридин-3-ил)пиразин-2-карбоксамида,
N-(5-(4-хлорфенил)-6-циклобутоксипиридин-3-ил)никотинамида,
N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-4-метил-3,4-дигидро-2H-пиридо[3,2-b][1,4]оксазин-7-карбоксамида,
N-(5-(4-хлор-3-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-4-метил-3,4-дигидро-2H-пиридо[3,2-b][1,4]оксазин-7-карбоксамида,
[5-(4-хлор-фенил)-6-циклобутокси-пиридин-3-ил]-амида 5-метил-оксазол-4-карбоновой кислоты,
N-[5-(4-хлор-фенил)-6-циклобутокси-пиридин-3-ил]-5-метил-никотинамида,
N5-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-N2-метилпиридин-2,5-дикарбоксамида,
5-бром-N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамида,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-2-метоксипропанамида,
N3-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-N5-метилпиридин-3,5-дикарбоксамида,
(+)-N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-2-метоксипропанамида,
(Е)-N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-2-(метоксиимино)пропанамида,
и их фармацевтически приемлемые соли.
14. Соединения формулы I по п.1, выбранные из группы, состоящей из
N-[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-никотинамида,
N-[5-(4-хлор-фенил)-6-циклопропилметокси-пиридин-3-ил]-никотинамида,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 3-метил-изоксазол-4-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида пиридазин-3-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 1,3-диметил-1 Н-пиразол-4-карбоновой кислоты,
[5-(4-хлор-фенил)-6-(2,2,2-трифтор-этокси)-пиридин-3-ил]-амида 5-метил-оксазол-4-карбоновой кислоты,
N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-никотинамида,
N-(5-(4-хлор-3-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)никотинамида,
(S)-N-(6-(4-хлорфенил)-5-(1,1,1-трифторпропан-2-илокси)пиразин-2-ил)никотинамида,
N-(6-(4-хлорфенил)-5-циклобутоксипиразин-2-ил)пиримидин-5-карбоксамида,
N-(5-(4-хлор-2-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиримидин-5-карбоксамида,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-2-гидроксибензамида,
N-(5-(4-хлор-3-метилфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-5-цианоникотинамида,
N-(5-(4-хлор-2-фторфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)пиридазин-3-карбоксамида,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-5-метилфуран-2-карбоксамида,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-4-метил-3,4-дигидро-2H-пиридо[3,2-b][1,4]оксазин-7-карбоксамида,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-5-метоксиникотинамида,
N-(5-(4-хлорфенил)-6-(2,2,2-трифторэтокси)пиридин-3-ил)-2-метоксипропанамида, и их фармацевтически приемлемые соли.
15. Фармацевтические композиции для повышения уровня холестерина ЛПВП, включающие соединение формулы I по любому из пп.1-14 и фармацевтически приемлемый носитель и/или вспомогательное вещество.
16. Соединения формулы I по любому из пп.1-14 для применения в качестве лекарства для повышения уровня холестерина ЛПВП.
17. Способ изготовления соединения формулы I, как определено в любом из пп.1-14, согласно которому связывают соединение формулы

где А и R1 - R6 являются такими, как определено в п.1, с кислотой формулы
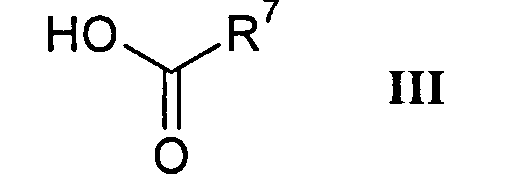
где R7 является таким, как определено в п.1, с помощью связующего вещества при основных условиях,
и при желании переводят полученное в результате соединение формулы I в фармацевтически приемлемую соль.
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
| СПОСОБ И ПРИСПОСОБЛЕНИЕ ДЛЯ ПРОИЗВОДСТВА ЛИСТОВОГО СТЕКЛА ПОСРЕДСТВОМ ВАЛЬЦОВАНИЯ | 1924 |
|
SU3673A1 |
| RU 2001125893 А, 10.07.2003 | |||
Авторы
Даты
2015-01-27—Публикация
2011-10-12—Подача