Область техники, к которой относится изобретение
Настоящее изобретение относится к области медицины, в частности онкологии и молекулярной биологии, и может быть использовано для ранней диагностики немелкоклеточного рака легкого (НМРЛ), в первую очередь плоскоклеточного рака легкого (ПРЛ).
Уровень техники
Рак легкого (РЛ) остается одной из основных причин смерти онкологических больных в мире. Смертность от этого заболевания превышает смертность от рака молочной железы, толстой кишки и простаты, вместе взятых [Jemal A., Siegel R., Ward Е., Murray Т., Xu J., Smigal С., Thun M.J. 2006. Cancer statistics, 2006. CA Cancer J Clin. 56, 6-30]. В России показатели смертности от рака легкого у мужчин 68,2 случая на 100 тысяч населения, у женщин - 6, 8 случая [Заридзе Д.Г. 2004. Эпидемиология и этиология злокачественных новообразований, стр.29-85 - в кн. Канцерогенез/ Под ред. Д.Г. Заридзе. - М.: Медицина]. Различают два основных вида РЛ: мелкоклеточный (МРЛ) и немелкоклеточный (НМРЛ), составляющих 15-20 и 75-80% соответственно. К НМРЛ относят плоскоклеточный рак легкого (ПРЛ), аденокарциному легкого (АКЛ) и крупноклеточный рак. Среди разных форм РЛ по частоте встречаемости ПРЛ занимает первое место, АКЛ - второе.
Диагноз в половине случаев НМРЛ устанавливают на далеко зашедшей стадии опухолевого процесса, что делает малореальным радикальное излечение. Современные методы лечения повышают среднюю пятилетнюю продолжительность жизни больных НМРЛ не более, чем на 15%. Этот показатель может быть существенно улучшен только с помощью разработки методов ранней диагностики.
Основными методами диагностики РЛ служат инструментальные методы - рентгеновские и эндоскопические. Используют также анализ мокроты на атипичные клетки, биопсию тканей легких, компьютерную томографию, флуоресцентную фиброскопию. Иммунологические методы диагностики находят пока ограниченное клиническое применение. Практическую значимость имеет определение опухолевых маркеров: СЕА - раково-эмбриональный антиген - онкомаркер рака прямой кишки, но может использоваться в оценке РЛ; NSE - нейрон-специфическая энолаза - в ряде случаев используют в оценке состояния пациентов с РЛ; тканевой полипептидный антиген (ТРА) - фрагмент цитокератина, более специфичный маркер РЛ. Эти маркеры применяют для контроля лечения, выявления рецидивов, но не для диагностики РЛ на ранней стадии. Для диагностики НМРЛ широко используют маркеры SCC - антиген плоскоклеточной карциномы и фрагмент цитокератина-19 (CYFRA 21.1) [Pastor A., Menendez R., Cremades M.J., Pastor V., Llopis R., Aznar J. 1997. Diagnostic value of SCC, CEA and CYFRA 21.1 in lung cancer: a Bayesian analysis. Eur Respir J. 10, 603-609; Buccheri G., Torchio P., Ferrigno D. 2003. Clinical Equivalence of Two Cytokeratin Markers in Non-small Cell Lung Cancer, A Study of Tissue Polypeptide Antigen and Cytokeratin 19 Fragments. Chest. 124, 622-632], которые, однако, малопригодны для ранней диагностики РЛ.
Диагностическими признаками злокачественной трансформации клеток могут служить также изменения генома в опухолевых клетках - точечные мутации в кодирующих и регуляторных участках генов, микросателлитная нестабильность, аллельные потери, изменение уровня транскрипции генов, метилирование промоторных участков генов и др., а также изменения функциональной активности многих генов. В отличие от белковых, молекулярно-генетические маркеры обладают значительно большей чувствительностью.
В числе перспективных потенциальных маркерных генов, вовлеченных в канцерогенез разных форм НМРЛ, рассматривают новые гены, потенциальные супрессоры опухолевого роста (TSG, tumor suppressor genes) на коротком плече хромосомы 3 человека [Zabarovsky E.R, Leiman M.L, Minna J.D. 2002. Tumor Suppressor Genes on Chromosome 3p Involved in the Pathogenesis of Lung and Other Cancers. Oncogene. 21, 6915-6935; Киселев Л.Л., Сенченко В.Н., Опарина Н.Ю., Брага Э.А, Забаровский Е.Р. 2005. Гены-супрессоры опухолевого роста, локализованные на коротком плече хромосомы 3 человека. Молекулярная медицина. 3, 17-28]. Цитогенетический район Зр21 по сравнению с другими обогащен белок-кодирующими генами [Bertone P, Stole V, Royce ТЕ, Rozowsky JS, Urban AE, Zhu X, Rinn JL, Tongprasit W, Samanta M, Weissman S, Gerstein M, Snyder M. 2004. Global identification of human transcribed sequences with genome tiling arrays. Science. 24, 2242-6]. С целью идентификации новых TSG проведено детальное картирование геми- и гомозиготных делеций на 3p при мелкоклеточном и немелкоклеточном РЛ и других карциномах человека с использованием различных методов [Брага Э.А., Киселев Л.Л., Забаровский Е.Р. 2004. От идентификации геномного полиморфизма к диагностическим и прогностическим маркерам эпителиальных опухолей. Молекулярная биология. 38, 145-154]. Полученные данные подтвердили существенную роль генов из района 3р21 в канцерогенезе, как и предполагали ранее [Van den Berg A., Hulsbeek M., de Jong D. Major role for a 3p21 region and lack of involvement of the t(3;8) breakpoint region in the development of renal cell carcinoma suggest by loss of heterozygosity analysis. 1997. Genes Chromosomes Cancer. 19, 228 - 2327]. В критичном области АР20 (3р22-р21.33, 3.5 млн.п.н.), для которого характерна высокая частота делеций в вышеперечисленных опухолях, в общей сложности идентифицировано 35 генов [Protopopov A, Kashuba V, Zabarovska VI, Muravenko OV, Lerman MI, Klein G, Zabarovsky ER. An integrated physical and gene map of the 3.5-Mb chromosome 3p21.3 (АР20) region implicated in major human epithelial malignancies. 2003. Cancer Res. 63(2), 404-12]. В число этих генов входит ген RBSP3 (от англ. RB1 serine phosphatase from human chromosome 3», где RB1 - retinoblastoma 1; другие обозначения гена CTDSPL; HYA22, SCP3 и др., GenBank accession Nos. A575644, AJ5755645) протяженностью 123 т.п.н., принадлежащий к семейству генов малых CTD (C-terminal domain) сериновых фосфатаз, основная функция которых - дефосфорилирование сериновых остатков в большой субъединице РНК-полимеразы и других белков.
Для выявления супрессорной активности белковых продуктов TSG, т.е. способности к частичному или полному подавлению роста опухолевых клеток, существует несколько методов [Брага Э.А., Киселев Л.Л., Забаровский Е.Р. 2004. От идентификации геномного полиморфизма к диагностическим и прогностическим маркерам эпителиальных опухолей. Молекулярная биология. 38,145-154; Ito I., Ji L., Tanaka F., Saito Y, Gopalan B, Branch CD, Xu K, Atkinson EN, Bekele BN, Stephens LC, Minna ID, Roth JA, Ramesh R. 2004. Liposomal vector mediated delivery of the 3p FUS1 gene demonstrates potent antitumor activity against human lung cancer in vivo. Cancer Gene Therapy. 11, 733-739]. Сравнительно новый функциональный тест GIT (Gene Inactivation Test) основан на инактивации TSG в опухолевых клетках in vivo и in vitro. Инактивация TSG осуществляется с помощью эукариотических векторов с регулируемой экспрессией, при этом тестируемые гены подвергаются мутациям или делециям в экспериментальных опухолях у иммуннодефицитных SCID-мышей или в опухолевых клеточных линиях. Потеря способности к подавлению роста опухолевых клеток мутантными трансгенами может служить свидетельством принадлежности гена к TSG. «Супрессорная» активность гена RBSP3 показана in vivo и in vitro различными методами, в том числе с помощью GIT. Одна из возможных функций «супрессорного» белка RBSP3 - активация pRb с помощью дефосфорилирования и предположительное участие в регуляции клеточного цикла [Kashuba VI, Li J, Wang F, Senchenko VN, Protopopov A, Malyukova A, Kutsenko AS, Kadyrova E, Zabarovska VI, Muravenko 0V, Zelenin AV, Kisselev LL, Kuzmin I, Minna JD, Winberg G, Emberg I, Braga E, Lerman MI, Klein G, Zabarovsky ER. RBSP3 (HYA22) is a tumor suppressor gene implicated in major epithelial malignancies. 2004. Proc. Natl. AcacL Sci USA. 101(14), 4906-4911]. Эту функцию относят к ключевым для нормального функционирования клетки и ее нарушение, несомненно, важное звено в канцерогенезе.
На уровне геномной ДНК обнаружен высокий уровень делеций, амплификаций и точечных мутаций в различных эпителиальных опухолях при использовании универсального Notl-STS маркера NLJ-003, расположенного на Зр (район АР 20, Зр.21.3), [Senchenko V., Liu J., Braga E. Mazurenko N., Loginov W., Seryogin Y., Bazov I., Protopopov A., Kisseljov FL., Kashuba V., Lerman MI., Klein G., Zabarovsky ER 2003. Deletion mapping of cervical carcinomas using quantitative real-time PCR identifies two frequently affected regions in 3p21.3. Oncogene. 22,2984-92]. Оказалось, что маркер NLJ-003 находится в промоторной области гена RBSP3, для него показана высокая частота геми- и гомозиготных делеций в образцах и клеточных линиях РЛ [Senchenko VN, Liu J, Loginov W, Bazov I, Angeloni D, Seryogin Y, Ermilova V, Kazubskaya T, Garkavtseva R, Zabarovska VI, Kashuba VI, Kisselev LL, Minna JD, Lerman MI, Klein G, Braga EA, Zabarovsky ER. Discovery of frequent homozygous deletions in chromosome 3p21. 3 LUCA and AP20 regions in renal, lung and breast carcinomas. 2004. Oncogene. 23(34), 5719-28].
Известно, что ген характеризуется невысоким уровнем экспрессии во всех видах эпителиальных тканей в норме, причем в легких наблюдается незначительное повышение. Ген образует мРНК и белок практически во всех исследованных тканях, включая эпителиальные. Согласно данным SAGE, для гена RBSP3 отмечено снижение экспрессии или даже отсутствие в разных опухолях [Киселев Л.Л., Сенченко В.Н., Опарина Н.Ю., Брага Э.А., Забаровский Е.Р. 2005. Гены-супрессоры опухолевго роста, локализованные на коротком плече хромосомы 3 человека. Молекулярная медицина. 3, 17-28].
Данные по количественной оценке уровня транскрипции гена RBSP3 при развитии ПРЛ практически отсутствуют. Предварительные данные по оценке уровня транскрипции ранее получены методом ПЦР в реальном времени (ПЦР-РВ) в 12 клеточных линиях основных типов карцином человека, причем обнаружено значительное снижение уровня транскрипции RBSP3 - более чем в 20 раз в 11 из 12 клеточных линий, в том числе в 4 - мелкоклеточного РЛ [Kashuba VI, Li J, Wang F, Senchenko VN, Protopopov A, Malyukova A, Kutsenko AS, Kadyrova E, Zabarovska VI, Muravenko OV, Zelenin AV, Kisselev LL, Kuzmin I, Minna JD, Winberg G, Emberg I, Braga E, Lerman MI, Klein G, Zabarovsky ER. RBSP3 (HYA22) is a tumor suppressor gene implicated in major epithelial malignancies. 2004. Proc. Natl. Acad. Sci USA. 101(14), 4906-4911]. Таким образом, до последнего времени детальное сравнение уровня транскрипции этого гена в норме и опухолях не проводилось.
Снижение уровня транскрипции показано для нескольких генов при НМРЛ. В работе [Terauchi К., Shimada J., Uekawa N., Yaoi Т., Maruyama M., Fushiki S. 2006. Cancer-associated loss of TARSH gene expression in human primary lung cancer. J. Cancer Res. din. Oncol. 132, 28-34] выявлено уменьшение транскрипции гена TARSH, одного из генов, связанных со старением клеток, в опухолевых клеточных линиях и образцах НМРЛ по сравнению с нормой. На основе полученных результатов авторы выдвинули предположение о возможном использовании этого гена в качестве биомаркера для диагностики НМРЛ. Однако в данной работе проведен анализ только 8 образцов ПРЛ - наиболее распространенной формы РЛ.
Изобретение, предлагающее способ диагностики различных карцином человека, в том числе РЛ, а также лимфом и лейкемий, основано на выявлении цитогенетических изменений и аллельных потерь для 10 генов-супрессоров опухолевого роста, расположенных в критичной области LUCA хромосомы 3 [Ji L., Minna J., Roth J., Lerman M. Chromosome 3p21.3 genes are tumor suppressors. 2002. Международные патенты № WO 0204511, № US 2004016006].
Изобретение, относящееся к способу диагностики рака молочной железы, толстой кишки, мочевого пузыря, основано на обнаружении повышения уровня мРНК множественных сплайсированных форм гена поверхностного гликопротеина CD44 в опухолевых тканях, соответствующих метастазах и биоптатах по сравнению с нормальными тканями, предполагает проведение ПЦР с радиоактивно мечеными праймерами [Tarin D., Matsumura Y. Diagnostic method. 1994. Международный патент №WO 94/02633].
Изобретение, предлагающее способ диагностики лимфом, основано на сравнении относительного уровня мРНК генов легких λ- и κ- иммуноглобулинов, вовлеченных в развитие лимфом, методом ПЦР-РВ [Stalberg A., Kubista M. Method to measure gene expression ratio of key genes. 2002. Патент №20004100112 РФ, международный патент №WO 02/099135 А1]. Данный аналог наиболее близок по технической сущности заявленному изобретению и принят за прототип.
В указанных выше, а также других изобретениях не использовали снижение уровня транскрипции гена RBSP3, в том числе с использованием метода ПЦР-РВ для диагностики рака легкого.
Для оценки уровня мРНК генов используют различные методы. Современный высокочувствительный метод ПЦР-РВ отличается от традиционных качественных и полуколичественных методов тем, что позволяет быстро и точно определить количество копий ДНК или кДНК в широком диапазоне концентраций [Livak K.J., Flood S.J., Marmaro J., Giusti W., Deets K. 1995. Oligonucleotides with fluorescent dyes at opposite ends provide a quenched probe system useful for detecting PCR product and nucleic acid hybridization. PCR Methods Appl. 4, 357-362]. Метод широко используют в мире как для научных, так и клинических целей, благодаря высокой производительности, обычно 96 реакций в одном опыте и в последних моделях приборов - 384 реакции. В отличие от обычной ПЦР, когда количество продуктов определяют на конечной стадии реакции, ПЦР-РВ позволяет следить за накоплением продуктов в экспоненциальной фазе реакции. В этой системе наряду с праймерами используют зонд (пробу), меченный флуоресцентным красителем. Проба является олигонуклеотидом, который гибридизуется с последовательностью ДНК/кДНК между двумя фланкирующими праймерами. ПЦР-РВ состоит из двух основных этапов: 1) гибридизации исследуемой матрицы с пробой и 2) ПЦР, катализируемой TaqДНК-полимеразой, обладающей 5'-экзонуклеазной активностью, расщепляющей зонд, что приводит к появлению и нарастанию флуоресцентного сигнала. Реакция может продолжаться 40 мин (приборы нового поколения), 2 часа (40 циклов ПЦР), 3 часа и более, в зависимости от поставленных задач. Результаты анализа становятся доступными сразу после завершения реакции.
На мировом рынке представлены различные модели приборов для ПЦР-РВ, разработанные известными фирмами-изготовителями - Applied Biosystems, Bio-Rad, Invitrogene, Eppendorf и др., а также отечественные приборы ДТ-322 (ДНК-Технология), АНК-32 (Институт Аналитического Приборостоения РАН, http://www.syntol.ru/productank.htm).
Несмотря на широкое использование ПЦР-РВ, основного метода количественной оценки уровня транскрипции генов на сегодняшний день, в России этот метод еще не получил достаточного распространения как в фундаментальных исследованиях, так и в клинике. Основная причина, ограничивающая его использование, относительно высокая стоимость приборов и реактивов. Обнадеживает появление на отечественном рынке недорогих приборов, разработанных российскими фирмами, а также недорогих отечественных наборов реактивов («Синтол», «ДНК-Технологии», «Изоген» и др.), сравнимых по эффективности с зарубежными наборами [Манзенюк О.Ю., Малахо С.Г., Пехов В.М., Косорукова И.С., Полтараус А.Б. Характеристика универсальных отечественных наборов реагентов для ПЦР в реальном времени. Опыт использования в молекулярной онкодиагностике. 2006. Молекулярная биология. 40, 349-356].
Методики и протоколы, описанные в данной заявке, предполагают, в основном, использование отечественных наборов, и хотя выполнены на приборе ABI Prism 7000 (Applied Biosystems, CIIIA), могут быть адаптированы для отечественных приборов. Сочетание недорогих приборов и наборов реактивов позволит сделать доступным этот технологичный метод для отечественных научных и клинических лабораторий.
Из изложенного ясно, что дифференциальный уровень транскрипции как молекулярный маркер для диагностики эпителиальных опухолей и, в частности РЛ пока не нашел широкого практического применения в клиниках. В данной области существует настоятельная потребность в поиске новых диагностических маркеров РЛ,позволяющих достоверно и уже на ранних стадиях диагностировать заболевание, а также в разработке на их основе простого, чувствительного, надежного, применимого в условиях клинических или поликлинических медицинских учреждений способа диагностики РЛ в частности НМРЛ.
Раскрытие изобретения
Данное изобретение стало возможным в результате проведенного авторами сравнительного анализа уровня транскрипции гена RBSP3 в различных опухолевых тканях легкого на разных этапах злокачественного перерождения и неожиданного открытия того факта, что уже ранние стадии развития злокачественной трансформации сопровождаются значительным снижением уровня транскрипции гена RBSP3.
Настоящее изобретение в своем первом аспекте относится к новому маркеру для диагностики немелкоклеточного рака легкого (НМРЛ), который представляет собой изменение уровня транскрипции гена RBSP3. Сниженный уровень транскрипции гена в предположительно пораженных раком тканях легкого человека по сравнению с его уровнем в нормальных/здоровых тканях служит диагностическим маркером различных типов НМРЛ, в первую очередь плоскоклеточного рака легкого (ПРЛ).
В одном из воплощений рак легкого, маркером которого является изменение уровня транскрипции гена RBSP3, является немелкоклеточным раком легкого.
В своем следующем аспекте настоящее изобретение относится к применению изменения уровня транскрипции гена RBSP3 в качестве маркера для диагностики немелкоклеточного рака легкого человека.
В одном из воплощений рак легкого, в отношении которого изменение уровня транскрипции гена RBSP3 служит в качестве диагностического маркера, является плоскоклеточным раком легкого.
В еще одном аспекте настоящее изобретение относится к способу диагностики немелкоклеточного рака легкого, в первую очередь плоскоклеточного рака легкого. Данный способ включает следующие стадии:
а) получение исходной пары образцов тканей от пациента, где один из образцов получен из предположительно пораженных раком тканей, а второй получен из прилегающих гистологически нормальных (условно-нормальных) тканей;
б) выделение и очистка препаратов РНК из исходной пары образцов;
в) синтез одноцепочечной или двуцепочечной кДНК на матрице РНК с использованием олигонуклеотидных праймеров;
г) нормирование концентрации кДНК RBSP3 по контрольному гену, уровень транскрипции которого относительно постоянен в норме и опухоли;
д) проведение количественной или полуколичественной реакции амплификации фрагмента гена RBSP3 с использованием кДНК, полученной на стадии в), в качестве матрицы и пары геноспецифичных олигонуклеотидных праймеров и зонда (в случае ПЦР-РВ);
е) сравнение количества амплифицированного фрагмента ДНК RBSP3 в образце, полученном из предположительно пораженных раком тканей легкого, с количеством амплифицированного фрагмента ДНК в образце, полученном из нормальных тканей, где указанные количества амплифицированного фрагмента ДНК отражают уровень транскрипции гена RBSP3, причем уменьшение транскрипции гена RBSP3 служит диагностическим маркером рака легкого.
В одном из воплощений заявленный способ предназначен для диагностики плоскоклеточного рака легкого.
В одном из воплощений способа изобретения на стадии в) олигонуклеотидные праймеры, используемые для синтеза одноцепочечной или двуцепочечной кДНК, выбирают из числа олиго(dT)-содержащих праймеров, случайных гексамеров, или их комбинации, а также геноспецифичных праймеров.
В следующем воплощении способа настоящего изобретения для амплификации кДНК на стадии д) используют олигонуклеотидные праймеры и зонд, подобранные таким образом, что они специфически гибридизуются с кДНК даже в присутствии в препарате примеси геномной ДНК.
В отдельном предпочтительном воплощении данного изобретения последовательность праймеров и зонда представлена SEQ ID NO:1, 2 и 3.
В еще одном воплощении способа настоящего изобретения на стадии д) количественная или полуколичественная реакция амплификации фрагмента гена RBSP3 представляет собой ПЦР в реальном времени или стандартную ОТ-ПЦР.
В одном воплощении заявленного способа на стадии г) в качестве контрольного гена используют ген GAPDH, кодирующий белок глицеральдегид-3-фосфат-дегидрогеназу.
Еще одним аспектом настоящего изобретения является набор праймеров и зонда для осуществления полимеразной цепной реакции с целью определения уровня транскрипции гена. RBSP3, имеющих последовательность SEQ ID NO: 1, 2 и 3.
Перечень чертежей.
Далее изобретение будет более подробно раскрыто со ссылкой на отдельные иллюстративные примеры и чертежи.
Фиг.1 Электрофоретическое разделение в 2%-ном агарозном геле продукта ПЦР-РВ-транскрипта гена RBSP3 (размер 154 п.н.). 1-я дорожка - М50, маркер молекулярных масс ДНК от 50 до 500 п.н. («Лаборатория Изоген»), 2-я и 3-я дорожки - транскрипт гена RBSP3 ожидаемого размера (N - норма, Т - опухоль).
Фиг.2. Изменение порогового цикла Ct, отражающего начальное мРНК контрольного гена GAPDH в норме (N) и опухоли (Т). Рассчитанные значения величины R (относительного уровня мРНК с учетом полученных Ct, см. формулу) для гена GAPDH не превышало 1.5-2 раза (Р<0.05) как в опухоли, так и норме, что свидетельствует о незначительной вариабельности его уровня мРНК и приемлемости этого гена для нормирования данных ПЦР-РВ.
Фиг.3. Относительный уровень мРНК гена RBSP3 (R) в различных гистологических типах РЛ (см. формулу). Значение R, равное 1, соответствует отсутствию изменений уровня мРНК исследуемого гена в опухоли по сравнению с нормой, нормированных относительно данных для контрольного гена GAPDH. Пунктиром показана вариабельность уровня мРНК для гена GAPDH. Значения R, равные 0.1 и 0.01, соответствуют снижению уровня мРНК в 10 и 100 раз соответственно. Как видно, снижение уровня транскрипции гена RBSP3 обнаружено в большинстве исследованных образцов.
Фиг.4. Уровень мРНК гена RBSP3 в образцах нормальных тканей легкого центральной и периферической локализаций от здоровых доноров: NCL10-14, NPL10-14, рассчитанный относительно усредненной условной нормы от 14 пациентов с диагнозом НМРЛ. Как видно, уровень мРНК гена в нормальных тканях варьировал в отдельных образцах не более чем в 2,5 раза и в среднем составил 1.0±0.5, что показывает приемлемость использования условных норм в качестве образцов сравнения при количественных изменениях методом ПЦР-РВ, а также дополнительных образцов сравнения от здоровых доноров и/или их пулов.
Осуществление изобретения
Данное изобретение предлагает способ диагностики немелкоклеточного рака легкого (НМРЛ), в первую очередь плоскоклеточного рака легкого (ПРЛ), основанный на определении изменения уровня транскрипции гена RBSP3. Это простой и надежный способ диагностики ПРЛ, а также других типов НМРЛ на разных стадиях развития злокачественной трансформации, включая начальные, который позволяет достоверно обнаружить различие в транскрипции гена RBSP3 в нормальных и опухолевых тканях.
Образцы тканей легких для анализа
В качестве образцов для проведения анализа могут быть использованы биоптаты, пунктаты, в том числе материал, полученный при бронхоскопии с прямой биопсией (центральный рак легкого) и трансторакальной (чрескожной) пункции опухоли (периферический рак).
Выделение РНК из образцов тканей легких
Способы выделения суммарной РНК из образцов тканей млекопитающих хорошо известны специалистам и, как правило, включают следующие стадии: измельчение в жидком азоте образцов опухолевых и нормальных тканей, лизис клеток, выделение РНК и ее очистку, проверку качества РНК электрофорезом в 1%-ном агарозном геле в присутствии красителя бромида этидия или в денатурирующем полиакриламидном геле, а также спектрофотометрическое определение количества РНК. Гомогенизацию кусочков тканей можно проводить вручную, растирая пестиком в керамической ступке, или с помощью механических гомогенизаторов, например, Omni Mixer или Micro-Dismembrator U фирмы Sartorius (Германия). Для выделения РНК могут быть использованы различные протоколы, широко известные специалистам в данной области. В классических методах выделения РНК используют сильные хаотропные агенты, такие как гуанидинхлорид и гуанидинизотиоцианат, растворяющие белки, и последовательные экстракции фенолом и хлороформом для денатурации и удаления белков [Sambrook J., Fritsch E.F., Maniatis Т., Molecular Cloning. A laboratory Manual. 2nd Edition ed. 1989, Cold Spring Harbour: CSHL Press]. Широко используют также метод с использованием реагента Trizol [GIBCO/Life Technologies]. Для предотвращения разрушения РНК РНКазами могут быть использованы ингибиторы, такие как игибитор RNAsin плацентарного или рекомбинантного происхождения или, например, ванадил-рибозидный комплекс - неспецифический ингибитор РНКаз широкого спектра действия.
Быстрое и качественное выделение РНК можно проводить с использованием ряда коммерчески доступных наборов (Клоноген, Санкт-Петербург; RNeasy kits (Qiagen); SV Total RNA Isolation System, Promega (CIIIA) и т.д.). Использование различных приборов, например, QuickGene-810 (Life Science, Япония), позволяет исключить работу с агрессивными агентами, ускорить и упростить выделение РНК. Для экстракции РНК в этом приборе используют 80 мкм пористую мембрану, которая в 12,5 раз тоньше обычно используемого в таких приборах стеклянного фильтра (1000 мкм), что позволяет уменьшить деградацию РНК и увеличить ее выход.
Реакция обратной транскрипции: синтез кДНК на матрице РНК, выделенной из образцов тканей легких, перевод в двуцепочечную форму
Реакция обратной транскрипции, в результате которой на РНК-матрице синтезируют одноцепочечную цепь ДНК, при необходимости, с достройкой второй цепи, позволяет перейти от нестабильных молекул РНК к более стабильным молекулам ДНК. Дальнейшая ПЦР-амплификация позволяет использовать очень малые количества исходной РНК (на уровне нескольких нанограмм), а следовательно, и количества исследуемых легочных тканей, из которых выделяют РНК.
Реакцию обратной транскрипции можно проводить с использованием коммерчески доступных препаратов обратных транскриптаз, таких как обратная транскриптаза вируса лейкоза мышей Молони (M-MLV), вируса миелобластоза птиц (AMV), PowerScript (точечная мутация M-MLV-RT), С.Therm Polymerase и др., с помощью которых можно получать продукты амплификации длиною до нескольких тысяч и даже несколько десятков тысяч пар нуклеотидов (т.п.н.). Может быть использована термостабильная ДНК-полимераза Thermus thermophilus (Tth), обладающая обратной транскриптазной активностью в присутствии ионов Mn2+.
Для обратной транскрипции могут быть использованы различные праймеры, например:
1) Олиго(dT)n-содержащие праймеры связываются с эндогенным полиА-хвостом на 3'-конце мРНК (число n обычно равно 12-18, но может достигать и большей величины). Эти праймеры наиболее часто используют для получения полноразмерных кДНК. К олиго(dT)-последователыюсти часто добавляют на 3'-конце нуклеотиды А, С или G, чтобы «заякорить» праймер на границу транскрипта и поли-А тракта;
2) Случайные гексануклеотидные праймеры (статистические затравки) гибридизуются с РНК в многочисленных участках. При обратной транскрипции с этими праймерами получают короткие кДНК. Случайные гексамеры используют для преодоления трудностей, связанных со вторичной структурой РНК, они более эффективны при обратной транскрипции 5'-областей мРНК;
3) гексамеры или другие короткие олигонуклеотиды (10-12 нуклеотидов) случайного состава могут быть также использованы в комбинации с олиго (dT)-содержащими праймерами;
4) Специфические олигонуклеотидные праймеры используют для транскрипции участка мРНК, представляющего интерес для исследования. Эти праймеры успешно применяют для диагностических целей.
Анализ транскрипции генов можно проводить, используя одноцепочечную или двуцепочечную и амплифицированную кДНК. Для синтеза второй цепи и ее амплификации наиболее часто используют специфичные праймеры. В продаже имеются наборы для синтеза кДНК, основанные на применении различных обратных транскриптаз и различных праймеров для затравки. Для получения кДНК разработан также SMART-метод (switching mechanism at the 5' end of RNA templates of reverse transcriptase), в основе которого лежит свойство обратных транскриптаз добавлять на 3'-конец синтезированной первой цепи кДНК несколько нуклеотидных остатков, преимущественно dC. Эта олиго(dC)-последовательностъ служит местом отжига олигонуклеотидного адаптера, имеющего комплементарную олиго(dG)-последовательность на 3'-конце. Обратная транскриптаза воспринимает праймер как продолжение РНК-матрицы и продолжает синтез первой цепи [Schmidt W.M., Mueller M.W. 1999. CapSelect: a highly sensitive method for 5' CAP-dependent enrichment of full-length cDNA in PCR-mediated analysis of mRNAs. Nucleic Acids Res. 27, e31]. Таким образом, первая цепь кДНК оказывается фланкирована с одной стороны последовательностью 3'-праймера с олиго(dT) на 3'-конце, а с другой - последовательностью, комплементарной адаптеру. Эти праймеры имеют одинаковые внешние последовательности, отличаясь только на 3'-конце. Затем первую цепь амплифицируют в ПЦР с праймером, соответствующим внешней части 3'-праймера и адаптера. Нуклеотидную последовательность общей части этих праймеров подбирают в зависимости от дальнейших целей, например получения клонотек, применения вычитающей гибридизации и т.д. В результате получают двухцепочечную ДНК, обогащенную полноразмерными последовательностями. За счет использования адаптера с заблокированным 3'-концом достигается существенное снижение фоновой амплификации. При использовании модифицированного SMART-метода за короткое время происходит амплификация исходного материала более, чем в 105 раз, что позволяет работать с очень небольшими количествами РНК (меньше 1 нанограмма), а следовательно, и с небольшим количеством исследуемых тканей [Zhu Y.Y., Machleder Е.М., Chenchik A., Li R., Siebert P.D. 2001. Reverse transcriptase template switching: a SMART approach for full-length cDNA library construction. Biotechniques 30, 892-897]. Наборы для получения кДНК этим способом выпускают различные фирмы, например, Евроген, Россия (набор MINT), Clontech, CIIIA и т.п.
Выбор специфических праймеров и зондов
Выбор специфических праймеров и зондов осуществляют способом, хорошо известным специалистам в данной области, для чего используют имеющиеся программы, многие из которых находятся в свободном доступе в Интернете. Среди таких программ можно упомянуть Oligo (версия 6.42), PrimerSelect из пакета Lasergene (www.dnastar.com). Primer Express (Applied Biosystems, USA), Primer Designer (ИМБ), FastPCR (http://www.biocenter.helsinki.fi/bi/Programs/fastpcr.htm), Primer Quest (http://scitools.idtdna.com/Primerquest/) и др. Высокая специфичность ПЦР-РВ обеспечивается за счет использования зонда, содержащего на 5'-конце флуоресцентный краситель (в данном случае, FAM - 6-carboxy-fluoroscein), а на 3'-конце - т.н. гаситель (в данном случае - DABCYL - 4-(dimethylaminoazo)benzene-4-carboxylic acid). В процессе ПЦР взаимодействие FAM и DABCYL нарушается за счет расщепления зонда Taq ДНК полимеразой, благодаря ее 5'-экзонуклеазной активности, при этом происходит эмиссия флуоресценции, регистрируемая прибором. Подбор зондов для проведения ПЦР-РВ осуществляется в соответствии со стандартными рекомендациями и требованиями метода (протоколы фирмы Applied Biosystems, http://docs.appliedbiosystems.com).
В предпочтительном воплощении используют праймеры и зонд:
RBSP3_F (SEQ ID NO: 1)5'-GCGAGAAAGCCTCCCAGTG-3';
RBSP3_R (SEQ ID NO: 2)5'-CCACCATTCTCCTCCACCAGT-3';
RBSP3_Z (SEQ ID NO: 3)5'-[FAM]-CCACATTGTAATCACGGAAGCAGCAGA-[Dabcyl]-3'.
Анализ уровня транскрипции гена RBSP3 методом ПЦР-РВ
Количественная оценка уровня транскрипции достигается с помощью параллельного проведения ПЦР-РВ с тестируемым и контрольным образцами. В качестве внутреннего контроля, относительно которого проводилось нормирование продуктов амплификации исследуемого гена RBSP3, выбран «ген домашнего хозяйства» - GAPDH, кодирующий глицеральдегид-3-фосфат-дегидрогеназу. Согласно предпочтительной форме осуществления количественной оценки уровня транкрипции генов необходимо выбрать контрольный ген, имеющий незначительную вариабельность уровня транскрипции в опухолевых и нормальных тканях легкого по сравнению вариабельностью уровня транскрипции исследуемых генов. Выбору подходящего контрольного гена для нормализации количественных данных посвящено много обзоров [Radonic A., Thulke S., Mackay I.M., Landt O., Siegert W., Nitsche A. 2004. Guideline to reference gene selection for quantitative real-time PCR Biochem BiophysRes Commun. 313, 856-862; Huggett J., Dheda K., Bustin S., Zumla A. 2005. Real-time RT-PCR normalisation; strategies and considerations. Genes and Immunity. 6. 279-284; Wong M.L, Medrano J.F. 2005. Real-time PCR for mRNA quantification. BioTechniques. 39, 1-11]. Чаще всего в качестве контрольных выбирают гены «домашнего хозяйства», хотя для этой цели может быть использован любой ген с относительно постоянным уровнем транскрипции в исследуемых образцах. Решение о выборе того или иного гена в качестве контрольного на самом деле зависит от степени выбранной/требуемой точности. В настоящем изобретении выбран традиционный часто используемый контрольный ген GAPDH, однако вариабельность уровня транскрипции необходимо проверять для каждого выбранного типа тканей. В ряде работ показана пригодность этого гена в качестве контрольного в образцах ПРЛ (например, см D.W.Liu, S.T.Chen, H.P.Liu. Choice of endogeneous control for gene expression in nonsmall lung cancer. 2005. Eur. Respir. J.26, 1002-1008).
Оценка уровня транскрипции генов может быть основана на абсолютном и относительном измерении количества копий исследуемых транскриптов - абсолютный метод (метод стандартной кривой) и метод относительных измерений (ΔΔCt-метод). Согласно предпочтительной форме количественной оценки уровня транкрипции генов в качестве основного метода измерений выбран второй из них, позволяющий проводить двойное сравнение данных для исследуемого и контрольного генов в опухоли и норме и не требующий выравнивания концентраций опухолевых и нормальных образцов РНК/кДНК, которое необходимо при использовании других методов, например, ОТ-ПЦР.
Выбор образцов сравнения
Согласно предпочтительной форме количественной оценки изменения уровня транскрипции генов важно проверить пригодность образцов сравнения, в данном случае условных норм. «Условной нормой» принято считать образец ткани легкого с отсутствующими макро- и микроскопическими признаками опухолевого роста. При «непригодности» образца условно-нормальной ткани (т.е. в случаях, когда при микроскопии обнаруживали опухолевые клетки или материал был трудно интерпретируемый) использовали дополнительные образцы сравнения, полученные от «здоровых» доноров (доноры, не страдавшие при жизни раком легкого) или усредненные нормы нескольких имеющихся условных норм.
Поскольку не для всех опухолевых образцов имелись пригодные парные условные нормы, расчеты относительного количества копий транскрипта RBSP3 (RкДНК) провели относительно разных образцов сравнения - парных условных норм, если они были, и усредненной условной нормы от нескольких больных, если парных норм не было. В качестве дополнительных образцов сравнения использовали по 5 образцов от здоровых доноров центральной и периферической локализации, для которых усредняли значение ΔCt=Ct(RBSP3)-Ct(GAPDH) и далее проводили расчеты RкДНК Заметное изменение наблюдали только для нескольких условных парных норм. Если гистологический анализ показал непригодность условных норм в соответствии с принятыми критериями (см. выше), либо по данным ПЦР-РВ выявлено заметное снижение количества транскрипта RBSP3 в норме по сравнению с опухолью, что может указывать на вовлеченность гена RBSP3 в ранние события, происходящие в прилежащих к опухоли тканях, и непригодность таких образцов для сравнения, то в этих случаях использовали усредненные нормы и нормы от здоровых доноров.
Учет эффективностей реакций
Согласно предпочтительной форме осуществления количественной оценки уровня транскрипции генов необходимо учитывать эффективности проводимых реакций, которые могут оказать значительное влияние на конечный результат. Для этого разработана программа математической обработки экспериментальных данных ПЦР-РВ относительным методом (ΔΔCt-методом) с расчетом эффективностей реакций. Программа совместима с файлами экспериментальных данных (Ct, ΔRn и др.) из программного обеспечения Applied Biosystems (ABI Prism SDS Software). Программа также осуществляет статистическую оценку достоверности измеряемых изменений и оценку пригодности выбранного контрольного гена.
Далее настоящее изобретение будет подробно проиллюстрировано со ссылкой на конкретные примеры, представляющие собой наиболее предпочтительные воплощения данного изобретения. При этом должно быть понятно, что изобретение не ограничивается этими описанными воплощениями. Напротив, предполагается, что оно включает любые альтернативы, модификации или эквиваленты, допустимые с учетом сущности и объема изобретения.
Пример 1. Образцы тканей легкого
Образцы тканей различных гистологических типов РЛ (Т), прилегающие к опухолям морфологически нормальные ткани (т.н. условные нормы (N), а также нормальные ткани легких центральной (NCL) и периферической локализации (NPL) от скоропостижно скончавшихся доноров были собраны и затем охарактеризованы независимо двумя различными группами сотрудников НИИ КО ГУ РОНЦ им Н.Н.Блохина РАМН. Клинический диагноз установлен с учетом данных ретроспективного анализа первичной медицинской документации больных, цито- и гистологического исследований биоптатов (полученых при фибробронхоскопии, трансторакальных пункциях) и операционного материала. Образцы тканей легкого (опухоль, условно-нормальная ткань) получены непосредственно после удаления опухоли. Каждый образец делили примерно на 3 равные части и хранили в жидком азоте. Общая коллекция опухолевых образцов, подлежащих исследованию, составила 51 (30+21) образец различных гистологических типов рака легкого, из которых 37 - плоскоклеточный рак, 11 - аденокарцинома легкого, из которых 3 - бронхиоло-альвеолярная аденокарцинома легкого, 2 - мелкоклеточный рак легкого, 1 - карциноид, а также 49 образцов условной нормы. Кроме того, использовали ткани легких, полученные постмортально от 10 человек, не имевших в анамнезе заболеваний раком (норма): пять образцов, взятых в центральных областях легких, и пять - в периферических областях. «Морфологически нормальной» принято считать ткань, в которой при микроскопическом исследовании не определялись признаки клеточной атипии, ткань могла быть представленной клетками мерцательного эпителия, кубического эпителия, альвеолярными макрофагами, лимфоидными элементами.
Средний возраст пациентов, среди которых 44 - мужчины, 4 - женщины, для 3 нет данных относительно пола и возраста, составляет около 60 лет (диапазон 31-76 лет). Диагноз в каждом случае устанавливали на основании результатов клинического, морфологического, эндоскопического и рентгенологического обследований. Все опухолевые образцы охарактеризованы согласно международной системе клинико-морфологической классификации опухолей TNM, где Т (tumor) - Т0-Т4 - категории, отражающие нарастание размера и/или местного распространения первичной опухоли, N (nodulus) - N0-N3 - категории, отражающие различную степень поражения метастазами регионарных лимфатических узлов; М (metastasis) - М0-М1 - характеризует отдаленные метастазы. Все возможные комбинации TNM объединяют в более крупные группы - стадии, отражающие течение опухолевого процесса.
Пример 2. Выделение РНК из образцов тканей
Методика 1
Суммарную РНК выделяли из замороженных, измельченных в жидком азоте образцов опухолевых и нормальных тканей. Образцы тканей гомогенизировали на приборе Micro-Dismembrator U (Sartorius, Германия). Очистку РНК проводили стандартным методом с использованием гуанидинизотиоцианата и фенола с последующим осаждением этиловым спиртом [Sambrook et al., 1989, supra]. Для удаления примесей гликопротеидов, которыми богаты ткани легких, использовали дополнительное осаждение РНК солевым раствором [Chomczynski P., Mackey К. 1995. Modification of the TRI reagent procedure for isolation of RNA from polysaccharide- and proteoglycan-rich sources. Biotechniques 19, 942-945]. После солевого осаждения все препараты РНК очищали с помощью набора "RNeasy Mini kit" (Qiagen, CIIIA) согласно прилагаемому изготовителем протоколу. Такая трехэтапная процедура очистки РНК позволила эффективно избавиться не только от труднорастворимых осадков гликопротеидов, но и от низкомолекулярных РНК. Качество препарата РНК проверяли электрофорезом в 1%-ном агарозном геле в присутствии бромида этидия. Количество РНК определяли спектрофотометрически [Sambrook et al., 1989, supra].
Методика 2
РНК из нормальных и опухолевых тканей человека выделяли с использованием набора реагентов Trizol RNA Prep («Лаборатория Изоген», Москва). Основные этапы включали: 1) разрушение ткани, замороженной в жидком азоте, с использованием микро-десмембратора («Sartorius»), и гомогенизацию разрушенного образца в лизирующем растворе, содержащем гуанидинизотиоцианат и фенол; 2) добавление смеси хлороформа и изоамилового спирта в соотношении их объемов 49:1 и центрифугирование 5 минут при 14000 об/мин (4°С); 3) повторную депротеинизацию водной фазы, содержащей РНК, фенолом и центрифугирование в течение 5 минут при 14000 об/мин (4°С); 4) осаждение РНК равным объемом изопропанола из водной фазы, образующейся после центрифугирования. Далее осадок РНК после повторного центрифугирования промывали водным 75% этиловым спиртом, высушивали и растворяли в стабилизирующем реагенте ЭкстраГен Е («Лаборатория Изоген»). Концентрацию РНК определяли на спектрофотометре («Nanodrop») при длине волны 260 нм. Качество выделенной РНК проверяли электрофорезом в 1% агарозе в присутствии бромистого этидия и по значению отношения 260/280 нм. Методика использована в ИМБ РАН.
Методика 3
РНК из нормальных и опухолевых тканей человека выделяли с использованием набора реагентов RNeasy Mini Kit («Qiagen», Германия) согласно протоколу. Основные этапы включали: 1) разрушение ткани, замороженной в жидком азоте, с использованием микро-десмембратора («Sartorius») и гомогенизацию разрушенного образца в лизирующем буфере RLT в расчете 600 мкл на 30 мкг ткани. 2) центрифугирование 3 минуты при 14000 об/мин (4°С); 3) добавление равного объема водного 70% этилового спирта к супернатанту; 4) нанесение на колонку; 5) промывание колонки после сорбции РНК один раз буфером RW1 объемом 700 мкл и дважды буфером RPE объемом 500 мкл; 5) элюцию РНК водой, свободной от РНКаз. Концентрацию РНК определяли на спектрофотометре («Nanodrop») при длине волны 260 нм. Качество выделенной РНК проверяли электрофорезом в 1% агарозе в присутствии бромистого этидия и по значению отношения 260/280 нм, которое составляло 1,8-2,0. Методика использована в ИМБ РАН.
Пример 3. Реакция обратной транскрипции
Синтез первой цепи кДНК выполнен двумя различными группами сотрудников ИБХ РАН и ИМБ РАН.
Методика 1
На матрице РНК, выделенной, как описано в Примере 2, синтезировали одноцепочечную кДНК. Для получения кДНК использовали модифицированный SMART-метод [Zhu Y.Y., Machleder E.M., Chenchik A., Li R-, Siebert P.D. 2001. Reverse transcriptase template switching: a SMART approach for full-length cDNA library construction. Biotechniques 30, 892-897], 2 нг - 1 мкг суммарной РНК, праймеры:
SMART (5'-AAGCAGTGGTATCAACGCAGAGTACGCrGrGrG-3') и
CDS(5'-AGCAGTGGTATCAACGCAGAGTAC(T)30N-1N-3'),
и обратную транскриптазу PowerScript (Clontech, CIIIA).
Условия реакции:
Состав реакционной смеси (10 мкл):
РНК (1 мкг/мкл) 1,0 мкл
праймер SMART (6 мкМ) 2,0 мкл
праймер CDS (10 мкМ) 1,0 мкл
стерильная деионизованная вода 1,0 мкл
Прогревали пробу при 72°С, 3 мин и помещали в лед. Добавляли 5 мкл смеси:
буфер (Clontech) для построения 1-ой цепи (5х) 2,0 мкл
dNTP (10 мМ) 1,0 мкл
DTT (20 мМ) 1,0 мкл
обратная транскриптаза PowerScript (Clontech) 1,0 мкл
Инкубировали при 42°С, 60 мин. Реакцию останавливали прогреванием при 65°С, 5 мин, добавляли 2 мкл 60 мМ ЭДТА и доводили объем пробы до 20 мкл. Эту методику использовали в ИБХ РАН и в ИМБ РАН.
Методика 2
Для проведения реакции обратной транскрипции брали по 1 мкг РНК, полученной одним из двух вышеописанных методов с использованием наборов реагентов Trizol RNA Prep («Лаборатория Изоген») или реагентов RNeasy Mini Kit («Qiagen»), предварительно обработанной не содержащей РНКаз ДНКазой I (Invitrogene), 100 нг гексануклеотидных праймеров, 1 мМ dNTP, 1x реакционный буфер («Fermentas», Литва), содержащий 250 мМ Tris-HCl (рН 8.3. 25°С), 250 мМ KCl, 20 мМ MgCl2, 50 мМ DTT и 200 единиц обратной транскриптазы M-MuLV (Fermentas.). Реакцию проводили в объеме 20 мкл при следующем температурном режиме: 25°С - 10 мин, 42°С - 60 мин, 50°С - 10 мин, 70°С - 10 мин. Методику использовали в ИМБ РАН.
Пример 4. Синтез второй цепи кДНК
Для синтеза второй цепи кДНК и амплификации брали 1/10 часть от объема реакционной смеси, полученной в Примере 3. Синтез проводили с помощью Advantage2 DNA Polymerase с праймером 5'-AAGCAGTGGTATCAACGCAGAGT-3' согласно протоколу «Advantage 2 PCR kit» (Clontech, Heidelberg, Germany).
Условия проведения ПЦР
Состав реакционной смеси (50 мкл):
ПЦР-буфер Advantage 2 (Clontech) (10x) 5,0 мкл
dNTP (2,5 мМ) 5,0 мкл
праймер 10 мкМ 1,0 мкл
кДНК (одноцепочечная) 1,0 мкл
Advantage 2 ДНК-полимераза (Clontech) 1,0 мкл
стерильная деионизованная вода 37,0 мкл
Условия амплификации:
95°С, 1,5 мин 1 цикл
95°С, 20 с; 65°С, 20 с; 72°С, 3 мин 14-17-20-23 цикла
Для каждого образца подбирали количество циклов, позволяющих получать одинаковое количество амплифицированного материала.
Пример 5. Подбор условий определения уровня транскрипции гена RBSP3 в образцах тканей легких
Для ОТ-ПЦР и ПЦР-РВ использовали одинаковые специфичные праймеры RBSP3_F(SEQ ID NO: 1)и RBSP3_R (SEQ ID NO: 2), которые были подобраны к разным экзонам гена RBSP3, причем один из праймеров перекрывает границу между экзонами. Для ПЦР-РВ дополнительно к праймерам использовали зонд RBSP3_R (SEQ ID NO: 3).
Размер ампликона - 154 п.н.
Последовательности выбранных праймеров и зондов для контрольного гена:
Прямой GAPDH-F 5'-CGGAGTCAACGGATTTGGTC-3'
Обратный GAPDH-R 5'-TGGGTGGAATCATATTGGAACAT- 3'…
Зонд GAPDH-Z - 5'-CCCTTCATTGACCTCAACTACATGGTTTACAT-3'
Размер ампликона - 141 п.н.
Для проведения ПЦР-РВ подобраны оптимальные концентрации праймеров и зондов исследуемого и контрольного генов. Концентрации праймеров варьировали в диапазоне 250-400 нМ при постоянной концентрации зондов, равной 100 нМ, затем концентрацию зондов варьировали при подобранной оптимальной концентрации праймеров в диапазоне 150-250 нМ. Для RBSP3 оптимальные концентрации праймеров составили 350 нМ и зонда 150 нМ, для GAPDH концентрация праймеров - 300 нМ, зонда - 150 нМ.
Авторы использовали прибор ABI PRISM ® 7000 Sequence Detection System, Applied Biosystems, CIIIA.
Пример 6. Количественная оценка уровня транскрипции гена RBSP3
Протокол определения изменения уровня транскрипции методом ПЦР-РВ
1.Готовили реакционные смеси для генов RBSP3 и GAPDH, осторожно смешав все компоненты реакции, кроме матрицы (кДНК), праймеры и зонд в оптимальных концентрациях, из расчета 1 реакция объемом 25 мкл для каждого образца +1 дополнительная реакция по 25 мкл.
2. В 96-луночный планшет добавляли по 20 мкл приготовленных реакционных смесей без матрицы.
3. Вносили по 5 мкл матрицы, плотно закрывали планшет пленкой.
4. Помещали планшет в приборное отделение, задавали названия ячеек, температурный режим для 40 циклов: 95°С - 10 мин - денатурация и активация фермента, 95°С - 15 сек - денатурация, 60°С - 1 мин - отжиг зонда и полимеризация, затем запускали прибор.
5. Реакции проводили в режиме относительных количественных измерений (программное обеспечение RQ (Relative Quantification, Applied Biosystems).
6. После завершения реакции амплификации сохраняли данные на CD-диске.
7. Отбирали 4 мкл продуктов амплификации (40 циклов), наносили образцы на 1.8% агарозный гель, содержащий 0.5 мг/л этидий бромида, и маркер молекулярных масс ДНК, позволяющий оценить размер продуктов амплификации (М50, «Изоген»). Гель-электрофорез проводили в ТВЕ-буфере, содержащим 10 мг/л этидий бромида. Длина разделения составляла 3-5 см геля. После гель-электрофореза визуализацию продуктов амплификации и их документирование проводили в ультрафиолете при длине волны 302 нм.
8. Нуклеотидный состав ампликонов подтверждали секвенированием на автоматическом секвенаторе 3730 DNA Analyzer (Applied Biosystems, CIIIA). Секвенирование проводили отдельно с 5'- и 3'-концевого праймеров с использованием реактивов DYEnamic ET Terminator Cycler Sequencing Kit ("Amersham").
9. Проводили математическую обработку данных ПЦР-РВ и представляли результаты в графическом и/или табличном виде.
Пример 7. Математическая обработка данных ПЦР-РВ
Данные ПЦР-РВ переносили в виде текстового файла в Microsoft Excel и проводили математическую обработку данных. Относительный уровень транскрипции RкДНК (далее R), представляющий отношение количества копий исследуемой последовательности кДНК к количеству копий контрольной последовательности в опухоли (Т) по сравнению с нормой (N), связан с основными параметрами ПЦР-РВ пороговым циклом Ct и эффективностью реакции Е общим выражением (Бюллетень 2, Applied Biosystems):
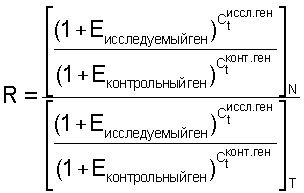
Интервал крайних значений R вычисляли с учетом рассчитанных отклонений е для значений Ct:
 где
где 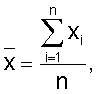 i=1, 2, …, n, где n - число повторов реакции (в нашем случае n=3). При суммировании величин отклонения вычисляют по формуле:
i=1, 2, …, n, где n - число повторов реакции (в нашем случае n=3). При суммировании величин отклонения вычисляют по формуле: 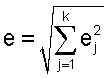 j=1, 2, …, k, где k - число суммируемых величин.
j=1, 2, …, k, где k - число суммируемых величин.
Достоверность наблюдаемых изменений оценивали исходя из нормального распределения данных. Данные считали достоверными при Р<0,05, где Р - показатель статистической значимости данных.
Результаты анализа уровня транскрипции гена RBSP3
Оценку уровня транскрипции гена RBSP3 выполнили на образцах кДНК двух групп, полученных исследователями различными методами в разных институтах (группа 1 - образцы с клиническими номерами от 1, 2…497, ИБХ РАН, группа 2 - образцы с номерами 1006, … 1086, ИМБ РАН), при этом использованы как зарубежные, так и отечественные наборы реактивов. Характеристика всех образцов приведена в таблице 1.
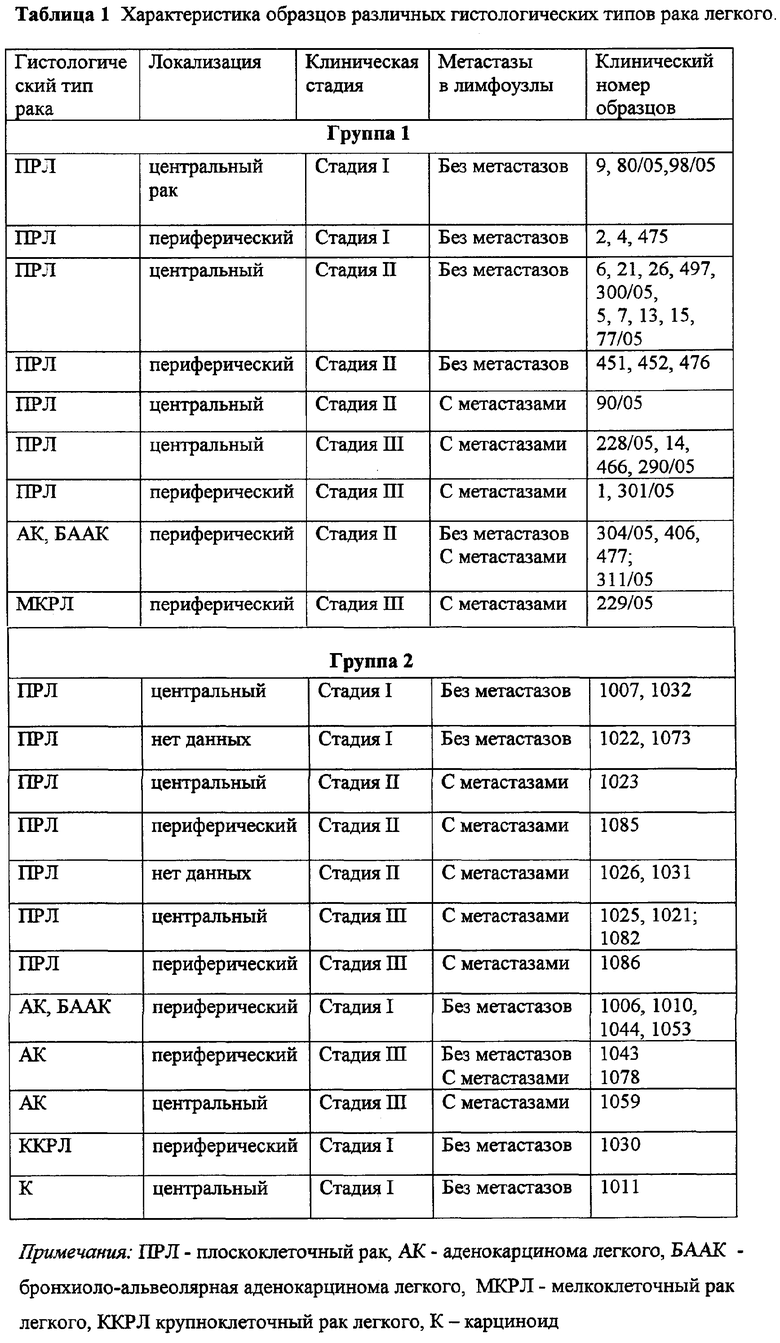
Сравнение уровня транскрипции гена RBSP3 в опухолевых образцах относительно различных образцов сравнения - норм (условная норма, усредненная условная норма и усредненная норма от здоровых доноров, не имевших онкозаболеваний) - показало близкие значения R с перекрывающимися интервалами, рассчитанными с учетом отклонений. Более того, результаты относительных расчетов практически не зависели от места локализации первичной опухоли (центральной или периферической), поскольку расчеты относительно усредненной нормы от 5 образцов тканей легкого здоровых доноров той или иной локализации давали также близкие значения R.
Частота снижений уровня транскрипции гена RBSP3 в двух группах образцов.
В каждой группе образцов выявлено снижение уровня транскрипции гена RBSP3 в опухоли по сравнению с нормой в большинстве образцов (табл.2). Так, в группе 1 общая частота снижений составила 81% (25/30), причем частота снижений в образцах ПРЛ составила 88% (22/25). В группе 2 общая частота снижений составила 90% (19/21) и частота снижений в образцах ПРЛ составила 100% (12/12). Кроме того, получены близкие значения относительного уровня транскрипции (R) на образцах кДНК одних и тех же опухолей, полученных двумя разными способами. Результаты для всей выборки исследованных образцов в более наглядной графической форме также представлены на фиг.3.
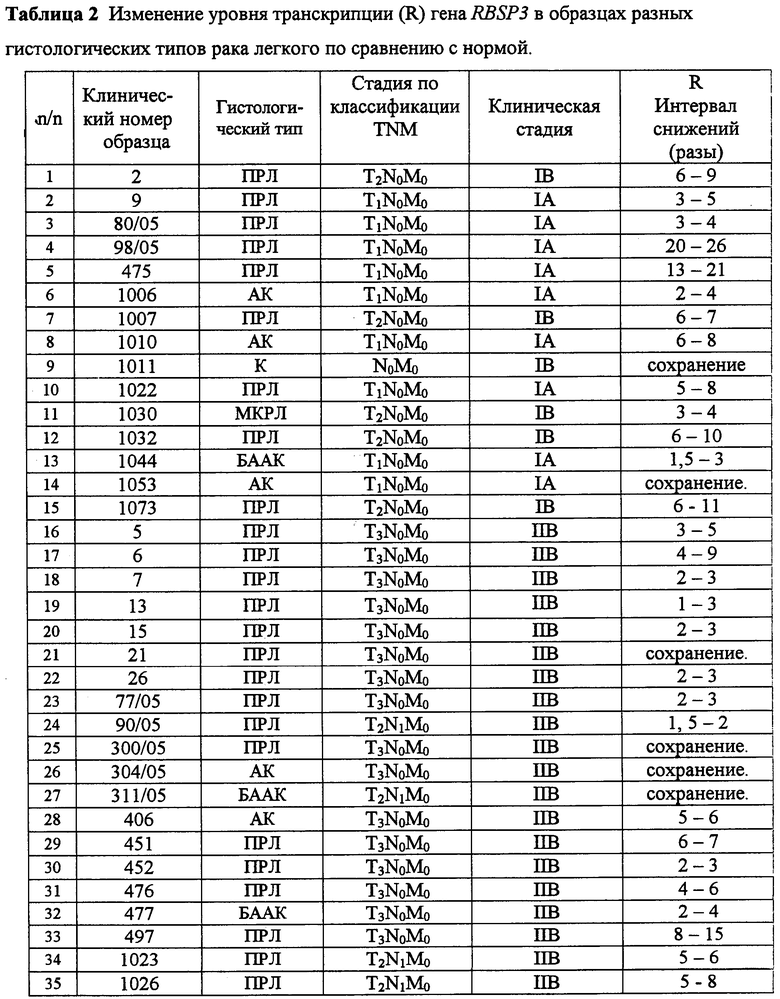

Степень снижения по стадиям и типам РЛ.
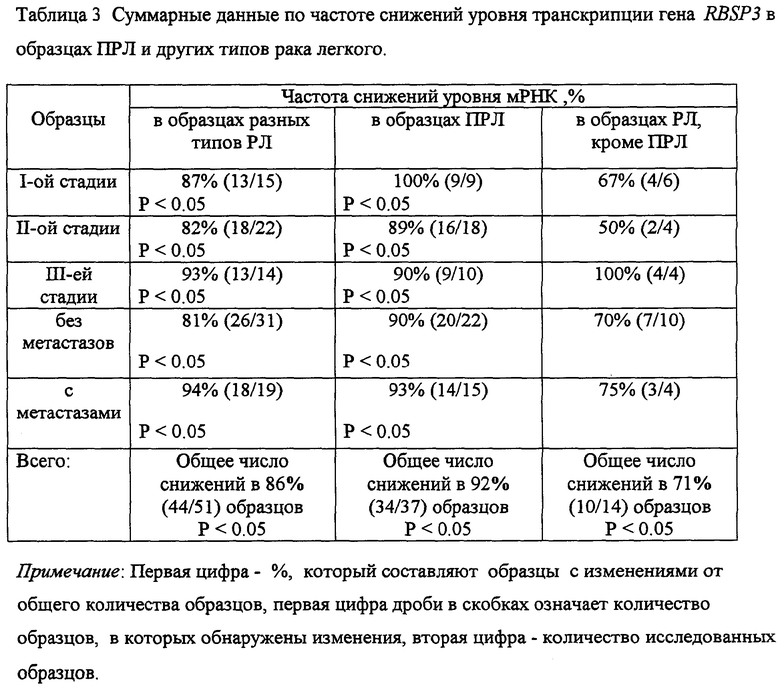
Как видно из фиг.3 и таблицы 2, уровень транскрипции гена RBSP3 снижается в образцах ПРЛ в основном от 2 до 10 раз, однако в некоторых образцах наблюдали также более значительные снижения при увеличении степени распространенности опухолевого заболевания. Анализ данных показал, что снижение уровня транскрипции гена RBSP3 происходит в 86% (44/51, Р<0.05) всех образцов, в 92% (34/37, Р<0.05) образцов ПРЛ и 71% (10/14) образцов различных типов рака легкого отличных от ПРЛ (таблица 3). Следует отметить, что при I стадии ПРЛ происходит снижение уровня транскрипции гена RBSP3 в 100% образцов (9/9, Р<0.05), при II и III стадиях - в 89% (16/18, Р<0,05) и 90% (9/10, Р<0,05) образцов соответственно.
Корреляция между различными характеристиками и снижением уровня транскрипции гена RBSP3.
В таблице 3 приведена частота снижения уровня транскрипции гена RBSP3 для образцов при наличии и отсутствии метастазов в региональные лимфатические узлы (категория N), что свидетельствует об отсутствии между этими показателями корреляции. Корреляции между изменением уровня транскрипции гена RBSP3 и такими характеристиками, как возраст пациента, локализация первичной опухоли, клиническая стадия, степень распространенности опухолевого заболевания также выявлено не было.
Анамнез курения.
Для второй группы известен анамнез курения для 14 пациентов, причем 5 из которых не курили в прошлом и настоящем, а все остальные (64%) - злостные курильщики со стажем курения от 15 до 50 лет, что подтверждает значение курения в качестве одной из основных причин возникновения рака легкого.
Настоящим изобретением также предусмотрено, что определение уровня транскрипции гена RBSP3 будет полезным при мониторинге эффективности проводимой противораковой терапии, причем анализ способом настоящего изобретения следует проводить до начала и после окончания курса лечения, а также при необходимости по ходу курса лечения. Повышение уровня транскрипции гена RBSP3 по ходу или по завершении курса лечения будет свидетельствовать о восстановлении активности гена-супрессора опухолевого роста RBSP3, что может говорить о положительных сдвигах при лечении. Дальнейшее снижение уровня транскрипции гена RBSP3 может указывать на отсутствие эффективности лечения.
Представленное выше подробное описание изобретения и его конкретных воплощений, приведенных в примерах со ссылкой на фигуры, предназначено исключительно для более полного уяснения сущности заявленного изобретения, но не для его ограничения. Специалисту будет ясно, что могут быть сделаны различные изменения, которые, тем не менее, будут соответствовать сущности и объему настоящего изобретения, которые определяются прилагаемой формулой изобретения.

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДИАГНОСТИКИ НЕМЕЛКОКЛЕТОЧНОГО РАКА ЛЕГКОГО И НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2008 |
|
RU2390780C1 |
| СПОСОБ ДИАГНОСТИКИ СВЕТЛОКЛЕТОЧНОЙ ПОЧЕЧНОКЛЕТОЧНОЙ КАРЦИНОМЫ И НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2009 |
|
RU2393472C1 |
| СПОСОБ ДИАГНОСТИКИ ПЛОСКОКЛЕТОЧНОГО РАКА ЛЕГКИХ И НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2006 |
|
RU2327162C1 |
| СПОСОБ ДИАГНОСТИКИ ПЛОСКОКЛЕТОЧНОГО РАКА ЛЕГКИХ И НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2006 |
|
RU2324186C1 |
| СПОСОБ ДИАГНОСТИКИ НЕМЕЛКОКЛЕТОЧНОГО РАКА ЛЕГКИХ И НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2006 |
|
RU2330285C1 |
| СПОСОБ ДИАГНОСТИКИ ПЛОСКОКЛЕТОЧНОГО РАКА ЛЕГКОГО И НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2014 |
|
RU2586779C2 |
| ОПРЕДЕЛЕНИЕ СНИЖЕНИЯ УРОВНЯ мРНК ГЕНОВ ITGA9, HYAL1 И HYAL2 КАК СПОСОБ ДИАГНОСТИКИ НЕМЕЛКОКЛЕТОЧНОГО РАКА ЛЕГКОГО И НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2008 |
|
RU2403575C2 |
| СПОСОБ ДИАГНОСТИКИ НЕМЕЛКОКЛЕТОЧНОГО РАКА ЛЕГКИХ И НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2010 |
|
RU2445627C1 |
| СПОСОБ ДИАГНОСТИКИ СВЕТЛОКЛЕТОЧНОЙ ПОЧЕЧНОКЛЕТОЧНОЙ КАРЦИНОМЫ И НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2012 |
|
RU2545995C2 |
| СПОСОБ ДИАГНОСТИКИ СВЕТЛОКЛЕТОЧНОЙ ПОЧЕЧНОКЛЕТОЧНОЙ КАРЦИНОМЫ И НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2012 |
|
RU2545998C2 |
Изобретение относится к области медицины, а именно к молекулярной диагностике в онкологии. Предложен способ диагностики немелкоклеточного рака легких, основанный на измерении уровня транскрипции гена RBSP3, и набор для его осуществления. Сниженный уровень транскрипции в предположительно пораженной раком ткани человека по сравнению с ее уровнем в здоровой ткани служит диагностическим признаком немелкоклеточного рака легкого. Способ позволяет с высокой достоверностью диагностировать немелкоклеточный рак легкого, в первую очередь плоскоклеточный рак, в том числе на самой ранней стадии прогрессии опухолевой трансформации. 2 н. и 5 з.п.ф-лы, 3 табл., 4 ил.
1. Способ диагностики немелкоклеточного рака легкого, включающий следующие стадии:
а) получение исходной пары образцов ткани от пациента, где один из образцов получен из предположительно пораженной раком ткани, а второй получен из прилегающей гистологически нормальной (условно-нормальной) ткани;
б) выделение и очистка препаратов РНК из исходной пары образцов;
в) синтез одноцепочечной или двуцепочечной кДНК на матрице РНК с использованием олигонуклеотидных праймеров;
г) нормирование концентрации кДНК RBSP3 по контрольному гену, уровень транскрипции которого относительно постоянен в норме и при раке легкого;
д) проведение количественной или полуколичественной реакции амплификации фрагмента гена RBSP3 с использованием кДНК, полученной на стадии в), в качестве матрицы, и пары геноспецифичных олигонуклеотидных праймеров с последовательностями SEQ ID NO: I, 2 и зонда с последовательностью SEQ ID NO: 3;
е) сравнение количества амплифицированного фрагмента ДНК RBSP3 для образца, полученного из предположительно пораженной раком ткани, с количеством амплифицированного фрагмента ДНК для образца, полученного из нормальной ткани, где указанные количества амплифицированного фрагмента ДНК отражают уровень транскрипции гена RBSP3, причем уменьшение транскрипции гена RBSP3 служит диагностическим признаком рака легкого.
2. Способ по п.1, в котором диагностируют плоскоклеточный рак легкого.
3. Способ по п.1 или 2, в котором на стадии в) олигонуклеотидные праймеры, используемые для синтеза одноцепочечной или двуцепочечной кДНК, выбирают из числа олиго(dT)-содержащих праймеров, случайных гексамеров или их комбинации, а также праймеров, специфичных к гену RBSP3.
4. Способ по п.1 или 2, в котором на стадии д) количественная или полуколичественная реакция амплификации фрагмента гена RBSP3 представляет собой подимеразную цепную реакцию (ПЦР) в реальном времени или стандартную полимеразную цепную реакцию с обратной транскрипцией (ОТ-ПЦР).
5. Способ по п.1 или 2, в котором на стадии г) в качестве контрольного гена используют ген GAPDH, кодирующий белок глицеральдегид-3-фосфат-дегидрогеназу.
6. Набор для диагностики немелкоклеточного рака легких по пп.1 и 2, соответственно, позволяющий определить уровень транскрипции гена RBSP3 методом полимеразной цепной реакции и включающий праймеры с последовательностью SEQ ID NO:1 и 2, а также олигонуклеотидный зонд с последовательностью SEQ ID NO:3.
7. Способ по п.1 или 2, отличающийся тем, что для проведения полимеразной цепной реакции в реальном времени используют первые цепи или амплификаты первых цепей кДНК.
| RU 2004100112 А, 20.04 | |||
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| СПОСОБ ДИАГНОСТИКИ НЕКАРЦИНОИДНЫХ ОПУХОЛЕЙ ЛЕГКОГО ЧЕЛОВЕКА | 1991 |
|
RU2033423C1 |
| KASHUBA VI at al | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Proc Nati Acad Sci U S A | |||
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| (ref..) | |||
| PROTOPOPOV A at al | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
Авторы
Даты
2009-04-10—Публикация
2007-11-19—Подача